Розчини Розчини – це гомогенні термодинамічна стійкі системи













![[H3O+].[OH-] = 1.10-14 – йонний добуток води. В нейтральному розчині [H3O+]=[OH]= [H3O+].[OH-] = 1.10-14 – йонний добуток води. В нейтральному розчині [H3O+]=[OH]=](https://present5.com/presentacii-2/20171211\29590-lek1_nova_stom.ppt\29590-lek1_nova_stom_14.jpg)
![якщо в розчині [Н3О+] = 10-3 моль/л, то середовище розчину кисле, а концентрація якщо в розчині [Н3О+] = 10-3 моль/л, то середовище розчину кисле, а концентрація](https://present5.com/presentacii-2/20171211\29590-lek1_nova_stom.ppt\29590-lek1_nova_stom_15.jpg)










29590-lek1_nova_stom.ppt
- Количество слайдов: 29
 Розчини Розчини – це гомогенні термодинамічна стійкі системи змінного складу, які складаються з двох або більше компонентів та продуктів їх взаємодії. Розчини – плазма крові, лімфа,сеча, спинномозкова рідина Плазма крові: 90-92% води 8-10% сухої речовини Вміст води:в ембріоні – 97% в новонародженого- 77% у зрілому віці- 50-60%
Розчини Розчини – це гомогенні термодинамічна стійкі системи змінного складу, які складаються з двох або більше компонентів та продуктів їх взаємодії. Розчини – плазма крові, лімфа,сеча, спинномозкова рідина Плазма крові: 90-92% води 8-10% сухої речовини Вміст води:в ембріоні – 97% в новонародженого- 77% у зрілому віці- 50-60%
 Добова потреба води в середньому 2,5л. Аномальні властивості: Висока теплоємність – терморегуляція Мінімальна теплоємність при 36,790С Мала в’язкість Висока діелектрична проникність
Добова потреба води в середньому 2,5л. Аномальні властивості: Висока теплоємність – терморегуляція Мінімальна теплоємність при 36,790С Мала в’язкість Висока діелектрична проникність
 Електроліти Електроліти - це речовини, які в розчиненому (чи розплавленому) стані проводять електричний струм. Електропровідність обумовлена дисоціацією на йони Електроліти ділять на 2 типи: сильні і слабкі. Електроліти визначають величину осмотичного тиску фізіологічних рідин. Наявність електролітів впливає на розчинність білків, амінокислот
Електроліти Електроліти - це речовини, які в розчиненому (чи розплавленому) стані проводять електричний струм. Електропровідність обумовлена дисоціацією на йони Електроліти ділять на 2 типи: сильні і слабкі. Електроліти визначають величину осмотичного тиску фізіологічних рідин. Наявність електролітів впливає на розчинність білків, амінокислот
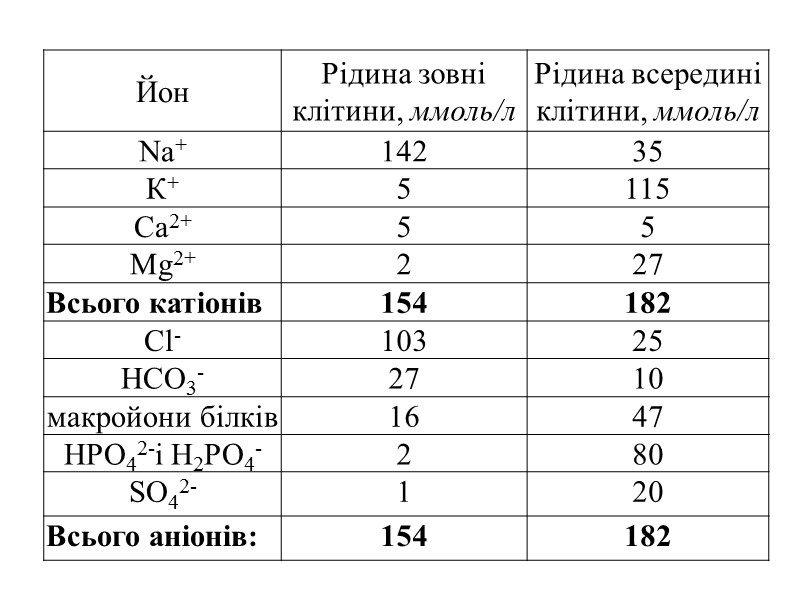
 В нормальному стані організму вміст електролітів: Катіонів в плазмі крові – 154 ммоль/л в основному це йони Nа+, К+, Са2+ і Мg2+. Аніонів – 154 ммоль/л в основному це - Cl–, HCO3–, а також багатозарядні макройони білків.
В нормальному стані організму вміст електролітів: Катіонів в плазмі крові – 154 ммоль/л в основному це йони Nа+, К+, Са2+ і Мg2+. Аніонів – 154 ммоль/л в основному це - Cl–, HCO3–, а також багатозарядні макройони білків.

 Порушення нормального електролітного балансу має негативні наслідки. Відомі патології обумовлені як недостатністю цих йонів в організмі (зниження осмoтичного тиску), так і їх надлишком (гіпертонія). Прикладом антагонізму є взаємний вплив катіонів калію і кальцію . Синергізм йонів є підсилення дії одного йона іншим.
Порушення нормального електролітного балансу має негативні наслідки. Відомі патології обумовлені як недостатністю цих йонів в організмі (зниження осмoтичного тиску), так і їх надлишком (гіпертонія). Прикладом антагонізму є взаємний вплив катіонів калію і кальцію . Синергізм йонів є підсилення дії одного йона іншим.
 Слабкі електроліти Слабкі електроліти в розчинах дисоціюють не повністю. СН3СООН СН3СОО- + Н+ Швидкість прямої реакції 1 = К1 [СНзСООН] зворотної реакції 2 = К2 [СНзСОО-] [Н+] При встановленні рівноваги 1 =2
Слабкі електроліти Слабкі електроліти в розчинах дисоціюють не повністю. СН3СООН СН3СОО- + Н+ Швидкість прямої реакції 1 = К1 [СНзСООН] зворотної реакції 2 = К2 [СНзСОО-] [Н+] При встановленні рівноваги 1 =2
 Оствальд встановив зв’язок між константою дисоціації (К), ступенем дисоціації (α) і молярною концентрацією розчину (С) Для оцтової кислоти, яка дисоціює не повністю, а лише певна її частина (α) - СН+ = ССН3СОО– = С . α концентрація недисоційованих молекул С – С . α = С (1-α)
Оствальд встановив зв’язок між константою дисоціації (К), ступенем дисоціації (α) і молярною концентрацією розчину (С) Для оцтової кислоти, яка дисоціює не повністю, а лише певна її частина (α) - СН+ = ССН3СОО– = С . α концентрація недисоційованих молекул С – С . α = С (1-α)
 Для слабких електролітів (α < 3%) 1-α = 1 - 0,03 ≈ 1. рівняння константи спрощується К = Сα2 звідки 1/С -розведення
Для слабких електролітів (α < 3%) 1-α = 1 - 0,03 ≈ 1. рівняння константи спрощується К = Сα2 звідки 1/С -розведення
 Закон розведення Оствальда Ступінь дисоціації слабих бінарних електролітів обернено пропорційна кореню квадратному із їх концентрації або прямо пропорційна їх розведенню. Наслідки: Чим більш розведений розчин, тим більша ступінь електролітичної дисоціації розчиненого електроліту. Ступінь електролітичної дисоціації двох електролітів однакової концентрації розчину більша у того електроліту, в якого більша константа
Закон розведення Оствальда Ступінь дисоціації слабих бінарних електролітів обернено пропорційна кореню квадратному із їх концентрації або прямо пропорційна їх розведенню. Наслідки: Чим більш розведений розчин, тим більша ступінь електролітичної дисоціації розчиненого електроліту. Ступінь електролітичної дисоціації двох електролітів однакової концентрації розчину більша у того електроліту, в якого більша константа
 Теорія кислот і основ Сучасні уявлення про природу кислот і основ дали Дж. Бренстед та І.Льюїс (1923р). За протонною теорією кислота - це речовина, що віддає протон (донор протону), а основа - речовина, що приймає протон (акцептор протона). НClО + Н2О СlO- + H3O+ спряжена спряжена спряжена спряжена кислота основа основа кислота І II І II
Теорія кислот і основ Сучасні уявлення про природу кислот і основ дали Дж. Бренстед та І.Льюїс (1923р). За протонною теорією кислота - це речовина, що віддає протон (донор протону), а основа - речовина, що приймає протон (акцептор протона). НClО + Н2О СlO- + H3O+ спряжена спряжена спряжена спряжена кислота основа основа кислота І II І II
 Дисоціація води Згідно з теорією Бренстеда вода відносно самої себе є одночасно і кислотою і основою (амфоліт) Н2О ОН- + Н+ Н2О + Н+ = Н3О+ Н2О + Н2О = Н3О+ + ОН- ця реакція називається автопротолізом води: кількісно визначається йонним добутком води.
Дисоціація води Згідно з теорією Бренстеда вода відносно самої себе є одночасно і кислотою і основою (амфоліт) Н2О ОН- + Н+ Н2О + Н+ = Н3О+ Н2О + Н2О = Н3О+ + ОН- ця реакція називається автопротолізом води: кількісно визначається йонним добутком води.
 Константи рівноваги К=1,8 .10-16 з 550 млн. молекул води - дисоціює тільки одна Маса 1 л води при 25°С - 1000 г [H3O+].[OH-]=K.[H2O]2=1,8.10-16.55,562=1.10-14
Константи рівноваги К=1,8 .10-16 з 550 млн. молекул води - дисоціює тільки одна Маса 1 л води при 25°С - 1000 г [H3O+].[OH-]=K.[H2O]2=1,8.10-16.55,562=1.10-14
![>[H3O+].[OH-] = 1.10-14 – йонний добуток води. В нейтральному розчині [H3O+]=[OH]= >[H3O+].[OH-] = 1.10-14 – йонний добуток води. В нейтральному розчині [H3O+]=[OH]=](https://present5.com/presentacii-2/20171211\29590-lek1_nova_stom.ppt\29590-lek1_nova_stom_14.jpg) [H3O+].[OH-] = 1.10-14 – йонний добуток води. В нейтральному розчині [H3O+]=[OH]= В кислому середовищі [H3O+]>[OH-] [H3O+]>10-7, а [OH-]<10-7 В лужному середовищі [H3O+]<[OH-] [H3O+]<10-7, [OH-]>10-7
[H3O+].[OH-] = 1.10-14 – йонний добуток води. В нейтральному розчині [H3O+]=[OH]= В кислому середовищі [H3O+]>[OH-] [H3O+]>10-7, а [OH-]<10-7 В лужному середовищі [H3O+]<[OH-] [H3O+]<10-7, [OH-]>10-7
![>якщо в розчині [Н3О+] = 10-3 моль/л, то середовище розчину кисле, а концентрація >якщо в розчині [Н3О+] = 10-3 моль/л, то середовище розчину кисле, а концентрація](https://present5.com/presentacii-2/20171211\29590-lek1_nova_stom.ppt\29590-lek1_nova_stom_15.jpg) якщо в розчині [Н3О+] = 10-3 моль/л, то середовище розчину кисле, а концентрація Водневий показник рН - це десятковий логарифм концентрації йонів гідроксонію, взятий з від’ємним знаком. pH = -lg[H3O+] Аналогічно рОН = -lg[OH-] рКводи = рН + рОН = 14
якщо в розчині [Н3О+] = 10-3 моль/л, то середовище розчину кисле, а концентрація Водневий показник рН - це десятковий логарифм концентрації йонів гідроксонію, взятий з від’ємним знаком. pH = -lg[H3O+] Аналогічно рОН = -lg[OH-] рКводи = рН + рОН = 14
 Для розчинів слабких кислот і основ, в яких кількість йонів значно менша за концентрацію кислоти чи основи, треба знати значення ступеня і константи йонізації. рН=-lg c∙α згідно з законом Оствальда де Ка - константа йонізації с - концентрація.
Для розчинів слабких кислот і основ, в яких кількість йонів значно менша за концентрацію кислоти чи основи, треба знати значення ступеня і константи йонізації. рН=-lg c∙α згідно з законом Оствальда де Ка - константа йонізації с - концентрація.
 для слабких основ рОН = -lg c∙α Для розчину СН3СООН з См = 0.1 моль/л
для слабких основ рОН = -lg c∙α Для розчину СН3СООН з См = 0.1 моль/л
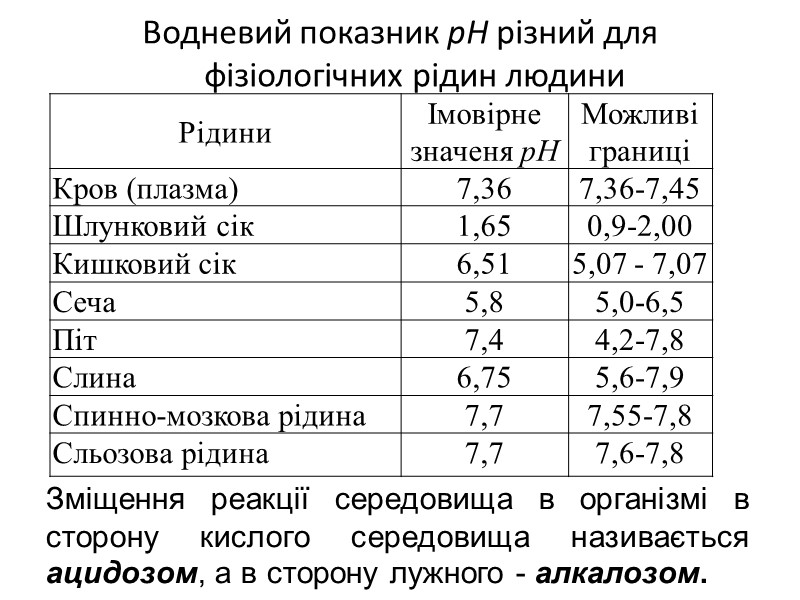
 Водневий показник рН різний для фізіологічних рідин людини Зміщення реакції середовища в організмі в сторону кислого середовища називається ацидозом, а в сторону лужного - алкалозом.
Водневий показник рН різний для фізіологічних рідин людини Зміщення реакції середовища в організмі в сторону кислого середовища називається ацидозом, а в сторону лужного - алкалозом.
 Буферні розчини Буферні розчини - здатні зберігати значення рН при розведенні або при додаванні невеликих кількостей кислоти чи лугу, а також при їх концентруванні. До таких розчинів належать: 1) розчини, що містять слабку кислоту і сіль цієї кислоти з сильною основою: СН3СООН + СН3СООNa - ацетатний буфер рН (3,72-5,57) (4,65) 2) розчини, що містять слабку основу і сіль цієї основи з сильною кислотою NН4ОН + NH4Cl - аміачний буфер pН (8,43-10,28) (9,37) 3) розчини, що містять солі багатоосновних слабких кислот Nа2НРО4 + NаН2PО4 - фосфатний буфер pН( 5,91-7,73) (6,81)
Буферні розчини Буферні розчини - здатні зберігати значення рН при розведенні або при додаванні невеликих кількостей кислоти чи лугу, а також при їх концентруванні. До таких розчинів належать: 1) розчини, що містять слабку кислоту і сіль цієї кислоти з сильною основою: СН3СООН + СН3СООNa - ацетатний буфер рН (3,72-5,57) (4,65) 2) розчини, що містять слабку основу і сіль цієї основи з сильною кислотою NН4ОН + NH4Cl - аміачний буфер pН (8,43-10,28) (9,37) 3) розчини, що містять солі багатоосновних слабких кислот Nа2НРО4 + NаН2PО4 - фосфатний буфер pН( 5,91-7,73) (6,81)
 Механізм дії буферних розчинів В ацетатному буфері кислота і сіль піддаються дисоціації СН3СООН СН3СОО- +Н+ СН3СООNа СН3СОО- + Nа+ кислота в розчині протолізується НСІ + Н2О = СІ- + Н3О+ СН3СОО- + Н3О+ СН3СООН + Н2О Якщо ж до цього самого розчину додати сильну основу NаОН, то електролітична дисоціація NаОН = Na+ + ОН- протоліз СН3СООН+Н2О СН3СОО- +Н3О+ нейтралізація Н3О++ ОН- = 2Н2О реакція середовища майже не змінюється.
Механізм дії буферних розчинів В ацетатному буфері кислота і сіль піддаються дисоціації СН3СООН СН3СОО- +Н+ СН3СООNа СН3СОО- + Nа+ кислота в розчині протолізується НСІ + Н2О = СІ- + Н3О+ СН3СОО- + Н3О+ СН3СООН + Н2О Якщо ж до цього самого розчину додати сильну основу NаОН, то електролітична дисоціація NаОН = Na+ + ОН- протоліз СН3СООН+Н2О СН3СОО- +Н3О+ нейтралізація Н3О++ ОН- = 2Н2О реакція середовища майже не змінюється.
 рівняння Гендерсона-Гассельбаха Для розрахунку pН кислотного буферного основного буферу
рівняння Гендерсона-Гассельбаха Для розрахунку pН кислотного буферного основного буферу
 Буферна ємність Буферна ємність - це розрахункова величина, яка визначається кількістю еквівалентів сильної кислоти n (1/1 НСІ) чи n(1/2 Н2SО4) або сильної основи n (1/1 NаОН), n(1/2 Вa(ОН)2) що треба додати до 1 л буферного розчину, щоб pН змінився на одиницю. Якщо В - буферна ємність, а n (Н3О+) і n (ОН-) — молярні концентрації еквівалентів відповідно кислоти і основи, то
Буферна ємність Буферна ємність - це розрахункова величина, яка визначається кількістю еквівалентів сильної кислоти n (1/1 НСІ) чи n(1/2 Н2SО4) або сильної основи n (1/1 NаОН), n(1/2 Вa(ОН)2) що треба додати до 1 л буферного розчину, щоб pН змінився на одиницю. Якщо В - буферна ємність, а n (Н3О+) і n (ОН-) — молярні концентрації еквівалентів відповідно кислоти і основи, то
 БУФЕРНІ СИСТЕМИ ОРГАНІЗМУ Гідрогенкарбонатна:Н2СО3+NaHCO3 (в еритроцитах і позаклітинних рідинах) Фосфатна:NaH2PO4+ Na2HPO4 (у клітинах, сечі, плазмі) Гемоглобінова:HРb+HHbO2 (в еритроцитах) Білкова:альбуміни плазми крові (у клітинах і тканинах)
БУФЕРНІ СИСТЕМИ ОРГАНІЗМУ Гідрогенкарбонатна:Н2СО3+NaHCO3 (в еритроцитах і позаклітинних рідинах) Фосфатна:NaH2PO4+ Na2HPO4 (у клітинах, сечі, плазмі) Гемоглобінова:HРb+HHbO2 (в еритроцитах) Білкова:альбуміни плазми крові (у клітинах і тканинах)
 Осмос Осмос - направлене переміщення розчинника із розчину меншої концентрації в розчин більшої концентрації якщо розчини різної концентрації розділити напівпроникною перегородкою. Осмос протікає проти градієнту концентрації. осмотичний тиск - тиск, який треба прикласти до розчину, щоб зупинити осмос
Осмос Осмос - направлене переміщення розчинника із розчину меншої концентрації в розчин більшої концентрації якщо розчини різної концентрації розділити напівпроникною перегородкою. Осмос протікає проти градієнту концентрації. осмотичний тиск - тиск, який треба прикласти до розчину, щоб зупинити осмос
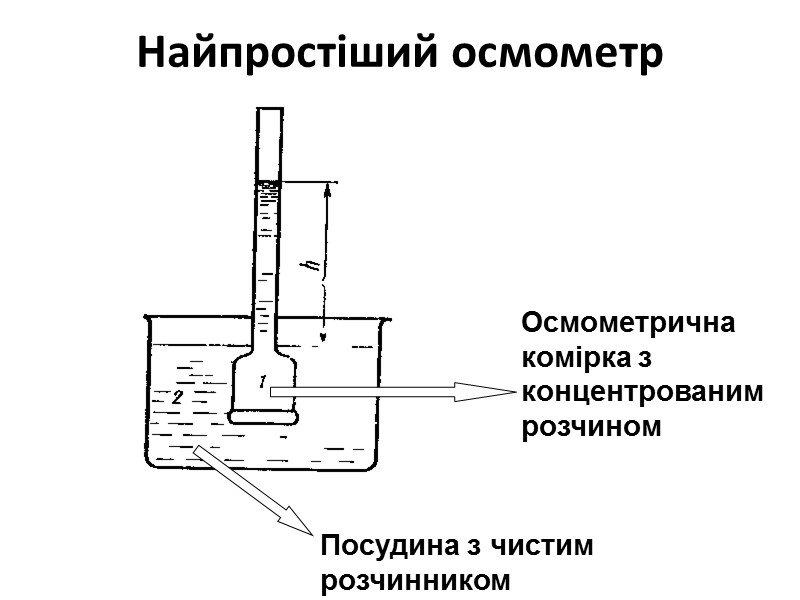
 Найпростіший осмометр
Найпростіший осмометр
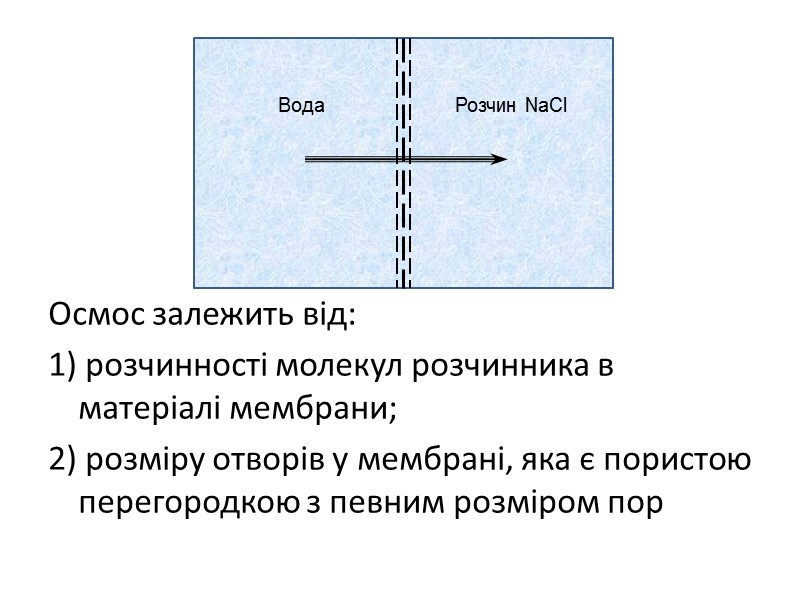
 Осмос залежить від: 1) розчинності молекул розчинника в матеріалі мембрани; 2) розміру отворів у мембрані, яка є пористою перегородкою з певним розміром пop
Осмос залежить від: 1) розчинності молекул розчинника в матеріалі мембрани; 2) розміру отворів у мембрані, яка є пористою перегородкою з певним розміром пop
 закон Вант-Гоффа осмотичний тиск розчину прямо пропорційний молярній концентрації і абсолютній температурі розчину. Для неелектролітів: π=CRT Для електролітів: π=іCRT Осмотичний тиск крові людини при 37 °С (310 К) 7,4 - 7,7 атм, або 740-780 кПа.
закон Вант-Гоффа осмотичний тиск розчину прямо пропорційний молярній концентрації і абсолютній температурі розчину. Для неелектролітів: π=CRT Для електролітів: π=іCRT Осмотичний тиск крові людини при 37 °С (310 К) 7,4 - 7,7 атм, або 740-780 кПа.
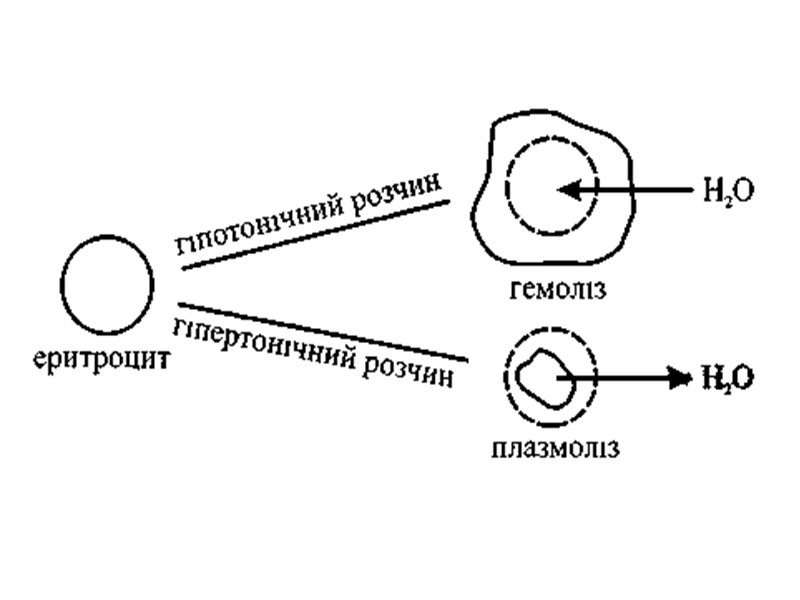
 онкотичний тиск 3,5 — 3,9 кПа. 0,5% загального тиску крові складають білки осмомолярна концентрація розчинених в плазмі речовин 0,287-0,303 моль/л. ізотонічний розчин з осмотичним тиском, що дорівнює осмотичному тиску прийнятого за стандарт гіпертонічний розчин з осмотичним тиском вищим, гіпотонічний – нижчим за стандарт . В медицині ізотонічними називають розчини з осмотичним тиском плазми крові. 0,85%-0,90% NaCl (0,146 моль/л) розчин глюкози 4,5 - 5% (0,3 моль/л).
онкотичний тиск 3,5 — 3,9 кПа. 0,5% загального тиску крові складають білки осмомолярна концентрація розчинених в плазмі речовин 0,287-0,303 моль/л. ізотонічний розчин з осмотичним тиском, що дорівнює осмотичному тиску прийнятого за стандарт гіпертонічний розчин з осмотичним тиском вищим, гіпотонічний – нижчим за стандарт . В медицині ізотонічними називають розчини з осмотичним тиском плазми крові. 0,85%-0,90% NaCl (0,146 моль/л) розчин глюкози 4,5 - 5% (0,3 моль/л).


