 Розчин та його компоненти: розчинник, розчинена речовина. Вода як розчинник. Будова молекули води, поняття про водневий зв’язок
Розчин та його компоненти: розчинник, розчинена речовина. Вода як розчинник. Будова молекули води, поняття про водневий зв’язок
 Відповісти на питання ØНа які дві групи поділяються дисперсні системи? ØЯкі розчини називаються колоїдними? ØЯкі розчини називаються істинними? ØЗ яких компонентів складається розчин? ØЧи можна стверджувати, що розчини мають постійний склад? Чому?
Відповісти на питання ØНа які дві групи поділяються дисперсні системи? ØЯкі розчини називаються колоїдними? ØЯкі розчини називаються істинними? ØЗ яких компонентів складається розчин? ØЧи можна стверджувати, що розчини мають постійний склад? Чому?
 Розчини — це багатокомпонентні системи. Один із компонентів називається розчинником. Зазвичай це речовина, що перебуває в тому ж агрегатному стані, що й розчин.
Розчини — це багатокомпонентні системи. Один із компонентів називається розчинником. Зазвичай це речовина, що перебуває в тому ж агрегатному стані, що й розчин.
 Вода — універсальний розчинник усіх речовин на Землі. • Наведіть приклади водних розчинів • Наведіть приклади неводних розчинів
Вода — універсальний розчинник усіх речовин на Землі. • Наведіть приклади водних розчинів • Наведіть приклади неводних розчинів
 За реакцією з водою всі речовини поділяються на три групи: Øрозчинні; Øмалорозчинні; Øпрактично нерозчинні.
За реакцією з водою всі речовини поділяються на три групи: Øрозчинні; Øмалорозчинні; Øпрактично нерозчинні.
 — Як можна пояснити таку особливість молекул води?
— Як можна пояснити таку особливість молекул води?
 Тип зв’язку — ковалентний полярний, кут зв’язку — 104, 5°. Тип кристалічної ґратки — молекулярний.
Тип зв’язку — ковалентний полярний, кут зв’язку — 104, 5°. Тип кристалічної ґратки — молекулярний.
 — Ґратка молекулярна? Чому ж за нормальних умов вода — рідина? Молекула води полярна — диполь. Між молекулами води виникає взаємне притягання за температури менш ніж 100°С. Такий зв’язок називається водневим.
— Ґратка молекулярна? Чому ж за нормальних умов вода — рідина? Молекула води полярна — диполь. Між молекулами води виникає взаємне притягання за температури менш ніж 100°С. Такий зв’язок називається водневим.
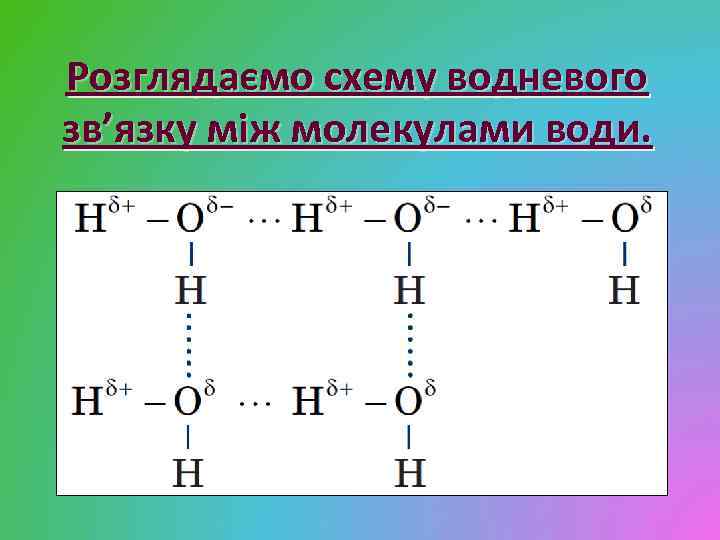 Розглядаємо схему водневого зв’язку між молекулами води.
Розглядаємо схему водневого зв’язку між молекулами води.
 Заповнюємо опорну схему Молекулярна формула: ____ Структурна формула: ____ M(H 2 O) ____________
Заповнюємо опорну схему Молекулярна формула: ____ Структурна формула: ____ M(H 2 O) ____________
 Поширення в природі В організмі людини: ______ На Землі: ___________ У Космосі: __________
Поширення в природі В організмі людини: ______ На Землі: ___________ У Космосі: __________
 Фізичні властивості За атмосферного тиску 1 атм: Ткип = 100°С, Тплав = 0°С, ρ = 1 г/см 3. Агрегатні стани:
Фізичні властивості За атмосферного тиску 1 атм: Ткип = 100°С, Тплав = 0°С, ρ = 1 г/см 3. Агрегатні стани:
 Хімічні властивості 1. H 2 O + Me 2 On → Me(OH)n (якщо Ме — активний, а основа — розчинна або малорозчинна) Na 2 O + H 2 O → Ca. O + H 2 O → Cu. O + H 2 O →
Хімічні властивості 1. H 2 O + Me 2 On → Me(OH)n (якщо Ме — активний, а основа — розчинна або малорозчинна) Na 2 O + H 2 O → Ca. O + H 2 O → Cu. O + H 2 O →
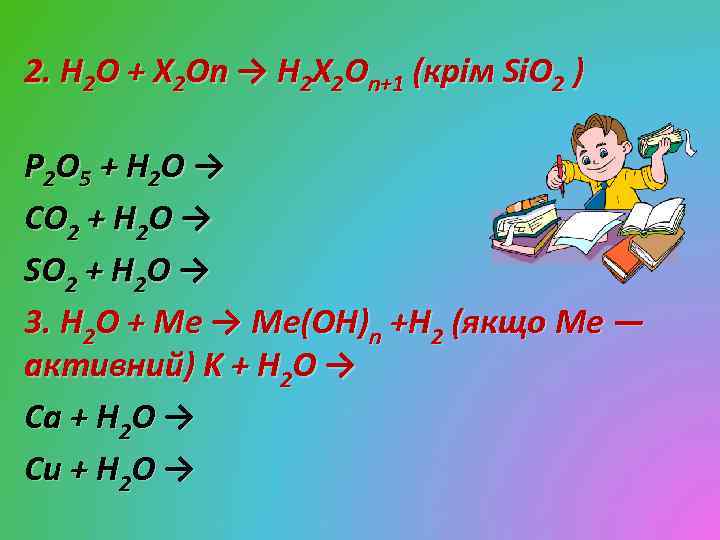 2. H 2 O + X 2 On → H 2 X 2 On+1 (крім Si. O 2 ) P 2 O 5 + H 2 O → CO 2 + H 2 O → SO 2 + H 2 O → 3. H 2 O + Me → Me(OH)n +H 2 (якщо Ме — активний) K + H 2 O → Ca + H 2 O → Cu + H 2 O →
2. H 2 O + X 2 On → H 2 X 2 On+1 (крім Si. O 2 ) P 2 O 5 + H 2 O → CO 2 + H 2 O → SO 2 + H 2 O → 3. H 2 O + Me → Me(OH)n +H 2 (якщо Ме — активний) K + H 2 O → Ca + H 2 O → Cu + H 2 O →
 Завдання 1 Обчисліть масу води, що утворюється внаслідок згоряння водню об’ємом 1, 12 л (за н. у. ). Обчисліть об’єм пари води цієї маси. Завдання 2 Обчисліть масу лугу, що утворюється в процесі розчинення у воді калію масою 3, 9 г.
Завдання 1 Обчисліть масу води, що утворюється внаслідок згоряння водню об’ємом 1, 12 л (за н. у. ). Обчисліть об’єм пари води цієї маси. Завдання 2 Обчисліть масу лугу, що утворюється в процесі розчинення у воді калію масою 3, 9 г.
 Домашнє завдання Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи. Розв’язати задачу: Обчисліть, яку масу сульфатної кислоти можна одержати з 3, 2 г сірки.
Домашнє завдання Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи. Розв’язати задачу: Обчисліть, яку масу сульфатної кислоти можна одержати з 3, 2 г сірки.