Sibur_AK_97-2003.ppt
- Количество слайдов: 25
 Российский химико-технологический университет им. Д. И. Менделеева Кафедра основного органического и нефтехимического синтеза Технологии Сибура Технология акриловой кислоты Мировое производство – 4, 4 млн. т/год Гусакова Д. Д. Москва, 2013
Российский химико-технологический университет им. Д. И. Менделеева Кафедра основного органического и нефтехимического синтеза Технологии Сибура Технология акриловой кислоты Мировое производство – 4, 4 млн. т/год Гусакова Д. Д. Москва, 2013
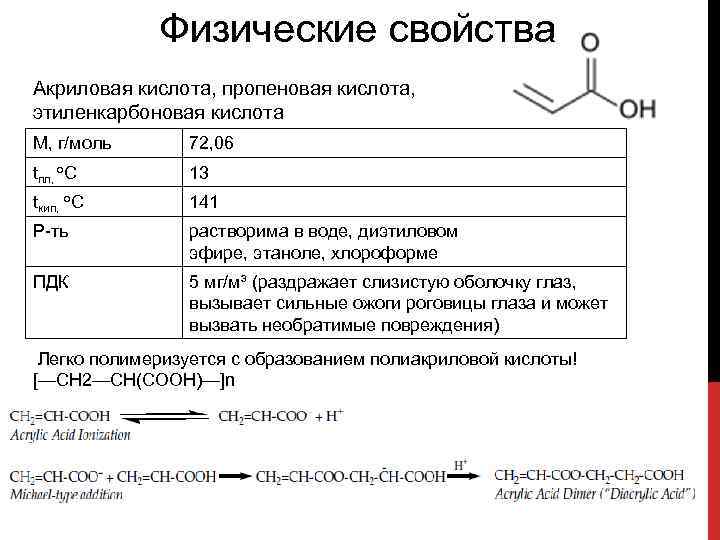 Физические свойства Акриловая кислота, пропеновая кислота, этиленкарбоновая кислота M, г/моль 72, 06 tпл, о. С 13 tкип, о. С 141 Р-ть растворима в воде, диэтиловом эфире, этаноле, хлороформе ПДК 5 мг/м³ (раздражает слизистую оболочку глаз, вызывает сильные ожоги роговицы глаза и может вызвать необратимые повреждения) Легко полимеризуется с образованием полиакриловой кислоты! [—СН 2—СН(СООН)—]n
Физические свойства Акриловая кислота, пропеновая кислота, этиленкарбоновая кислота M, г/моль 72, 06 tпл, о. С 13 tкип, о. С 141 Р-ть растворима в воде, диэтиловом эфире, этаноле, хлороформе ПДК 5 мг/м³ (раздражает слизистую оболочку глаз, вызывает сильные ожоги роговицы глаза и может вызвать необратимые повреждения) Легко полимеризуется с образованием полиакриловой кислоты! [—СН 2—СН(СООН)—]n
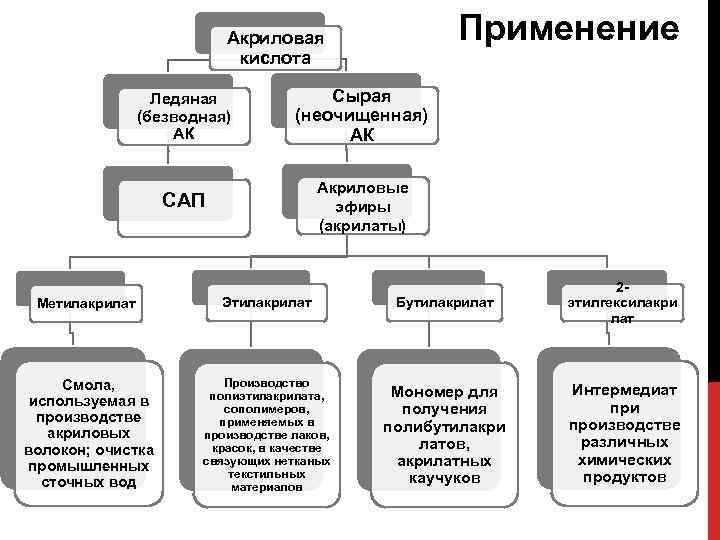 Применение Акриловая кислота Ледяная (безводная) АК Сырая (неочищенная) АК САП Акриловые эфиры (акрилаты) Метилакрилат Этилакрилат Бутилакрилат 2 этилгексилакри лат Cмола, используемая в производстве акриловых волокон; очистка промышленных сточных вод Производство полиэтилакрилата, сополимеров, применяемых в производстве лаков, красок, в качестве связующих нетканых текстильных материалов Мономер для получения полибутилакри латов, акрилатных каучуков Интермедиат при производстве различных химических продуктов
Применение Акриловая кислота Ледяная (безводная) АК Сырая (неочищенная) АК САП Акриловые эфиры (акрилаты) Метилакрилат Этилакрилат Бутилакрилат 2 этилгексилакри лат Cмола, используемая в производстве акриловых волокон; очистка промышленных сточных вод Производство полиэтилакрилата, сополимеров, применяемых в производстве лаков, красок, в качестве связующих нетканых текстильных материалов Мономер для получения полибутилакри латов, акрилатных каучуков Интермедиат при производстве различных химических продуктов
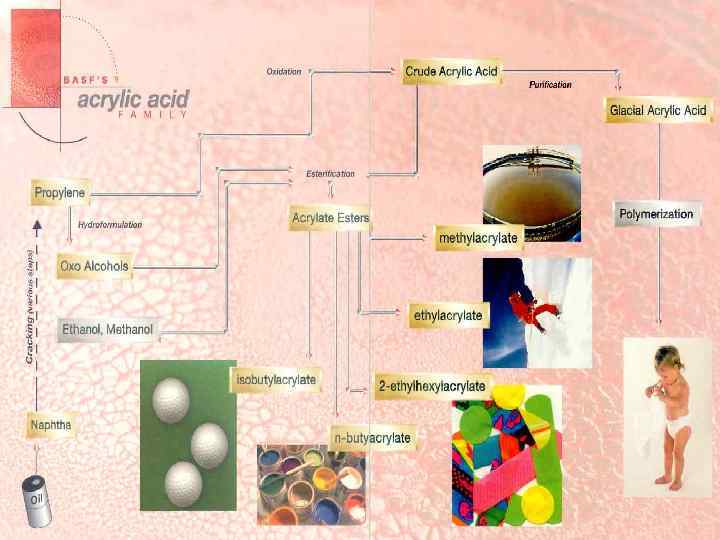
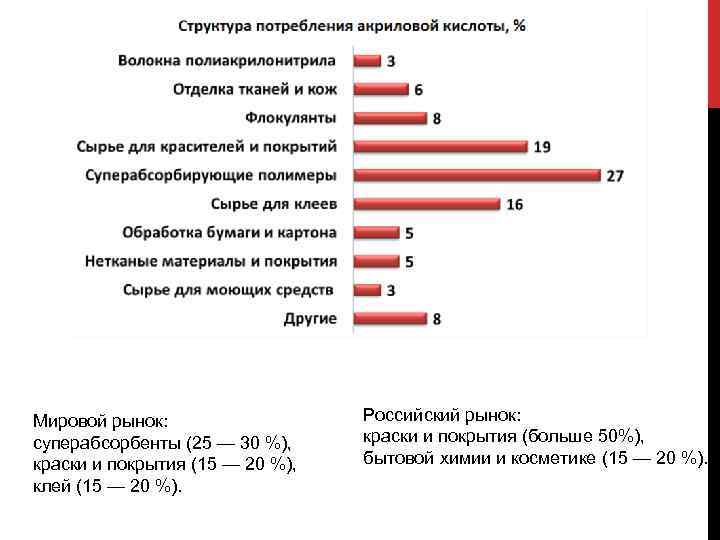 Мировой рынок: суперабсорбенты (25 — 30 %), краски и покрытия (15 — 20 %), клей (15 — 20 %). Российский рынок: краски и покрытия (больше 50%), бытовой химии и косметике (15 — 20 %).
Мировой рынок: суперабсорбенты (25 — 30 %), краски и покрытия (15 — 20 %), клей (15 — 20 %). Российский рынок: краски и покрытия (больше 50%), бытовой химии и косметике (15 — 20 %).
 Одним из основных методов получения эфиров акриловой кислоты является прямая этерификация кислот спиртами жидкая фаза, под вакуумом (остаточное давление 20 -100 к. Па), t = 70 -100 o. C Kt – серная кислота (+антиоксиданты) или катионные ионообменные смолы Преимущества ионообменных смол по сравнению с гомогенными катализаторами: • легкость отделения реакционной массы от катализатора; • селективность действия ионитов, т. е. в образование эфиров с высоким выходом и хорошим качеством; • не требуется отмывки продукта; • исключается или уменьшается коррозия аппаратуры.
Одним из основных методов получения эфиров акриловой кислоты является прямая этерификация кислот спиртами жидкая фаза, под вакуумом (остаточное давление 20 -100 к. Па), t = 70 -100 o. C Kt – серная кислота (+антиоксиданты) или катионные ионообменные смолы Преимущества ионообменных смол по сравнению с гомогенными катализаторами: • легкость отделения реакционной массы от катализатора; • селективность действия ионитов, т. е. в образование эфиров с высоким выходом и хорошим качеством; • не требуется отмывки продукта; • исключается или уменьшается коррозия аппаратуры.
 Способы получения акриловой кислоты В промышленности нашли применение следующие способы получения акриловой кислоты: гидролиз этиленциангидрина; гидролиз акрилонитрила; гидрокарбоксилирование ацетилена; окислительное карбонилирование этилена; окисление пропилена в паровой фазе с промежуточным образованием акролеина.
Способы получения акриловой кислоты В промышленности нашли применение следующие способы получения акриловой кислоты: гидролиз этиленциангидрина; гидролиз акрилонитрила; гидрокарбоксилирование ацетилена; окислительное карбонилирование этилена; окисление пропилена в паровой фазе с промежуточным образованием акролеина.
 Гидролиз этиленциангидрина метод разработан фирмой "Union Carbide " • взаимодействие этиленоксида с циангидрином t > 90 o. C (без катализатора) t = 55 -60 o. C Kt - Na. OH, Ca. O, Mg. CO 3, цианиды щелочноземельных металлов или третичные амины • гидролиз этиленциангидрина t = 150 o. C 75 -80%-ная серная кислота Общий выход акриловой кислоты не превышает 60 -70% Последняя действовавшая установка по этому методу была остановлена в 1971 г
Гидролиз этиленциангидрина метод разработан фирмой "Union Carbide " • взаимодействие этиленоксида с циангидрином t > 90 o. C (без катализатора) t = 55 -60 o. C Kt - Na. OH, Ca. O, Mg. CO 3, цианиды щелочноземельных металлов или третичные амины • гидролиз этиленциангидрина t = 150 o. C 75 -80%-ная серная кислота Общий выход акриловой кислоты не превышает 60 -70% Последняя действовавшая установка по этому методу была остановлена в 1971 г
 Гидролиз акрилонитрила водная среда t = 50 -80 o. C Kt – серная кислота Гидролиз нитрилов является экономически непривлекательным из-за низкого выхода и большого количества отходов (NH 4 HSO 4). От процесса отказались Ugine Kuhlmann, Mitsubishi Petrochemical и Mitsubishi Rayon. Тем не менее, он попрежнему эксплуатируется в Asahi Chemical
Гидролиз акрилонитрила водная среда t = 50 -80 o. C Kt – серная кислота Гидролиз нитрилов является экономически непривлекательным из-за низкого выхода и большого количества отходов (NH 4 HSO 4). От процесса отказались Ugine Kuhlmann, Mitsubishi Petrochemical и Mitsubishi Rayon. Тем не менее, он попрежнему эксплуатируется в Asahi Chemical
 Гидрокарбоксилирование ацетилена (метод фирмы Rohm and Haas Co) t = 40 o. C p = 1 атм Ацетилен : CO = 1: 1 Kt - тетракарбонил никеля Процесс высокого давления Реппе (процесс фирмы Dow Badische Chemical Co, освоенный с 1960 г. ) t=200 °C p = 140 атм Kt - бромид никеля или меди (II) Данный процесс в значительной степени был заменен процессом прямого окисления пропилена. Хотя BASF до сих пор производит часть акриловой кислоты гидрокарбоксилированием ацетилена(91 тыс тонн/год).
Гидрокарбоксилирование ацетилена (метод фирмы Rohm and Haas Co) t = 40 o. C p = 1 атм Ацетилен : CO = 1: 1 Kt - тетракарбонил никеля Процесс высокого давления Реппе (процесс фирмы Dow Badische Chemical Co, освоенный с 1960 г. ) t=200 °C p = 140 атм Kt - бромид никеля или меди (II) Данный процесс в значительной степени был заменен процессом прямого окисления пропилена. Хотя BASF до сих пор производит часть акриловой кислоты гидрокарбоксилированием ацетилена(91 тыс тонн/год).
 Окислительное карбонилирование этилена метод разработан фирмой "Union Oil" СН 2=СН 2 + Pd. Cl 2 + Н 2 О + СО → СН 2=СН—СООН + Pd + 2 НСl Pd + 2 Cu. Cl 2 → 2 Cu. Cl + Pd. Cl 2 2 Cu. Cl + 2 HCl + 0, 5 О 2→H 2 O + 2 Cu. Cl 2 t = 135 -150 o. C p = 75 атм (ж. ф. ) Kt - хлориды палладия и меди Побочная реакция: СН 2=СН 2 + СО + 0, 5 O 2 + СН 3 СООН→СН 3 СООСН 2 СООН Выход акриловой кислоты 60 -70%
Окислительное карбонилирование этилена метод разработан фирмой "Union Oil" СН 2=СН 2 + Pd. Cl 2 + Н 2 О + СО → СН 2=СН—СООН + Pd + 2 НСl Pd + 2 Cu. Cl 2 → 2 Cu. Cl + Pd. Cl 2 2 Cu. Cl + 2 HCl + 0, 5 О 2→H 2 O + 2 Cu. Cl 2 t = 135 -150 o. C p = 75 атм (ж. ф. ) Kt - хлориды палладия и меди Побочная реакция: СН 2=СН 2 + СО + 0, 5 O 2 + СН 3 СООН→СН 3 СООСН 2 СООН Выход акриловой кислоты 60 -70%
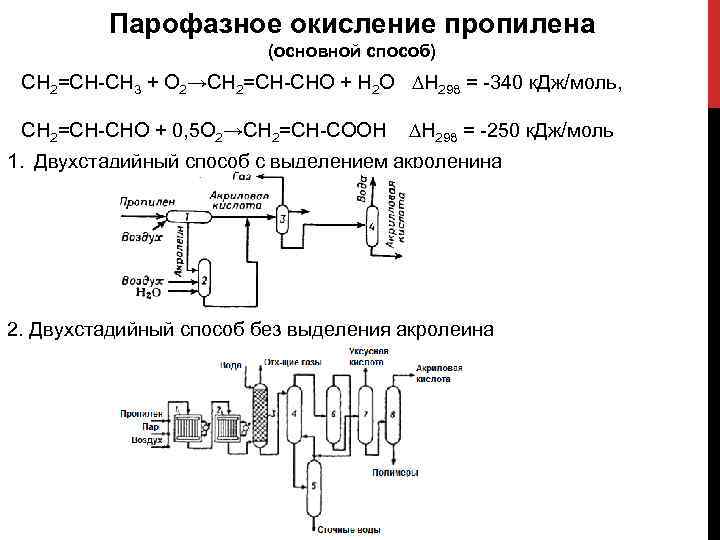 Парофазное окисление пропилена (основной способ) CH 2=CH-CH 3 + O 2→CH 2=CH-CHO + H 2 O ∆H 298 = -340 к. Дж/моль, СН 2=СН-СНО + 0, 5 O 2→СН 2=СН-СООН ∆Н 298 = -250 к. Дж/моль 1. Двухстадийный способ с выделением акроленина 2. Двухстадийный способ без выделения акролеина
Парофазное окисление пропилена (основной способ) CH 2=CH-CH 3 + O 2→CH 2=CH-CHO + H 2 O ∆H 298 = -340 к. Дж/моль, СН 2=СН-СНО + 0, 5 O 2→СН 2=СН-СООН ∆Н 298 = -250 к. Дж/моль 1. Двухстадийный способ с выделением акроленина 2. Двухстадийный способ без выделения акролеина
 1. 1 Окисление пропилена СН 2=СНСН 3 + О 2 → СН 2=СНСНО+Н 2 О Побочные реакции: t = 300 -350 o. C p = 1 -3 атм Kt - оксиды Bi, Со, Ni, Fe, Sn и др Мольное соотношение: вода : пропилен = 4 -5, воздух : пропилен = 2. Степень конверсии пропилена за один проход составляет 90 -95%, Выход акролеина и акриловой кислоты – 80 -90%.
1. 1 Окисление пропилена СН 2=СНСН 3 + О 2 → СН 2=СНСНО+Н 2 О Побочные реакции: t = 300 -350 o. C p = 1 -3 атм Kt - оксиды Bi, Со, Ni, Fe, Sn и др Мольное соотношение: вода : пропилен = 4 -5, воздух : пропилен = 2. Степень конверсии пропилена за один проход составляет 90 -95%, Выход акролеина и акриловой кислоты – 80 -90%.
 1. 2 Окисление акролеина СН 2=СН-СНО + 0, 5 O 2→СН 2=СН-СООН Побочные реакции – реакции полного окисления до СО, СО 2 и Н 2 О t = 250 -280 o. C p = 1 -2 атм Время контакта - 0. 5 -2 с. в присутствии водяного пара Kt - Mо. O 3 > V 2 O 5 > WO 3 > Se. O 2 > Ta 2 O 5 >Cr. O 3 Мольное соотношение вода: акролеин = 2 : 1 Степень конверсии за один проход составляет 95 -97%, Выход АК- более 93% в расчете на акролеин, 84% - на пропилен. Вещество t кип, °C Примечание пропилен − 47. 6 Пределы воспламенения в воздухе 2. 3 -11. 1% акролеин 52, 7 Азеотроп с водой tкип = 52, 36°С (97, 4% акролеина) ацетальдегид 20. 2 - акриловая кислота 141 -
1. 2 Окисление акролеина СН 2=СН-СНО + 0, 5 O 2→СН 2=СН-СООН Побочные реакции – реакции полного окисления до СО, СО 2 и Н 2 О t = 250 -280 o. C p = 1 -2 атм Время контакта - 0. 5 -2 с. в присутствии водяного пара Kt - Mо. O 3 > V 2 O 5 > WO 3 > Se. O 2 > Ta 2 O 5 >Cr. O 3 Мольное соотношение вода: акролеин = 2 : 1 Степень конверсии за один проход составляет 95 -97%, Выход АК- более 93% в расчете на акролеин, 84% - на пропилен. Вещество t кип, °C Примечание пропилен − 47. 6 Пределы воспламенения в воздухе 2. 3 -11. 1% акролеин 52, 7 Азеотроп с водой tкип = 52, 36°С (97, 4% акролеина) ацетальдегид 20. 2 - акриловая кислота 141 -

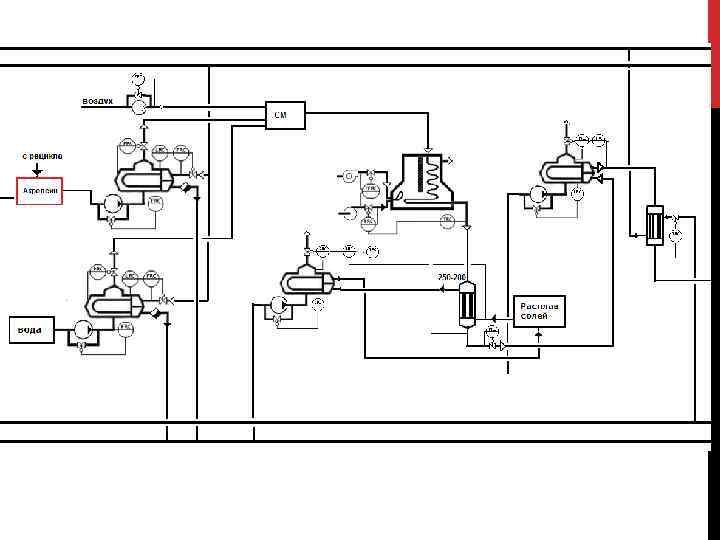
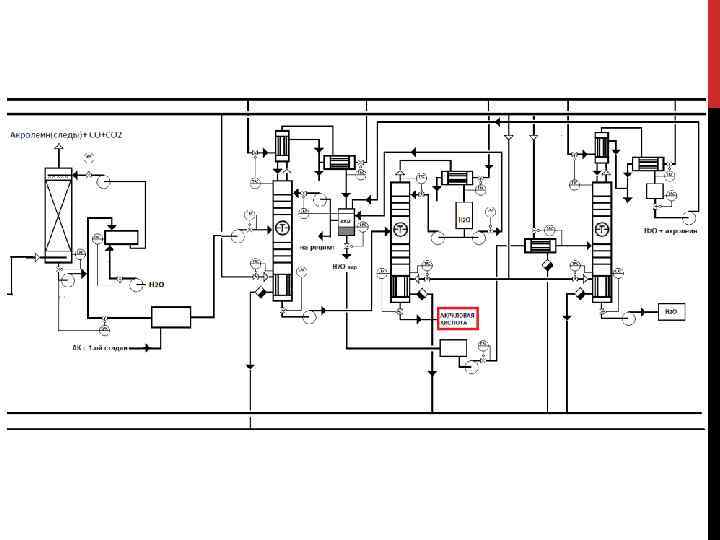
 2. В промышленности акриловую кислоту получают двухстадийным способом окисления пропилена без разделения и очистки образующегося на первой стадии акролеина. Побочные реакции: • Побочные реакции при получении акролеина; • Реакции дальнейшего окисления побочных продуктов, полученных при окислении акролеина (значительное количество уксусной кислоты); • Реакции полного окисления до СО, СО 2 и Н 2 О. Условия процесса – аналогичны условиям процесса получения акриловой кислоты с промежуточным выделением акролеина Конверсия пропилена - 99, 3% Селективность акриловой кислоты – 95, 5% Выход – 94, 8%
2. В промышленности акриловую кислоту получают двухстадийным способом окисления пропилена без разделения и очистки образующегося на первой стадии акролеина. Побочные реакции: • Побочные реакции при получении акролеина; • Реакции дальнейшего окисления побочных продуктов, полученных при окислении акролеина (значительное количество уксусной кислоты); • Реакции полного окисления до СО, СО 2 и Н 2 О. Условия процесса – аналогичны условиям процесса получения акриловой кислоты с промежуточным выделением акролеина Конверсия пропилена - 99, 3% Селективность акриловой кислоты – 95, 5% Выход – 94, 8%
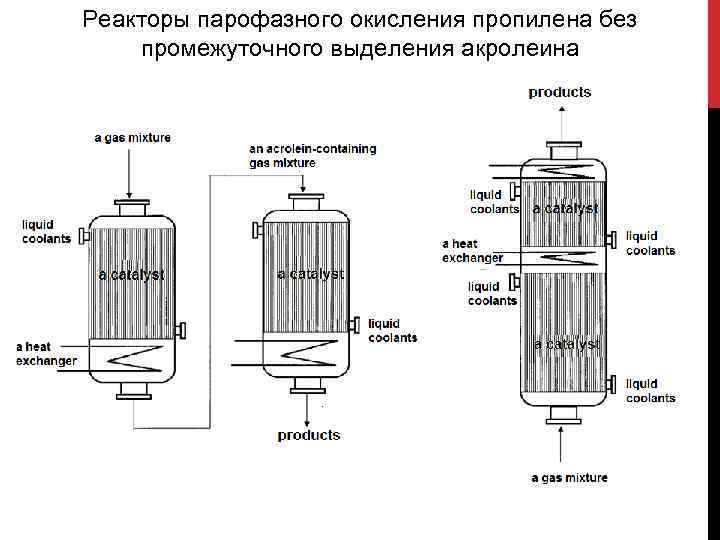 Реакторы парофазного окисления пропилена без промежуточного выделения акролеина
Реакторы парофазного окисления пропилена без промежуточного выделения акролеина
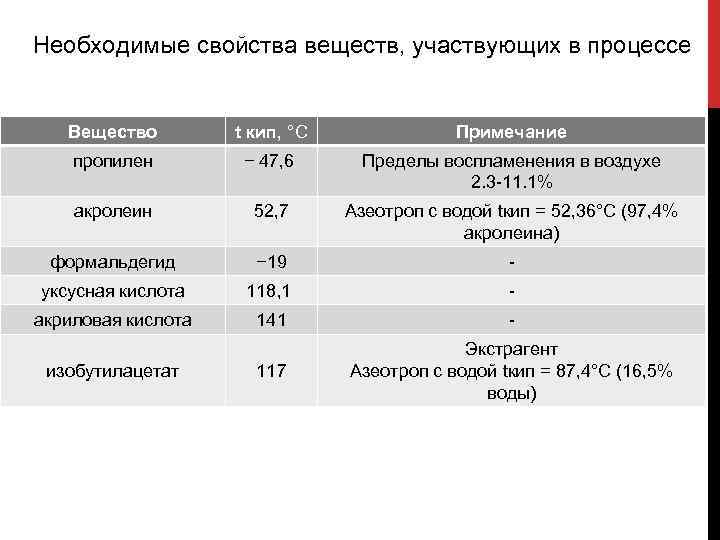 Необходимые свойства веществ, участвующих в процессе Вещество t кип, °C Примечание пропилен − 47, 6 Пределы воспламенения в воздухе 2. 3 -11. 1% акролеин 52, 7 Азеотроп с водой tкип = 52, 36°С (97, 4% акролеина) формальдегид − 19 - уксусная кислота 118, 1 - акриловая кислота 141 - 117 Экстрагент Азеотроп с водой tкип = 87, 4°С (16, 5% воды) изобутилацетат
Необходимые свойства веществ, участвующих в процессе Вещество t кип, °C Примечание пропилен − 47, 6 Пределы воспламенения в воздухе 2. 3 -11. 1% акролеин 52, 7 Азеотроп с водой tкип = 52, 36°С (97, 4% акролеина) формальдегид − 19 - уксусная кислота 118, 1 - акриловая кислота 141 - 117 Экстрагент Азеотроп с водой tкип = 87, 4°С (16, 5% воды) изобутилацетат

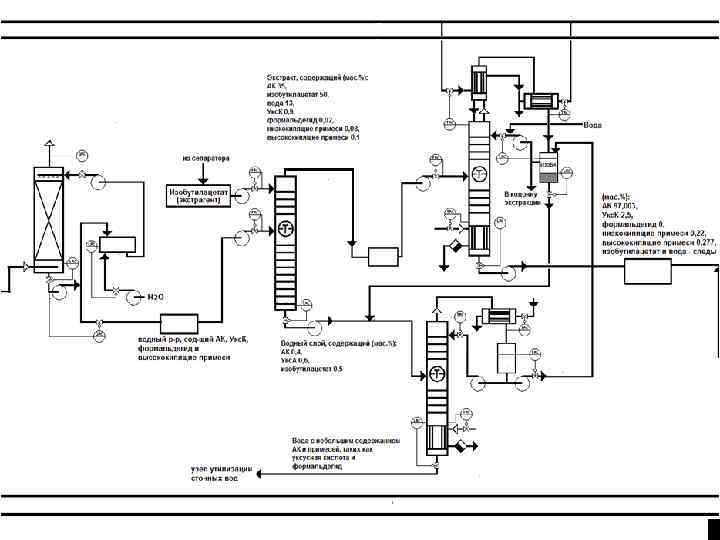
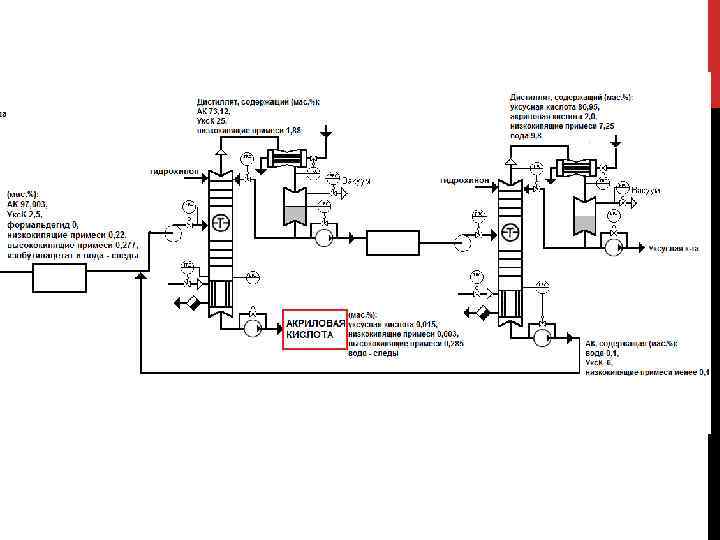
 Производство акриловой кислоты в России осуществляется на ОАО «Акрилат» (г. Дзержинск), 100% акций которого принадлежат компании СИБУР Производство акриловой кислоты введено в эксплуатацию: ноябрь 2004 г. Поставщик технологического процесса – компания NISSHO IWAI. Производственные мощности ОАО «Акрилат» составляют: - 25 тыс. т/год акриловой кислоты эфирного сорта, - 2 тыс. т/год акриловой кислоты полимерного сорта, - 36 тыс. т/год тяжелых эфиров (бутилакрилат) и - 10 тыс. т/год легких эфиров (метил- и этилакрилат). Планируется! В 2015 году в ОАО «Газпром Нефтехим Салават» на проектную мощность выйдет новый технологический комплекс по производству акриловой кислоты и ее эфиров В него войдут производства с годовой мощностью: - 80 тыс. т акриловой кислоты, - 80 тыс. т. бутилакрилата , - 35 тыс. т. ледяной акриловой кислоты.
Производство акриловой кислоты в России осуществляется на ОАО «Акрилат» (г. Дзержинск), 100% акций которого принадлежат компании СИБУР Производство акриловой кислоты введено в эксплуатацию: ноябрь 2004 г. Поставщик технологического процесса – компания NISSHO IWAI. Производственные мощности ОАО «Акрилат» составляют: - 25 тыс. т/год акриловой кислоты эфирного сорта, - 2 тыс. т/год акриловой кислоты полимерного сорта, - 36 тыс. т/год тяжелых эфиров (бутилакрилат) и - 10 тыс. т/год легких эфиров (метил- и этилакрилат). Планируется! В 2015 году в ОАО «Газпром Нефтехим Салават» на проектную мощность выйдет новый технологический комплекс по производству акриловой кислоты и ее эфиров В него войдут производства с годовой мощностью: - 80 тыс. т акриловой кислоты, - 80 тыс. т. бутилакрилата , - 35 тыс. т. ледяной акриловой кислоты.
 Спасибо за внимание!
Спасибо за внимание!


