e0f57717d398ac8053f185d35d7860e3.ppt
- Количество слайдов: 50

Российский университет дружбы народов Кафедра управления и экономики фармации Система качества, эффективности, безопасности лекарственных средств Доктор фармацевтических наук, профессор Лагуткина Татьяна Петровна

Главная задача системы государственного контроля качества ЛС защита потребителей от негативных последствий применения лекарственных средств, что может быть связано с: l l недостаточной изученностью ЛС на этапе разрешения и внедрения в практику ЛС выпуском внутри страны или ввозом в страну субстандартных ЛС нарушениями условий хранения лекарственных средств на любом из этапов товародвижения ЛС нарушениями условий реализации ЛС

Система качества, эффективности, безопасности лекарственных средств l федеральный уровень l территориальный уровень l производственный уровень

1. Федеральный уровень l МЗ РФ - Департамент государственного регулирования обращения ЛС l МЗ РФ - Департамент лекарственного обеспечения и регулирования обращения МИ l Научный центр экспертизы средств медицинского применения l Федеральная служба по надзору в сфере здравоохранения и социального развития (Росздравнадзор)

Задачи федерального уровня государственная регистрация ЛП и МИ l организация экспертизы ЛС l организация этической экспертизы возможности проведения клинического исследования ЛП l государственный контроль l мониторинг безопасности ЛП (фармаконадзор) l


Государственная регистрация ЛП 1) регистрации подлежат: • ЛП, впервые вводимые в обращение в РФ; • ЛП, зарегистрированные ранее, но произведенные в других лекарственных формах, в новой дозировке при доказательстве ее клинической значимости и эффективности; • новые комбинации зарегистрированных ранее ЛП. 2) регистрация ЛП осуществляется по результатам экспертизы ЛС, а регистрация орфанных ЛП дополнительно требует экспертизы документов, представленных для определения возможности рассматривать ЛП в качестве орфанного ЛП. 3) регистрация осуществляется по результатам экспертизы ЛС и этической экспертизы возможности проведения клинического исследования ЛС для медицинского применения. 4) регистрация осуществляется в срок, не превышающий 160 рабочих дней со дня принятия заявления о государственной регистрации ЛП.

Государственной регистрации не подлежат: 1) ЛП, изготовленные аптечными организациями, ветеринарными аптечными организациями, индивидуальными предпринимателями, которые имеют лицензию на фармацевтическую деятельность, по рецептам на ЛП и требованиям медицинских организаций, ветеринарных организаций; 2) ЛП, приобретенные физическими лицами за пределами РФ и предназначенные для личного использования; 3) ЛП , ввозимые в РФ для оказания медицинской помощи по жизненным показаниям конкретного пациента на основании разрешения, выданного уполномоченным федеральным органом исполнительной власти; 4) ЛС, ввозимые в РФ для проведения клинических исследований ЛП и (или) проведения экспертизы ЛС для осуществления государственной регистрации ЛП ; 5) фармацевтические субстанции; 6) радиофармацевтические ЛП, изготовленные непосредственно в медицинских организациях; 7) ЛП, производимые для экспорта.

Не допускается государственная регистрация 1) ЛП, отличающихся друг от друга качественным составом действующих веществ, под одинаковым торговым наименованием; 2) одного ЛП, выпускаемого производителем под различными торговыми наименованиями и представленного на государственную регистрацию в виде двух и более лекарственных препаратов.

Иммунобиологические лекарственные препараты ЛП, предназначенные для формирования иммунитета, или диагностики наличия иммунитета, или диагностики/выработки специфического приобретенного изменения иммунологического ответа на аллергизирующие вещества (вакцины, анатоксины, сыворотки, иммуноглобулины и аллергены)

Радиофармацевтические лекарственные средства, которые содержат в готовой для использования форме один радионуклид или несколько радионуклидов (радиоактивных изотопов)

Биоаналоговый (биоподобный) ЛП(биоаналог) биологический ЛП, схожий по параметрам качества, эффективности и безопасности с референтным биологическим ЛП в такой же лекарственной форме и имеющий идентичный способ введения

Воспроизведенный ЛП ЛП, который имеет такой же качественный состав и количественный состав действующих веществ в такой же лекарственной форме, что и референтный ЛП, биоэквивалентность или терапевтическая эквивалентность которого референтному ЛП подтверждена соответствующими исследованиями

Референтный ЛП ЛП, впервые зарегистрированный в РФ, качество, эффективность и безопасность которого доказаны на основании результатов доклинических и клинических исследований ЛП, и который используется для оценки биоэквивалентности или терапевтической эквивалентности, качества, эффективности и безопасности воспроизведенного или биоаналогового (биоподобного) ЛП

Взаимозаменяемый ЛП ЛП с доказанной терапевтической эквивалентностью или биоэквивалентностью в отношении референтного ЛП, имеющий эквивалентные ему качественный состав и количественный состав действующих веществ, состав вспомогательных веществ, лекарственную форму и способ введения.

Биодоступность ФЗ 61 скорость и степень, с которыми действующее вещество (его активная часть) высвобождается из лекарственной формы и становится доступным в системном кровотоке

Государственная регистрация ЛП для применения в условиях: военных действий, чрезвычайных ситуаций, профилактики и лечения заболеваний и поражений, полученных в результате воздействия неблагоприятных химических, биологических, радиационных факторов, и разработанных по заданию федеральных органов исполнительной власти, уполномоченных в области обороны страны и безопасности государства, осуществляется в порядке, установленном Правительством РФ

Регистрационное удостоверение ЛП 1)Регистрационное удостоверение ЛП с указанием лекарственных форм и дозировок выдается бессрочно, за исключением регистрационного удостоверения ЛП, выдаваемого сроком на 5 лет на впервые регистрируемые в РФ ЛП. 2) По истечении 5 лет выдается бессрочное регистрационное удостоверение ЛП при условии подтверждения его регистрации 3) Подтверждение государственной регистрации ЛП осуществляется по результатам экспертизы отношения ожидаемой пользы к возможному риску применения ЛП

Государственный (выборочный) контроль качества ЛС: 1) обработка сведений, в обязательном порядке предоставляемых субъектами обращения ЛС, о сериях, партиях ЛС, поступающих в гражданский оборот в РФ; 2) отбор образцов ЛС у субъектов обращения ЛС в целях проведения испытаний на их соответствие требованиям нормативной документации или нормативных документов; 3) принятие по результатам испытаний решения о дальнейшем гражданском обороте ЛС 4) принятие решения о переводе ЛС на посерийный выборочный контроль качества ЛС в случае повторного выявления несоответствия качества ЛС установленным требованиям и (при необходимости) о проверке субъекта обращения ЛС.

Проблемы недоброкачественности ЛС 1) неэффективное функционирование системы обеспечения качества, что приводит к производству продукции несоответствующего качества 2) нарушения правил хранения сырья и исходных материалов, включая размещение сырья и продукции, условия отбора проб и пр. 3) использование фармацевтических субстанций, не предусмотренных нормативной документацией 4) несоответствие помещений и оборудования условиям, требуемым для производства заявленных лекарственных средств, а также производство несовместимых лекарственных средств в одних производственных помещениях 5) отсутствие данных по валидации чистоты помещений, системы водоподготовки, критических технологических операций и пр.


Фармаконадзор (ст. 64 - 66 ФЗ «Об обращении ЛС» ) ЛП, находящиеся в обращении в РФ, подлежат мониторингу эффективности и безопасности в целях выявления возможных негативных последствий их применения, индивидуальной непереносимости, предупреждения медицинских работников, ветеринарных специалистов, пациентов или владельцев животных и их защиты от применения таких лекарственных препаратов.

Фармаконадзор осуществляется путем анализа предоставляемой субъектами обращения ЛС информации о: n побочных действиях, n нежелательных реакциях, серьезных нежелательных реакциях, непредвиденных нежелательных реакциях применении ЛП, n индивидуальной непереносимости, n отсутствии эффективности ЛП, n а также об иных фактах и обстоятельствах, представляющих угрозу жизни или здоровью человека либо животного применении ЛП и выявленных на всех этапах обращения ЛП в РФ и других государствах.

При выявлении информации о серьезных нежелательных реакциях и непредвиденных нежелательных реакциях применении ЛП, об особенностях их взаимодействия с другими ЛП, индивидуальной непереносимости, и т. д. , держатели или владельцы регистрационных удостоверений ЛП, обязаны принять меры, направленные на устранение негативных последствий применения таких ЛП, предупреждение причинения вреда жизни или здоровью человека , защиту их от применения таких ЛП, на дополнительный сбор данных об эффективности и безопасности таких ЛП. Крайняя мера – см. ст. 32 ФЗ 61

ВОЗ n n n Неблагоприятные реакции на лекарства (НРЛ) входят в число десяти ведущих причин смерти во многих странах. Большинство НРЛ можно предотвратить. В некоторых странах расходы, связанные с НРЛ, такие как: расходы на госпитализацию, хирургические вмешательства, превышают стоимость лекарственной терапии. Нет ни одного лекарства, прием которого не был бы сопряжен с риском. Тщательная оценка рисков и преимуществ лекарств способствует безопасности пациентов. Глобальный обмен информацией о побочных эффектах укрепляет безопасность лекарств в странах и может способствовать принятию своевременных решений для защиты безопасности пациентов в случае возникновения проблем.

Классификация рисков применения ЛС, FDA, 2009 Непредотвратимые (неуправляемые) риски 1. Отравления ЛС как следствие пробелов в современной науке a. b. выход новых ЛП на рынок использование ЛП не по зарегистрированным показаниям (метотрексат, тегретол, габапентин и др. ) 2. Отравления ЛС как Предотвратимые (управляемые) риски 1. Ошибки применения ЛС: l l l Информационные ошибки врача Информационные ошибки потребителя (пациента) Информационные ошибки фармацевтических специалистов следствие непредотвратимых известных побочных эффектов 2. Случайные отравления ЛП 3. Злоупотребления ЛП

Информационные ошибки врача нет полного доступа к информации о ЛП, либо не использует информацию о ЛП или пациенте Прописывание ЛП, l обладающих тератогенным действием, женщинам репродуктивного возраста (без теста на беременность) l не рекомендуемых к применению лицами старше 65 лет (список Бирса) l взаимодействующего с ЛП, который пациент уже принимает l без учета индивидуальных особенностей больного (аллергия на ЛП) l в завышенных дозах для подстраховки.

Информационные ошибки потребителей, которых не информировали о ЛП или они сами не в состоянии использовать информацию о ЛП. a. b. увеличение дозы для повышения эффективности или неосознанное использование несколько вариантов одного и того же ЛП одновременно недоступная для понимания потребителем маркировка ЛП и сопровождающая ЛП информация

Информационные ошибки фармацевтических специалистов l l l трудночитаемый почерк врача неясности в инструкции для использования ошибки в рецепте ЛП (пропущенный суффикс в названии ЛП и т. д. ) схожесть наименований ЛП схожесть внешнего вида упаковок одного ЛП разных дозировок или разных ЛП

ЛС, с которыми связан наибольший % ошибок у потребителей тамифлю - терафлю капотен - кларитин тиреотом - тиреокомб оцилококцинум - оцилак линекс - линкас флемоксин - флемоклав простамол - парацетамол бифоформ - бификол ранитидин - ремантадин норвесол - овесол темпалгин - пенталгин фенотропил - генотропин скинкап - скинорен долобене - гепабене кавинтон - гематон теравит - таривид ренисан - ранисан травесил - фенистил энам - энап бисакодил - бисептол

ЛС, с которыми связан наибольший % ошибок у специалистов Азилект Азитрал Амиксин Амиксид Аципол Ацизол Ванкоцин Видокцин Домперидон Дроперидол Кардил Карсил Листенон Инстенон Мекасол Мексидол Митотакс Микомакс Новинет Норилет Осетрон Орсотен Теветен Тенотен Трилептал Тримектал Цефекон Цераксон

II. Предотвратимые факторы отравлений (управляемые риски) 2. Случайные отравления ЛП Оценивается десятками тысяч случаев по каждой из стран, ведущих статистику. Особенно часто страдают дети в результате приема безрецептурных ЛП от кашля и простуды, прописанных другим членам семьи, особенно жидких ЛП, которые дети в возрасте от 2 до 5 лет в состоянии открыть и выпить.

II. Предотвратимые факторы отравлений (управляемые риски) 3. Злоупотребление ЛП l l постоянное или разовое преднамеренное избыточное потребление ЛП, несущее угрозу негативных последствий для физического и/или психического здоровья. включает наркотическое применение, суицидальное применение, прием с целью одурманивания, с целью опьянения, самолечение и, как частный случай этого, ошибочный чрезмерный прием. Именно этот комплекс причин явился точкой приложения нашего исследования.

Злоупотребление рецептурными ЛП (Rx ) США кодеинсодержащие, нейролептики, транквилизаторы, антидепрессанты, седативные, барбитураты, стероиды Канада нейролептики, транквилизаторы, седативные, барбитураты Германия нейролептики, транквилизаторы, седативные, барбитураты, стероиды Франция Способы получения Rx: поддельные рецепты, продажа рецептов, получение рецепта сразу у нескольких врачей, интернет – аптеки. l нейролептики, транквилизаторы, седативные, барбитураты, бензодиазепины Скандинавские нейролептики, транквилизаторы, седативные, барбитураты, бензодиазепины страны РФ противосудорожные кодеинсодержащие нейролептики антидепрессанты

Злоупотребление безрецептурными ЛП (ОТС) США Канада Германия ненаркотические анальгетики, противокашлевые(декстрометорфан), антигистаминные, противоотечные, седативные, слабительные противокашлевые(декстрометорфан) противоотечные (псевдоэфедрин), седативные, антигистаминные, слабительные ненаркотические анальгетики, противокашлевые(декстрометорфан), антигистаминные, противоотечные, седативные, слабительные l мужчины злоупотребляют больше, чем женщины, всеми группами, за исключением слабительных lпожилые люди анальгетиками, подростки – противокашлевыми, среднего возраста – остальными l с ростом доходов пожилые Англия противокашлевые(декстрометорфан) противоотечные (псевдоэфедрин), седативные, антигистаминные, слабительные люди начинают злоупотреблять алкоголем, молодые и среднего возраста – наркотическими средствами Иордания ненаркотические анальгетики, противокашлевые, противоотечные, антигистаминные препараты, слабительные средства l о росте злоупотребления ОТС РФ ненаркотические анальгетики кодеинсодержащие препаратами заявляют от 58 до 69% сотрудников аптек по разным странам и континентам

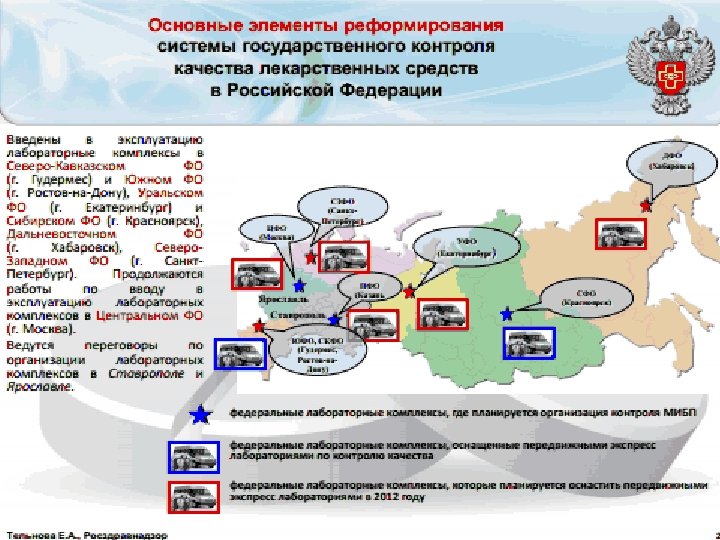
2. Территориальный уровень (уровень субъектов РФ) l l территориальные управления Росздравнадзора испытательные лаборатории, функционирующие в системе подтверждения соответствия ЛС центры контроля качества ЛС, осуществляющие экспертизу качества ЛС на основании договоров с субъектами обращения лекарственных средств федеральные лабораторные комплексы, на базе которых проводится контроль качества ЛС, находящихся в обращении, в рамках мероприятий по государственному контролю качества.

Задача территориального уровня государственный контроль обращения ЛС: l организация мероприятий по выявлению и предотвращению попадания в обращение субстандартных ЛС l организация проведения выборочного контроля качества ЛС l инспектирование организаций здравоохранения, аптечных учреждений по вопросам изготовления ЛС l контроль качества и оценка их соответствия, l организация проведения экспертизы качества ЛС.

3. Производственный уровень системы качества l предприятий – производителей ЛС, l дистрибьюторов ЛС l аптечных организаций

Задача производственного уровня обеспечение возможности приобретения потребителем качественных ЛС, что включает гарантирование сохранности качества ЛС, поступающих в аптечную организацию, и качества услуг по реализации ЛС.

Государственный информационный стандарт ЛС(ГИСЛС) (пр. МЗ РФ № 88 от 26. 03. 2001 г. ) требования и структура официальной информации о ЛС ГИСЛС состоит из 4 элементов 1. фармакопейная статья ЛС 2. формулярная статья ЛС 3. клинико-фармакологическая статья ЛП • типовая клинико-фармакологическая статья ЛС (ТКФС) • клинико-фармакологическая статья ЛП ( КФС) 4. паспорт ЛП.

1. Формулярная статья - это нормативный документ, содержащий стандартизированные по форме и содержанию сведения о применении ЛС при определенном заболевании. 2. ТКФС - это официальный документ, содержащий сведения об основных свойствах ЛС под международным непатентованным названием (МНН), разрабатывается экспертным органом и утверждается МЗ РФ. КФС - это официальный документ, который отражает совокупность клинико-фармакологических данных конкретного ЛП под определенным торговым наименованием и разрабатывается на основе соответствующей типовой клиникофармакологической статьи ЛС производителем, проходит экспертизу при регистрации и утверждается МЗ РФ. Паспорт лекарственного препарата - это официальный документ, содержащий обобщенную информацию о ЛП, имеющую юридическое значение в сфере обращения ЛС, в том числе - идентифицирующую отличительные свойства упаковки. 3. 4.

На основе ГИСЛС разрабатывается l Государственный реестр ЛС l Инструкции по применению ЛП l Перечень жизненно необходимых и важнейших ЛП l Список льготного отпуска ЛС l Список ЛС, отпускаемых без рецепта врача l Обязательный ассортимент ЛС для аптечных организаций, обслуживающих амбулаторных больных l Федеральное руководство для врачей по использованию ЛС.

Постановлением Правительства РФ от 29. 04 2006 г. N 255 "О внесении изменения в постановление Правительства РФ от 10. 02. 2004 г. N 72" с 1 января 2007 г. сертификация лекарственных средств заменена декларированием соответствия.

l l l В соответствии с действующим законодательством декларация о соответствии ЛС принимается на все поступающие с 1 января 2007 г. в обращение на территории РФ лекарственные средства. Лекарственные средства, находящиеся в обращении по состоянию на 1 января 2007 г. и имеющие сертификат соответствия, выданный в установленном порядке, не подлежат декларированию. Декларация о соответствии принимается в отношении каждой серии (партии) лекарственного средства, выпускаемой в обращение. Декларация о соответствии принимается на срок, установленный изготовителем (продавцом) лекарственного средства, но не более установленного срока годности лекарственного средства.

l l Сопровождение товара копией декларации о соответствии не предусмотрено. Зарегистрированная декларация о соответствии лекарственного средства вместе с документами, на основании которых она была принята, хранится у декларанта не менее 3 лет после окончания срока ее действия. Копии зарегистрированной декларации о соответствии лекарственного средства и сопроводительных документов (доказательственных материалов) хранятся в архиве органа по сертификации также в течение не менее 3 лет после окончания срока ее действия. По желанию декларанта орган по сертификации может проводить заверение копий зарегистрированных деклараций о соответствии.

При розничной реализации ЛС сведения о соответствии ЛС установленным требованиям подтверждается одним из следующих документов l l l сертификатом соответствия или декларацией о соответствии копией сертификата соответствия, заверенной держателем подлинника сертификата, нотариусом или органом по сертификации, выдавшим сертификат товарно-сопроводительными документами, оформленными поставщиком, содержащими по каждому наименованию товара следующие сведения (номер сертификата соответствия или регистрационный номер декларации о соответствии; срок действия; орган, выдавший сертификат или зарегистрировавший декларацию о соответствии), и заверенными подписью и печатью производителя (поставщика, продавца) с указанием его адреса и телефона.

Постановление правительства РФ № 1007 от 14. 10. 2012 12. Продавец обязан по требованию потребителя ознакомить его с товарно-сопроводительной документацией на товар, содержащей по каждому наименованию товара сведения об обязательном подтверждении соответствия согласно законодательству РФ о техническом регулировании (сертификат соответствия, его номер, срок его действия, орган, выдавший сертификат, или сведения о декларации о соответствии, в том числе ее регистрационный номер, срок ее действия, наименование лица, принявшего декларацию, и орган, ее зарегистрировавший). Эти документы должны быть заверены подписью и печатью поставщика или продавца с указанием его места нахождения (адреса) и телефона.


Перечень документов, определяющих принятие и регистрацию деклараций о соответствии 1. 2. 3. Постановление Правительства РФ от 01. 12. 09. № 982, утвердившее единый перечень продукции, подлежащей обязательной сертификации , и единый перечень продукции, подтверждение соответствия которой осуществляется в форме принятия декларации о соответствии . Постановление Правительства РФ от 7. 07. 1999 г. № 766, утвердившее форму декларации о соответствии, порядок ее принятия и регистрации. Методические рекомендации по принятию и регистрации декларации о соответствии лекарственных средств (утв. приказом Министерства промышленности и энергетики РФ от 26 декабря 2006 г. N 425) 4.
e0f57717d398ac8053f185d35d7860e3.ppt