Роль воды в химических реакциях.ppt
- Количество слайдов: 16
 Роль воды в химических реакциях ПЛАН 1. Электролитическая диссоциация 2. Кислоты, основания, соли в свете тории ЭДС 3. Значение электролитов
Роль воды в химических реакциях ПЛАН 1. Электролитическая диссоциация 2. Кислоты, основания, соли в свете тории ЭДС 3. Значение электролитов
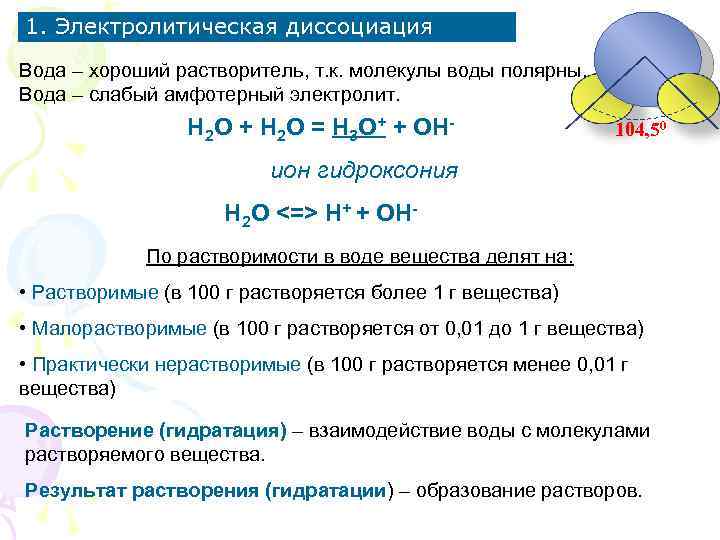 1. Электролитическая диссоциация Вода – хороший растворитель, т. к. молекулы воды полярны. Вода – слабый амфотерный электролит. Н 2 О + Н 2 О = Н 3 О+ + ОН- 104, 50 ион гидроксония Н 2 О <=> Н+ + ОНПо растворимости в воде вещества делят на: • Растворимые (в 100 г растворяется более 1 г вещества) • Малорастворимые (в 100 г растворяется от 0, 01 до 1 г вещества) • Практически нерастворимые (в 100 г растворяется менее 0, 01 г вещества) Растворение (гидратация) – взаимодействие воды с молекулами растворяемого вещества. Результат растворения (гидратации) – образование растворов.
1. Электролитическая диссоциация Вода – хороший растворитель, т. к. молекулы воды полярны. Вода – слабый амфотерный электролит. Н 2 О + Н 2 О = Н 3 О+ + ОН- 104, 50 ион гидроксония Н 2 О <=> Н+ + ОНПо растворимости в воде вещества делят на: • Растворимые (в 100 г растворяется более 1 г вещества) • Малорастворимые (в 100 г растворяется от 0, 01 до 1 г вещества) • Практически нерастворимые (в 100 г растворяется менее 0, 01 г вещества) Растворение (гидратация) – взаимодействие воды с молекулами растворяемого вещества. Результат растворения (гидратации) – образование растворов.
 Сванте Август Аррениус 1887 г. сформулировал основные положения теории электролитической диссоциации С. Аррениус 1859 -1927 • Все вещества по их способности проводить электрический ток в растворах делят на электролиты и неэлектролиты • В растворах электролиты диссоциируют (распадаются) на положительные и отрицательные ионы Электролитическая диссоциация – процесс распада электролита на ионы в растворе или расплаве
Сванте Август Аррениус 1887 г. сформулировал основные положения теории электролитической диссоциации С. Аррениус 1859 -1927 • Все вещества по их способности проводить электрический ток в растворах делят на электролиты и неэлектролиты • В растворах электролиты диссоциируют (распадаются) на положительные и отрицательные ионы Электролитическая диссоциация – процесс распада электролита на ионы в растворе или расплаве
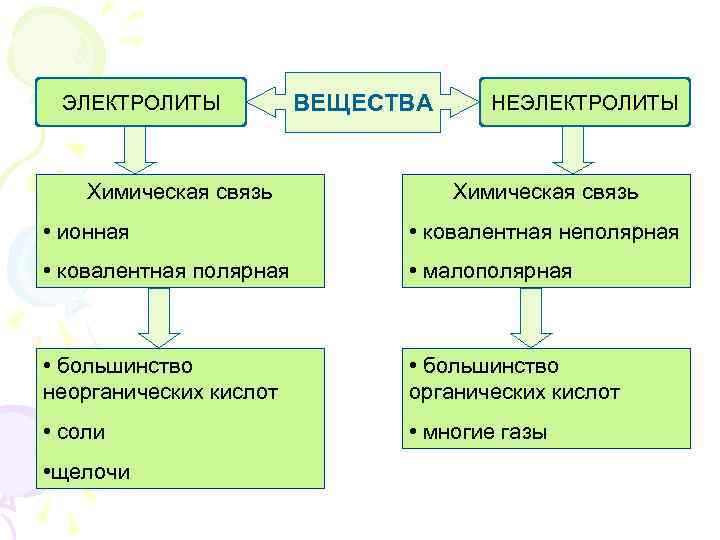 ЭЛЕКТРОЛИТЫ Химическая связь ВЕЩЕСТВА НЕЭЛЕКТРОЛИТЫ Химическая связь • ионная • ковалентная неполярная • ковалентная полярная • малополярная • большинство неорганических кислот • большинство органических кислот • соли • многие газы • щелочи
ЭЛЕКТРОЛИТЫ Химическая связь ВЕЩЕСТВА НЕЭЛЕКТРОЛИТЫ Химическая связь • ионная • ковалентная неполярная • ковалентная полярная • малополярная • большинство неорганических кислот • большинство органических кислот • соли • многие газы • щелочи
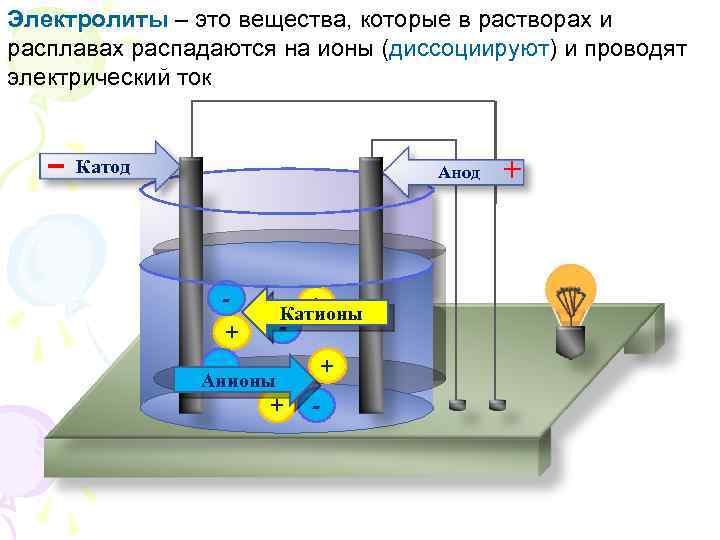 Электролиты – это вещества, которые в растворах и расплавах распадаются на ионы (диссоциируют) и проводят электрический ток - Катод Анод + - + Катионы - Анионы + + - +
Электролиты – это вещества, которые в растворах и расплавах распадаются на ионы (диссоциируют) и проводят электрический ток - Катод Анод + - + Катионы - Анионы + + - +
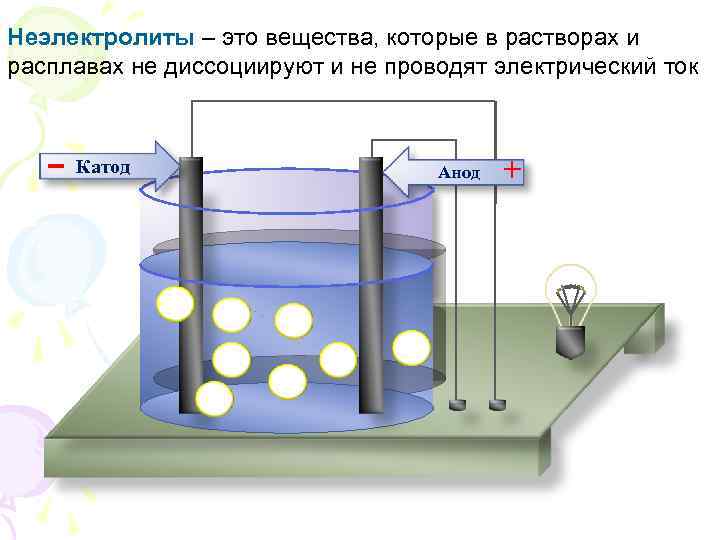 Неэлектролиты – это вещества, которые в растворах и расплавах не диссоциируют и не проводят электрический ток - Катод Анод +
Неэлектролиты – это вещества, которые в растворах и расплавах не диссоциируют и не проводят электрический ток - Катод Анод +
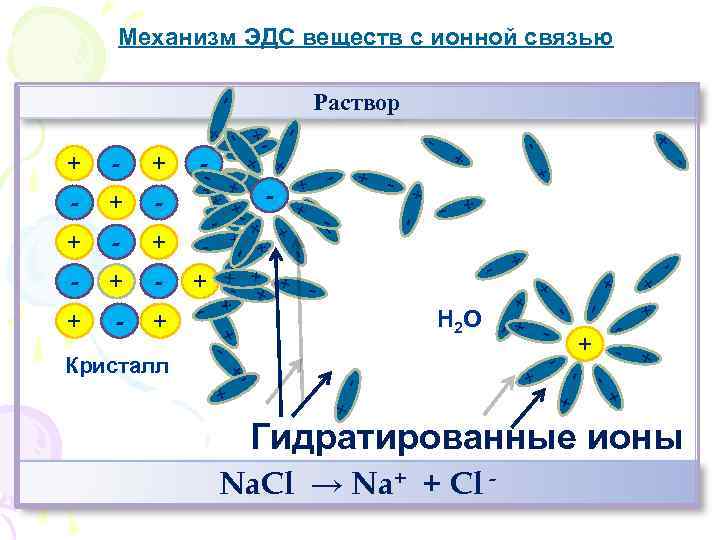 Механизм ЭДС веществ с ионной связью - + + - - - +- - - + + + - + - - - + + + - Н 2 О - + + + + - - - + + - - - + + + -- - + - - Кристалл + + - - + + + - Раствор Гидратированные ионы Na. Cl → Na+ + Cl -
Механизм ЭДС веществ с ионной связью - + + - - - +- - - + + + - + - - - + + + - Н 2 О - + + + + - - - + + - - - + + + -- - + - - Кристалл + + - - + + + - Раствор Гидратированные ионы Na. Cl → Na+ + Cl -
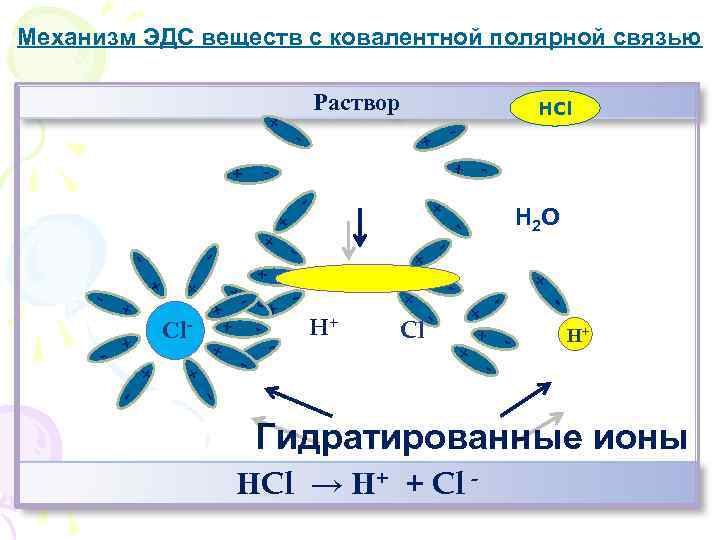 Механизм ЭДС веществ с ковалентной полярной связью Раствор + - - - + + + + -+ -+ - + + H+ - Н 2 О - - + + + Cl - + + + - + Сl + + - + + - HCl Н+ - - - Гидратированные ионы НCl → Н+ + Cl - -
Механизм ЭДС веществ с ковалентной полярной связью Раствор + - - - + + + + -+ -+ - + + H+ - Н 2 О - - + + + Cl - + + + - + Сl + + - + + - HCl Н+ - - - Гидратированные ионы НCl → Н+ + Cl - -
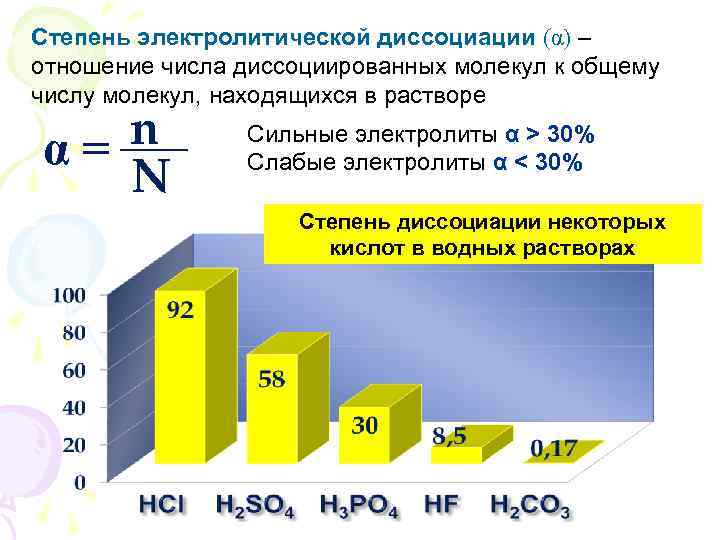 Степень электролитической диссоциации (α) – отношение числа диссоциированных молекул к общему числу молекул, находящихся в растворе n α= N Сильные электролиты α > 30% Слабые электролиты α < 30% Степень диссоциации некоторых кислот в водных растворах
Степень электролитической диссоциации (α) – отношение числа диссоциированных молекул к общему числу молекул, находящихся в растворе n α= N Сильные электролиты α > 30% Слабые электролиты α < 30% Степень диссоциации некоторых кислот в водных растворах
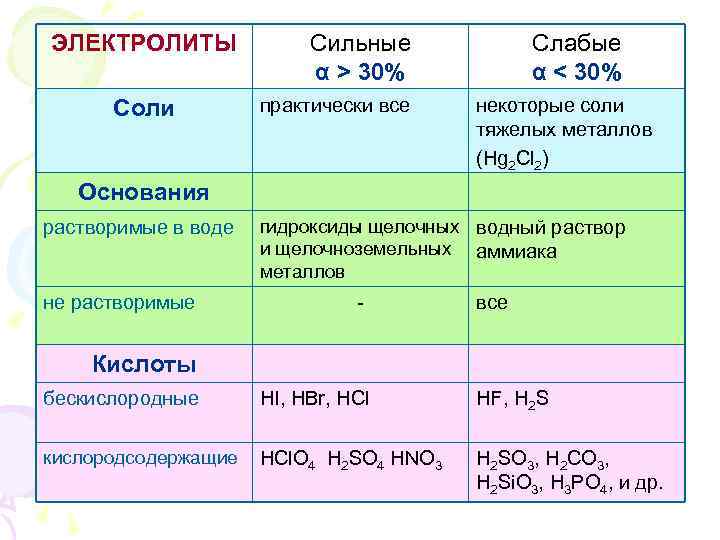 ЭЛЕКТРОЛИТЫ Соли Сильные α > 30% практически все Слабые α < 30% некоторые соли тяжелых металлов (Hg 2 Cl 2) Основания растворимые в воде не растворимые гидроксиды щелочных водный раствор и щелочноземельных аммиака металлов - все Кислоты бескислородные HI, HBr, HCl HF, H 2 S кислородсодержащие HCl. O 4 H 2 SO 4 HNO 3 H 2 SO 3, H 2 CO 3, H 2 Si. O 3, Н 3 РO 4, и др.
ЭЛЕКТРОЛИТЫ Соли Сильные α > 30% практически все Слабые α < 30% некоторые соли тяжелых металлов (Hg 2 Cl 2) Основания растворимые в воде не растворимые гидроксиды щелочных водный раствор и щелочноземельных аммиака металлов - все Кислоты бескислородные HI, HBr, HCl HF, H 2 S кислородсодержащие HCl. O 4 H 2 SO 4 HNO 3 H 2 SO 3, H 2 CO 3, H 2 Si. O 3, Н 3 РO 4, и др.
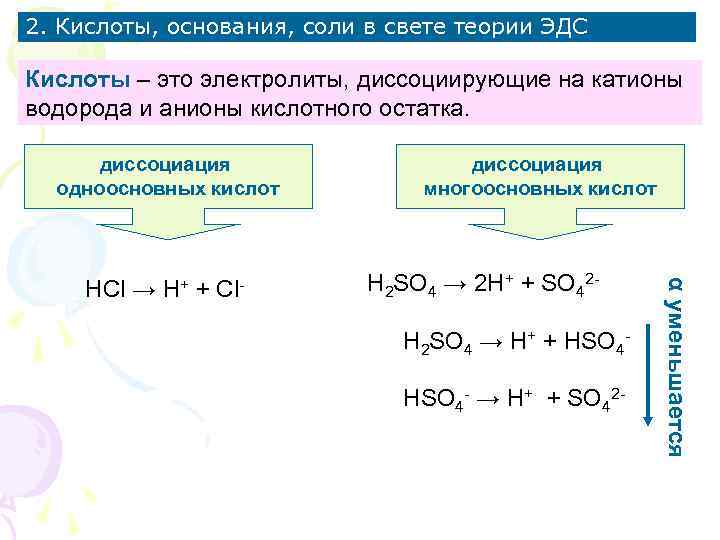 2. Кислоты, основания, соли в свете теории ЭДС Кислоты – это электролиты, диссоциирующие на катионы водорода и анионы кислотного остатка. диссоциация одноосновных кислот + Cl- H 2 SO 4 → 2 H+ + SO 42 H 2 SO 4 → H+ + HSO 4 - → H+ + SO 42 - α уменьшается HCl → H+ диссоциация многоосновных кислот
2. Кислоты, основания, соли в свете теории ЭДС Кислоты – это электролиты, диссоциирующие на катионы водорода и анионы кислотного остатка. диссоциация одноосновных кислот + Cl- H 2 SO 4 → 2 H+ + SO 42 H 2 SO 4 → H+ + HSO 4 - → H+ + SO 42 - α уменьшается HCl → H+ диссоциация многоосновных кислот
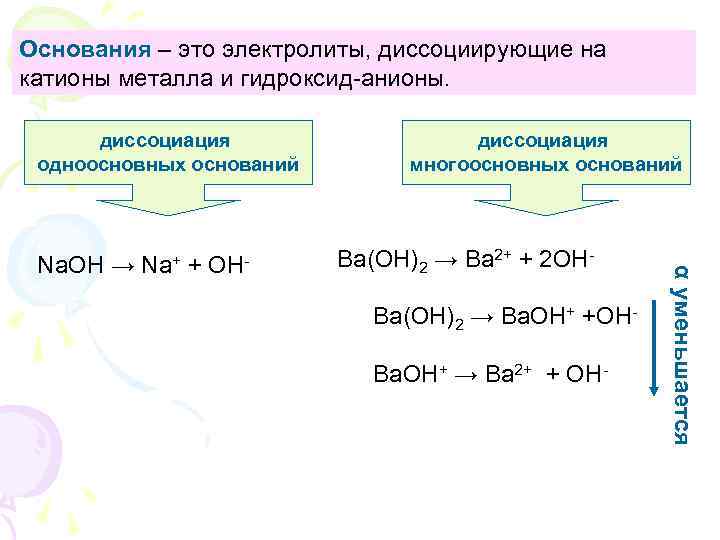 Основания – это электролиты, диссоциирующие на катионы металла и гидроксид-анионы. диссоциация одноосновных оснований + OH- Ba(OH)2 → Ba 2+ + 2 OHBa(OH)2 → Ba. OH+ +ОНBa. OH+ → Ba 2+ + OH- α уменьшается Na. OH → Na+ диссоциация многоосновных оснований
Основания – это электролиты, диссоциирующие на катионы металла и гидроксид-анионы. диссоциация одноосновных оснований + OH- Ba(OH)2 → Ba 2+ + 2 OHBa(OH)2 → Ba. OH+ +ОНBa. OH+ → Ba 2+ + OH- α уменьшается Na. OH → Na+ диссоциация многоосновных оснований
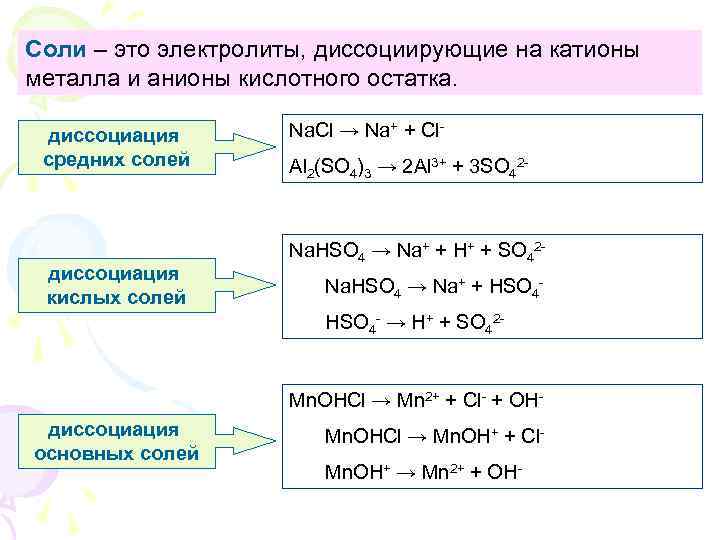 Соли – это электролиты, диссоциирующие на катионы металла и анионы кислотного остатка. диссоциация средних солей диссоциация кислых солей Na. Cl → Na+ + Cl. Al 2(SO 4)3 → 2 Al 3+ + 3 SO 42 - Na. HSO 4 → Na+ + H+ + SO 42 Na. HSO 4 → Na+ + HSO 4 - → H+ + SO 42 - Mn. OHCl → Mn 2+ + Cl- + OHдиссоциация основных солей Mn. OHCl → Mn. OH+ + Cl. Mn. OH+ → Mn 2+ + OH-
Соли – это электролиты, диссоциирующие на катионы металла и анионы кислотного остатка. диссоциация средних солей диссоциация кислых солей Na. Cl → Na+ + Cl. Al 2(SO 4)3 → 2 Al 3+ + 3 SO 42 - Na. HSO 4 → Na+ + H+ + SO 42 Na. HSO 4 → Na+ + HSO 4 - → H+ + SO 42 - Mn. OHCl → Mn 2+ + Cl- + OHдиссоциация основных солей Mn. OHCl → Mn. OH+ + Cl. Mn. OH+ → Mn 2+ + OH-
 3. Значение электролитов для живых систем Электролиты – составная часть жидкостей и плотных тканей живых организмов. Ионы Na+, K+, Ca 2+, Mg 2+, H+, OH-, Cl-, SO 42 - имеют большое значение для физиологических и биохимических процессов: • ионы Н+ и ОН- играют большую роль в работе ферментов, обмене веществ, переваривании пищи и др. • ионы I- влияют на работу щитовидной железы
3. Значение электролитов для живых систем Электролиты – составная часть жидкостей и плотных тканей живых организмов. Ионы Na+, K+, Ca 2+, Mg 2+, H+, OH-, Cl-, SO 42 - имеют большое значение для физиологических и биохимических процессов: • ионы Н+ и ОН- играют большую роль в работе ферментов, обмене веществ, переваривании пищи и др. • ионы I- влияют на работу щитовидной железы
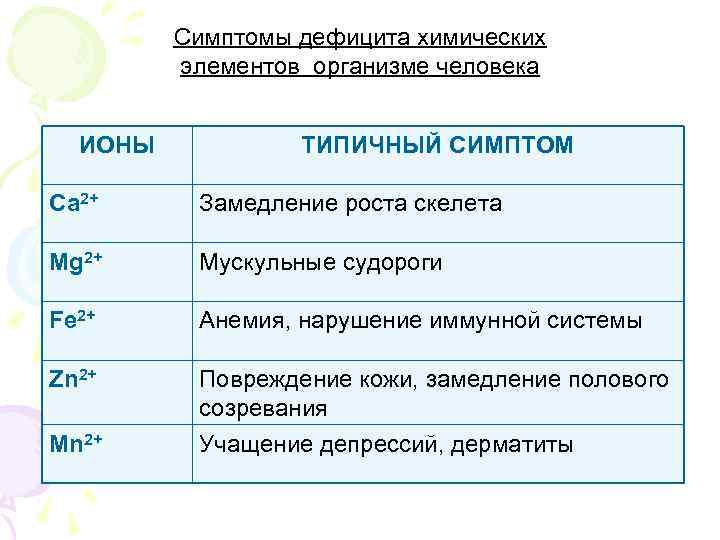 Симптомы дефицита химических элементов организме человека ИОНЫ ТИПИЧНЫЙ СИМПТОМ Ca 2+ Замедление роста скелета Mg 2+ Мускульные судороги Fe 2+ Анемия, нарушение иммунной системы Zn 2+ Повреждение кожи, замедление полового созревания Учащение депрессий, дерматиты Mn 2+
Симптомы дефицита химических элементов организме человека ИОНЫ ТИПИЧНЫЙ СИМПТОМ Ca 2+ Замедление роста скелета Mg 2+ Мускульные судороги Fe 2+ Анемия, нарушение иммунной системы Zn 2+ Повреждение кожи, замедление полового созревания Учащение депрессий, дерматиты Mn 2+
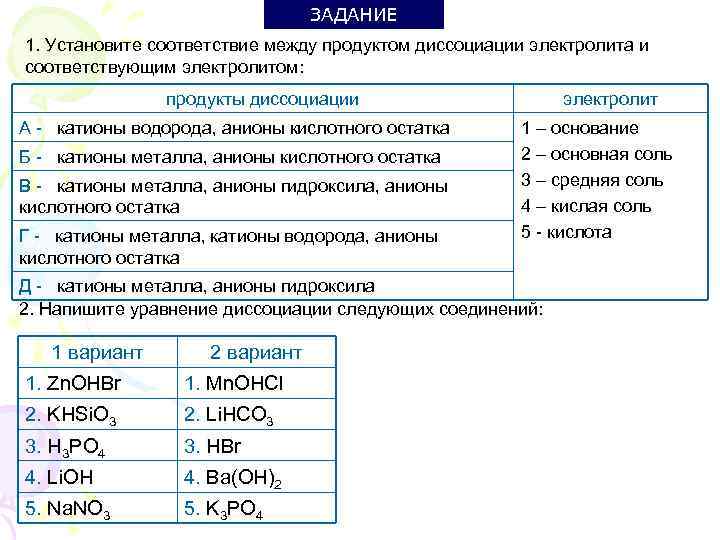 ЗАДАНИЕ 1. Установите соответствие между продуктом диссоциации электролита и соответствующим электролитом: продукты диссоциации А - катионы водорода, анионы кислотного остатка Б - катионы металла, анионы кислотного остатка В - катионы металла, анионы гидроксила, анионы кислотного остатка Г - катионы металла, катионы водорода, анионы кислотного остатка электролит 1 – основание 2 – основная соль 3 – средняя соль 4 – кислая соль 5 - кислота Д - катионы металла, анионы гидроксила 2. Напишите уравнение диссоциации следующих соединений: 1 вариант 2 вариант 1. Zn. OHBr 1. Mn. OHCl 2. KHSi. O 3 2. Li. HCO 3 3. H 3 PO 4 3. HBr 4. Li. OH 4. Ba(OH)2 5. Na. NO 3 5. K 3 PO 4
ЗАДАНИЕ 1. Установите соответствие между продуктом диссоциации электролита и соответствующим электролитом: продукты диссоциации А - катионы водорода, анионы кислотного остатка Б - катионы металла, анионы кислотного остатка В - катионы металла, анионы гидроксила, анионы кислотного остатка Г - катионы металла, катионы водорода, анионы кислотного остатка электролит 1 – основание 2 – основная соль 3 – средняя соль 4 – кислая соль 5 - кислота Д - катионы металла, анионы гидроксила 2. Напишите уравнение диссоциации следующих соединений: 1 вариант 2 вариант 1. Zn. OHBr 1. Mn. OHCl 2. KHSi. O 3 2. Li. HCO 3 3. H 3 PO 4 3. HBr 4. Li. OH 4. Ba(OH)2 5. Na. NO 3 5. K 3 PO 4


