Роль В-клеток.ppt
- Количество слайдов: 49

Роль B-клеток и аутоиммунных антител при ревматоидном артрите

Содержание Ревматоидный артрит (РА) Предпосылки: нормальное функционирование иммунной системы Роль B-клеток в иммунном ответе Аутоиммунные B-клетки и аутоиммунные антитела при РА Роль аутоиммунных антител при РА: доклинические данные Ритуксимаб при РА избирательно воздействует на B-клетки Ответ на ритуксимаб у пациентов с РА, серопозитивных в отношении РФ и/или анти-ЦЦП Резюме
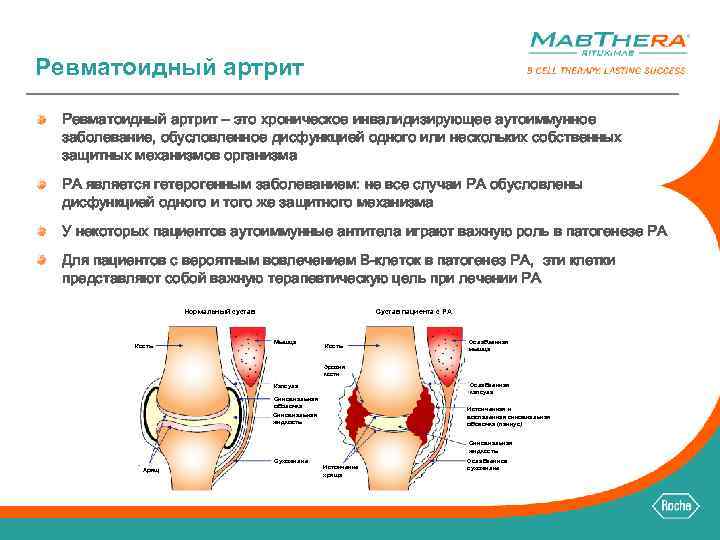
Ревматоидный артрит – это хроническое инвалидизирующее аутоиммунное заболевание, обусловленное дисфункцией одного или нескольких собственных защитных механизмов организма РА является гетерогенным заболеванием: не все случаи РА обусловлены дисфункцией одного и того же защитного механизма У некоторых пациентов аутоиммунные антитела играют важную роль в патогенезе РА Для пациентов с вероятным вовлечением B-клеток в патогенез РА, эти клетки представляют собой важную терапевтическую цель при лечении РА Нормальный сустав Кость Сустав пациента с РА Мышца Кость Ослабленная мышца Эрозия кости Ослабленная капсула Капсула Синовиальная оболочка Истонченная и воспаленная синовиальная оболочка (паннус) Синовиальная жидкость Сухожилие Хрящ Истончение хряща Ослабленное сухожилие

Предпосылки: нормальное функционирование иммунной системы Иммунная система состоит из множества независимых клеток, тканей и органов, которые совместно работают для защиты организма от инфекции и роста опухолевых клеток Иммунный ответ разделяется на два компонента: 1. Распознавание: инородные (или «не свои» ) молекулы или антигены обнаруживаются и помечаются для удаления 2. Защитный ответ: антиген-специфические антитела запускают многоклеточную атаку против инородного антигена Конечная цель иммунного ответа состоит в уничтожении инородного антигена путем гибели клетки или поглощения и расщепления Roitt и соавт. , 2001

Типы иммунных клеток Основными клетками, вовлеченными в иммунный ответ, являются белые клетки крови (лейкоциты) Лимфоциты – существенный компонент белых клеток крови – разделяют на клетки двух типов, которые вместе работают для защиты организма: T-клетки и B-клетки обнаруживают чужеродный антиген и продуцируют против них специфические антитела T-клетки уничтожают клетки, пораженные патогенами, а также клетки, которые функционируют неправильно T-хелперы продуцируют и секретируют химические вещества, которые активизируют продукцию большого количества эффекторных клеток и клеток памяти Цитотоксические T-клетки элиминируют инфицированные клетки организма и опухолевые клетки Roitt и соавт. , 2001
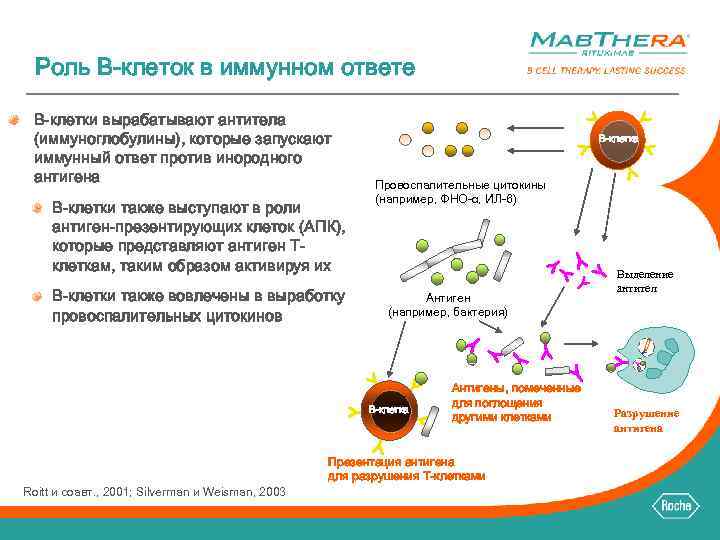
Роль B-клеток в иммунном ответе B-клетки вырабатывают антитела (иммуноглобулины), которые запускают иммунный ответ против инородного антигена B-клетки также выступают в роли антиген-презентирующих клеток (АПК), которые представляют антиген Tклеткам, таким образом активируя их B-клетки также вовлечены в выработку провоспалительных цитокинов B-клетка Провоспалительные цитокины (например, ФНО-α, ИЛ-6) Антиген (например, бактерия) B-клетка Roitt и соавт. , 2001; Silverman и Weisman, 2003 Антигены, помеченные для поглощения другими клетками Презентация антигена для разрушения T-клетками Выделение антител Разрушение антигена
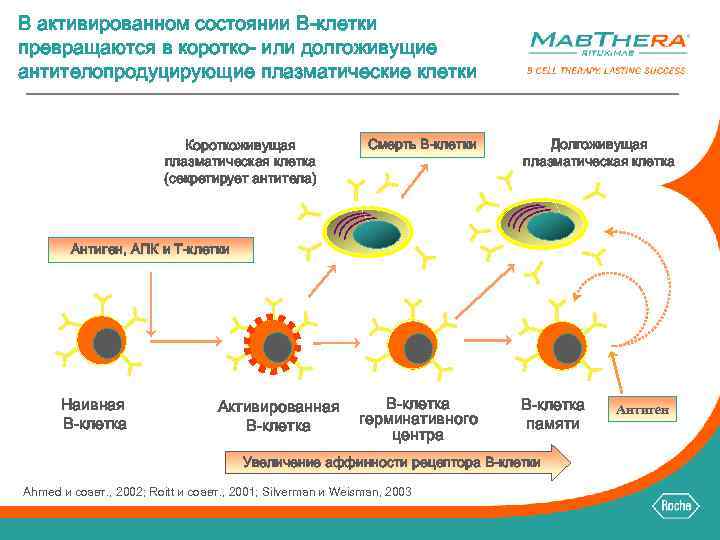
В активированном состоянии B-клетки превращаются в коротко- или долгоживущие антителопродуцирующие плазматические клетки Короткоживущая плазматическая клетка (секретирует антитела) Смерть B-клетки Долгоживущая плазматическая клетка Антиген, АПК и T-клетки Наивная B-клетка Активированная B-клетка герминативного центра B-клетка памяти Увеличение аффинности рецептора B-клетки Ahmed и соавт. , 2002; Roitt и соавт. , 2001; Silverman и Weisman, 2003 Антиген
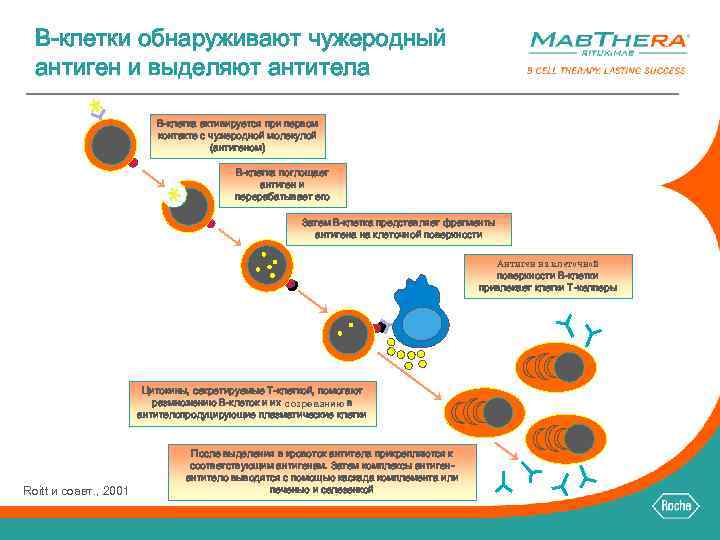
B-клетки обнаруживают чужеродный антиген и выделяют антитела B-клетка активируется при первом контакте с чужеродной молекулой (антигеном) B-клетка поглощает антиген и перерабатывает его Затем B-клетка представляет фрагменты антигена на клеточной поверхности Антиген на клеточной поверхности B-клетки привлекает клетки T-хелперы Цитокины, секретируемые T-клеткой, помогают размножению B-клеток и их созреванию в антителопродуцирующие плазматические клетки Roitt и соавт. , 2001 После выделения в кровоток антитела прикрепляются к соответствующим антигенам. Затем комплексы антигенантитело выводятся с помощью каскада комплемента или печенью и селезенкой
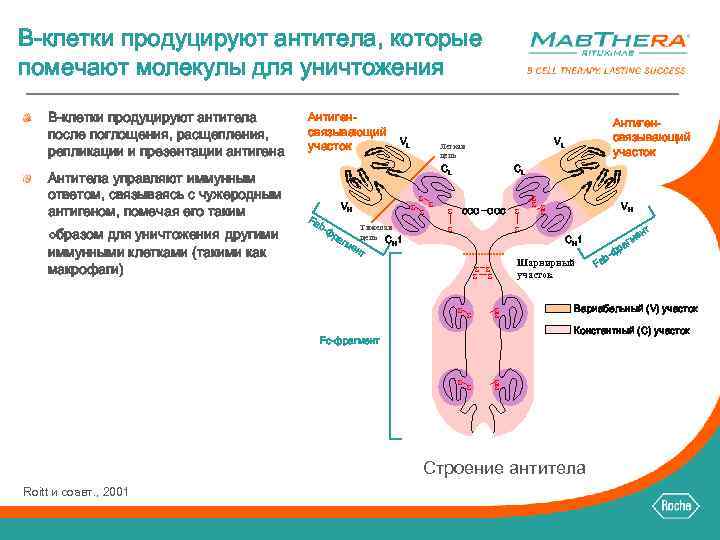
B-клетки продуцируют антитела, которые помечают молекулы для уничтожения B-клетки продуцируют антитела после поглощения, расщепления, репликации и презентации антигена Антитела управляют иммунным ответом, связываясь с чужеродным антигеном, помечая его таким образом для уничтожения другими иммунными клетками (такими как макрофаги) Антигенсвязывающий участок VL VL Легкая цепь CL Fa VH b-ф ра гм ен S Тяжелая цепь C т H 1 S S Антигенсвязывающий участок CL COO OOC S S VH S S b- Fa Вариабельный (V) участок Константный (C) участок Fc-фрагмент S S Строение антитела Roitt и соавт. , 2001 т ен гм ра ф CH 1 Шарнирный участок S S S S S
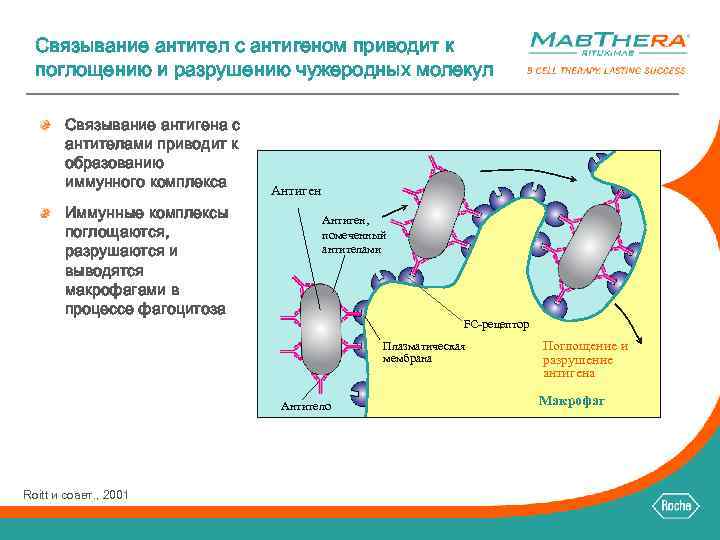
Связывание антител с антигеном приводит к поглощению и разрушению чужеродных молекул Связывание антигена с антителами приводит к образованию иммунного комплекса Иммунные комплексы поглощаются, разрушаются и выводятся макрофагами в процессе фагоцитоза Антиген, помеченный антителами FC-рецептор Плазматическая мембрана Антитело Roitt и соавт. , 2001 Поглощение и разрушение антигена Макрофаг
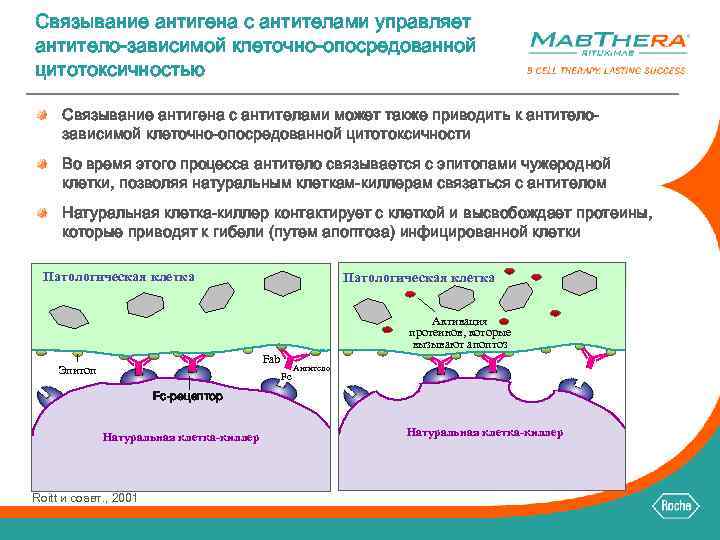
Связывание антигена с антителами управляет антитело-зависимой клеточно-опосредованной цитотоксичностью Связывание антигена с антителами может также приводить к антителозависимой клеточно-опосредованной цитотоксичности Во время этого процесса антитело связывается с эпитопами чужеродной клетки, позволяя натуральным клеткам-киллерам связаться с антителом Натуральная клетка-киллер контактирует с клеткой и высвобождает протеины, которые приводят к гибели (путем апоптоза) инфицированной клетки Патологическая клетка Активация протеинов, которые вызывают апоптоз Fab Эпитоп Fc Антитело Fc-рецептор Натуральная клетка-киллер Roitt и соавт. , 2001 Натуральная клетка-киллер
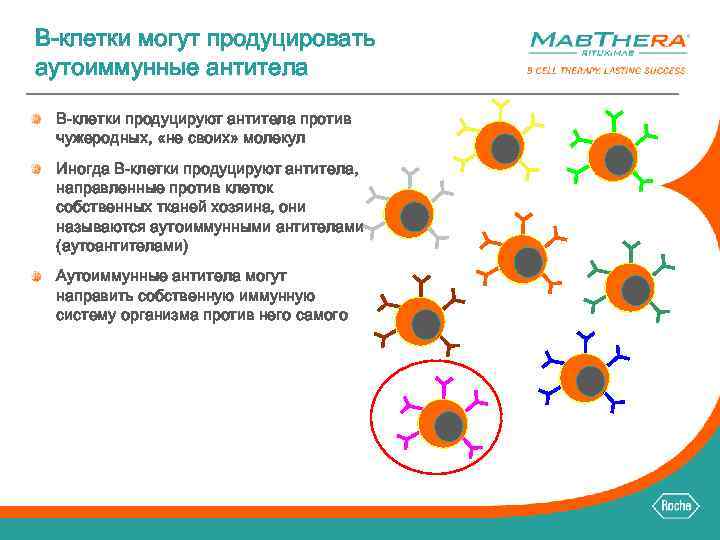
B-клетки могут продуцировать аутоиммунные антитела B-клетки продуцируют антитела против чужеродных, «не своих» молекул Иногда B-клетки продуцируют антитела, направленные против клеток собственных тканей хозяина, они называются аутоиммунными антителами (аутоантителами) Аутоиммунные антитела могут направить собственную иммунную систему организма против него самого
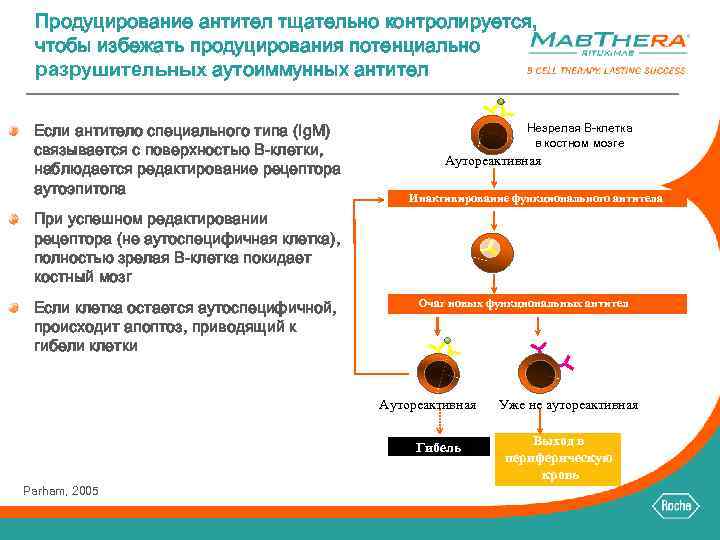
Продуцирование антител тщательно контролируется, чтобы избежать продуцирования потенциально разрушительных аутоиммунных антител Если антитело специального типа (Ig. M) связывается с поверхностью B-клетки, наблюдается редактирование рецептора аутоэпитопа Незрелая B-клетка в костном мозге Аутореактивная Инактивирование функционального антитела При успешном редактировании рецептора (не аутоспецифичная клетка), полностью зрелая B-клетка покидает костный мозг Если клетка остается аутоспецифичной, происходит апоптоз, приводящий к гибели клетки Очаг новых функциональных антител Аутореактивная Гибель Parham, 2005 Уже не аутореактивная Выход в периферическую кровь
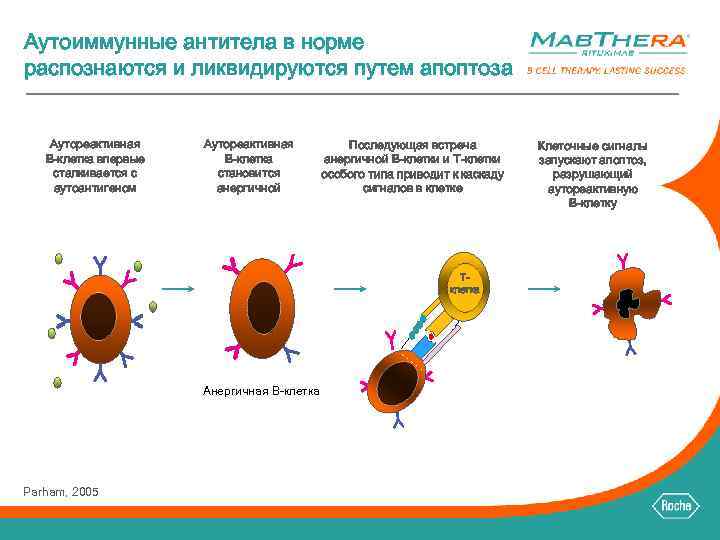
Аутоиммунные антитела в норме распознаются и ликвидируются путем апоптоза Аутореактивная B-клетка впервые сталкивается с аутоантигеном Аутореактивная B-клетка становится анергичной Последующая встреча анергичной B-клетки и T-клетки особого типа приводит к каскаду сигналов в клетке Tклетка Анергичная B-клетка Parham, 2005 Клеточные сигналы запускают апоптоз, разрушающий аутореактивную B-клетку

Если аутореактивные B-клетки выживают и продуцируют аутоиммунные антитела, это может привести к аутоиммунным заболеваниям, таким как РА Некоторые B-клетки, которые продуцируют аутоантитела, могут избежать этих механизмов элиминации и продолжить существование Эти B-клетки дифференцируются в аутоиммунные плазматические клетки, которые продуцируют большое количество аутоиммунных антител Продуцирование большого количества аутоиммунных антител может привести к аутоиммунным заболеваниям, таким как РА Роль аутореактивных B-клеток в патофизиологии РА в настоящее время хорошо исследована Silvermann и Carson, 2003
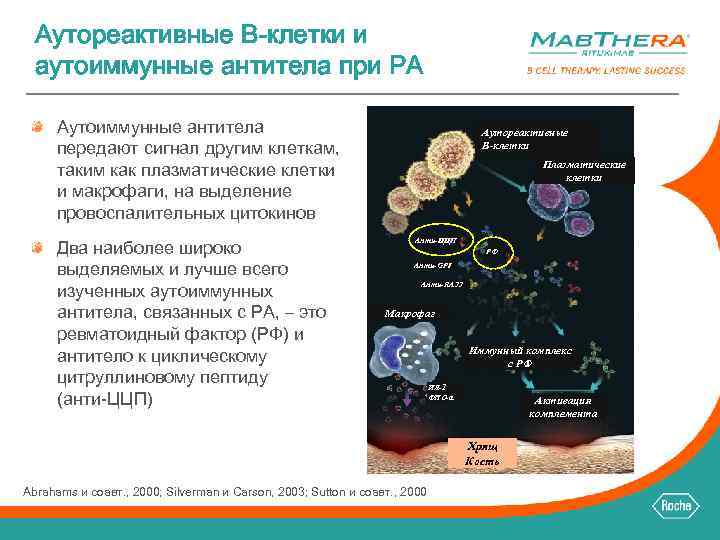
Аутореактивные B-клетки и аутоиммунные антитела при РА Аутоиммунные антитела передают сигнал другим клеткам, таким как плазматические клетки и макрофаги, на выделение провоспалительных цитокинов Два наиболее широко выделяемых и лучше всего изученных аутоиммунных антитела, связанных с РА, – это ревматоидный фактор (РФ) и антитело к циклическому цитруллиновому пептиду (анти-ЦЦП) Аутореактивные B-клетки Плазматические клетки Анти-ЦЦП РФ Анти-GPI Анти-RA 33 Макрофаг Иммунный комплекс с РФ ИЛ-1 ФНО-α Активация комплемента Хрящ Кость Abrahams и соавт. , 2000; Silverman и Carson, 2003; Sutton и соавт. , 2000
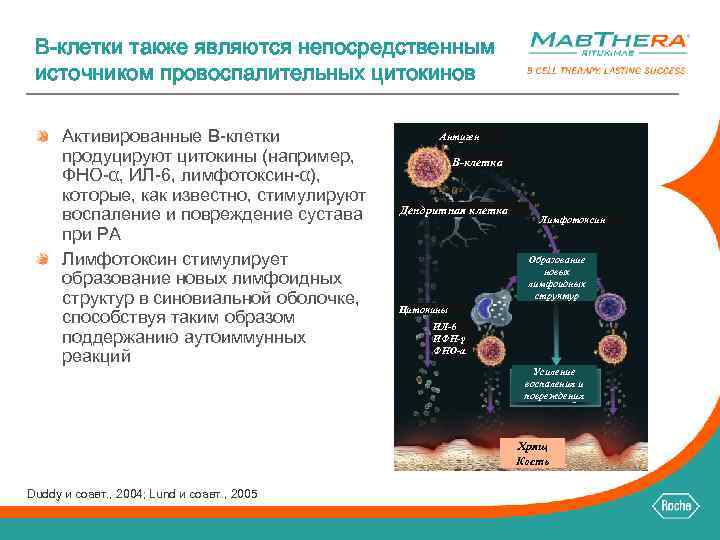
B-клетки также являются непосредственным источником провоспалительных цитокинов Активированные B-клетки продуцируют цитокины (например, ФНО-α, ИЛ-6, лимфотоксин-α), которые, как известно, стимулируют воспаление и повреждение сустава при РА Лимфотоксин стимулирует образование новых лимфоидных структур в синовиальной оболочке, способствуя таким образом поддержанию аутоиммунных реакций Антиген B-клетка Дендритная клетка Лимфотоксин Образование новых лимфоидных структур Цитокины ИЛ-6 ИФН-γ ФНО-α Усиление воспаления и повреждения Хрящ Кость Duddy и соавт. , 2004; Lund и соавт. , 2005
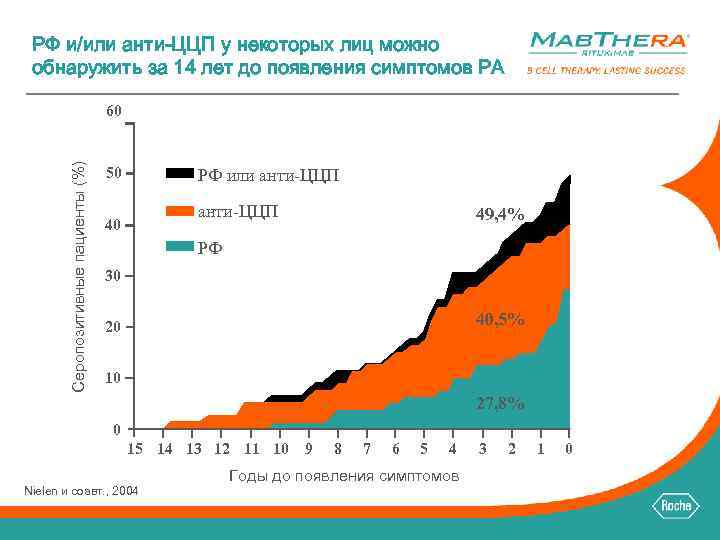
РФ и/или анти-ЦЦП у некоторых лиц можно обнаружить за 14 лет до появления симптомов РА Серопозитивные пациенты (%) 60 50 РФ или анти-ЦЦП 40 49, 4% РФ 30 40, 5% 20 10 27, 8% 0 15 14 13 12 11 10 9 Nielen и соавт. , 2004 8 7 6 5 4 Годы до появления симптомов 3 2 1 0
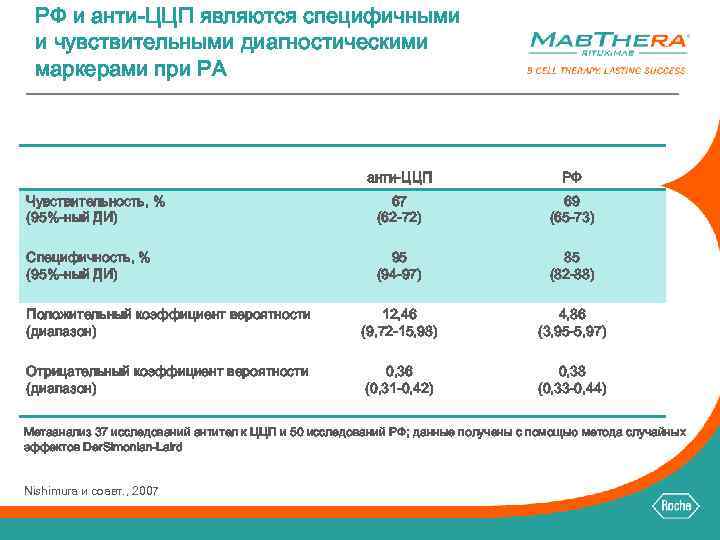
РФ и анти-ЦЦП являются специфичными и чувствительными диагностическими маркерами при РА анти-ЦЦП РФ Чувствительность, % (95%-ный ДИ) 67 (62 -72) 69 (65 -73) Специфичность, % (95%-ный ДИ) 95 (94 -97) 85 (82 -88) Положительный коэффициент вероятности (диапазон) 12, 46 (9, 72 -15, 98) 4, 86 (3, 95 -5, 97) Отрицательный коэффициент вероятности (диапазон) 0, 36 (0, 31 -0, 42) 0, 38 (0, 33 -0, 44) Метаанализ 37 исследований антител к ЦЦП и 50 исследований РФ; данные получены с помощью метода случайных эффектов Der. Simonian-Laird Nishimura и соавт. , 2007
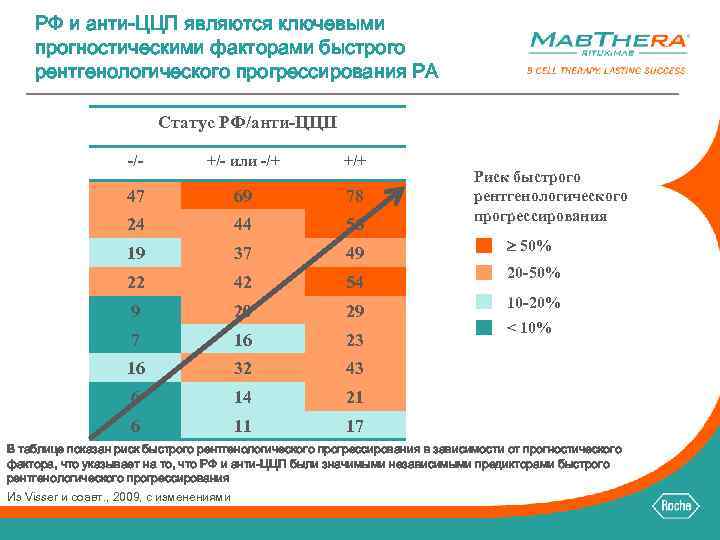
РФ и анти-ЦЦП являются ключевыми прогностическими факторами быстрого рентгенологического прогрессирования РА Статус РФ/анти-ЦЦП -/- +/- или -/+ +/+ 47 69 78 24 44 56 19 37 49 22 42 54 9 20 29 7 16 23 16 32 43 6 14 21 6 11 17 Риск быстрого рентгенологического прогрессирования 50% 20 -50% 10 -20% < 10% В таблице показан риск быстрого рентгенологического прогрессирования в зависимости от прогностического фактора, что указывает на то, что РФ и анти-ЦЦП были значимыми независимыми предикторами быстрого рентгенологического прогрессирования Из Visser и соавт. , 2009, с изменениями
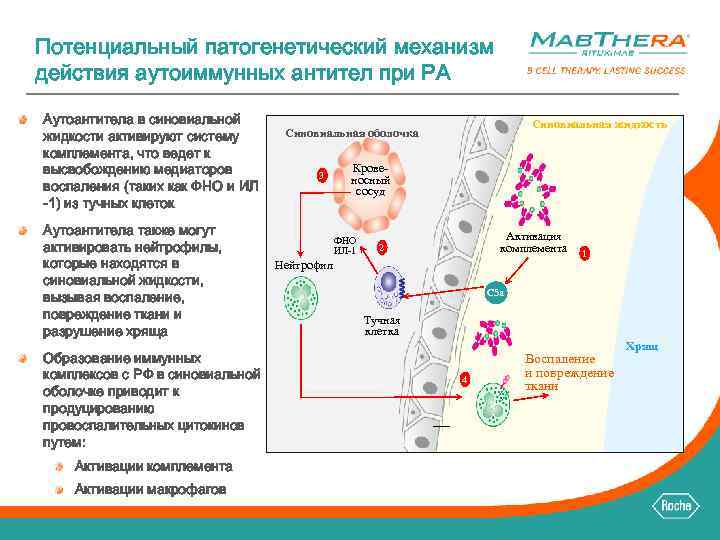
Потенциальный патогенетический механизм действия аутоиммунных антител при РА Аутоантитела в синовиальной жидкости активируют систему комплемента, что ведет к высвобождению медиаторов воспаления (таких как ФНО и ИЛ -1) из тучных клеток Аутоантитела также могут активировать нейтрофилы, которые находятся в синовиальной жидкости, вызывая воспаление, повреждение ткани и разрушение хряща Образование иммунных комплексов с РФ в синовиальной оболочке приводит к продуцированию провоспалительных цитокинов путем: Активации комплемента Активации макрофагов Синовиальная жидкость Синовиальная оболочка 3 Кровеносный сосуд ФНО ИЛ-1 Активация комплемента 2 Нейтрофил 1 C 5 a Тучная клетка 4 Воспаление и повреждение ткани Хрящ Выстилка синовиальной оболочки

Доклинические признаки: роль аутоиммунных антител при РА Предварительные данные доклинических моделей говорят о прямой роли аутоиммунных антител в патогенезе РА Внутривенное введение аутоантител вызывает воспалительный артрит у мышей Богатая аутоантителами плазма или сыворотка, полученная от пациентов с активным РА, может вызывать у мышей воспаление и гистологические поражения, соответствующие артриту Kuhn и соавт. , 2006; Petkova и соавт. , 2006
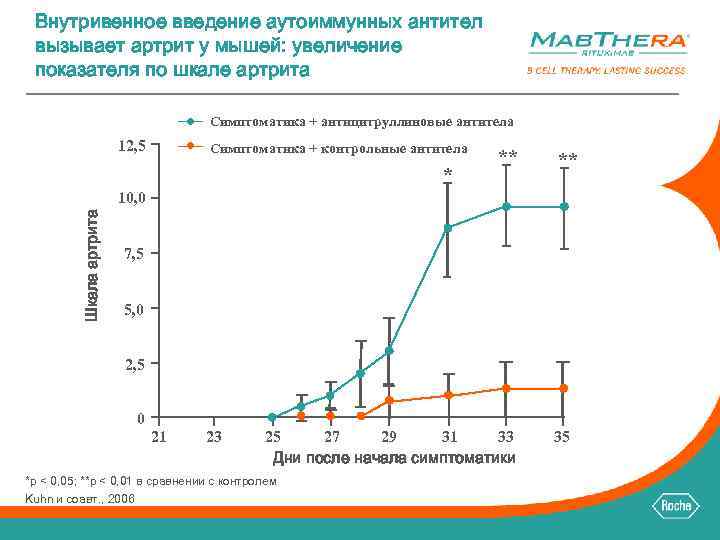
Внутривенное введение аутоиммунных антител вызывает артрит у мышей: увеличение показателя по шкале артрита Симптоматика + антицитруллиновые антитела 12, 5 Симптоматика + контрольные антитела * ** ** Шкала артрита 10, 0 7, 5 5, 0 2, 5 0 21 23 25 27 29 31 33 Дни после начала симптоматики *p < 0, 05; **p < 0, 01 в сравнении с контролем Kuhn и соавт. , 2006 35
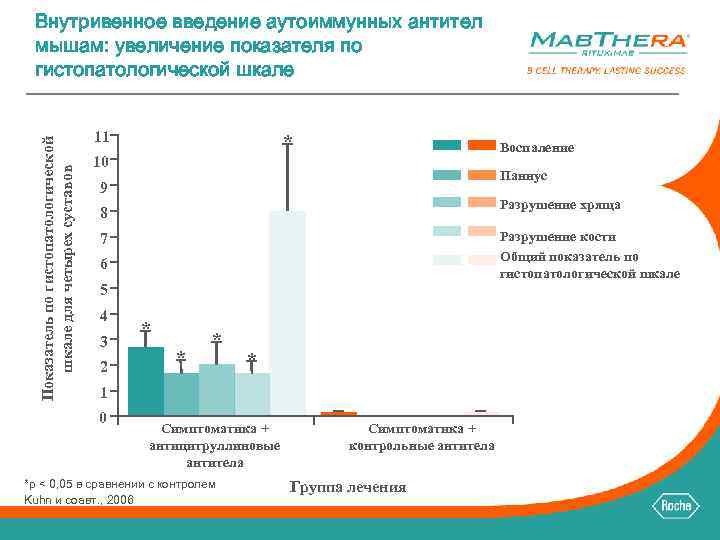
Показатель по гистопатологической шкале для четырех суставов Внутривенное введение аутоиммунных антител мышам: увеличение показателя по гистопатологической шкале 11 * Воспаление 10 Паннус 9 Разрушение хряща 8 Разрушение кости Общий показатель по гистопатологической шкале 7 6 5 4 3 2 * * 1 0 Симптоматика + антицитруллиновые антитела *p < 0, 05 в сравнении с контролем Kuhn и соавт. , 2006 Симптоматика + контрольные антитела Группа лечения

Резюме: доклинические признаки, поддерживающие гипотезу о роли аутоиммунных антител при РА Внутривенное введение антицитруллиновых аутоиммунных антител вызывает воспалительный артрит у мышей Эти доклинические данные говорят о том, что наличие аутоиммунных антител связано с развитием у мышей воспаления, соответствующего РА Нацеленность на продуцирование аутоиммунных антител при клиническом лечении пациентов с серопозитивным РА может оказаться эффективной терапевтической стратегией

Обобщенные доказательства роли аутореактивных B-клеток при РА В синовиальной оболочке суставов, пораженных РА, наблюдается избыток B-клетки являются источником аутоиммунных антител, таких как РФ и анти-ЦЦП Появление аутоиммунных антител часто предшествует началу РА, они удобны для постановки диагноза РА, и их наличие связано с агрессивной формой РА с плохим прогнозом Внутривенное введение аутоиммунных антител мышам вызывает РА -подобный ответ

Важные вопросы Влияет ли направленное на B-клетки лечение на профиль аутоантител при РА? Приводит ли лечение серопозитивных пациентов препаратами, направленными на B-клетки, к лучшим клиническим исходам в сравнении с серонегативными пациентами?

Ритуксимаб селективно снижает число B-клеток, вовлеченных в патогенез РА Ритуксимаб (Мабтера®) – это генно-инженерный биологический препарат, который селективно действует и уменьшает количество B -клеток, вовлеченных в патогенез РА Ритуксимаб эффективно уменьшает количество B-клеток, на клеточной поверхности которых представлен антиген CD 20 экспрессируется во время созревания на B-клетках, но не на стволовых клетках и не на зрелых плазматических клетках, что делает их идеальной терапевтической мишенью
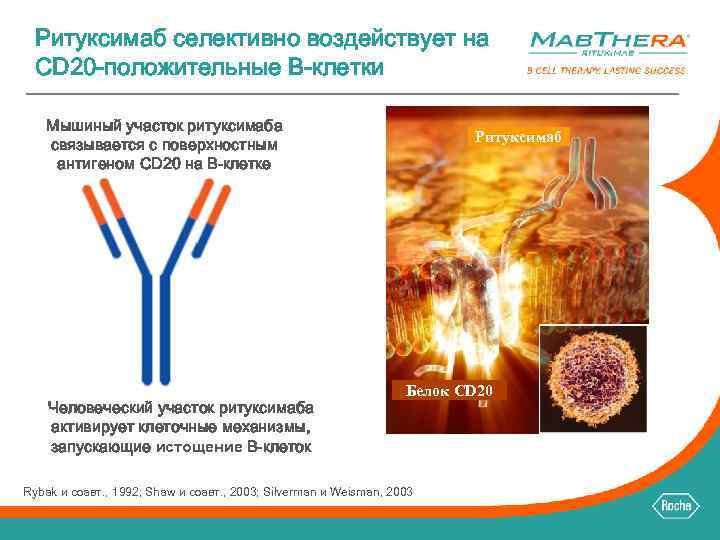
Ритуксимаб селективно воздействует на CD 20 -положительные B-клетки Мышиный участок ритуксимаба связывается с поверхностным антигеном CD 20 на B-клетке Человеческий участок ритуксимаба активирует клеточные механизмы, запускающие истощение B-клеток Ритуксимаб Белок CD 20 Rybak и соавт. , 1992; Shaw и соавт. , 2003; Silverman и Weisman, 2003
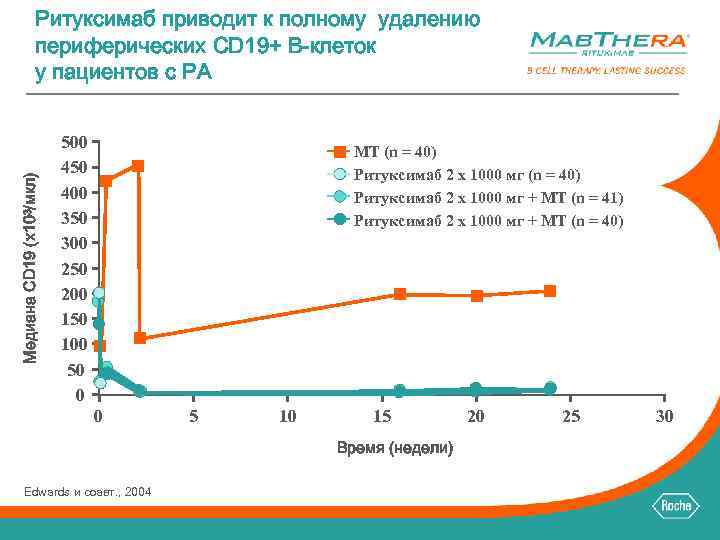
Медиана CD 19 (x 103/мкл) Ритуксимаб приводит к полному удалению периферических CD 19+ B-клеток у пациентов с РА 500 450 400 350 300 250 200 150 100 50 0 МТ (n = 40) Ритуксимаб 2 x 1000 мг + МТ (n = 41) Ритуксимаб 2 x 1000 мг + МТ (n = 40) 0 5 10 15 Время (недели) Edwards и соавт. , 2004 20 25 30
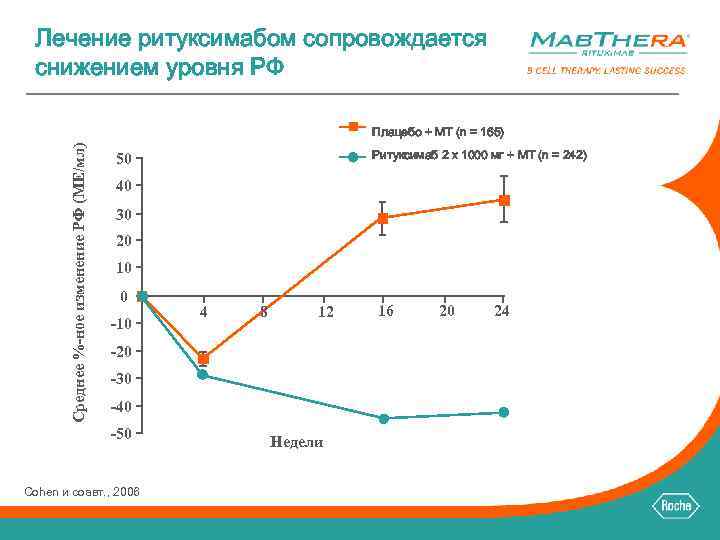
Лечение ритуксимабом сопровождается снижением уровня РФ Среднее %-ное изменение РФ (МЕ/мл) Плацебо + МТ (n = 165) Ритуксимаб 2 x 1000 мг + МТ (n = 242) 50 40 30 20 10 0 -10 4 8 12 -20 -30 -40 -50 Cohen и соавт. , 2006 Недели 16 20 24
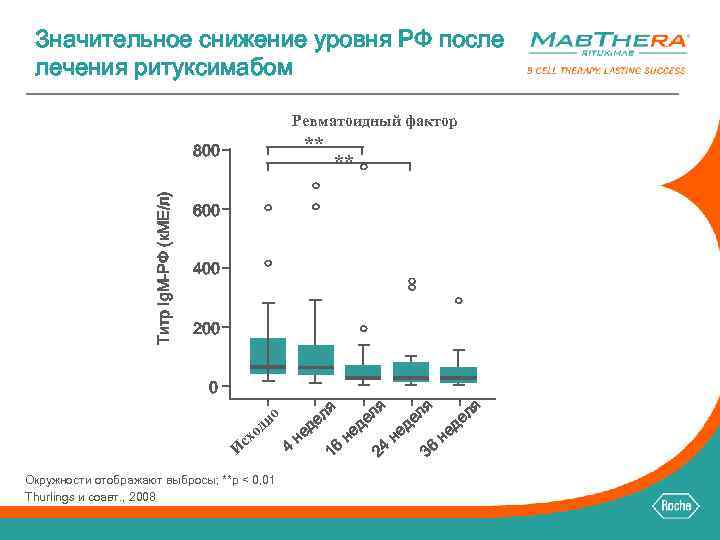
Значительное снижение уровня РФ после лечения ритуксимабом Ревматоидный фактор ** Титр Ig. M-РФ (к. МЕ/л) 800 ** 600 400 200 0 о сх И Окружности отображают выбросы; **p < 0, 01 Thurlings и соавт. , 2008 я я о дн 4 не л де 16 не л де 24 я не л де 36 я не л де
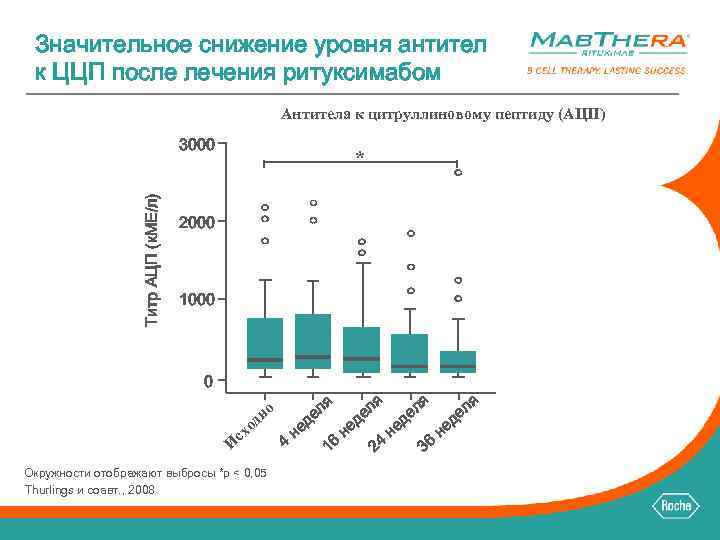
Значительное снижение уровня антител к ЦЦП после лечения ритуксимабом Антитела к цитруллиновому пептиду (АЦП) Титр АЦП (к. МЕ/л) 3000 * 2000 1000 0 но д о сх И Окружности отображают выбросы *p < 0, 05 Thurlings и соавт. , 2008 4 не д я ел 16 я не л де 24 я не л де 36 не я ел д
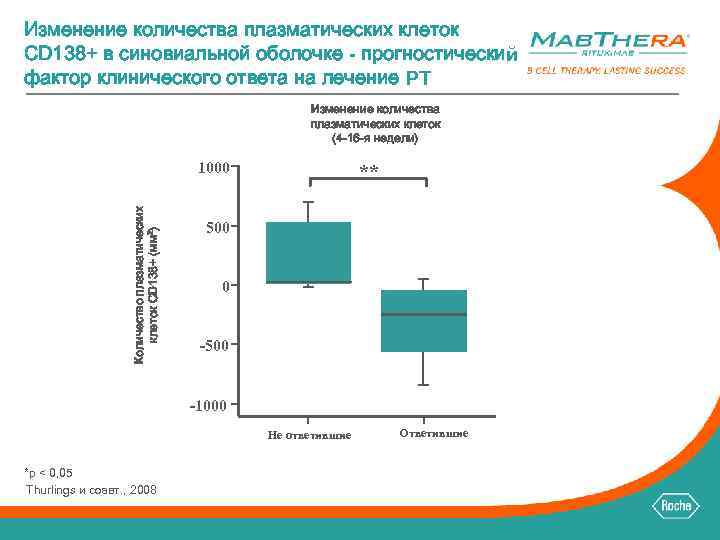
Изменение количества плазматических клеток CD 138+ в синовиальной оболочке - прогностический фактор клинического ответа на лечение РТ Изменение количества плазматических клеток (4 -16 -я недели) Количество плазматических клеток CD 138+ (мм 2) 1000 ** 500 0 -500 -1000 Не ответившие *p < 0, 05 Thurlings и соавт. , 2008 Ответившие

Ответ на ритуксимаб у пациентов с РА, серопозитивных в отношении РФ и/или анти-ЦЦП Серопозитивные (РФ и/или анти-ЦЦП) пациенты с большей вероятностью отвечают и, при наличии ответа, показывают лучший ответ на лечение ритуксимабом Это было показано в нескольких клинических исследованиях REFLEX DANCER SERENE и MIRROR (объединенная выборка) IMAGE Как при ранних, так и при развившихся формах заболевания
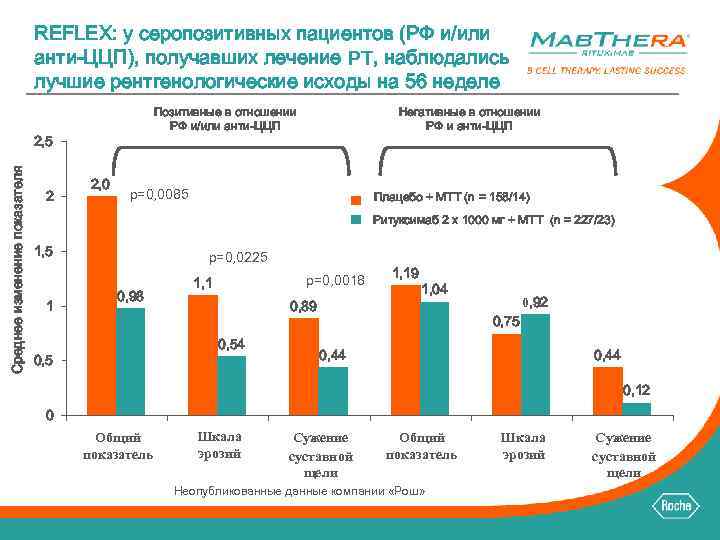
REFLEX: у серопозитивных пациентов (РФ и/или анти-ЦЦП), получавших лечение РТ, наблюдались лучшие рентгенологические исходы на 56 неделе Позитивные в отношении РФ и/или анти-ЦЦП Среднее изменение показателя 2, 5 2 2, 0 Негативные в отношении РФ и анти-ЦЦП p=0, 0085 Плацебо + МТТ (n = 158/14) Ритуксимаб 2 x 1000 мг + МТТ (n = 227/23) 1, 5 1 p=0, 0225 0, 98 p=0, 0018 1, 1 0, 89 0, 54 0, 5 1, 19 1, 04 0, 92 0, 75 0, 44 0, 12 0 Общий показатель Шкала эрозий Сужение суставной щели Общий показатель Неопубликованные данные компании «Рош» Шкала эрозий Сужение суставной щели
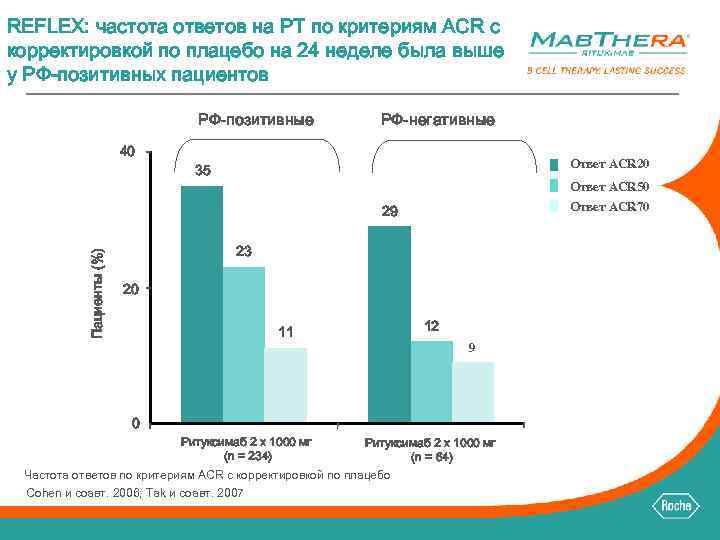
REFLEX: частота ответов на РТ по критериям ACR с корректировкой по плацебо на 24 неделе была выше у РФ-позитивных пациентов РФ-позитивные РФ-негативные 40 Ответ ACR 20 35 Ответ ACR 50 Ответ ACR 70 Пациенты (%) 29 23 20 11 12 9 0 Ритуксимаб 2 x 1000 мг (n = 234) Ритуксимаб 2 x 1000 мг (n = 64) Частота ответов по критериям ACR с корректировкой по плацебо Cohen и соавт. 2006; Tak и соавт. 2007
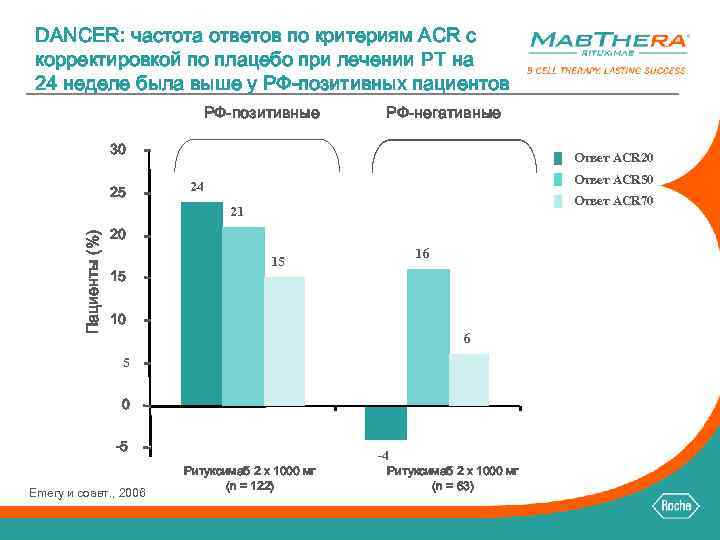
DANCER: частота ответов по критериям ACR с корректировкой по плацебо при лечении РТ на 24 неделе была выше у РФ-позитивных пациентов РФ-позитивные РФ-негативные 30 25 Ответ ACR 20 Ответ ACR 50 24 Ответ ACR 70 Пациенты (%) 21 20 15 16 15 10 6 5 0 -5 Emery и соавт. , 2006 -4 Ритуксимаб 2 x 1000 мг (n = 122) Ритуксимаб 2 x 1000 мг (n = 63)
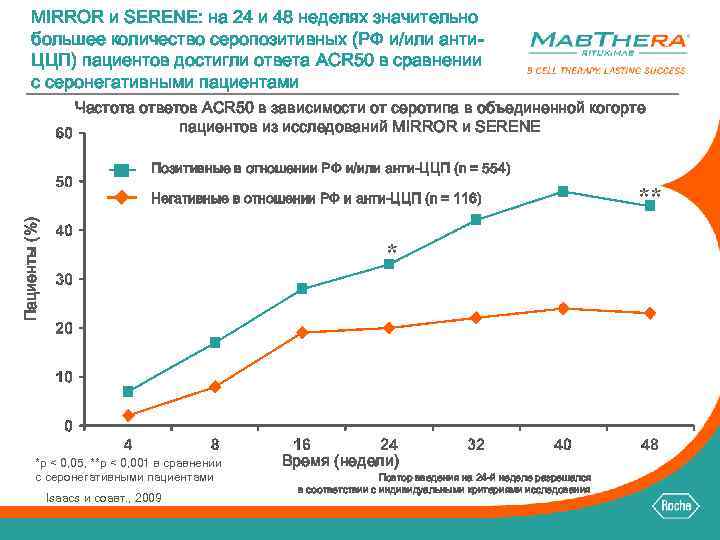
MIRROR и SERENE: на 24 и 48 неделях значительно большее количество серопозитивных (РФ и/или анти. ЦЦП) пациентов достигли ответа ACR 50 в сравнении с серонегативными пациентами Частота ответов ACR 50 в зависимости от серотипа в объединенной когорте пациентов из исследований MIRROR и SERENE Позитивные в отношении РФ и/или анти-ЦЦП (n = 554) Пациенты (%) Негативные в отношении РФ и анти-ЦЦП (n = 116) * *p < 0, 05, **p < 0, 001 в сравнении с серонегативными пациентами Isaacs и соавт. , 2009 Время (недели) Повтор введения на 24 -й неделе разрешался в соответствии с индивидуальными критериями исследования **
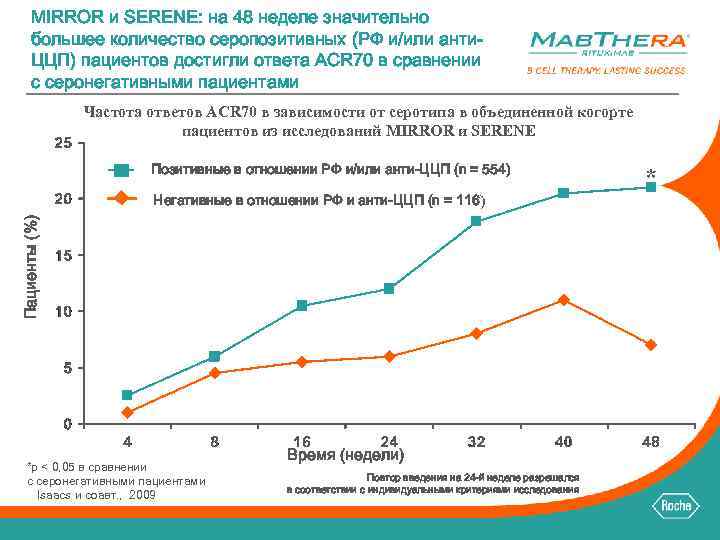
MIRROR и SERENE: на 48 неделе значительно большее количество серопозитивных (РФ и/или анти. ЦЦП) пациентов достигли ответа ACR 70 в сравнении с серонегативными пациентами Частота ответов ACR 70 в зависимости от серотипа в объединенной когорте пациентов из исследований MIRROR и SERENE Позитивные в отношении РФ и/или анти-ЦЦП (n = 554) Пациенты (%) Негативные в отношении РФ и анти-ЦЦП (n = 116) *p < 0, 05 в сравнении с серонегативными пациентами Isaacs и соавт. , 2009 Время (недели) Повтор введения на 24 -й неделе разрешался в соответствии с индивидуальными критериями исследования *
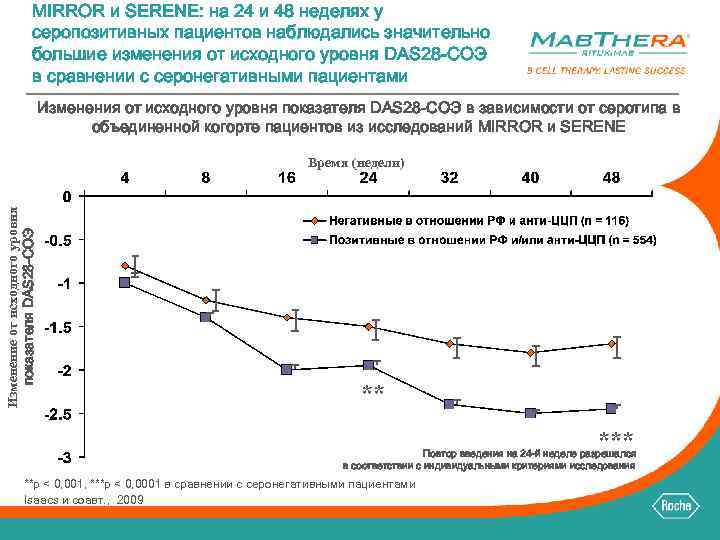
MIRROR и SERENE: на 24 и 48 неделях у серопозитивных пациентов наблюдались значительно большие изменения от исходного уровня DAS 28 -СОЭ в сравнении с серонегативными пациентами Изменения от исходного уровня показателя DAS 28 -СОЭ в зависимости от серотипа в объединенной когорте пациентов из исследований MIRROR и SERENE Изменение от исходного уровня показателя DAS 28 -СОЭ Время (недели) ** *** Повтор введения на 24 -й неделе разрешался в соответствии с индивидуальными критериями исследования **p < 0, 001, ***p < 0, 0001 в сравнении с серонегативными пациентами Isaacs и соавт. , 2009
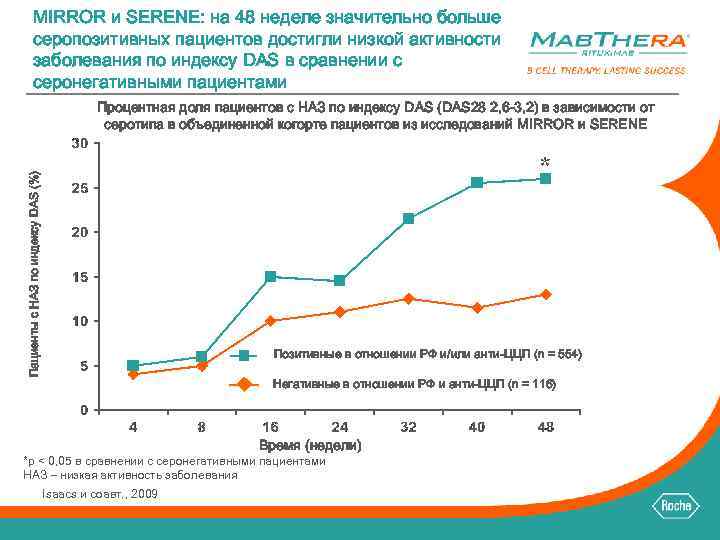
MIRROR и SERENE: на 48 неделе значительно больше серопозитивных пациентов достигли низкой активности заболевания по индексу DAS в сравнении с серонегативными пациентами Процентная доля пациентов с НАЗ по индексу DAS (DAS 28 2, 6 -3, 2) в зависимости от серотипа в объединенной когорте пациентов из исследований MIRROR и SERENE Пациенты с НАЗ по индексу DAS (%) * Позитивные в отношении РФ и/или анти-ЦЦП (n = 554) Негативные в отношении РФ и анти-ЦЦП (n = 116) Время (недели) *p < 0, 05 в сравнении с серонегативными пациентами НАЗ – низкая активность заболевания Isaacs и соавт. , 2009
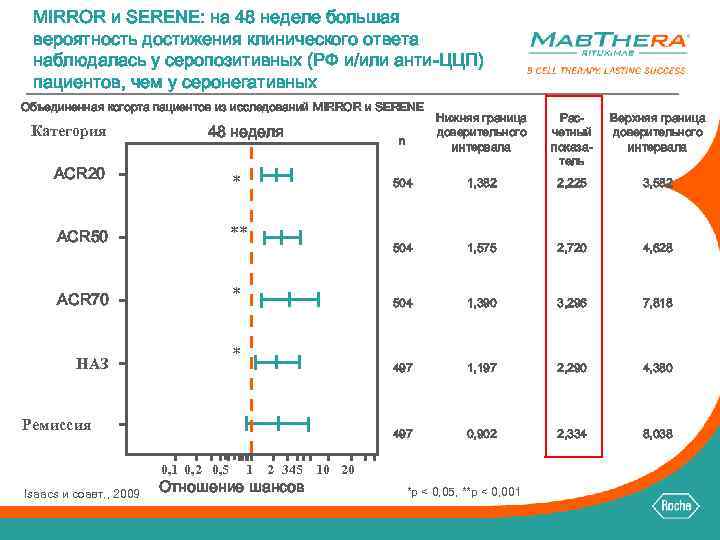
MIRROR и SERENE: на 48 неделе большая вероятность достижения клинического ответа наблюдалась у серопозитивных (РФ и/или анти-ЦЦП) пациентов, чем у серонегативных Объединенная когорта пациентов из исследований MIRROR и SERENE Категория ACR 70 * * НАЗ Ремиссия 0, 1 0, 2 0, 5 Isaacs и соавт. , 2009 1 3, 582 1, 575 2, 720 4, 628 1, 390 3, 296 7, 818 1, 197 2, 290 4, 380 497 ** 2, 225 497 ACR 50 1, 382 504 * Верхняя граница доверительного интервала 504 ACR 20 n Расчетный показатель 504 48 неделя Нижняя граница доверительного интервала 0, 902 2, 334 8, 038 2 345 10 20 Отношение шансов *p < 0, 05, **p < 0, 001
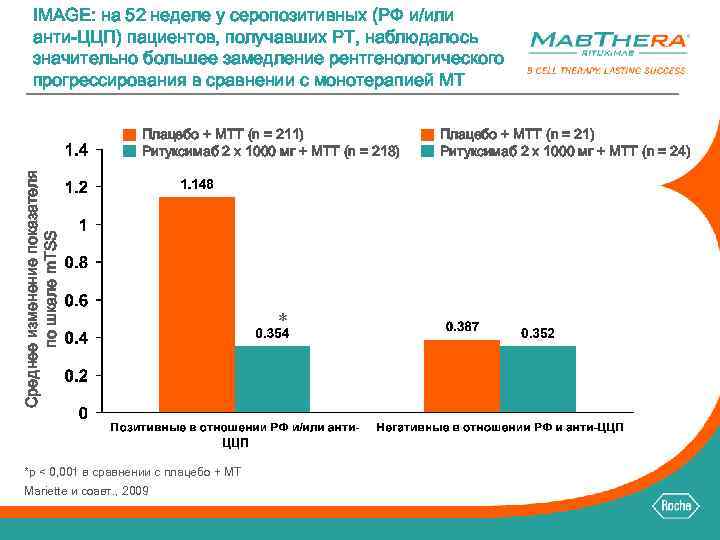
IMAGE: на 52 неделе у серопозитивных (РФ и/или анти-ЦЦП) пациентов, получавших РТ, наблюдалось значительно большее замедление рентгенологического прогрессирования в сравнении с монотерапией МТ Среднее изменение показателя по шкале m. TSS Плацебо + МТТ (n = 211) Ритуксимаб 2 x 1000 мг + МТТ (n = 218) *p < 0, 001 в сравнении с плацебо + МТ Mariette и соавт. , 2009 * Плацебо + МТТ (n = 21) Ритуксимаб 2 x 1000 мг + МТТ (n = 24)
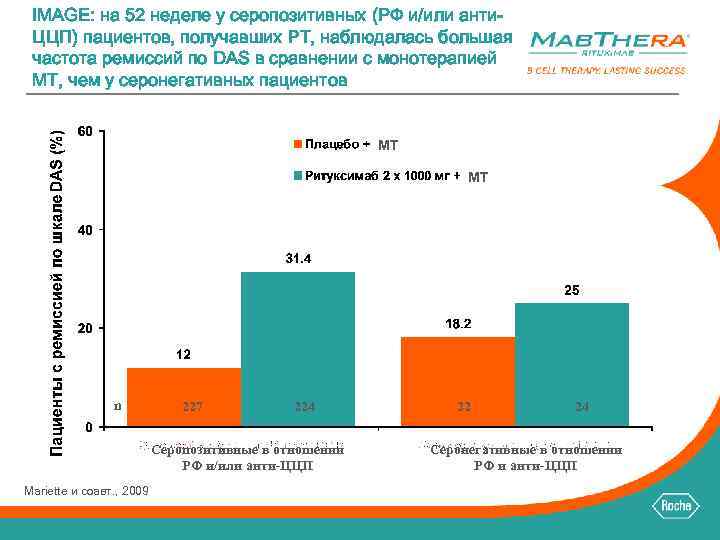
IMAGE: на 52 неделе у серопозитивных (РФ и/или анти. ЦЦП) пациентов, получавших РТ, наблюдалась большая частота ремиссий по DAS в сравнении с монотерапией МТ, чем у серонегативных пациентов МТ МТ n 227 224 Серопозитивные в отношении РФ и/или анти-ЦЦП Mariette и соавт. , 2009 22 24 Серонегативные в отношении РФ и анти-ЦЦП
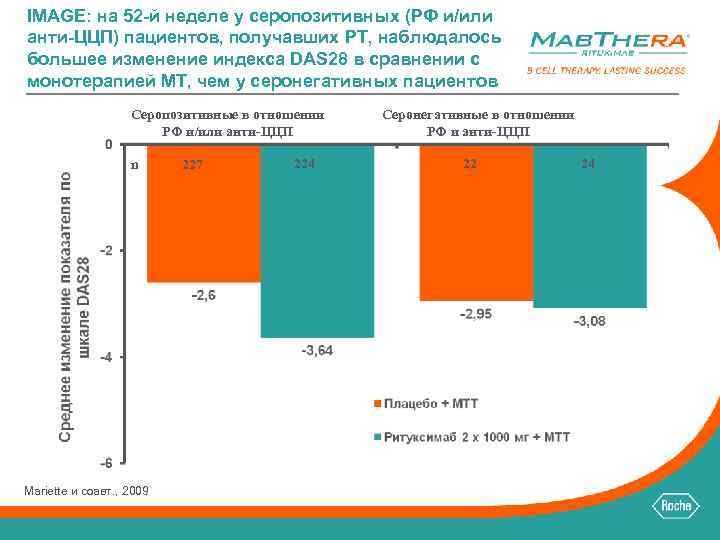
IMAGE: на 52 -й неделе у серопозитивных (РФ и/или анти-ЦЦП) пациентов, получавших РТ, наблюдалось большее изменение индекса DAS 28 в сравнении с монотерапией МТ, чем у серонегативных пациентов Серопозитивные в отношении РФ и/или анти-ЦЦП n Mariette и соавт. , 2009 227 224 Серонегативные в отношении РФ и анти-ЦЦП 22 24

Резюме: клинические данные, подтверждающие гипотезу о роли аутоиммунных антител при РА Ритуксимаб селективно воздействует на B-клетки и приводит к полному удалению B-клеток из периферической крови У пациентов с РА удаление B-клеток с помощью ритуксимаба коррелирует со снижением уровней РФ и анти-ЦЦП Пациенты, серопозитивные с отношении РФ и/или анти-ЦЦП, с большей вероятностью отвечают и при наличии ответа показывают лучший ответ на лечение ритуксимабом, направленное на B-клетки, чем серонегативные пациенты Это продемонстрировано для пациентов с ранними и развившимися формами РА

После курса лечения ритуксимабом организм заменяет удаленные аутореактивные Bклетки B-клетками наивных популяций Исследования у пациентов с РА показывают, что после удаления аутореактивных B-клеток с помощью ритуксимаба наблюдается новое наполнение периферического кровотока B-клетками В процессе этой рекапитуляции вновь образованные незрелые B-клетки дифференцируются в доминантные, промежуточные и наивные B-клетки Roll и соавт. , 2008; Dorner и соавт. , 2009

Общее резюме B-клетки играют основную роль в патофизиологии РА Продуцируют аутоиммунные антитела Выделяют провоспалительные цитокины Активируют T-клетки B-клетки продуцируют аутоиммунные антитела (РФ и анти-ЦЦП), которые имеются у многих пациентов с РА и связаны с быстрым прогрессированием заболевания РА Ритуксимаб эффективно удаляет CD 20+ B-клетки и, в свою очередь, воздействует на источник этих аутоиммунных антител Пациенты, серопозитивные в отношении РФ и/или анти-ЦЦП, с большей вероятностью отвечают и при наличии ответа показывают лучший ответ на лечение ритуксимабом в сравнении с серонегативными пациентами Наличие аутоиммунных антител (продуцируемых B-клетками) может указывать на подгруппу пациентов с РА, имеющих большую вовлеченность в процесс B-клеток
Роль В-клеток.ppt