2 Растворы. Электролиты.ppt
- Количество слайдов: 17



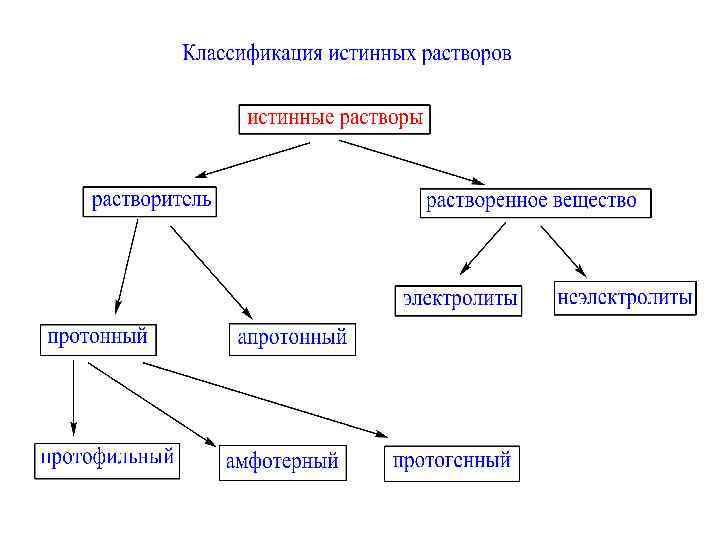

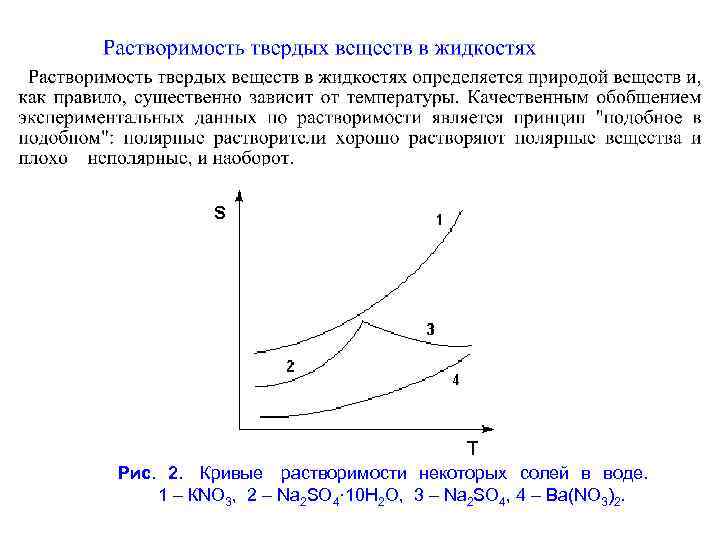 Рис. 2. Кривые растворимости некоторых солей в воде. 1 – КNО 3, 2 – Nа 2 SО 4· 10 Н 2 О, 3 – Nа 2 SО 4, 4 – Ва(NО 3)2.
Рис. 2. Кривые растворимости некоторых солей в воде. 1 – КNО 3, 2 – Nа 2 SО 4· 10 Н 2 О, 3 – Nа 2 SО 4, 4 – Ва(NО 3)2.
 Растворимость S – способность вещества раство- ряться в том или ином растворителе. Она характеризу- ется концентрацией насыщенного раствора. Насыщенный раствор – раствор, находящийся в равновесии с растворенным веществом. Растворимость часто выражают количеством граммов растворяемого вещества в 100 г растворителя. Если раствор содержит растворенного вещества больше, чем это соответствует растворимости при данной температуре, то он называ- ется пересыщенным. Возможность существования пересыщенного раствора объясняется трудностью возникновения центров кристаллизации. В случае растворения твердых или жидких веществ в жидкостях растворимость возрастает с повышением температуры, а для газов – убывает. На растворимость газов большое влияние оказывает давление.
Растворимость S – способность вещества раство- ряться в том или ином растворителе. Она характеризу- ется концентрацией насыщенного раствора. Насыщенный раствор – раствор, находящийся в равновесии с растворенным веществом. Растворимость часто выражают количеством граммов растворяемого вещества в 100 г растворителя. Если раствор содержит растворенного вещества больше, чем это соответствует растворимости при данной температуре, то он называ- ется пересыщенным. Возможность существования пересыщенного раствора объясняется трудностью возникновения центров кристаллизации. В случае растворения твердых или жидких веществ в жидкостях растворимость возрастает с повышением температуры, а для газов – убывает. На растворимость газов большое влияние оказывает давление.

 1. Теория электролитической диссоциации (ТЭД). Сванте Аррениус В 1887 г. Шведский учёный С. Аррениус для объяснения особенностей водных растворов веществ предложил теорию электролитической диссоциации. В дальнейшем эта теория была развита многими учёными, в том числе И. А. Каблуковым и В. А. Кистяковским.
1. Теория электролитической диссоциации (ТЭД). Сванте Аррениус В 1887 г. Шведский учёный С. Аррениус для объяснения особенностей водных растворов веществ предложил теорию электролитической диссоциации. В дальнейшем эта теория была развита многими учёными, в том числе И. А. Каблуковым и В. А. Кистяковским.
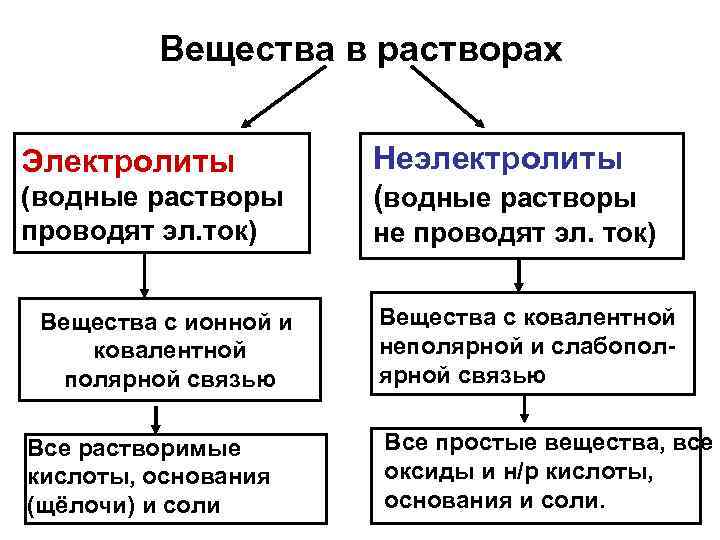 Вещества в растворах Электролиты (водные растворы проводят эл. ток) Вещества с ионной и ковалентной полярной связью Все растворимые кислоты, основания (щёлочи) и соли Неэлектролиты (водные растворы не проводят эл. ток) Вещества с ковалентной неполярной и слабополярной связью Все простые вещества, все оксиды и н/р кислоты, основания и соли.
Вещества в растворах Электролиты (водные растворы проводят эл. ток) Вещества с ионной и ковалентной полярной связью Все растворимые кислоты, основания (щёлочи) и соли Неэлектролиты (водные растворы не проводят эл. ток) Вещества с ковалентной неполярной и слабополярной связью Все простые вещества, все оксиды и н/р кислоты, основания и соли.
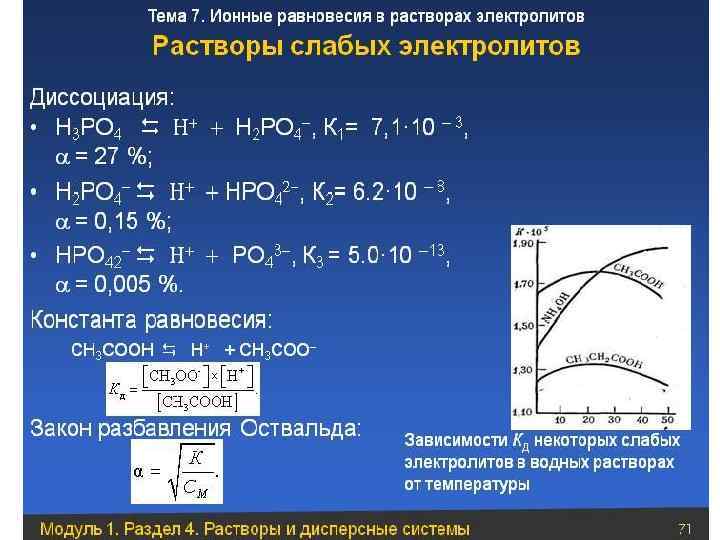
 Электролиты – вещества, которые при растворении подвергаются диссоциации на ионы. В результате раствор приобретает способность проводить электрический ток, т. к. в нем появляются подвижные носители электрического заряда. Например, при растворении в воде уксусная кислота диссоциирует на ион водорода и ацетат-ион: CH 3 COO– + H+ = CH 3 COOH Необходимым условием, определяющим возможность процесса электролитической диссоциации, является наличие в растворяемом веществе ионных или полярных связей , а также достаточная полярность самого растворителя. Количественная оценка процесса электролитической диссоциации дается двумя величинами: степенью диссоциации α и константой диссоциации K.
Электролиты – вещества, которые при растворении подвергаются диссоциации на ионы. В результате раствор приобретает способность проводить электрический ток, т. к. в нем появляются подвижные носители электрического заряда. Например, при растворении в воде уксусная кислота диссоциирует на ион водорода и ацетат-ион: CH 3 COO– + H+ = CH 3 COOH Необходимым условием, определяющим возможность процесса электролитической диссоциации, является наличие в растворяемом веществе ионных или полярных связей , а также достаточная полярность самого растворителя. Количественная оценка процесса электролитической диссоциации дается двумя величинами: степенью диссоциации α и константой диссоциации K.
 Степенью диссоциации (α) электролита называется отношение числа его молекул, распавшихся на ионы, к общему числу молекул электролита в растворе, т. е. Степень электролитической диссоциации зависит как от природы растворенного вещества, так и от концентрации раствора, увеличиваясь с его разбавлением. Электролиты можно разделить на две большие группы: сильные и слабые. Сильные электролиты (например, H 2 SO 4, HCl, HNO 3, H 3 PO 4, HCl. O 3, HCl. O 4, KOH, Na. Cl, KBr, NH 4 NO 3 и др. ) диссоциируют практически полностью. Для слабых электролитов устанавливается равновесие между недиссоциированными молекулами и ионами. К слабым электролитам относятся плохо растворимые соли,
Степенью диссоциации (α) электролита называется отношение числа его молекул, распавшихся на ионы, к общему числу молекул электролита в растворе, т. е. Степень электролитической диссоциации зависит как от природы растворенного вещества, так и от концентрации раствора, увеличиваясь с его разбавлением. Электролиты можно разделить на две большие группы: сильные и слабые. Сильные электролиты (например, H 2 SO 4, HCl, HNO 3, H 3 PO 4, HCl. O 3, HCl. O 4, KOH, Na. Cl, KBr, NH 4 NO 3 и др. ) диссоциируют практически полностью. Для слабых электролитов устанавливается равновесие между недиссоциированными молекулами и ионами. К слабым электролитам относятся плохо растворимые соли,
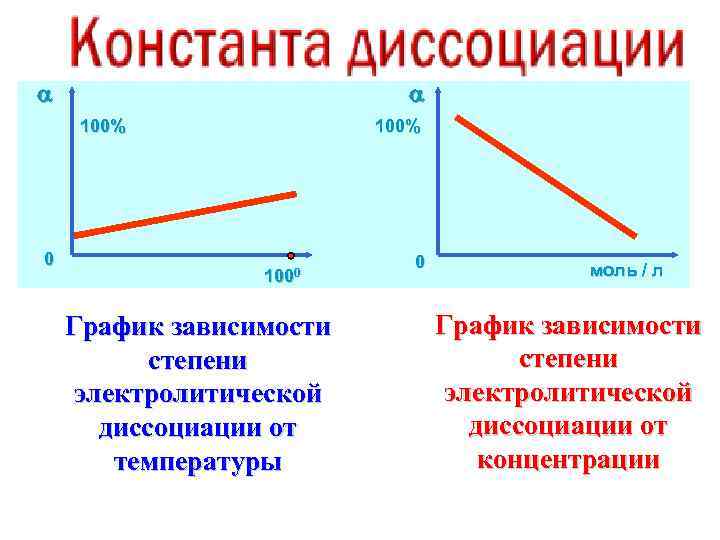 100% 0 100% 1000 График зависимости степени электролитической диссоциации от температуры 0 моль / л График зависимости степени электролитической диссоциации от концентрации
100% 0 100% 1000 График зависимости степени электролитической диссоциации от температуры 0 моль / л График зависимости степени электролитической диссоциации от концентрации
 вода и большинство органических кислот (например, уксусная CH 3 COOH, муравьиная HCOOH), а также неорганические соединения: H 2 CO 3, H 2 S, HCN, H 2 Si. O 3, H 2 SO 3, HNO 2, HCl. O, HCNO, NH 4 OH и др. Константа равновесия для процесса диссоциации называется константой диссоциации (K). В общем случае для электролита, . диссоциирующего на два иона: АВ А + + В– Для приведенного выше процесса диссоциации уксусной кислоты: Если обозначить концентрацию электролита, распадающегося на два иона, через C, то [A+] = [B–] = a. C; [AB] = C(1–a);
вода и большинство органических кислот (например, уксусная CH 3 COOH, муравьиная HCOOH), а также неорганические соединения: H 2 CO 3, H 2 S, HCN, H 2 Si. O 3, H 2 SO 3, HNO 2, HCl. O, HCNO, NH 4 OH и др. Константа равновесия для процесса диссоциации называется константой диссоциации (K). В общем случае для электролита, . диссоциирующего на два иона: АВ А + + В– Для приведенного выше процесса диссоциации уксусной кислоты: Если обозначить концентрацию электролита, распадающегося на два иона, через C, то [A+] = [B–] = a. C; [AB] = C(1–a);
 Это уравнение соответствует закону разбавления Оствальда. Если электролит слабый, и диссоциация очень мала (a<<1), то закон разбав - ления Оствальда упрощается: K=a 2 C; Многоосновные кислоты, а также основания многовалентных метал - лов диссоциируют ступенчато. Например: H 2 CO 3 HCO 3– H+ + CO 32– Первое равновесие – диссоциация по первой ступени – характеризуется константой KI = 4, 3× 10– 7, KII = 5, 6× 10– 11. Для ступенчатой диссоциации всегда KI>KIII>¼, т. к. энергия, которую необходимо затратить для отрыва иона, минимальна при отрыве его от нейтральной молекулы.
Это уравнение соответствует закону разбавления Оствальда. Если электролит слабый, и диссоциация очень мала (a<<1), то закон разбав - ления Оствальда упрощается: K=a 2 C; Многоосновные кислоты, а также основания многовалентных метал - лов диссоциируют ступенчато. Например: H 2 CO 3 HCO 3– H+ + CO 32– Первое равновесие – диссоциация по первой ступени – характеризуется константой KI = 4, 3× 10– 7, KII = 5, 6× 10– 11. Для ступенчатой диссоциации всегда KI>KIII>¼, т. к. энергия, которую необходимо затратить для отрыва иона, минимальна при отрыве его от нейтральной молекулы.