Введение стом. материаловед Ричард...ppt
- Количество слайдов: 57
 Ричард ван Нурт Основы стоматологического материаловедения (2 -е изд. ) Mosby, 2004. - 304 с. ISBN 0 -7234 -3215 -5 (англ. ), ISBN 5 -9900267 -1 -4 PDF (14, 29 mb) язык русский качество хорошее (текст распознан, иллюстрации цветные)
Ричард ван Нурт Основы стоматологического материаловедения (2 -е изд. ) Mosby, 2004. - 304 с. ISBN 0 -7234 -3215 -5 (англ. ), ISBN 5 -9900267 -1 -4 PDF (14, 29 mb) язык русский качество хорошее (текст распознан, иллюстрации цветные)
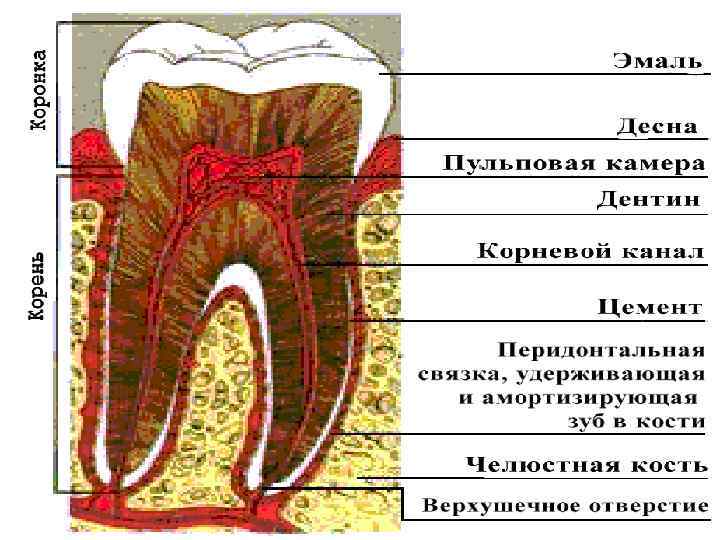
 Эмаль (enamelum) - это ткань, покрывающая коронку зуба, самая твердая ткань организма. На жевательной поверхности ее толщина 1, 5 - 1, 7 мм. На боковых поверхностях эмаль значительно тоньше и сходит на нет к шейке, к месту соединения с цементом корня. Она на 98% состоит из неорганических веществ. Основными компонентами кристаллов эмали являются кальций и фосфор. Дентин (dentinum) - составляет основную массу зуба. В нем содержится 70% неорганических веществ и 30% органических веществ и воды. Основу неорганического вещества составляют фосфат кальция (гидроксилапатит), карбонат кальция и фторид кальция. В дентине имеются канальцы, содержащие окончания чувствительных волокон.
Эмаль (enamelum) - это ткань, покрывающая коронку зуба, самая твердая ткань организма. На жевательной поверхности ее толщина 1, 5 - 1, 7 мм. На боковых поверхностях эмаль значительно тоньше и сходит на нет к шейке, к месту соединения с цементом корня. Она на 98% состоит из неорганических веществ. Основными компонентами кристаллов эмали являются кальций и фосфор. Дентин (dentinum) - составляет основную массу зуба. В нем содержится 70% неорганических веществ и 30% органических веществ и воды. Основу неорганического вещества составляют фосфат кальция (гидроксилапатит), карбонат кальция и фторид кальция. В дентине имеются канальцы, содержащие окончания чувствительных волокон.
 Цемент (cementum) - это прослойка ткани, покрывающая корень зуба и состоящая из 68% неорганических и 32% органических веществ. По химическому составу цемент напоминает костную ткань. В отличие от кости цемент не имеет кровеносных сосудов. Пульпа (pulpa) является самой чувствительной тканью зуба, состоящей из сплетения нервных волокон и кровеносных сосудов. Они проникают в зуб через отверстие, которое имеется на верхушке каждого корня. Между корнем зуба и стенкой лунки имеется щельпериодонт, в которой располагаются связки, обеспечивающие фиксацию корня и распределяющие жевательное давление.
Цемент (cementum) - это прослойка ткани, покрывающая корень зуба и состоящая из 68% неорганических и 32% органических веществ. По химическому составу цемент напоминает костную ткань. В отличие от кости цемент не имеет кровеносных сосудов. Пульпа (pulpa) является самой чувствительной тканью зуба, состоящей из сплетения нервных волокон и кровеносных сосудов. Они проникают в зуб через отверстие, которое имеется на верхушке каждого корня. Между корнем зуба и стенкой лунки имеется щельпериодонт, в которой располагаются связки, обеспечивающие фиксацию корня и распределяющие жевательное давление.
 Требования, предъявляемые к биоматериалам. Химические свойства: • отсутствие нежелательных химических реакций с тканями и межтканевыми жидкостями • отсутствие коррозии, или растворение с контролируемой скоростью Механические свойства: • прочность • трещиностойкость • сопротивление замедленному разрушению (усталости) • износостойкость Биологические свойства: • отсутствие реакций со стороны иммунной системы (биосовместимость) • срастание с костной тканью • стимулирование остеосинтеза
Требования, предъявляемые к биоматериалам. Химические свойства: • отсутствие нежелательных химических реакций с тканями и межтканевыми жидкостями • отсутствие коррозии, или растворение с контролируемой скоростью Механические свойства: • прочность • трещиностойкость • сопротивление замедленному разрушению (усталости) • износостойкость Биологические свойства: • отсутствие реакций со стороны иммунной системы (биосовместимость) • срастание с костной тканью • стимулирование остеосинтеза
 Биосовмеситмым называется материал, который не обладает отрицательным действием на биологические ткани. Важно помнить, что взаимодействие между материалами и биологической средой может проходить по двум направлениям. Одно из них — когда материал подвергается влиянию биологических тканей, а второе — когда на биологические ткани воздействует материал. Взаимодействие между стоматологическим восстановительным материалом и биологической средой может проявляться в виде: • послеоперационной чувствительности; • признаков проявления токсичности; • коррозии материала; • гиперчувствительности/аллергии.
Биосовмеситмым называется материал, который не обладает отрицательным действием на биологические ткани. Важно помнить, что взаимодействие между материалами и биологической средой может проходить по двум направлениям. Одно из них — когда материал подвергается влиянию биологических тканей, а второе — когда на биологические ткани воздействует материал. Взаимодействие между стоматологическим восстановительным материалом и биологической средой может проявляться в виде: • послеоперационной чувствительности; • признаков проявления токсичности; • коррозии материала; • гиперчувствительности/аллергии.
 Основные области применения биоматериалов: • стоматологические восстановительные материалы, к которым относятся металлические и композитные пломбировочные материалы, а также керамика для несъемного протезирования и материалы для съемных зубных протезов; • имплантаты, например внутричелюстные , имплантаты, челюстно-лицевых суставов и др. ; • сердечно-сосудистые имплантаты, такие как катетеры, протезы клапанов сердца и сосудов, а также материалы для диализа и кислородонасыщающие мембраны.
Основные области применения биоматериалов: • стоматологические восстановительные материалы, к которым относятся металлические и композитные пломбировочные материалы, а также керамика для несъемного протезирования и материалы для съемных зубных протезов; • имплантаты, например внутричелюстные , имплантаты, челюстно-лицевых суставов и др. ; • сердечно-сосудистые имплантаты, такие как катетеры, протезы клапанов сердца и сосудов, а также материалы для диализа и кислородонасыщающие мембраны.
 Отклик организма на имплантат Если материал: I. токсичный - окружающие ткани отмирают II. биоинертный- образуется соединительная волокнистая ткань III. биоактивный - образуется костная ткань IV. биорезорбируемый - происходит замена материала костной тканью
Отклик организма на имплантат Если материал: I. токсичный - окружающие ткани отмирают II. биоинертный- образуется соединительная волокнистая ткань III. биоактивный - образуется костная ткань IV. биорезорбируемый - происходит замена материала костной тканью
 Разрушение зубов не ново. 600 - до н. э. Этрусками изготовлен мостовидный протез из золота… 1500 -е Из слоновой кости гравируются зубные протезы 1744 -первый протез из фарфора… 1839 Издан первый стоматологический журнал 1879 Внедрен цинк-фосфатный цемент. 1880 -е Разработан силикатный цемент 1950 -е Внедрение акриловой пластмассы. 1978 -появление свето-отверждаемых композитов 1985 Разрабатываются адгезивы для дентина 1994 На рынке появляется первый компомер
Разрушение зубов не ново. 600 - до н. э. Этрусками изготовлен мостовидный протез из золота… 1500 -е Из слоновой кости гравируются зубные протезы 1744 -первый протез из фарфора… 1839 Издан первый стоматологический журнал 1879 Внедрен цинк-фосфатный цемент. 1880 -е Разработан силикатный цемент 1950 -е Внедрение акриловой пластмассы. 1978 -появление свето-отверждаемых композитов 1985 Разрабатываются адгезивы для дентина 1994 На рынке появляется первый компомер
 Все материалы состоят из атомов и молекул, и неудивительно, что между атомным строением материала и его свойствами существует тесная взаимосвязь. Поэтому особую важность приобретает природа атомов и их расположение в молекуле. От сочетания атомов в молекуле зависит микроструктура твердого вещества, и, как следствие, его свойства. Следовательно, если мы хотим понять, от чего зависят свойства материала, мы должны представлять себе, как группируются атомы, образующие твердое вещество.
Все материалы состоят из атомов и молекул, и неудивительно, что между атомным строением материала и его свойствами существует тесная взаимосвязь. Поэтому особую важность приобретает природа атомов и их расположение в молекуле. От сочетания атомов в молекуле зависит микроструктура твердого вещества, и, как следствие, его свойства. Следовательно, если мы хотим понять, от чего зависят свойства материала, мы должны представлять себе, как группируются атомы, образующие твердое вещество.
 Существует три вида первичных связей: ковалентная, ионная и металлическая. Ковалентная связь является простейшей и, в то же время, самой прочной из трех видов связей. Она образуется в том случае, если электроны двух связанных атомов обобществляются таким образом, чтобы завершить строение электронной оболочки каждого из них до состояния оболочки инертного газа.
Существует три вида первичных связей: ковалентная, ионная и металлическая. Ковалентная связь является простейшей и, в то же время, самой прочной из трех видов связей. Она образуется в том случае, если электроны двух связанных атомов обобществляются таким образом, чтобы завершить строение электронной оболочки каждого из них до состояния оболочки инертного газа.
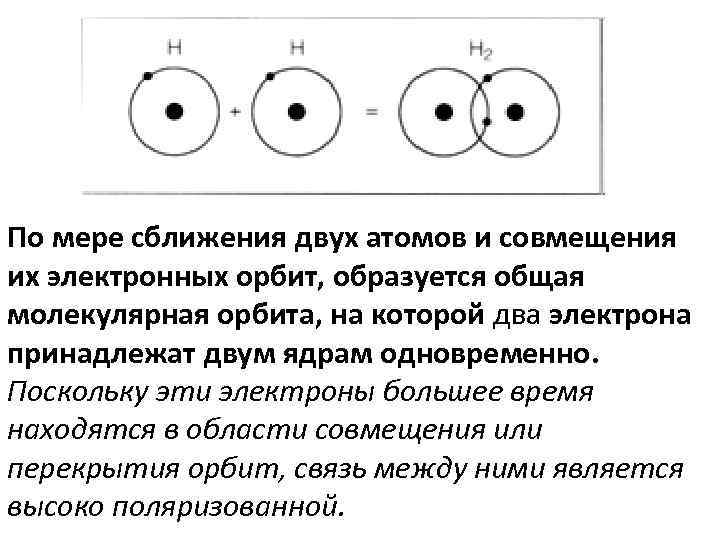 По мере сближения двух атомов и совмещения их электронных орбит, образуется общая молекулярная орбита, на которой два электрона принадлежат двум ядрам одновременно. Поскольку эти электроны большее время находятся в области совмещения или перекрытия орбит, связь между ними является высоко поляризованной.
По мере сближения двух атомов и совмещения их электронных орбит, образуется общая молекулярная орбита, на которой два электрона принадлежат двум ядрам одновременно. Поскольку эти электроны большее время находятся в области совмещения или перекрытия орбит, связь между ними является высоко поляризованной.
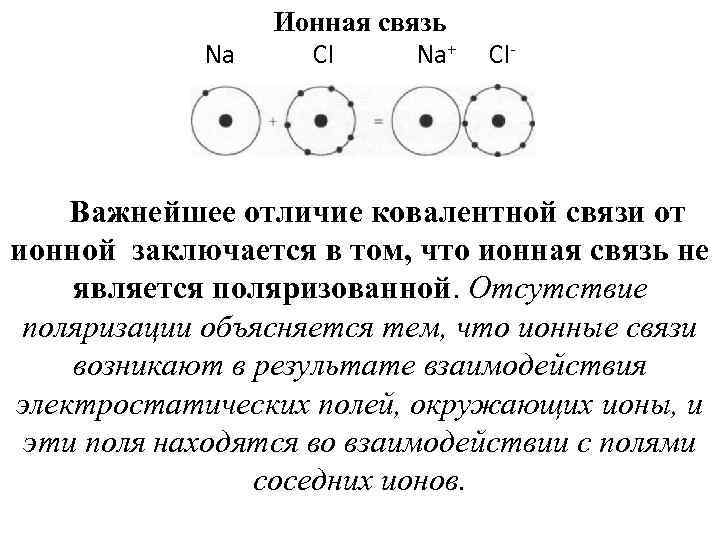 Ионная связь Na CI Na+ СI- Важнейшее отличие ковалентной связи от ионной заключается в том, что ионная связь не является поляризованной. Отсутствие поляризации объясняется тем, что ионные связи возникают в результате взаимодействия электростатических полей, окружающих ионы, и эти поля находятся во взаимодействии с полями соседних ионов.
Ионная связь Na CI Na+ СI- Важнейшее отличие ковалентной связи от ионной заключается в том, что ионная связь не является поляризованной. Отсутствие поляризации объясняется тем, что ионные связи возникают в результате взаимодействия электростатических полей, окружающих ионы, и эти поля находятся во взаимодействии с полями соседних ионов.
 Элементы подобные натрию, легко теряют свой единственный валентный электрон если рядом окажется другой атом, который сможет с готовностью принять отдаваемый электрон. Этими элементами являются фтор, хлор, бром и йод, известные под названием галогенов. Таким образом, если обеспечить взаимодействие атомов натрия и хлора, то произойдет полный переход валентного электрона от атома натрия к атому хлора. Оба этих атома приобретут структуру инертного газа, при этом натрий будет иметь положительный заряд, так как он отдал свой отрицательно заряженный электрон хлору, а хлор приобретет отрицательный заряд за счет принятия дополнительного электрона от натрия. Эти два иона будут притягиваться один к другому за счет взаимодействия противоположных электрических зарядов, при этом их полная энергия снизится.
Элементы подобные натрию, легко теряют свой единственный валентный электрон если рядом окажется другой атом, который сможет с готовностью принять отдаваемый электрон. Этими элементами являются фтор, хлор, бром и йод, известные под названием галогенов. Таким образом, если обеспечить взаимодействие атомов натрия и хлора, то произойдет полный переход валентного электрона от атома натрия к атому хлора. Оба этих атома приобретут структуру инертного газа, при этом натрий будет иметь положительный заряд, так как он отдал свой отрицательно заряженный электрон хлору, а хлор приобретет отрицательный заряд за счет принятия дополнительного электрона от натрия. Эти два иона будут притягиваться один к другому за счет взаимодействия противоположных электрических зарядов, при этом их полная энергия снизится.
 Третьим видом первичной связи является металлическая связь. Она возникает при сильном сближении атомов, обычно в твердых телах, которые легко отдают электроны со своих валентных электронных оболочек. В таких случаях, электроны могут достаточно свободно перемещаться в структуре твердого тела. Электронные орбиты в металлической связи обладают более низкой энергией по сравнению с электронными орбитами отдельных атомов. Это объясняется тем, что электроны внешних электронных оболочек всегда находятся на более близком расстоянии от того или иного ядра, чем находились бы в случае изолированного атома. Подобно ионной, металлическая связь не поляризована.
Третьим видом первичной связи является металлическая связь. Она возникает при сильном сближении атомов, обычно в твердых телах, которые легко отдают электроны со своих валентных электронных оболочек. В таких случаях, электроны могут достаточно свободно перемещаться в структуре твердого тела. Электронные орбиты в металлической связи обладают более низкой энергией по сравнению с электронными орбитами отдельных атомов. Это объясняется тем, что электроны внешних электронных оболочек всегда находятся на более близком расстоянии от того или иного ядра, чем находились бы в случае изолированного атома. Подобно ионной, металлическая связь не поляризована.
 В зависимости от степени взаимодействия между атомами может возникнуть одно их трех известных состояний вещества: газы, жидкости или твердые тела. Все атомы стремятся к энергетическому состоянию с наименьшей энергией, и это равносильно абсолютному заполнению самой дальней от центра электронной орбиты, наподобие того, что наблюдается у инертных газов. В образовании связи участвуют только те электроны, которые расположены на внешних электронных орбитах, т. е. валентные электроны.
В зависимости от степени взаимодействия между атомами может возникнуть одно их трех известных состояний вещества: газы, жидкости или твердые тела. Все атомы стремятся к энергетическому состоянию с наименьшей энергией, и это равносильно абсолютному заполнению самой дальней от центра электронной орбиты, наподобие того, что наблюдается у инертных газов. В образовании связи участвуют только те электроны, которые расположены на внешних электронных орбитах, т. е. валентные электроны.
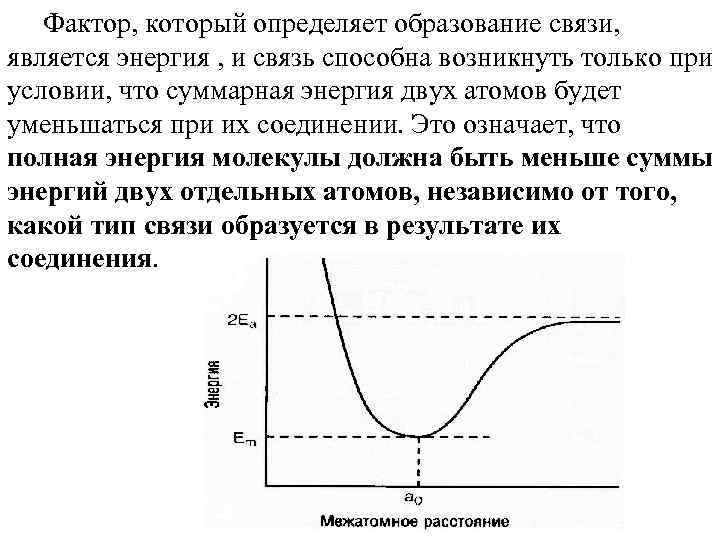 Фактор, который определяет образование связи, является энергия , и связь способна возникнуть только при условии, что суммарная энергия двух атомов будет уменьшаться при их соединении. Это означает, что полная энергия молекулы должна быть меньше суммы энергий двух отдельных атомов, независимо от того, какой тип связи образуется в результате их соединения.
Фактор, который определяет образование связи, является энергия , и связь способна возникнуть только при условии, что суммарная энергия двух атомов будет уменьшаться при их соединении. Это означает, что полная энергия молекулы должна быть меньше суммы энергий двух отдельных атомов, независимо от того, какой тип связи образуется в результате их соединения.
 Энергия связи — это количество энергии, которое должно быть приложено для разделения двух атомов. Общая особенность, в том, что ковалентные связи являются самыми прочными , за ними следуют ионные связи, и , наконец, металлические. Энергия металлической связи изменяется в широких пределах — в некоторых случаях ее величина близко подходит к значениям энергий ионной связи, а в других — является крайне низкой(Ртуть).
Энергия связи — это количество энергии, которое должно быть приложено для разделения двух атомов. Общая особенность, в том, что ковалентные связи являются самыми прочными , за ними следуют ионные связи, и , наконец, металлические. Энергия металлической связи изменяется в широких пределах — в некоторых случаях ее величина близко подходит к значениям энергий ионной связи, а в других — является крайне низкой(Ртуть).
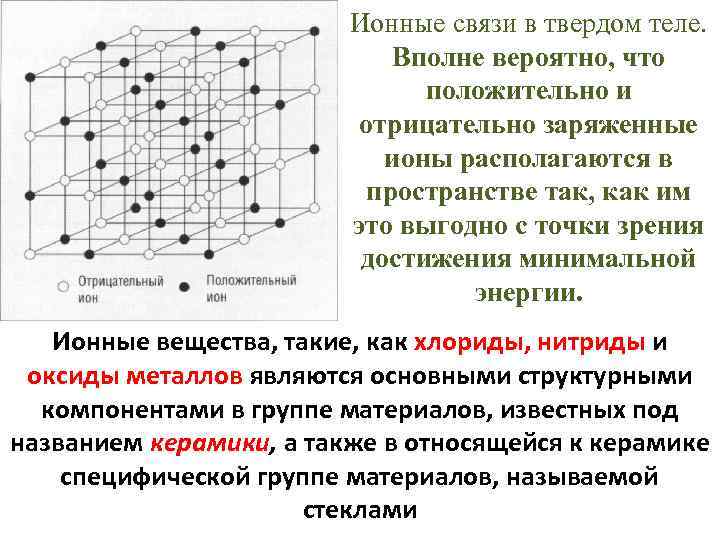 Ионные связи в твердом теле. Вполне вероятно, что положительно и отрицательно заряженные ионы располагаются в пространстве так, как им это выгодно с точки зрения достижения минимальной энергии. Ионные вещества, такие, как хлориды, нитриды и оксиды металлов являются основными структурными компонентами в группе материалов, известных под названием керамики, а также в относящейся к керамике специфической группе материалов, называемой стеклами
Ионные связи в твердом теле. Вполне вероятно, что положительно и отрицательно заряженные ионы располагаются в пространстве так, как им это выгодно с точки зрения достижения минимальной энергии. Ионные вещества, такие, как хлориды, нитриды и оксиды металлов являются основными структурными компонентами в группе материалов, известных под названием керамики, а также в относящейся к керамике специфической группе материалов, называемой стеклами
 Металлические связи в твердом теле. Расположение (кристаллическое), подобное ионным решеткам, может существовать и при наличии металлической связи. В этом случае отдельные атомы удерживаются не за счет сил прочного электростатического притяжения, наблюдаемого между атомами в ионных твердых телах, а за счет обобщенного облака электронов. Это облако придает особые свойства металлам(стягивает их атомы). Ковалентные связи в твердом теле Существует всего несколько твердых веществ с ковалентной связью — ими являются углерод, кремний и германий. Основным отличием ковалентной связи от двух других первичных связей является ее полярность.
Металлические связи в твердом теле. Расположение (кристаллическое), подобное ионным решеткам, может существовать и при наличии металлической связи. В этом случае отдельные атомы удерживаются не за счет сил прочного электростатического притяжения, наблюдаемого между атомами в ионных твердых телах, а за счет обобщенного облака электронов. Это облако придает особые свойства металлам(стягивает их атомы). Ковалентные связи в твердом теле Существует всего несколько твердых веществ с ковалентной связью — ими являются углерод, кремний и германий. Основным отличием ковалентной связи от двух других первичных связей является ее полярность.
 Твердые вещества с ковалентными связями, состоящие из одного элемента, встречаются крайне редко. Чаще ковалентные связи образуются между разными элементами. Поскольку для образования таких связей элементы вступают в химическую реакцию, образовавшаяся молекула становится крайне инертной по отношению к другим молекулам. Электронные орбиты перекрываются и электроны становятся общими, что приводит к полному завершению электронных орбит.
Твердые вещества с ковалентными связями, состоящие из одного элемента, встречаются крайне редко. Чаще ковалентные связи образуются между разными элементами. Поскольку для образования таких связей элементы вступают в химическую реакцию, образовавшаяся молекула становится крайне инертной по отношению к другим молекулам. Электронные орбиты перекрываются и электроны становятся общими, что приводит к полному завершению электронных орбит.
 СТРУКТУРНОЕ РАСПОЛОЖЕНИЕ АТОМОВ В ТВЕРДОМ ТЕЛЕ Несмотря на то, что силы притяжения удерживают атомы на близком расстоянии друг от друга, взаимное отталкивание ядер означает, что равновесное пространственное положение атомов достигается только при сбалансированных силах притяжения и отталкивания. При упорядоченном расположении атомов (с минимальной суммарной энергией) материал называют кристаллическим. Важной особенностью кристаллических структур является то, что какой бы атом мы не рассматривали в данной структуре, расположение соседних с ним атомов по отношению к нему всегда будет идентичным.
СТРУКТУРНОЕ РАСПОЛОЖЕНИЕ АТОМОВ В ТВЕРДОМ ТЕЛЕ Несмотря на то, что силы притяжения удерживают атомы на близком расстоянии друг от друга, взаимное отталкивание ядер означает, что равновесное пространственное положение атомов достигается только при сбалансированных силах притяжения и отталкивания. При упорядоченном расположении атомов (с минимальной суммарной энергией) материал называют кристаллическим. Важной особенностью кристаллических структур является то, что какой бы атом мы не рассматривали в данной структуре, расположение соседних с ним атомов по отношению к нему всегда будет идентичным.
 Одним из простейших расположений атомов в пространстве является куб, в котором атомы занимают положения в восьми углах. Каждая сфера соприкасается со своим ближайшим соседом, таким образом, длина стороны куба равна диаметру атома (элементарная ячейка). В пределах структурной единицы атомы не находятся в неподвижном состоянии — они совершают колебательные движения. Доля пространства, занимаемая атомами, называется фактором упаковки, и ее легко рассчитать.
Одним из простейших расположений атомов в пространстве является куб, в котором атомы занимают положения в восьми углах. Каждая сфера соприкасается со своим ближайшим соседом, таким образом, длина стороны куба равна диаметру атома (элементарная ячейка). В пределах структурной единицы атомы не находятся в неподвижном состоянии — они совершают колебательные движения. Доля пространства, занимаемая атомами, называется фактором упаковки, и ее легко рассчитать.
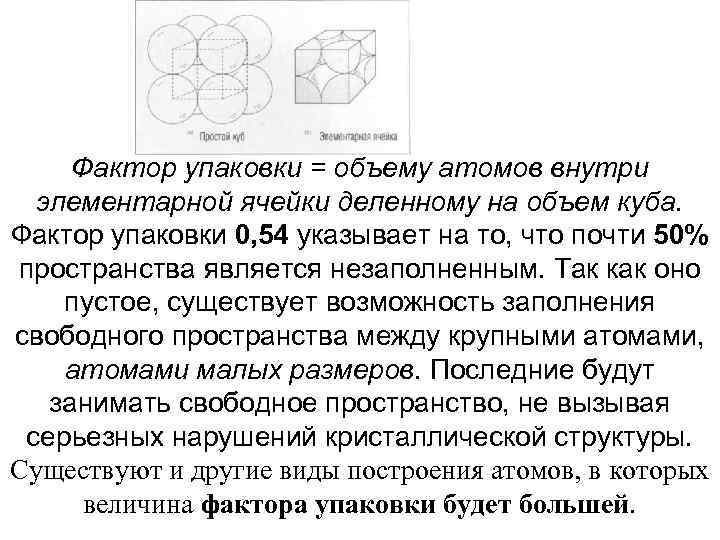 Фактор упаковки = объему атомов внутри элементарной ячейки деленному на объем куба. Фактор упаковки 0, 54 указывает на то, что почти 50% пространства является незаполненным. Так как оно пустое, существует возможность заполнения свободного пространства между крупными атомами, атомами малых размеров. Последние будут занимать свободное пространство, не вызывая серьезных нарушений кристаллической структуры. Существуют и другие виды построения атомов, в которых величина фактора упаковки будет большей.
Фактор упаковки = объему атомов внутри элементарной ячейки деленному на объем куба. Фактор упаковки 0, 54 указывает на то, что почти 50% пространства является незаполненным. Так как оно пустое, существует возможность заполнения свободного пространства между крупными атомами, атомами малых размеров. Последние будут занимать свободное пространство, не вызывая серьезных нарушений кристаллической структуры. Существуют и другие виды построения атомов, в которых величина фактора упаковки будет большей.
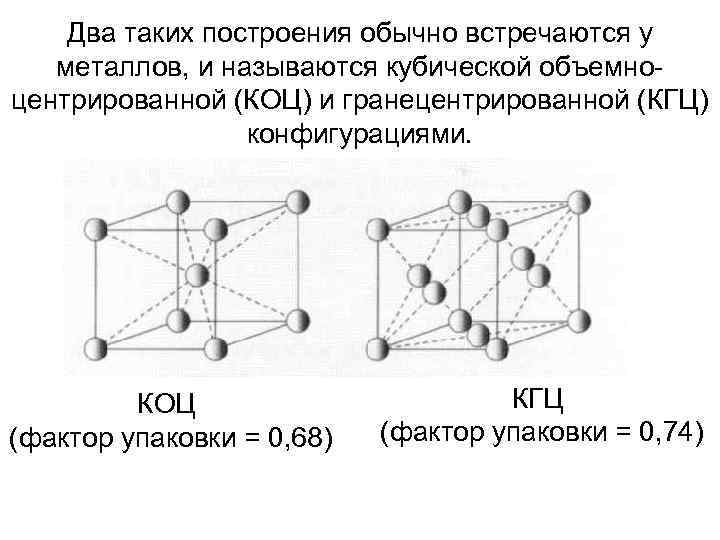 Два таких построения обычно встречаются у металлов, и называются кубической объемноцентрированной (КОЦ) и гранецентрированной (КГЦ) конфигурациями. КОЦ (фактор упаковки = 0, 68) КГЦ (фактор упаковки = 0, 74)
Два таких построения обычно встречаются у металлов, и называются кубической объемноцентрированной (КОЦ) и гранецентрированной (КГЦ) конфигурациями. КОЦ (фактор упаковки = 0, 68) КГЦ (фактор упаковки = 0, 74)
 Существуют три основных группы твердых веществ: • керамика, строение которой основано на ионной связи; керамика может существовать в кристаллической и аморфной формах, керамические материалы в аморфной форме называются стеклами; • металлы, строение которых основано на металлической связи • твердые тела, основанные на ковалентной и вторичной связях, включая важнейшие группы материалов, известных под названием полимеры. .
Существуют три основных группы твердых веществ: • керамика, строение которой основано на ионной связи; керамика может существовать в кристаллической и аморфной формах, керамические материалы в аморфной форме называются стеклами; • металлы, строение которых основано на металлической связи • твердые тела, основанные на ковалентной и вторичной связях, включая важнейшие группы материалов, известных под названием полимеры. .
 Существует еще одна важнейшая группа материалов. Это — композиты, представляющие собой комбинацию двух или большего числа твердых тел. Существует много примеров композитных материалов, как натурального, так и синтетического происхождения. Примерами композитов натурального происхождения являются костные ткани и дентин, состоящие из коллагена (полимера) и апатита (керамического вещества). Примерами композитов синтетической природы могут быть полимеры, армированные стеклянными волокнами, и полимеры, в состав которых входят частицы керамического наполнителя. Другим примером использования структуры композитов являются керметы, которые применяются в качестве наполнителя для изготовления некоторых стеклоиономерных цементов.
Существует еще одна важнейшая группа материалов. Это — композиты, представляющие собой комбинацию двух или большего числа твердых тел. Существует много примеров композитных материалов, как натурального, так и синтетического происхождения. Примерами композитов натурального происхождения являются костные ткани и дентин, состоящие из коллагена (полимера) и апатита (керамического вещества). Примерами композитов синтетической природы могут быть полимеры, армированные стеклянными волокнами, и полимеры, в состав которых входят частицы керамического наполнителя. Другим примером использования структуры композитов являются керметы, которые применяются в качестве наполнителя для изготовления некоторых стеклоиономерных цементов.
 Керамика представляет собой соединения металлических и неметаллических элементов, и состоит из таких веществ, как оксиды, нитриды и силикаты (оксид цинка широко используется в стоматологии). В керамических материалах отрицательно заряженные ионы (анионы) значительно отличаются размерами от положительно заряженных ионов (катионов). Ионы хлора занимают положения в узлах гранецентрированной решетки, в то время как ионы натрия (значительно меньше по размеру) находятся между ионами хлора, и их место нахождения можно назвать внутрипространственным расположением.
Керамика представляет собой соединения металлических и неметаллических элементов, и состоит из таких веществ, как оксиды, нитриды и силикаты (оксид цинка широко используется в стоматологии). В керамических материалах отрицательно заряженные ионы (анионы) значительно отличаются размерами от положительно заряженных ионов (катионов). Ионы хлора занимают положения в узлах гранецентрированной решетки, в то время как ионы натрия (значительно меньше по размеру) находятся между ионами хлора, и их место нахождения можно назвать внутрипространственным расположением.
 Оксид кремния (Si 02 ) является основой многих керамических материалов. Хотя его химическая формула достаточно проста, этот материал очень изменчив и может существовать в самых разных формах. Как кристаллический материал, он может быть в виде кварца, кристобалита и тридимита, но он может быть также в виде стекла, представляющего собой затвердевший расплав оксида кремния. Способность соединений, подобных оксиду кремния, существовать в разных модификациях, существенно отличающихся друг от друга своими свойствами, известна под названием полиморфизма. Оксид кремния используется в качестве основы для изготовления многих керамических материалов сложного состава алюмосиликатаые стекла, используемые для изготовления стеклоиономерных цементов (натриевый полевой шпат альбит, имеющий формулу Na. Al. Si 3 O 8 ).
Оксид кремния (Si 02 ) является основой многих керамических материалов. Хотя его химическая формула достаточно проста, этот материал очень изменчив и может существовать в самых разных формах. Как кристаллический материал, он может быть в виде кварца, кристобалита и тридимита, но он может быть также в виде стекла, представляющего собой затвердевший расплав оксида кремния. Способность соединений, подобных оксиду кремния, существовать в разных модификациях, существенно отличающихся друг от друга своими свойствами, известна под названием полиморфизма. Оксид кремния используется в качестве основы для изготовления многих керамических материалов сложного состава алюмосиликатаые стекла, используемые для изготовления стеклоиономерных цементов (натриевый полевой шпат альбит, имеющий формулу Na. Al. Si 3 O 8 ).
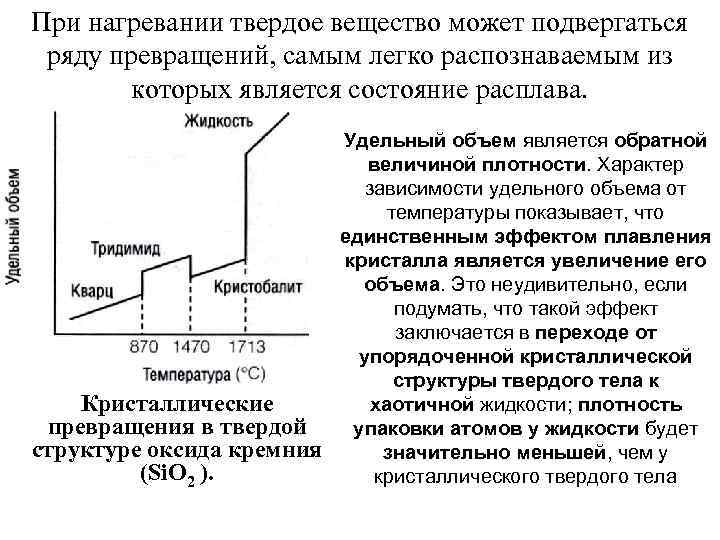 При нагревании твердое вещество может подвергаться ряду превращений, самым легко распознаваемым из которых является состояние расплава. Кристаллические превращения в твердой структуре оксида кремния (Si. О 2 ). Удельный объем является обратной величиной плотности. Характер зависимости удельного объема от температуры показывает, что единственным эффектом плавления кристалла является увеличение его объема. Это неудивительно, если подумать, что такой эффект заключается в переходе от упорядоченной кристаллической структуры твердого тела к хаотичной жидкости; плотность упаковки атомов у жидкости будет значительно меньшей, чем у кристаллического твердого тела
При нагревании твердое вещество может подвергаться ряду превращений, самым легко распознаваемым из которых является состояние расплава. Кристаллические превращения в твердой структуре оксида кремния (Si. О 2 ). Удельный объем является обратной величиной плотности. Характер зависимости удельного объема от температуры показывает, что единственным эффектом плавления кристалла является увеличение его объема. Это неудивительно, если подумать, что такой эффект заключается в переходе от упорядоченной кристаллической структуры твердого тела к хаотичной жидкости; плотность упаковки атомов у жидкости будет значительно меньшей, чем у кристаллического твердого тела
 При комнатной температуре оксид кремния, Si 02 существует в виде кварца; при повышении температуры до 870°С кварц превращается в тридимит. Дальнейшая трансформация кварца происходит уже при температуре 1471°С — тридимит превращается в кристобалит. И, наконец, при температуре 1713°С кристобалит начинает плавиться. Таким образом, по изменению удельного объема мы можем определить не только точку перехода кристаллического Si 02 из твердого состояния в жидкое, но и из твердого — в твердое.
При комнатной температуре оксид кремния, Si 02 существует в виде кварца; при повышении температуры до 870°С кварц превращается в тридимит. Дальнейшая трансформация кварца происходит уже при температуре 1471°С — тридимит превращается в кристобалит. И, наконец, при температуре 1713°С кристобалит начинает плавиться. Таким образом, по изменению удельного объема мы можем определить не только точку перехода кристаллического Si 02 из твердого состояния в жидкое, но и из твердого — в твердое.
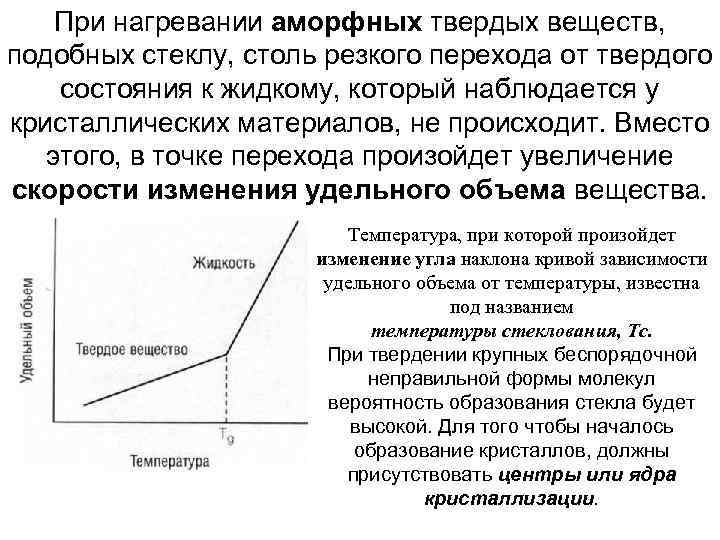 При нагревании аморфных твердых веществ, подобных стеклу, столь резкого перехода от твердого состояния к жидкому, который наблюдается у кристаллических материалов, не происходит. Вместо этого, в точке перехода произойдет увеличение скорости изменения удельного объема вещества. Температура, при которой произойдет изменение угла наклона кривой зависимости удельного объема от температуры, известна под названием температуры стеклования, Тс. При твердении крупных беспорядочной неправильной формы молекул вероятность образования стекла будет высокой. Для того чтобы началось образование кристаллов, должны присутствовать центры или ядра кристаллизации.
При нагревании аморфных твердых веществ, подобных стеклу, столь резкого перехода от твердого состояния к жидкому, который наблюдается у кристаллических материалов, не происходит. Вместо этого, в точке перехода произойдет увеличение скорости изменения удельного объема вещества. Температура, при которой произойдет изменение угла наклона кривой зависимости удельного объема от температуры, известна под названием температуры стеклования, Тс. При твердении крупных беспорядочной неправильной формы молекул вероятность образования стекла будет высокой. Для того чтобы началось образование кристаллов, должны присутствовать центры или ядра кристаллизации.
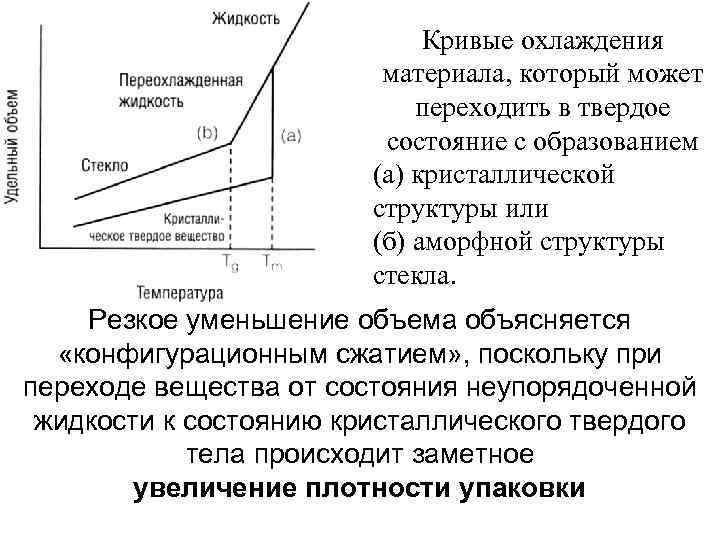 Кривые охлаждения материала, который может переходить в твердое состояние с образованием (а) кристаллической структуры или (б) аморфной структуры стекла. Резкое уменьшение объема объясняется «конфигурационным сжатием» , поскольку при переходе вещества от состояния неупорядоченной жидкости к состоянию кристаллического твердого тела происходит заметное увеличение плотности упаковки
Кривые охлаждения материала, который может переходить в твердое состояние с образованием (а) кристаллической структуры или (б) аморфной структуры стекла. Резкое уменьшение объема объясняется «конфигурационным сжатием» , поскольку при переходе вещества от состояния неупорядоченной жидкости к состоянию кристаллического твердого тела происходит заметное увеличение плотности упаковки
 Когда стекло начинает кристаллизоваться, такой процесс называется девитрификацией. Девитрификация может начаться, если стекло выдерживают при повышенной температуре в течение длительного времени, что приводит к перестройке расположения молекул. Стекло становится полупрозрачным в результате рассеяния света поверхностями небольших кристаллов. Этот процесс является основой изготовления стеклокерамических материалов. Процесс нагревания материала, позволяющий молекулам или атомам перераспределяться в пространстве, называется обжигом и играет важную роль в технологиях изготовления многих материалов.
Когда стекло начинает кристаллизоваться, такой процесс называется девитрификацией. Девитрификация может начаться, если стекло выдерживают при повышенной температуре в течение длительного времени, что приводит к перестройке расположения молекул. Стекло становится полупрозрачным в результате рассеяния света поверхностями небольших кристаллов. Этот процесс является основой изготовления стеклокерамических материалов. Процесс нагревания материала, позволяющий молекулам или атомам перераспределяться в пространстве, называется обжигом и играет важную роль в технологиях изготовления многих материалов.
 СТРУКТУРА МЕТАЛЛОВ И СПЛАВОВ Металлы обычно не образуют единого кристалла при твердении (переходе из состояния , называемого расплавом), вместо этого они образуют структуру, состоящую из множества мелких кристаллов. Это происходит потому, что внутри расплавленного металла рассеяно множество ядер или центров кристаллизации. Такие ядра могут образовываться при существенной потере тепловой энергии четырьмя атомами. Благодаря этому четыре атома способны образовать элементарную ячейку. Эти элементарные ячейки растут по мере того, как все большее количество атомов достигает низкого энергетического уровня и начинает присоединяться к ним, в результате чего и происходит образование кристалла. Этот процесс известен под названием гомогенной кристаллизации.
СТРУКТУРА МЕТАЛЛОВ И СПЛАВОВ Металлы обычно не образуют единого кристалла при твердении (переходе из состояния , называемого расплавом), вместо этого они образуют структуру, состоящую из множества мелких кристаллов. Это происходит потому, что внутри расплавленного металла рассеяно множество ядер или центров кристаллизации. Такие ядра могут образовываться при существенной потере тепловой энергии четырьмя атомами. Благодаря этому четыре атома способны образовать элементарную ячейку. Эти элементарные ячейки растут по мере того, как все большее количество атомов достигает низкого энергетического уровня и начинает присоединяться к ним, в результате чего и происходит образование кристалла. Этот процесс известен под названием гомогенной кристаллизации.
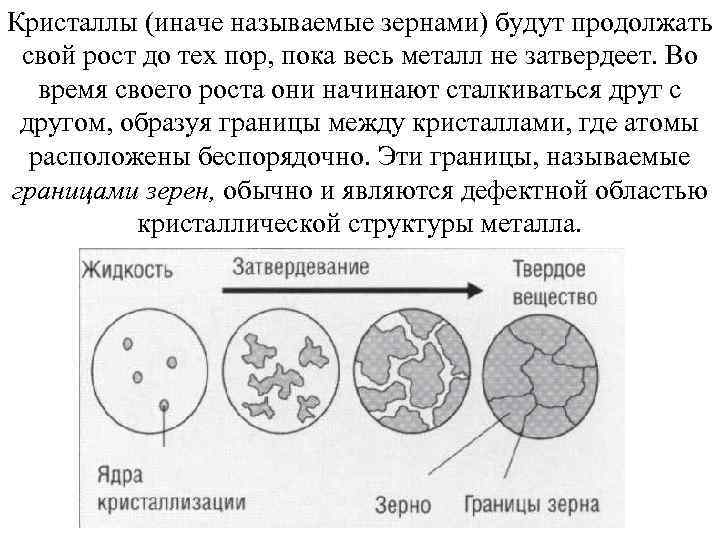 Кристаллы (иначе называемые зернами) будут продолжать свой рост до тех пор, пока весь металл не затвердеет. Во время своего роста они начинают сталкиваться друг с другом, образуя границы между кристаллами, где атомы расположены беспорядочно. Эти границы, называемые границами зерен, обычно и являются дефектной областью кристаллической структуры металла.
Кристаллы (иначе называемые зернами) будут продолжать свой рост до тех пор, пока весь металл не затвердеет. Во время своего роста они начинают сталкиваться друг с другом, образуя границы между кристаллами, где атомы расположены беспорядочно. Эти границы, называемые границами зерен, обычно и являются дефектной областью кристаллической структуры металла.
 Альтернативным способом получения мелкозернистых структур является обеспечение множества центров кристаллизации. Это можно получить добавкой иридия к стоматологическим литейным сплавам на основе золота. Иридий создает множество центров кристаллизации и, тем самым, позволяет ограничить рост зерен. Детальное изучение структуры металлов, а именно, размеров кристаллов, их формы и состава, исключительно важно для выяснения их свойств и технологии получения.
Альтернативным способом получения мелкозернистых структур является обеспечение множества центров кристаллизации. Это можно получить добавкой иридия к стоматологическим литейным сплавам на основе золота. Иридий создает множество центров кристаллизации и, тем самым, позволяет ограничить рост зерен. Детальное изучение структуры металлов, а именно, размеров кристаллов, их формы и состава, исключительно важно для выяснения их свойств и технологии получения.
 Равноосная структура Металл, форма которого была изменена путем деформации, называется кованым. Радиальная структура Большинство широко используемых металлов представляют собой смесь двух или более металлических элементов, иногда с добавкой неметаллических компонентов при температурах, превышающих их температуру плавления. Такие смеси двух или более металлов называют сплавами
Равноосная структура Металл, форма которого была изменена путем деформации, называется кованым. Радиальная структура Большинство широко используемых металлов представляют собой смесь двух или более металлических элементов, иногда с добавкой неметаллических компонентов при температурах, превышающих их температуру плавления. Такие смеси двух или более металлов называют сплавами
 Чаще всего сплав состоит из нескольких отдельных, четко определенных, твердых фаз. Фазой называют структурно однородную (гомогенную) часть системы, которая отделена от других частей системы четко определенными физическими границами. Каждая фаза будет иметь свою собственную, отчетливо выраженную структуру, и связанные с ней свойства. Фазы в металле могут представлять собой смеси металлов. В состав меди может входить до 40% цинка без разрушения ее кубической гранецентрированной (КГЦ) решетки. Такие структуры называют твердыми растворами, и эти структуры соответствуют ряду специальных условий.
Чаще всего сплав состоит из нескольких отдельных, четко определенных, твердых фаз. Фазой называют структурно однородную (гомогенную) часть системы, которая отделена от других частей системы четко определенными физическими границами. Каждая фаза будет иметь свою собственную, отчетливо выраженную структуру, и связанные с ней свойства. Фазы в металле могут представлять собой смеси металлов. В состав меди может входить до 40% цинка без разрушения ее кубической гранецентрированной (КГЦ) решетки. Такие структуры называют твердыми растворами, и эти структуры соответствуют ряду специальных условий.
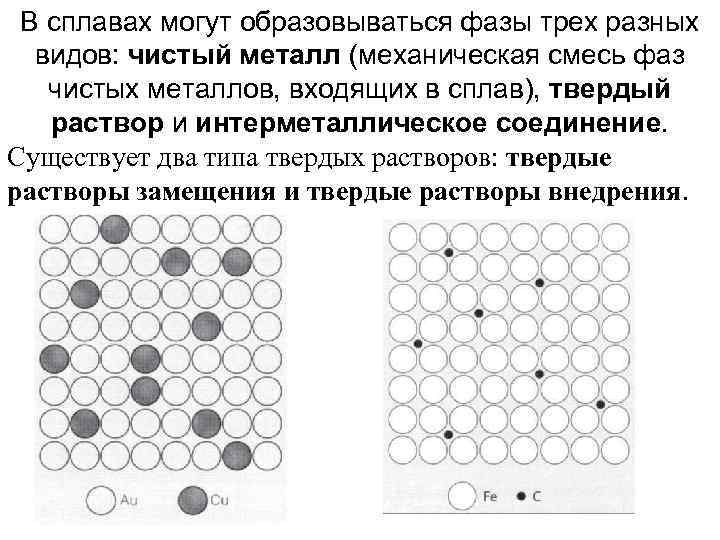 В сплавах могут образовываться фазы трех разных видов: чистый металл (механическая смесь фаз чистых металлов, входящих в сплав), твердый раствор и интерметаллическое соединение. Существует два типа твердых растворов: твердые растворы замещения и твердые растворы внедрения.
В сплавах могут образовываться фазы трех разных видов: чистый металл (механическая смесь фаз чистых металлов, входящих в сплав), твердый раствор и интерметаллическое соединение. Существует два типа твердых растворов: твердые растворы замещения и твердые растворы внедрения.
 Твердые растворы замещения возможны если: • атомы имеют одинаковую валентность; • атомы образуют одинаковую кристаллическую структуру (например, КГЦ решетку); • размеры атомов отличаются друг от друга не более чем на 15%. (от 100% золота до 100% меди) Твердые растворы внедрения: Атомы растворимого элемента должны быть намного меньше атомов растворителя. Практически диаметр атома растворимого элемента должен составлять менее 60% диаметра атома растворителя.
Твердые растворы замещения возможны если: • атомы имеют одинаковую валентность; • атомы образуют одинаковую кристаллическую структуру (например, КГЦ решетку); • размеры атомов отличаются друг от друга не более чем на 15%. (от 100% золота до 100% меди) Твердые растворы внедрения: Атомы растворимого элемента должны быть намного меньше атомов растворителя. Практически диаметр атома растворимого элемента должен составлять менее 60% диаметра атома растворителя.
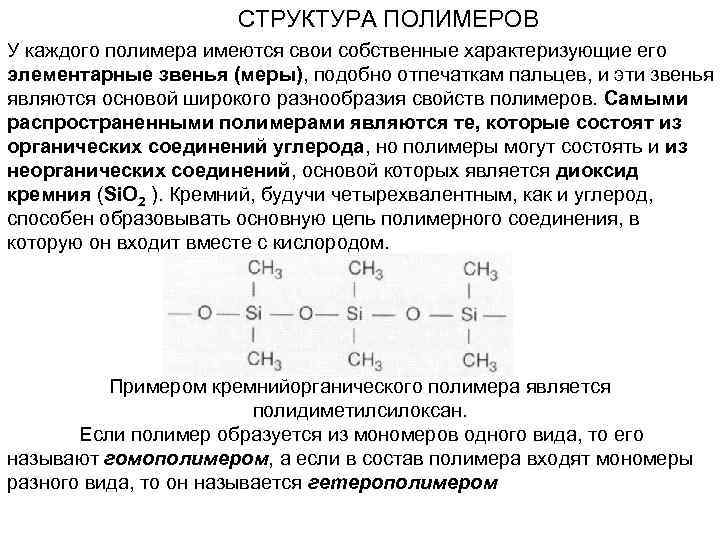 СТРУКТУРА ПОЛИМЕРОВ У каждого полимера имеются свои собственные характеризующие его элементарные звенья (меры), подобно отпечаткам пальцев, и эти звенья являются основой широкого разнообразия свойств полимеров. Самыми распространенными полимерами являются те, которые состоят из органических соединений углерода, но полимеры могут состоять и из неорганических соединений, основой которых является диоксид кремния (Si. О 2 ). Кремний, будучи четырехвалентным, как и углерод, способен образовывать основную цепь полимерного соединения, в которую он входит вместе с кислородом. Примером кремнийорганического полимера является полидиметилсилоксан. Если полимер образуется из мономеров одного вида, то его называют гомополимером, а если в состав полимера входят мономеры разного вида, то он называется гетерополимером
СТРУКТУРА ПОЛИМЕРОВ У каждого полимера имеются свои собственные характеризующие его элементарные звенья (меры), подобно отпечаткам пальцев, и эти звенья являются основой широкого разнообразия свойств полимеров. Самыми распространенными полимерами являются те, которые состоят из органических соединений углерода, но полимеры могут состоять и из неорганических соединений, основой которых является диоксид кремния (Si. О 2 ). Кремний, будучи четырехвалентным, как и углерод, способен образовывать основную цепь полимерного соединения, в которую он входит вместе с кислородом. Примером кремнийорганического полимера является полидиметилсилоксан. Если полимер образуется из мономеров одного вида, то его называют гомополимером, а если в состав полимера входят мономеры разного вида, то он называется гетерополимером
 МЕХАНИЗМЫ ПОЛИМЕРИЗАЦИИ
МЕХАНИЗМЫ ПОЛИМЕРИЗАЦИИ
 Общим для всех мономеров, представленных в Таблице, является наличие двойной связи, которая раскрывается, позволяя мономеру соединиться с соседним мономером. Существует два возможных пути полимеризации: аддитивный и конденсационный. Аддитивная полимеризация: • активация; • инициирование; • рост цепи; • обрыв цепи. Конденсационная полимеризация Происходит в тех случаях, когда в результате реакции между двумя молекулами (обычно разнородными) образуется большая молекула с выделением побочного низкомолекулярного продукта (чаще молекулы воды).
Общим для всех мономеров, представленных в Таблице, является наличие двойной связи, которая раскрывается, позволяя мономеру соединиться с соседним мономером. Существует два возможных пути полимеризации: аддитивный и конденсационный. Аддитивная полимеризация: • активация; • инициирование; • рост цепи; • обрыв цепи. Конденсационная полимеризация Происходит в тех случаях, когда в результате реакции между двумя молекулами (обычно разнородными) образуется большая молекула с выделением побочного низкомолекулярного продукта (чаще молекулы воды).
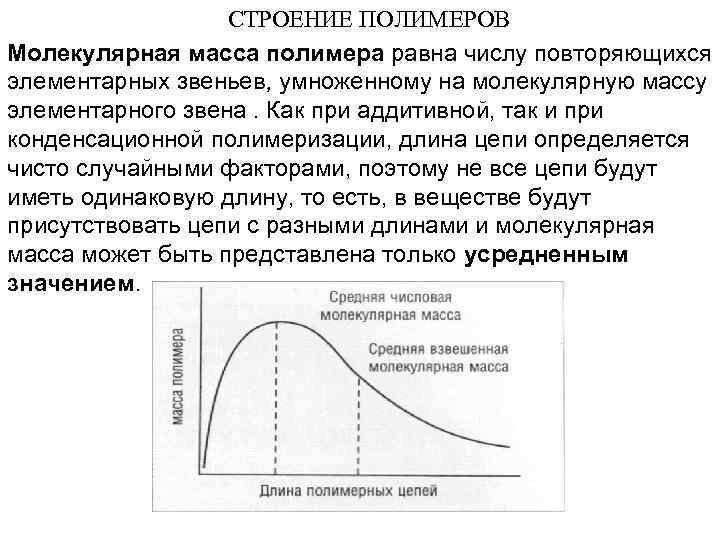 СТРОЕНИЕ ПОЛИМЕРОВ Молекулярная масса полимера равна числу повторяющихся элементарных звеньев, умноженному на молекулярную массу элементарного звена. Как при аддитивной, так и при конденсационной полимеризации, длина цепи определяется чисто случайными факторами, поэтому не все цепи будут иметь одинаковую длину, то есть, в веществе будут присутствовать цепи с разными длинами и молекулярная масса может быть представлена только усредненным значением.
СТРОЕНИЕ ПОЛИМЕРОВ Молекулярная масса полимера равна числу повторяющихся элементарных звеньев, умноженному на молекулярную массу элементарного звена. Как при аддитивной, так и при конденсационной полимеризации, длина цепи определяется чисто случайными факторами, поэтому не все цепи будут иметь одинаковую длину, то есть, в веществе будут присутствовать цепи с разными длинами и молекулярная масса может быть представлена только усредненным значением.
 Молекулярная масса полимера представляет особую важность для объяснения различий между физическими свойствами разных полимеров. Например, прочность при растяжении и удлинение , требуемые для разрыва полимерного материала, резко возрастают для некоторых полимеров, молекулярная масса которых находится в пределах от 50 000 до 200 000. Однако, улучшение физических свойств материала за счет увеличения молекулярной массы сопровождается быстрым увеличением вязкости расплава, что ведет к повышению температуры стеклования, и затрудняет технологическую переработку полимеров.
Молекулярная масса полимера представляет особую важность для объяснения различий между физическими свойствами разных полимеров. Например, прочность при растяжении и удлинение , требуемые для разрыва полимерного материала, резко возрастают для некоторых полимеров, молекулярная масса которых находится в пределах от 50 000 до 200 000. Однако, улучшение физических свойств материала за счет увеличения молекулярной массы сопровождается быстрым увеличением вязкости расплава, что ведет к повышению температуры стеклования, и затрудняет технологическую переработку полимеров.
 Конфигурации цепи Полимерные цепи удерживаются за счет вторичных связей (сил Ван дер Ваальса), а при достаточной длине цепей — за счет переплетения. Чем выше молекулярная масса полимера, тем сильнее будут переплетены между собой полимерные цепи, тем выше будут жесткость и прочность полимерного материала. У таких полимерных материалов, как полиэтилен, обладающих линейной конфигурацией цепи, слабая связь между цепями может быть легко разорвана при нагревании полимера. Как только начинают нагревать материал, цепи будут скользить относительно друга, полимер начнет размягчаться и легко деформироваться. При охлаждении связи восстанавливаются, и полимер снова становится твердым, сохраня ту форму, которую приобрел при повышенной температуре. Температура, при которой происходит пластическое размягчение материала и передвижение молекул, называется температурой стеклования
Конфигурации цепи Полимерные цепи удерживаются за счет вторичных связей (сил Ван дер Ваальса), а при достаточной длине цепей — за счет переплетения. Чем выше молекулярная масса полимера, тем сильнее будут переплетены между собой полимерные цепи, тем выше будут жесткость и прочность полимерного материала. У таких полимерных материалов, как полиэтилен, обладающих линейной конфигурацией цепи, слабая связь между цепями может быть легко разорвана при нагревании полимера. Как только начинают нагревать материал, цепи будут скользить относительно друга, полимер начнет размягчаться и легко деформироваться. При охлаждении связи восстанавливаются, и полимер снова становится твердым, сохраня ту форму, которую приобрел при повышенной температуре. Температура, при которой происходит пластическое размягчение материала и передвижение молекул, называется температурой стеклования
 Полимеры, которые могут размягчаться и которым при нагревании выше температуры стеклования можно придать нужную форму, называются термопластичными полимерами. Примерами термопластичных полимеров являются полистирол, полиметилметакрилат и полиэтилен. Полимеры, которые разрушаются при нагревании, не достигая состояния стеклования, называются термореактивными полимерами. Кристалличность полимеров В полимерном материале макромолекулы обычно имеют различные пространственные конфигурации, они могут быть скручены спиралями и переплетены беспорядочным образом. Иногда, однако, существуют зоны, где молекулы способны располагаться более пли менее параллельно друг к другу.
Полимеры, которые могут размягчаться и которым при нагревании выше температуры стеклования можно придать нужную форму, называются термопластичными полимерами. Примерами термопластичных полимеров являются полистирол, полиметилметакрилат и полиэтилен. Полимеры, которые разрушаются при нагревании, не достигая состояния стеклования, называются термореактивными полимерами. Кристалличность полимеров В полимерном материале макромолекулы обычно имеют различные пространственные конфигурации, они могут быть скручены спиралями и переплетены беспорядочным образом. Иногда, однако, существуют зоны, где молекулы способны располагаться более пли менее параллельно друг к другу.
 В таких случаях полимер имеет кристаллические участки и проявляет в некоторой степени свойства кристалличности. Относительное соотношение кристаллических и некристаллических областей в полимере зависит от его химического состава, конфигурации молекул и технологии изготовления материала. Когда цепи полимера соединены с помощью химических связей, его называют сшитым. Сшивание оказывает выраженное воздействие на свойства полимерного материала: оно позволяет сделать из термопластичного полимера термореактивный. Еще более важным является то, что сшивание позволяет превратить жидкий полимер в твердый: этот процесс используют для отверждения многих оттискных материалов.
В таких случаях полимер имеет кристаллические участки и проявляет в некоторой степени свойства кристалличности. Относительное соотношение кристаллических и некристаллических областей в полимере зависит от его химического состава, конфигурации молекул и технологии изготовления материала. Когда цепи полимера соединены с помощью химических связей, его называют сшитым. Сшивание оказывает выраженное воздействие на свойства полимерного материала: оно позволяет сделать из термопластичного полимера термореактивный. Еще более важным является то, что сшивание позволяет превратить жидкий полимер в твердый: этот процесс используют для отверждения многих оттискных материалов.
 Образование частых сшивающих молекулы связей в полимеpax ведет к образованию твердых и хрупких материалов. Если полимер состоит из особенно длинных и гибких молекулярных цепей , эти молекулы могут быть сшитыми в нескольких точках своей длины, могут иметь конфигурацию в виде сильно скрученных спиралей, когда они находятся в свободном состоянии, и могут растягиваться на большую длину (за счет распрямления спирали) под действием нагрузки. Когда нагрузку снимают, цепи снова принимают свою спиральную конфигурацию под воздействием сшивающих поперечных связей. Называются эластомерами и обладают отличительными особенностями : • Этот материал мягкий и имеет низкий модуль упругости (эластичности). • Проявляет очень высокие деформации при растяжении (> 100%). • Эти деформации обратимы. • Материал используют в области температур, превышающих температуру его стеклования.
Образование частых сшивающих молекулы связей в полимеpax ведет к образованию твердых и хрупких материалов. Если полимер состоит из особенно длинных и гибких молекулярных цепей , эти молекулы могут быть сшитыми в нескольких точках своей длины, могут иметь конфигурацию в виде сильно скрученных спиралей, когда они находятся в свободном состоянии, и могут растягиваться на большую длину (за счет распрямления спирали) под действием нагрузки. Когда нагрузку снимают, цепи снова принимают свою спиральную конфигурацию под воздействием сшивающих поперечных связей. Называются эластомерами и обладают отличительными особенностями : • Этот материал мягкий и имеет низкий модуль упругости (эластичности). • Проявляет очень высокие деформации при растяжении (> 100%). • Эти деформации обратимы. • Материал используют в области температур, превышающих температуру его стеклования.
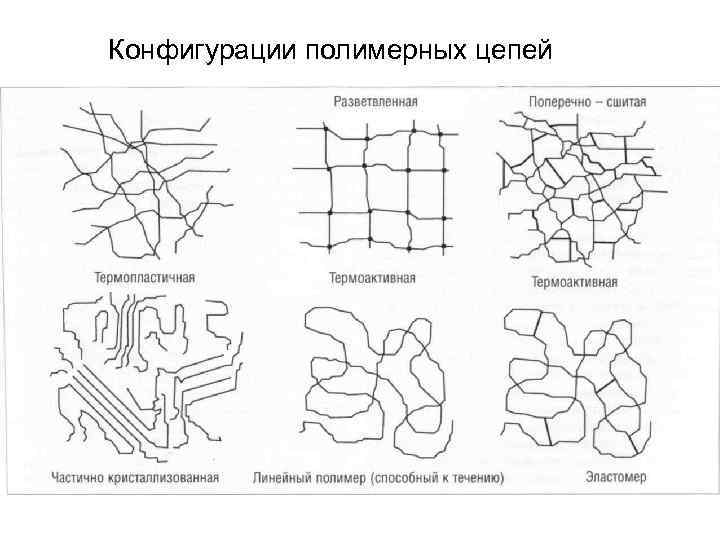 Конфигурации полимерных цепей
Конфигурации полимерных цепей
 КОМПОЗИЦИИ ПОЛИМЕРОВ Полимеры редко используются в чистом виде. Об одной из таких модификаций уже упоминалось, когда рассматривалось сшивание полимерных цепей для получения термореактивных полимеров из термопластичных. Поскольку термореактивные полимеры не могут размягчаться и принимать нужную форму, она должна быть придана материалу до проведения сшивания, и это налагает серьезные ограничения на технологию изготовления изделия. Существуют технологические методы изготовления полимерных изделий, такие , как смешивание, сополимеризация и получение композитов
КОМПОЗИЦИИ ПОЛИМЕРОВ Полимеры редко используются в чистом виде. Об одной из таких модификаций уже упоминалось, когда рассматривалось сшивание полимерных цепей для получения термореактивных полимеров из термопластичных. Поскольку термореактивные полимеры не могут размягчаться и принимать нужную форму, она должна быть придана материалу до проведения сшивания, и это налагает серьезные ограничения на технологию изготовления изделия. Существуют технологические методы изготовления полимерных изделий, такие , как смешивание, сополимеризация и получение композитов
 Смешивание — это процесс, наиболее часто используемый для изготовления термопластичных полимеров. Свойства смешанного полимера обычно находятся где-то посередине между свойствами составляющих его компонентов. Их химические составы должны быть схожими. Это налагает ряд ограничений на изменение их свойств. Альтернативой смешиванию является процесс, называемый сополимеризацией.
Смешивание — это процесс, наиболее часто используемый для изготовления термопластичных полимеров. Свойства смешанного полимера обычно находятся где-то посередине между свойствами составляющих его компонентов. Их химические составы должны быть схожими. Это налагает ряд ограничений на изменение их свойств. Альтернативой смешиванию является процесс, называемый сополимеризацией.
 Сополимеризация — соединение двух полимеров в процессе их совместной полимеризации. Например , если мономер А и мономер В смешать перед полимеризацией, то они будут сополимеризоваться с образованием полимерных цепей, состоящих как из элементарных звеньев А, так и из звеньев В. Последовательность соединения исходных мономеров, образующих полимер, может быть произвольной, и в этом случае будет образовываться неупорядоченный (атактический) сополимер, молекулярная цепь которого приведена ниже: _А_А_В_В_А_В_В_В_А_А_В_В_А_В_ Если мономеры более склонны к самополимеризации, чем к совместной полимеризации, это приведет к образованию блок+ сополимер, в макромолекулах которого соединены блоки каждого гомополимера: _А_А_А_В_В_А_А_А_В_В_В_ В таких системах можно получать полимеры со свойствами, существенно отличающимися от свойств гомополимеров в отдельности.
Сополимеризация — соединение двух полимеров в процессе их совместной полимеризации. Например , если мономер А и мономер В смешать перед полимеризацией, то они будут сополимеризоваться с образованием полимерных цепей, состоящих как из элементарных звеньев А, так и из звеньев В. Последовательность соединения исходных мономеров, образующих полимер, может быть произвольной, и в этом случае будет образовываться неупорядоченный (атактический) сополимер, молекулярная цепь которого приведена ниже: _А_А_В_В_А_В_В_В_А_А_В_В_А_В_ Если мономеры более склонны к самополимеризации, чем к совместной полимеризации, это приведет к образованию блок+ сополимер, в макромолекулах которого соединены блоки каждого гомополимера: _А_А_А_В_В_А_А_А_В_В_В_ В таких системах можно получать полимеры со свойствами, существенно отличающимися от свойств гомополимеров в отдельности.
 Например, один исходный полимер может быть совершенно жестким, а другой — очень гибким. Получение блок_сополимера позволит регулировать степень жесткости конечного материала за счет регулирования длины блоков и относительного количества каждого полимера в композиции. Пластификаторы Если вещество с низким молекулярным весом добавить в полимер, то это приведет к снижению температуры стеклования и модуля упругости материала. Эти вещества, называемые пластификаторами, уменьшают силы притяжения между цепями полимеров, благодаря чему цепи становятся более гибкими, и могут скользить относительно друга при температурах более низких, чем температура их стеклования. Основным требованием, которому должен отвечать пластификатор, является его совместимость с полимером, и постоянство действия.
Например, один исходный полимер может быть совершенно жестким, а другой — очень гибким. Получение блок_сополимера позволит регулировать степень жесткости конечного материала за счет регулирования длины блоков и относительного количества каждого полимера в композиции. Пластификаторы Если вещество с низким молекулярным весом добавить в полимер, то это приведет к снижению температуры стеклования и модуля упругости материала. Эти вещества, называемые пластификаторами, уменьшают силы притяжения между цепями полимеров, благодаря чему цепи становятся более гибкими, и могут скользить относительно друга при температурах более низких, чем температура их стеклования. Основным требованием, которому должен отвечать пластификатор, является его совместимость с полимером, и постоянство действия.
 Композитом называется комбинация материалов, в которой каждый компонент сохраняет свои индивидуальные физические свойства. Или, что более важно, композит — это материал, состоящий из нескольких фаз, имеющий улучшенные свойства по сравнению со свойствами каждой из фаз в отдельности. В композитах, состоящих из двух компонентов, выделяют две фазы — матрицу и наполнитель, при этом, матрица является тем компонентом, который связывает между собой частицы наполнителя.
Композитом называется комбинация материалов, в которой каждый компонент сохраняет свои индивидуальные физические свойства. Или, что более важно, композит — это материал, состоящий из нескольких фаз, имеющий улучшенные свойства по сравнению со свойствами каждой из фаз в отдельности. В композитах, состоящих из двух компонентов, выделяют две фазы — матрицу и наполнитель, при этом, матрица является тем компонентом, который связывает между собой частицы наполнителя.
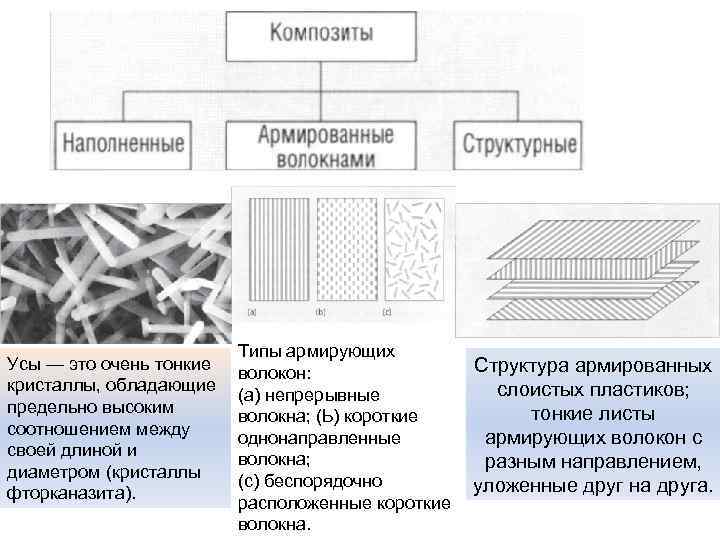 Усы — это очень тонкие кристаллы, обладающие предельно высоким соотношением между своей длиной и диаметром (кристаллы фторканазита). Типы армирующих волокон: (а) непрерывные волокна; (Ь) короткие однонаправленные волокна; (с) беспорядочно расположенные короткие волокна. Структура армированных слоистых пластиков; тонкие листы армирующих волокон с разным направлением, уложенные друг на друга.
Усы — это очень тонкие кристаллы, обладающие предельно высоким соотношением между своей длиной и диаметром (кристаллы фторканазита). Типы армирующих волокон: (а) непрерывные волокна; (Ь) короткие однонаправленные волокна; (с) беспорядочно расположенные короткие волокна. Структура армированных слоистых пластиков; тонкие листы армирующих волокон с разным направлением, уложенные друг на друга.


