0cebcda3a6ffcc5d1c9b97499c12c6a8.ppt
- Количество слайдов: 23

Результаты адьювантной аутоиммунотерапии препаратом Онкофаг® (HSPPC-96) у больных почечно-клеточным раком (III фаза) Горелов А. И. Санкт-Петербургский Государственный Университет Медицинский факультет Москва - 4 октября 2007 1

Введение Предпосылки для создания Онкофага® (HSPPC-96) Метод выбора при лечении локализованных форм почечно-клеточного рака - нефрэктомия У 20 -30% больных после нефрэктомии развивается рецидив заболевания Среднее время до развития рецидива – 15 -18 месяцев Через 5 лет рецидив болезни регистрируют у 40% больных Современные методы лечения рецидивов почечноклеточного рака практически неэффективны Москва, 4 октября 2007 г. 2

Онкофаг® (HSPPC-96) - новый препарат для адъювантной терапии почечно-клеточно рака Основой препарата является комплекс белков теплового шока и опухоль-специфических пептидов (HSPPC) Белки теплового шока (БТШ) - это наиболее часто встречающиеся протеины всех типов клеток, включая опухолевые Полученный из опухоли комплекс БТШ и пептидов вызывает усиление опухоль-специфического иммунного ответа при введении пациенту Москва, 4 октября 2007 г. 3
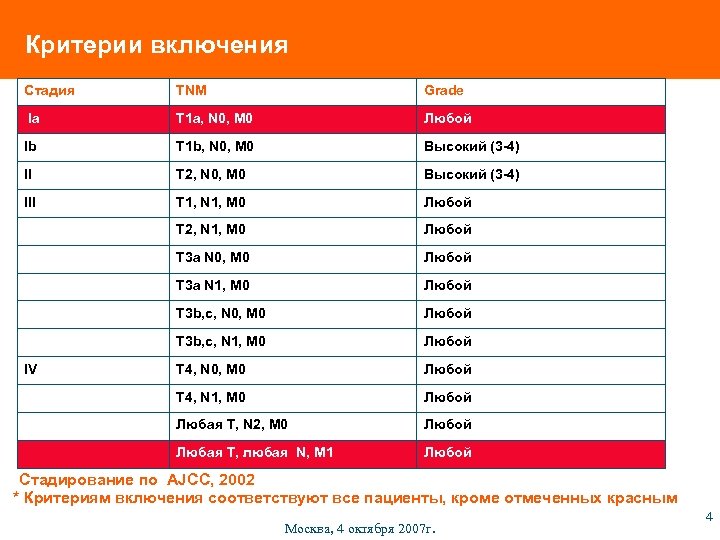
Критерии включения Стадия TNM Grade Ia T 1 a, N 0, M 0 Любой Ib T 1 b, N 0, M 0 Высокий (3 -4) II T 2, N 0, M 0 Высокий (3 -4) III T 1, N 1, M 0 Любой T 2, N 1, M 0 Любой T 3 a N 0, M 0 Любой T 3 a N 1, M 0 Любой T 3 b, c, N 0, M 0 Любой T 3 b, c, N 1, M 0 Любой T 4, N 0, M 0 Любой T 4, N 1, M 0 Любой Любая T, N 2, M 0 Любой Любая T, любая N, M 1 Любой IV Стадирование по AJCC, 2002 * Критериям включения соответствуют все пациенты, кроме отмеченных красным Москва, 4 октября 2007 г. 4

Критерии включения (продолжение) Возраст > 18 лет Статус по шкале Zubrod/ECOG/WHO <1 Для женщин детородного возраста – отрицательный тест на беременность Подписанное информированное согласие Москва, 4 октября 2007 г. 5
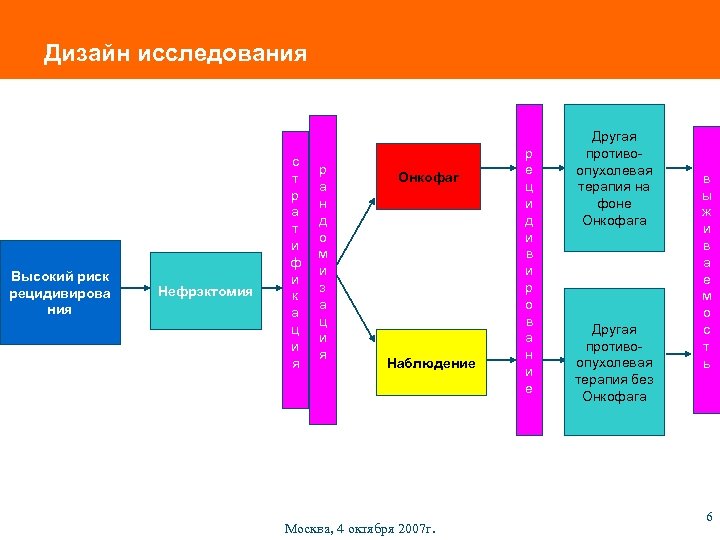
Дизайн исследования Высокий риск рецидивирова ния Нефрэктомия с т р а т и ф и к а ц и я р а н д о м и з а ц и я Онкофаг Наблюдение Москва, 4 октября 2007 г. р е ц и д и в и р о в а н и е Другая противоопухолевая терапия на фоне Онкофага Другая противоопухолевая терапия без Онкофага в ы ж и в а е м о с т ь 6

Задачи исследования Оценка безрецидивной выживаемости Оценка общей выживаемости Получение данных о безопасности лечения Онкофагом Москва, 4 октября 2007 г. 7
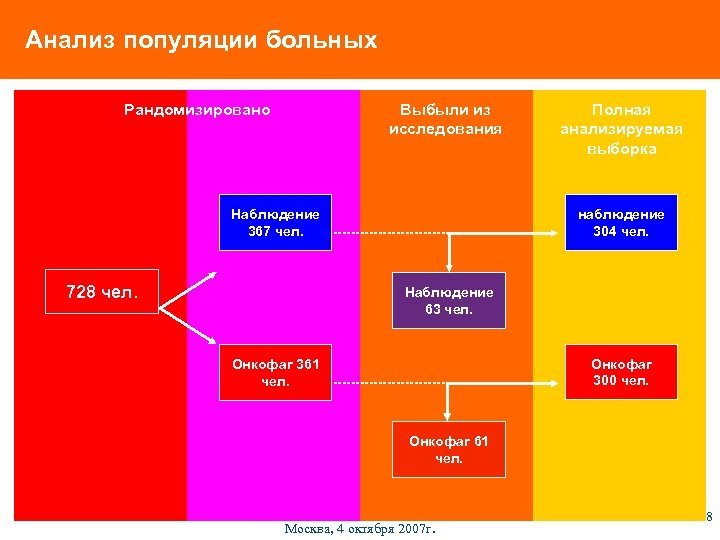
Анализ популяции больных Рандомизировано Выбыли из исследования Наблюдение 367 чел. 728 чел. Полная анализируемая выборка наблюдение 304 чел. Наблюдение 63 чел. Онкофаг 300 чел. Онкофаг 361 чел. Онкофаг 61 чел. Москва, 4 октября 2007 г. 8
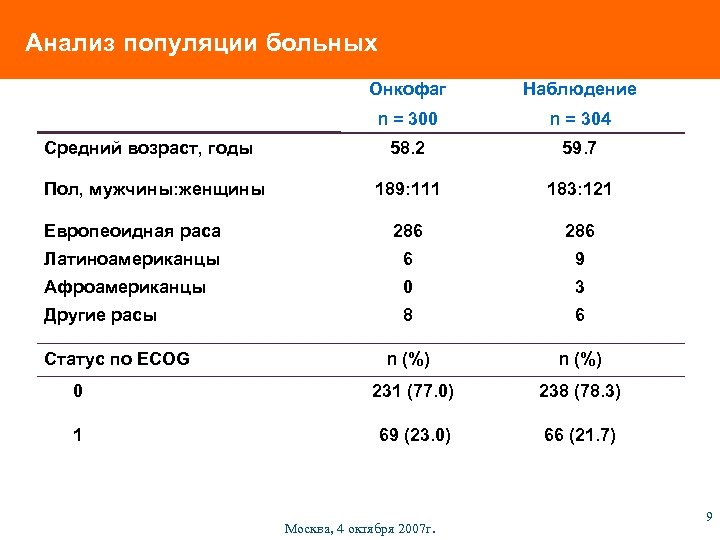
Анализ популяции больных Онкофаг Наблюдение n = 300 n = 304 58. 2 59. 7 189: 111 183: 121 Европеоидная раса 286 Латиноамериканцы 6 9 Афроамериканцы 0 3 Другие расы 8 6 n (%) 0 231 (77. 0) 238 (78. 3) 1 69 (23. 0) 66 (21. 7) Средний возраст, годы Пол, мужчины: женщины Статус по ECOG Москва, 4 октября 2007 г. 9
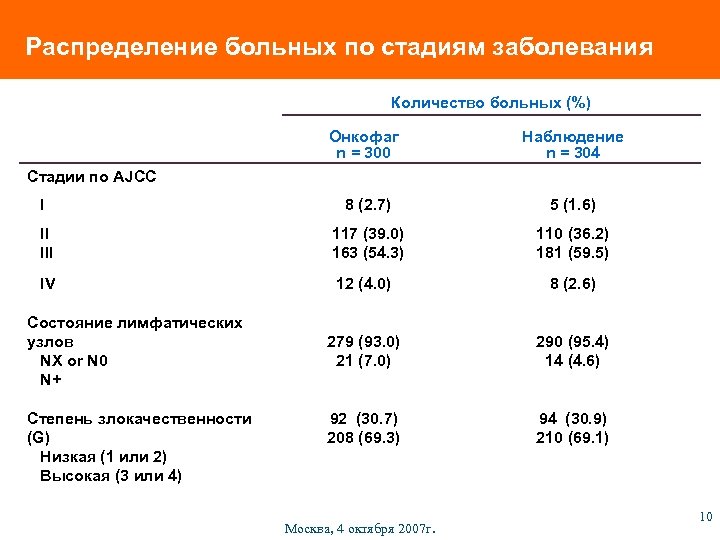
Распределение больных по стадиям заболевания Количество больных (%) Онкофаг n = 300 Наблюдение n = 304 I 8 (2. 7) 5 (1. 6) II III 117 (39. 0) 163 (54. 3) 110 (36. 2) 181 (59. 5) IV 12 (4. 0) 8 (2. 6) 279 (93. 0) 21 (7. 0) 290 (95. 4) 14 (4. 6) 92 (30. 7) 208 (69. 3) 94 (30. 9) 210 (69. 1) Стадии по AJCC Состояние лимфатических узлов NX or N 0 N+ Степень злокачественности (G) Низкая (1 или 2) Высокая (3 или 4) Москва, 4 октября 2007 г. 10
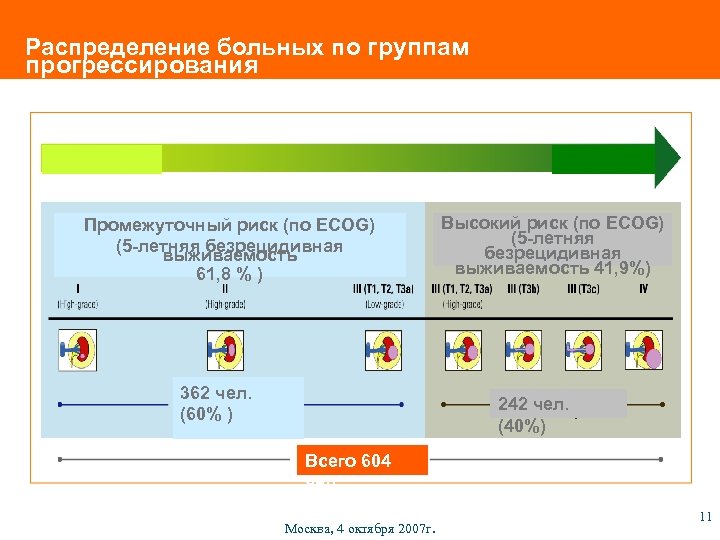
Распределение больных по группам прогрессирования Промежуточный риск (по ECOG) (5 -летняя безрецидивная выживаемость 61, 8 % ) 362 чел. (60% ) Высокий риск (по ECOG) (5 -летняя безрецидивная выживаемость 41, 9%) 242 чел. (40%) Всего 604 чел. Москва, 4 октября 2007 г. 11
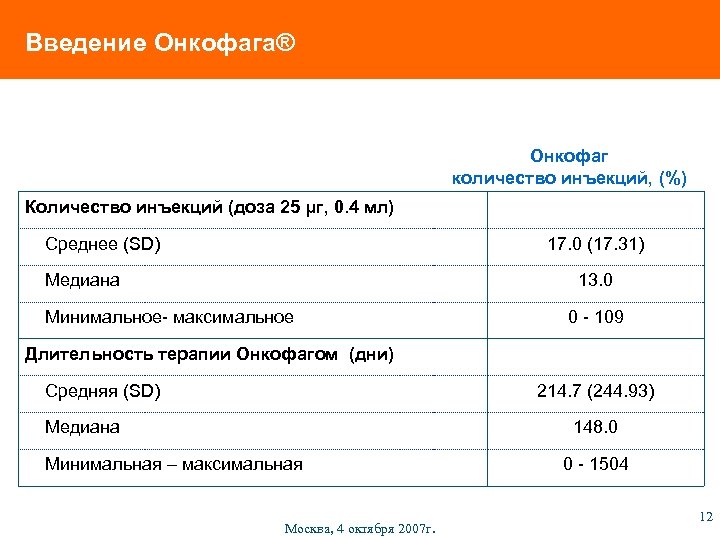
Введение Онкофага® Онкофаг количество инъекций, (%) Количество инъекций (доза 25 µг, 0. 4 мл) Среднее (SD) 17. 0 (17. 31) Медиана 13. 0 Минимальное- максимальное 0 - 109 Длительность терапии Онкофагом (дни) Средняя (SD) 214. 7 (244. 93) Медиана 148. 0 Минимальная – максимальная Москва, 4 октября 2007 г. 0 - 1504 12
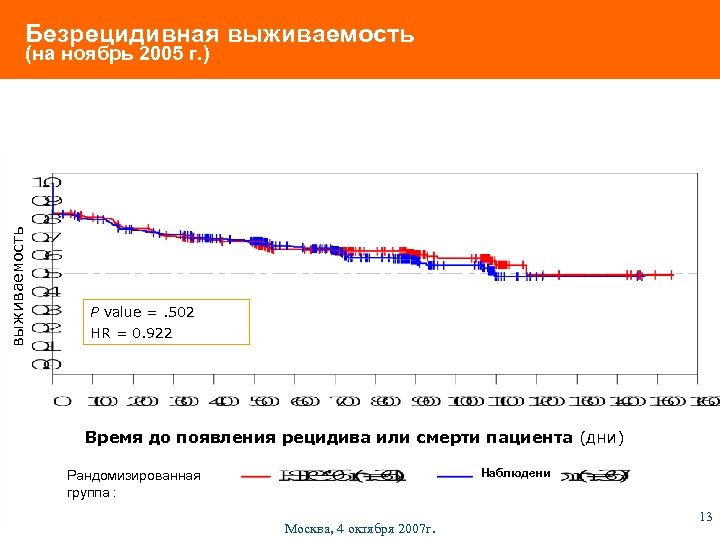
Безрецидивная выживаемость (на ноябрь 2005 г. ) P value =. 502 HR = 0. 922 Время до появления рецидива или смерти пациента (дни) Наблюдени е Рандомизированная группа : Москва, 4 октября 2007 г. 13
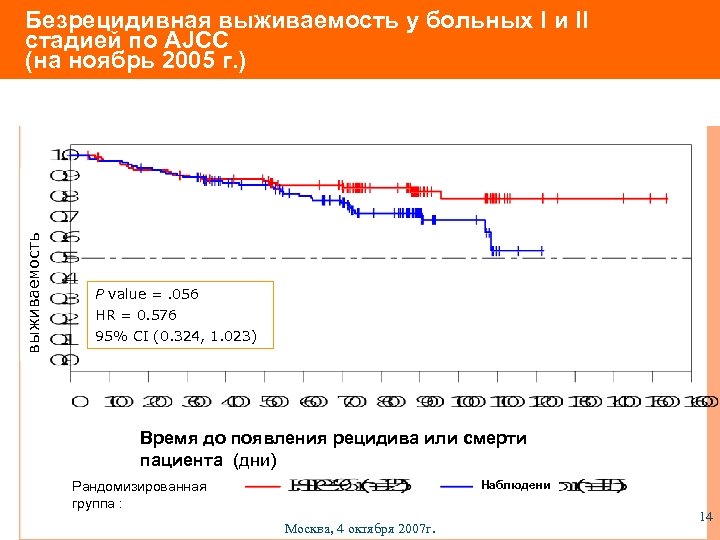
выживаемость Безрецидивная выживаемость у больных I и II стадией по AJCC (на ноябрь 2005 г. ) P value =. 056 HR = 0. 576 95% CI (0. 324, 1. 023) Время до появления рецидива или смерти пациента (дни) Наблюдени е Рандомизированная группа : Москва, 4 октября 2007 г. 14
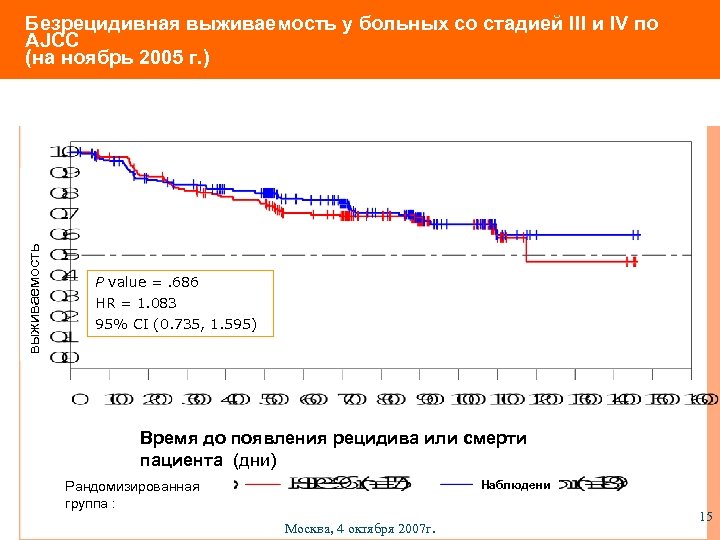
выживаемость Безрецидивная выживаемость у больных со стадией III и IV по AJCC (на ноябрь 2005 г. ) P value =. 686 HR = 1. 083 95% CI (0. 735, 1. 595) Время до появления рецидива или смерти пациента (дни) Наблюдени е Рандомизированная группа : Москва, 4 октября 2007 г. 15
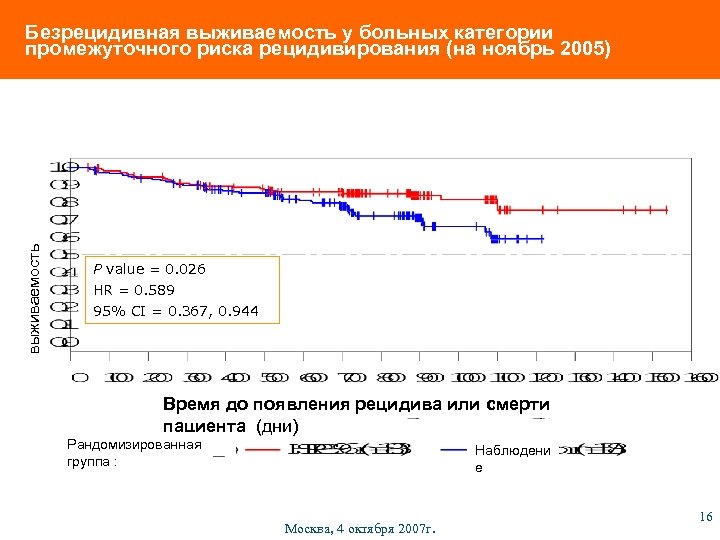
выживаемость Безрецидивная выживаемость у больных категории промежуточного риска рецидивирования (на ноябрь 2005) P value = 0. 026 HR = 0. 589 95% CI = 0. 367, 0. 944 Время до появления рецидива или смерти пациента (дни) Рандомизированная группа : Наблюдени е Москва, 4 октября 2007 г. 16
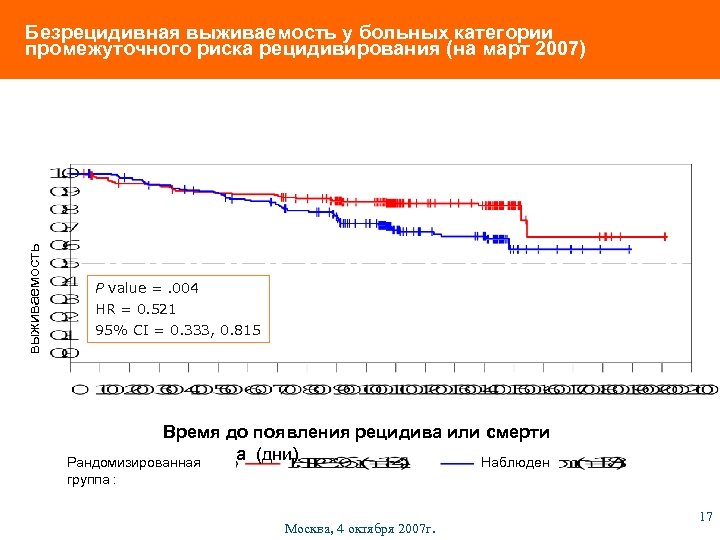
выживаемость Безрецидивная выживаемость у больных категории промежуточного риска рецидивирования (на март 2007) P value =. 004 HR = 0. 521 95% CI = 0. 333, 0. 815 Время до появления рецидива или смерти пациента (дни) Рандомизированная Наблюден группа : ие Москва, 4 октября 2007 г. 17
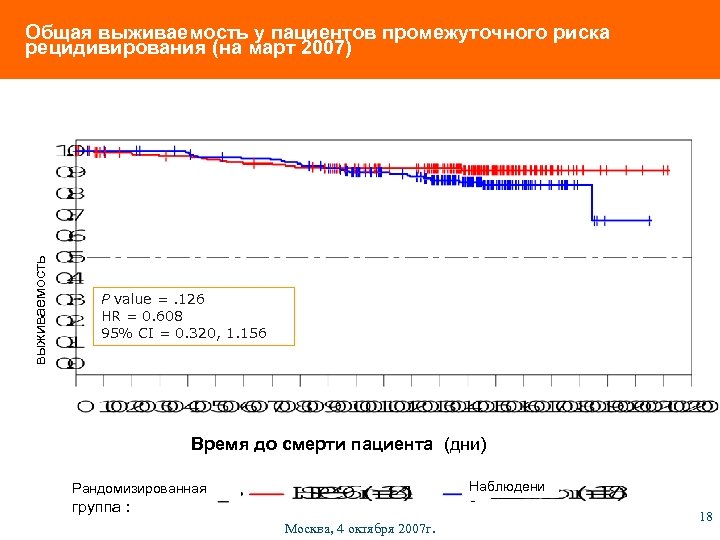
выживаемость Общая выживаемость у пациентов промежуточного риска рецидивирования (на март 2007) P value =. 126 HR = 0. 608 95% CI = 0. 320, 1. 156 Время до смерти пациента (дни) Наблюдени е Рандомизированная группа : Москва, 4 октября 2007 г. 18
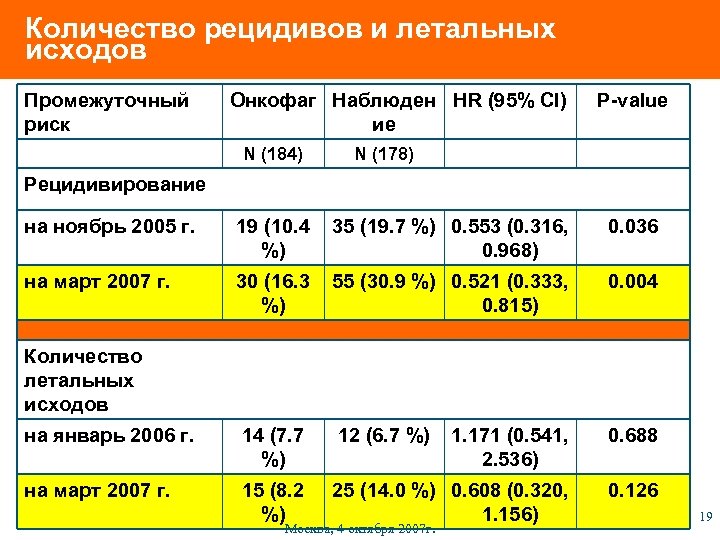
Количество рецидивов и летальных исходов Промежуточный риск Онкофаг Наблюден HR (95% Cl) ие N (184) P-value N (178) Рецидивирование на ноябрь 2005 г. 19 (10. 4 %) 35 (19. 7 %) 0. 553 (0. 316, 0. 968) 0. 036 на март 2007 г. 30 (16. 3 %) 55 (30. 9 %) 0. 521 (0. 333, 0. 815) 0. 004 на январь 2006 г. 14 (7. 7 %) 12 (6. 7 %) 1. 171 (0. 541, 2. 536) 0. 688 на март 2007 г. 15 (8. 2 %) 25 (14. 0 %) 0. 608 (0. 320, 1. 156) 0. 126 Количество летальных исходов Москва, 4 октября 2007 г. 19

Преимущества лечения ОНКОФАГОМ С ОНКОФАГОМ БЕЗ ОНКОФАГА Без рецидива С рецидивом Москва, 4 октября 2007 г. 20
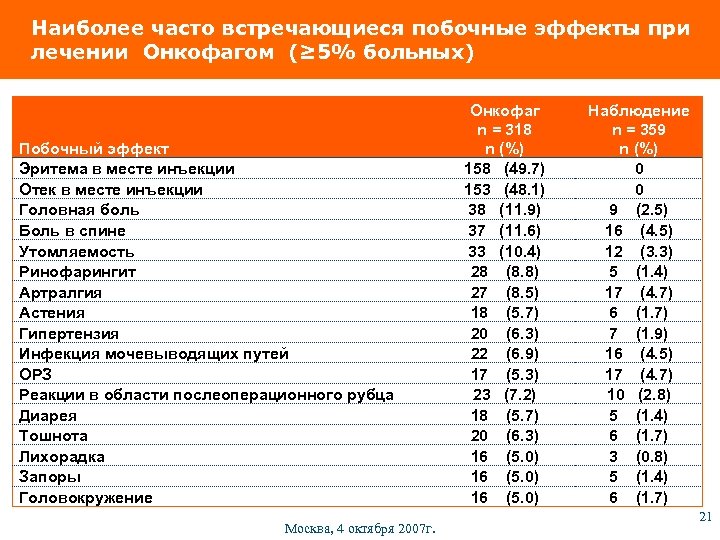
Наиболее часто встречающиеся побочные эффекты при лечении Онкофагом (≥ 5% больных) Побочный эффект Эритема в месте инъекции Отек в месте инъекции Головная боль Боль в спине Утомляемость Ринофарингит Артралгия Астения Гипертензия Инфекция мочевыводящих путей ОРЗ Реакции в области послеоперационного рубца Диарея Тошнота Лихорадка Запоры Головокружение Москва, 4 октября 2007 г. Онкофаг n = 318 n (%) 158 (49. 7) 153 (48. 1) 38 (11. 9) 37 (11. 6) 33 (10. 4) 28 (8. 8) 27 (8. 5) 18 (5. 7) 20 (6. 3) 22 (6. 9) 17 (5. 3) 23 (7. 2) 18 (5. 7) 20 (6. 3) 16 (5. 0) Наблюдение n = 359 n (%) 0 0 9 (2. 5) 16 (4. 5) 12 (3. 3) 5 (1. 4) 17 (4. 7) 6 (1. 7) 7 (1. 9) 16 (4. 5) 17 (4. 7) 10 (2. 8) 5 (1. 4) 6 (1. 7) 3 (0. 8) 5 (1. 4) 6 (1. 7) 21

Выводы Безрецидивная выживаемость : - достоверно выше у пациентов в стадии I и II (AJCC), получавших Онкофаг, по сравнению с группой наблюдения - достоверно выше у пациентов с промежуточным риском рецидивирования (ECOG), получавших Онкофаг, по сравнению с контрольной группой Общая выживаемость: - отмечена тенденция к увеличению продолжительности жизни у больных, получавщих Онкофаг, однако требуется дальнейшее наблюдение Препарат Онкофаг безопасен в применении Москва, 4 октября 2007 г. 22

Заключение Онкофаг открывает перспективу адъювантной терапии у больных почечно-клеточным раком с промежуточным риском прогрессирования Москва, 4 октября 2007 г. 23
0cebcda3a6ffcc5d1c9b97499c12c6a8.ppt