09b95173cf3370762781ab68ed78abb5.ppt
- Количество слайдов: 23

Reunión Bibliográfica - Oncología Sanatorio Allende Martes 07 -10 -14

Introducción • 50% de melanomas cutáneo metastásico albergan una mutación BRAF V 600 • MAPK pathway. • Estos descubrimientos condujeron al desarrollo de agentes que se dirigen específicamente a esta mutación. • El Vemurafenib inhibidor de BRAF. Beneficio en PFS y OS. (Fase III) la reducción relativa en el riesgo de muerte fue 63% y en el riesgo de progresión de la enfermedad fue 74%. • Resultados similares para otro inhibidor de BRAF, dabrafenib. • Eventos tóxicos con ambos agentes son similares erupción cutánea, fatiga y dolor en las articulaciones. • Carcinomas de células escamosas y queratoacantomas 14 a 26% generalmente dentro de los primeros 2 a 3 meses de terapia.

• Los tumores de la piel se desarrollan debido a una activación paradójica de la vía MAPK en queratinocitos por Mutaciones RAS preexistentes, que se pueden bloquear con la adición de un inhibitor MEK. • La progresión después de un período de respuesta tumoral (resistencia adquirida) es común con un solo agente (PFS 6 a 7 m). En 2/3 de los casos es por reactivación de MAPK. • La inhibición inicial de MEK y BRAF podrían ser una estrategia: • ↑ Respuesta del tumor inicial, prevenir la resistencia adquirida. • ↓ frecuencia y severidad de los eventos tóxicos

• Trametinib, un inhibidor de MEK, fue aprobado para el tratamiento del melanoma metastásico BRAF mutado como agente único y en combinación con dabrafenib. • Cobimetinib es una inhibidor de MEK biodisponible por vía oral, selectivo. • Los eventos tóxicos más comunes asociados con Cobimetinib en la (fase 1) diarrea, erupción cutánea, fatiga y edema; grado 3 o más incluyeron diarrea, erupción cutánea, y fatiga.

• Cobimetinib + Vemurafenib (fase 1 b) melanoma avanzado BRAF V 600 mutado. • Dosis escalada se detuvo en la máxima tolerada. • Administrado por 21 días, seguidos de 7 días sin actividad. • Respuesta objetiva confirmada se observó en el 55 de 63 pacientes (87%) • Eventos adversos fueron similares a los observados con los agentes individuales e incluyeron erupción cutánea, diarrea, fotosensibilidad, y aumento de enzimas hepáticas, y como se esperaba, la incidencia de cánceres secundarios cutáneos se redujo. co. BRIM aleatorizado de fase 3, internacional, multicéntrico; evaluó la eficacia y seguridad de cobimetinib combinado con vemurafenib en pacientes con melanoma avanzado BRAF mutado, previamente no tratado.

Métodos PACIENTES • > 18 años de edad • Melanoma histológicamente confirmado, irresecable, localmente avanzado IIIC o IV • Mutación BRAF V 600. PCR • Enfermedad medible, de acuerdo con los Criterios de Evaluación de Respuesta en Tumores Sólidos (RECIST) • PS (ECOG) 0 -1 • Función hematológica, hepática, renal y cardíaca conservada • Los pacientes con metástasis cerebrales tratados fueron elegibles si presentaban 3 semanas de enfermedad estable.

ALEATORIZACIÓN Y TRATAMIENTO • Enero 2013 a enero 2014 495 pacientes en 135 sitios en los Estados Unidos, Canadá, Australia, Nueva Zelanda, Europa, Rusia, Turquía e Israel. • Los pacientes fueron asignados al azar en una proporción de 1: 1 para recibir vemurafenib por vía oral (a un dosis de 960 mg dos veces al día) con placebo (grupo de control) o cobimetinib (a una dosis de 60 mg una vez al día durante 21 días, seguidos de 7 días off) (grupo de combinación). • El tratamiento del estudio continuó hasta que los pacientes retiraron el consentimiento, efectos adversos inaceptable o progresión de la enfermedad. • No se le permitió cruce después de la progresión de la enfermedad. • Permitido modificaciones a la dosis (pre-especificado) para los eventos tóxicos (es decir, grado ≥ 2).

END POINTs Primario • PFS Objetivos secundarios: • OS, la tasa de respuesta objetiva, duración de la respuesta, PFS según la evaluación de revisión independiente, y seguridad. Las evaluaciones se llevaron a cabo al inicio y cada 8 semanas. Se realizo una revisión central independiente, ciega, de evaluación tumoral.

ANÁLISIS ESTADÍSTICO • El número predefinido de eventos de progresión (206 eventos) se alcanzó en mayo de 2014. Análisis de Julio 2014. • Todos los análisis de eficacia se llevaron a cabo en la población con intención de tratar. • Estimamos que 206 acontecimientos de progresión proporcionarían el estudio con al menos el 95% de potencia para detectar HR por muerte o progresión de la enfermedad de 0, 55. • El análisis final de supervivencia global se producirá después de registrar 385 muertes, que estimamos proporcionará el estudio con una potencia del 80% para detectar un HR de muerte de 0, 75.

Resultados • PACIENTES
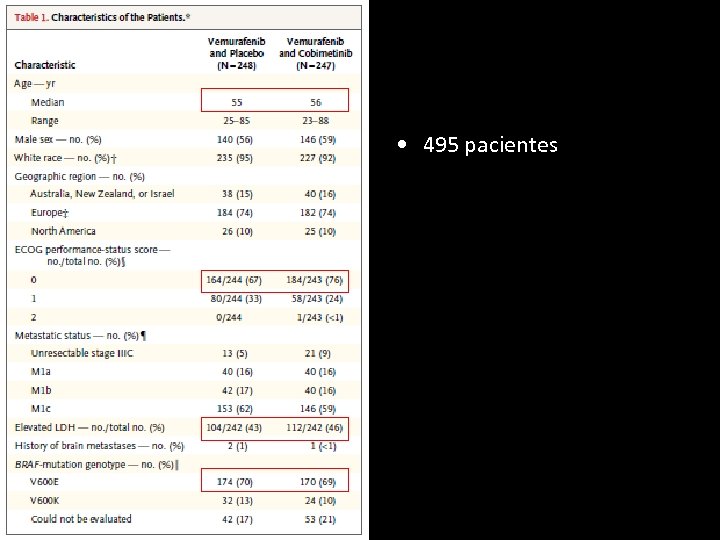
• 495 pacientes
![EFICACIA PFS (ITT) • vemurafenib y cobimetinib: 9, 9 meses (IC del 95% [IC]: EFICACIA PFS (ITT) • vemurafenib y cobimetinib: 9, 9 meses (IC del 95% [IC]:](https://present5.com/presentation/09b95173cf3370762781ab68ed78abb5/image-12.jpg)
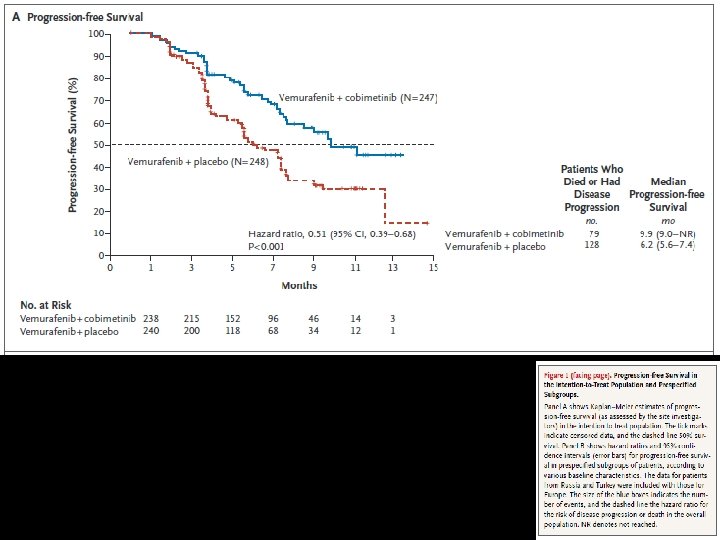
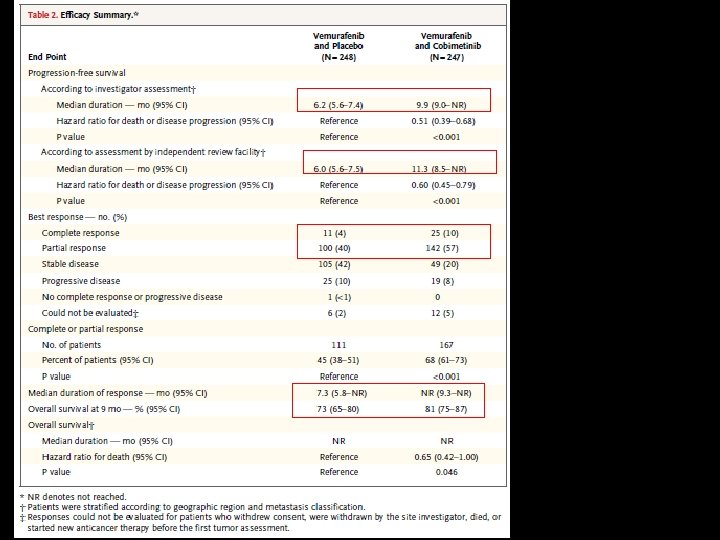
EFICACIA PFS (ITT) • vemurafenib y cobimetinib: 9, 9 meses (IC del 95% [IC]: 9, 0 a no alcanzado), • vemurafenib y placebo: 6, 2 meses (IC del 95%, 5, 6 a 7. 4) • El HR de riesgo de muerte o progresión fue de 0, 51 (IC 95%, 0, 39 -0, 68; P <0, 001) (Fig. 1 A). • El beneficio para PFS fue evidente en todos los subgrupos de pacientes (Fig. 1 B)
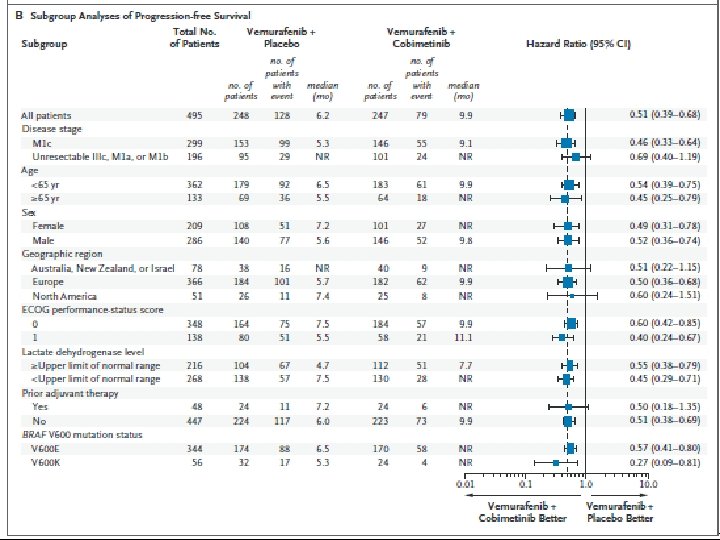

OS (El análisis intermedio a los 9 meses) • vemurafenib y cobimetinib: 81% (IC del 95%, el 75 a 87) • vemurafenib y el placebo: 73% (95% CI, 65 a 80) (Tabla 2 y fig. 2). • El HR fue de 0, 65; 95% CI, 0, 42 a 1, 00; P = 0, 046; P <0, 0000037. • El número de muertes absoluto fue de 34 en el grupo combinado y 51 en el grupo control.
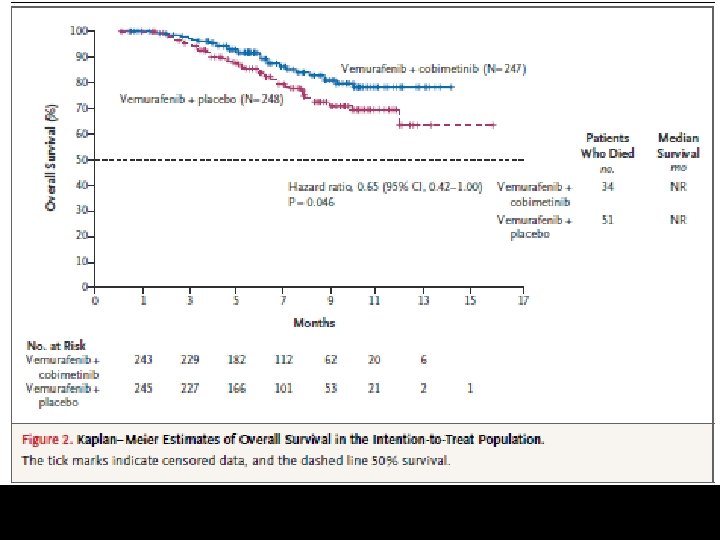

Respuesta • La tasa de respuesta. Rta Objetiva fue de 68% de pacientes en el grupo de combinación, en comparación con 45% en el control grupo (P <0, 001) • La tasa de Rta Completa fue significativamente mayor en la combinación que en el control (10% frente al 4%). • La mayoría de las respuestas fueron vistos en la primera evaluación. • La mediana de la duración de la respuesta fue de 7, 3 meses en el grupo control, y no se alcanzó en el grupo de combinación (Tabla 2).

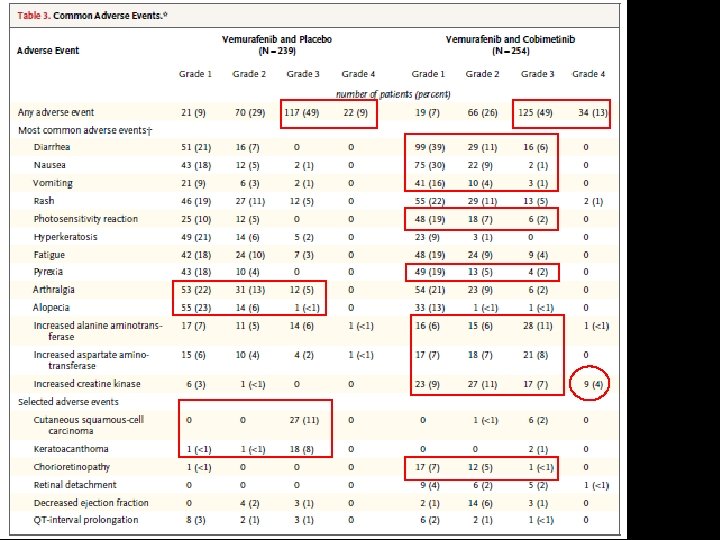
SEGURIDAD • Un total de 493 pacientes (> 99%) recibieron al menos una dosis del fármaco del estudio y se incluyeron en el análisis de seguridad. • La combinación de vemurafenib y cobimetinib se asoció con una mayor frecuencia de retinopatía, eventos gastrointestinales (diarrea, náuseas o vómitos), fotosensibilidad, niveles de transaminasas, y CK; la mayoría (> 50%) de estos eventos individuales fueron grado 1 o 2. • Grado 3 eventos (49%) • Grado 4 eventos (9% vs 13% en el grupo de combinación) • ↑CK (efecto conocido bloqueo de MEK) • ↓Queratoacantomas y carcinoma de células escamosas cutánea, alopecia, y artralgias. (Grupo Combinado) • Seis muertes se atribuyeron a eventos adversos en el grupo de combinación y tres muertes en el grupo de control • Eventos adversos que condujo a la retirada del tratamiento fue 12% en el grupo de control y 13% en el grupo de combinación.

Discusión • Este estudio de fase 3 mostró una mejora en la tasa de respuesta y la supervivencia libre de progresión cuando se añadió cobimetinib al vemurafenib. • Junto con los resultados de un ensayo de fase 3 comparando dabrafenib más trametinib vs dabrafenib solo, estos resultados proporcionan evidencia clara de el beneficio de MEK combinado con la inhibición BRAF. • Los datos que combinan BRAF y MEK necesitan ser puestos en contexto con la rápida evolución: el desarrollo de inmunoterapias o PDL-1.

• Es posible que la administración intermitente de cobimetinib, podría tener un efecto sobre los resultados de la combinación con vemurafenib: datos preclínicos sugieren que el bloqueo intermitente podría retrasar el desarrollo de resistencia adquirida. • La mayoría de los eventos tóxicos comunes visto con la combinación de vemurafenib y cobimetinib fueron de grado 1 o 2.

En conclusión, la combinación de vemurafenib y cobimetinib, en comparación con vemurafenib solo, resultó en una mejora en la PFS y en respuestas objetivas, con las primeras evidencias de mejora en OS y un mayor perfil de toxicidad, entre los pacientes con melanoma avanzado BRAF mutado.
09b95173cf3370762781ab68ed78abb5.ppt