ВИЧ.ppt
- Количество слайдов: 33
 Ретровирусы
Ретровирусы
 Классификация семейства Retroviridae Ø Ø Ø Подсемейство Oncovirinae Род Oncovirus A Род Oncovirus В Род Oncovirus С Род Oncovirus D Подсемейство Spumavirinae «Пенящие» вирусы Cинцитиальные вирусы Подсемейство Lentivirinae «Медленные» ретровирусы Вирусы иммунодефицита человека
Классификация семейства Retroviridae Ø Ø Ø Подсемейство Oncovirinae Род Oncovirus A Род Oncovirus В Род Oncovirus С Род Oncovirus D Подсемейство Spumavirinae «Пенящие» вирусы Cинцитиальные вирусы Подсемейство Lentivirinae «Медленные» ретровирусы Вирусы иммунодефицита человека
 Ø Первые ретровирусы были обнаружены в начале XX в. Эллерманном, Бангом и Раусом, установившими вирусную природу эритробластоза и саркомы кур, но в самостоятельное семейство они были выделены лишь в 1974 г. Ø Характерная особенность членов семейства Retroviridae - наличие обратной транскриптазы (РНК-зависимая ДНКполимераза), а в латинском варианте их названия приставка retro (обратный) также обозначает обратную направленность потока генетической информации (не от ДНК к РНК, а наоборот, от РНК к ДНК). Ø Вирусы покрыты липидной оболочкой; геном образован однонитевой +РНК, образующей комплекс из двух идентичных субъединиц около 3000 к. Д каждая
Ø Первые ретровирусы были обнаружены в начале XX в. Эллерманном, Бангом и Раусом, установившими вирусную природу эритробластоза и саркомы кур, но в самостоятельное семейство они были выделены лишь в 1974 г. Ø Характерная особенность членов семейства Retroviridae - наличие обратной транскриптазы (РНК-зависимая ДНКполимераза), а в латинском варианте их названия приставка retro (обратный) также обозначает обратную направленность потока генетической информации (не от ДНК к РНК, а наоборот, от РНК к ДНК). Ø Вирусы покрыты липидной оболочкой; геном образован однонитевой +РНК, образующей комплекс из двух идентичных субъединиц около 3000 к. Д каждая
 Т-клеточные лимфотропные вирусы человека (HTLV) обладают низким онкогенным потенциалом и выделяются при различных поражениях Тлимфоцитов. Заболевания распознают выявлением AT к возбудителю. Ø 1. HTLV-1 вызывает Т-клеточные лейкозы (лимфосаркомы) и миелопатии (тропический спастический парапарез) у взрослого населения Юго. Запада Японии, Экваториальной Африки, Севера США и стран Карибского бассейна. Ø 2. HTLV-II выделяют при некоторых формах хронического лимфолейкоза (волосатоклеточный лейкоз), однако прямых доказательств патогенного действия нет. Ø
Т-клеточные лимфотропные вирусы человека (HTLV) обладают низким онкогенным потенциалом и выделяются при различных поражениях Тлимфоцитов. Заболевания распознают выявлением AT к возбудителю. Ø 1. HTLV-1 вызывает Т-клеточные лейкозы (лимфосаркомы) и миелопатии (тропический спастический парапарез) у взрослого населения Юго. Запада Японии, Экваториальной Африки, Севера США и стран Карибского бассейна. Ø 2. HTLV-II выделяют при некоторых формах хронического лимфолейкоза (волосатоклеточный лейкоз), однако прямых доказательств патогенного действия нет. Ø
 Первая встреча Ø Ø Ø 1981 г. США у мужчин гомосексуалистов впервые вяывленая новая болезнь - синдром приобретенного иммунодефицита 1982 г. Р. Галло в США предположение, выделил вирус СПИДа - ретровирус 1983 г. Л. Монтанье сотрудник Пастеровского института в Париже из л. у. Выделил еще один вирус тропный к CD 4 рецепторамлимфоцитов 1986 г. Международный комитет по таксономии Human immunodeficiency virus (HIV)
Первая встреча Ø Ø Ø 1981 г. США у мужчин гомосексуалистов впервые вяывленая новая болезнь - синдром приобретенного иммунодефицита 1982 г. Р. Галло в США предположение, выделил вирус СПИДа - ретровирус 1983 г. Л. Монтанье сотрудник Пастеровского института в Париже из л. у. Выделил еще один вирус тропный к CD 4 рецепторамлимфоцитов 1986 г. Международный комитет по таксономии Human immunodeficiency virus (HIV)
 Саркома Капоши на лице
Саркома Капоши на лице
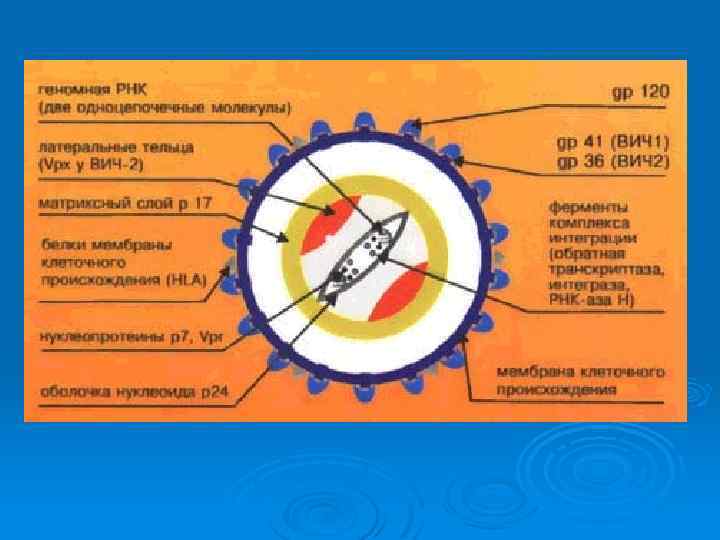
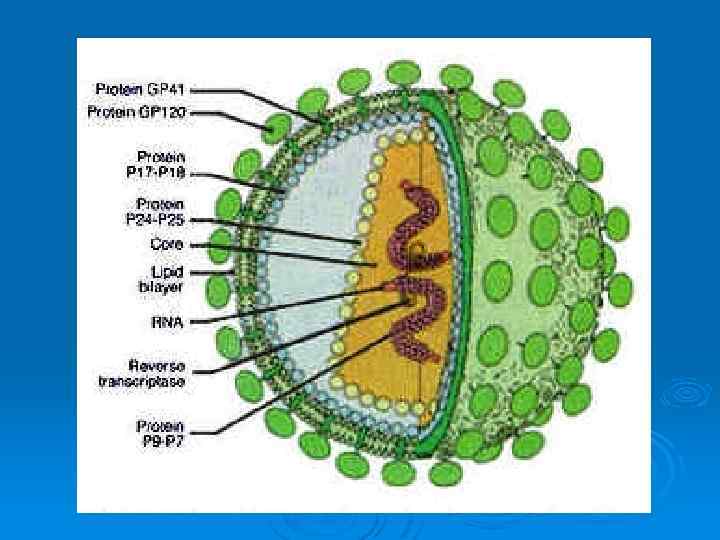
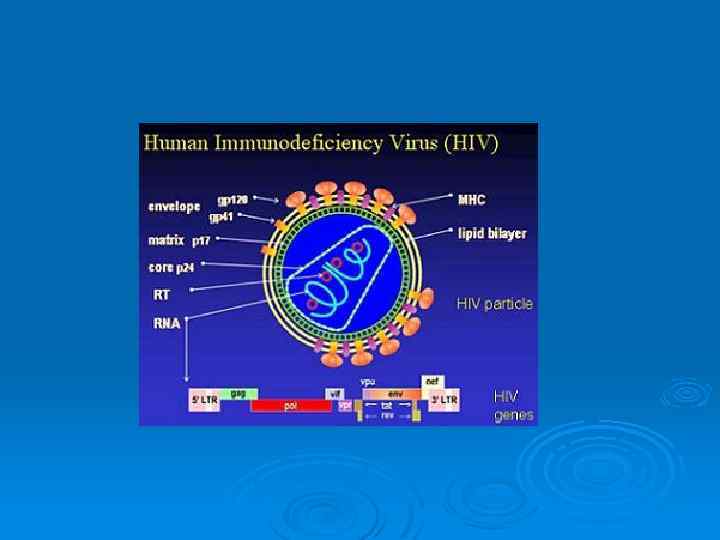
 Строение ВИЧ имеют сферическую форму, их размеры не превышают 100 -120 нм в диаметре. Ø Наружная оболочка образована двойным липидным слоем с гликопротеиновыми «шипами» . Ø Каждый содержит две субъединицы (gp 41 и gpl 20); первый белок пронизывает липидный слой насквозь. Ø Под оболочкой расположена сердцевина цилиндрической или конусовидной формы; её образуют белки р18 и р24. В сердцевине располагаются РНК, внутренние белки (р7 и р9) и обратная транскриптаза. Ø
Строение ВИЧ имеют сферическую форму, их размеры не превышают 100 -120 нм в диаметре. Ø Наружная оболочка образована двойным липидным слоем с гликопротеиновыми «шипами» . Ø Каждый содержит две субъединицы (gp 41 и gpl 20); первый белок пронизывает липидный слой насквозь. Ø Под оболочкой расположена сердцевина цилиндрической или конусовидной формы; её образуют белки р18 и р24. В сердцевине располагаются РНК, внутренние белки (р7 и р9) и обратная транскриптаза. Ø
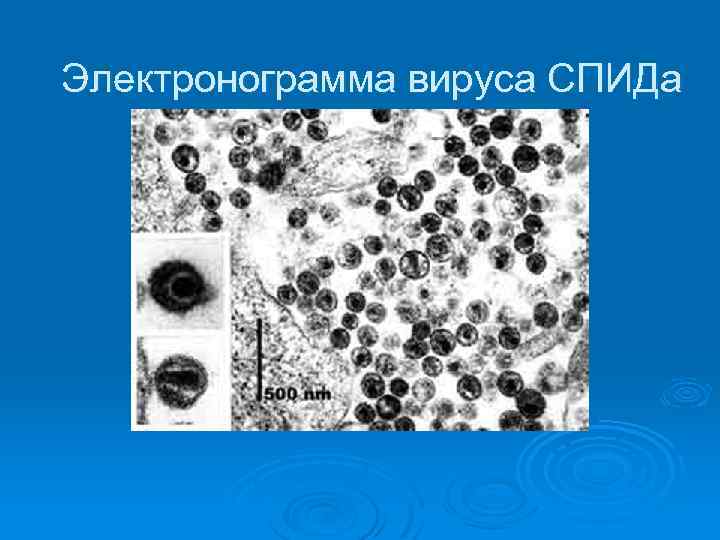 Электронограмма вируса СПИДа
Электронограмма вируса СПИДа
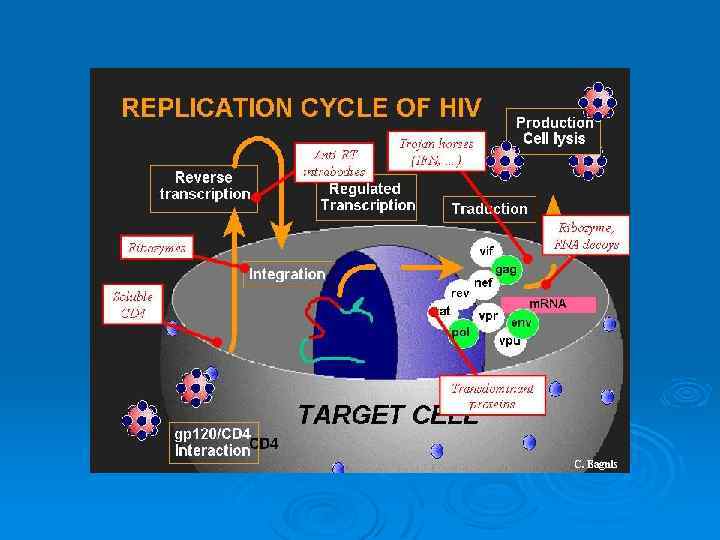
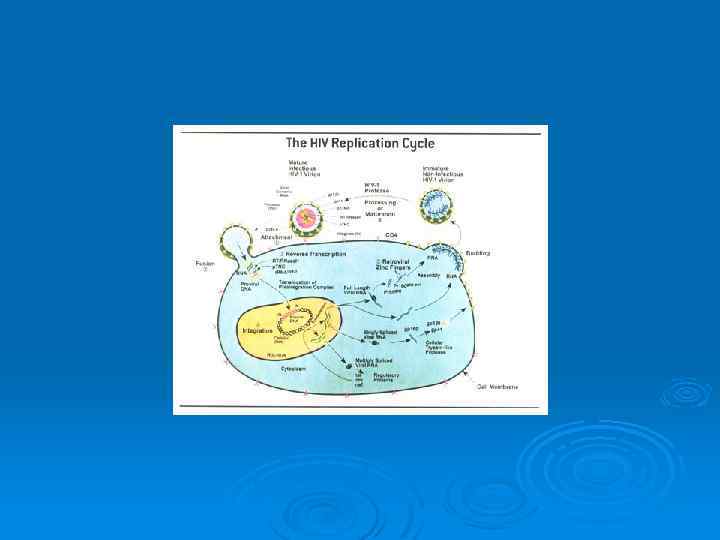
 Специфические белки вирусов 1. Протеины групповых Аг (Gag-белки) соединяют сердцевину вируса с вирусной РНК (может быть 3 или 4); белки сердцевины формируют группо- и видоспецифичные Аг (кошачий, мышиный и т. д. ) Ø 2. Pol- (полимеразный) протеин представлен обратной транскриптазой. Ø 3. Env-белки оболочки образуют группу типоспецифичных гликопротеиновых Аг поверхностной мембраны. Ø
Специфические белки вирусов 1. Протеины групповых Аг (Gag-белки) соединяют сердцевину вируса с вирусной РНК (может быть 3 или 4); белки сердцевины формируют группо- и видоспецифичные Аг (кошачий, мышиный и т. д. ) Ø 2. Pol- (полимеразный) протеин представлен обратной транскриптазой. Ø 3. Env-белки оболочки образуют группу типоспецифичных гликопротеиновых Аг поверхностной мембраны. Ø
 Некоторые особенности патогенеза Ø Ø Ø СD 4 - главная молекулярная мишень для ВИЧ - связь с gp 120 -- Т-лимфоциты обеспечиваю репликацию вируса на 90%. CD 4 40 % МФ, Nk, дендритные клетки и некотрые Влф (в культуре клеток CD 4 - ВИЧ репродуцируютсярастут !! Могут взаимодействовать с маннозным рецептором МФ и дендритных клеток и галактозилцерамидом нейроглии Чтобы попасть в клетку вирусу нужен gp 41 cуперкуапсида --попадание в клетку за счет слияния мембран , связь с F белком мембран (может быть блокирована хемокинами
Некоторые особенности патогенеза Ø Ø Ø СD 4 - главная молекулярная мишень для ВИЧ - связь с gp 120 -- Т-лимфоциты обеспечиваю репликацию вируса на 90%. CD 4 40 % МФ, Nk, дендритные клетки и некотрые Влф (в культуре клеток CD 4 - ВИЧ репродуцируютсярастут !! Могут взаимодействовать с маннозным рецептором МФ и дендритных клеток и галактозилцерамидом нейроглии Чтобы попасть в клетку вирусу нужен gp 41 cуперкуапсида --попадание в клетку за счет слияния мембран , связь с F белком мембран (может быть блокирована хемокинами
 Иммуногенность Ag ВИЧ Ø Наиболее иммуногенными белками вирусной частицы, как и других известных форм вирусных инфекций, являются поверхностные гликопротеины gp 160/120, а также трансмембранный белок gp 41, которые кодируются геном env. Антитела к белкам, кодируемым геном env, появляются относительно рано, выявляются у 98% инфицированных и более стабильны, чем антитела к другим антигенам. Антитела к основным внутренним белкам ВИЧ (р17 и р24) выявляются примерно у 75% инфицированных и не чаще, чем у 50% больных с клинически выраженным СПИДом.
Иммуногенность Ag ВИЧ Ø Наиболее иммуногенными белками вирусной частицы, как и других известных форм вирусных инфекций, являются поверхностные гликопротеины gp 160/120, а также трансмембранный белок gp 41, которые кодируются геном env. Антитела к белкам, кодируемым геном env, появляются относительно рано, выявляются у 98% инфицированных и более стабильны, чем антитела к другим антигенам. Антитела к основным внутренним белкам ВИЧ (р17 и р24) выявляются примерно у 75% инфицированных и не чаще, чем у 50% больных с клинически выраженным СПИДом.
 Геном ВИЧ Ø Ø Ø Ø Ø образуют две нити +РНК, соединённые вблизи их 5'терминалей; включает следующие гены: 1. Ген gag кодирует полипротеин, постсинтетически расщепляющийся на отдельные иммуногенные структурные белки (группоспецифичные Аг). 2. Ген pol кодирует синтез обратной транскриптазы (ревертазы). 3. Гены, локализованные вблизи соединения gag-pol, 4. Ген env кодирует гликопротеины оболочки. 5. Регуляторные гены а. Ген tat (трансактиватор транскрипции) б. Ген rev (регулятор экспрессии вирусных белков). Ген nef (отрицательный фактор экспрессии) в. Ген vif (фактор инфекционности вируса)
Геном ВИЧ Ø Ø Ø Ø Ø образуют две нити +РНК, соединённые вблизи их 5'терминалей; включает следующие гены: 1. Ген gag кодирует полипротеин, постсинтетически расщепляющийся на отдельные иммуногенные структурные белки (группоспецифичные Аг). 2. Ген pol кодирует синтез обратной транскриптазы (ревертазы). 3. Гены, локализованные вблизи соединения gag-pol, 4. Ген env кодирует гликопротеины оболочки. 5. Регуляторные гены а. Ген tat (трансактиватор транскрипции) б. Ген rev (регулятор экспрессии вирусных белков). Ген nef (отрицательный фактор экспрессии) в. Ген vif (фактор инфекционности вируса)
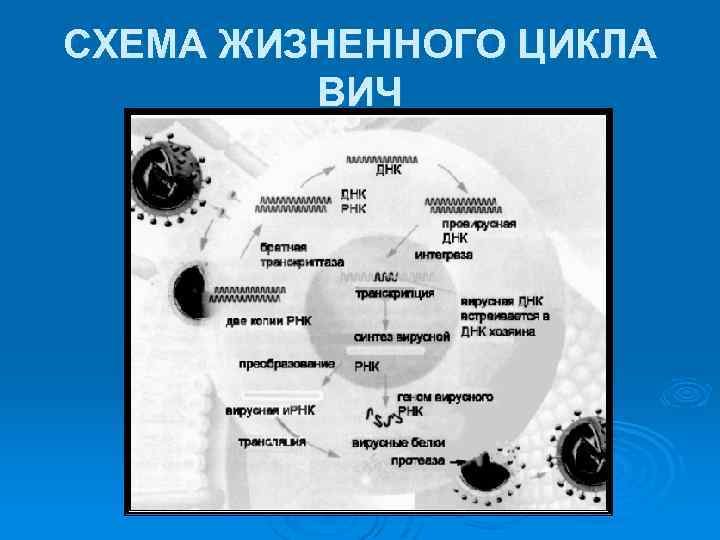 СХЕМА ЖИЗНЕННОГО ЦИКЛА ВИЧ
СХЕМА ЖИЗНЕННОГО ЦИКЛА ВИЧ
 Вирусы иммунодефицита человека (ВИЧ) Большинство исследователей склоняются к мысли об африканском происхождении заболевания и его распространении в США через страны Карибского бассейна, т. к. ещё в начале 70 -х гг. у жителей некоторых африканских стран обнаруживали AT к ВИЧ. Ø К настоящему времени идентифицировано два вида ВИЧ. Ø
Вирусы иммунодефицита человека (ВИЧ) Большинство исследователей склоняются к мысли об африканском происхождении заболевания и его распространении в США через страны Карибского бассейна, т. к. ещё в начале 70 -х гг. у жителей некоторых африканских стран обнаруживали AT к ВИЧ. Ø К настоящему времени идентифицировано два вида ВИЧ. Ø
 наличие делеции в гене CKR-5 (CСR-5) защищает от заражения вирусом иммунодефицита человека, причём устойчивость к ВИЧ-инфицированию передаётся по наследству. Тем не менее, массивное поступление ВИЧ в организм при переливании крови никакая иммунная система сдержать не в силах: вероятность заражения при гемотрансфузиях превышает 90%.
наличие делеции в гене CKR-5 (CСR-5) защищает от заражения вирусом иммунодефицита человека, причём устойчивость к ВИЧ-инфицированию передаётся по наследству. Тем не менее, массивное поступление ВИЧ в организм при переливании крови никакая иммунная система сдержать не в силах: вероятность заражения при гемотрансфузиях превышает 90%.
 Пути инфицирования Половой -85 -90% (5 -10% гомо- остальные гетеро-) Инъекционный гемотрансузия 3 -5% НАРКОМАНЫ >10 % Вертикальный во время беременности и родов Контактный кровь!!!!!!сперма, слизь шейки матки +- молоко, мед. персонал
Пути инфицирования Половой -85 -90% (5 -10% гомо- остальные гетеро-) Инъекционный гемотрансузия 3 -5% НАРКОМАНЫ >10 % Вертикальный во время беременности и родов Контактный кровь!!!!!!сперма, слизь шейки матки +- молоко, мед. персонал
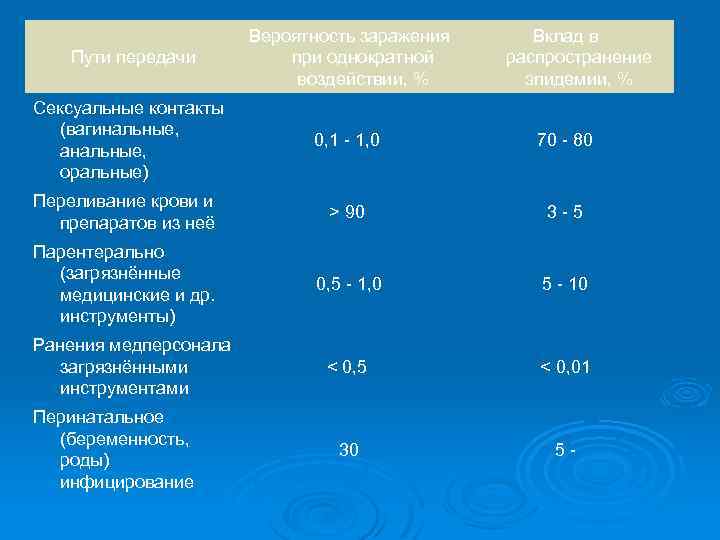 Пути передачи Вероятность заражения при однократной воздействии, % Сексуальные контакты (вагинальные, анальные, оральные) 0, 1 - 1, 0 70 - 80 Переливание крови и препаратов из неё > 90 3 - 5 Парентерально (загрязнённые медицинские и др. инструменты) 0, 5 - 1, 0 5 - 10 < 0, 5 < 0, 01 30 5 - Ранения медперсонала загрязнёнными инструментами Перинатальное (беременность, роды) инфицирование Вклад в распространение эпидемии, %
Пути передачи Вероятность заражения при однократной воздействии, % Сексуальные контакты (вагинальные, анальные, оральные) 0, 1 - 1, 0 70 - 80 Переливание крови и препаратов из неё > 90 3 - 5 Парентерально (загрязнённые медицинские и др. инструменты) 0, 5 - 1, 0 5 - 10 < 0, 5 < 0, 01 30 5 - Ранения медперсонала загрязнёнными инструментами Перинатальное (беременность, роды) инфицирование Вклад в распространение эпидемии, %
 Спид-ассоциированные инфекции • • • • Бактериальные инфекции кожи Опоясывающий лишай Молочница ротовой полости Тяжелые грибковые инфекции стоп Волосистая лейкоплакия слизистой ротовой полости Туберкулез Пневмоцистная пневмония Глубокие микозы Токсоплазмоз Простой герпес ЦМВ-инфекция Микобактериоз Папилломавирусная инфекция Саркома Капоши γ-Herpesvirinae Rhadinovirus (HHV-8) Атипичный микобактериоз Кандидоз смерть
Спид-ассоциированные инфекции • • • • Бактериальные инфекции кожи Опоясывающий лишай Молочница ротовой полости Тяжелые грибковые инфекции стоп Волосистая лейкоплакия слизистой ротовой полости Туберкулез Пневмоцистная пневмония Глубокие микозы Токсоплазмоз Простой герпес ЦМВ-инфекция Микобактериоз Папилломавирусная инфекция Саркома Капоши γ-Herpesvirinae Rhadinovirus (HHV-8) Атипичный микобактериоз Кандидоз смерть
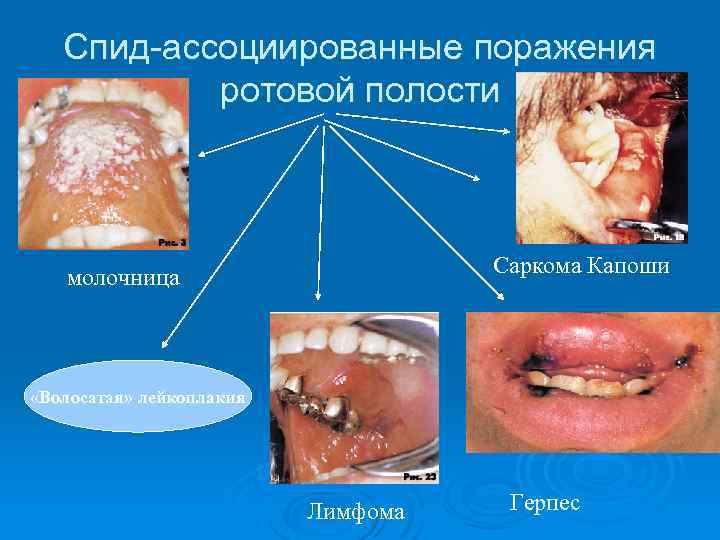 Спид-ассоциированные поражения ротовой полости Саркома Капоши молочница «Волосатая» лейкоплакия Лимфома Герпес
Спид-ассоциированные поражения ротовой полости Саркома Капоши молочница «Волосатая» лейкоплакия Лимфома Герпес
 Лабораторная диагностика Ø Ø Ø ретровирусных инфекций достаточно затруднительна. 1. Выделение возбудителя возможно на культурах клеток, а видов, патогенных для животных, — заражением чувствительных животных моделей (зеленые мартышки и макаки) у новорожденных. 2. Большее распространение нашли методы идентификации, основанные на выявлении вирусных Аг и AT к ним, например, метод иммунофлюоресценции, ИФА, РНГА, иммуноблотинг. 3. ПЦР, ДНК-зонды 4. СD 4/CD 8 снижение 4. При диагностике также учитывают некоторые биологические свойства, например, способность к образованию синцития, способность индуцировать появление онко-Аг в клеточных культурах или in vivo, также проводят измерение активности обратной транскриптазы с использованием синтетической «затравки-матрицы» , например, олиго-d. Т: поли-г. А.
Лабораторная диагностика Ø Ø Ø ретровирусных инфекций достаточно затруднительна. 1. Выделение возбудителя возможно на культурах клеток, а видов, патогенных для животных, — заражением чувствительных животных моделей (зеленые мартышки и макаки) у новорожденных. 2. Большее распространение нашли методы идентификации, основанные на выявлении вирусных Аг и AT к ним, например, метод иммунофлюоресценции, ИФА, РНГА, иммуноблотинг. 3. ПЦР, ДНК-зонды 4. СD 4/CD 8 снижение 4. При диагностике также учитывают некоторые биологические свойства, например, способность к образованию синцития, способность индуцировать появление онко-Аг в клеточных культурах или in vivo, также проводят измерение активности обратной транскриптазы с использованием синтетической «затравки-матрицы» , например, олиго-d. Т: поли-г. А.
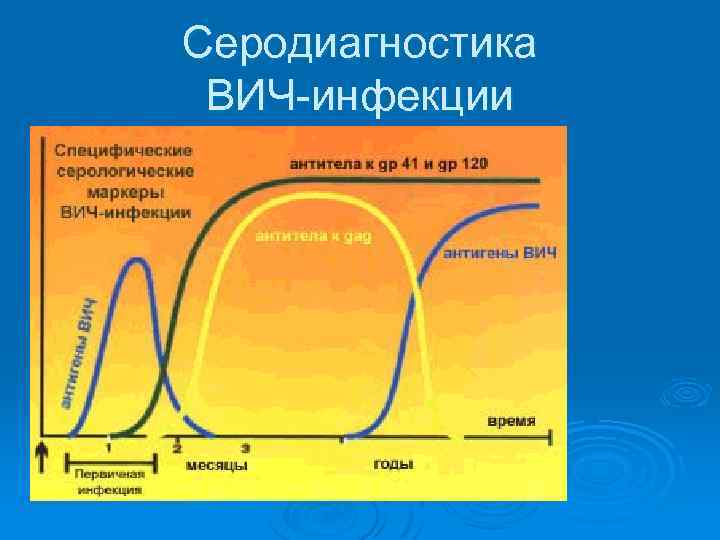 Cеродиагностика ВИЧ-инфекции
Cеродиагностика ВИЧ-инфекции
 Иммуноблоттинг
Иммуноблоттинг
 Для поздних стадии СПИДа характерны общая лимфопения, нейтропения, тромбоцитопения ( соответственно, снижение числа лимфоцитов, нейтрофилов и тромбоцитов), анемия. Эти изменения могут быть следствием центрального угнетения кроветворения за счёт поражения кроветворных органов вирусом, а также - аутоиммунного разрушения клеточных субпопуляции на периферии. Кроме того, для СПИДа характерно умеренное увеличение количества гамма-глобулинов с доминирующим увеличением содержания Ig. G. Больные с выраженными симптомами СПИДа нередко имеют повышенный уровень Ig. A. На некоторых стадиях заболевания существенно повышается уровень таких маркёров СПИДа, как β 1 -микроглобулин, кислотостабильный α-интерферон, α 1 -тимозин. То же происходит с секрецией свободного неоптерина — метаболита макрофагов.
Для поздних стадии СПИДа характерны общая лимфопения, нейтропения, тромбоцитопения ( соответственно, снижение числа лимфоцитов, нейтрофилов и тромбоцитов), анемия. Эти изменения могут быть следствием центрального угнетения кроветворения за счёт поражения кроветворных органов вирусом, а также - аутоиммунного разрушения клеточных субпопуляции на периферии. Кроме того, для СПИДа характерно умеренное увеличение количества гамма-глобулинов с доминирующим увеличением содержания Ig. G. Больные с выраженными симптомами СПИДа нередко имеют повышенный уровень Ig. A. На некоторых стадиях заболевания существенно повышается уровень таких маркёров СПИДа, как β 1 -микроглобулин, кислотостабильный α-интерферон, α 1 -тимозин. То же происходит с секрецией свободного неоптерина — метаболита макрофагов.
 Терапия ВИЧ-инфекции Ø I. Ингибиторы обратной транскриптазы Ø 1. аналоги нуклеозидов: тимидина (зидовудин=азидотимидин=ретровир, фозфазид, ставудин); Ø аденина (диданозин); цитидина (ламивудин, зальцитабин); гуанина Ø (абакавир), комбинированные препараты: комбивир(зидовудин +ламивудин); абакавир (зидовудин+ламивудин); Ø Ø 2. ненуклеозидные ингибиторы обратной тракскриптазы: невирапин, эфавиренц, делавердин II. Ингибиторы протеазы: ампренавир, аманазавир, индинавир, ретонавир, саквинавир, нельфинавир Ø Интерфероны+ их индукторы+ интерлейкины Инф 8!!, , препараты тимуса, пересадка костного мозга, , переливание лимфоцитарной массы, экстрокорпоральная иммуносорбция
Терапия ВИЧ-инфекции Ø I. Ингибиторы обратной транскриптазы Ø 1. аналоги нуклеозидов: тимидина (зидовудин=азидотимидин=ретровир, фозфазид, ставудин); Ø аденина (диданозин); цитидина (ламивудин, зальцитабин); гуанина Ø (абакавир), комбинированные препараты: комбивир(зидовудин +ламивудин); абакавир (зидовудин+ламивудин); Ø Ø 2. ненуклеозидные ингибиторы обратной тракскриптазы: невирапин, эфавиренц, делавердин II. Ингибиторы протеазы: ампренавир, аманазавир, индинавир, ретонавир, саквинавир, нельфинавир Ø Интерфероны+ их индукторы+ интерлейкины Инф 8!!, , препараты тимуса, пересадка костного мозга, , переливание лимфоцитарной массы, экстрокорпоральная иммуносорбция
 Лечение беременных Ø ВИЧ-инфекция - абсолютное показание для прерывания беременности Ø Отсутствует тератогенный эффект у диданозина, фосфазида, ритонавира, саквинавира Ø Азидотимидин, зальцитабин, эфавиренц тератогенны
Лечение беременных Ø ВИЧ-инфекция - абсолютное показание для прерывания беременности Ø Отсутствует тератогенный эффект у диданозина, фосфазида, ритонавира, саквинавира Ø Азидотимидин, зальцитабин, эфавиренц тератогенны
 ХИМОПРОФИЛАКТИКА ВИЧ во время родов Ø азидотимидин в/в от начала до завершения родов Ø азидотимидин per os от начала до з часов до окончания родов Ø невирапин per ps однократно до завершения родов Ø фосфазид при начале родовой деятельности затем каждые 4 часа
ХИМОПРОФИЛАКТИКА ВИЧ во время родов Ø азидотимидин в/в от начала до завершения родов Ø азидотимидин per os от начала до з часов до окончания родов Ø невирапин per ps однократно до завершения родов Ø фосфазид при начале родовой деятельности затем каждые 4 часа
 ХИМИОПРОФИЛАКТИКА ВИЧ-инфекции у новорожденных Ø Если не проводилось лечение матери в период беременности и родов и не была назначена в первые 24 часа - бессмысленна Ø В первые с 8 -часа жизни азидотимидин в сиропе + невирапин Ø без лечения 30% ВИЧ-инфицированных детей умирают до 6 меясецев, 17 -25 - до 2 лет, при своевременно начатом лечении 75 % доживают до 6 лет, 50% до 9 лет.
ХИМИОПРОФИЛАКТИКА ВИЧ-инфекции у новорожденных Ø Если не проводилось лечение матери в период беременности и родов и не была назначена в первые 24 часа - бессмысленна Ø В первые с 8 -часа жизни азидотимидин в сиропе + невирапин Ø без лечения 30% ВИЧ-инфицированных детей умирают до 6 меясецев, 17 -25 - до 2 лет, при своевременно начатом лечении 75 % доживают до 6 лет, 50% до 9 лет.
 Экстренная химиопрофилактика профессионального заражения ВИЧ Медработники, имеющие контакт с больными при инвазивных манипуляциях (стоматологи, хирурги, гинекологи. . ) сотрудники лабораторий, работающие с потенциально инфицированным биологическим материалом) Ø НАЧАЛО ПРОФИЛАКТИКИ не позже 72 часов (азидотимидин+ ламивудин+индинавир) Ø местная обработка ( механическое удаление и обеззараживание) Ø Вопрос об организации ЭХТ половой передачи ВИЧ материально государством не финансируется Ø
Экстренная химиопрофилактика профессионального заражения ВИЧ Медработники, имеющие контакт с больными при инвазивных манипуляциях (стоматологи, хирурги, гинекологи. . ) сотрудники лабораторий, работающие с потенциально инфицированным биологическим материалом) Ø НАЧАЛО ПРОФИЛАКТИКИ не позже 72 часов (азидотимидин+ ламивудин+индинавир) Ø местная обработка ( механическое удаление и обеззараживание) Ø Вопрос об организации ЭХТ половой передачи ВИЧ материально государством не финансируется Ø


