 Решение заданий к к/р № 1 по темам «Растворы. Кислород. ТХУ. Водород»
Решение заданий к к/р № 1 по темам «Растворы. Кислород. ТХУ. Водород»
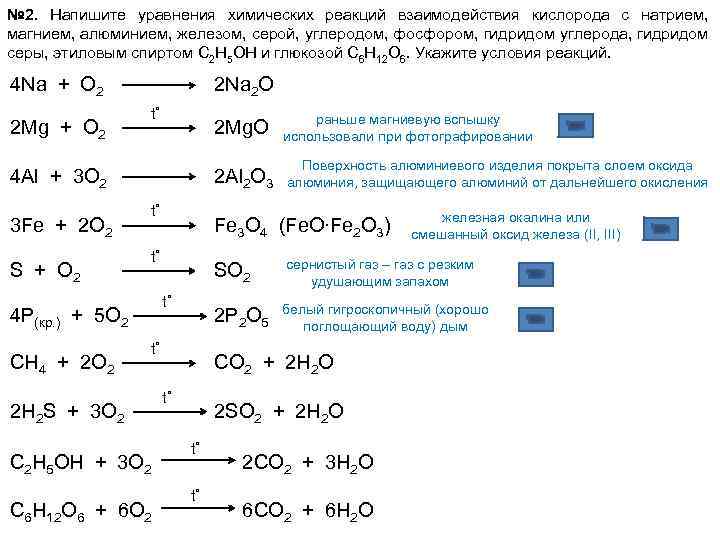 № 2. Напишите уравнения химических реакций взаимодействия кислорода с натрием, магнием, алюминием, железом, серой, углеродом, фосфором, гидридом углерода, гидридом серы, этиловым спиртом C 2 H 5 OH и глюкозой C 6 H 12 O 6. Укажите условия реакций. 4 Na + O 2 2 Mg + O 2 2 Na 2 O t˚ 2 Mg. O 2 Al 2 O 3 4 Al + 3 O 2 3 Fe + 2 O 2 S + O 2 t˚ CH 4 + 2 O 2 C 6 H 12 O 6 + 6 O 2 сернистый газ – газ с резким удушающим запахом 2 P 2 O 5 t˚ C 2 H 5 OH + 3 O 2 железная окалина или смешанный оксид железа (II, III) SO 2 t˚ 2 H 2 S + 3 O 2 Поверхность алюминиевого изделия покрыта слоем оксида алюминия, защищающего алюминий от дальнейшего окисления Fe 3 O 4 (Fe. O∙Fe 2 O 3) t˚ 4 P(кр. ) + 5 O 2 раньше магниевую вспышку использовали при фотографировании белый гигроскопичный (хорошо поглощающий воду) дым CO 2 + 2 H 2 O t˚ 2 SO 2 + 2 H 2 O t˚ t˚ 2 CO 2 + 3 H 2 O 6 CO 2 + 6 H 2 O
№ 2. Напишите уравнения химических реакций взаимодействия кислорода с натрием, магнием, алюминием, железом, серой, углеродом, фосфором, гидридом углерода, гидридом серы, этиловым спиртом C 2 H 5 OH и глюкозой C 6 H 12 O 6. Укажите условия реакций. 4 Na + O 2 2 Mg + O 2 2 Na 2 O t˚ 2 Mg. O 2 Al 2 O 3 4 Al + 3 O 2 3 Fe + 2 O 2 S + O 2 t˚ CH 4 + 2 O 2 C 6 H 12 O 6 + 6 O 2 сернистый газ – газ с резким удушающим запахом 2 P 2 O 5 t˚ C 2 H 5 OH + 3 O 2 железная окалина или смешанный оксид железа (II, III) SO 2 t˚ 2 H 2 S + 3 O 2 Поверхность алюминиевого изделия покрыта слоем оксида алюминия, защищающего алюминий от дальнейшего окисления Fe 3 O 4 (Fe. O∙Fe 2 O 3) t˚ 4 P(кр. ) + 5 O 2 раньше магниевую вспышку использовали при фотографировании белый гигроскопичный (хорошо поглощающий воду) дым CO 2 + 2 H 2 O t˚ 2 SO 2 + 2 H 2 O t˚ t˚ 2 CO 2 + 3 H 2 O 6 CO 2 + 6 H 2 O
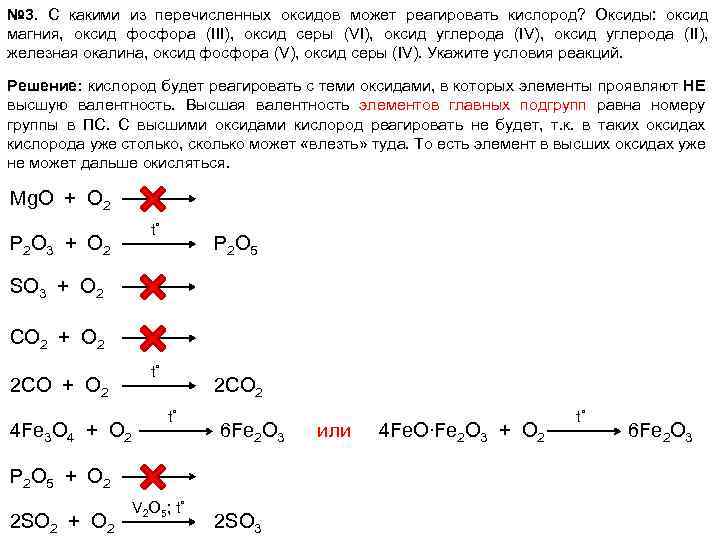 № 3. С какими из перечисленных оксидов может реагировать кислород? Оксиды: оксид магния, оксид фосфора (III), оксид серы (VI), оксид углерода (IV), оксид углерода (II), железная окалина, оксид фосфора (V), оксид серы (IV). Укажите условия реакций. Решение: кислород будет реагировать с теми оксидами, в которых элементы проявляют НЕ высшую валентность. Высшая валентность элементов главных подгрупп равна номеру группы в ПС. С высшими оксидами кислород реагировать не будет, т. к. в таких оксидах кислорода уже столько, сколько может «влезть» туда. То есть элемент в высших оксидах уже не может дальше окисляться. Mg. O + O 2 P 2 O 3 + O 2 t˚ P 2 O 5 SO 3 + O 2 CO 2 + O 2 2 CO + O 2 4 Fe 3 O 4 + O 2 t˚ 2 CO 2 t˚ 6 Fe 2 O 3 P 2 O 5 + O 2 2 SO 2 + O 2 V 2 O 5; t˚ 2 SO 3 или 4 Fe. O∙Fe 2 O 3 + O 2 t˚ 6 Fe 2 O 3
№ 3. С какими из перечисленных оксидов может реагировать кислород? Оксиды: оксид магния, оксид фосфора (III), оксид серы (VI), оксид углерода (IV), оксид углерода (II), железная окалина, оксид фосфора (V), оксид серы (IV). Укажите условия реакций. Решение: кислород будет реагировать с теми оксидами, в которых элементы проявляют НЕ высшую валентность. Высшая валентность элементов главных подгрупп равна номеру группы в ПС. С высшими оксидами кислород реагировать не будет, т. к. в таких оксидах кислорода уже столько, сколько может «влезть» туда. То есть элемент в высших оксидах уже не может дальше окисляться. Mg. O + O 2 P 2 O 3 + O 2 t˚ P 2 O 5 SO 3 + O 2 CO 2 + O 2 2 CO + O 2 4 Fe 3 O 4 + O 2 t˚ 2 CO 2 t˚ 6 Fe 2 O 3 P 2 O 5 + O 2 2 SO 2 + O 2 V 2 O 5; t˚ 2 SO 3 или 4 Fe. O∙Fe 2 O 3 + O 2 t˚ 6 Fe 2 O 3
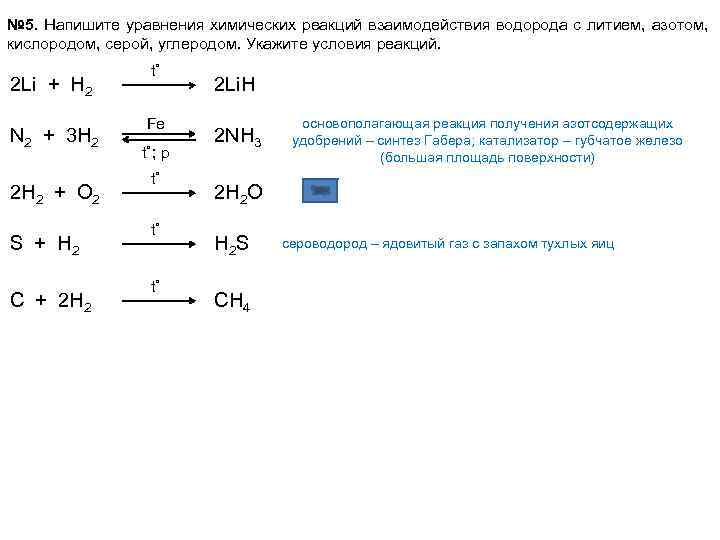 № 5. Напишите уравнения химических реакций взаимодействия водорода с литием, азотом, кислородом, серой, углеродом. Укажите условия реакций. 2 Li + H 2 N 2 + 3 H 2 2 H 2 + O 2 S + H 2 С + 2 H 2 t˚ Fe t˚; p t˚ t˚ t˚ 2 Li. H 2 NH 3 основополагающая реакция получения азотсодержащих удобрений – синтез Габера; катализатор – губчатое железо (большая площадь поверхности) 2 H 2 O H 2 S СH 4 сероводород – ядовитый газ с запахом тухлых яиц
№ 5. Напишите уравнения химических реакций взаимодействия водорода с литием, азотом, кислородом, серой, углеродом. Укажите условия реакций. 2 Li + H 2 N 2 + 3 H 2 2 H 2 + O 2 S + H 2 С + 2 H 2 t˚ Fe t˚; p t˚ t˚ t˚ 2 Li. H 2 NH 3 основополагающая реакция получения азотсодержащих удобрений – синтез Габера; катализатор – губчатое железо (большая площадь поверхности) 2 H 2 O H 2 S СH 4 сероводород – ядовитый газ с запахом тухлых яиц
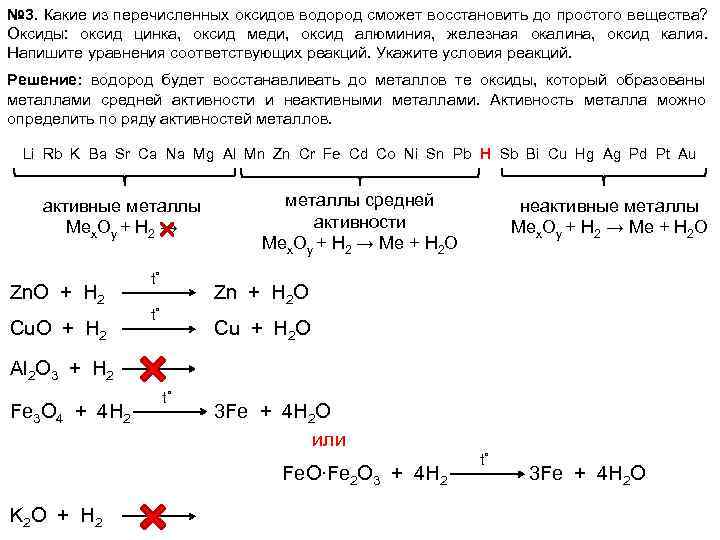 № 3. Какие из перечисленных оксидов водород сможет восстановить до простого вещества? Оксиды: оксид цинка, оксид меди, оксид алюминия, железная окалина, оксид калия. Напишите уравнения соответствующих реакций. Укажите условия реакций. Решение: водород будет восстанавливать до металлов те оксиды, который образованы металлами средней активности и неактивными металлами. Активность металла можно определить по ряду активностей металлов. Li Rb K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Cd Co Ni Sn Pb H Sb Bi Cu Hg Ag Pd Pt Au активные металлы Mex. Oy + H 2 → Zn. O + H 2 Cu. O + H 2 t˚ металлы средней активности Mex. Oy + H 2 → Me + H 2 O неактивные металлы Mex. Oy + H 2 → Me + H 2 O Zn + H 2 O t˚ Cu + H 2 O Al 2 O 3 + H 2 Fe 3 O 4 + 4 H 2 t˚ 3 Fe + 4 H 2 O или Fe. O∙Fe 2 O 3 + 4 H 2 K 2 O + H 2 t˚ 3 Fe + 4 H 2 O
№ 3. Какие из перечисленных оксидов водород сможет восстановить до простого вещества? Оксиды: оксид цинка, оксид меди, оксид алюминия, железная окалина, оксид калия. Напишите уравнения соответствующих реакций. Укажите условия реакций. Решение: водород будет восстанавливать до металлов те оксиды, который образованы металлами средней активности и неактивными металлами. Активность металла можно определить по ряду активностей металлов. Li Rb K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Cd Co Ni Sn Pb H Sb Bi Cu Hg Ag Pd Pt Au активные металлы Mex. Oy + H 2 → Zn. O + H 2 Cu. O + H 2 t˚ металлы средней активности Mex. Oy + H 2 → Me + H 2 O неактивные металлы Mex. Oy + H 2 → Me + H 2 O Zn + H 2 O t˚ Cu + H 2 O Al 2 O 3 + H 2 Fe 3 O 4 + 4 H 2 t˚ 3 Fe + 4 H 2 O или Fe. O∙Fe 2 O 3 + 4 H 2 K 2 O + H 2 t˚ 3 Fe + 4 H 2 O