fffa03d238984945bee572fa1adcab88.ppt
- Количество слайдов: 37

Реимберсмент и ценообразование в Турции Ассоциация Научно-исследовательских Фармацевтических Компаний

План q Основные направления развития системы здравоохранения Турции за прошедшие 10 лет q Рост затрат на здравоохранение q Рост потребления лекарственных средств q Развитие реимберсмента в современных условиях q Проблемы существующих стандартов оценки медицинских технологий q Недавние изменения/ решения, принятые 4 декабря q Исполнение глобального бюджета q Оценка медицинских технологий в Турции q Принципы ценообразования

Основные направления развития системы здравоохранения Турции за прошедшие 10 лет

Основные направления развития системы здравоохранения Турции за прошедшие 10 лет q Объединение государственных больниц здравоохранения (январь 2004 года) Министерства q Предоставление населению возможности получать помощь во всех медицинских учреждениях и аптеках (февраль 2005 года) q В качестве льготных услуг обладателям Зеленой карты предоставляются рецептурные лекарства (май 2005 года) q Обеспечение одинаково доступной медицинской помощи для различных слоев населения q Обобщение принципов оплаты медицинских услуг, предоставляемых частными организациями (Июнь 2007 года) q Создание единой системы медицинского страхования q Внедрение Семейной медицины
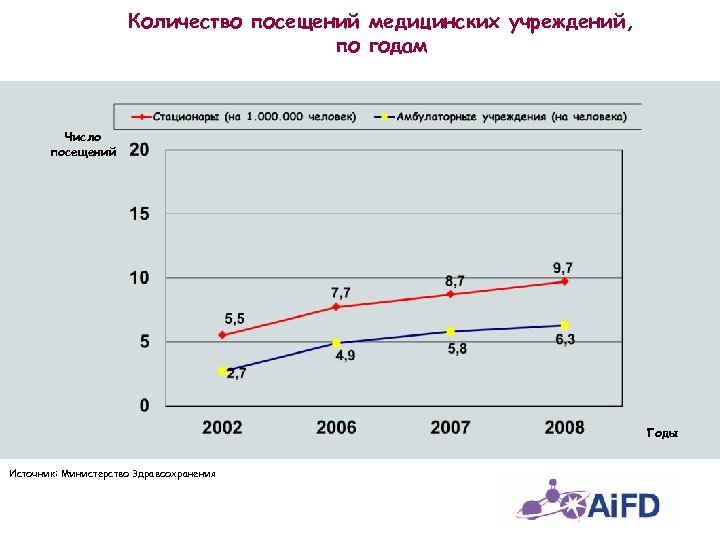
Количество посещений медицинских учреждений, по годам Число посещений Годы Источник: Министерство Здравоохранения
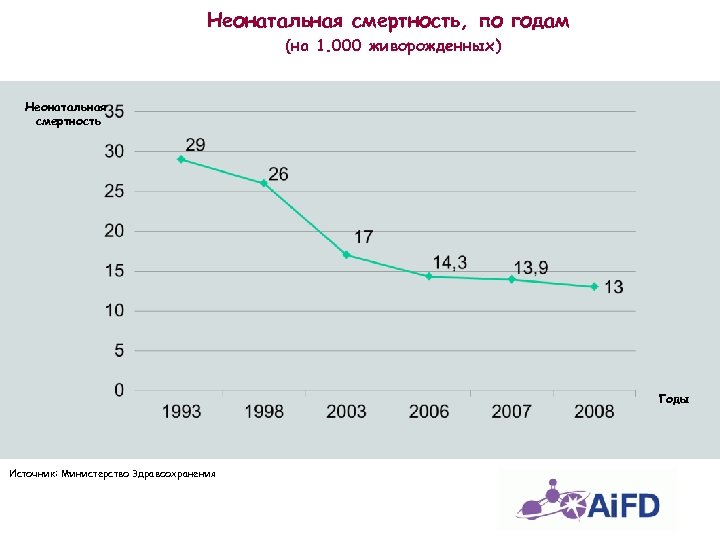
Неонатальная смертность, по годам (на 1. 000 живорожденных) Неонатальная смертность Годы Источник: Министерство Здравоохранения
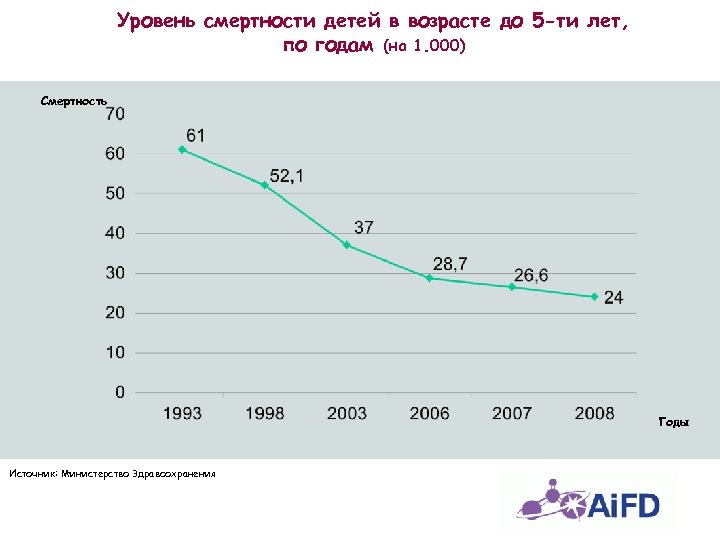
Уровень смертности детей в возрасте до 5 -ти лет, по годам (на 1. 000) Смертность Годы Источник: Министерство Здравоохранения
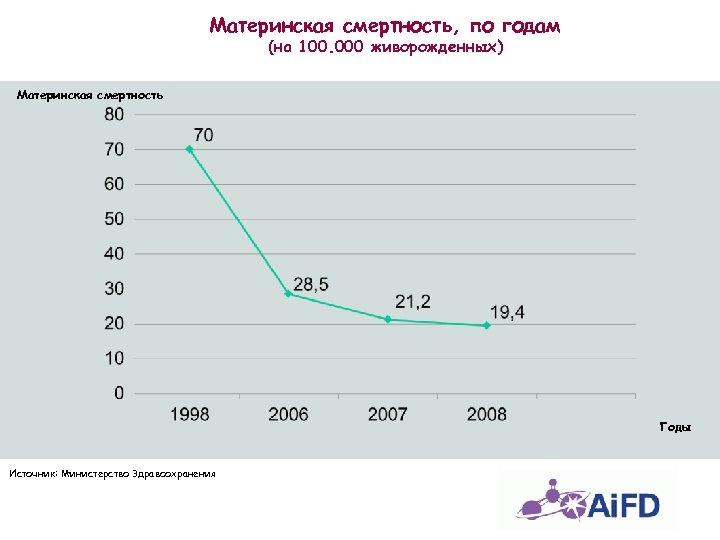
Материнская смертность, по годам (на 100. 000 живорожденных) Материнская смертность Годы Источник: Министерство Здравоохранения
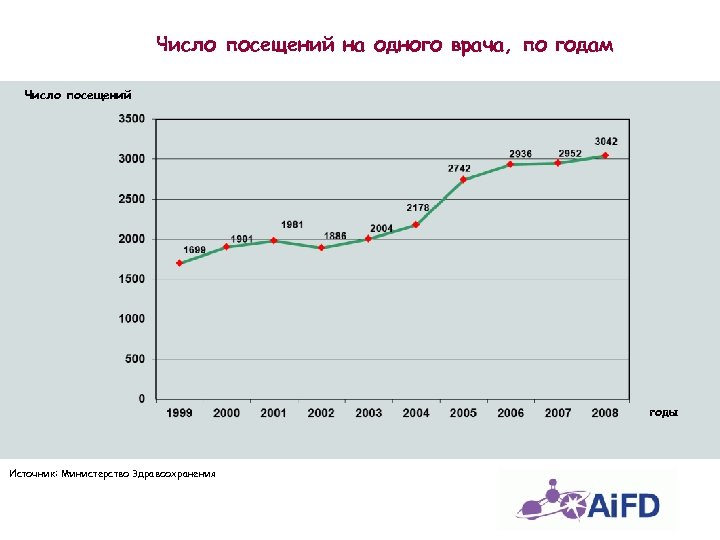
Число посещений на одного врача, по годам Число посещений годы Источник: Министерство Здравоохранения
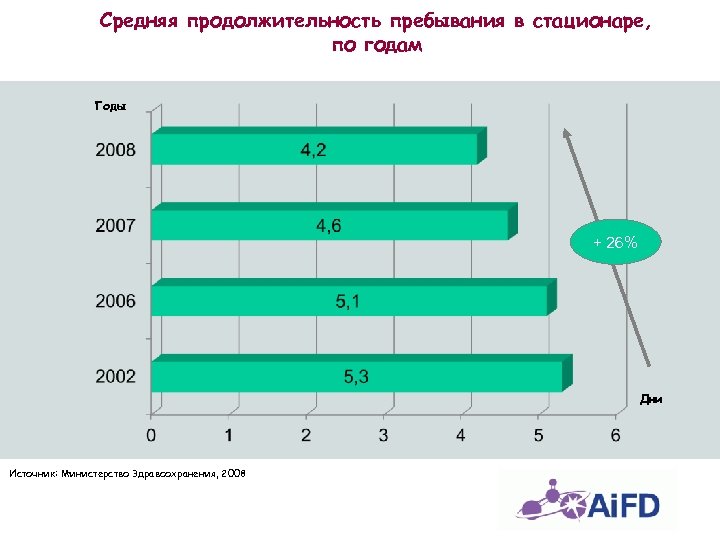
Средняя продолжительность пребывания в стационаре, по годам Годы + 26% Дни Источник: Министерство Здравоохранения, 2008
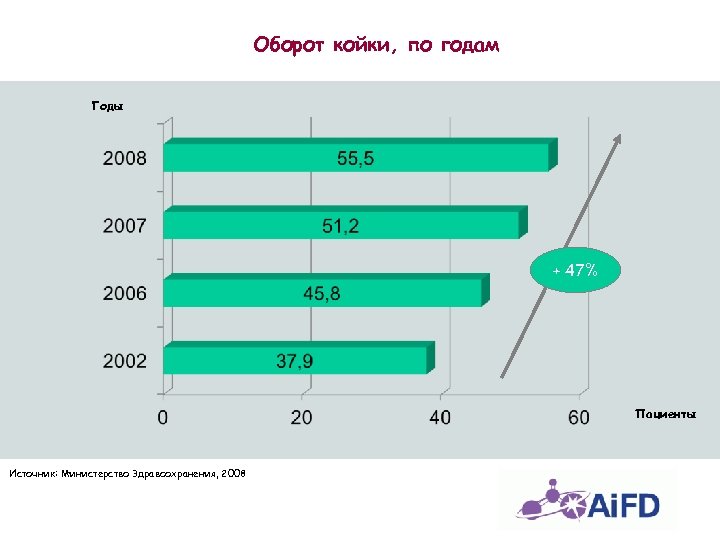
Оборот койки, по годам Годы + 47% Пациенты Источник: Министерство Здравоохранения, 2008
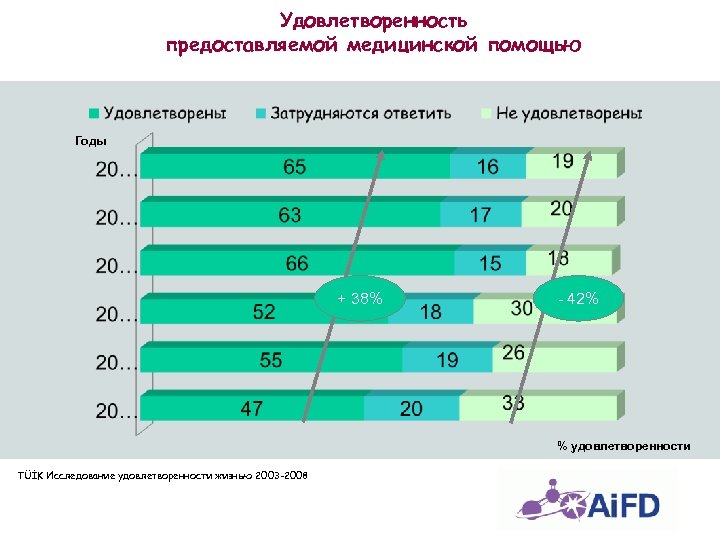
Удовлетворенность предоставляемой медицинской помощью Годы + 38% - 42% % удовлетворенности TÜİK Исследование удовлетворенности жизнью 2003 -2008
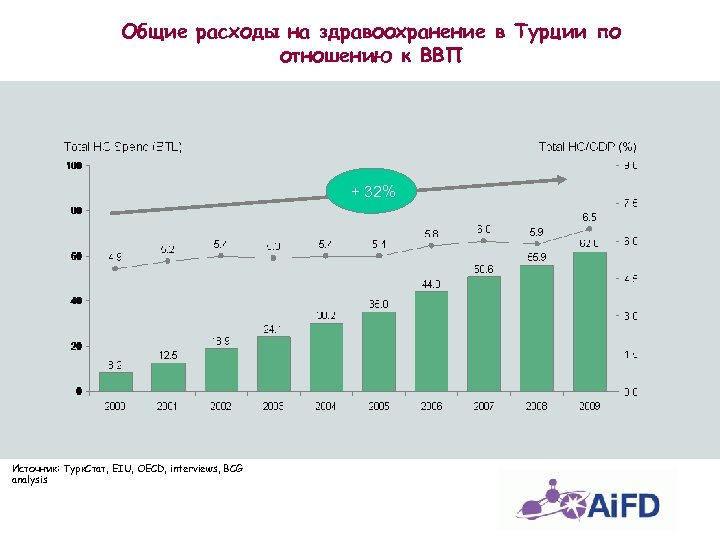
Общие расходы на здравоохранение в Турции по отношению к ВВП + 32% Источник: Турк. Стат, EIU, OECD, interviews, BCG analysis

Причины роста потребления лекарственных средств в Турции q Ведущая причина – более частое и регулярное посещение населением врачей и медицинских учреждений. В Турции частота обращения к врачу возросла с 2, 7 в 2002 году до 6, 3 в 2008 году q «Старение» населения, улучшение благосостояния, образ жизни и повышение осведомленности пациентов q Возмещение затрат на амбулаторную помощь владельцам Зеленой карты q Физиологическое повышение спроса благодаря Семейной медицине
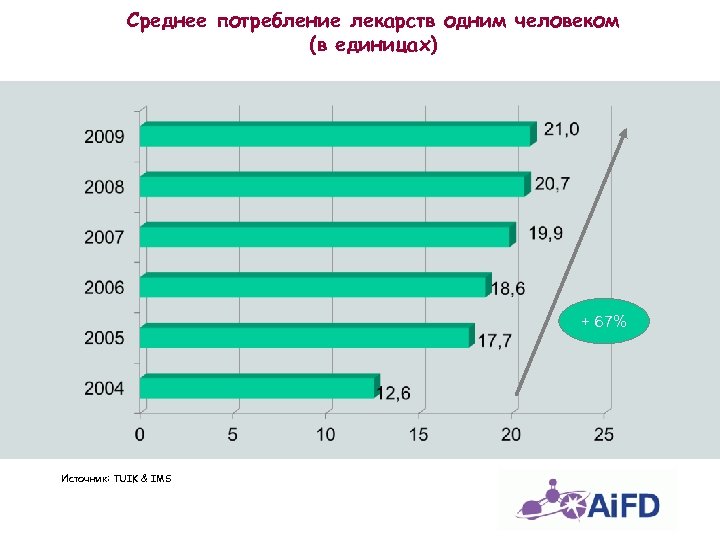
Среднее потребление лекарств одним человеком (в единицах) + 67% Источник: TUIK & IMS
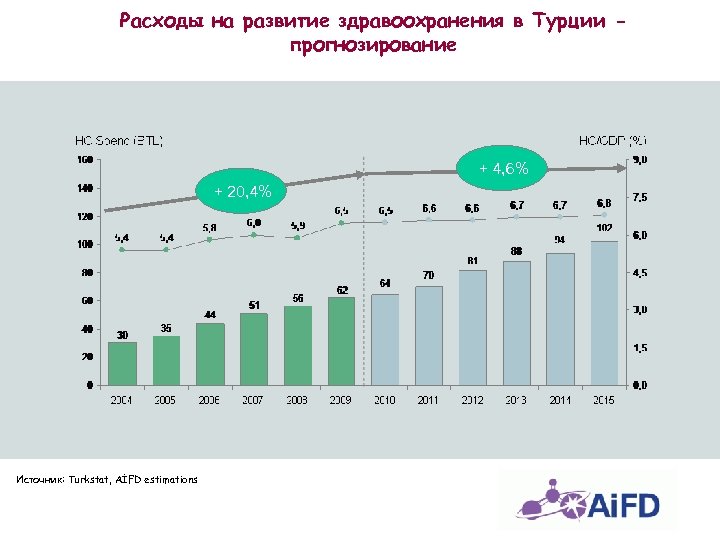
Расходы на развитие здравоохранения в Турции прогнозирование + 4, 6% + 20, 4% Источник: Turkstat, AİFD estimations

Процесс реимберсмента В Турции

Процесс реимберсмента q Институт Социального Обеспечения (называемый SGK) является ключевым игроком в новой системе оценки, так как несет ответственность за определение методов лечения и лекарств, подлежащих реимберсменту. q Фармкомпании обращаются в Институт Социального Обеспечения с целью определения статуса Реимберсмента фармацевтических препаратов. q Помимо Института Социального Обеспечения в процесс реимберсмента заинтересованы Министерство Финансов, Министерство здравоохранения, Организация Государственного Планирования, Подсекретариат Казначейства, KOLs и представители фарминдустрии.

Процесс реимберсмента ü Представленные продукты в первую очередь оцениваются Комиссией по Медицинской и Экономической Оценке, окончательное решение принимает Комиссия по Реимбесрменту. ü Окончательный пересмотренный список оглашается после официального утверждения Главой SGK. ü В Турции время с момента подачи заявки на Реимберсмент до принятия окончательного решения, как правило, составляет 1 год, что также является причиной задержки появления на рынке.

Документы, необходимые для подачи заявки Фармкомпании обращаются в Институт Социального Обеспечения с целью определения статуса Реимберсмента фармацевтических препаратов. Помимо письменного заявления. Необходимо предоставить: • Разрешение FDA на продажу и регистрационный номер препарата, • Разрешение EMA на продажу и сертификат по совместному маркетингу, • Нормативный статус в странах ОЭСР • Клинические данные • Безопасность • Эффект Фармакоэкономические сведения – Должен быть проведен фармакоэкономический анализ, к которому должен прилагаться соответствующий анализ чувствительности. – Должно быть проведено сравнение с наиболее часто используемым альтернативным продуктом. – В качестве приложения к фармакоэкономического анализа должны быть представлены анализ «затраты-эффективность» , «минимизация затрат» , «затраты-полезность (могут быть представлены заявителем). – Модель воздействия бюджета для плательщика
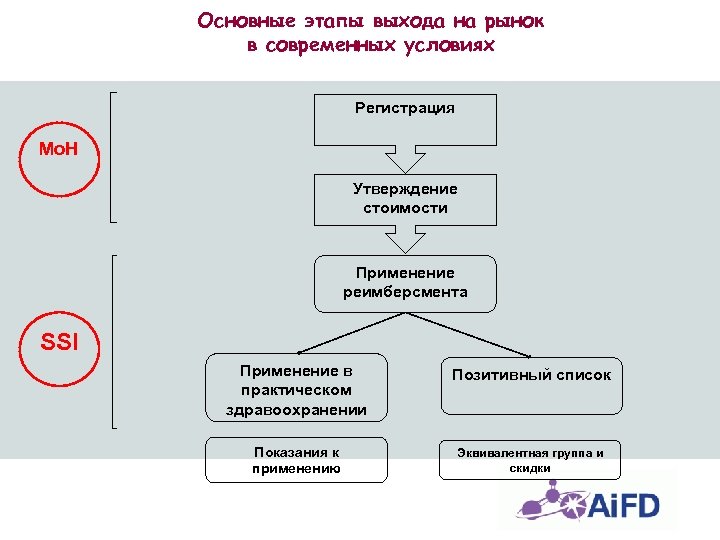
Основные этапы выхода на рынок в современных условиях Регистрация Mo. H Утверждение стоимости Применение реимберсмента SSI Применение в практическом здравоохранении Позитивный список Показания к применению Эквивалентная группа и скидки
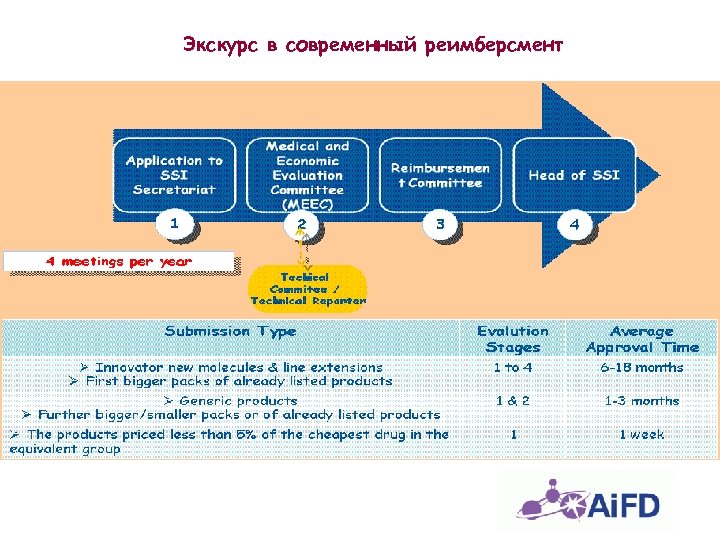
Экскурс в современный реимберсмент

Характеристика современной модели оценки Позитивные аспекты современной системы оценки q Позволяет представителям производителей принимать участие в процессе. Негативные аспекты современной системы оценки q SGK сравнивает стоимость препарата с альтернативными вариантами и не оценивает общую стоимость лечения. q Сравнительная оценка медицинских изделий с терапевтическими альтернативами в современных условиях SGK не используется. q Результаты фармакоэкономического анализа в досье препарата при обсуждении во внимание не принимаются. q Обсуждение влияния бюджета оказывает решающее влияние принятии решения.

Ведение глобального бюджета В Турции

ГЛОБАЛЬНЫЙ БЮДЖЕТ Правительство обещает предоставить 7% рост в течение последующих 3 лет

Протокол Глобального Бюджета: ценообразование УКАЗ Оригинальные препараты и их дженерики – 66% от референтной цены Оригинальные препараты без дженериков – 23% (базовая скидка 11% + 12%) Референтные цены будут применяться в течение 20 лет (дополнительная скидка 13% до получения референтной цены)

Протокол Глобального Бюджета, закупки q Для внедрения новых молекул и инновационных препаратов на рынок будет предусмотрена скидка 11% с целью включения в Список лекарств, которые подлежат реимберсменту. q В период с 2010 по 2012 год планируется внедрение среднесрочной программы финансирования, терапевтическая эквивалентность применяться не будет.

Если фактические расходы превышают бюджет На первом этапе; скидка на оригинальный препарат, не имеющий дженерика, возрастет на 13%. На втором этапе; уровень референтных цен на оригинальные препараты и их дженерики постепенно будет снижен с 66 до 60%.
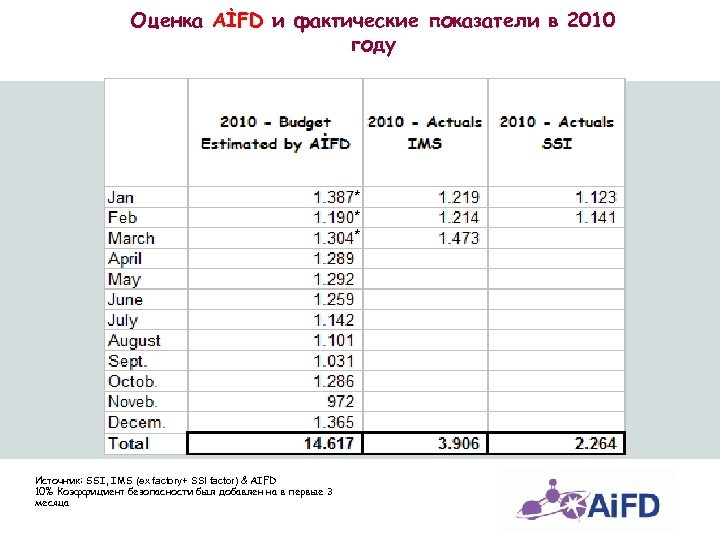
Оценка AİFD и фактические показатели в 2010 году * * * Источник: SSI, IMS (ex factory+ SSI factor) & AIFD 10% Коэффициент безопасности был добавлен на в первые 3 месяца
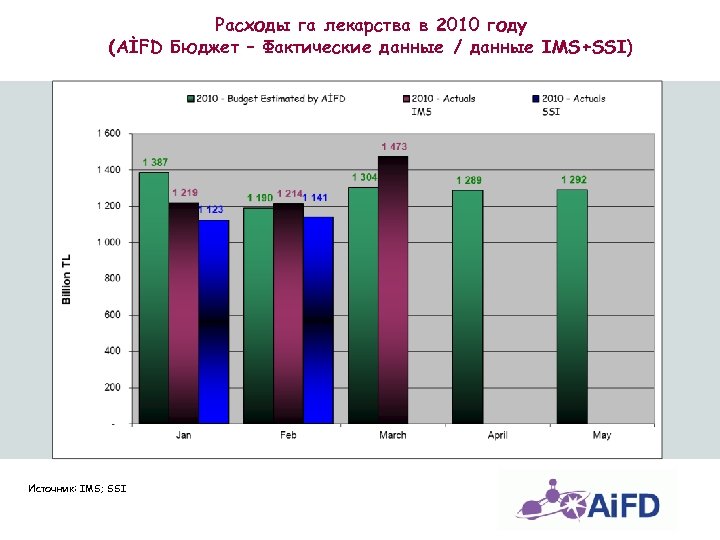
Расходы га лекарства в 2010 году (AİFD Бюджет – Фактические данные / данные IMS+SSI) January Источник: IMS; SSI February March April

Ценообразование в Турции

Ценообразование в Турции/ Условия до 4 декабря 2009 года – (1) Ценообразование было основано на внешних данных: Цена завода-производителя определяется министерством здравоохранения на основании перечисленных ниже признаков: * Цена в 5 сравниваемых стран (Франция, Греция, Италия, Испания и Португалия) / 31 августа * цена в стане, из которой был привезен данный препарат * Цена в стране, в которой был произведен данный препарат (место выпуска) *Если препарат не продается в указанных выше странах, самая низкая STS в ЕС. Ценообразование, основанное на внутренних данных: Объем Реимберсмента определяется Учреждениями по Социальной Защите, принимая во внимание стоимость эквивалентных препаратов с аналогичными показаниями к применению.

Ценообразование в Турции/ Условия до 4 декабря 2009 года – (2) • Любые изменения, происходящие в Турции, превышающие 3% вследствиеснижения референтной цены, доводятся до сведения Минздрава и отражаются на ценах в течение последующих 3 месяцев. • В отношении оригинальных препаратов: компании могут претендовать на сумму до 100% от референтной цены. • В отношении дженериков: компании могут претендовать на сумму до 80% от референтной цены. • Производители как оригинальных препаратов, так и дженериков могут претендовать на определенную цену. • 20 -летние препараты: препараты, впервые появившиеся на мировом рынке лекарственных средств до 1. 08. 1987 года, исключены из системы референтных цен, поддерживается их нынешняя цена. • Снижение цен не распространяется на препараты с ценой ниже 3 лир
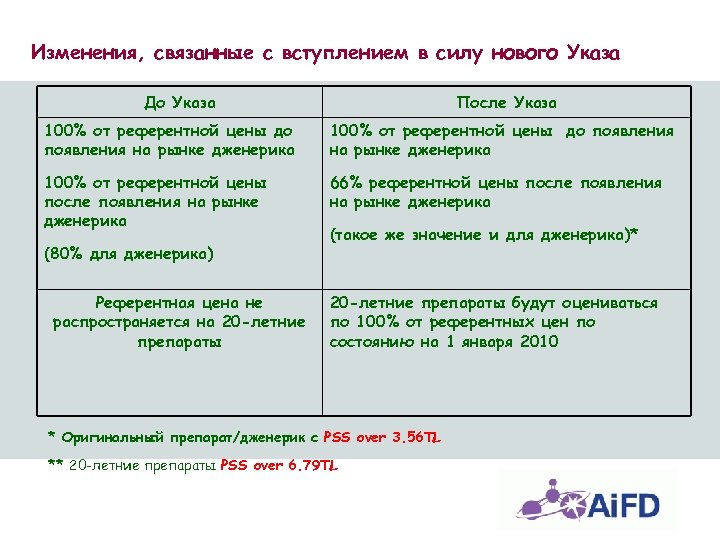
Изменения, связанные с вступлением в силу нового Указа До Указа После Указа 100% от референтной цены до появления на рынке дженерика 100% от референтной цены после появления на рынке дженерика 66% референтной цены после появления на рынке дженерика (80% для дженерика) Референтная цена не распространяется на 20 -летние препараты (такое же значение и для дженерика)* 20 -летние препараты будут оцениваться по 100% от референтных цен по состоянию на 1 января 2010 * Оригинальный препарат/дженерик с PSS over 3. 56 TL ** 20 -летние препараты PSS over 6. 79 TL

Оценка медицинских технологий в Турции q Для Турции это новая концепция q. Были разработаны 3 различных модели (SSI, Hacettepe Uni and AIFD) q AIFD’s предложение основано на улучшении терапевтических качеств, бремени заболевания, фаармакоэкономической оценке и влиянии бюджета q Сотрудничество всех заинтересованных сторон будет иметь важнейшее значение для внедрение наилучшей для Турции модели q AİFD and SGK создадут платформу для обеспечения взаимосвязи принципов и терминологии. На втором этапе мы планируем начать создание устойчивой специфичной для Турции модели.

Резервный слайд

Комиссия по Медицинской и Экономической Оценке q В состав Комиссии по Медицинской и Экономической Оценке входит 13 членов: . 4 члена от Института Социального Обеспечения , 2 от Министерства Здравоохранения, по 1 от Министерства Финансов, Организации Государственного Планирования и Подсекретариата Казначейства, 2 фармаколога и 2 представителя фармпромышленности являются постоянными членами Комиссии. q Расписание заседаний должны быть объявлено в начале каждого года, Комиссия заседает 4 раза в год. Решения принимаются на основе голосования, все участники, включая представителей фарминдустрии. Имеют один голос. q После заседания Комиссии по Медицинской и Экономической Оценке окончательное решение принимает Комиссия по Реимбесрменту по представлению Комиссии по Оценке. Окончательный пересмотренный список оглашается после официального утверждения Главой SGK.
fffa03d238984945bee572fa1adcab88.ppt