Везикулярный транспорт lecture1-introduction.ppt
- Количество слайдов: 36

РЕГУЛЯЦИЯ ВЕЗИКУЛЯРНОГО ТРАНСПОРТА Елена Сергеевна Корнилова Лаборатория динамики внутриклеточных мембран Институт цитологии РАН, С. -Петербург
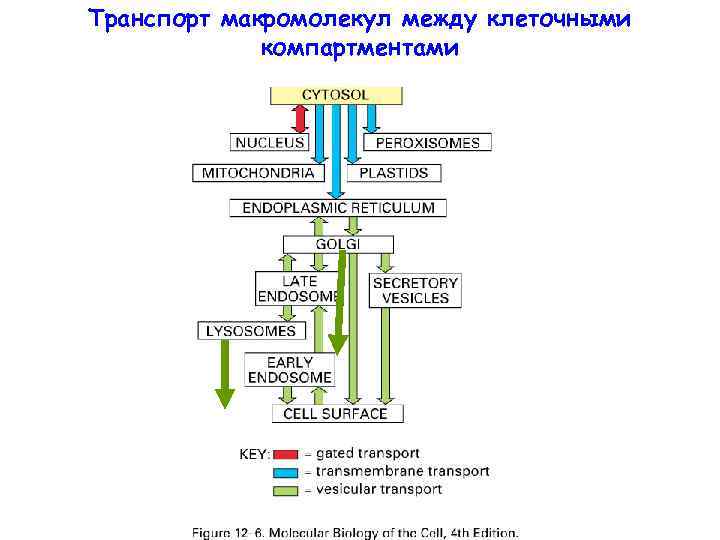
Транспорт макромолекул между клеточными компартментами

Press Release The Nobel Assembly at Karolinska Institutet has today decided to award The 2013 Nobel Prize in Physiology or Medicine jointly to James E. Rothman, Randy W. Schekman and Thomas C. Südhof for their discoveries of machinery regulating vesicle traffic, major transport system in our cells traffic The three Nobel Laureates have discovered the molecular principles that govern how this cargo is delivered to the right place at the right time in the cell.

Везикулярный транспорт – это перенос макромолекул-грузов, «упакованных» в мембранные пузырьки, или везикулы, от одного мембранного компартмента клетки к другому. Грузами могут быть как белки, так и липиды В этом процессе участвуют все мембранные компартменты, кроме митохондрий

Компартмент: Имеет характерную морфологию, постоянный липидно-белковый состав, выполняет набор определенных функций существует постоянно ( preexisting) – стабилен Транспортная везикула: Несет груз, возникает на мембране компартмента-донора и исчезает после слияния с компартментом-мишенью
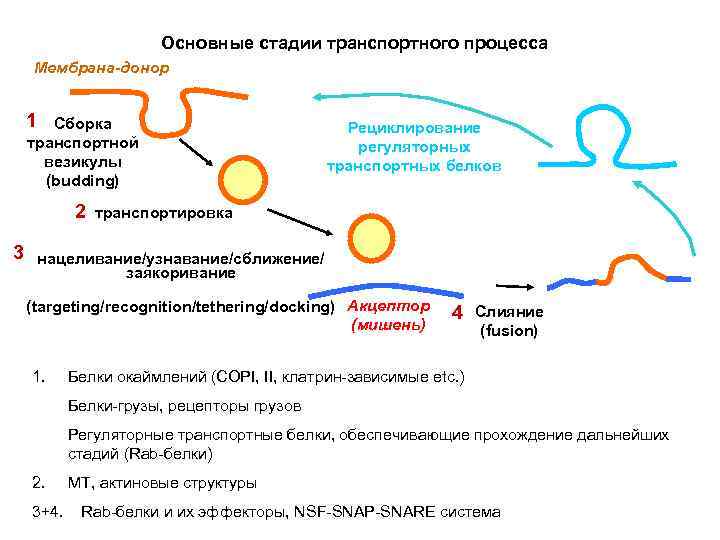
Основные стадии транспортного процесса Мембрана-донор 1 Сборка транспортной везикулы (budding) 2 3 Рециклирование регуляторных транспортных белков транспортировка нацеливание/узнавание/сближение/ заякоривание (targeting/recognition/tethering/docking) Акцептор (мишень) 1. 4 Слияние (fusion) Белки окаймлений (COPI, II, клатрин-зависимые etc. ) Белки-грузы, рецепторы грузов Регуляторные транспортные белки, обеспечивающие прохождение дальнейших стадий (Rab-белки) 2. 3+4. МТ, актиновые структуры Rab-белки и их эффекторы, NSF-SNAP-SNARE система
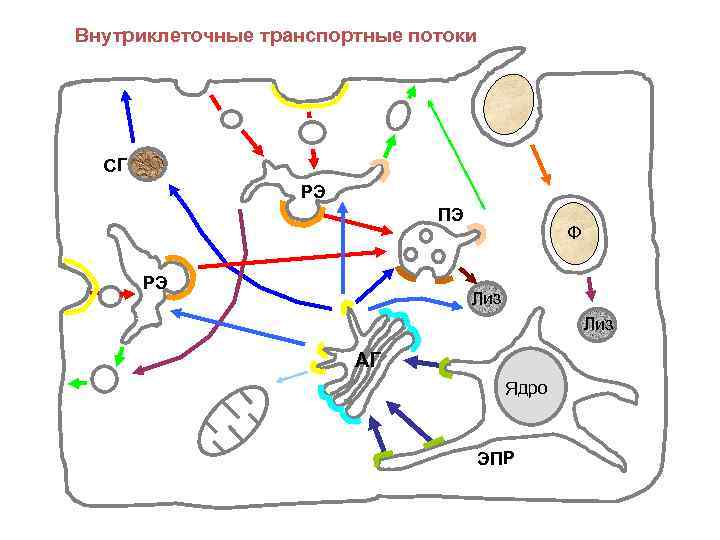
Внутриклеточные транспортные потоки СГ РЭ ПЭ РЭ Ф Лиз АГ Ядро ЭПР
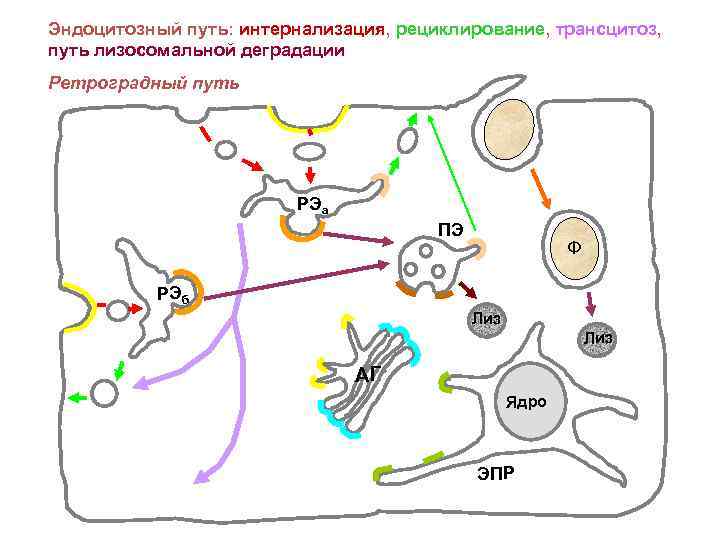
Эндоцитозный путь: интернализация, рециклирование, трансцитоз, путь лизосомальной деградации Ретроградный путь РЭа ПЭ Ф РЭб Лиз АГ Ядро ЭПР
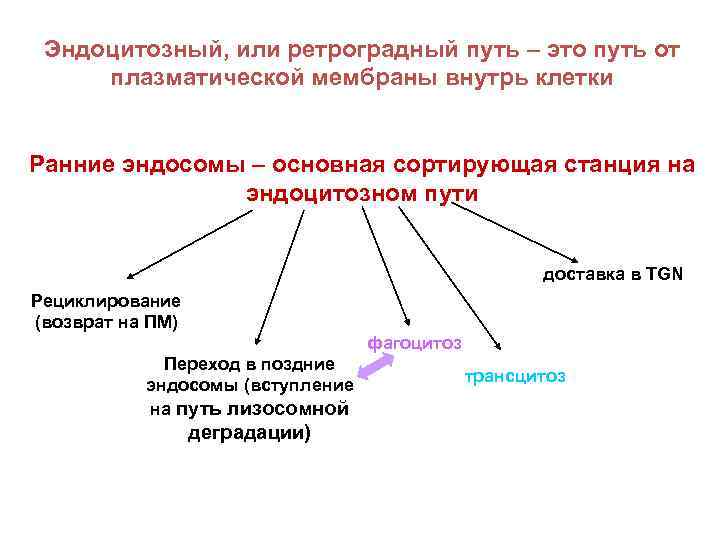
Эндоцитозный, или ретроградный путь – это путь от плазматической мембраны внутрь клетки Ранние эндосомы – основная сортирующая станция на эндоцитозном пути доставка в TGN Рециклирование (возврат на ПМ) фагоцитоз Переход в поздние эндосомы (вступление на путь лизосомной деградации) трансцитоз
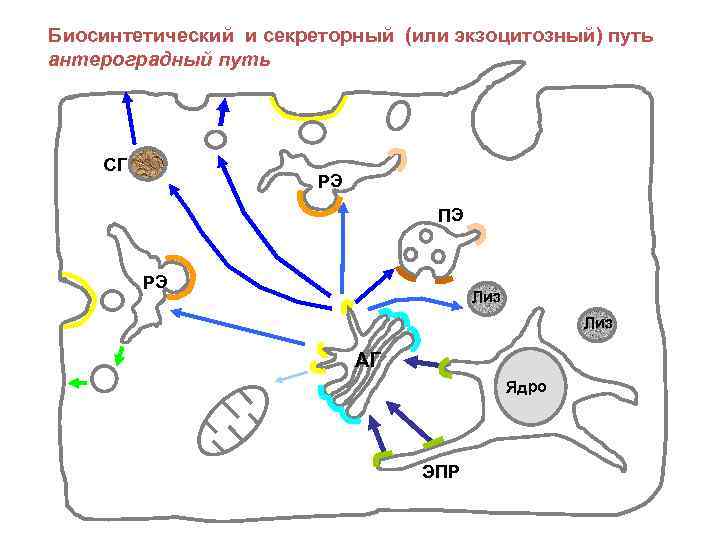
Биосинтетический и секреторный (или экзоцитозный) путь антероградный путь СГ РЭ ПЭ РЭ Лиз АГ Ядро ЭПР
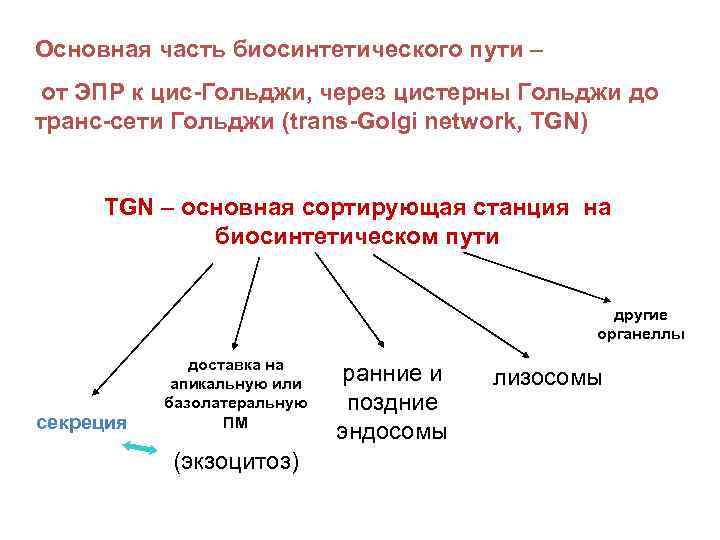
Основная часть биосинтетического пути – от ЭПР к цис-Гольджи, через цистерны Гольджи до транс-сети Гольджи (trans-Golgi network, TGN) TGN – основная сортирующая станция на биосинтетическом пути другие органеллы секреция доставка на апикальную или базолатеральную ПМ (экзоцитоз) ранние и поздние эндосомы лизосомы

В ходе везикулярного транспорта идет постоянный процесс сортировки компонентов мембран: т. наз. резидентные компоненты удерживаются в мембране органеллы, тогда как компоненты- «грузы» исключаются из нее пример: аппарат Гольджи При огромном потоке синтезированных de novo белков, перемещающихся из цис-цистерн в транс-цистерны, сами цистерны сохраняют свою идентичность (т. е. определенный набор белков и липидов)

Тонко отлаженный баланс транспортных потоков “in-out” позволяет нам думать, что в клетке существуют стабильные компартменты на самом деле они являются высокодинамическими структурами
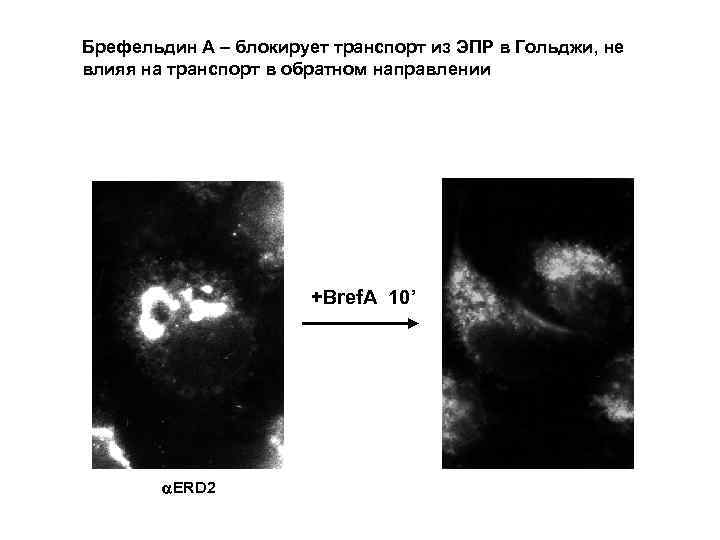
Брефельдин А – блокирует транспорт из ЭПР в Гольджи, не влияя на транспорт в обратном направлении +Bref. A 10’ ERD 2
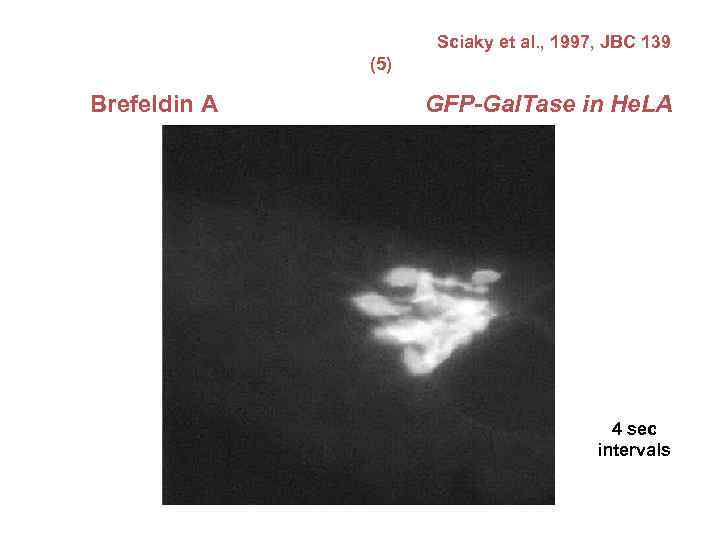
Sciaky et al. , 1997, JBC 139 (5) Brefeldin A GFP-Gal. Tase in He. LA 4 sec intervals

Sciaky et al. , 1997, JBC 139 (5) Brefeldin A В присутствии микротрубочек GFP-Gal. Tase in He. LA МТ разобраны Нокодазолом Брефельдин А – блокирует транспорт из ЭПР в Гольджи, не влияя на транспорт в обратном направлении
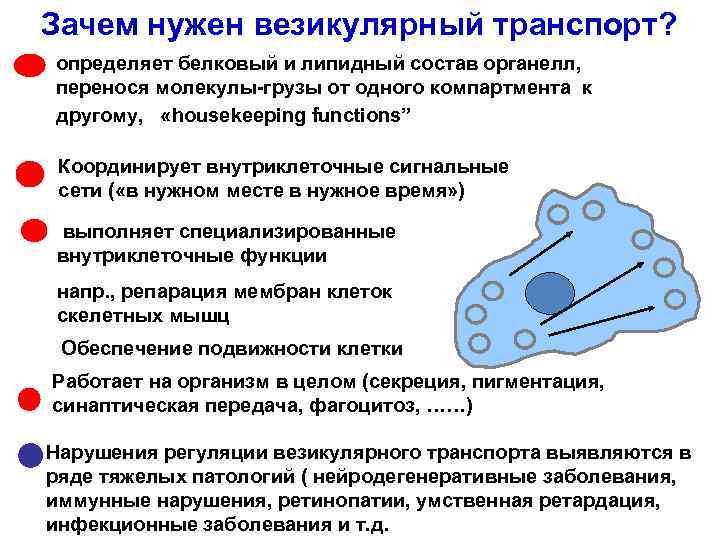
Зачем нужен везикулярный транспорт? определяет белковый и липидный состав органелл, перенося молекулы-грузы от одного компартмента к другому, «housekeeping functions” Координирует внутриклеточные сигнальные сети ( «в нужном месте в нужное время» ) выполняет специализированные внутриклеточные функции напр. , репарация мембран клеток скелетных мышц Обеспечение подвижности клетки Работает на организм в целом (секреция, пигментация, синаптическая передача, фагоцитоз, ……) Нарушения регуляции везикулярного транспорта выявляются в ряде тяжелых патологий ( нейродегенеративные заболевания, иммунные нарушения, ретинопатии, умственная ретардация, инфекционные заболевания и т. д.
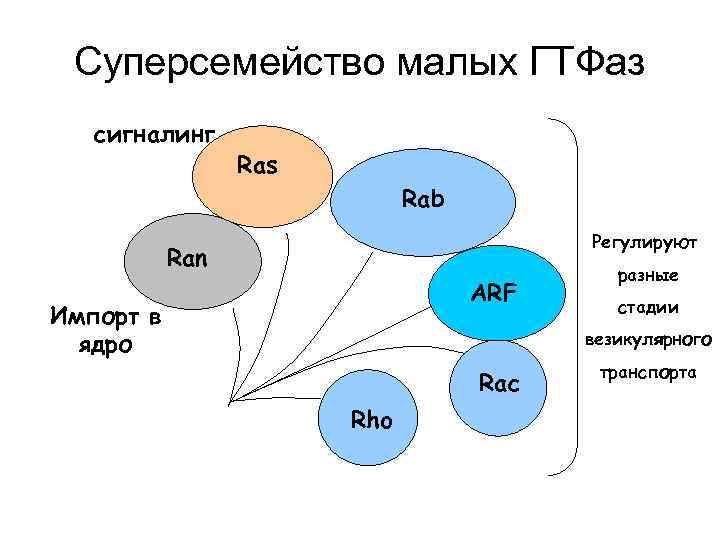
Суперсемейство малых ГТФаз сигналинг Ras Rab Регулируют Ran ARF Импорт в ядро разные стадии везикулярного Rac Rho транспорта
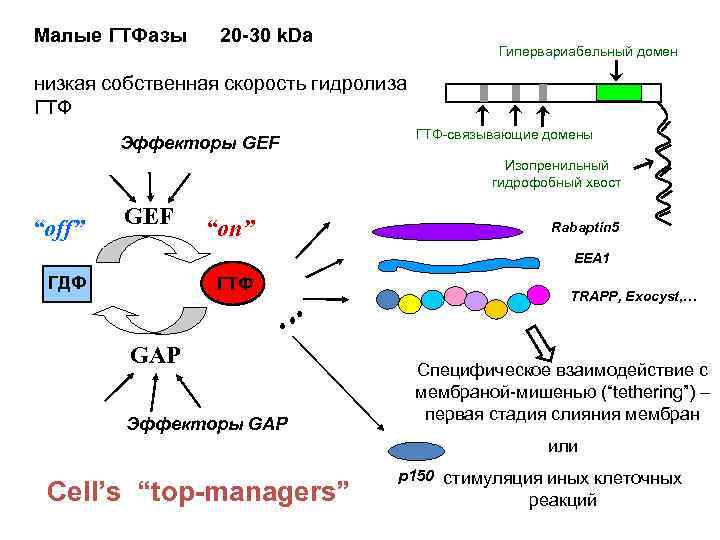
Малые ГТФазы 20 -30 k. Da Гипервариабельный домен низкая собственная скорость гидролиза ГТФ Эффекторы GEF ГТФ-связывающие домены Изопренильный гидрофобный хвост “off” GEF “on” Rabaptin 5 EEA 1 ГДФ ГТФ GAP Эффекторы GAP TRAPP, Exocyst, … Специфическое взаимодействие с мембраной-мишенью (“tethering”) – первая стадия слияния мембран или Cell’s “top-managers” p 150 стимуляция иных клеточных реакций

МЕТОДЫ 1. Микроскопия (флуоресцентная, электронная) 2. Фракционирование (дифференциальное, в градиентах плотности 3. Биохимические методы 4. Системы in vitro Генно-инженерные подходы Методы системной биологии, моделирование
Генно-инженерные методы : мутантные формы белков Нокауты si. RNA Флуоресцентные методы Окраска антителами фиксированных клеток конструкции «белок-GFP» комплексы лигандов с флуорофорами (Cy 3 Alexa, QDs)
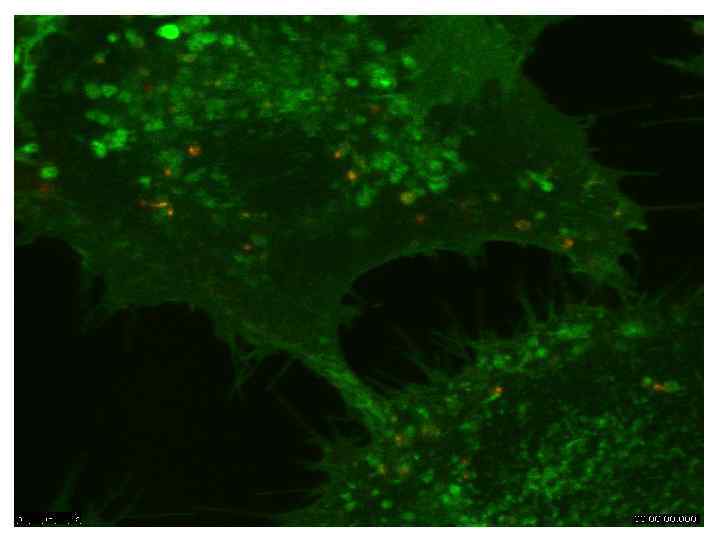
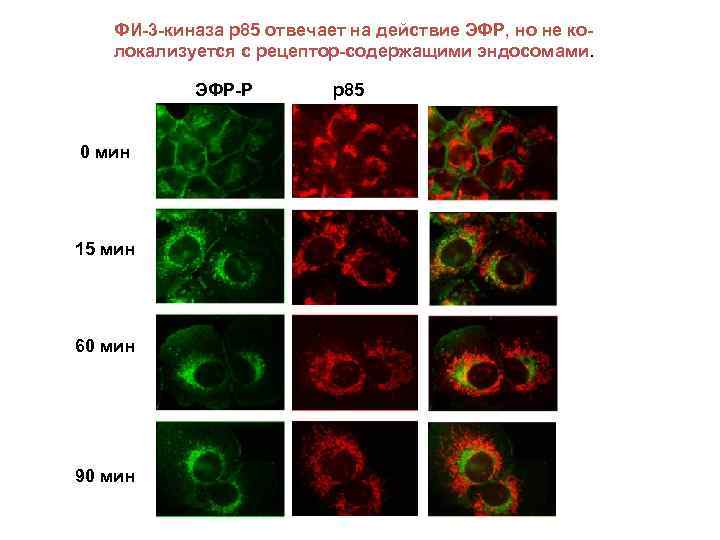
ФИ-3 -киназа р85 отвечает на действие ЭФР, но не колокализуется с рецептор-содержащими эндосомами. ЭФР-Р 0 мин 15 мин 60 мин 90 мин р85
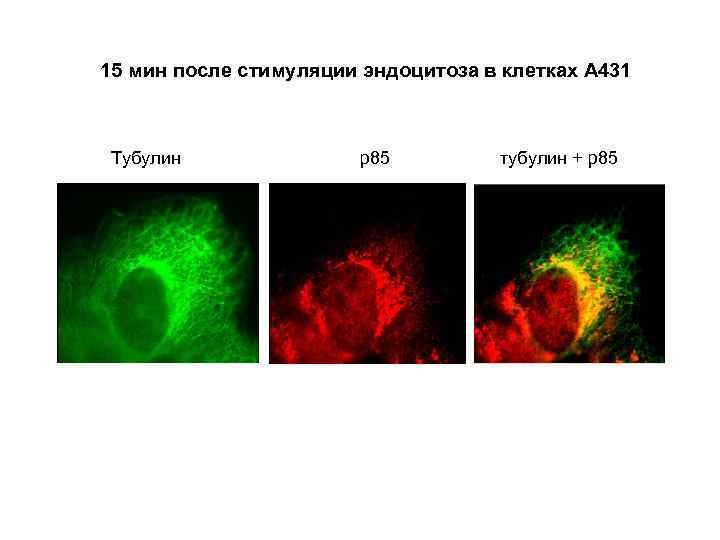
15 мин после стимуляции эндоцитоза в клетках А 431 Тубулин р85 тубулин + р85
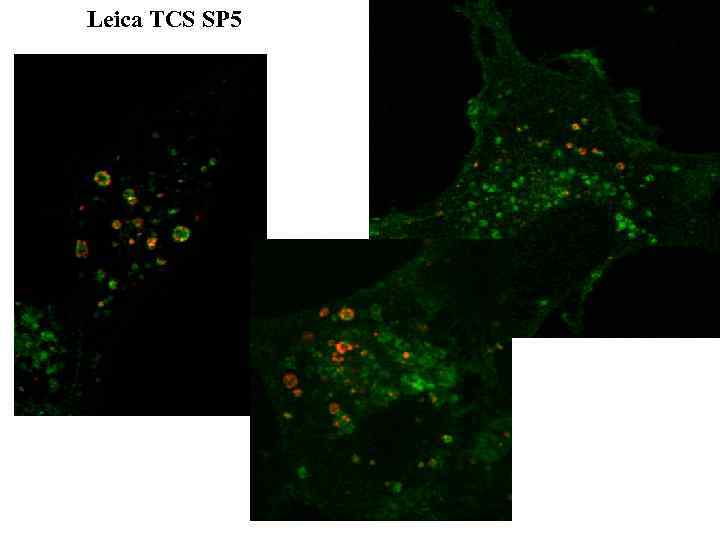
Leica TCS SP 5
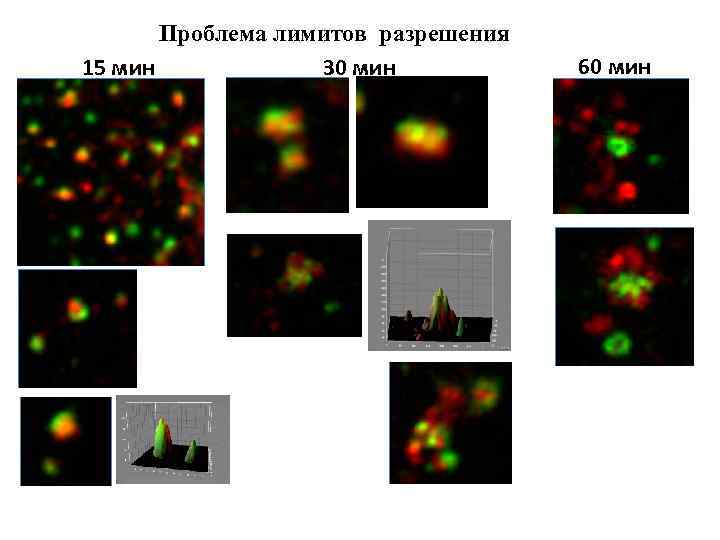
Проблема лимитов разрешения 15 мин 30 мин 60 мин
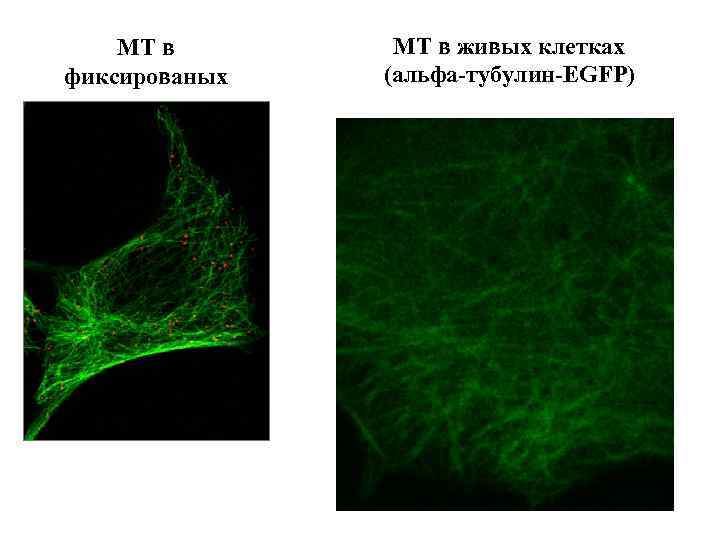
МТ в фиксированых клетках МТ в живых клетках (альфа-тубулин-EGFP)

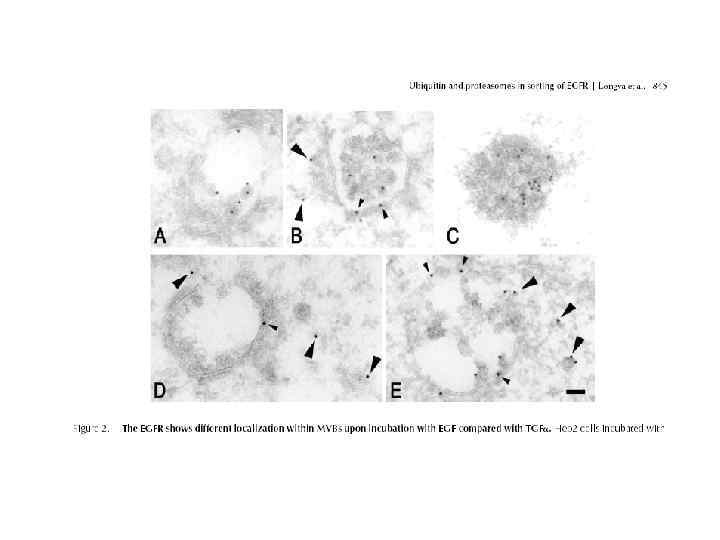
Электронная микроскопия: тонкая структура, но маленькое поле; артефакты при обработке ЭФР-ФЭ 15 мин 37 о. С ЭФР-ПХ, N ЭФР-ФЭ 15 мин 37 о. С, 3 ч 18 о. С
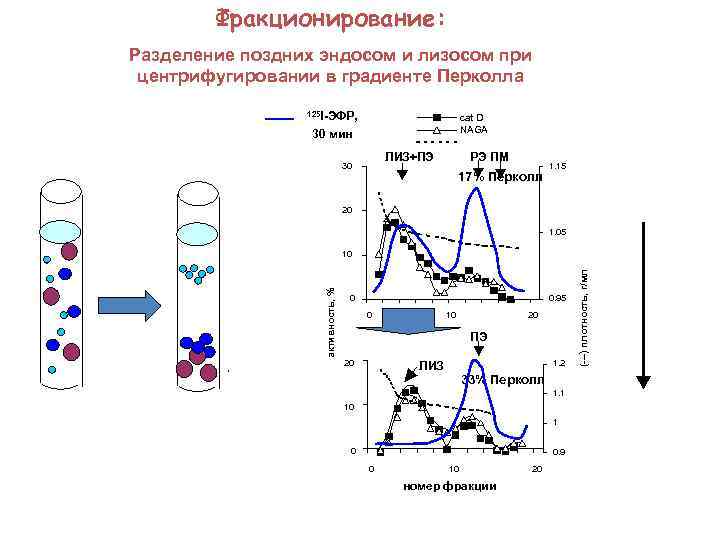
Фракционирование: Разделение поздних эндосом и лизосом при центрифугировании в градиенте Перколла 125 I-ЭФР, cat D NAGA 30 мин ЛИЗ+ПЭ 30 РЭ ПМ 17% Перколл 1. 15 20 1. 05 0 0. 95 0 10 20 ПЭ 20 1. 2 ЛИЗ 33% Перколл 1. 1 10 1 0 0. 9 0 10 номер фракции 20 (---) плотность, г/мл активность, % 10
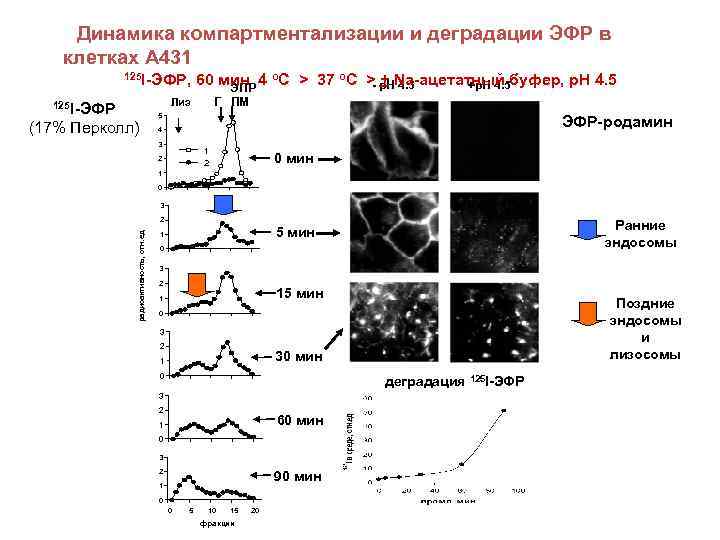
Динамика компартментализации и деградации ЭФР в клетках А 431 125 I-ЭФР, 60 мин 4 о. С > 37 о. С > р. НNa-ацетатный буфер, р. Н 4. 5 - + 4. 5 +р. Н 4. 5 ЭПР Г ПМ Лиз 125 I-ЭФР (17% Перколл) 5 ЭФР-родамин 4 3 1 2 2 0 мин 1 0 3 радиоактивность, отн. ед 2 Ранние эндосомы 5 мин 1 0 3 2 15 мин 1 Поздние эндосомы и лизосомы 0 3 2 30 мин 1 0 деградация 125 I-ЭФР 3 2 60 мин 1 0 3 2 90 мин 1 0 0 5 10 15 фракции 20
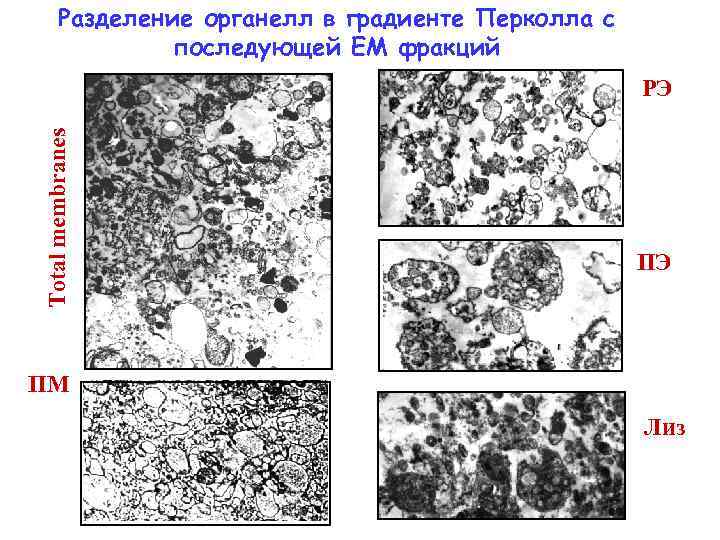
Разделение органелл в градиенте Перколла с последующей ЕМ фракций Total membranes РЭ ПЭ ПМ Лиз

Степень ассоциации Rab 7 c ПЭ коррелирует с эффективностью сортировки рецептора ЭФР- Р Rab 7 РЭ ПЭ+Л
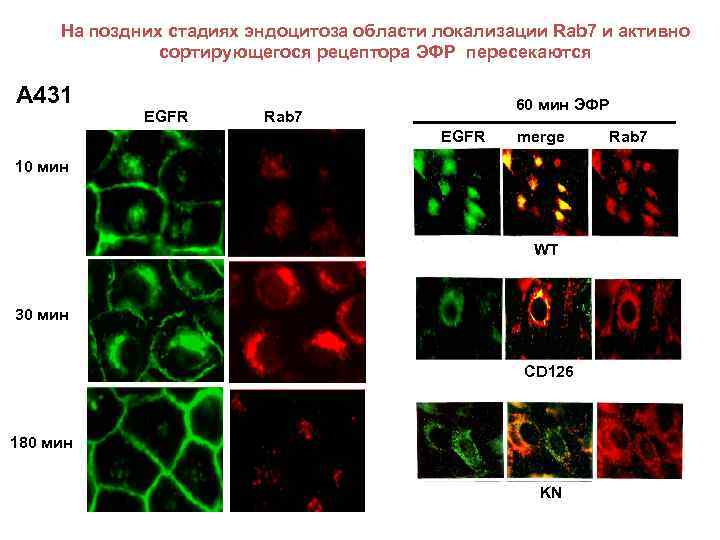
На поздних стадиях эндоцитоза области локализации Rab 7 и активно сортирующегося рецептора ЭФР пересекаются А 431 EGFR 60 мин ЭФР Rab 7 EGFR merge 10 мин WT 30 мин CD 126 180 мин KN Rab 7
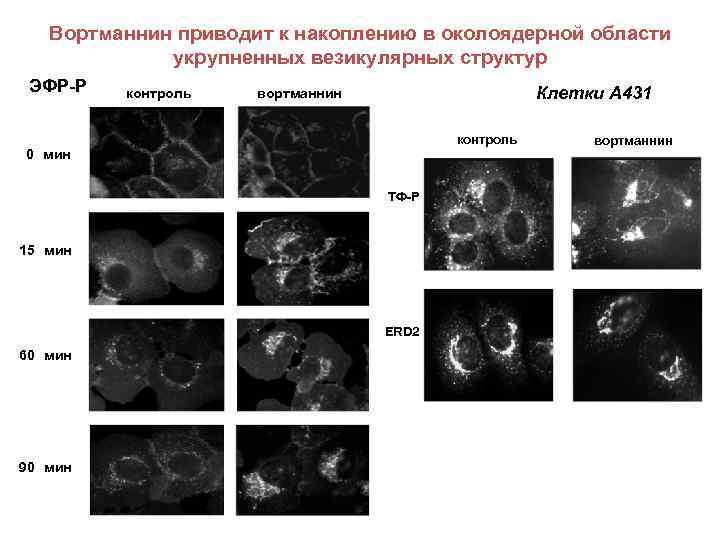
Вортманнин приводит к накоплению в околоядерной области укрупненных везикулярных структур ЭФР-Р контроль Клетки А 431 вортманнин контроль 0 мин ТФ-Р 15 мин ERD 2 60 мин 90 мин вортманнин

Везикулярный транспорт lecture1-introduction.ppt