РЕГУЛЯЦИЯ ГЛИКОЛИЗА И ГЛЮКОНЕОГЕНЕЗА.ppt
- Количество слайдов: 31
 РЕГУЛЯЦИЯ ГЛИКОЛИЗА И ГЛЮКОНЕОГЕНЕЗА В ПЕЧЕНИ
РЕГУЛЯЦИЯ ГЛИКОЛИЗА И ГЛЮКОНЕОГЕНЕЗА В ПЕЧЕНИ
 В печени, в отличие от других тканей, могут происходить два противоположно направленных процесса гликолиз и глюконеогенез. Эти процессы имеют разное биологическое значение, поэтому скорость каждого из них определяется физиологическим состоянием организма. Основную роль в регуляции синтеза и катаболизма глюкозы играют доступность субстратов, энергетический потенциал и гормоны (инсулин, глюкагон и кортизол). Действие этих гормонов направлено на изменение скорости необратимых реакций гликолиза и глюконеогенеза, которые образуют три субстратных цикла. Скорость реакций субстратных циклов зависят от активности ферментов, которые их катализируют.
В печени, в отличие от других тканей, могут происходить два противоположно направленных процесса гликолиз и глюконеогенез. Эти процессы имеют разное биологическое значение, поэтому скорость каждого из них определяется физиологическим состоянием организма. Основную роль в регуляции синтеза и катаболизма глюкозы играют доступность субстратов, энергетический потенциал и гормоны (инсулин, глюкагон и кортизол). Действие этих гормонов направлено на изменение скорости необратимых реакций гликолиза и глюконеогенеза, которые образуют три субстратных цикла. Скорость реакций субстратных циклов зависят от активности ферментов, которые их катализируют.
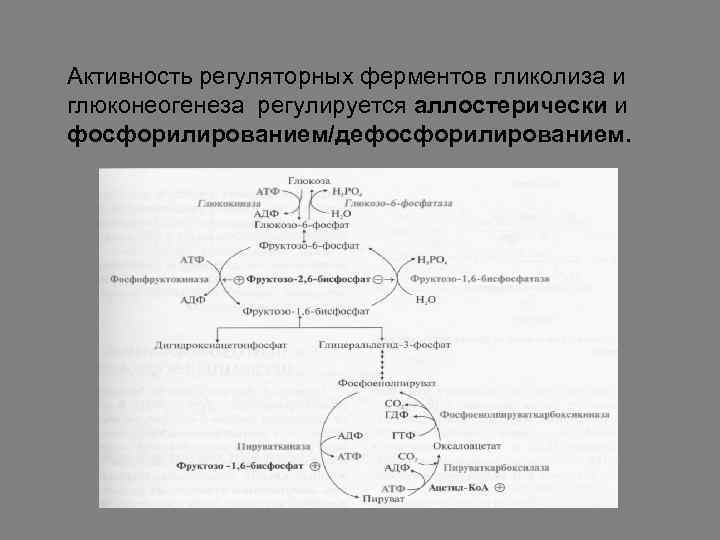 Активность регуляторных ферментов гликолиза и глюконеогенеза регулируется аллостерически и фосфорилированием/дефосфорилированием.
Активность регуляторных ферментов гликолиза и глюконеогенеза регулируется аллостерически и фосфорилированием/дефосфорилированием.
 При повышении уровня глюкозы в крови ускоряются реакции гликолиза и снижаются реакции глюконеогенеза осуществляются несколькими механизмами. Глюкоза, поступающая в клетки печени при пищеварении, активирует глюкокиназу – гликолитический фермент 1 субстратного цикла Инсулин индуцирует синтез глюкокиназы, фосфофруктокиназы и пируваткиназы – ферментов гликолиза 1, 2 и 3 субстратных циклов
При повышении уровня глюкозы в крови ускоряются реакции гликолиза и снижаются реакции глюконеогенеза осуществляются несколькими механизмами. Глюкоза, поступающая в клетки печени при пищеварении, активирует глюкокиназу – гликолитический фермент 1 субстратного цикла Инсулин индуцирует синтез глюкокиназы, фосфофруктокиназы и пируваткиназы – ферментов гликолиза 1, 2 и 3 субстратных циклов
 Аллостерически регулируется активность ферментов 2 субстратного цикла. Этот цикл составляют реакция фосфорилирования фруктозо-6 -фосфата с образованием фруктозо-1, 6 -бифосфата, которую катализирует фосфофруктокиназа, и реакция дефосфорилирования фруктозо-1, 6 бифосфата под действием фруктозо-1, 6 бифосфатазы. Аллостерический регулятор ферментов этого цикла фруктозо-2, 6 -бифосфат активирует фосфофруктокиназу и ингибирует фруктозо 2, 6 -бифосфатазу.
Аллостерически регулируется активность ферментов 2 субстратного цикла. Этот цикл составляют реакция фосфорилирования фруктозо-6 -фосфата с образованием фруктозо-1, 6 -бифосфата, которую катализирует фосфофруктокиназа, и реакция дефосфорилирования фруктозо-1, 6 бифосфата под действием фруктозо-1, 6 бифосфатазы. Аллостерический регулятор ферментов этого цикла фруктозо-2, 6 -бифосфат активирует фосфофруктокиназу и ингибирует фруктозо 2, 6 -бифосфатазу.
 Фруктозо-2, 6 -бифосфат образуется при фосфорилировании фруктозо-6 -фосфата бифункциональным ферментом (БИФ). Кроме того, этот фермент может катализировать реакцию дефосфорилирования фруктозо-2, 6 -бифосфата с образованием фруктозо-6 -фосфата. БИФ проявляет активность киназы (БИФ-ОН) или фосфатазы (БИФ-Р).
Фруктозо-2, 6 -бифосфат образуется при фосфорилировании фруктозо-6 -фосфата бифункциональным ферментом (БИФ). Кроме того, этот фермент может катализировать реакцию дефосфорилирования фруктозо-2, 6 -бифосфата с образованием фруктозо-6 -фосфата. БИФ проявляет активность киназы (БИФ-ОН) или фосфатазы (БИФ-Р).
 Инсулин вызывает активацию специфической протеинфосфатазы, которая дефосфорилирует БИФ-Р. Дефосфорилированный (БИФ-ОН) обладает киназной активностью и фосфорилирует фруктозо-6 -фосфат с образованием фруктозо 2, 6 -бифосфата. Фруктозо-2, 6 -бифосфат аллостерически активирует фосфофруктокиназу и ингибирует фруктозо-2, 6 -бифосфатазу.
Инсулин вызывает активацию специфической протеинфосфатазы, которая дефосфорилирует БИФ-Р. Дефосфорилированный (БИФ-ОН) обладает киназной активностью и фосфорилирует фруктозо-6 -фосфат с образованием фруктозо 2, 6 -бифосфата. Фруктозо-2, 6 -бифосфат аллостерически активирует фосфофруктокиназу и ингибирует фруктозо-2, 6 -бифосфатазу.
 В 3 субстратном цикле образование пирувата из фосфоенолпирувата в гликолизе катализирует пируваткиназа. В глюконеогенезе пируват превращается в фосфоенолпируват в результате двух последовательных реакций, которые катализируют пируваткарбоксилаза и фосфоенолпируваткарбоксикиназа.
В 3 субстратном цикле образование пирувата из фосфоенолпирувата в гликолизе катализирует пируваткиназа. В глюконеогенезе пируват превращается в фосфоенолпируват в результате двух последовательных реакций, которые катализируют пируваткарбоксилаза и фосфоенолпируваткарбоксикиназа.
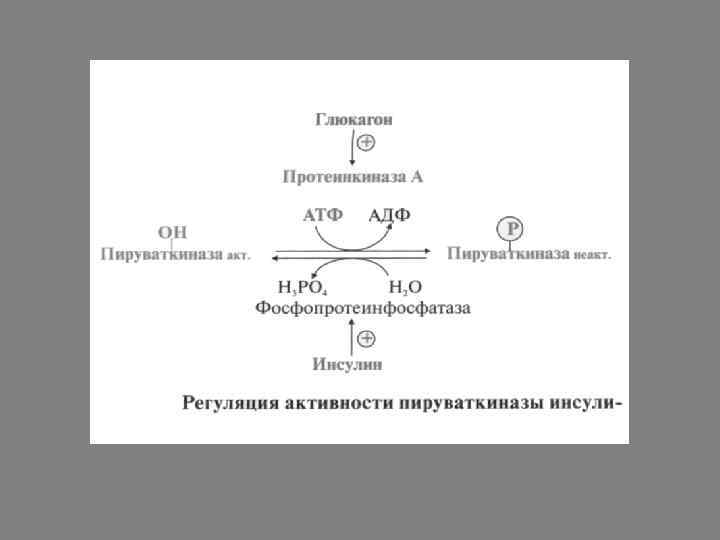
 Активность пируваткиназы регулируется аллостерически и фосфорилированием/дефосфорилировани ем. Фруктозо-1, 6 -бифосфат, образующийся в реакции, катализируемой фосфофруктокиназой, аллорстерически активирует пируваткиназу, таким образом обеспечивается ускорение всех этапов гликолиза. Инсулин вызывает активацию специфической протеинфосфатазы, которая дефосфорилирует и активирует пируваткиназу.
Активность пируваткиназы регулируется аллостерически и фосфорилированием/дефосфорилировани ем. Фруктозо-1, 6 -бифосфат, образующийся в реакции, катализируемой фосфофруктокиназой, аллорстерически активирует пируваткиназу, таким образом обеспечивается ускорение всех этапов гликолиза. Инсулин вызывает активацию специфической протеинфосфатазы, которая дефосфорилирует и активирует пируваткиназу.
 При голодании ускорение глюконеогенеза и замедление гликолиза обусловлено следующими механизмами регуляции. Фермент глюконеогенеза 3 субстратного цикла пируваткарбоксилаза аллостерически активируется ацетил-Со. А. Ацетил-Со. А аллостерически ингибирует окисление пирувата и ускоряет включение пирувата в глюконеогенез.
При голодании ускорение глюконеогенеза и замедление гликолиза обусловлено следующими механизмами регуляции. Фермент глюконеогенеза 3 субстратного цикла пируваткарбоксилаза аллостерически активируется ацетил-Со. А. Ацетил-Со. А аллостерически ингибирует окисление пирувата и ускоряет включение пирувата в глюконеогенез.
 Глюкагон, передавая сигнал в клетку через аденилатциклазную систему, вызывает активацию протеинкиназы А. Этот фермент фосфорилирует: • пируваткиназу, вызывая ее активацию • БИФ, который в фосфорилированной форме проявляет гидролазную активность и дефосфорилирует фруктозо-2, 6 -бифосфат. Уменьшение образования этого метаболита повышает активность фермента глюконеогенеза фруктозо-1, 6 -бифосфатазы и снижает активность фермента гликолиза фосфофруктокиназы.
Глюкагон, передавая сигнал в клетку через аденилатциклазную систему, вызывает активацию протеинкиназы А. Этот фермент фосфорилирует: • пируваткиназу, вызывая ее активацию • БИФ, который в фосфорилированной форме проявляет гидролазную активность и дефосфорилирует фруктозо-2, 6 -бифосфат. Уменьшение образования этого метаболита повышает активность фермента глюконеогенеза фруктозо-1, 6 -бифосфатазы и снижает активность фермента гликолиза фосфофруктокиназы.
 • специфические белки – факторы транскрипции, стимулирующие транскрипцию генов фосфоенолпируваткарбоксикиназы и фруктозо-2, 6 -бифосфатазы. Следовательно, гормон голода глюкагон ускоряет реакции глюконеогенеза и тормозит реакции гликолиза 3 и 2 субстратных циклов.
• специфические белки – факторы транскрипции, стимулирующие транскрипцию генов фосфоенолпируваткарбоксикиназы и фруктозо-2, 6 -бифосфатазы. Следовательно, гормон голода глюкагон ускоряет реакции глюконеогенеза и тормозит реакции гликолиза 3 и 2 субстратных циклов.
 При голодании, стрессе, физической работе в коре надпочечников увеличиваются синтез и секреция стероидного гормона кортизола. Он поступает в клетки печени и, взаимодействуя с внутриклеточным рецептором, ускоряет транскрипцию гена фосфоенолпируваткарбоксикиназы и таким образом увеличивает количество фермента в клетке.
При голодании, стрессе, физической работе в коре надпочечников увеличиваются синтез и секреция стероидного гормона кортизола. Он поступает в клетки печени и, взаимодействуя с внутриклеточным рецептором, ускоряет транскрипцию гена фосфоенолпируваткарбоксикиназы и таким образом увеличивает количество фермента в клетке.
 Снижение скорости гликолиза происходит также за счет того, что в связи с ускорением окисления жирных кислот в клетках печени увеличивается образование NADH и АТФ, которые аллостерически ингибируют фосфофруктокиназу и пируваткиназу.
Снижение скорости гликолиза происходит также за счет того, что в связи с ускорением окисления жирных кислот в клетках печени увеличивается образование NADH и АТФ, которые аллостерически ингибируют фосфофруктокиназу и пируваткиназу.
 РЕГУЛЯЦИЯ СОДЕРЖАНИЯ ГЛЮКОЗЫ В КРОВИ
РЕГУЛЯЦИЯ СОДЕРЖАНИЯ ГЛЮКОЗЫ В КРОВИ
 Результат регуляции метаболических путей превращения глюкозы - постоянство концентрации глюкозы в крови. Концентрация глюкозы в артериальной крови в течение суток поддерживается на постоянном уровне 60 -100 мг/дл (3, 3 -5, 5 ммоль/л). После приёма углеводной пищи уровень глюкозы возрастает в течение примерно 1 ч до 150 мг/дл, а затем возвращается к нормальному уровню (примерно через 2 ч).
Результат регуляции метаболических путей превращения глюкозы - постоянство концентрации глюкозы в крови. Концентрация глюкозы в артериальной крови в течение суток поддерживается на постоянном уровне 60 -100 мг/дл (3, 3 -5, 5 ммоль/л). После приёма углеводной пищи уровень глюкозы возрастает в течение примерно 1 ч до 150 мг/дл, а затем возвращается к нормальному уровню (примерно через 2 ч).
 Для предотвращения чрезмерного повышения концентрации глюкозы в крови при пищеварении основное значение имеет потребление глюкозы печенью и мышцами, в меньшей мере - жировой тканью. Следует напомнить, что более половины всей глюкозы (60%), поступающей из кишечника в воротную вену, поглощается печенью. Около 2/3 этого количества откладывается в печени в форме гликогена, остальная часть превращается в жиры и окисляется, обеспечивая синтез АТФ. Ускорение этих процессов инициируется повышением инсулинглюкагонового индекса.
Для предотвращения чрезмерного повышения концентрации глюкозы в крови при пищеварении основное значение имеет потребление глюкозы печенью и мышцами, в меньшей мере - жировой тканью. Следует напомнить, что более половины всей глюкозы (60%), поступающей из кишечника в воротную вену, поглощается печенью. Около 2/3 этого количества откладывается в печени в форме гликогена, остальная часть превращается в жиры и окисляется, обеспечивая синтез АТФ. Ускорение этих процессов инициируется повышением инсулинглюкагонового индекса.
 Другая часть глюкозы, поступающей из кишечника, попадает в общий кровоток. Примерно 2/3 этого количества поглощается мышцами и жировой тканью. Это обусловлено увеличением проницаемости мембран мышечных и жировых клеток для глюкозы под влиянием высокой концентрации инсулина. Глюкоза в мышцах откладывается в форме гликогена, а в жировых клетках превращается в жиры. Остальная часть глюкозы общего кровотока поглощается другими инсулинонезависимыми клетками.
Другая часть глюкозы, поступающей из кишечника, попадает в общий кровоток. Примерно 2/3 этого количества поглощается мышцами и жировой тканью. Это обусловлено увеличением проницаемости мембран мышечных и жировых клеток для глюкозы под влиянием высокой концентрации инсулина. Глюкоза в мышцах откладывается в форме гликогена, а в жировых клетках превращается в жиры. Остальная часть глюкозы общего кровотока поглощается другими инсулинонезависимыми клетками.
 При нормальном ритме питания и сбалансированном рационе концентрация глюкозы в крови и снабжение глюкозой всех органов поддерживается главным образом за счёт синтеза и распада гликогена. Лишь к концу ночного сна, т. е. к концу самого большого перерыва между приёмами пищи, может несколько увеличиться роль глюконеогенеза, значение которого будет возрастать, если завтрак не состоится и голодание продолжится.
При нормальном ритме питания и сбалансированном рационе концентрация глюкозы в крови и снабжение глюкозой всех органов поддерживается главным образом за счёт синтеза и распада гликогена. Лишь к концу ночного сна, т. е. к концу самого большого перерыва между приёмами пищи, может несколько увеличиться роль глюконеогенеза, значение которого будет возрастать, если завтрак не состоится и голодание продолжится.
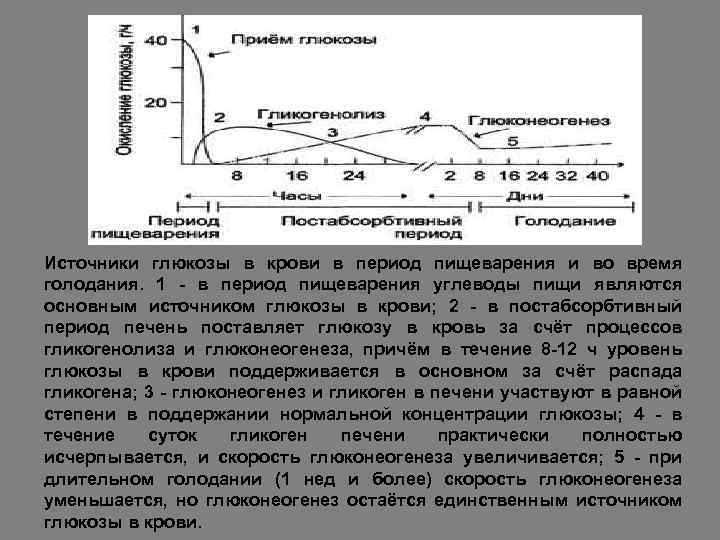 Источники глюкозы в крови в период пищеварения и во время голодания. 1 - в период пищеварения углеводы пищи являются основным источником глюкозы в крови; 2 - в постабсорбтивный период печень поставляет глюкозу в кровь за счёт процессов гликогенолиза и глюконеогенеза, причём в течение 8 -12 ч уровень глюкозы в крови поддерживается в основном за счёт распада гликогена; 3 - глюконеогенез и гликоген в печени участвуют в равной степени в поддержании нормальной концентрации глюкозы; 4 - в течение суток гликоген печени практически полностью исчерпывается, и скорость глюконеогенеза увеличивается; 5 - при длительном голодании (1 нед и более) скорость глюконеогенеза уменьшается, но глюконеогенез остаётся единственным источником глюкозы в крови.
Источники глюкозы в крови в период пищеварения и во время голодания. 1 - в период пищеварения углеводы пищи являются основным источником глюкозы в крови; 2 - в постабсорбтивный период печень поставляет глюкозу в кровь за счёт процессов гликогенолиза и глюконеогенеза, причём в течение 8 -12 ч уровень глюкозы в крови поддерживается в основном за счёт распада гликогена; 3 - глюконеогенез и гликоген в печени участвуют в равной степени в поддержании нормальной концентрации глюкозы; 4 - в течение суток гликоген печени практически полностью исчерпывается, и скорость глюконеогенеза увеличивается; 5 - при длительном голодании (1 нед и более) скорость глюконеогенеза уменьшается, но глюконеогенез остаётся единственным источником глюкозы в крови.
 Регуляция содержания глюкозы в крови предельном голодании
Регуляция содержания глюкозы в крови предельном голодании
 При голодании в течение первых суток исчерпываются запасы гликогена в организме, и в дальнейшем источником глюкозы служит только глюконеогенез (из лактата, глицерина и аминокислот). Глюконеогенез при этом ускоряется, а гликолиз замедляется вследствие низкой концентрации инсулина и высокой концентрации глюкагона.
При голодании в течение первых суток исчерпываются запасы гликогена в организме, и в дальнейшем источником глюкозы служит только глюконеогенез (из лактата, глицерина и аминокислот). Глюконеогенез при этом ускоряется, а гликолиз замедляется вследствие низкой концентрации инсулина и высокой концентрации глюкагона.
 Но, кроме того, через 1 -2 суток существенно проявляется действие и другого механизма регуляции - индукции и репрессии синтеза некоторых ферментов: снижается количество гликолитических ферментов и, наоборот, повышается количество ферментов глюконеогенеза. Изменение синтеза ферментов также связано с влиянием инсулина и глюкагона.
Но, кроме того, через 1 -2 суток существенно проявляется действие и другого механизма регуляции - индукции и репрессии синтеза некоторых ферментов: снижается количество гликолитических ферментов и, наоборот, повышается количество ферментов глюконеогенеза. Изменение синтеза ферментов также связано с влиянием инсулина и глюкагона.
 Начиная со второго дня голодания достигается максимальная скорость глюконеогенеза из аминокислот и глицерина. Скорость глюконеогенеза из лактата остаётся постоянной. В результате синтезируется около 100 г глюкозы ежесуточно, главным образом в печени. Следует отметить, что при голодании глюкоза не используется мышечными и жировыми клетками, поскольку в отсутствие инсулина не проникает в них и таким образом сберегается для снабжения мозга и других глюкозозависимых клеток.
Начиная со второго дня голодания достигается максимальная скорость глюконеогенеза из аминокислот и глицерина. Скорость глюконеогенеза из лактата остаётся постоянной. В результате синтезируется около 100 г глюкозы ежесуточно, главным образом в печени. Следует отметить, что при голодании глюкоза не используется мышечными и жировыми клетками, поскольку в отсутствие инсулина не проникает в них и таким образом сберегается для снабжения мозга и других глюкозозависимых клеток.
 Поскольку при других условиях мышцы - один из основных потребителей глюкозы, то прекращение потребления глюкозы мышцами при голодании имеет существенное значение для обеспечения глюкозой мозга. При достаточно продолжительном голодании (несколько дней и больше) мозг начинает использовать и другие источники энергии.
Поскольку при других условиях мышцы - один из основных потребителей глюкозы, то прекращение потребления глюкозы мышцами при голодании имеет существенное значение для обеспечения глюкозой мозга. При достаточно продолжительном голодании (несколько дней и больше) мозг начинает использовать и другие источники энергии.
 Вариантом голодания является несбалансированное питание, в частности такое, когда по калорийности рацион содержит мало углеводов - углеводное голодание. В этом случае также активируется глюконеогенез, и для синтеза глюкозы используются аминокислоты и глицерол, образующиеся из пищевых белков и жиров.
Вариантом голодания является несбалансированное питание, в частности такое, когда по калорийности рацион содержит мало углеводов - углеводное голодание. В этом случае также активируется глюконеогенез, и для синтеза глюкозы используются аминокислоты и глицерол, образующиеся из пищевых белков и жиров.
 Регуляция содержания глюкозы в крови в период покоя и во время физической нагрузки
Регуляция содержания глюкозы в крови в период покоя и во время физической нагрузки
 Как в период покоя, так и во время продолжительной физической работы сначала источником глюкозы для мышц служит гликоген, запасённый в самих мышцах, а затем глюкоза крови. Известно, что 100 г гликогена расходуется на бег примерно в течение 15 мин, а запасы гликогена в мышцах после приёма углеводной пищи могут составлять 200 -300 г.
Как в период покоя, так и во время продолжительной физической работы сначала источником глюкозы для мышц служит гликоген, запасённый в самих мышцах, а затем глюкоза крови. Известно, что 100 г гликогена расходуется на бег примерно в течение 15 мин, а запасы гликогена в мышцах после приёма углеводной пищи могут составлять 200 -300 г.
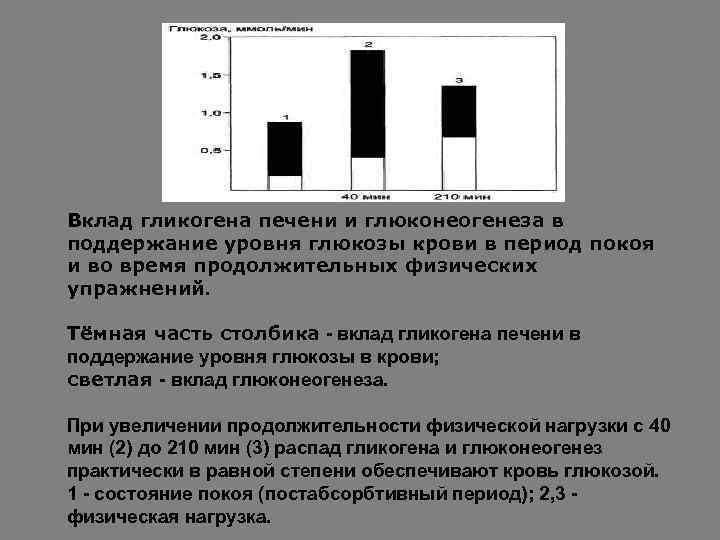 Вклад гликогена печени и глюконеогенеза в поддержание уровня глюкозы крови в период покоя и во время продолжительных физических упражнений. Тёмная часть столбика - вклад гликогена печени в поддержание уровня глюкозы в крови; светлая - вклад глюконеогенеза. При увеличении продолжительности физической нагрузки с 40 мин (2) до 210 мин (3) распад гликогена и глюконеогенез практически в равной степени обеспечивают кровь глюкозой. 1 - состояние покоя (постабсорбтивный период); 2, 3 физическая нагрузка.
Вклад гликогена печени и глюконеогенеза в поддержание уровня глюкозы крови в период покоя и во время продолжительных физических упражнений. Тёмная часть столбика - вклад гликогена печени в поддержание уровня глюкозы в крови; светлая - вклад глюконеогенеза. При увеличении продолжительности физической нагрузки с 40 мин (2) до 210 мин (3) распад гликогена и глюконеогенез практически в равной степени обеспечивают кровь глюкозой. 1 - состояние покоя (постабсорбтивный период); 2, 3 физическая нагрузка.
 Координация скоростей гликолиза, глюконеогенеза, синтеза и распада гликогена с участием гормонов обеспечивает: • предотвращение чрезмерного повышения концентрации глюкозы в крови после приёма пищи; • запасание гликогена и его использование в промежутках между приёмами пищи; • снабжение глюкозой мышц, потребность которых в энергии быстро возрастает при мышечной работе; • снабжение глюкозой клеток, которые при голодании в качестве источника энергии используют преимущественно глюкозу (нервные клетки, эритроциты, мозговое вещество почек).
Координация скоростей гликолиза, глюконеогенеза, синтеза и распада гликогена с участием гормонов обеспечивает: • предотвращение чрезмерного повышения концентрации глюкозы в крови после приёма пищи; • запасание гликогена и его использование в промежутках между приёмами пищи; • снабжение глюкозой мышц, потребность которых в энергии быстро возрастает при мышечной работе; • снабжение глюкозой клеток, которые при голодании в качестве источника энергии используют преимущественно глюкозу (нервные клетки, эритроциты, мозговое вещество почек).


