Биох 4 ферм.pptx
- Количество слайдов: 18
 Регуляция активности ферментов Скорость ферм реакции зависит от конц ферментов, конц субстрата, от температуры, Паш среды, наличия активаторов и ингибиторов. Ферм д-ют в мягких условиях, т. е при опр паш, давлении и т. д скорость ферм реакции может увеличиваться или уменьш. Зависимость скорости фер реакции от конц субстрата была сформул-на в 1913 г Михаэлесом и Ментеном и была названа законом кинетики ферм реакции. Или законом Михаэлеса-Ментена. В основе его лежит феномен насыщения. В клетках организма человека существует постоянная концентрация ферментов, кот способны насыщаться. При увеличении конц субстрата скоррсть ферм ре-и возрастает в прямой пропорциональной конц субстрата. Это реакция первого порядка. Она действ-ет при невысоких конц субстрата. Если конц субстрата увелич. до опред-ой величины, то скорость фермент реакции увеличивается незначительно. Это реакция второго порядка ( смешанного). При достижении определенной конц субстрата, при увеличении ее, скорость ферм р-и не изменяется, т. е не зависит от конц субстрата. Это р-я нулевого порядка. По мере того, как увелич конц субстрата, скорость ферм р-и остается постоянной и модет даже понижаться. Это обусловлено насыщением фермента субстратом. Все молекулы субстрата станотся переходными и скорость ферм р-и не увеличивается. Данную зависимость можно
Регуляция активности ферментов Скорость ферм реакции зависит от конц ферментов, конц субстрата, от температуры, Паш среды, наличия активаторов и ингибиторов. Ферм д-ют в мягких условиях, т. е при опр паш, давлении и т. д скорость ферм реакции может увеличиваться или уменьш. Зависимость скорости фер реакции от конц субстрата была сформул-на в 1913 г Михаэлесом и Ментеном и была названа законом кинетики ферм реакции. Или законом Михаэлеса-Ментена. В основе его лежит феномен насыщения. В клетках организма человека существует постоянная концентрация ферментов, кот способны насыщаться. При увеличении конц субстрата скоррсть ферм ре-и возрастает в прямой пропорциональной конц субстрата. Это реакция первого порядка. Она действ-ет при невысоких конц субстрата. Если конц субстрата увелич. до опред-ой величины, то скорость фермент реакции увеличивается незначительно. Это реакция второго порядка ( смешанного). При достижении определенной конц субстрата, при увеличении ее, скорость ферм р-и не изменяется, т. е не зависит от конц субстрата. Это р-я нулевого порядка. По мере того, как увелич конц субстрата, скорость ферм р-и остается постоянной и модет даже понижаться. Это обусловлено насыщением фермента субстратом. Все молекулы субстрата станотся переходными и скорость ферм р-и не увеличивается. Данную зависимость можно

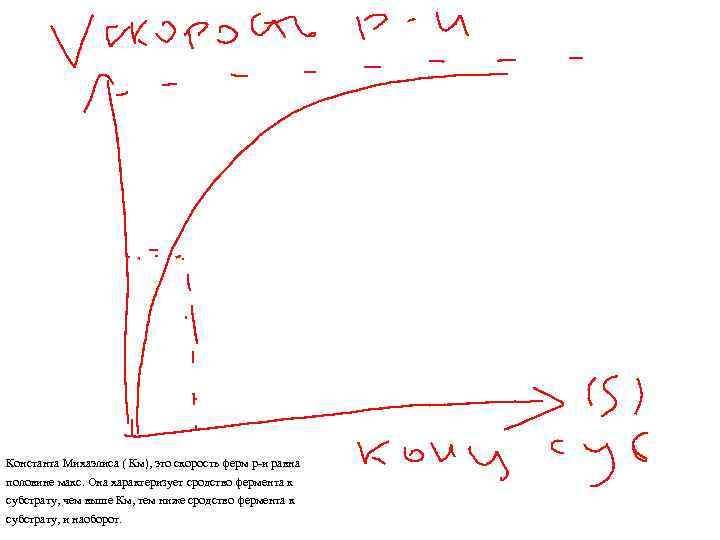 Константа Михаэлиса ( Км), это скорость ферм р-и равна половине макс. Она характеризует сродство фермента к субстрату, чем выше Км, тем ниже сродство фермента к субстрату, и наоборот.
Константа Михаэлиса ( Км), это скорость ферм р-и равна половине макс. Она характеризует сродство фермента к субстрату, чем выше Км, тем ниже сродство фермента к субстрату, и наоборот.
 . . . в организме чел-ка сущ-ет 2 фермента гексакеназа и глюкокеназа, кот катализируют одну и ту же р-ю фосфорилирования глюкозы с образованием глюкоза 6 фосфата. Они отличаются друг от друга Км, гексакеназа имеет низкую Км и высокое сродство к субстрату глюкозе. Т. о он акиивен в условиях гипогликемии или номрогликемии, а ферм глюкокеназа имеет высокую Км и низкое сродство к субстрату глюкозе. Он активен в печени в условиях гипергликемии. Км определяет тучасть молекул субстрата, кот связаны с активным центром ыермента.
. . . в организме чел-ка сущ-ет 2 фермента гексакеназа и глюкокеназа, кот катализируют одну и ту же р-ю фосфорилирования глюкозы с образованием глюкоза 6 фосфата. Они отличаются друг от друга Км, гексакеназа имеет низкую Км и высокое сродство к субстрату глюкозе. Т. о он акиивен в условиях гипогликемии или номрогликемии, а ферм глюкокеназа имеет высокую Км и низкое сродство к субстрату глюкозе. Он активен в печени в условиях гипергликемии. Км определяет тучасть молекул субстрата, кот связаны с активным центром ыермента.
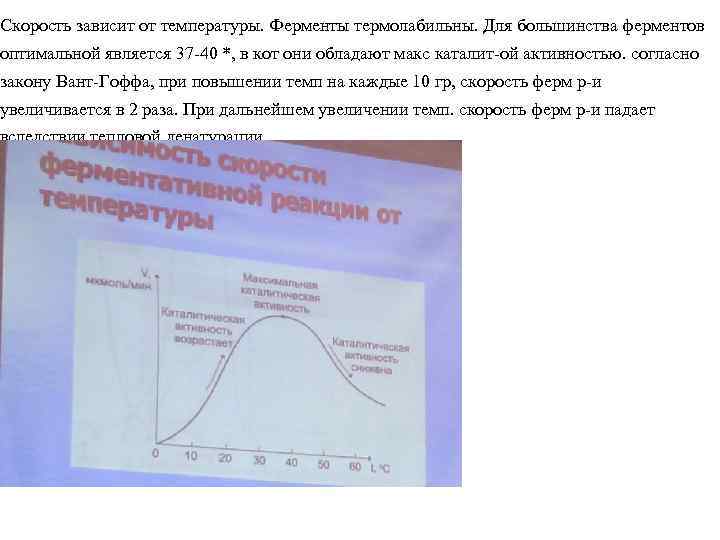 Скорость зависит от температуры. Ферменты термолабильны. Для большинства ферментов оптимальной является 37 -40 *, в кот они обладают макс каталит-ой активностью. согласно закону Вант-Гоффа, при повышении темп на каждые 10 гр, скорость ферм р-и увеличивается в 2 раза. При дальнейшем увеличении темп. скорость ферм р-и падает вследствии тепловой денатурации.
Скорость зависит от температуры. Ферменты термолабильны. Для большинства ферментов оптимальной является 37 -40 *, в кот они обладают макс каталит-ой активностью. согласно закону Вант-Гоффа, при повышении темп на каждые 10 гр, скорость ферм р-и увеличивается в 2 раза. При дальнейшем увеличении темп. скорость ферм р-и падает вследствии тепловой денатурации.
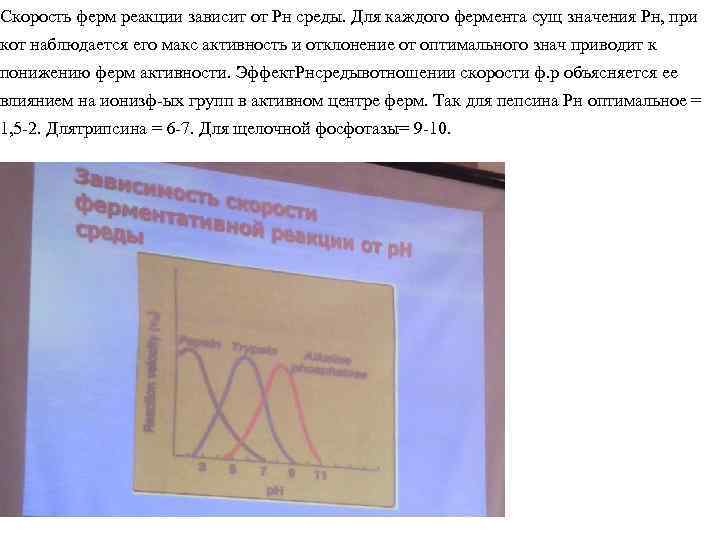 Скорость ферм реакции зависит от Рн среды. Для каждого фермента сущ значения Рн, при кот наблюдается его макс активность и отклонение от оптимального знач приводит к понижению ферм активности. Эффект. Рнсредывотношении скорости ф. р объясняется ее влиянием на ионизф-ых групп в активном центре ферм. Так для пепсина Рн оптимальное = 1, 5 -2. Длятрипсина = 6 -7. Для щелочной фосфотазы= 9 -10.
Скорость ферм реакции зависит от Рн среды. Для каждого фермента сущ значения Рн, при кот наблюдается его макс активность и отклонение от оптимального знач приводит к понижению ферм активности. Эффект. Рнсредывотношении скорости ф. р объясняется ее влиянием на ионизф-ых групп в активном центре ферм. Так для пепсина Рн оптимальное = 1, 5 -2. Длятрипсина = 6 -7. Для щелочной фосфотазы= 9 -10.
 Скорость ф р зависит от конц ферментов. При ее увеличении скорость увеличивается прямопропорционально. Скорость ф р зависит от наличия активаторов или ингибиторов. Активаторами наз в-ва усиливаюшие каталитическую акт-ть фермента и увеличивающие скорость протекания реакции. Ингибиторами наз-ся в-ва понижающие каталитическую активность фермента и уменьшающие скорость протекания реакции. Регуляцию акт ферм:
Скорость ф р зависит от конц ферментов. При ее увеличении скорость увеличивается прямопропорционально. Скорость ф р зависит от наличия активаторов или ингибиторов. Активаторами наз в-ва усиливаюшие каталитическую акт-ть фермента и увеличивающие скорость протекания реакции. Ингибиторами наз-ся в-ва понижающие каталитическую активность фермента и уменьшающие скорость протекания реакции. Регуляцию акт ферм:
 Активирование - это увеличение каталитической активности фермента под влиянием активаторов. Различают акт-е путем химич модификации. К данному виду относят ковалентную модификацию. Это активирование достигается путем ковалентного присоединения к ферменту определенной группировки ( например фосфорильной), благодаря чему происходит изменение структуры фермента и активного центра т. о, что повышается каталит активность фермента. Например фермент фосфорилаза А, это ферм кот способствует мобилизации гликогена в печени и он является результатом ковалентной модификации фосфорилазы Б. В реакции фосфорилирования. Данный фермент фосфорилаза активен только в фосфорилированном сост. А фермент глигоген-синтетаза это ферм кот принимает участие в синтезе гликогена. Он активен в Д фосфорилированном состоянии.
Активирование - это увеличение каталитической активности фермента под влиянием активаторов. Различают акт-е путем химич модификации. К данному виду относят ковалентную модификацию. Это активирование достигается путем ковалентного присоединения к ферменту определенной группировки ( например фосфорильной), благодаря чему происходит изменение структуры фермента и активного центра т. о, что повышается каталит активность фермента. Например фермент фосфорилаза А, это ферм кот способствует мобилизации гликогена в печени и он является результатом ковалентной модификации фосфорилазы Б. В реакции фосфорилирования. Данный фермент фосфорилаза активен только в фосфорилированном сост. А фермент глигоген-синтетаза это ферм кот принимает участие в синтезе гликогена. Он активен в Д фосфорилированном состоянии.
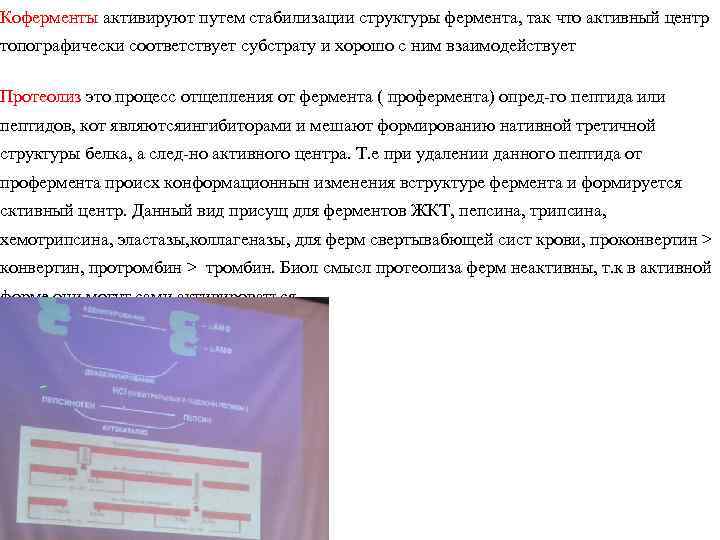 Коферменты активируют путем стабилизации структуры фермента, так что активный центр топографически соответствует субстрату и хорошо с ним взаимодействует Протеолиз это процесс отщепления от фермента ( профермента) опред-го пептида или пептидов, кот являютсяингибиторами и мешают формированию нативной третичной структуры белка, а след-но активного центра. Т. е при удалении данного пептида от профермента происх конформационнын изменения вструктуре фермента и формируется сктивный центр. Данный вид присущ для ферментов ЖКТ, пепсина, трипсина, хемотрипсина, эластазы, коллагеназы, для ферм свертывабющей сист крови, проконвертин > конвертин, протромбин > тромбин. Биол смысл протеолиза ферм неактивны, т. к в активной форме они могут сами активироваться
Коферменты активируют путем стабилизации структуры фермента, так что активный центр топографически соответствует субстрату и хорошо с ним взаимодействует Протеолиз это процесс отщепления от фермента ( профермента) опред-го пептида или пептидов, кот являютсяингибиторами и мешают формированию нативной третичной структуры белка, а след-но активного центра. Т. е при удалении данного пептида от профермента происх конформационнын изменения вструктуре фермента и формируется сктивный центр. Данный вид присущ для ферментов ЖКТ, пепсина, трипсина, хемотрипсина, эластазы, коллагеназы, для ферм свертывабющей сист крови, проконвертин > конвертин, протромбин > тромбин. Биол смысл протеолиза ферм неактивны, т. к в активной форме они могут сами активироваться
 Диссоциация происходит благодаря разъединению фермента на определенные субъединицы, такой вид активирования приемлем для олигомерных ферментов, т. е сост из двух или более субъединиц. Регулятор может взаимодействовать с 1 субъед в результате чего фермент распадаетс на отдельные сбъединицы и стан активным. В противоположность ассоциация это объединение отдельных субъединиц в одну макромолекулу и в этом сост фермент становится активным. Например лактатдегидрогеназа сост из 4 -ех субъед и он активен только в ассоциированном сост. При удалении одной субъединицы фермент теряет свою каталитическую активность.
Диссоциация происходит благодаря разъединению фермента на определенные субъединицы, такой вид активирования приемлем для олигомерных ферментов, т. е сост из двух или более субъединиц. Регулятор может взаимодействовать с 1 субъед в результате чего фермент распадаетс на отдельные сбъединицы и стан активным. В противоположность ассоциация это объединение отдельных субъединиц в одну макромолекулу и в этом сост фермент становится активным. Например лактатдегидрогеназа сост из 4 -ех субъед и он активен только в ассоциированном сост. При удалении одной субъединицы фермент теряет свою каталитическую активность.
 Аллостерическая регуляция касается аллостерических фер ентрв, кот в своей молекуле кроме активного центра сод-ит аллостерический центр. Это особый центр, с кот могут связываться низкомолекулярные в-ва эффектопы или модуляторы, изменяющие каталитическую активность фермента вследствии конформационных изменений. Молекула аллостерического фермента имеет 4 - ю структуру и каждая субъединица модет обладать аллостерическим центром. Эффекторы могут быть положительными или отриц. Эффекторы это в-ва чаще низкомолекулярные, кот по своейструктуре отличаются от структуры субстрата, и обычно образуются в конце метаболического пути, но могут оказыаать влияние, т. е активировать или ингибировать начальные реакции. Сущ-ет несколько теорий аллостер-й регуляции: модель согласованного аллостерического взаимодействия, была открыта Моно и Уайтманом. Согласно этрй теории олигтмерный фермент может быть в двух формах. В Т форме ( неактивное) и Р форме (активное). Вторая модел. Это последовательного аллостерического взаимодействия и предполагает сущ-е переходной Т-Р формы фермента.
Аллостерическая регуляция касается аллостерических фер ентрв, кот в своей молекуле кроме активного центра сод-ит аллостерический центр. Это особый центр, с кот могут связываться низкомолекулярные в-ва эффектопы или модуляторы, изменяющие каталитическую активность фермента вследствии конформационных изменений. Молекула аллостерического фермента имеет 4 - ю структуру и каждая субъединица модет обладать аллостерическим центром. Эффекторы могут быть положительными или отриц. Эффекторы это в-ва чаще низкомолекулярные, кот по своейструктуре отличаются от структуры субстрата, и обычно образуются в конце метаболического пути, но могут оказыаать влияние, т. е активировать или ингибировать начальные реакции. Сущ-ет несколько теорий аллостер-й регуляции: модель согласованного аллостерического взаимодействия, была открыта Моно и Уайтманом. Согласно этрй теории олигтмерный фермент может быть в двух формах. В Т форме ( неактивное) и Р форме (активное). Вторая модел. Это последовательного аллостерического взаимодействия и предполагает сущ-е переходной Т-Р формы фермента.
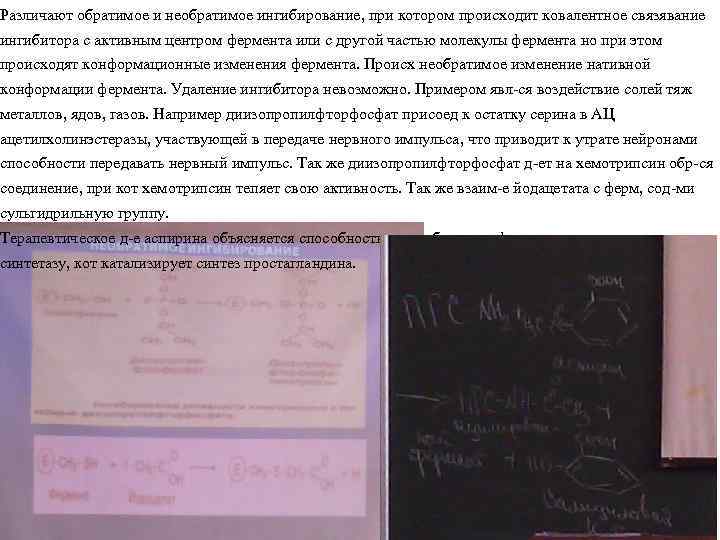 Различают обратимое и необратимое ингибирование, при котором происходит ковалентное связявание ингибитора с активным центром фермента или с другой частью молекулы фермента но при этом происходят конформационные изменения фермента. Происх необратимое изменение нативной конформации фермента. Удаление ингибитора невозможно. Примером явл-ся воздействие солей тяж металлов, ядов, газов. Например диизопропилфторфосфат присоед к остатку серина в АЦ ацетилхолинэстеразы, участвующей в передаче нервного импульса, что приводит к утрате нейронами способности передавать нервный импульс. Так же диизопропилфторфосфат д-ет на хемотрипсин обр-ся соединение, при кот хемотрипсин тепяет свою активность. Так же взаим-е йодацетата с ферм, сод-ми сульгидрильную группу. Терапевтическое д-е аспирина объясняется способностью ингибировать фермент простагландин синтетазу, кот катализирует синтез простагландина.
Различают обратимое и необратимое ингибирование, при котором происходит ковалентное связявание ингибитора с активным центром фермента или с другой частью молекулы фермента но при этом происходят конформационные изменения фермента. Происх необратимое изменение нативной конформации фермента. Удаление ингибитора невозможно. Примером явл-ся воздействие солей тяж металлов, ядов, газов. Например диизопропилфторфосфат присоед к остатку серина в АЦ ацетилхолинэстеразы, участвующей в передаче нервного импульса, что приводит к утрате нейронами способности передавать нервный импульс. Так же диизопропилфторфосфат д-ет на хемотрипсин обр-ся соединение, при кот хемотрипсин тепяет свою активность. Так же взаим-е йодацетата с ферм, сод-ми сульгидрильную группу. Терапевтическое д-е аспирина объясняется способностью ингибировать фермент простагландин синтетазу, кот катализирует синтез простагландина.
 При обратимомингибировании связи не ковалентные и возможно восстановление кат активности. Различ конкурентное, неконкурентное и безконкурентное. При первом ингибитор с руктурно схож с субсьратом, т. еэто процесс потрможения ферм активности, вызванный присутствием ингибитора схожего с субстратом. При этом и субстрат и ингибитор связываются с АЦ т. е конкурируют за связывание с АЦ фермента. Степень ингибирования зависит от концентрации субстрата и ингибирования. При повышении конц ингибитора скорость ферм р-и понижается т. к с активным центром связывается ингибитор. При увеличении конц субстрата скорость ферм р-и увеличивается, т. к с АЦ связывается субстрат. Пример -малоновая к-та.
При обратимомингибировании связи не ковалентные и возможно восстановление кат активности. Различ конкурентное, неконкурентное и безконкурентное. При первом ингибитор с руктурно схож с субсьратом, т. еэто процесс потрможения ферм активности, вызванный присутствием ингибитора схожего с субстратом. При этом и субстрат и ингибитор связываются с АЦ т. е конкурируют за связывание с АЦ фермента. Степень ингибирования зависит от концентрации субстрата и ингибирования. При повышении конц ингибитора скорость ферм р-и понижается т. к с активным центром связывается ингибитор. При увеличении конц субстрата скорость ферм р-и увеличивается, т. к с АЦ связывается субстрат. Пример -малоновая к-та.
 Метод конкурентного ингибирования нашел применение в медицинской практике. Антиметаболиты они могут вступать в р-и синтеза, в рез-те кот образуется аномальные днк. Эти препараты ппимен-ся в качествехимиопрепаратов. Производные АМК, произв аминоаденина и фторурациоа.
Метод конкурентного ингибирования нашел применение в медицинской практике. Антиметаболиты они могут вступать в р-и синтеза, в рез-те кот образуется аномальные днк. Эти препараты ппимен-ся в качествехимиопрепаратов. Производные АМК, произв аминоаденина и фторурациоа.
 Антиметеболиты применяют для лечения ифекционных заболеваний. Сульфаниламидные препараты являются аналогами парааминобензойной к-ты, кот бактериальная клетка использует для систеща фолиевой к-ты, явл-ся сост частью ферментов бактерийй. Этот препарат благодаря ся
Антиметеболиты применяют для лечения ифекционных заболеваний. Сульфаниламидные препараты являются аналогами парааминобензойной к-ты, кот бактериальная клетка использует для систеща фолиевой к-ты, явл-ся сост частью ферментов бактерийй. Этот препарат благодаря ся
 Неконкурентное ингибирование
Неконкурентное ингибирование
 Энзимодиагностика это исп-е ферментов для диагностики различных заболеваний. Это определение в биол жидкостях. Различают плазмаспецифические и органоспециф ферменты. Н ацетилбетадеглюкоаминидаза для почек, нуклеатидаза для гепатобиллиарного тракта. Щелочная фосфатаза для печени ктстей по, ек. Т. о энзимодиагностика основана на неравномерном распределении ферментов или изоферментов среди органов и тканей в кот они функционируют, при этом активность ферм в сыворотке бывпет низкий, а повышение аквсыворотке указывает н. патологию Органа, кот этим ферментом богат. Активность может повышаться при некрозе, старении клеток и отмирании, при увеличеннойпртницаемости клет мембран врез-те. Повыш акт
Энзимодиагностика это исп-е ферментов для диагностики различных заболеваний. Это определение в биол жидкостях. Различают плазмаспецифические и органоспециф ферменты. Н ацетилбетадеглюкоаминидаза для почек, нуклеатидаза для гепатобиллиарного тракта. Щелочная фосфатаза для печени ктстей по, ек. Т. о энзимодиагностика основана на неравномерном распределении ферментов или изоферментов среди органов и тканей в кот они функционируют, при этом активность ферм в сыворотке бывпет низкий, а повышение аквсыворотке указывает н. патологию Органа, кот этим ферментом богат. Активность может повышаться при некрозе, старении клеток и отмирании, при увеличеннойпртницаемости клет мембран врез-те. Повыш акт



