Lektsia_3_Fermenty_Regulyatsia_aktivnosti_fermentov.ppt
- Количество слайдов: 23
 Регуляция активности ферментов (регуляция скорости ферментативных реакций) 1. Эффекторы. Типы. Механизмы действия. 2. Уровни регуляции активности ферментов; 3. Механизмы регуляции активности регуляторных ферментов. 4. Изоферменты
Регуляция активности ферментов (регуляция скорости ферментативных реакций) 1. Эффекторы. Типы. Механизмы действия. 2. Уровни регуляции активности ферментов; 3. Механизмы регуляции активности регуляторных ферментов. 4. Изоферменты
 Влияние эффекторов на активность (скорость реакции) ферментов • Эффекторы – вещества, которые связываясь с молекулой фермента, ингибируют( ингибиторы) или усиливают (активаторы) активность фермента. • Эффекторы: а. метаболиты, гормоны, образующиеся в организме, регулируют метаболизм, направляя его в нужное русло. б. лекарственные препараты В. яды.
Влияние эффекторов на активность (скорость реакции) ферментов • Эффекторы – вещества, которые связываясь с молекулой фермента, ингибируют( ингибиторы) или усиливают (активаторы) активность фермента. • Эффекторы: а. метаболиты, гормоны, образующиеся в организме, регулируют метаболизм, направляя его в нужное русло. б. лекарственные препараты В. яды.
 Ингибиторы. Типы. • По степени прочности связывания с ферментом делят на необратимые и обратимые. • Обратимые ингибиторы – нековалентно связываются с ферментами, образуя комплекс E I , который способен диссоциировать при определенных условиях. Активность фермента восстанавливается EI E+I
Ингибиторы. Типы. • По степени прочности связывания с ферментом делят на необратимые и обратимые. • Обратимые ингибиторы – нековалентно связываются с ферментами, образуя комплекс E I , который способен диссоциировать при определенных условиях. Активность фермента восстанавливается EI E+I
 Ингибиторы. Типы. • Необратимые ингибиторы – ковалентно связываются c ферментом, образуя прочный комплекс E I , который препятствуют образованию нормального комплекса ES. EI – практически не диссоциирует. Примеры: яды !!( ДФФ- диизопропилфторфосфат) – нервнопаралитический яд. Ингибируют фермент ацетилхолинэстеразу, которая участвует в передаче нервных импульсов от нейрона к нейрону. (На его основе – синтезированы многие инсектициды) Лекарственные препараты: Аспирин – противовоспалительный нестероидный препарат. Ингибирует фермент циклооксигеназу, который катализирует образование простагландинов из арахидоновой кислоты. Ингибированные молекулы фермента разрушаются. Простагландины – медиаторы воспаления. Их синтез восстанавливается только после синтеза новых молекул фермента.
Ингибиторы. Типы. • Необратимые ингибиторы – ковалентно связываются c ферментом, образуя прочный комплекс E I , который препятствуют образованию нормального комплекса ES. EI – практически не диссоциирует. Примеры: яды !!( ДФФ- диизопропилфторфосфат) – нервнопаралитический яд. Ингибируют фермент ацетилхолинэстеразу, которая участвует в передаче нервных импульсов от нейрона к нейрону. (На его основе – синтезированы многие инсектициды) Лекарственные препараты: Аспирин – противовоспалительный нестероидный препарат. Ингибирует фермент циклооксигеназу, который катализирует образование простагландинов из арахидоновой кислоты. Ингибированные молекулы фермента разрушаются. Простагландины – медиаторы воспаления. Их синтез восстанавливается только после синтеза новых молекул фермента.
 Типы обратимых ингибиторов. Конкурентные ингибиторы • Обратимые ингибиторы делят на конкурентные и неконкурентные. • К конкурентным ингибиторам (тип ингибирования конкурентный) относят эффекторы, которые обратимо ингибируют активность фермента, путем связывания с активным центром фермента. Ингибитор структурный аналог субстрата. В результате чего возникает конкуренция субстрата и ингибитора за активный центр фермента. Виды взаимодействия молекул в этой ситуации: E+S → ES→E+P; E+I→EI
Типы обратимых ингибиторов. Конкурентные ингибиторы • Обратимые ингибиторы делят на конкурентные и неконкурентные. • К конкурентным ингибиторам (тип ингибирования конкурентный) относят эффекторы, которые обратимо ингибируют активность фермента, путем связывания с активным центром фермента. Ингибитор структурный аналог субстрата. В результате чего возникает конкуренция субстрата и ингибитора за активный центр фермента. Виды взаимодействия молекул в этой ситуации: E+S → ES→E+P; E+I→EI
![Результат действия конкурентного ингибирования на графике зависимости V от [S] контроль С ингибитором Км Результат действия конкурентного ингибирования на графике зависимости V от [S] контроль С ингибитором Км](https://present5.com/presentation/250030700_451494123/image-6.jpg) Результат действия конкурентного ингибирования на графике зависимости V от [S] контроль С ингибитором Км –повышается; V max – const. При достаточно высокой [S] субстрат вытесняет ингибитор из активного центра
Результат действия конкурентного ингибирования на графике зависимости V от [S] контроль С ингибитором Км –повышается; V max – const. При достаточно высокой [S] субстрат вытесняет ингибитор из активного центра
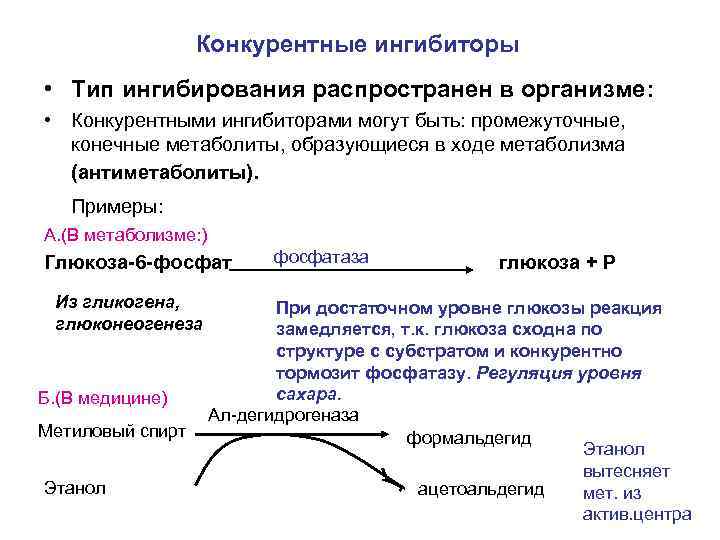 Конкурентные ингибиторы • Тип ингибирования распространен в организме: • Конкурентными ингибиторами могут быть: промежуточные, конечные метаболиты, образующиеся в ходе метаболизма (антиметаболиты). Примеры: А. (В метаболизме: ) Глюкоза-6 -фосфат Из гликогена, глюконеогенеза Б. (В медицине) Метиловый спирт Этанол фосфатаза глюкоза + Р При достаточном уровне глюкозы реакция замедляется, т. к. глюкоза сходна по структуре с субстратом и конкурентно тормозит фосфатазу. Регуляция уровня сахара. Ал-дегидрогеназа формальдегид Этанол вытесняет ацетоальдегид мет. из актив. центра
Конкурентные ингибиторы • Тип ингибирования распространен в организме: • Конкурентными ингибиторами могут быть: промежуточные, конечные метаболиты, образующиеся в ходе метаболизма (антиметаболиты). Примеры: А. (В метаболизме: ) Глюкоза-6 -фосфат Из гликогена, глюконеогенеза Б. (В медицине) Метиловый спирт Этанол фосфатаза глюкоза + Р При достаточном уровне глюкозы реакция замедляется, т. к. глюкоза сходна по структуре с субстратом и конкурентно тормозит фосфатазу. Регуляция уровня сахара. Ал-дегидрогеназа формальдегид Этанол вытесняет ацетоальдегид мет. из актив. центра
 Неконкурентные ингибиторы • Неконкурентные ингибиторы. Тип ингибирования – неконкурентный. Неконкурентный ингибитор не обладает сходством структуры с субстратом и связывается с ферментом вне активного центра (иногда затрагивается каталитический участок). Образуется тройной неактивный комплекс: E+S+ I ESI Сродство фермента к субстрата не изменяется, т. е. Км – не меняется
Неконкурентные ингибиторы • Неконкурентные ингибиторы. Тип ингибирования – неконкурентный. Неконкурентный ингибитор не обладает сходством структуры с субстратом и связывается с ферментом вне активного центра (иногда затрагивается каталитический участок). Образуется тройной неактивный комплекс: E+S+ I ESI Сродство фермента к субстрата не изменяется, т. е. Км – не меняется
![Результат действия неконкурентного ингибитора на графике зависимости [S] контроль V с ингибитором 1/2 Vмах Результат действия неконкурентного ингибитора на графике зависимости [S] контроль V с ингибитором 1/2 Vмах](https://present5.com/presentation/250030700_451494123/image-9.jpg) Результат действия неконкурентного ингибитора на графике зависимости [S] контроль V с ингибитором 1/2 Vмах Км [S] Км – не изменяется; Vмах – снижается. При увеличении концентрации субстрата ингибирование не снижается.
Результат действия неконкурентного ингибитора на графике зависимости [S] контроль V с ингибитором 1/2 Vмах Км [S] Км – не изменяется; Vмах – снижается. При увеличении концентрации субстрата ингибирование не снижается.
 Уровни регуляции скорости ферментативных реакций • Для сохранения клеточного гомеостаза в клетках скорости ферментативных реакций в клетке изменяются в зависимости от условий среды и физиологического состояния организма (гипоксия, голод, физические нагрузки, стресс). Регуляция скорости реакции в клетке осуществляется на 3 -х независимых уровнях: 1. Регуляция количества фермента в клетке; 2. Наличие и концентрация субстрата в клетке; 3. Изменение активности фермента
Уровни регуляции скорости ферментативных реакций • Для сохранения клеточного гомеостаза в клетках скорости ферментативных реакций в клетке изменяются в зависимости от условий среды и физиологического состояния организма (гипоксия, голод, физические нагрузки, стресс). Регуляция скорости реакции в клетке осуществляется на 3 -х независимых уровнях: 1. Регуляция количества фермента в клетке; 2. Наличие и концентрация субстрата в клетке; 3. Изменение активности фермента
 1. Регуляция количества молекул фермента в клетке • Количество ферментов определяется соотношением скоростей двух процессов – синтеза, фолдинга белка и распада белка в клетке (тканевой протеолиз): синтез Аминокислоты фермент (белок) распад Синтез и фолдинг регулируются на разных этапах. Наиболее изучен механизм на уровне транскрипции(индукция – активация; репрессия – угнетение). Регуляция осуществляется метаболитами, гормонами и др. Регуляция распада ( протеолиз) менее изучена, но также, вероятно, на генетическом уровне.
1. Регуляция количества молекул фермента в клетке • Количество ферментов определяется соотношением скоростей двух процессов – синтеза, фолдинга белка и распада белка в клетке (тканевой протеолиз): синтез Аминокислоты фермент (белок) распад Синтез и фолдинг регулируются на разных этапах. Наиболее изучен механизм на уровне транскрипции(индукция – активация; репрессия – угнетение). Регуляция осуществляется метаболитами, гормонами и др. Регуляция распада ( протеолиз) менее изучена, но также, вероятно, на генетическом уровне.
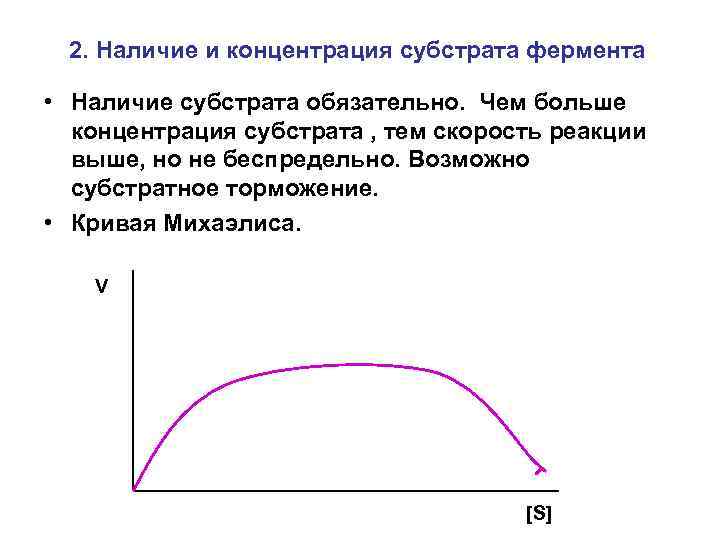 2. Наличие и концентрация субстрата фермента • Наличие субстрата обязательно. Чем больше концентрация субстрата , тем скорость реакции выше, но не беспредельно. Возможно субстратное торможение. • Кривая Михаэлиса. V [S]
2. Наличие и концентрация субстрата фермента • Наличие субстрата обязательно. Чем больше концентрация субстрата , тем скорость реакции выше, но не беспредельно. Возможно субстратное торможение. • Кривая Михаэлиса. V [S]
 3. Регуляция каталитической активности ключевого (регуляторного) фермента метаболического пути • • 1. 2. 3. 4. Высокоэффективный способ регуляции метаболизма. Основные механизмы регуляции каталитической активности регуляторного ферментов: Аллостерическая регуляция; Регуляция путем ассоциации/диссоциации протомеров молекул ферментов; Регуляция путем фосфорилирования/ дефосфорилирования молекулы фермента; Регуляция путем частичного протеолиза
3. Регуляция каталитической активности ключевого (регуляторного) фермента метаболического пути • • 1. 2. 3. 4. Высокоэффективный способ регуляции метаболизма. Основные механизмы регуляции каталитической активности регуляторного ферментов: Аллостерическая регуляция; Регуляция путем ассоциации/диссоциации протомеров молекул ферментов; Регуляция путем фосфорилирования/ дефосфорилирования молекулы фермента; Регуляция путем частичного протеолиза
 Аллостерическая регуляция • Характерна для олигомерных ферментов (четвертичная структура). В структуре имеются каталитические протомеры( с активным центром) и протомеры - регуляторные ( с аллостерич. центром) • Аллостерические ферменты меняют активность не только от концентрации субстрата , но и под действием эффекторов (результат- изменение конфигурации молекулы и активного центра). • Аллостерические ферменты- регуляторные ферменты метаболических путей, катализируют 1 -ю необратимую (самую медленную) реакцию метаболического пути. • Активность остальных ферментов этого пути от [S] • S P 1 P 2 P 3→ P E 1 E 2 E 3 E 4
Аллостерическая регуляция • Характерна для олигомерных ферментов (четвертичная структура). В структуре имеются каталитические протомеры( с активным центром) и протомеры - регуляторные ( с аллостерич. центром) • Аллостерические ферменты меняют активность не только от концентрации субстрата , но и под действием эффекторов (результат- изменение конфигурации молекулы и активного центра). • Аллостерические ферменты- регуляторные ферменты метаболических путей, катализируют 1 -ю необратимую (самую медленную) реакцию метаболического пути. • Активность остальных ферментов этого пути от [S] • S P 1 P 2 P 3→ P E 1 E 2 E 3 E 4
 Аллостерические эффекторы • Отличаются по химической природе от субстрата. • Активаторы и ингибиторы. • Аллостерические ингибиторы- конечный продукт метаболического пути. Аллостерическое ингибирование распространено в регуляции скорости метаболических путей. • Аллостерическое ингибирование часто называют – механизм отрицательной обратной связи • S E 1 P 1 E 2 P 2 E 3 P 3 E 4 P
Аллостерические эффекторы • Отличаются по химической природе от субстрата. • Активаторы и ингибиторы. • Аллостерические ингибиторы- конечный продукт метаболического пути. Аллостерическое ингибирование распространено в регуляции скорости метаболических путей. • Аллостерическое ингибирование часто называют – механизм отрицательной обратной связи • S E 1 P 1 E 2 P 2 E 3 P 3 E 4 P
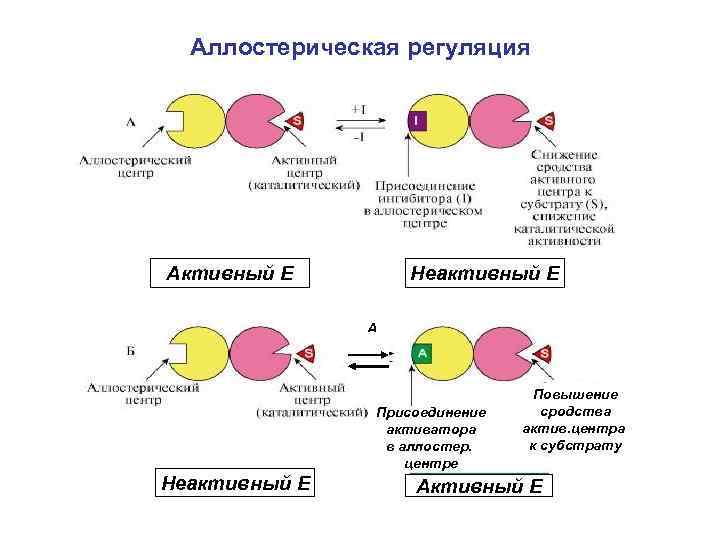 Аллостерическая регуляция Активный E Неактивный E А Присоединение активатора в аллостер. центре Неактивный E Повышение сродства актив. центра к субстрату Активный E
Аллостерическая регуляция Активный E Неактивный E А Присоединение активатора в аллостер. центре Неактивный E Повышение сродства актив. центра к субстрату Активный E
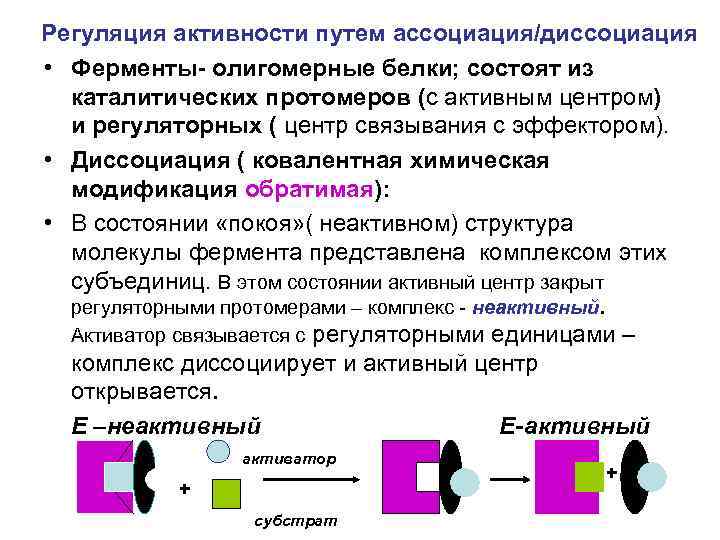 Регуляция активности путем ассоциация/диссоциация • Ферменты- олигомерные белки; состоят из каталитических протомеров (с активным центром) и регуляторных ( центр связывания с эффектором). • Диссоциация ( ковалентная химическая модификация обратимая): • В состоянии «покоя» ( неактивном) структура молекулы фермента представлена комплексом этих субъединиц. В этом состоянии активный центр закрыт регуляторными протомерами – комплекс - неактивный. Активатор связывается с регуляторными единицами – комплекс диссоциирует и активный центр открывается. E –неактивный E-активный активатор + субстрат +
Регуляция активности путем ассоциация/диссоциация • Ферменты- олигомерные белки; состоят из каталитических протомеров (с активным центром) и регуляторных ( центр связывания с эффектором). • Диссоциация ( ковалентная химическая модификация обратимая): • В состоянии «покоя» ( неактивном) структура молекулы фермента представлена комплексом этих субъединиц. В этом состоянии активный центр закрыт регуляторными протомерами – комплекс - неактивный. Активатор связывается с регуляторными единицами – комплекс диссоциирует и активный центр открывается. E –неактивный E-активный активатор + субстрат +
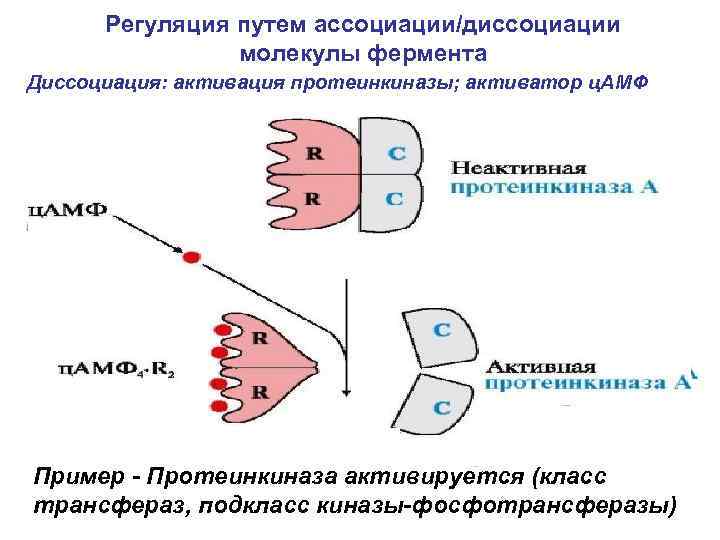 Регуляция путем ассоциации/диссоциации молекулы фермента Диссоциация: активация протеинкиназы; активатор ц. АМФ активатор Пример - Протеинкиназа активируется (класс трансфераз, подкласс киназы-фосфотрансферазы)
Регуляция путем ассоциации/диссоциации молекулы фермента Диссоциация: активация протеинкиназы; активатор ц. АМФ активатор Пример - Протеинкиназа активируется (класс трансфераз, подкласс киназы-фосфотрансферазы)
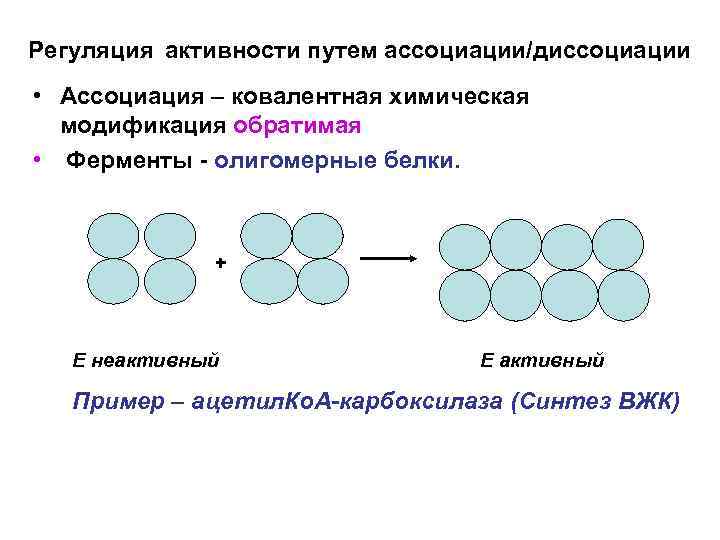 Регуляция активности путем ассоциации/диссоциации • Ассоциация – ковалентная химическая модификация обратимая • Ферменты - олигомерные белки. + E неактивный E активный Пример – ацетил. Ко. А-карбоксилаза (Синтез ВЖК)
Регуляция активности путем ассоциации/диссоциации • Ассоциация – ковалентная химическая модификация обратимая • Ферменты - олигомерные белки. + E неактивный E активный Пример – ацетил. Ко. А-карбоксилаза (Синтез ВЖК)
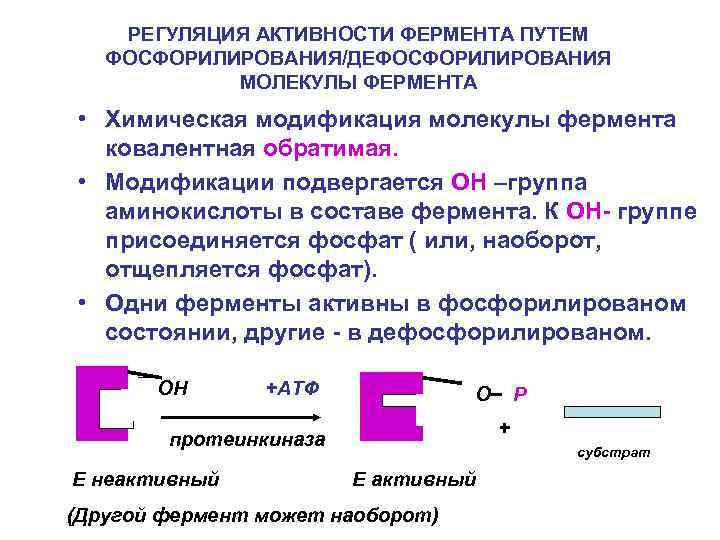 РЕГУЛЯЦИЯ АКТИВНОСТИ ФЕРМЕНТА ПУТЕМ ФОСФОРИЛИРОВАНИЯ/ДЕФОСФОРИЛИРОВАНИЯ МОЛЕКУЛЫ ФЕРМЕНТА • Химическая модификация молекулы фермента ковалентная обратимая. • Модификации подвергается ОН –группа аминокислоты в составе фермента. К ОН- группе присоединяется фосфат ( или, наоборот, отщепляется фосфат). • Одни ферменты активны в фосфорилированом состоянии, другие - в дефосфорилированом. ОН +АТФ О + протеинкиназа E неактивный Р субстрат E активный (Другой фермент может наоборот)
РЕГУЛЯЦИЯ АКТИВНОСТИ ФЕРМЕНТА ПУТЕМ ФОСФОРИЛИРОВАНИЯ/ДЕФОСФОРИЛИРОВАНИЯ МОЛЕКУЛЫ ФЕРМЕНТА • Химическая модификация молекулы фермента ковалентная обратимая. • Модификации подвергается ОН –группа аминокислоты в составе фермента. К ОН- группе присоединяется фосфат ( или, наоборот, отщепляется фосфат). • Одни ферменты активны в фосфорилированом состоянии, другие - в дефосфорилированом. ОН +АТФ О + протеинкиназа E неактивный Р субстрат E активный (Другой фермент может наоборот)
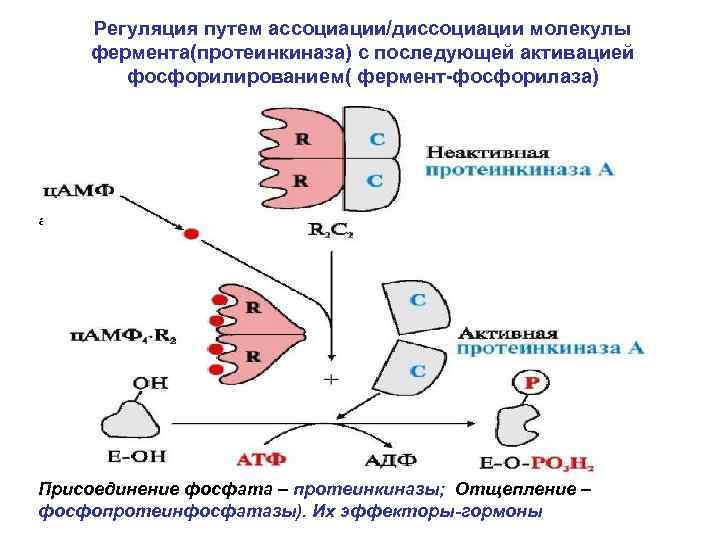 Регуляция путем ассоциации/диссоциации молекулы фермента(протеинкиназа) с последующей активацией фосфорилированием( фермент-фосфорилаза) активатор Присоединение фосфата – протеинкиназы; Отщепление – фосфопротеинфосфатазы). Их эффекторы-гормоны
Регуляция путем ассоциации/диссоциации молекулы фермента(протеинкиназа) с последующей активацией фосфорилированием( фермент-фосфорилаза) активатор Присоединение фосфата – протеинкиназы; Отщепление – фосфопротеинфосфатазы). Их эффекторы-гормоны
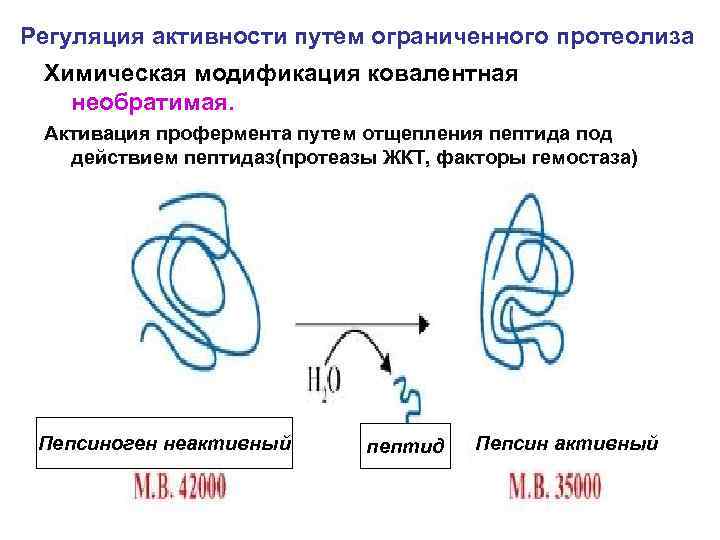 Регуляция активности путем ограниченного протеолиза Химическая модификация ковалентная необратимая. Активация профермента путем отщепления пептида под действием пептидаз(протеазы ЖКТ, факторы гемостаза) Пепсиноген неактивный пептид Пепсин активный
Регуляция активности путем ограниченного протеолиза Химическая модификация ковалентная необратимая. Активация профермента путем отщепления пептида под действием пептидаз(протеазы ЖКТ, факторы гемостаза) Пепсиноген неактивный пептид Пепсин активный
 Изоферменты • Изоферменты – множественные формы ферментов, которые катализируют один тип реакции в разных тканях, но отличаются по составу, заряду и иммунологическим свойствам. • Это олигомерные белки. • например: лактатдегидрогеназа: Лактат +НАД Пировиноградная кислота +НАДН это тетрамер состоит из двух типов протомеров (субъединиц), Н – сердце ( heart) и М –мышцы( muscle) – Существует 5 изомеров. Строго распределены по органам. ЛДГ 1(Н 4); ЛДГ 2 (Н 3 М 1); ЛДГ 3 (Н 2 М 2); ЛДГ 4 (Н 1 М 3); ЛДГ 5 (М 4) Определяются с помощью электрофореза. Принцип методаразная скорость движения в электрическом поле всвязи с разным зарядом и ММ.
Изоферменты • Изоферменты – множественные формы ферментов, которые катализируют один тип реакции в разных тканях, но отличаются по составу, заряду и иммунологическим свойствам. • Это олигомерные белки. • например: лактатдегидрогеназа: Лактат +НАД Пировиноградная кислота +НАДН это тетрамер состоит из двух типов протомеров (субъединиц), Н – сердце ( heart) и М –мышцы( muscle) – Существует 5 изомеров. Строго распределены по органам. ЛДГ 1(Н 4); ЛДГ 2 (Н 3 М 1); ЛДГ 3 (Н 2 М 2); ЛДГ 4 (Н 1 М 3); ЛДГ 5 (М 4) Определяются с помощью электрофореза. Принцип методаразная скорость движения в электрическом поле всвязи с разным зарядом и ММ.


