17e40b0480ea4f17ad308233653865e5.ppt
- Количество слайдов: 20
 Региональная медико-фармацевтическая научно-практическая конференция и профессиональный конкурс «МЕДФАРМКОНВЕНЦИЯ-2006» г. Курск 25 - 26 мая 2006 Организация государственного контроля проведения клинических исследований лекарственных средств в Российской Федерации Ю. В. Афончиков, Т. Н. Николаева, С. В. Романова, С. В. Филюнин Отдел организации государственного контроля доклинических исследований лекарственных средств Росздравнадзора
Региональная медико-фармацевтическая научно-практическая конференция и профессиональный конкурс «МЕДФАРМКОНВЕНЦИЯ-2006» г. Курск 25 - 26 мая 2006 Организация государственного контроля проведения клинических исследований лекарственных средств в Российской Федерации Ю. В. Афончиков, Т. Н. Николаева, С. В. Романова, С. В. Филюнин Отдел организации государственного контроля доклинических исследований лекарственных средств Росздравнадзора
 Нормативные документы Ø Федеральный закон «О лекарственных средствах» (22. 06. 1998 № 86 -ФЗ) Ø ОСТ 42 -511 -99 «Правила проведения качественных клинических исследований в Российской Федерации» Ø Приказ Минздрава России «Об утверждении Правил клинической практики в Российской Федерации» (19. 06. 2003 № 266) 2
Нормативные документы Ø Федеральный закон «О лекарственных средствах» (22. 06. 1998 № 86 -ФЗ) Ø ОСТ 42 -511 -99 «Правила проведения качественных клинических исследований в Российской Федерации» Ø Приказ Минздрава России «Об утверждении Правил клинической практики в Российской Федерации» (19. 06. 2003 № 266) 2
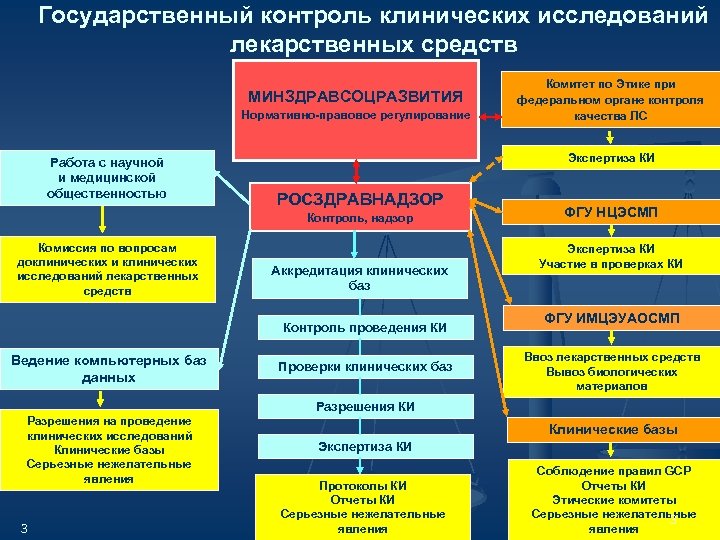 Государственный контроль клинических исследований лекарственных средств МИНЗДРАВСОЦРАЗВИТИЯ Нормативно-правовое регулирование Работа с научной и медицинской общественностью Экспертиза КИ РОСЗДРАВНАДЗОР Контроль, надзор Комиссия по вопросам доклинических исследований лекарственных средств Аккредитация клинических баз Контроль проведения КИ Ведение компьютерных баз данных Комитет по Этике при федеральном органе контроля качества ЛС Проверки клинических баз ФГУ НЦЭСМП Экспертиза КИ Участие в проверках КИ ФГУ ИМЦЭУАОСМП Ввоз лекарственных средств Вывоз биологических материалов Разрешения КИ Разрешения на проведение клинических исследований Клинические базы Серьезные нежелательные явления 3 Клинические базы Экспертиза КИ Протоколы КИ Отчеты КИ Серьезные нежелательные явления Соблюдение правил GCP Отчеты КИ о результатах КИ Этические комитеты Серьезные нежелательные 3 явления
Государственный контроль клинических исследований лекарственных средств МИНЗДРАВСОЦРАЗВИТИЯ Нормативно-правовое регулирование Работа с научной и медицинской общественностью Экспертиза КИ РОСЗДРАВНАДЗОР Контроль, надзор Комиссия по вопросам доклинических исследований лекарственных средств Аккредитация клинических баз Контроль проведения КИ Ведение компьютерных баз данных Комитет по Этике при федеральном органе контроля качества ЛС Проверки клинических баз ФГУ НЦЭСМП Экспертиза КИ Участие в проверках КИ ФГУ ИМЦЭУАОСМП Ввоз лекарственных средств Вывоз биологических материалов Разрешения КИ Разрешения на проведение клинических исследований Клинические базы Серьезные нежелательные явления 3 Клинические базы Экспертиза КИ Протоколы КИ Отчеты КИ Серьезные нежелательные явления Соблюдение правил GCP Отчеты КИ о результатах КИ Этические комитеты Серьезные нежелательные 3 явления
 ФЕДЕРАЛЬНАЯ СЛУЖБА ПО НАДЗОРУ В СФЕРЕ ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ (РОСЗДРАВНАДЗОР) ПРИКАЗ от 26 января 2005 г. № 115 -Пр/05 О создании Комиссии по вопросам доклинических исследований лекарственных средств ПРИКАЗ от 30 июня 2005 г. № 1412 -Пр/05 О внесении изменений в приказ Росздравнадзора от 26. 01. 2005 № 115 -Пр/05 4
ФЕДЕРАЛЬНАЯ СЛУЖБА ПО НАДЗОРУ В СФЕРЕ ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ (РОСЗДРАВНАДЗОР) ПРИКАЗ от 26 января 2005 г. № 115 -Пр/05 О создании Комиссии по вопросам доклинических исследований лекарственных средств ПРИКАЗ от 30 июня 2005 г. № 1412 -Пр/05 О внесении изменений в приказ Росздравнадзора от 26. 01. 2005 № 115 -Пр/05 4
 ФЕДЕРАЛЬНАЯ СЛУЖБА ПО НАДЗОРУ В СФЕРЕ ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ (РОСЗДРАВНАДЗОР) ПРИКАЗ от 21 сентября 2005 г. № 2042 -Пр/05 О проведении мероприятий по контролю 5
ФЕДЕРАЛЬНАЯ СЛУЖБА ПО НАДЗОРУ В СФЕРЕ ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ (РОСЗДРАВНАДЗОР) ПРИКАЗ от 21 сентября 2005 г. № 2042 -Пр/05 О проведении мероприятий по контролю 5
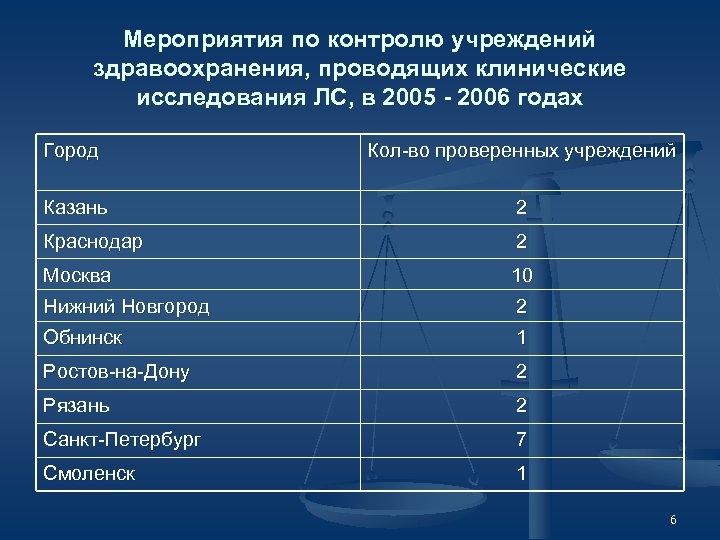 Мероприятия по контролю учреждений здравоохранения, проводящих клинические исследования ЛС, в 2005 - 2006 годах Город Кол-во проверенных учреждений Казань 2 Краснодар 2 Москва 10 Нижний Новгород 2 Обнинск 1 Ростов-на-Дону 2 Рязань 2 Санкт-Петербург 7 Смоленск 1 6
Мероприятия по контролю учреждений здравоохранения, проводящих клинические исследования ЛС, в 2005 - 2006 годах Город Кол-во проверенных учреждений Казань 2 Краснодар 2 Москва 10 Нижний Новгород 2 Обнинск 1 Ростов-на-Дону 2 Рязань 2 Санкт-Петербург 7 Смоленск 1 6
 www. roszdravnadzor. ru 7
www. roszdravnadzor. ru 7
 Субъектам обращения лекарственных средств ФЕДЕРАЛЬНАЯ СЛУЖБА ПО НАДЗОРУ В СФЕРЕ ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ 109074, МОСКВА, СЛАВЯНСКАЯ ПЛ. , Д. 4, СТР. 1 О Перечне учреждений здравоохранения, имеющих право проводить клинические исследования лекарственных средств № 01 И - 417/06 от 22. 05. 2006 Федеральная служба по надзору в сфере здравоохранения и социального развития доводит до Вашего сведения Перечень учреждений здравоохранения, имеющих право проводить клинические исследования лекарственных средств (по состоянию на 12. 05. 2006). 8
Субъектам обращения лекарственных средств ФЕДЕРАЛЬНАЯ СЛУЖБА ПО НАДЗОРУ В СФЕРЕ ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ 109074, МОСКВА, СЛАВЯНСКАЯ ПЛ. , Д. 4, СТР. 1 О Перечне учреждений здравоохранения, имеющих право проводить клинические исследования лекарственных средств № 01 И - 417/06 от 22. 05. 2006 Федеральная служба по надзору в сфере здравоохранения и социального развития доводит до Вашего сведения Перечень учреждений здравоохранения, имеющих право проводить клинические исследования лекарственных средств (по состоянию на 12. 05. 2006). 8
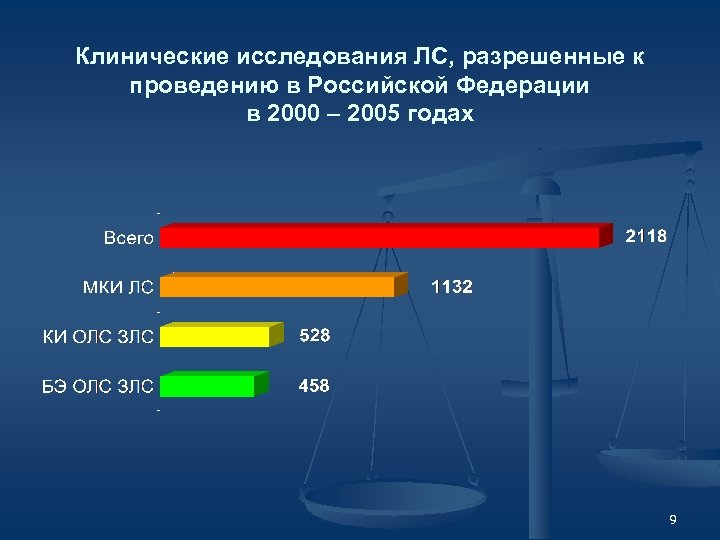 Клинические исследования ЛС, разрешенные к проведению в Российской Федерации в 2000 – 2005 годах 9
Клинические исследования ЛС, разрешенные к проведению в Российской Федерации в 2000 – 2005 годах 9
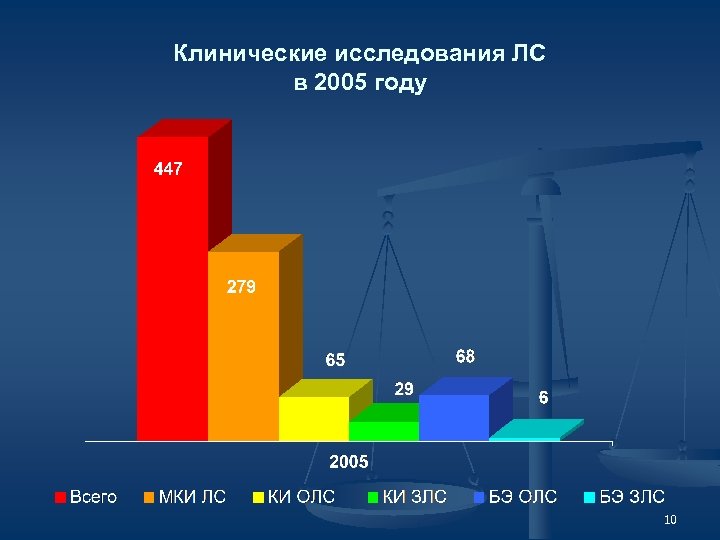 Клинические исследования ЛС в 2005 году 10
Клинические исследования ЛС в 2005 году 10
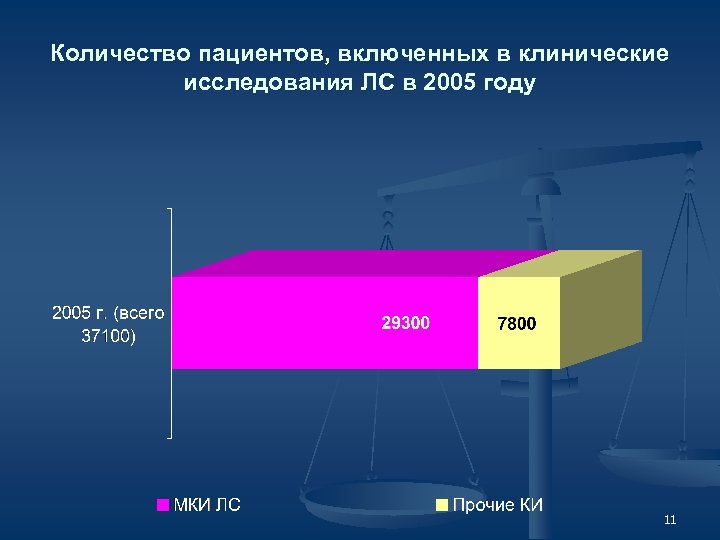 Количество пациентов, включенных в клинические исследования ЛС в 2005 году 11
Количество пациентов, включенных в клинические исследования ЛС в 2005 году 11
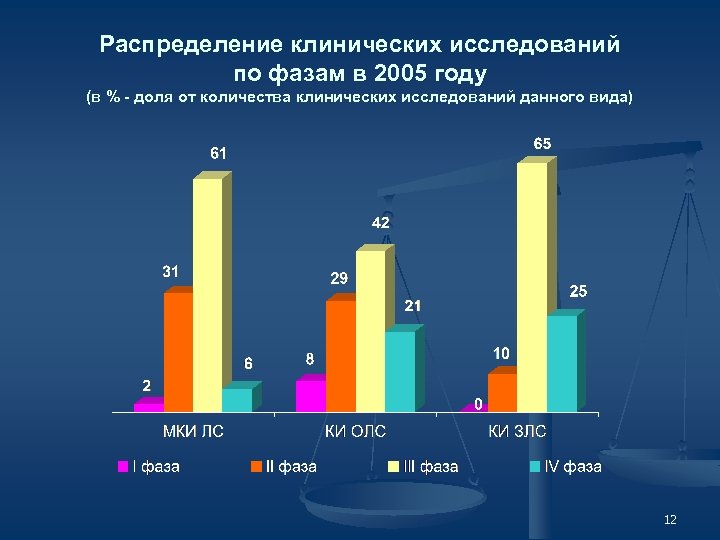 Распределение клинических исследований по фазам в 2005 году (в % - доля от количества клинических исследований данного вида) 12
Распределение клинических исследований по фазам в 2005 году (в % - доля от количества клинических исследований данного вида) 12
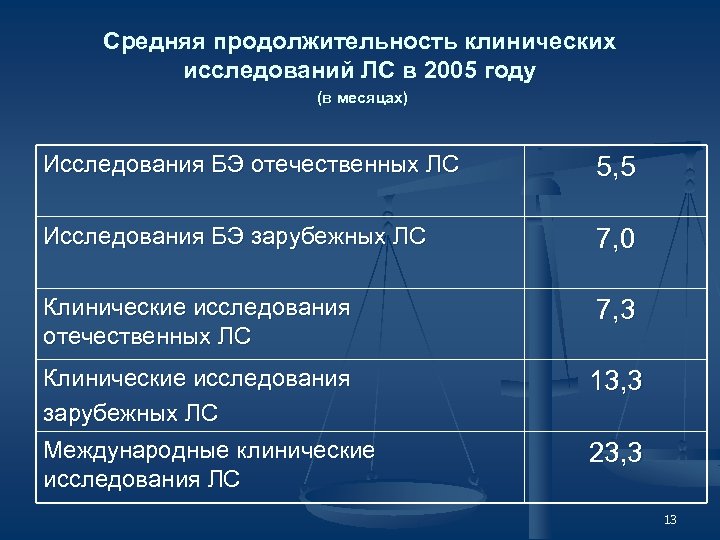 Средняя продолжительность клинических исследований ЛС в 2005 году (в месяцах) Исследования БЭ отечественных ЛС 5, 5 Исследования БЭ зарубежных ЛС 7, 0 Клинические исследования отечественных ЛС 7, 3 Клинические исследования зарубежных ЛС Международные клинические исследования ЛС 13, 3 23, 3 13
Средняя продолжительность клинических исследований ЛС в 2005 году (в месяцах) Исследования БЭ отечественных ЛС 5, 5 Исследования БЭ зарубежных ЛС 7, 0 Клинические исследования отечественных ЛС 7, 3 Клинические исследования зарубежных ЛС Международные клинические исследования ЛС 13, 3 23, 3 13
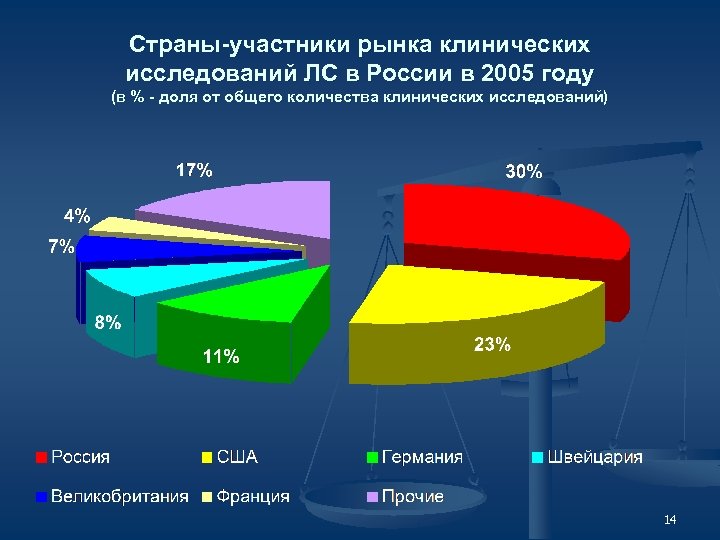 Страны-участники рынка клинических исследований ЛС в России в 2005 году (в % - доля от общего количества клинических исследований) 14
Страны-участники рынка клинических исследований ЛС в России в 2005 году (в % - доля от общего количества клинических исследований) 14
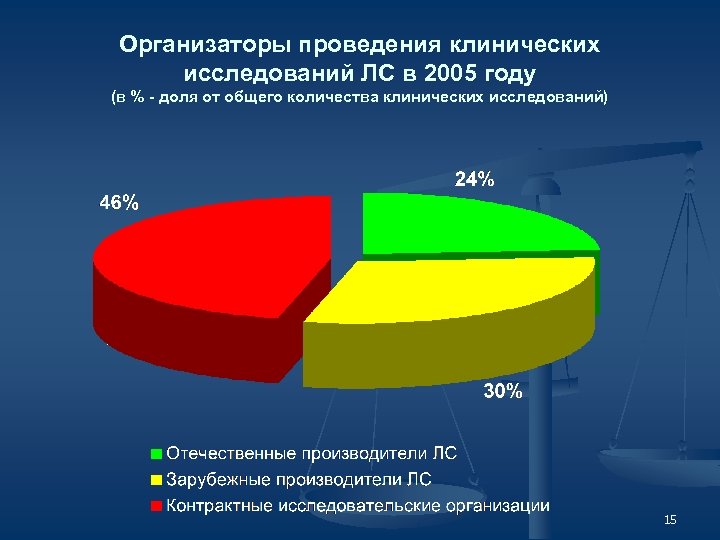 Организаторы проведения клинических исследований ЛС в 2005 году (в % - доля от общего количества клинических исследований) 15
Организаторы проведения клинических исследований ЛС в 2005 году (в % - доля от общего количества клинических исследований) 15
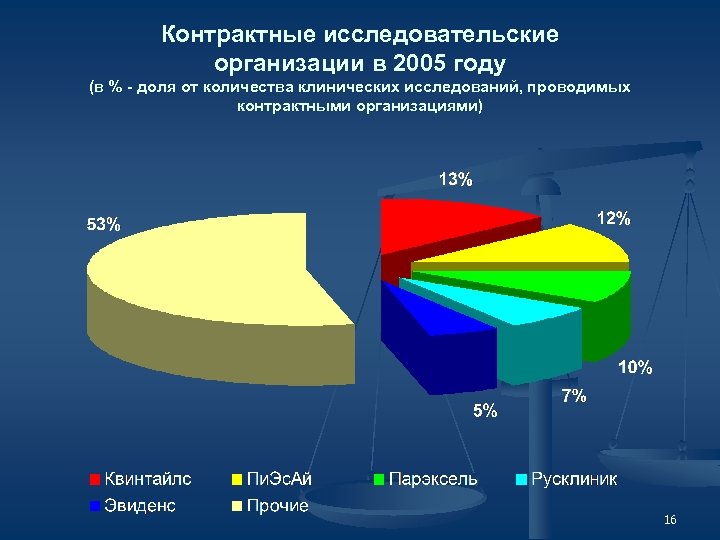 Контрактные исследовательские организации в 2005 году (в % - доля от количества клинических исследований, проводимых контрактными организациями) 16
Контрактные исследовательские организации в 2005 году (в % - доля от количества клинических исследований, проводимых контрактными организациями) 16
 Производители ЛС в 2005 году (количество исследований, проводимых производителями непосредственно и с участием контрактных организаций) Отечественные производители ЛС Зарубежные производители ЛС Щелковский витаминный завод 9 Пфайзер 22 Верофарм 7 Глаксо. Смит. Кляйн 21 Нижфарм 6 Новартис 18 Синтез 6 Санофи-Авентис 16 НИОПИК 6 Джонсон и Джонсон 15 17
Производители ЛС в 2005 году (количество исследований, проводимых производителями непосредственно и с участием контрактных организаций) Отечественные производители ЛС Зарубежные производители ЛС Щелковский витаминный завод 9 Пфайзер 22 Верофарм 7 Глаксо. Смит. Кляйн 21 Нижфарм 6 Новартис 18 Синтез 6 Санофи-Авентис 16 НИОПИК 6 Джонсон и Джонсон 15 17
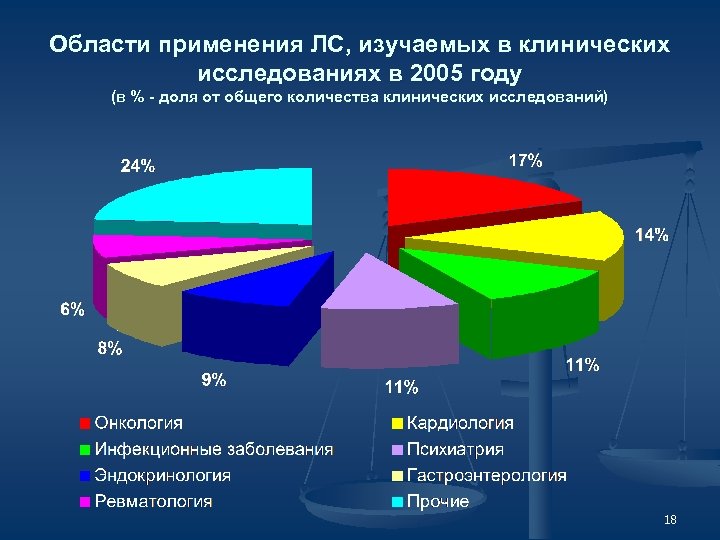 Области применения ЛС, изучаемых в клинических исследованиях в 2005 году (в % - доля от общего количества клинических исследований) 18
Области применения ЛС, изучаемых в клинических исследованиях в 2005 году (в % - доля от общего количества клинических исследований) 18
 Области применения ЛС, изучаемых в международных клинических исследованиях (в % - доля от общего количества международных исследований) Онкология 23, 7% Психиатрия 14, 3% Кардиология 10, 7% Эндокринология 10, 0% Гастроэнтерология 7, 2% 19
Области применения ЛС, изучаемых в международных клинических исследованиях (в % - доля от общего количества международных исследований) Онкология 23, 7% Психиатрия 14, 3% Кардиология 10, 7% Эндокринология 10, 0% Гастроэнтерология 7, 2% 19
 Области применения отечественных ЛС, изучаемых в клинических исследованиях (в % - доля от общего количества КИ ОЛС и БЭ ОЛС) Инфекционные заболевания 24, 8% Кардиология 22, 5% Ревматология 9, 0% Гастроэнтерология 6, 8% Онкология 6, 0% 20
Области применения отечественных ЛС, изучаемых в клинических исследованиях (в % - доля от общего количества КИ ОЛС и БЭ ОЛС) Инфекционные заболевания 24, 8% Кардиология 22, 5% Ревматология 9, 0% Гастроэнтерология 6, 8% Онкология 6, 0% 20


