Лекция 10-2012(ОВР2).ppt
- Количество слайдов: 19
 Редоксметрия 1. Устойчивость водных растворов окислителей и восстановителей. 2. Перманганатометрия. Кривые титрования 3. Хроматометрия. Выбор индикатора 4. Йодометрия. Методы предварительного окислениявосстановления
Редоксметрия 1. Устойчивость водных растворов окислителей и восстановителей. 2. Перманганатометрия. Кривые титрования 3. Хроматометрия. Выбор индикатора 4. Йодометрия. Методы предварительного окислениявосстановления
 Устойчивость водных растворов окислителей и восстановителей Вода Н 2+О 2 - может быть окислителем или восстановителем Вода как восстановитель О 2 + 4 Н+ + 4 е- → 2 Н 2 О 2 - Е 0 = 1, 23 В Реальный потенциал зависит от р. Н: Е 0/ = 1, 23 – 0, 059 р. Н Вода как окислитель 2 Н 2 О + 2 е- → Н 2 + 2 ОНИли: 2 Н+ + 2 е- → Н 2 Е 0 = 0, 0 В Реальный потенциал: Е 0/ = 0, 0 – 0, 059 р. Н ( при р. Н = 0 )
Устойчивость водных растворов окислителей и восстановителей Вода Н 2+О 2 - может быть окислителем или восстановителем Вода как восстановитель О 2 + 4 Н+ + 4 е- → 2 Н 2 О 2 - Е 0 = 1, 23 В Реальный потенциал зависит от р. Н: Е 0/ = 1, 23 – 0, 059 р. Н Вода как окислитель 2 Н 2 О + 2 е- → Н 2 + 2 ОНИли: 2 Н+ + 2 е- → Н 2 Е 0 = 0, 0 В Реальный потенциал: Е 0/ = 0, 0 – 0, 059 р. Н ( при р. Н = 0 )
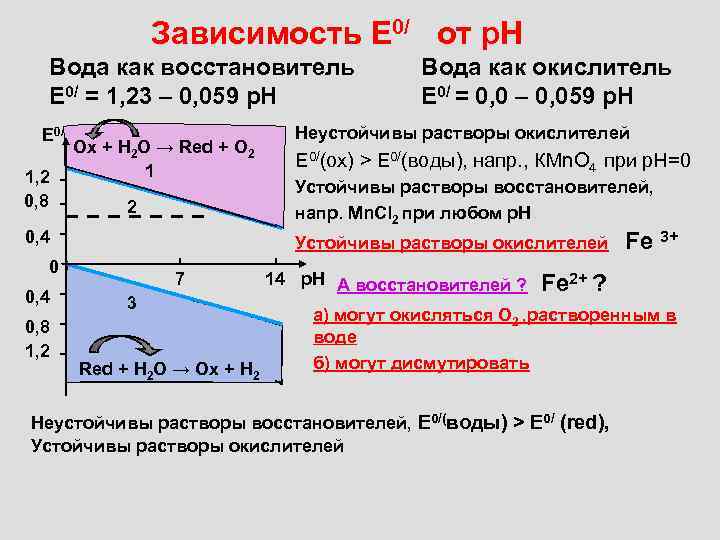 Зависимость Е 0/ от р. Н Вода как восстановитель Е 0/ = 1, 23 – 0, 059 р. Н Е 0/ 1, 2 0, 8 Ох + Н 2 О → Red + О 2 1 2 0, 4 0, 8 1, 2 Неустойчивы растворы окислителей Е 0/(ох) > Е 0/(воды), напр. , КМn. О 4 при р. Н=0 Устойчивы растворы восстановителей, напр. Мn. Cl 2 при любом р. Н Устойчивы растворы окислителей 0 0, 4 Вода как окислитель Е 0/ = 0, 0 – 0, 059 р. Н 7 3 Red + Н 2 О → Ox + H 2 14 р. Н А восстановителей ? Fe 3+ Fe 2+ ? а) могут окисляться О 2 , растворенным в воде б) могут дисмутировать Неустойчивы растворы восстановителей, Е 0/(воды) > Е 0/ (red), Устойчивы растворы окислителей
Зависимость Е 0/ от р. Н Вода как восстановитель Е 0/ = 1, 23 – 0, 059 р. Н Е 0/ 1, 2 0, 8 Ох + Н 2 О → Red + О 2 1 2 0, 4 0, 8 1, 2 Неустойчивы растворы окислителей Е 0/(ох) > Е 0/(воды), напр. , КМn. О 4 при р. Н=0 Устойчивы растворы восстановителей, напр. Мn. Cl 2 при любом р. Н Устойчивы растворы окислителей 0 0, 4 Вода как окислитель Е 0/ = 0, 0 – 0, 059 р. Н 7 3 Red + Н 2 О → Ox + H 2 14 р. Н А восстановителей ? Fe 3+ Fe 2+ ? а) могут окисляться О 2 , растворенным в воде б) могут дисмутировать Неустойчивы растворы восстановителей, Е 0/(воды) > Е 0/ (red), Устойчивы растворы окислителей
 Оценка устойчивости растворов восстановителей Fe. Cl 2 Fe 3+ + e- = Fe 2+ E 0 = 0, 77 B С водой не взаимодействует Окисление О 2 , растворенным в воде О 2 + 4 Н+ + 4 е- → 2 Н 2 О При р. Н = 7 : Е 0 = 1, 23 В Е 0/ = 1, 23 – 0, 059. 7 ≈ 0, 8 В не будет окисляться кислородом ! Дисмутация Fe 3+ + e- = Fe 2+ + 2 e- = Fe 0 e- Fe 3+ ← Fe 2+ + Fe 2+ → Fe 0 E 0 = 0, 77 B (Fe 2+ - восстановитель) E 0 = -0, 44 B ( Fe 2+ - окислитель) не будет дисмутировать! Вывод: растворы Fe. Cl 2 устойчивы в нейтральной среде
Оценка устойчивости растворов восстановителей Fe. Cl 2 Fe 3+ + e- = Fe 2+ E 0 = 0, 77 B С водой не взаимодействует Окисление О 2 , растворенным в воде О 2 + 4 Н+ + 4 е- → 2 Н 2 О При р. Н = 7 : Е 0 = 1, 23 В Е 0/ = 1, 23 – 0, 059. 7 ≈ 0, 8 В не будет окисляться кислородом ! Дисмутация Fe 3+ + e- = Fe 2+ + 2 e- = Fe 0 e- Fe 3+ ← Fe 2+ + Fe 2+ → Fe 0 E 0 = 0, 77 B (Fe 2+ - восстановитель) E 0 = -0, 44 B ( Fe 2+ - окислитель) не будет дисмутировать! Вывод: растворы Fe. Cl 2 устойчивы в нейтральной среде
 Sn. Cl 2 Sn 4+ + 2 e- = Sn 2+ E 0 = 0, 15 B С водой не взаимодействует Окисление О 2 , растворенным в воде О 2 + 4 Н+ + 4 е- → 2 Н 2 О При р. Н = 7 : Е 0 = 1, 23 В Е 0/ = 1, 23 – 0, 059. 7 ≈ 0, 8 В будет окисляться кислородом ! Дисмутация e- Sn 4+ ← Sn 2+ + Sn 2+ → Sn 0 Sn 4+ + 2 e- = Sn 2+ E 0 = 0, 15 B (Sn 2+ - восстановитель) Sn 2+ + 2 e- = Sn 0 E 0 = -0, 14 B ( Sn 2+ - окислитель) не будет дисмутировать! Вывод: растворы Sn. Cl 2 неустойчивы– окисляются растворенным в воде О 2
Sn. Cl 2 Sn 4+ + 2 e- = Sn 2+ E 0 = 0, 15 B С водой не взаимодействует Окисление О 2 , растворенным в воде О 2 + 4 Н+ + 4 е- → 2 Н 2 О При р. Н = 7 : Е 0 = 1, 23 В Е 0/ = 1, 23 – 0, 059. 7 ≈ 0, 8 В будет окисляться кислородом ! Дисмутация e- Sn 4+ ← Sn 2+ + Sn 2+ → Sn 0 Sn 4+ + 2 e- = Sn 2+ E 0 = 0, 15 B (Sn 2+ - восстановитель) Sn 2+ + 2 e- = Sn 0 E 0 = -0, 14 B ( Sn 2+ - окислитель) не будет дисмутировать! Вывод: растворы Sn. Cl 2 неустойчивы– окисляются растворенным в воде О 2
 Редокс-реакции в титриметрии Часто применяемые методы: Перманганатометрия Титрант – KMn. O 4 Хроматометрия Титрант – K 2 Cr 2 O 7 Йодометрия Титранты – I 2, Na 2 S 2 O 3 Эквивалент вещества в ОВР: отношение молярной массы (M)к числу отданных или принятых электронов(n) Э = М/n
Редокс-реакции в титриметрии Часто применяемые методы: Перманганатометрия Титрант – KMn. O 4 Хроматометрия Титрант – K 2 Cr 2 O 7 Йодометрия Титранты – I 2, Na 2 S 2 O 3 Эквивалент вещества в ОВР: отношение молярной массы (M)к числу отданных или принятых электронов(n) Э = М/n
 Перманганатометрия Е 0 = 1, 51 В Mn. O 4 - + 8 H+ + 5 e- = Mn 2+ + 4 H 2 O Выбор р. Н для хранения растворов КMn. O 4 Вода как восстановитель О 2 + 4 Н+ + 4 е- → 2 Н 2 О 2 Е 0 = 1, 23 В ( при р. Н = 0 ) При р. Н = 7 : Вода : Е 0/ = 1, 23 – 0, 059. 7 ≈ 0, 8 В Вывод: растворы Кмn. О 4 устойчивы в нейтральной среде. Их готовят по примерной навеске КMn. O 4.
Перманганатометрия Е 0 = 1, 51 В Mn. O 4 - + 8 H+ + 5 e- = Mn 2+ + 4 H 2 O Выбор р. Н для хранения растворов КMn. O 4 Вода как восстановитель О 2 + 4 Н+ + 4 е- → 2 Н 2 О 2 Е 0 = 1, 23 В ( при р. Н = 0 ) При р. Н = 7 : Вода : Е 0/ = 1, 23 – 0, 059. 7 ≈ 0, 8 В Вывод: растворы Кмn. О 4 устойчивы в нейтральной среде. Их готовят по примерной навеске КMn. O 4.
 Стандартизация растворов Кмn. О 4 Щавелевая кислота, оксалат натрия 5 C 2 O 4 2 - + 2 Mn. O 4 - + 8 H+ = 10 CO 2 + 2 Mn 2+ + 4 H 2 O Хранят растворы Кмn. О 4 в склянках темного стекла. Титрование ведут в среде серной кислоты при нагревании, без индикатора. Определяют восстановители: - неорганические (прямое титрование) -органические (обратное титрование, титрант- Fe 2+) -неустойчивые (заместительное титрование) Окислители: -обратное титрование
Стандартизация растворов Кмn. О 4 Щавелевая кислота, оксалат натрия 5 C 2 O 4 2 - + 2 Mn. O 4 - + 8 H+ = 10 CO 2 + 2 Mn 2+ + 4 H 2 O Хранят растворы Кмn. О 4 в склянках темного стекла. Титрование ведут в среде серной кислоты при нагревании, без индикатора. Определяют восстановители: - неорганические (прямое титрование) -органические (обратное титрование, титрант- Fe 2+) -неустойчивые (заместительное титрование) Окислители: -обратное титрование
 Кривые титрования – зависимость потенциала раствора от степени оттитрванности, f n 2 Red 1 + n 1 Ox 2 ↔ n 2 Ox 1 + n 1 Red 2 титран Ох 1 + n 1 e Red 1 Е 01 Ох 2 + n 2 e Red 2 Е 02 До т. э. расчет ведут по уравнению Нернста системы титруемого вещества, после т. э. – по системе титранта.
Кривые титрования – зависимость потенциала раствора от степени оттитрванности, f n 2 Red 1 + n 1 Ox 2 ↔ n 2 Ox 1 + n 1 Red 2 титран Ох 1 + n 1 e Red 1 Е 01 Ох 2 + n 2 e Red 2 Е 02 До т. э. расчет ведут по уравнению Нернста системы титруемого вещества, после т. э. – по системе титранта.
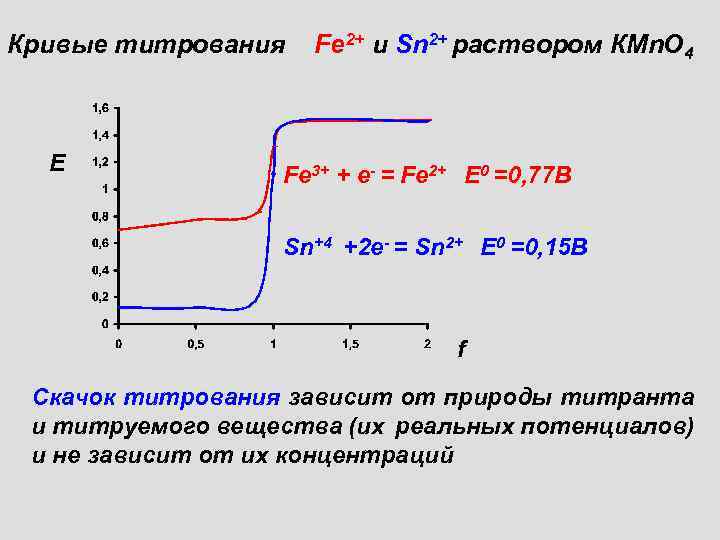 Кривые титрования Е Fe 2+ и Sn 2+ раствором КМn. О 4 Fe 3+ + е- = Fe 2+ Е 0 =0, 77 В Sn+4 +2 е- = Sn 2+ Е 0 =0, 15 В f Скачок титрования зависит от природы титранта и титруемого вещества (их реальных потенциалов) и не зависит от их концентраций
Кривые титрования Е Fe 2+ и Sn 2+ раствором КМn. О 4 Fe 3+ + е- = Fe 2+ Е 0 =0, 77 В Sn+4 +2 е- = Sn 2+ Е 0 =0, 15 В f Скачок титрования зависит от природы титранта и титруемого вещества (их реальных потенциалов) и не зависит от их концентраций
 Хроматометрия Cr 2 O 7 2 - + 14 H+ + 6 e- = 2 Cr 3+ + 7 H 2 O Е 0 = 1, 36 В При р. Н = 2 растворы K 2 Cr 2 O 7 устойчивы : Вода : Е 0/ = 1, 23 – 0, 059. 2 ≈ 1, 11 В Растворы K 2 Cr 2 O 7 готовят по точной навеске в среде серной кислоты. Стандартизация не требуется. Титрование ведут в кислой среде в присутствии ред-окс индикаторов.
Хроматометрия Cr 2 O 7 2 - + 14 H+ + 6 e- = 2 Cr 3+ + 7 H 2 O Е 0 = 1, 36 В При р. Н = 2 растворы K 2 Cr 2 O 7 устойчивы : Вода : Е 0/ = 1, 23 – 0, 059. 2 ≈ 1, 11 В Растворы K 2 Cr 2 O 7 готовят по точной навеске в среде серной кислоты. Стандартизация не требуется. Титрование ведут в кислой среде в присутствии ред-окс индикаторов.
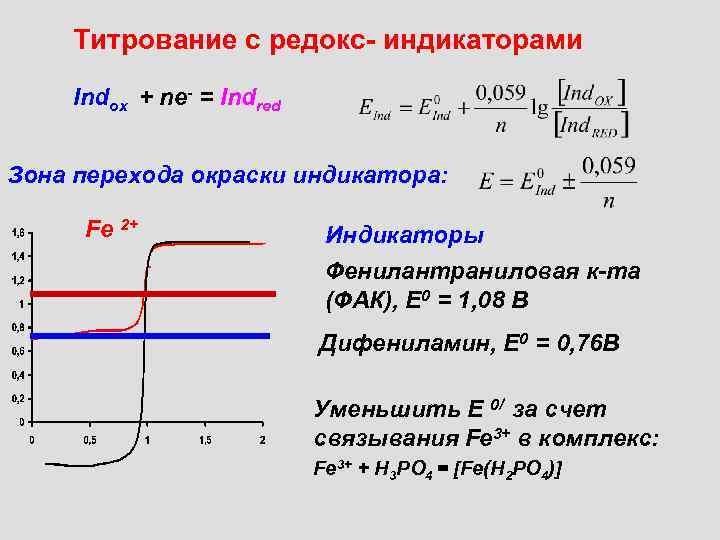 Титрование с редокс- индикаторами Indox + ne- = Indred Зона перехода окраски индикатора: Fe 2+ Индикаторы Фенилантраниловая к-та (ФАК), Е 0 = 1, 08 В Дифениламин, Е 0 = 0, 76 В Уменьшить Е 0/ за счет связывания Fe 3+ в комплекс: Fe 3+ + H 3 PO 4 = [Fe(H 2 PO 4)]
Титрование с редокс- индикаторами Indox + ne- = Indred Зона перехода окраски индикатора: Fe 2+ Индикаторы Фенилантраниловая к-та (ФАК), Е 0 = 1, 08 В Дифениламин, Е 0 = 0, 76 В Уменьшить Е 0/ за счет связывания Fe 3+ в комплекс: Fe 3+ + H 3 PO 4 = [Fe(H 2 PO 4)]
 Йодометрия Титранты: раствор I 2, раствор Na 2 S 2 O 3 вспомогательный раствор KI I 2 +2 e- = 2 I- E 0 = 0, 55 B I 2+ 2 S 2 O 32 -= 2 I-+ S 4 O 62 - + 2 e- = 2 S 2 O 32 - E 0 =0, 09 B Раствор I 2 готовят по примерной навеске в р-ре КI. Стандартизуют фиксанальным раствором Na 2 S 2 O 3. Растворы I 2 , и Na 2 S 2 O 3 неустойчивы при хранении: I 2 может частично испаряться, Na 2 S 2 O 3 – окисляться кислородом, растворенным в воде. Со временем оба раствора требуют стандартизации. Вначале стандартизуют Na 2 S 2 O 3 , затем по нему – раствор иода. КI также неустойчив (окисляется растворенным в воде кислородом) , но его раствор не стандартизуют.
Йодометрия Титранты: раствор I 2, раствор Na 2 S 2 O 3 вспомогательный раствор KI I 2 +2 e- = 2 I- E 0 = 0, 55 B I 2+ 2 S 2 O 32 -= 2 I-+ S 4 O 62 - + 2 e- = 2 S 2 O 32 - E 0 =0, 09 B Раствор I 2 готовят по примерной навеске в р-ре КI. Стандартизуют фиксанальным раствором Na 2 S 2 O 3. Растворы I 2 , и Na 2 S 2 O 3 неустойчивы при хранении: I 2 может частично испаряться, Na 2 S 2 O 3 – окисляться кислородом, растворенным в воде. Со временем оба раствора требуют стандартизации. Вначале стандартизуют Na 2 S 2 O 3 , затем по нему – раствор иода. КI также неустойчив (окисляется растворенным в воде кислородом) , но его раствор не стандартизуют.
 Титрование ведут в широком диапазоне р. Н – от слабощелочной среды до слабокислой, БЕЗ НАГРЕВАНИЯ Индикатор – крахмал. Предварительное окисление-восстановление Титрование редокс - систем, имеющих Е 0 < 0, 55 В Sn 4+ + 2 е- = Sn 2+ Е 0 =0, 15 В Прямое титрование восстановителей I 2 +Sn 2+ = 2 I- + Sn 4+ Титрование окислителей Sn 4+ + 2 е- = Sn 2+ Предварительно восстановить, затем титровать напрямую йодом
Титрование ведут в широком диапазоне р. Н – от слабощелочной среды до слабокислой, БЕЗ НАГРЕВАНИЯ Индикатор – крахмал. Предварительное окисление-восстановление Титрование редокс - систем, имеющих Е 0 < 0, 55 В Sn 4+ + 2 е- = Sn 2+ Е 0 =0, 15 В Прямое титрование восстановителей I 2 +Sn 2+ = 2 I- + Sn 4+ Титрование окислителей Sn 4+ + 2 е- = Sn 2+ Предварительно восстановить, затем титровать напрямую йодом
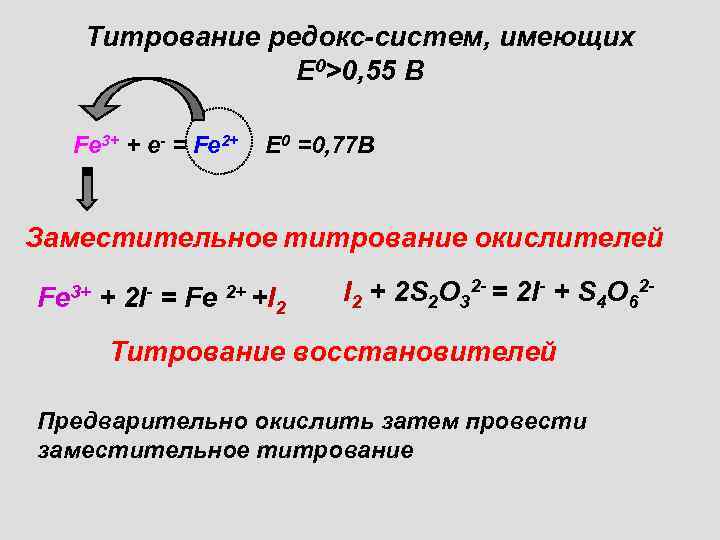 Титрование редокс-систем, имеющих Е 0>0, 55 В Fe 3+ + е- = Fe 2+ Е 0 =0, 77 В Заместительное титрование окислителей Fe 3+ + 2 I- = Fe 2+ +I 2 + 2 S 2 O 32 - = 2 I- + S 4 O 62 - Титрование восстановителей Предварительно окислить затем провести заместительное титрование
Титрование редокс-систем, имеющих Е 0>0, 55 В Fe 3+ + е- = Fe 2+ Е 0 =0, 77 В Заместительное титрование окислителей Fe 3+ + 2 I- = Fe 2+ +I 2 + 2 S 2 O 32 - = 2 I- + S 4 O 62 - Титрование восстановителей Предварительно окислить затем провести заместительное титрование
 Требования к веществам, применяемым для предварительного окисления или восстановления - -Должен количественно переводить определяемый компонент (Х)в необходимую с. о. -Должен легко удаляться из раствора -Если остается в растворе, то не должен мешать дальнейшему определению Х Используют неустойчивые или легко отделяемые от раствора вещества: Н 2 О 2 (окисление) SO 2 , редуктор Джонса (восстановление) Fe 3+ Zn е. Fe 3+ Fe 2+
Требования к веществам, применяемым для предварительного окисления или восстановления - -Должен количественно переводить определяемый компонент (Х)в необходимую с. о. -Должен легко удаляться из раствора -Если остается в растворе, то не должен мешать дальнейшему определению Х Используют неустойчивые или легко отделяемые от раствора вещества: Н 2 О 2 (окисление) SO 2 , редуктор Джонса (восстановление) Fe 3+ Zn е. Fe 3+ Fe 2+
 Йодометрия в анализе нефтепродуктов • Определение суммы непредельных у/в R-(СН=СН 2) + I 2 = R-(СНI- СН 2 I) И. ч. (йодное число)– cколько г(мг) йода ушло на реакцию с 100 г нефтепродукта • Определение воды в жидких органических веществах (смесях) по Фишеру титруют реактивом Фишера (раствор SO 2, I 2 и пиридина в метаноле) Определение органических восстановителей R-COH + I 2+ КОН= R-COOК + КI + H 2 O
Йодометрия в анализе нефтепродуктов • Определение суммы непредельных у/в R-(СН=СН 2) + I 2 = R-(СНI- СН 2 I) И. ч. (йодное число)– cколько г(мг) йода ушло на реакцию с 100 г нефтепродукта • Определение воды в жидких органических веществах (смесях) по Фишеру титруют реактивом Фишера (раствор SO 2, I 2 и пиридина в метаноле) Определение органических восстановителей R-COH + I 2+ КОН= R-COOК + КI + H 2 O
 Йодометрическое определение кислот Основано на реакции иодида и иодата калия в присутствии кислоты. Берут аликвоту кислоты, добавляют избыток KI и KIO 3: 5 KI + KIO 3 + 6 HCl = 3 I 2 + 6 KCl + 3 H 2 O I 2 + 2 Na 2 S 2 O 3 = 2 Na. I + Na 2 S 4 O 6 2 IO 3 - + 10 е- + 12 H+ = I 2 + 6 Н 2 О Е 0 = 1, 19 в При р. Н=9 потенциал системы становится равным 0, 55 В и реакция прекращается. Метод более чувствителен, чем метод нейтрализации
Йодометрическое определение кислот Основано на реакции иодида и иодата калия в присутствии кислоты. Берут аликвоту кислоты, добавляют избыток KI и KIO 3: 5 KI + KIO 3 + 6 HCl = 3 I 2 + 6 KCl + 3 H 2 O I 2 + 2 Na 2 S 2 O 3 = 2 Na. I + Na 2 S 4 O 6 2 IO 3 - + 10 е- + 12 H+ = I 2 + 6 Н 2 О Е 0 = 1, 19 в При р. Н=9 потенциал системы становится равным 0, 55 В и реакция прекращается. Метод более чувствителен, чем метод нейтрализации
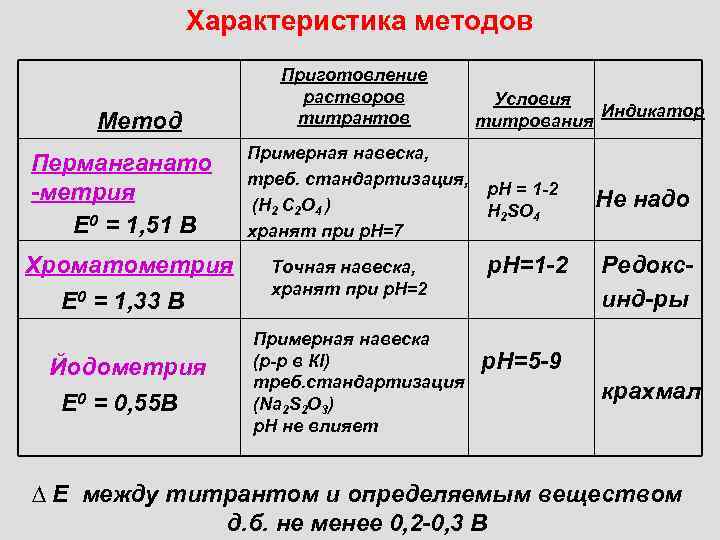 Характеристика методов Метод Перманганато -метрия Е 0 = 1, 51 В Хроматометрия Е 0 = 1, 33 В Йодометрия Е 0 = 0, 55 В Приготовление растворов титрантов Примерная навеска, треб. cтандартизация, (Н 2 С 2 О 4 ) хранят при р. Н=7 Точная навеска, хранят при р. Н=2 Примерная навеска (р-р в КI) треб. стандартизация (Na 2 S 2 O 3) р. Н не влияет Условия Индикатор титрования р. Н = 1 -2 Н 2 SO 4 Не надо р. Н=1 -2 Редоксинд-ры р. Н=5 -9 крахмал ∆ Е между титрантом и определяемым веществом д. б. не менее 0, 2 -0, 3 В
Характеристика методов Метод Перманганато -метрия Е 0 = 1, 51 В Хроматометрия Е 0 = 1, 33 В Йодометрия Е 0 = 0, 55 В Приготовление растворов титрантов Примерная навеска, треб. cтандартизация, (Н 2 С 2 О 4 ) хранят при р. Н=7 Точная навеска, хранят при р. Н=2 Примерная навеска (р-р в КI) треб. стандартизация (Na 2 S 2 O 3) р. Н не влияет Условия Индикатор титрования р. Н = 1 -2 Н 2 SO 4 Не надо р. Н=1 -2 Редоксинд-ры р. Н=5 -9 крахмал ∆ Е между титрантом и определяемым веществом д. б. не менее 0, 2 -0, 3 В


