Везикулярный транспорт Lecture8-signaling2.ppt
- Количество слайдов: 54
 РЕЦЕПТОР ЭПИДЕРМАЛЬНОГО ФАКТОРА РОСТА (ЭФР): ЭНДОЦИТОЗ И ПЕРЕДАЧА СИГНАЛА ЭФР через свой трансмембранный рецептор участвует в эмбриогенезе, регулирует пролиферацию, дифференцировку, апоптоз и подвижность многих типов клеток. В то же время, ЭФР после связывания с рецептором на ПМ подвергается эндоцитозу. ЭФР-рецепторная система, таким образом, является прекрасной моделью для изучения как механизмов регуляции сигналинга и эндоцитоза, так и механизмов координации сигнальных путей и их организации во времени и в пространстве.
РЕЦЕПТОР ЭПИДЕРМАЛЬНОГО ФАКТОРА РОСТА (ЭФР): ЭНДОЦИТОЗ И ПЕРЕДАЧА СИГНАЛА ЭФР через свой трансмембранный рецептор участвует в эмбриогенезе, регулирует пролиферацию, дифференцировку, апоптоз и подвижность многих типов клеток. В то же время, ЭФР после связывания с рецептором на ПМ подвергается эндоцитозу. ЭФР-рецепторная система, таким образом, является прекрасной моделью для изучения как механизмов регуляции сигналинга и эндоцитоза, так и механизмов координации сигнальных путей и их организации во времени и в пространстве.
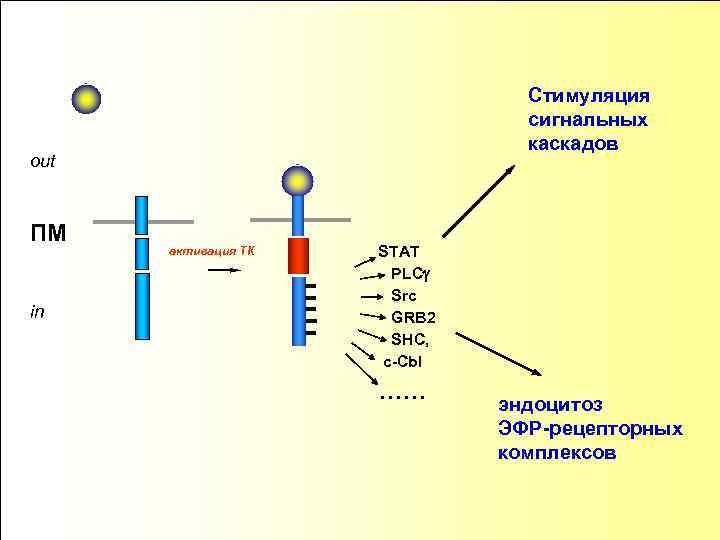 Стимуляция сигнальных каскадов out ПМ in активация ТК STAT PLCg Src GRB 2 SHC, c-Cbl …… эндоцитоз ЭФР-рецепторных комплексов
Стимуляция сигнальных каскадов out ПМ in активация ТК STAT PLCg Src GRB 2 SHC, c-Cbl …… эндоцитоз ЭФР-рецепторных комплексов
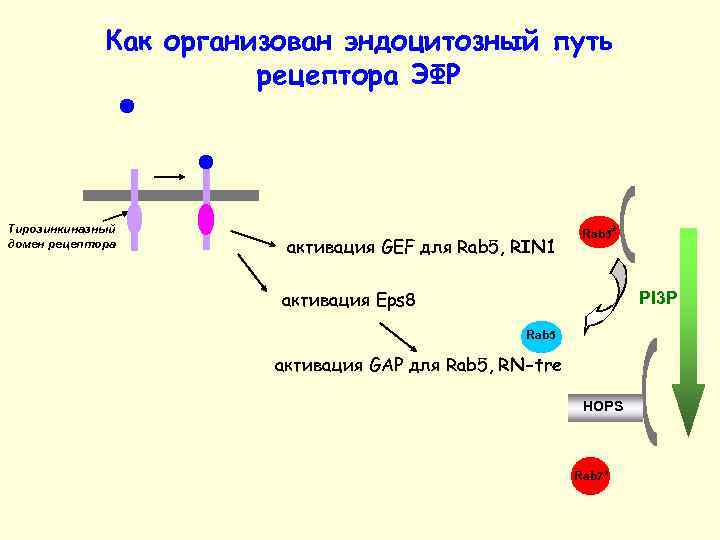 Как организован эндоцитозный путь рецептора ЭФР Тирозинкиназный домен рецептора активация GEF для Rab 5, RIN 1 Rab 5* активация Eps 8 PI 3 P Rab 5 активация GAP для Rab 5, RN-tre HOPS Rab 7*
Как организован эндоцитозный путь рецептора ЭФР Тирозинкиназный домен рецептора активация GEF для Rab 5, RIN 1 Rab 5* активация Eps 8 PI 3 P Rab 5 активация GAP для Rab 5, RN-tre HOPS Rab 7*
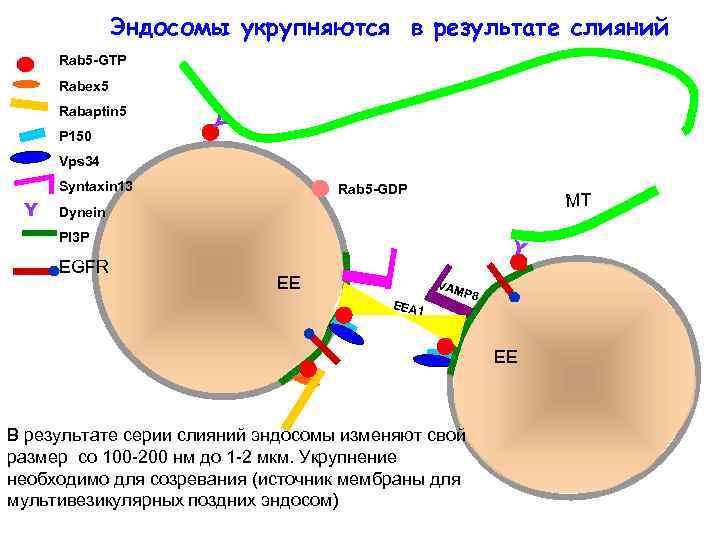 Эндосомы укрупняются в результате слияний Rab 5 -GTP Rabex 5 Rabaptin 5 Y P 150 Vps 34 Syntaxin 13 Y Rab 5 -GDP MT Dynein PI 3 P EGFR Y EE VAM EEA 1 P 8 EE В результате серии слияний эндосомы изменяют свой размер со 100 -200 нм до 1 -2 мкм. Укрупнение необходимо для созревания (источник мембраны для мультивезикулярных поздних эндосом)
Эндосомы укрупняются в результате слияний Rab 5 -GTP Rabex 5 Rabaptin 5 Y P 150 Vps 34 Syntaxin 13 Y Rab 5 -GDP MT Dynein PI 3 P EGFR Y EE VAM EEA 1 P 8 EE В результате серии слияний эндосомы изменяют свой размер со 100 -200 нм до 1 -2 мкм. Укрупнение необходимо для созревания (источник мембраны для мультивезикулярных поздних эндосом)
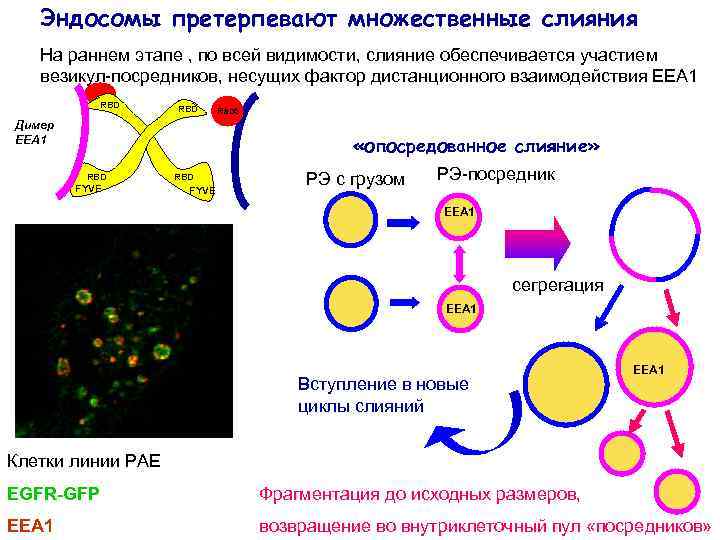 Эндосомы претерпевают множественные слияния На раннем этапе , по всей видимости, слияние обеспечивается участием везикул-посредников, несущих фактор дистанционного взаимодействия ЕЕА 1 RBD Димер ЕЕА 1 Rab 5 «опосредованное слияние» RBD FYVE РЭ с грузом РЭ-посредник ЕЕА 1 сегрегация ЕЕА 1 Вступление в новые циклы слияний ЕЕА 1 Клетки линии РАЕ EGFR-GFP Фрагментация до исходных размеров, EEA 1 возвращение во внутриклеточный пул «посредников»
Эндосомы претерпевают множественные слияния На раннем этапе , по всей видимости, слияние обеспечивается участием везикул-посредников, несущих фактор дистанционного взаимодействия ЕЕА 1 RBD Димер ЕЕА 1 Rab 5 «опосредованное слияние» RBD FYVE РЭ с грузом РЭ-посредник ЕЕА 1 сегрегация ЕЕА 1 Вступление в новые циклы слияний ЕЕА 1 Клетки линии РАЕ EGFR-GFP Фрагментация до исходных размеров, EEA 1 возвращение во внутриклеточный пул «посредников»
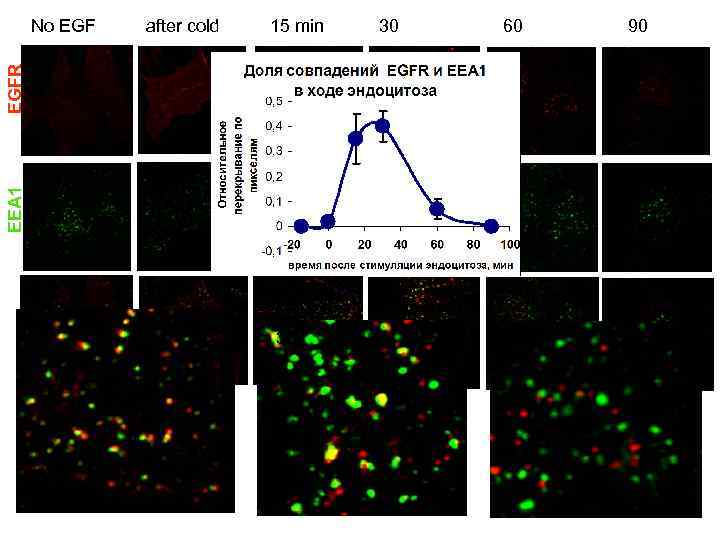 after cold 15 min 30 60 90 EEA 1 EGFR No EGF 15 30 60
after cold 15 min 30 60 90 EEA 1 EGFR No EGF 15 30 60
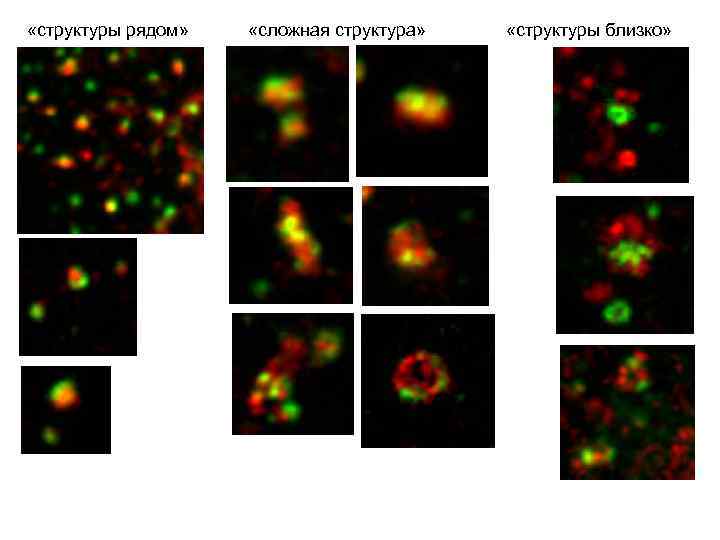 «структуры рядом» «сложная структура» «структуры близко»
«структуры рядом» «сложная структура» «структуры близко»
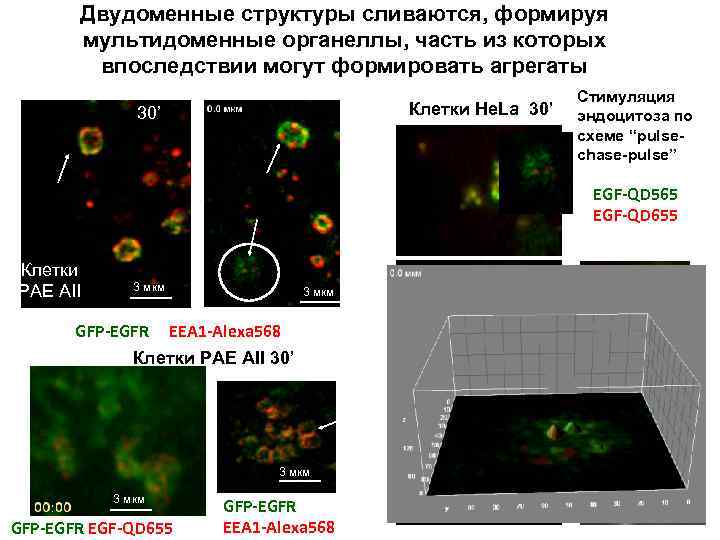 Двудоменные структуры сливаются, формируя мультидоменные органеллы, часть из которых впоследствии могут формировать агрегаты Клетки He. La 30’ Стимуляция эндоцитоза по схеме “pulsechase-pulse” EGF-QD 565 EGF-QD 655 Клетки РАЕ AII 3 мкм GFP-EGFR EEA 1 -Alexa 568 Клетки РАЕ AII 30’ 3 мкм GFP-EGFR EGF-QD 655 GFP-EGFR EEA 1 -Alexa 568
Двудоменные структуры сливаются, формируя мультидоменные органеллы, часть из которых впоследствии могут формировать агрегаты Клетки He. La 30’ Стимуляция эндоцитоза по схеме “pulsechase-pulse” EGF-QD 565 EGF-QD 655 Клетки РАЕ AII 3 мкм GFP-EGFR EEA 1 -Alexa 568 Клетки РАЕ AII 30’ 3 мкм GFP-EGFR EGF-QD 655 GFP-EGFR EEA 1 -Alexa 568
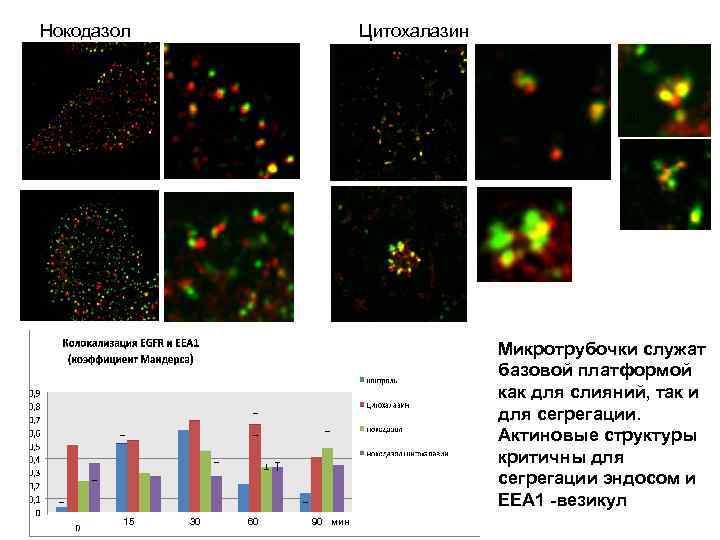 Нокодазол Цитохалазин 15 15 30 60 60 Микротрубочки служат базовой платформой как для слияний, так и для сегрегации. Актиновые структуры критичны для сегрегации эндосом и ЕЕА 1 -везикул 15 30 60 90 мин
Нокодазол Цитохалазин 15 15 30 60 60 Микротрубочки служат базовой платформой как для слияний, так и для сегрегации. Актиновые структуры критичны для сегрегации эндосом и ЕЕА 1 -везикул 15 30 60 90 мин
 ЕЕА 1 -везикулы Укрупнение ранних эндосом опосредуется формированием гибридных структур с участием ЕЕА 1 -везикул эндосомы «вторичные слияния» и/или образование кластеров эндосом и ЕЕА 1 -везикул возвращение ЕЕА 1 -везикул в исходный пул Возникновение крупных доменов эндосом, содержащих рецептор ЭФР Попарное формирование гибридных эндосом Сегрегация везикул МТ -, МФ - поздние эндосомы МТ + Микротрубочки работают как платформа, обеспечивающая слияния везикул. Последующая актин-зависимая сегрегация везикул без МТ невозможна МТ +, МФ + ЛИЗ
ЕЕА 1 -везикулы Укрупнение ранних эндосом опосредуется формированием гибридных структур с участием ЕЕА 1 -везикул эндосомы «вторичные слияния» и/или образование кластеров эндосом и ЕЕА 1 -везикул возвращение ЕЕА 1 -везикул в исходный пул Возникновение крупных доменов эндосом, содержащих рецептор ЭФР Попарное формирование гибридных эндосом Сегрегация везикул МТ -, МФ - поздние эндосомы МТ + Микротрубочки работают как платформа, обеспечивающая слияния везикул. Последующая актин-зависимая сегрегация везикул без МТ невозможна МТ +, МФ + ЛИЗ
 По всей видимости, параллельно с ЕЕА 1 -зависимыми слияниями идет процесс созревания, приводящий к формированию мультивезикулярных поздних эндосом. После сегрегации ЕЕА 1 -везикул (ранних эндосом) и рецепторсодержащих эндосом последние , возможно, взаимодействуют с Rab 7 везикулами, роль которых в основном в позиционировании поздних эндосом в ОЯО (через RILP_dynein), что способствует формированию гибридных органелл с лизосомами Т. обр. , ЕЕА 1 -везикулы, Rab 7 -везикулы и Lamp 1 лизосомы можно рассматривать как истинные «предсуществующие» компартменты эндоцитозного пути, везикулярного типа, каждому из которых свойственна строго определенная функция ЕЕА 1 -зависимые слияния и сегрегация ЕЕА 1 -доменов и грузсодержащих доменов поддерживается динамичными микротрубочками, тогда как поздние этапы – стабильными высокоацетилированными МТ Актин ввиде коротких филаментов, объединенных с динамичные сети через Arp 2/3, участвует в поддержке искривления мембран и процессах сегрегации доменов
По всей видимости, параллельно с ЕЕА 1 -зависимыми слияниями идет процесс созревания, приводящий к формированию мультивезикулярных поздних эндосом. После сегрегации ЕЕА 1 -везикул (ранних эндосом) и рецепторсодержащих эндосом последние , возможно, взаимодействуют с Rab 7 везикулами, роль которых в основном в позиционировании поздних эндосом в ОЯО (через RILP_dynein), что способствует формированию гибридных органелл с лизосомами Т. обр. , ЕЕА 1 -везикулы, Rab 7 -везикулы и Lamp 1 лизосомы можно рассматривать как истинные «предсуществующие» компартменты эндоцитозного пути, везикулярного типа, каждому из которых свойственна строго определенная функция ЕЕА 1 -зависимые слияния и сегрегация ЕЕА 1 -доменов и грузсодержащих доменов поддерживается динамичными микротрубочками, тогда как поздние этапы – стабильными высокоацетилированными МТ Актин ввиде коротких филаментов, объединенных с динамичные сети через Arp 2/3, участвует в поддержке искривления мембран и процессах сегрегации доменов
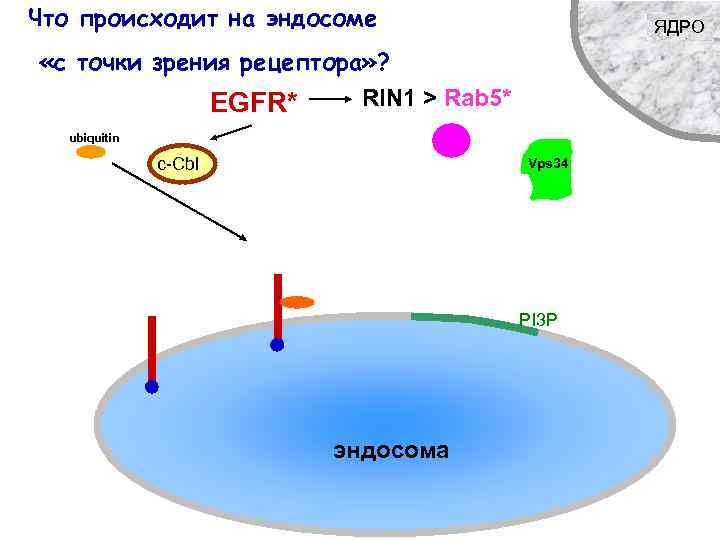 Что происходит на эндосоме ЯДРО «с точки зрения рецептора» ? EGFR* RIN 1 > Rab 5* ubiquitin c-Cbl Vps 34 PI 3 P эндосома
Что происходит на эндосоме ЯДРО «с точки зрения рецептора» ? EGFR* RIN 1 > Rab 5* ubiquitin c-Cbl Vps 34 PI 3 P эндосома
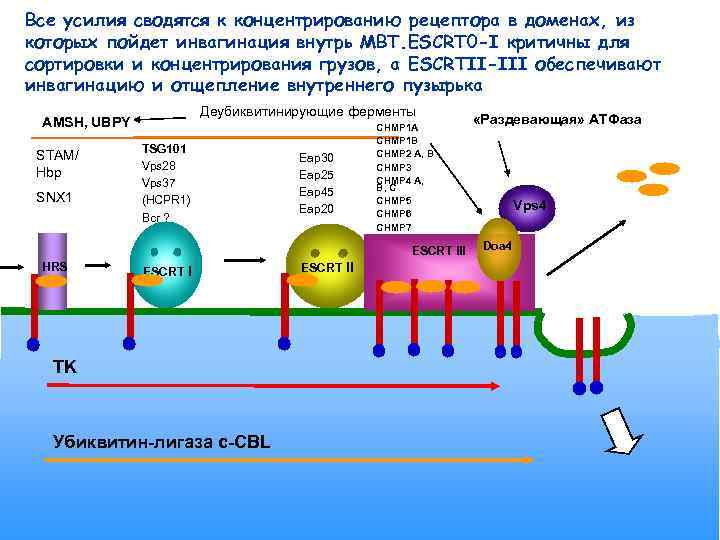 Все усилия сводятся к концентрированию рецептора в доменах, из которых пойдет инвагинация внутрь МВТ. ESCRT 0 -I критичны для сортировки и концентрирования грузов, а ESCRTII-III обеспечивают инвагинацию и отщепление внутреннего пузырька Деубиквитинирующие ферменты AMSH, UBPY STAM/ Hbp SNX 1 TSG 101 Vps 28 Vps 37 (HCPR 1) Bcr ? Eap 30 Eap 25 Eap 45 Eap 20 CHMP 1 A CHMP 1 B CHMP 2 A, B CHMP 3 CHMP 4 A, B, C CHMP 5 CHMP 6 CHMP 7 ESCRT III HRS ESCRT I TK Убиквитин-лигаза c-CBL ESCRT II «Раздевающая» АТФаза Vps 4 Doa 4
Все усилия сводятся к концентрированию рецептора в доменах, из которых пойдет инвагинация внутрь МВТ. ESCRT 0 -I критичны для сортировки и концентрирования грузов, а ESCRTII-III обеспечивают инвагинацию и отщепление внутреннего пузырька Деубиквитинирующие ферменты AMSH, UBPY STAM/ Hbp SNX 1 TSG 101 Vps 28 Vps 37 (HCPR 1) Bcr ? Eap 30 Eap 25 Eap 45 Eap 20 CHMP 1 A CHMP 1 B CHMP 2 A, B CHMP 3 CHMP 4 A, B, C CHMP 5 CHMP 6 CHMP 7 ESCRT III HRS ESCRT I TK Убиквитин-лигаза c-CBL ESCRT II «Раздевающая» АТФаза Vps 4 Doa 4
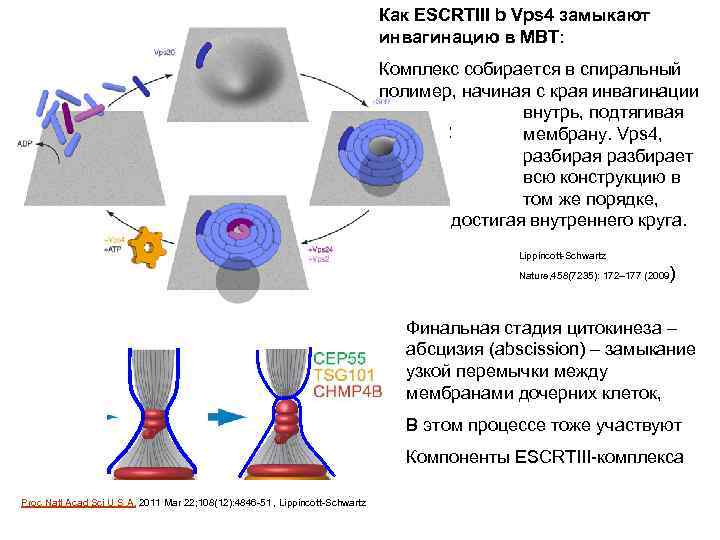 Как ESCRTIII b Vps 4 замыкают инвагинацию в МВТ: Комплекс собирается в спиральный полимер, начиная с края инвагинации внутрь, подтягивая Nature. 2009 March 12 мембрану. Vps 4, разбирая разбирает всю конструкцию в том же порядке, достигая внутреннего круга. Lippincott-Schwartz ) Nature, 458(7235): 172– 177 (2009 Финальная стадия цитокинеза – абсцизия (abscission) – замыкание узкой перемычки между мембранами дочерних клеток, В этом процессе тоже участвуют Компоненты ESCRTIII-комплекса Proc Natl Acad Sci U S A. 2011 Mar 22; 108(12): 4846 -51 , Lippincott-Schwartz
Как ESCRTIII b Vps 4 замыкают инвагинацию в МВТ: Комплекс собирается в спиральный полимер, начиная с края инвагинации внутрь, подтягивая Nature. 2009 March 12 мембрану. Vps 4, разбирая разбирает всю конструкцию в том же порядке, достигая внутреннего круга. Lippincott-Schwartz ) Nature, 458(7235): 172– 177 (2009 Финальная стадия цитокинеза – абсцизия (abscission) – замыкание узкой перемычки между мембранами дочерних клеток, В этом процессе тоже участвуют Компоненты ESCRTIII-комплекса Proc Natl Acad Sci U S A. 2011 Mar 22; 108(12): 4846 -51 , Lippincott-Schwartz
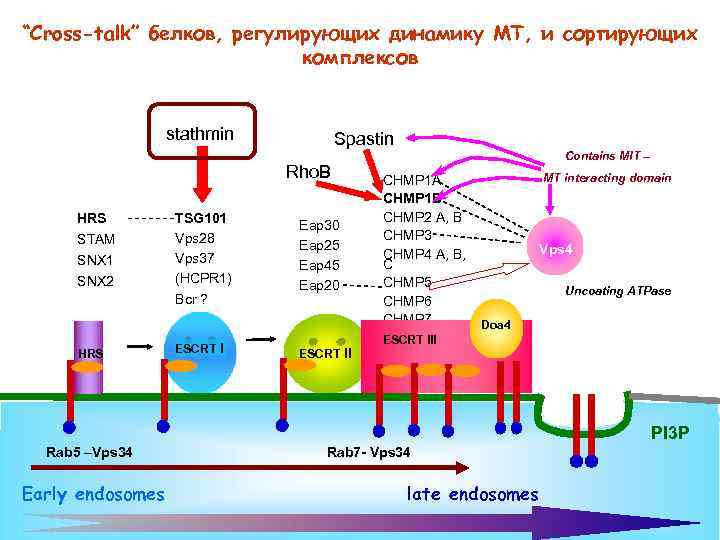 “Cross-talk” белков, регулирующих динамику МТ, и сортирующих комплексов stathmin Spastin Rho. B HRS STAM SNX 1 SNX 2 HRS TSG 101 Vps 28 Vps 37 (HCPR 1) Bcr ? ESCRT I Eap 30 Eap 25 Eap 45 Eap 20 ESCRT II Contains MIT – CHMP 1 A CHMP 1 B CHMP 2 A, B CHMP 3 CHMP 4 A, B, C CHMP 5 CHMP 6 CHMP 7 MT interacting domain Vps 4 Uncoating ATPase Doa 4 ESCRT III PI 3 P Rab 5 –Vps 34 Early endosomes Rab 7 - Vps 34 late endosomes
“Cross-talk” белков, регулирующих динамику МТ, и сортирующих комплексов stathmin Spastin Rho. B HRS STAM SNX 1 SNX 2 HRS TSG 101 Vps 28 Vps 37 (HCPR 1) Bcr ? ESCRT I Eap 30 Eap 25 Eap 45 Eap 20 ESCRT II Contains MIT – CHMP 1 A CHMP 1 B CHMP 2 A, B CHMP 3 CHMP 4 A, B, C CHMP 5 CHMP 6 CHMP 7 MT interacting domain Vps 4 Uncoating ATPase Doa 4 ESCRT III PI 3 P Rab 5 –Vps 34 Early endosomes Rab 7 - Vps 34 late endosomes
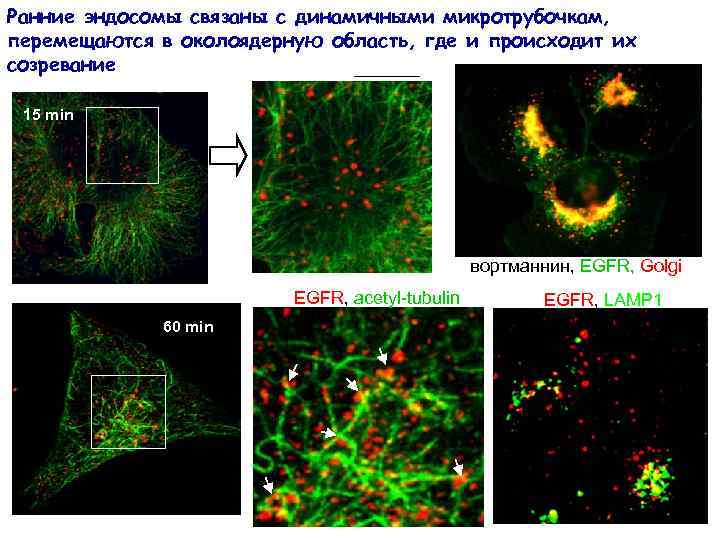 Ранние эндосомы связаны с динамичными микротрубочкам, перемещаются в околоядерную область, где и происходит их созревание 15 min вортманнин, EGFR, Golgi EGFR, acetyl-tubulin 60 min EGFR, LAMP 1
Ранние эндосомы связаны с динамичными микротрубочкам, перемещаются в околоядерную область, где и происходит их созревание 15 min вортманнин, EGFR, Golgi EGFR, acetyl-tubulin 60 min EGFR, LAMP 1
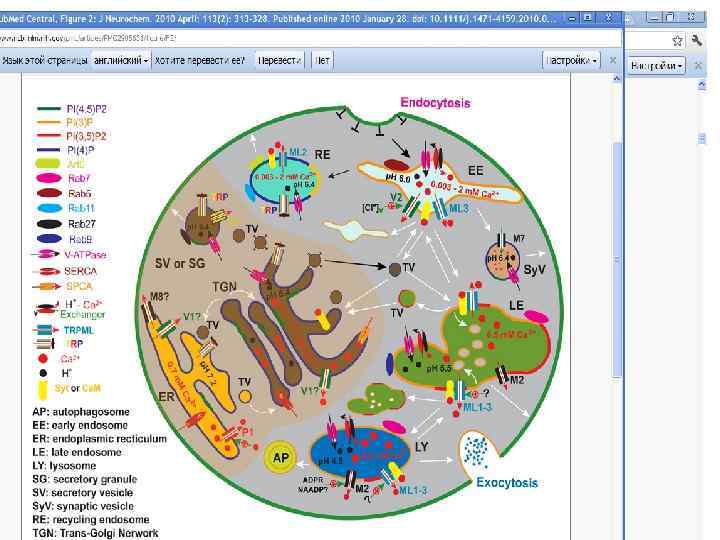
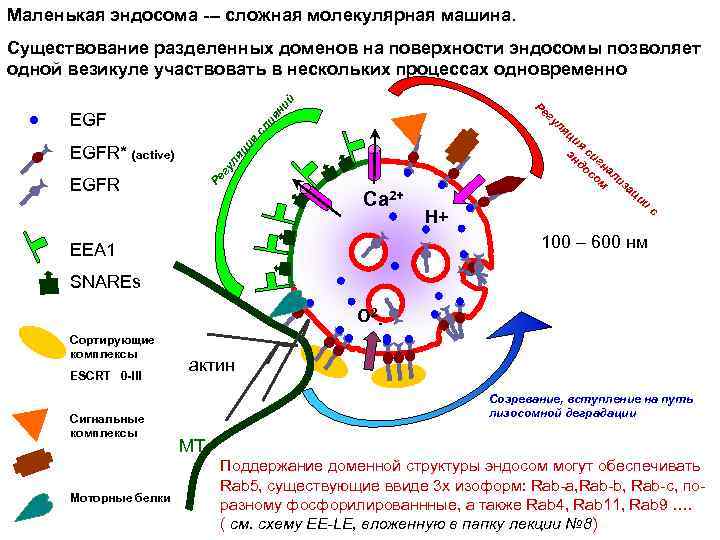 Маленькая эндосома --- сложная молекулярная машина. Существование разделенных доменов на поверхности эндосомы позволяет одной везикуле участвовать в нескольких процессах одновременно ия ни й Ре гу ля ци я эн си до гн со ал м иза ци я сл EGF гу ля EGFR* (active) Ре EGFR Са 2+ Н+ ци и с 100 – 600 нм EEA 1 SNAREs О 2 Сортирующие комплексы ESCRT 0 -III Сигнальные комплексы Моторные белки актин Созревание, вступление на путь лизосомной деградации МТ Поддержание доменной структуры эндосом могут обеспечивать Rab 5, существующие ввиде 3 х изоформ: Rab-a, Rab-b, Rab-c, поразному фосфорилированнные, а также Rab 4, Rab 11, Rab 9 …. ( см. схему EE-LE, вложенную в папку лекции № 8)
Маленькая эндосома --- сложная молекулярная машина. Существование разделенных доменов на поверхности эндосомы позволяет одной везикуле участвовать в нескольких процессах одновременно ия ни й Ре гу ля ци я эн си до гн со ал м иза ци я сл EGF гу ля EGFR* (active) Ре EGFR Са 2+ Н+ ци и с 100 – 600 нм EEA 1 SNAREs О 2 Сортирующие комплексы ESCRT 0 -III Сигнальные комплексы Моторные белки актин Созревание, вступление на путь лизосомной деградации МТ Поддержание доменной структуры эндосом могут обеспечивать Rab 5, существующие ввиде 3 х изоформ: Rab-a, Rab-b, Rab-c, поразному фосфорилированнные, а также Rab 4, Rab 11, Rab 9 …. ( см. схему EE-LE, вложенную в папку лекции № 8)
 «Динамическая нестабильность» эндоцитоза – механизм адаптации к внешним сигналам
«Динамическая нестабильность» эндоцитоза – механизм адаптации к внешним сигналам
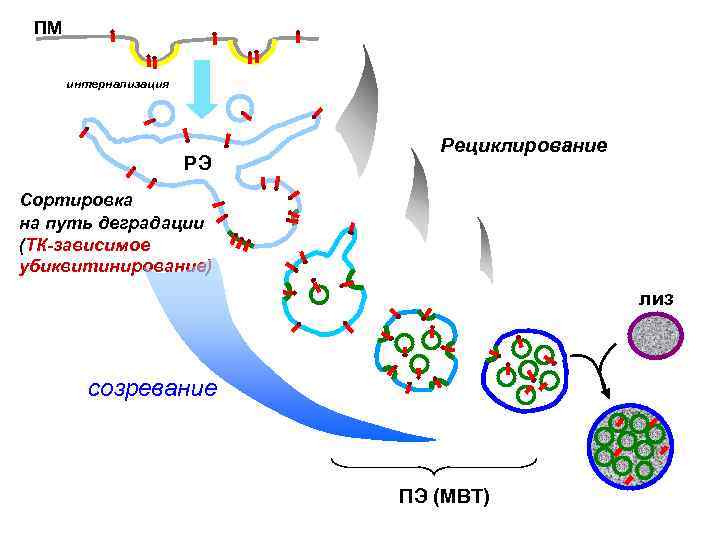 ПМ интернализация РЭ Рециклирование Сортировка на путь деградации (ТК-зависимое убиквитинирование) лиз созревание ПЭ (МВТ)
ПМ интернализация РЭ Рециклирование Сортировка на путь деградации (ТК-зависимое убиквитинирование) лиз созревание ПЭ (МВТ)
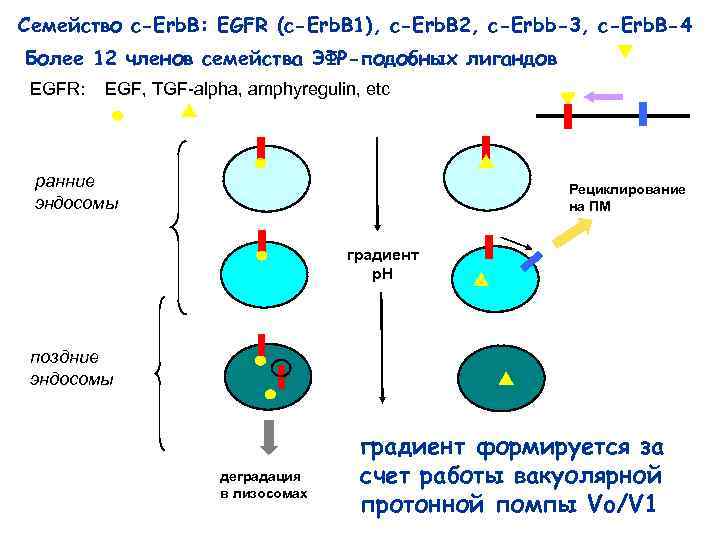 Семейство c-Erb. B: EGFR (c-Erb. B 1), c-Erb. B 2, c-Erbb-3, c-Erb. B-4 Более 12 членов семейства ЭФР-подобных лигандов EGFR: EGF, TGF-alpha, amphyregulin, etc ранние эндосомы Рециклирование на ПМ градиент р. Н поздние эндосомы деградация в лизосомах градиент формируется за счет работы вакуолярной протонной помпы Vo/V 1
Семейство c-Erb. B: EGFR (c-Erb. B 1), c-Erb. B 2, c-Erbb-3, c-Erb. B-4 Более 12 членов семейства ЭФР-подобных лигандов EGFR: EGF, TGF-alpha, amphyregulin, etc ранние эндосомы Рециклирование на ПМ градиент р. Н поздние эндосомы деградация в лизосомах градиент формируется за счет работы вакуолярной протонной помпы Vo/V 1
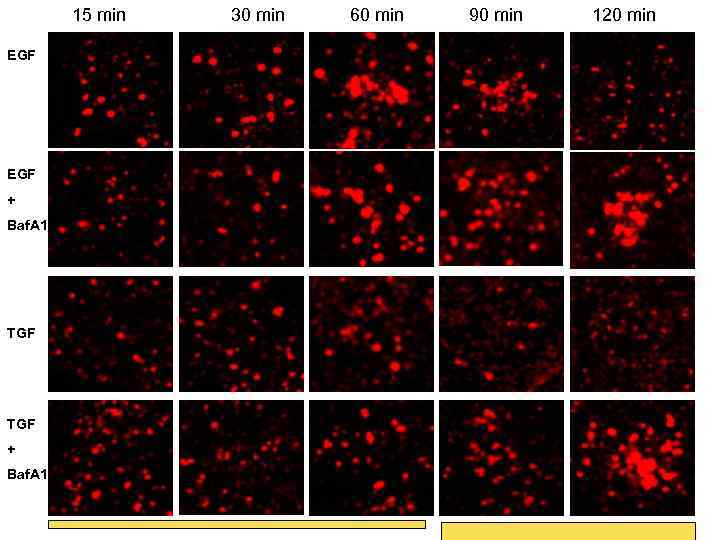 15 min EGF + Baf. A 1 TGF + Baf. A 1 30 min 60 min 90 min 120 min
15 min EGF + Baf. A 1 TGF + Baf. A 1 30 min 60 min 90 min 120 min
 Первоначально эндоцитоз сигнальных рецепторов рассматривали исключительно как способ аттенюации генерируемого на плазматической мембране сигнала: эндоцитоз просто убирает лишние рецепторы с ПМ, «десенситизируя» клетку к действию ростового фактора Но: рецептор в эндосомах может сохранять тирозинкиназную активность вплоть до попадания в МВЭ
Первоначально эндоцитоз сигнальных рецепторов рассматривали исключительно как способ аттенюации генерируемого на плазматической мембране сигнала: эндоцитоз просто убирает лишние рецепторы с ПМ, «десенситизируя» клетку к действию ростового фактора Но: рецептор в эндосомах может сохранять тирозинкиназную активность вплоть до попадания в МВЭ
 Время жизни активированного рецептора ЭФР на ПМ значительно меньше, чем в эндосомах. Рецептор ЭФР в эндосомах ? проведение сигнала
Время жизни активированного рецептора ЭФР на ПМ значительно меньше, чем в эндосомах. Рецептор ЭФР в эндосомах ? проведение сигнала
 MAP-киназный каскад: МАРККК МАРК EGFR > Shc, GRB 2 > m. Sos> Ras > Raf > MEK > Erk > Elk , Jun, Fos Плазматическая мембрана ядро При стимуляции эндоцитоза ЭФР белки МАР-киназного каскада Shc, GRB 2, m-Sos, Raf, MEK, ERK локализуются на эндосомах (Pol et al. , 1998, FEBS Lett. , 441: 34 -38; Rizzo et al. , 1999, JBC, 274: 1131 -1139; Oksvold et al. , 2001, Eur. JCB 80: 285 -294; Jiang and Sorkin, 2002, MCB, 13: 1522 -1535)
MAP-киназный каскад: МАРККК МАРК EGFR > Shc, GRB 2 > m. Sos> Ras > Raf > MEK > Erk > Elk , Jun, Fos Плазматическая мембрана ядро При стимуляции эндоцитоза ЭФР белки МАР-киназного каскада Shc, GRB 2, m-Sos, Raf, MEK, ERK локализуются на эндосомах (Pol et al. , 1998, FEBS Lett. , 441: 34 -38; Rizzo et al. , 1999, JBC, 274: 1131 -1139; Oksvold et al. , 2001, Eur. JCB 80: 285 -294; Jiang and Sorkin, 2002, MCB, 13: 1522 -1535)
 Сигнал с эндосом: Поддержание стимулированного на плазматической мембране или генерация нового сигнала?
Сигнал с эндосом: Поддержание стимулированного на плазматической мембране или генерация нового сигнала?
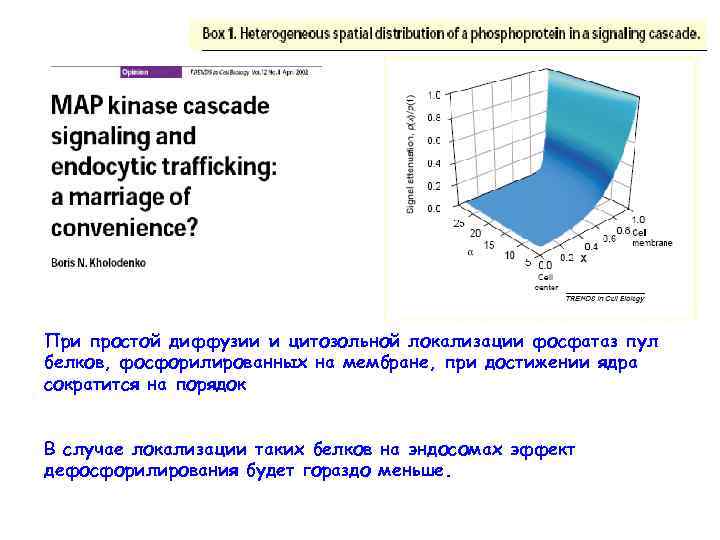 При простой диффузии и цитозольной локализации фосфатаз пул белков, фосфорилированных на мембране, при достижении ядра сократится на порядок В случае локализации таких белков на эндосомах эффект дефосфорилирования будет гораздо меньше.
При простой диффузии и цитозольной локализации фосфатаз пул белков, фосфорилированных на мембране, при достижении ядра сократится на порядок В случае локализации таких белков на эндосомах эффект дефосфорилирования будет гораздо меньше.
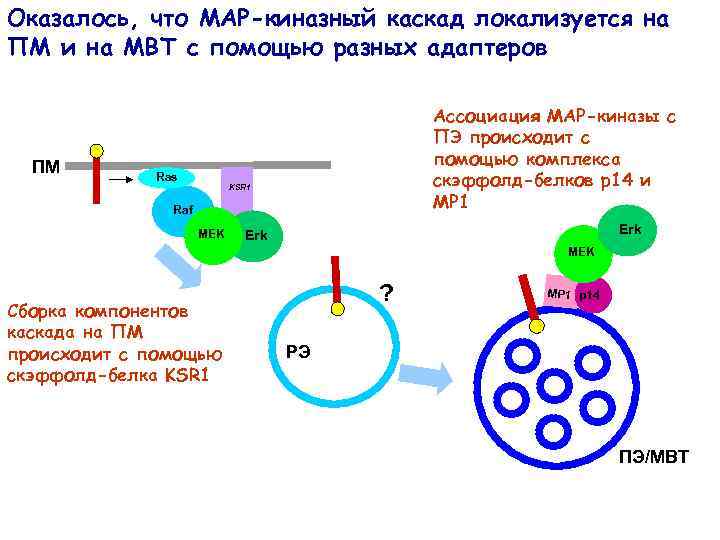 Оказалось, что МАР-киназный каскад локализуется на ПМ и на МВТ с помощью разных адаптеров ПМ Ras Ассоциация МАР-киназы с ПЭ происходит с помощью комплекса скэффолд-белков р14 и МР 1 KSR 1 Raf MEK Erk MEK Сборка компонентов каскада на ПМ происходит с помощью скэффолд-белка KSR 1 ? МР 1 р14 РЭ ПЭ/МВТ
Оказалось, что МАР-киназный каскад локализуется на ПМ и на МВТ с помощью разных адаптеров ПМ Ras Ассоциация МАР-киназы с ПЭ происходит с помощью комплекса скэффолд-белков р14 и МР 1 KSR 1 Raf MEK Erk MEK Сборка компонентов каскада на ПМ происходит с помощью скэффолд-белка KSR 1 ? МР 1 р14 РЭ ПЭ/МВТ
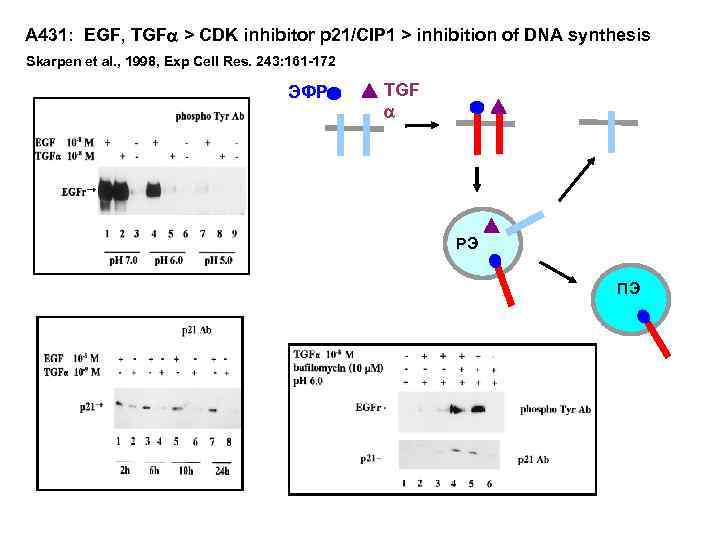 A 431: EGF, TGF > CDK inhibitor p 21/CIP 1 > inhibition of DNA synthesis Skarpen et al. , 1998, Exp Cell Res. 243: 161 -172 ЭФР TGF РЭ ПЭ
A 431: EGF, TGF > CDK inhibitor p 21/CIP 1 > inhibition of DNA synthesis Skarpen et al. , 1998, Exp Cell Res. 243: 161 -172 ЭФР TGF РЭ ПЭ
 APPL 1/2(Adaptor protein containing PH domain, PTB domain and Leucine zipper motif) Локализуется на мембранах ранних эндосом (ЕЕА 1 негативных) В ответ на EGF или окислительный стресс, APPL 1 транслоцируется с мембран в ядро, где взаимодействует с Nu. RD/Me. CP 1 (nucleosome remodeling and histone deacetylase multiprotein complex) – регулятором структуры хроматина и экспрессии генов. APPL 1 и 2 участвуют в регуляции пролиферации. Для их функционирования необходима связь с Rab 5
APPL 1/2(Adaptor protein containing PH domain, PTB domain and Leucine zipper motif) Локализуется на мембранах ранних эндосом (ЕЕА 1 негативных) В ответ на EGF или окислительный стресс, APPL 1 транслоцируется с мембран в ядро, где взаимодействует с Nu. RD/Me. CP 1 (nucleosome remodeling and histone deacetylase multiprotein complex) – регулятором структуры хроматина и экспрессии генов. APPL 1 и 2 участвуют в регуляции пролиферации. Для их функционирования необходима связь с Rab 5
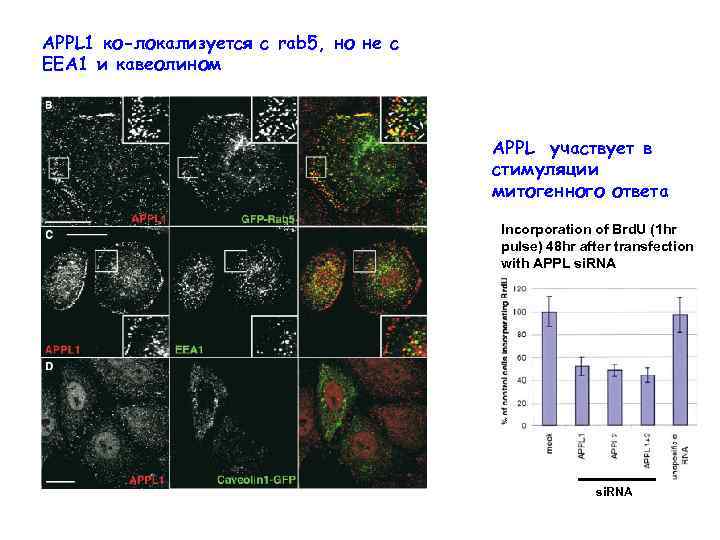 APPL 1 ко-локализуется с rab 5, но не с ЕЕА 1 и кавеолином APPL участвует в стимуляции митогенного ответа Incorporation of Brd. U (1 hr pulse) 48 hr after transfection with APPL si. RNA
APPL 1 ко-локализуется с rab 5, но не с ЕЕА 1 и кавеолином APPL участвует в стимуляции митогенного ответа Incorporation of Brd. U (1 hr pulse) 48 hr after transfection with APPL si. RNA
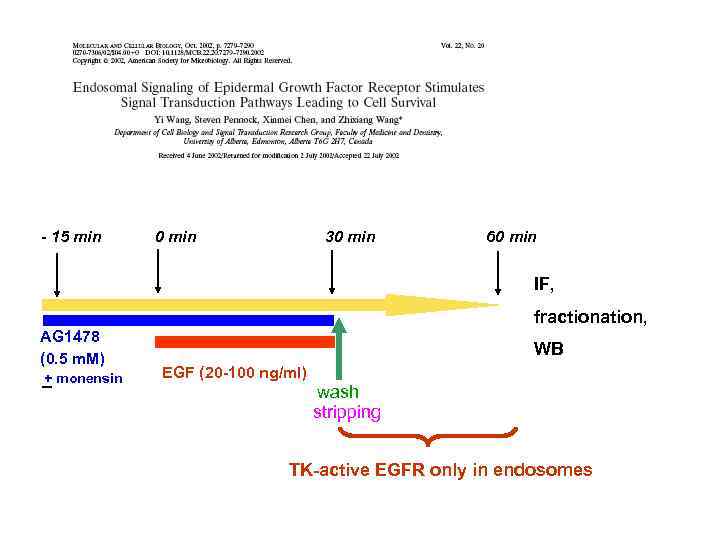 - 15 min 0 min 30 min 60 min IF, fractionation, AG 1478 (0. 5 m. M) + monensin WB EGF (20 -100 ng/ml) wash stripping TK-active EGFR only in endosomes
- 15 min 0 min 30 min 60 min IF, fractionation, AG 1478 (0. 5 m. M) + monensin WB EGF (20 -100 ng/ml) wash stripping TK-active EGFR only in endosomes
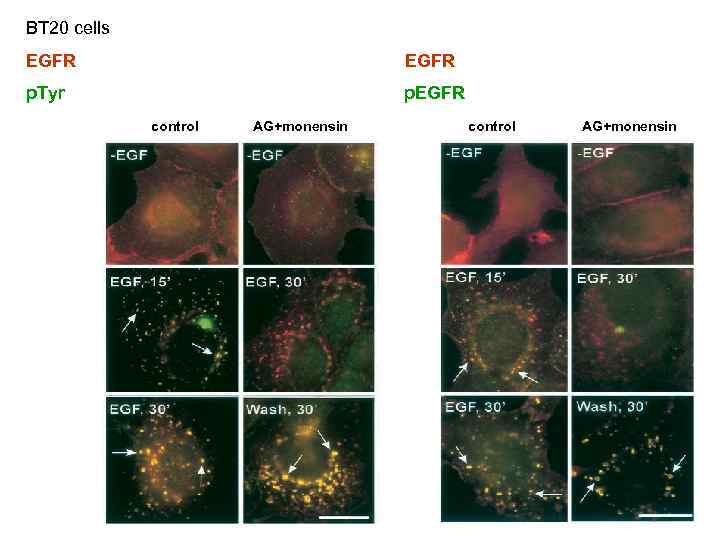 BT 20 cells EGFR p. Tyr p. EGFR control AG+monensin
BT 20 cells EGFR p. Tyr p. EGFR control AG+monensin
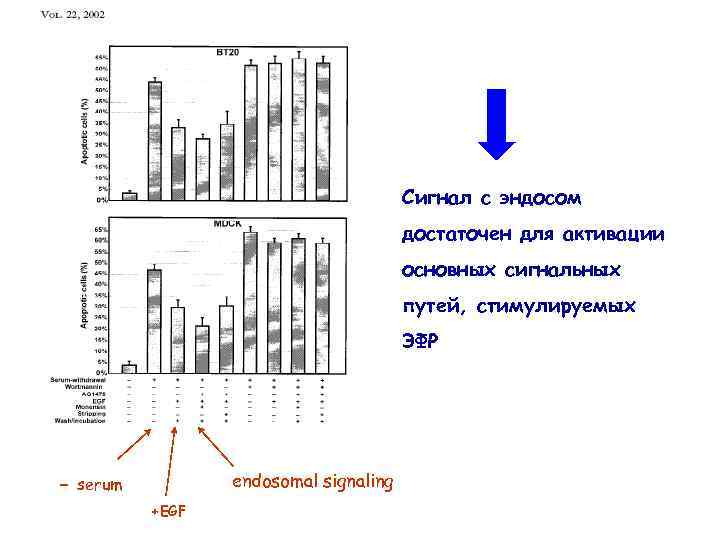 Сигнал с эндосом достаточен для активации основных сигнальных путей, стимулируемых ЭФР - endosomal signaling serum +EGF
Сигнал с эндосом достаточен для активации основных сигнальных путей, стимулируемых ЭФР - endosomal signaling serum +EGF
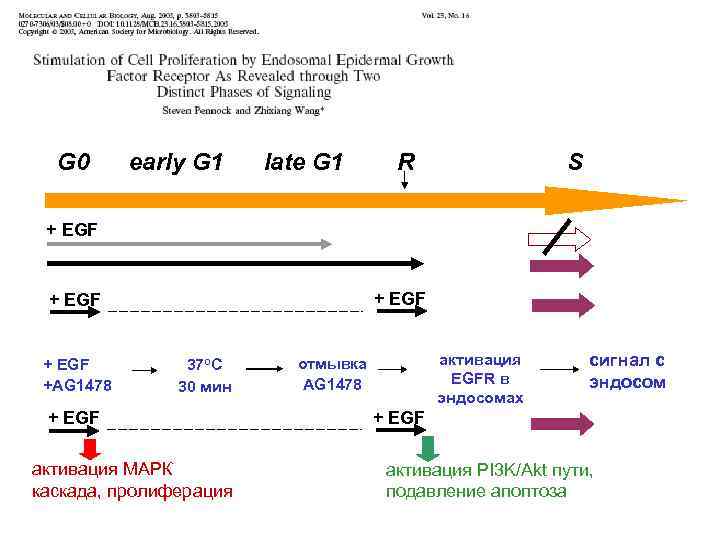 G 0 early G 1 late G 1 R S + EGF +AG 1478 37 o. C 30 мин + EGF активация МАРК каскада, пролиферация активация EGFR в эндосомах отмывка AG 1478 сигнал с эндосом + EGF активация PI 3 K/Akt пути, подавление апоптоза
G 0 early G 1 late G 1 R S + EGF +AG 1478 37 o. C 30 мин + EGF активация МАРК каскада, пролиферация активация EGFR в эндосомах отмывка AG 1478 сигнал с эндосом + EGF активация PI 3 K/Akt пути, подавление апоптоза
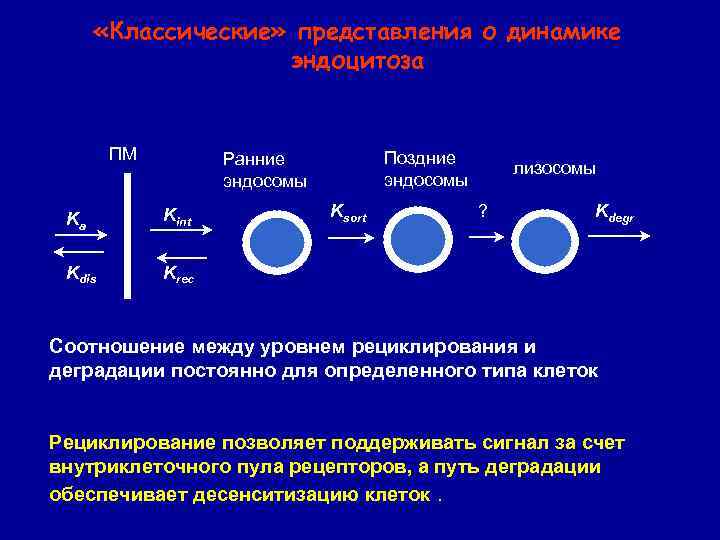 «Классические» представления о динамике эндоцитоза ПМ Поздние эндосомы Ранние эндосомы Ka Kint Kdis Ksort лизосомы ? Kdegr Krec Соотношение между уровнем рециклирования и деградации постоянно для определенного типа клеток Рециклирование позволяет поддерживать сигнал за счет внутриклеточного пула рецепторов, а путь деградации обеспечивает десенситизацию клеток.
«Классические» представления о динамике эндоцитоза ПМ Поздние эндосомы Ранние эндосомы Ka Kint Kdis Ksort лизосомы ? Kdegr Krec Соотношение между уровнем рециклирования и деградации постоянно для определенного типа клеток Рециклирование позволяет поддерживать сигнал за счет внутриклеточного пула рецепторов, а путь деградации обеспечивает десенситизацию клеток.
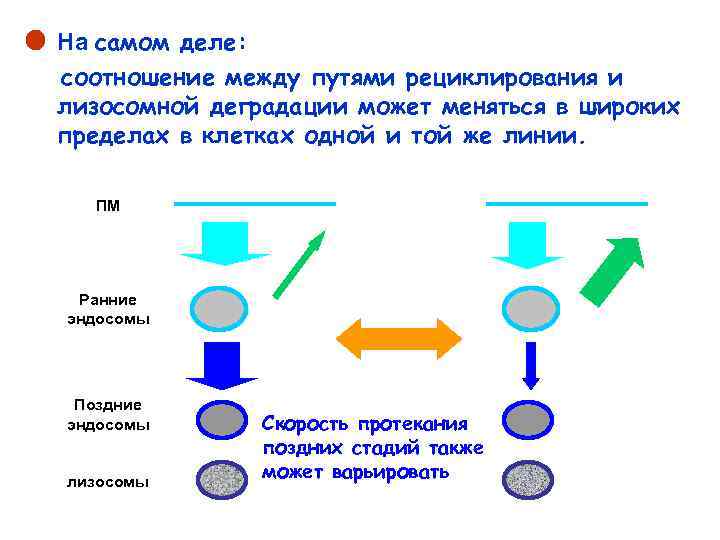 • На самом деле: соотношение между путями рециклирования и лизосомной деградации может меняться в широких пределах в клетках одной и той же линии. ПМ Ранние эндосомы Поздние эндосомы лизосомы Скорость протекания поздних стадий также может варьировать
• На самом деле: соотношение между путями рециклирования и лизосомной деградации может меняться в широких пределах в клетках одной и той же линии. ПМ Ранние эндосомы Поздние эндосомы лизосомы Скорость протекания поздних стадий также может варьировать
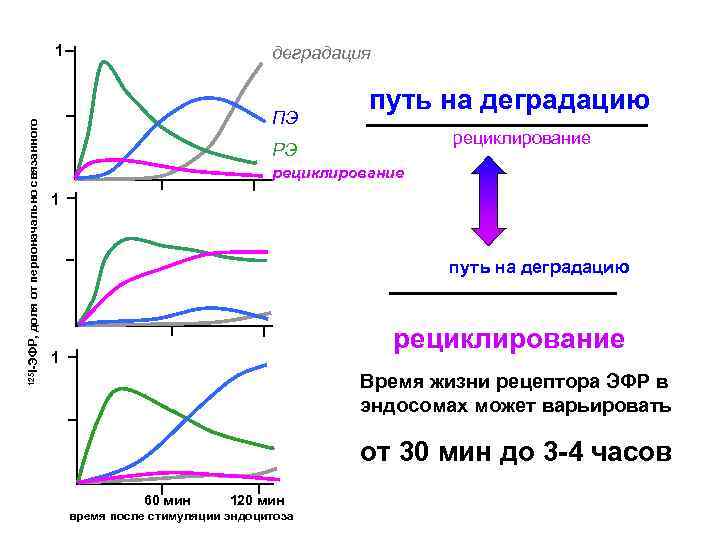 125 I-ЭФР, доля от первоначально связанного 1 деградация ПЭ путь на деградацию рециклирование РЭ рециклирование 1 путь на деградацию рециклирование 1 Время жизни рецептора ЭФР в эндосомах может варьировать от 30 мин до 3 -4 часов 60 мин 120 мин время после стимуляции эндоцитоза
125 I-ЭФР, доля от первоначально связанного 1 деградация ПЭ путь на деградацию рециклирование РЭ рециклирование 1 путь на деградацию рециклирование 1 Время жизни рецептора ЭФР в эндосомах может варьировать от 30 мин до 3 -4 часов 60 мин 120 мин время после стимуляции эндоцитоза
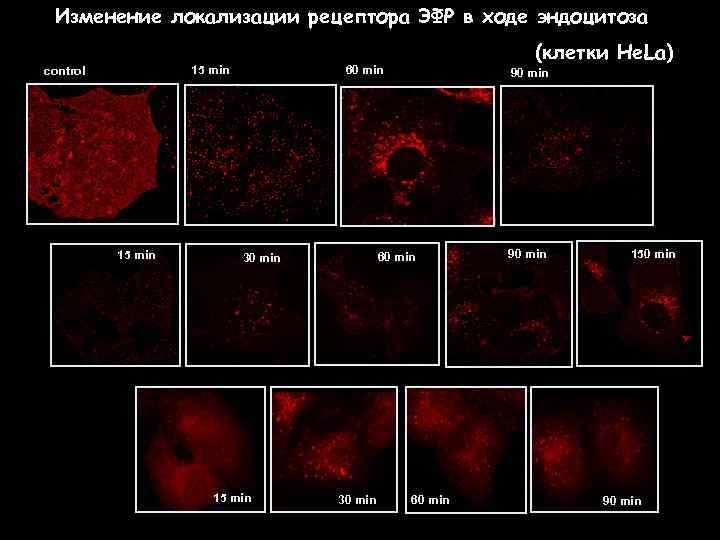 Изменение локализации рецептора ЭФР в ходе эндоцитоза 60 min 15 min control 15 min (клетки He. La) 60 min 30 min 15 min 90 min 30 min 60 min 90 min 150 min 90 min
Изменение локализации рецептора ЭФР в ходе эндоцитоза 60 min 15 min control 15 min (клетки He. La) 60 min 30 min 15 min 90 min 30 min 60 min 90 min 150 min 90 min
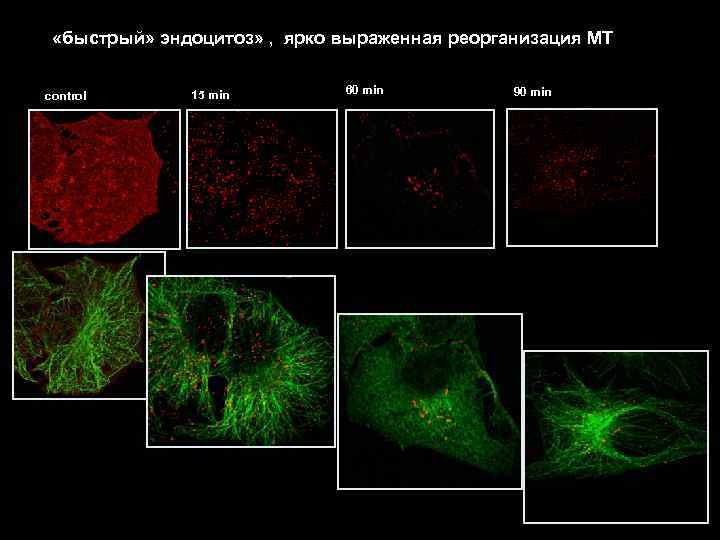 «быстрый» эндоцитоз» , ярко выраженная реорганизация МТ control 15 min 60 min 90 min
«быстрый» эндоцитоз» , ярко выраженная реорганизация МТ control 15 min 60 min 90 min
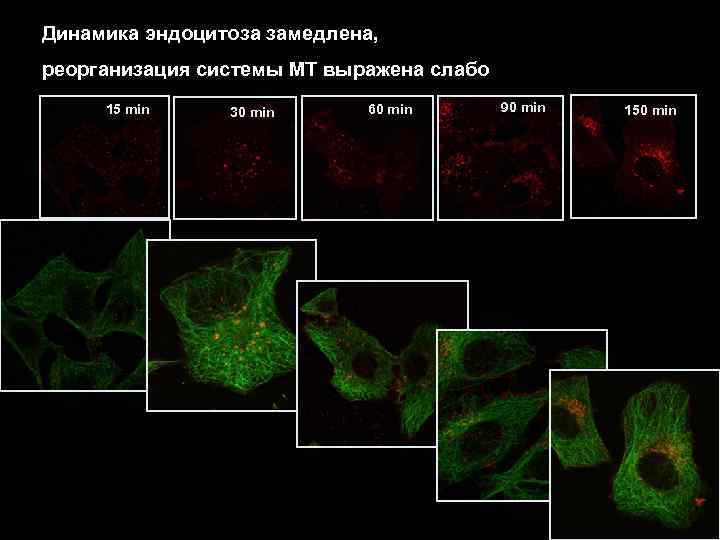 Динамика эндоцитоза замедлена, реорганизация системы МТ выражена слабо 15 min 30 min 60 min 90 min 150 min
Динамика эндоцитоза замедлена, реорганизация системы МТ выражена слабо 15 min 30 min 60 min 90 min 150 min
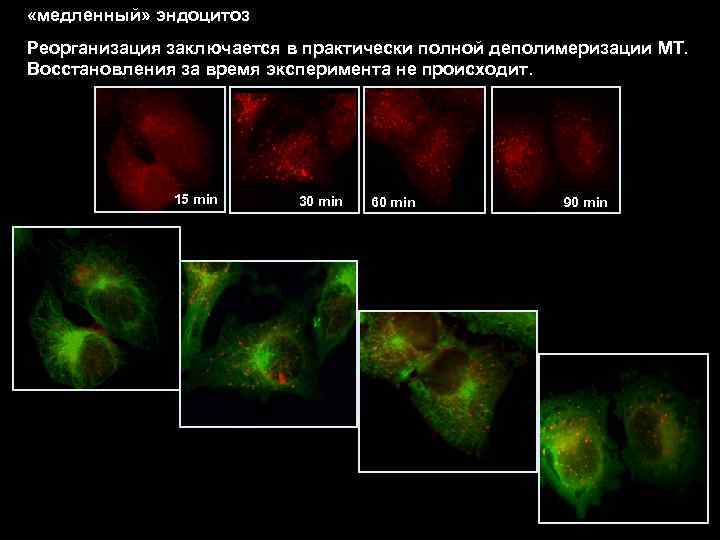 «медленный» эндоцитоз Реорганизация заключается в практически полной деполимеризации МТ. Восстановления за время эксперимента не происходит. 15 min 30 min 60 min 90 min
«медленный» эндоцитоз Реорганизация заключается в практически полной деполимеризации МТ. Восстановления за время эксперимента не происходит. 15 min 30 min 60 min 90 min
 MAP-киназный каскад: МАРККК МАРК EGFR > Shc, GRB 2 > m. Sos> Ras > Raf > MEK > Erk > Elk , Jun, Fos Плазматическая мембрана ядро При стимуляции эндоцитоза ЭФР белки МАРкиназного каскада Shc, GRB 2, m-Sos, Raf, MEK, ERK локализуются на эндосомах (Pol et al. , 1998, FEBS Lett. , 441: 34 -38; Rizzo et al. , 1999, JBC, 274: 1131 -1139; Oksvold et al. , 2001, Eur. JCB 80: 285 -294; Jiang and Sorkin, 2002, MCB, 13: 1522 -1535)
MAP-киназный каскад: МАРККК МАРК EGFR > Shc, GRB 2 > m. Sos> Ras > Raf > MEK > Erk > Elk , Jun, Fos Плазматическая мембрана ядро При стимуляции эндоцитоза ЭФР белки МАРкиназного каскада Shc, GRB 2, m-Sos, Raf, MEK, ERK локализуются на эндосомах (Pol et al. , 1998, FEBS Lett. , 441: 34 -38; Rizzo et al. , 1999, JBC, 274: 1131 -1139; Oksvold et al. , 2001, Eur. JCB 80: 285 -294; Jiang and Sorkin, 2002, MCB, 13: 1522 -1535)
 Inhibitors of clathrin-mediated endocytosis: Эндоцитоз существенен для полной активации МАР-киназы: Эндоцитоз не существенен для полной активации МАР-киназы:
Inhibitors of clathrin-mediated endocytosis: Эндоцитоз существенен для полной активации МАР-киназы: Эндоцитоз не существенен для полной активации МАР-киназы:
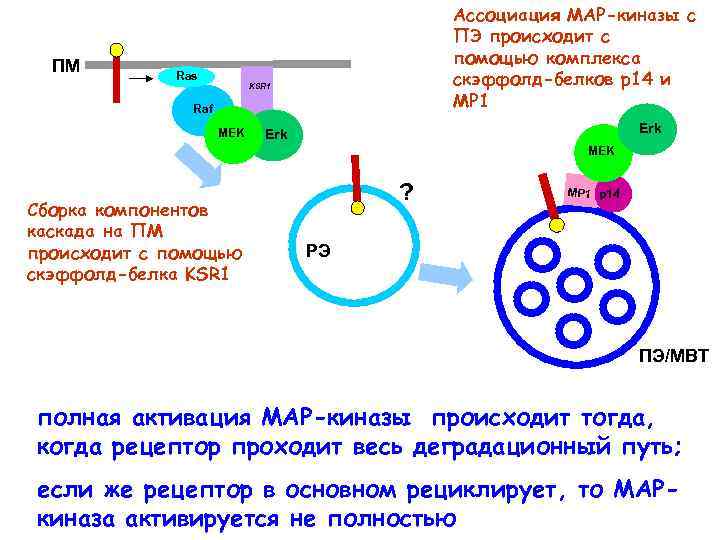 ПМ Ras Ассоциация МАР-киназы с ПЭ происходит с помощью комплекса скэффолд-белков р14 и МР 1 KSR 1 Raf MEK Erk MEK Сборка компонентов каскада на ПМ происходит с помощью скэффолд-белка KSR 1 ? МР 1 р14 РЭ ПЭ/МВТ полная активация МАР-киназы происходит тогда, когда рецептор проходит весь деградационный путь; если же рецептор в основном рециклирует, то МАРкиназа активируется не полностью
ПМ Ras Ассоциация МАР-киназы с ПЭ происходит с помощью комплекса скэффолд-белков р14 и МР 1 KSR 1 Raf MEK Erk MEK Сборка компонентов каскада на ПМ происходит с помощью скэффолд-белка KSR 1 ? МР 1 р14 РЭ ПЭ/МВТ полная активация МАР-киназы происходит тогда, когда рецептор проходит весь деградационный путь; если же рецептор в основном рециклирует, то МАРкиназа активируется не полностью
 Inhibitors of clathrin-mediated endocytosis: Эндоцитоз существенен для полной активации МАР-киназы: Эндоцитоз не существенен для полной активации МАР-киназы:
Inhibitors of clathrin-mediated endocytosis: Эндоцитоз существенен для полной активации МАР-киназы: Эндоцитоз не существенен для полной активации МАР-киназы:
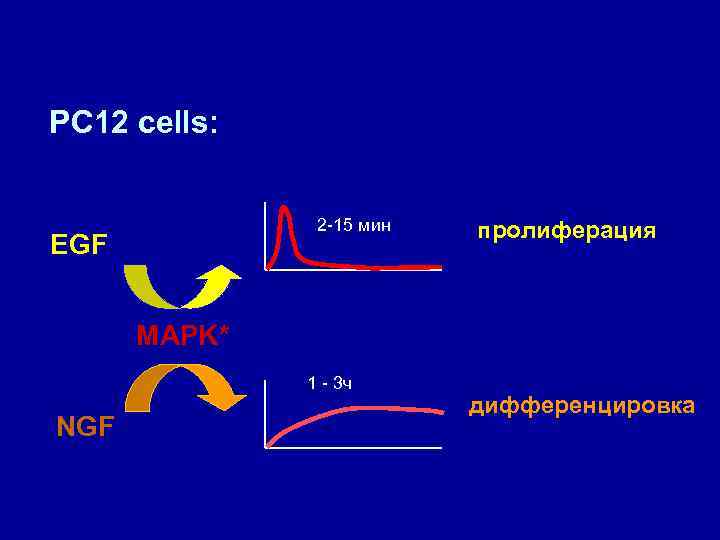 PC 12 cells: 2 -15 мин EGF пролиферация MAPK* 1 - 3 ч NGF дифференцировка
PC 12 cells: 2 -15 мин EGF пролиферация MAPK* 1 - 3 ч NGF дифференцировка
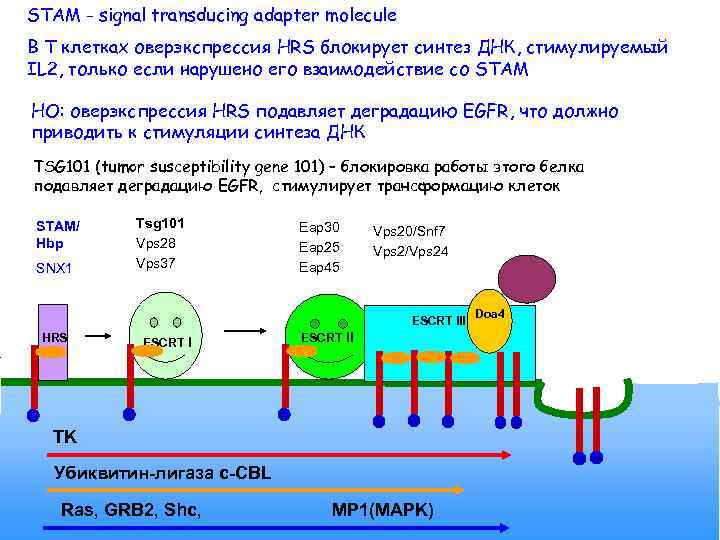 STAM - signal transducing adapter molecule В Т клетках оверэкспрессия HRS блокирует синтез ДНК, стимулируемый IL 2, только если нарушено его взаимодействие со STAM НО: оверэкспрессия HRS подавляет деградацию EGFR, что должно приводить к стимуляции синтеза ДНК TSG 101 (tumor susceptibility gene 101) – блокировка работы этого белка Vps 4 подавляет деградацию EGFR, стимулирует трансформацию клеток STAM/ Hbp SNX 1 Tsg 101 Vps 28 Vps 37 Eap 30 Eap 25 Eap 45 Vps 20/Snf 7 Vps 2/Vps 24 ESCRT III HRS ESCRT II TK Убиквитин-лигаза c-CBL Ras, GRB 2, Shc, MP 1(MAPK) Doa 4
STAM - signal transducing adapter molecule В Т клетках оверэкспрессия HRS блокирует синтез ДНК, стимулируемый IL 2, только если нарушено его взаимодействие со STAM НО: оверэкспрессия HRS подавляет деградацию EGFR, что должно приводить к стимуляции синтеза ДНК TSG 101 (tumor susceptibility gene 101) – блокировка работы этого белка Vps 4 подавляет деградацию EGFR, стимулирует трансформацию клеток STAM/ Hbp SNX 1 Tsg 101 Vps 28 Vps 37 Eap 30 Eap 25 Eap 45 Vps 20/Snf 7 Vps 2/Vps 24 ESCRT III HRS ESCRT II TK Убиквитин-лигаза c-CBL Ras, GRB 2, Shc, MP 1(MAPK) Doa 4
 APPL ½ (Adaptor protein containing PH domain, PTB domain and Leucine zipper motif) Локализуется на мембранах ранних эндосом (ЕЕА 1 -негативных), может связываться с ТК рецепторами через РТВ-домен, стимулирует Akt 1, регулирует транслокацию GLUT 4 В ответ на EGF или окислительный стресс, APPL 1 транслоцируется с мембран в ядро, где взаимодействует с Nu. RD/Me. CP 1 (nucleosome remodeling and histone deacetylase multiprotein complex) – регулятором структуры хроматина и экспрессии генов. APPL 1 и 2 участвуют в регуляции пролиферации. Для их функционирования необходима связь с Rab 5 STAM - signal transducing adapter molecule, партнер HRS по ESCRT 0 -комплексу; ассоциируется с Janus киназой, индуцирует экспрессию с-myc под действием IL-2 RIN 1 взаимодействует со STAM 2; Профиль тирозинового фосфорилирования HRS-STAM комплекса при действии EGF, PDGF, HGF различается STAM действует и на биосинтетическом пути, ассоциируется с COPII- везикулами Sar 1 p-зависимым образом, регулирует морфологию аппарата Гольджи: При оверэкспрессии STAM Гольджи фрагментируется, а при нокауте – коллапсирует в области ЦОМТ TOM 1 L 1 – взаимодействует с HRS (ESCRT 0) и Tsg 101(ESCRTI), Имеет несколько остатков тирозина, фосфорилируемых киназами Src-семейства, что определяет его взаимодействие с GRB 2 и р85 -PI 3 -киназой
APPL ½ (Adaptor protein containing PH domain, PTB domain and Leucine zipper motif) Локализуется на мембранах ранних эндосом (ЕЕА 1 -негативных), может связываться с ТК рецепторами через РТВ-домен, стимулирует Akt 1, регулирует транслокацию GLUT 4 В ответ на EGF или окислительный стресс, APPL 1 транслоцируется с мембран в ядро, где взаимодействует с Nu. RD/Me. CP 1 (nucleosome remodeling and histone deacetylase multiprotein complex) – регулятором структуры хроматина и экспрессии генов. APPL 1 и 2 участвуют в регуляции пролиферации. Для их функционирования необходима связь с Rab 5 STAM - signal transducing adapter molecule, партнер HRS по ESCRT 0 -комплексу; ассоциируется с Janus киназой, индуцирует экспрессию с-myc под действием IL-2 RIN 1 взаимодействует со STAM 2; Профиль тирозинового фосфорилирования HRS-STAM комплекса при действии EGF, PDGF, HGF различается STAM действует и на биосинтетическом пути, ассоциируется с COPII- везикулами Sar 1 p-зависимым образом, регулирует морфологию аппарата Гольджи: При оверэкспрессии STAM Гольджи фрагментируется, а при нокауте – коллапсирует в области ЦОМТ TOM 1 L 1 – взаимодействует с HRS (ESCRT 0) и Tsg 101(ESCRTI), Имеет несколько остатков тирозина, фосфорилируемых киназами Src-семейства, что определяет его взаимодействие с GRB 2 и р85 -PI 3 -киназой
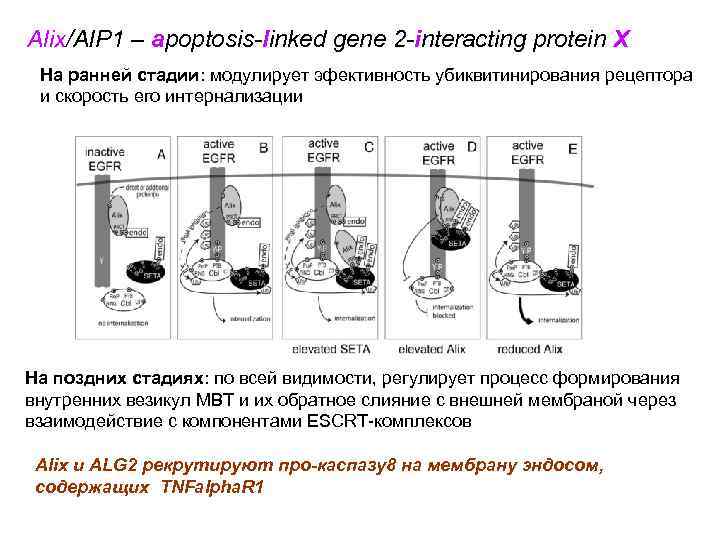 Alix/AIP 1 – apoptosis-linked gene 2 -interacting protein X На ранней стадии: модулирует эфективность убиквитинирования рецептора и скорость его интернализации На поздних стадиях: по всей видимости, регулирует процесс формирования внутренних везикул МВТ и их обратное слияние с внешней мембраной через взаимодействие с компонентами ESCRT-комплексов Аlix и ALG 2 рекрутируют про-каспазу8 на мембрану эндосом, содержащих TNFalpha. R 1
Alix/AIP 1 – apoptosis-linked gene 2 -interacting protein X На ранней стадии: модулирует эфективность убиквитинирования рецептора и скорость его интернализации На поздних стадиях: по всей видимости, регулирует процесс формирования внутренних везикул МВТ и их обратное слияние с внешней мембраной через взаимодействие с компонентами ESCRT-комплексов Аlix и ALG 2 рекрутируют про-каспазу8 на мембрану эндосом, содержащих TNFalpha. R 1
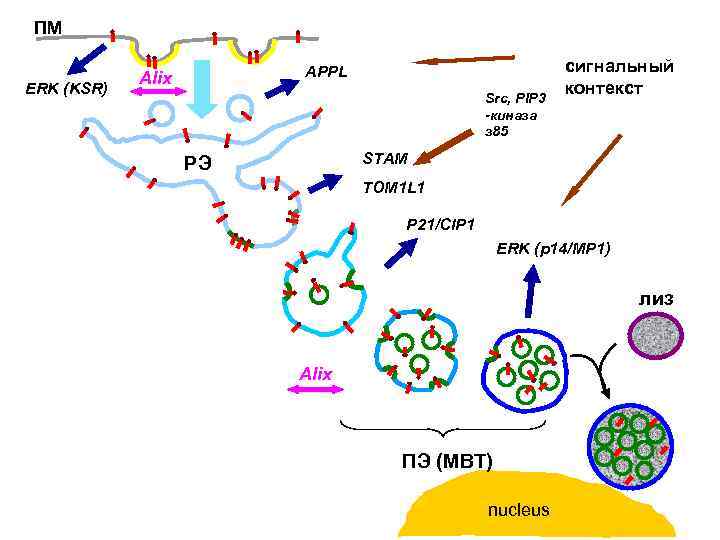 ПМ ERK (KSR) APPL Alix Src, PIP 3 -киназа з 85 сигнальный контекст STAM РЭ TOM 1 L 1 P 21/CIP 1 ERK (p 14/MP 1) лиз Alix ПЭ (МВТ) nucleus
ПМ ERK (KSR) APPL Alix Src, PIP 3 -киназа з 85 сигнальный контекст STAM РЭ TOM 1 L 1 P 21/CIP 1 ERK (p 14/MP 1) лиз Alix ПЭ (МВТ) nucleus
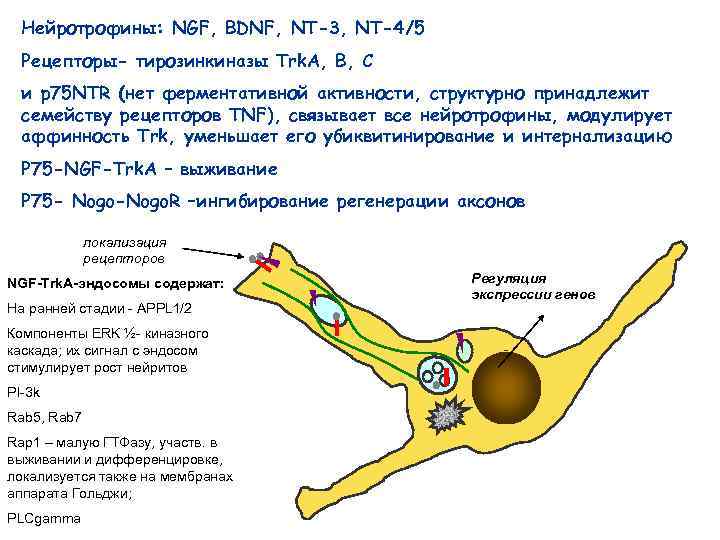 Нейротрофины: NGF, BDNF, NT-3, NT-4/5 Рецепторы- тирозинкиназы Trk. A, B, C и p 75 NTR (нет ферментативной активности, структурно принадлежит семейству рецепторов TNF), связывает все нейротрофины, модулирует аффинность Trk, уменьшает его убиквитинирование и интернализацию P 75 -NGF-Trk. А – выживание P 75 - Nogo-Nogo. R –ингибирование регенерации аксонов локализация рецепторов NGF-Trk. A-эндосомы содержат: На ранней стадии - APPL 1/2 Компоненты ERK ½- киназного каскада; их сигнал с эндосом стимулирует рост нейритов PI-3 k Rab 5, Rab 7 Rap 1 – малую ГТФазу, участв. в выживании и дифференцировке, локализуется также на мембранах аппарата Гольджи; PLCgamma Регуляция экспрессии генов
Нейротрофины: NGF, BDNF, NT-3, NT-4/5 Рецепторы- тирозинкиназы Trk. A, B, C и p 75 NTR (нет ферментативной активности, структурно принадлежит семейству рецепторов TNF), связывает все нейротрофины, модулирует аффинность Trk, уменьшает его убиквитинирование и интернализацию P 75 -NGF-Trk. А – выживание P 75 - Nogo-Nogo. R –ингибирование регенерации аксонов локализация рецепторов NGF-Trk. A-эндосомы содержат: На ранней стадии - APPL 1/2 Компоненты ERK ½- киназного каскада; их сигнал с эндосом стимулирует рост нейритов PI-3 k Rab 5, Rab 7 Rap 1 – малую ГТФазу, участв. в выживании и дифференцировке, локализуется также на мембранах аппарата Гольджи; PLCgamma Регуляция экспрессии генов
 Эндоцитоз сигналинг
Эндоцитоз сигналинг


