 Реальные газы.
Реальные газы.
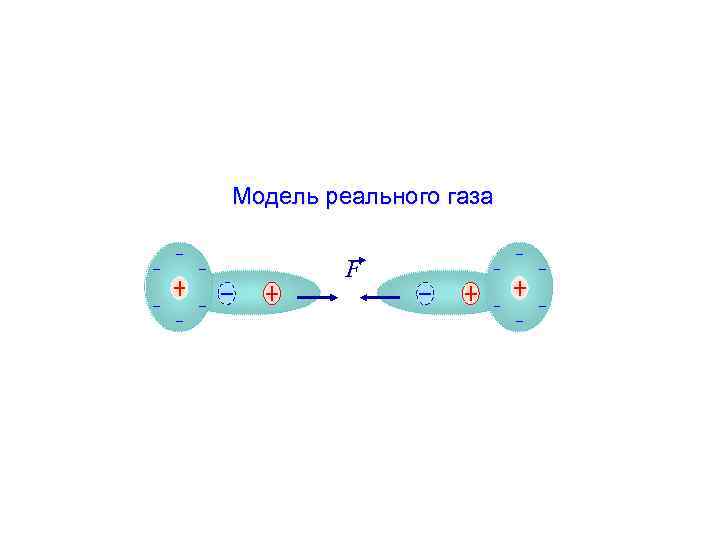 Модель реального газа F
Модель реального газа F
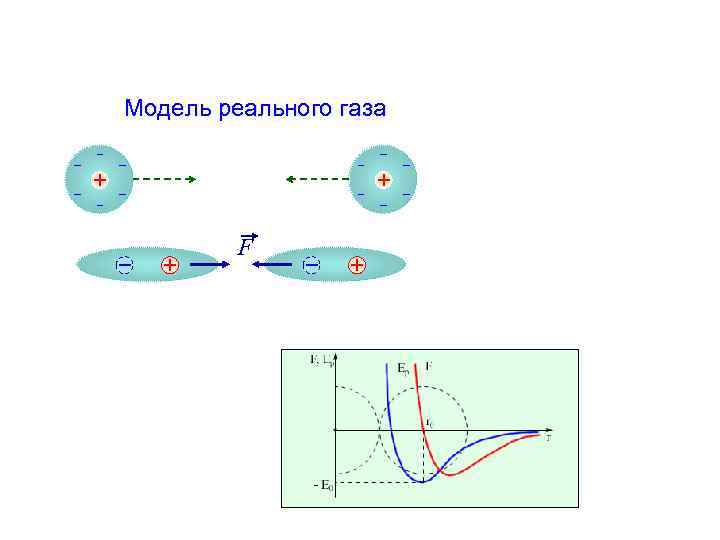 Модель реального газа F
Модель реального газа F
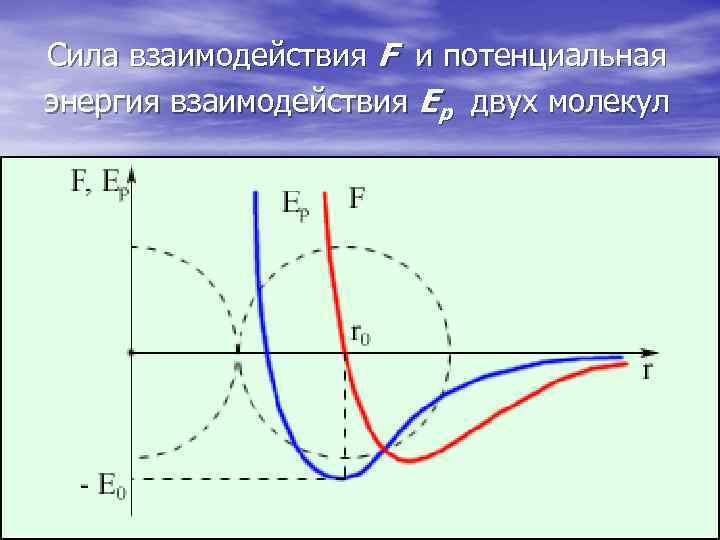 Сила взаимодействия F и потенциальная энергия взаимодействия Eр двух молекул
Сила взаимодействия F и потенциальная энергия взаимодействия Eр двух молекул
 Модель идеального газа: Модель Ван-дер-Ваальса Уравнение Ван-дер-Ваальса Ван-дер-Ваальс (van der Waals) Ян (1837 – 1923)
Модель идеального газа: Модель Ван-дер-Ваальса Уравнение Ван-дер-Ваальса Ван-дер-Ваальс (van der Waals) Ян (1837 – 1923)
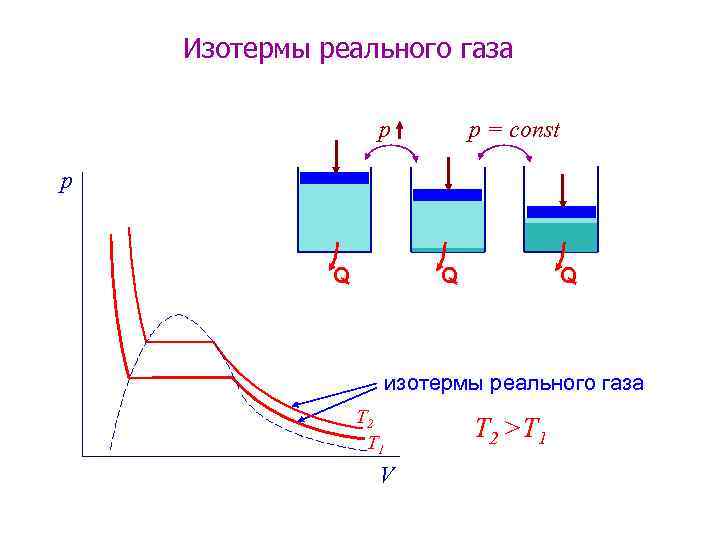 Изотермы реального газа р р = const p Q Q Q изотермы реального газа T 2 T 1 V T 2 >T 1
Изотермы реального газа р р = const p Q Q Q изотермы реального газа T 2 T 1 V T 2 >T 1
 Водяной пар (1) и вода (2). Молекулы воды увеличены примерно в 5· 107 раз.
Водяной пар (1) и вода (2). Молекулы воды увеличены примерно в 5· 107 раз.
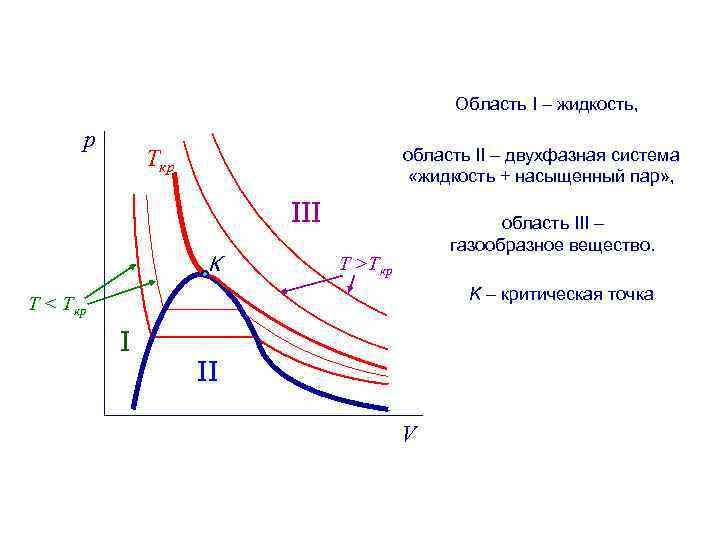 Область I – жидкость, p область II – двухфазная система «жидкость + насыщенный пар» , Ткр III K область III – газообразное вещество. T >Tкр K – критическая точка T < Tкр I II V
Область I – жидкость, p область II – двухфазная система «жидкость + насыщенный пар» , Ткр III K область III – газообразное вещество. T >Tкр K – критическая точка T < Tкр I II V
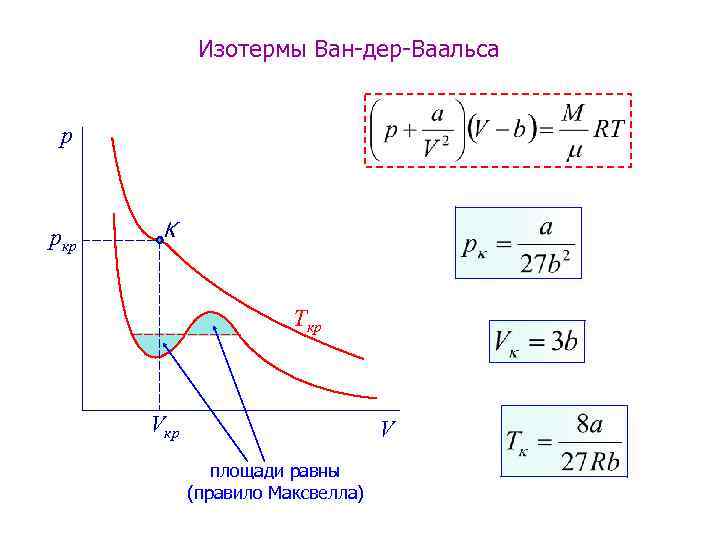 Изотермы Ван-дер-Ваальса p pкр K Ткр V площади равны (правило Максвелла)
Изотермы Ван-дер-Ваальса p pкр K Ткр V площади равны (правило Максвелла)
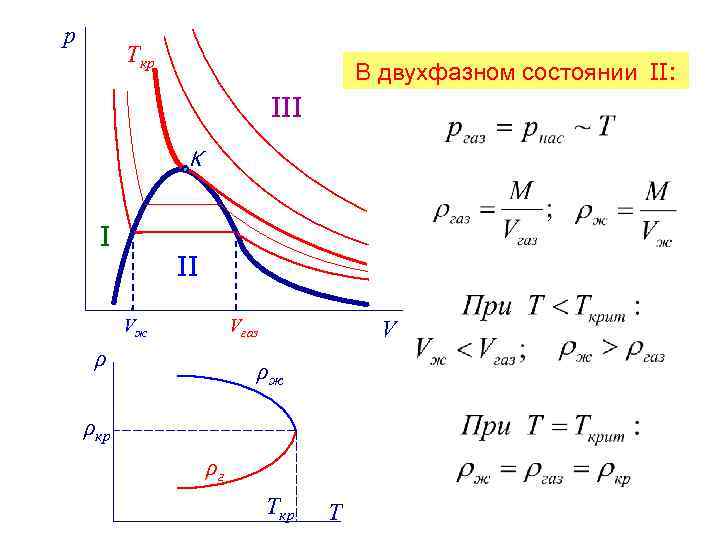 p Ткр В двухфазном состоянии II: III K I II Vж Vгаз ρ V ρж ρкр ρг Tкр T
p Ткр В двухфазном состоянии II: III K I II Vж Vгаз ρ V ρж ρкр ρг Tкр T
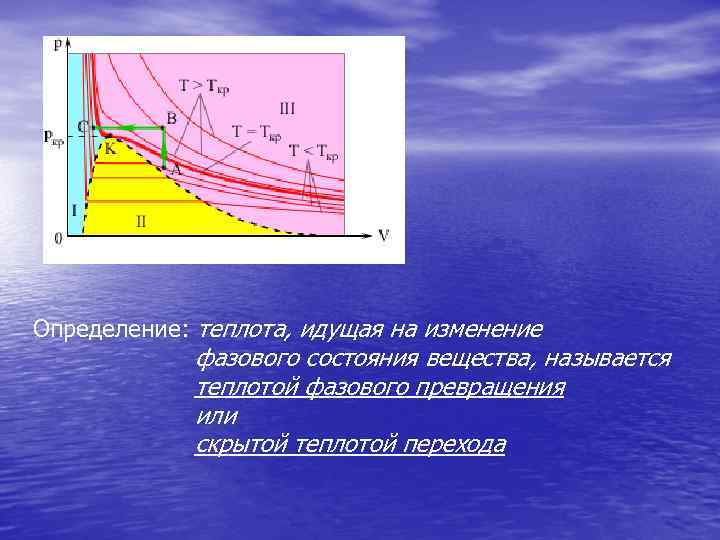 Определение: теплота, идущая на изменение фазового состояния вещества, называется теплотой фазового превращения или скрытой теплотой перехода
Определение: теплота, идущая на изменение фазового состояния вещества, называется теплотой фазового превращения или скрытой теплотой перехода
 p p p-dp δQ =0 цикл Карно Q 1 T δQ=0 T-d. T Q 2 V 1 V V 2 скрытая теплота парообразования - уравнение Клапейрона - Клаузиуса Клапейрон (Clapeyron) Бенуа Поль Эмиль (1799 – 1864) Клаузиус (Clausius) Рудольф Юлиус Эмануэль (1822 – 1888)
p p p-dp δQ =0 цикл Карно Q 1 T δQ=0 T-d. T Q 2 V 1 V V 2 скрытая теплота парообразования - уравнение Клапейрона - Клаузиуса Клапейрон (Clapeyron) Бенуа Поль Эмиль (1799 – 1864) Клаузиус (Clausius) Рудольф Юлиус Эмануэль (1822 – 1888)
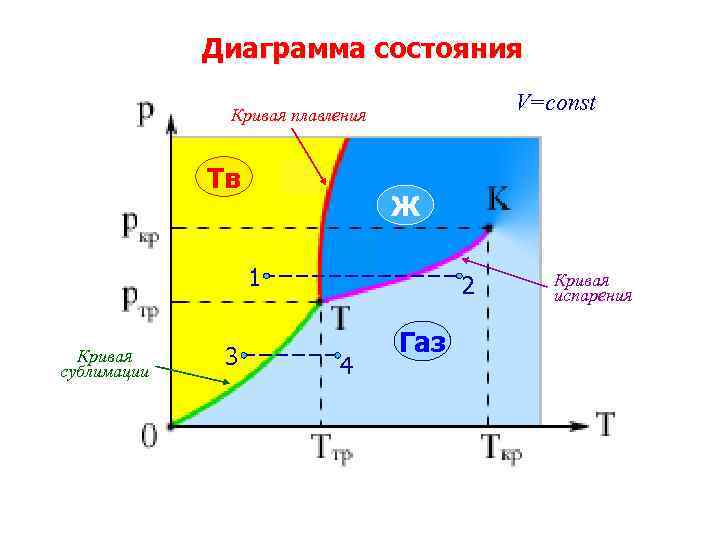 Диаграмма состояния V=const Кривая плавления Тв Ж 1 Кривая сублимации 3 2 4 Газ Кривая испарения
Диаграмма состояния V=const Кривая плавления Тв Ж 1 Кривая сублимации 3 2 4 Газ Кривая испарения