 «Реальная структура твердого тела» . Лекция 1. Термины. Классификация дефектов. Точечные дефекты. Лаборатория неорганического материаловедения, Химфак МГУ Евгений Алексеевич ГУДИЛИН д. х. н. , к. 548 goodilin@inorg. chem. msu. ru fmg. inorg. chem. msu. ru 939 -47 -29 Москва 2006 1
«Реальная структура твердого тела» . Лекция 1. Термины. Классификация дефектов. Точечные дефекты. Лаборатория неорганического материаловедения, Химфак МГУ Евгений Алексеевич ГУДИЛИН д. х. н. , к. 548 goodilin@inorg. chem. msu. ru fmg. inorg. chem. msu. ru 939 -47 -29 Москва 2006 1
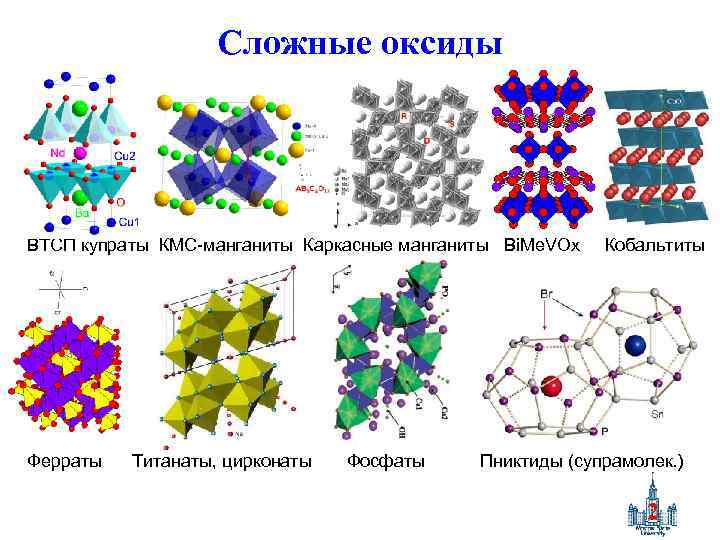 Сложные оксиды ВТСП купраты КМС-манганиты Каркасные манганиты Bi. Me. VOx Кобальтиты Ферраты Титанаты, цирконаты Фосфаты Пниктиды (супрамолек. ) 2
Сложные оксиды ВТСП купраты КМС-манганиты Каркасные манганиты Bi. Me. VOx Кобальтиты Ферраты Титанаты, цирконаты Фосфаты Пниктиды (супрамолек. ) 2
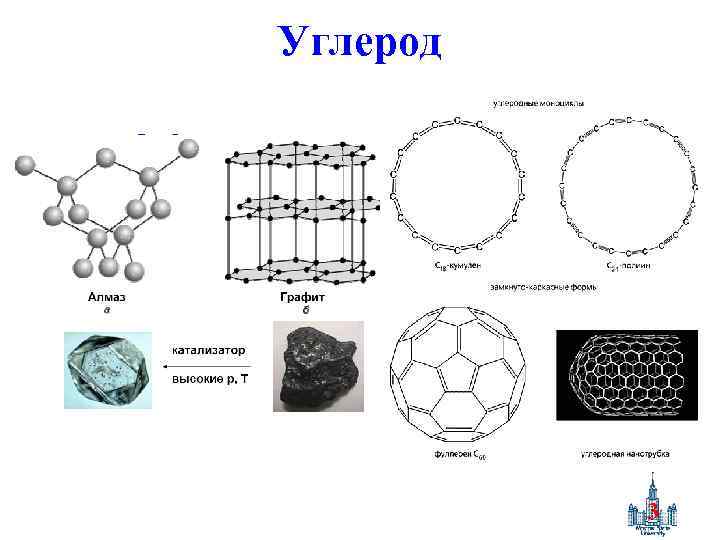 Углерод 3
Углерод 3
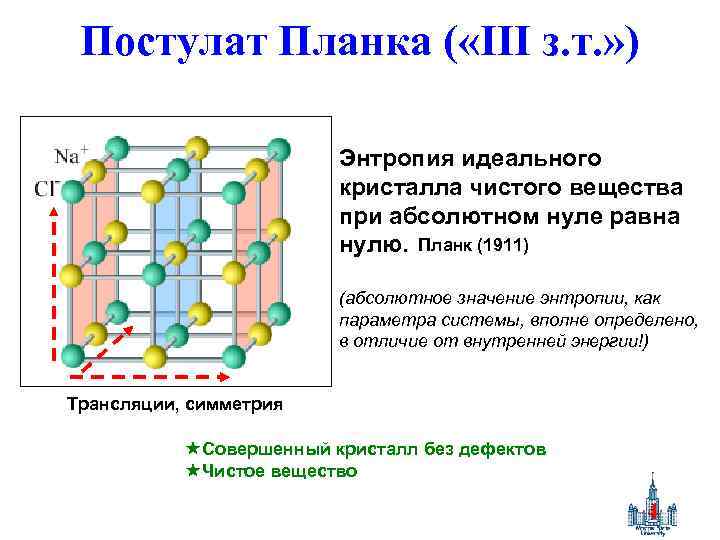 Постулат Планка ( «III з. т. » ) Энтропия идеального кристалла чистого вещества при абсолютном нуле равна нулю. Планк (1911) (абсолютное значение энтропии, как параметра системы, вполне определено, в отличие от внутренней энергии!) Трансляции, симметрия Совершенный кристалл без дефектов Чистое вещество 4
Постулат Планка ( «III з. т. » ) Энтропия идеального кристалла чистого вещества при абсолютном нуле равна нулю. Планк (1911) (абсолютное значение энтропии, как параметра системы, вполне определено, в отличие от внутренней энергии!) Трансляции, симметрия Совершенный кристалл без дефектов Чистое вещество 4
 Огранка кристаллов Концепция периодических цепочек связей 5
Огранка кристаллов Концепция периодических цепочек связей 5
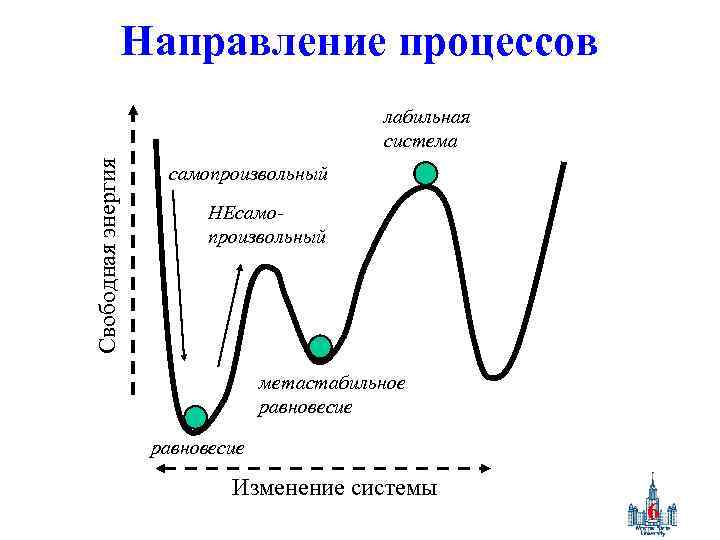 Направление процессов Свободная энергия лабильная система самопроизвольный НЕсамопроизвольный метастабильное равновесие Изменение системы 6
Направление процессов Свободная энергия лабильная система самопроизвольный НЕсамопроизвольный метастабильное равновесие Изменение системы 6
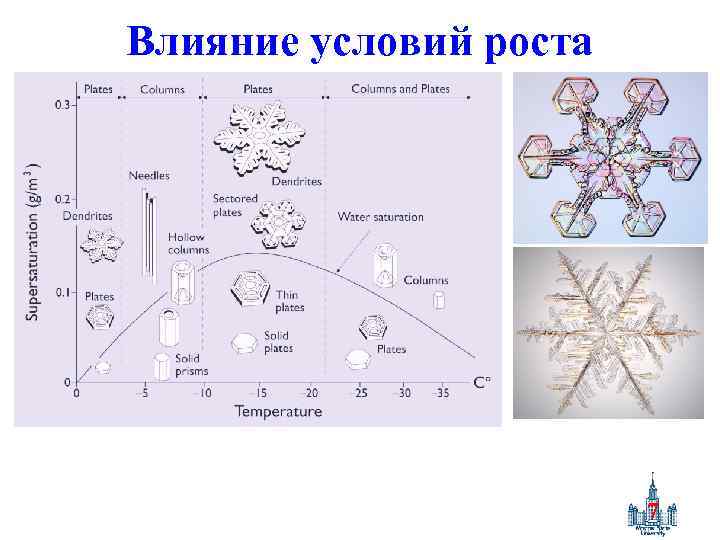 Влияние условий роста 7
Влияние условий роста 7
 Ростовая морфология Nd 213: ренуклеация на дефектах типа двугранного угла R 2 Ba. Cu 3 Oz 8
Ростовая морфология Nd 213: ренуклеация на дефектах типа двугранного угла R 2 Ba. Cu 3 Oz 8
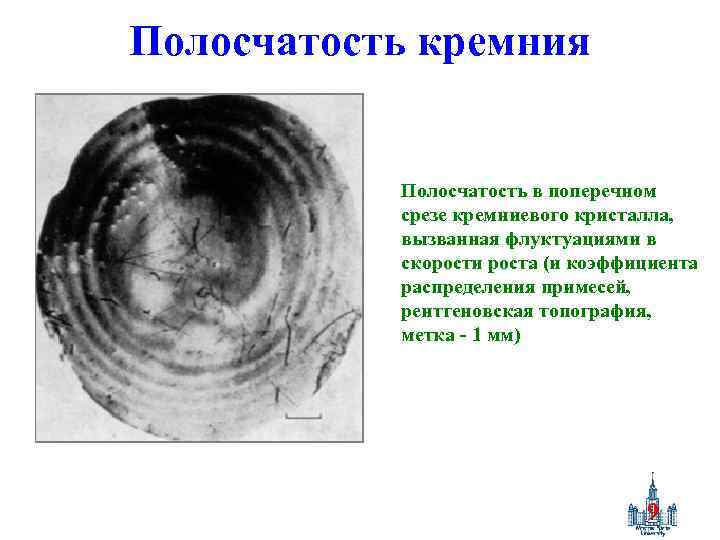 Полосчатость кремния Полосчатость в поперечном срезе кремниевого кристалла, вызванная флуктуациями в скорости роста (и коэффициента распределения примесей, рентгеновская топография, метка - 1 мм) 9
Полосчатость кремния Полосчатость в поперечном срезе кремниевого кристалла, вызванная флуктуациями в скорости роста (и коэффициента распределения примесей, рентгеновская топография, метка - 1 мм) 9
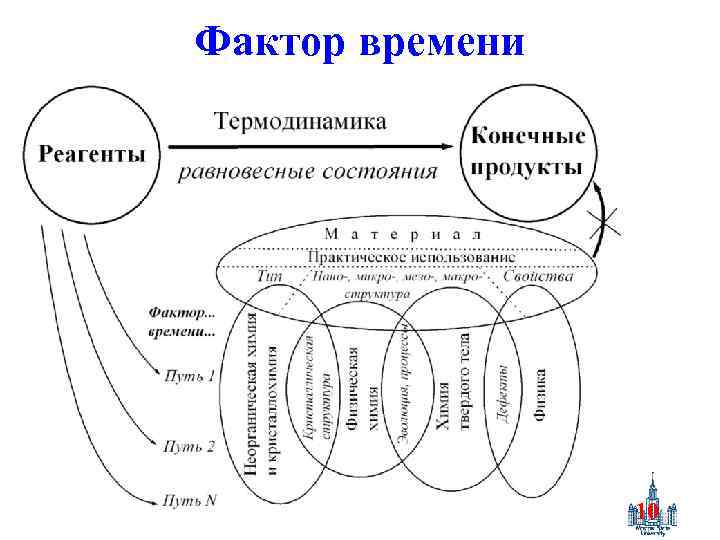 Фактор времени 10
Фактор времени 10
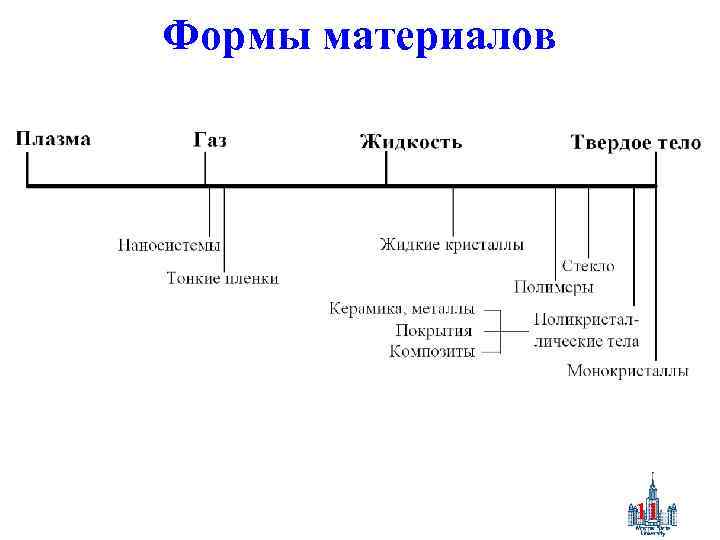 Формы материалов 11
Формы материалов 11
 Кристаллы, керамика, композиты ВТСП Вискеры-суперионики П/п Кобальтиты ВТСП Манганиты Цирконаты, биокерамика -спонтанная кристаллизация, метод Бриджмена, ПЖК, электрокристаллизация -керамический метод, расплавные технологии, керамические пены -криохимическая технология, пиролиз аэрозолей 12
Кристаллы, керамика, композиты ВТСП Вискеры-суперионики П/п Кобальтиты ВТСП Манганиты Цирконаты, биокерамика -спонтанная кристаллизация, метод Бриджмена, ПЖК, электрокристаллизация -керамический метод, расплавные технологии, керамические пены -криохимическая технология, пиролиз аэрозолей 12
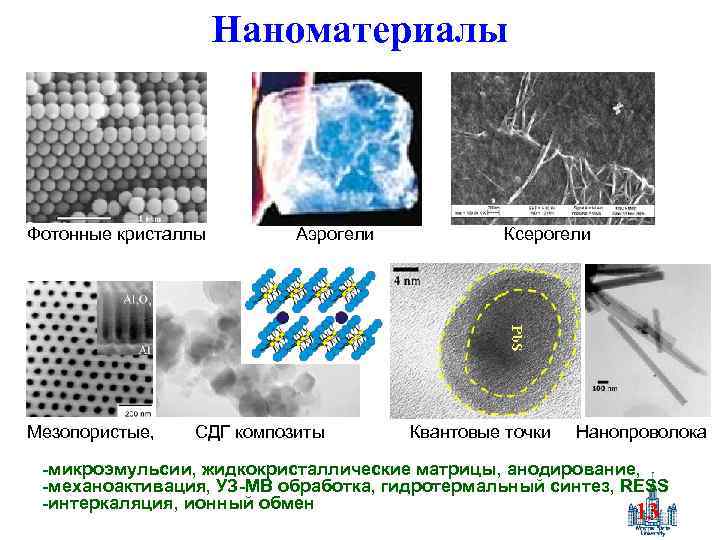 Наноматериалы Фотонные кристаллы Аэрогели Ксерогели Мезопористые, СДГ композиты Квантовые точки Нанопроволока -микроэмульсии, жидкокристаллические матрицы, анодирование, -механоактивация, УЗ-МВ обработка, гидротермальный синтез, RESS -интеркаляция, ионный обмен 13
Наноматериалы Фотонные кристаллы Аэрогели Ксерогели Мезопористые, СДГ композиты Квантовые точки Нанопроволока -микроэмульсии, жидкокристаллические матрицы, анодирование, -механоактивация, УЗ-МВ обработка, гидротермальный синтез, RESS -интеркаляция, ионный обмен 13
 Углеродные нанотрубки (CNT) Многостенные CNT Интеркалированные CNT 14
Углеродные нанотрубки (CNT) Многостенные CNT Интеркалированные CNT 14
 Нанотрубки оксида ванадия a б 15
Нанотрубки оксида ванадия a б 15
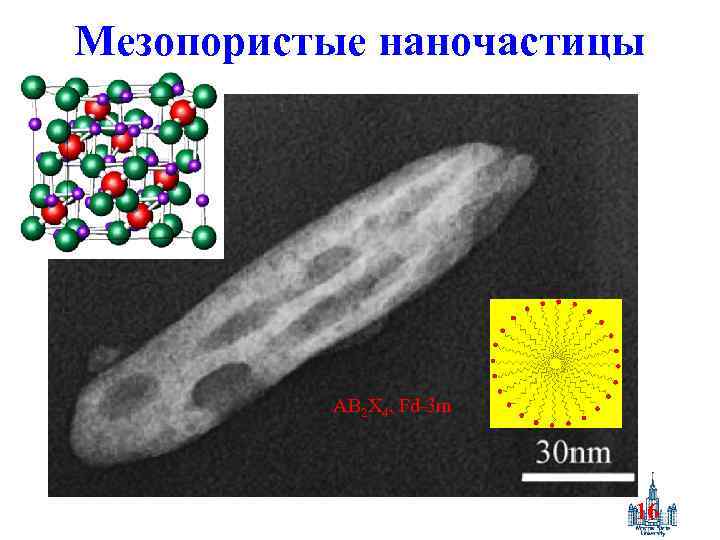 Мезопористые наночастицы AB 2 X 4, Fd-3 m 16
Мезопористые наночастицы AB 2 X 4, Fd-3 m 16
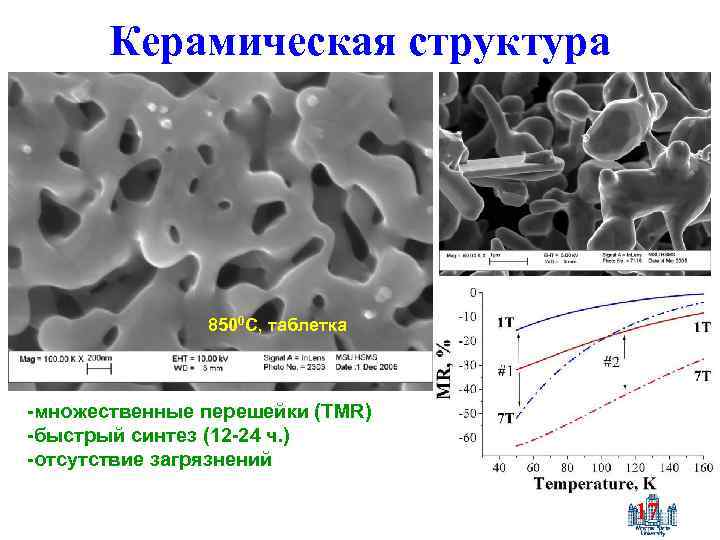 Керамическая структура 8500 С, таблетка -множественные перешейки (TMR) -быстрый синтез (12 -24 ч. ) -отсутствие загрязнений 17
Керамическая структура 8500 С, таблетка -множественные перешейки (TMR) -быстрый синтез (12 -24 ч. ) -отсутствие загрязнений 17
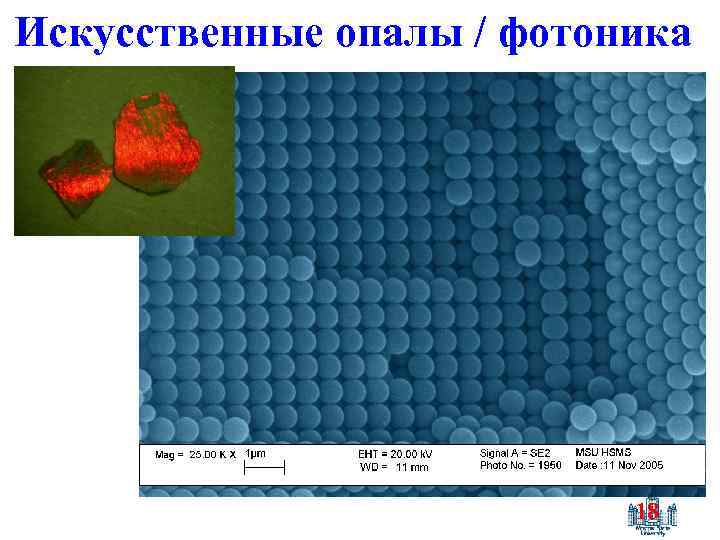 Искусственные опалы / фотоника 18
Искусственные опалы / фотоника 18
 Жемчуг и крылья бабочек 19
Жемчуг и крылья бабочек 19
 Кермет WC, Ta. C, BC Ti. C-Co (Cr, Bi, W, Mo, Fe, Al…) твердость карбидов + вязкость металла -Износоустойчивость -Удароустойчивость -Термоустойчивость Карбид бора в алюминии 20
Кермет WC, Ta. C, BC Ti. C-Co (Cr, Bi, W, Mo, Fe, Al…) твердость карбидов + вязкость металла -Износоустойчивость -Удароустойчивость -Термоустойчивость Карбид бора в алюминии 20
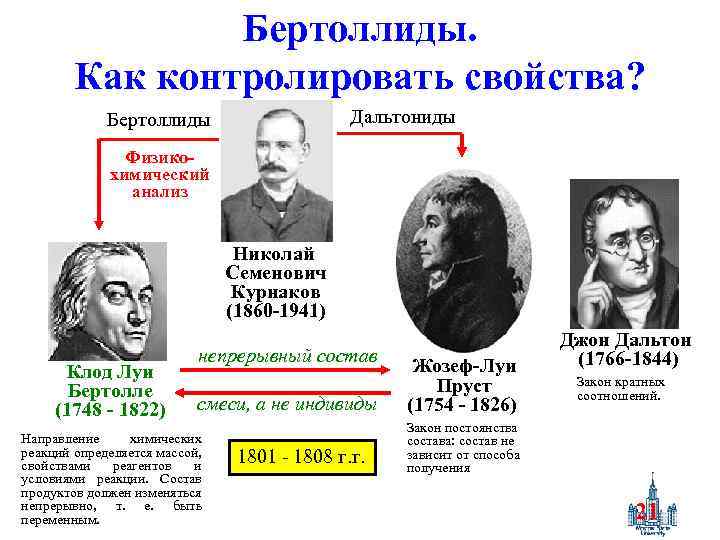 Бертоллиды. Как контролировать свойства? Дальтониды Бертоллиды Физикохимический анализ Николай Семенович Курнаков (1860 -1941) Клод Луи Бертолле (1748 - 1822) непрерывный состав смеси, а не индивиды Направление химических реакций определяется массой, свойствами реагентов и условиями реакции. Состав продуктов должен изменяться непрерывно, т. е. быть переменным. 1801 - 1808 г. г. Жозеф-Луи Пруст (1754 - 1826) Джон Дальтон (1766 -1844) Закон кратных соотношений. Закон постоянства состава: состав не зависит от способа получения 21
Бертоллиды. Как контролировать свойства? Дальтониды Бертоллиды Физикохимический анализ Николай Семенович Курнаков (1860 -1941) Клод Луи Бертолле (1748 - 1822) непрерывный состав смеси, а не индивиды Направление химических реакций определяется массой, свойствами реагентов и условиями реакции. Состав продуктов должен изменяться непрерывно, т. е. быть переменным. 1801 - 1808 г. г. Жозеф-Луи Пруст (1754 - 1826) Джон Дальтон (1766 -1844) Закон кратных соотношений. Закон постоянства состава: состав не зависит от способа получения 21
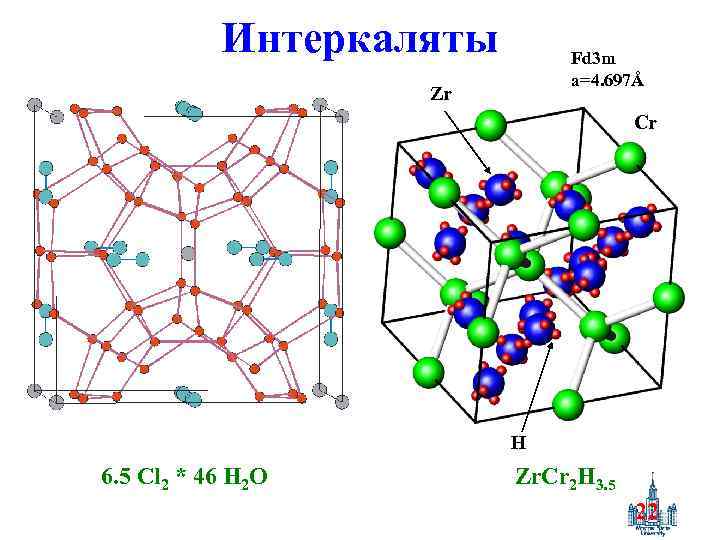 Интеркаляты Fd 3 m a=4. 697Å Zr Cr H 6. 5 Cl 2 * 46 H 2 O Zr. Cr 2 H 3. 5 22
Интеркаляты Fd 3 m a=4. 697Å Zr Cr H 6. 5 Cl 2 * 46 H 2 O Zr. Cr 2 H 3. 5 22
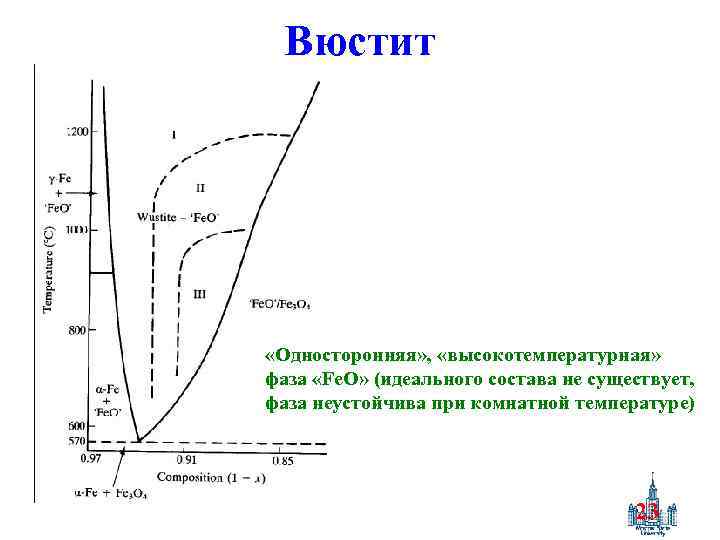 Вюстит «Односторонняя» , «высокотемпературная» фаза «Fe. O» (идеального состава не существует, фаза неустойчива при комнатной температуре) 23
Вюстит «Односторонняя» , «высокотемпературная» фаза «Fe. O» (идеального состава не существует, фаза неустойчива при комнатной температуре) 23
 Область гомогенности Серии образцов ABCD: Одинаковая предыстория Tprep. = const варьирование x re ctu u str o m icr ) M C( C(M): Одинаковый состав (x) Tprep. = const разная микроструктура C 1…C 4: Одинаковая предыстория Одинаковый состав (x) разные Tprep. 24
Область гомогенности Серии образцов ABCD: Одинаковая предыстория Tprep. = const варьирование x re ctu u str o m icr ) M C( C(M): Одинаковый состав (x) Tprep. = const разная микроструктура C 1…C 4: Одинаковая предыстория Одинаковый состав (x) разные Tprep. 24
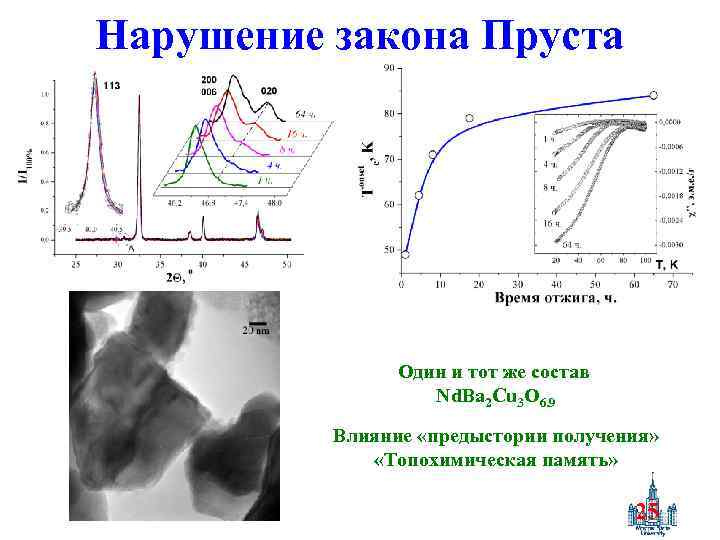 Нарушение закона Пруста Один и тот же состав Nd. Ba 2 Cu 3 O 6. 9 Влияние «предыстории получения» «Топохимическая память» 25
Нарушение закона Пруста Один и тот же состав Nd. Ba 2 Cu 3 O 6. 9 Влияние «предыстории получения» «Топохимическая память» 25
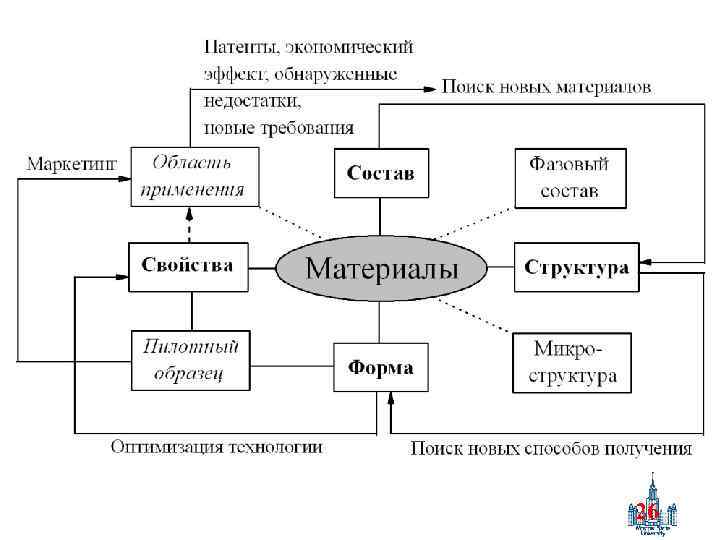 26
26
 Признаки • • • Неравновесность Особое состояние (форма материала) Нестехиометрия / композиты Зависимость от предыстории получения Иерархическая дефектная структура 27
Признаки • • • Неравновесность Особое состояние (форма материала) Нестехиометрия / композиты Зависимость от предыстории получения Иерархическая дефектная структура 27
 Сравнение определений Элемент – совокупность атомов Вещество – соединение химических элементов определенного состава Фаза - совокупности всех гомогенных частей гетерогенной системы с постоянным составом и свойствами, отделенной от других частей системы межфазными границами. Материал – вещество, обладающее свойствами, которые предопределяют то или иное его практическое применение. (акад. И. В. Тананаев) Состав + агрегатное состояние (газ, жидкость, твердое) + аллотропия (различные молекулярные формы элемента) + полиморфизм (различные кристаллические формы вещества одного и того же состава) + дефекты. Лишь в гипотетическом, абсолютно химически чистом идеальном кристалле существует бесконечная решетка из строго периодически расположенных в пространстве атомов, которые находятся в покое в своих равновесных положениях. Совершенный кристалл – кристалл, в котором (дополнительно) существуют термические колебания атомов. Реальный кристалл ограничен гранями и содержит точечные и протяженные дефекты. Дефекты (от лат. defectus — недостаток, изъян) – нарушения периодичности кристаллической структуры. Помимо статических дефектов, существуют отклонения от идеальной решётки другого рода, связанные с тепловыми колебаниями частиц, составляющих решётку (динамические дефекты). 28
Сравнение определений Элемент – совокупность атомов Вещество – соединение химических элементов определенного состава Фаза - совокупности всех гомогенных частей гетерогенной системы с постоянным составом и свойствами, отделенной от других частей системы межфазными границами. Материал – вещество, обладающее свойствами, которые предопределяют то или иное его практическое применение. (акад. И. В. Тананаев) Состав + агрегатное состояние (газ, жидкость, твердое) + аллотропия (различные молекулярные формы элемента) + полиморфизм (различные кристаллические формы вещества одного и того же состава) + дефекты. Лишь в гипотетическом, абсолютно химически чистом идеальном кристалле существует бесконечная решетка из строго периодически расположенных в пространстве атомов, которые находятся в покое в своих равновесных положениях. Совершенный кристалл – кристалл, в котором (дополнительно) существуют термические колебания атомов. Реальный кристалл ограничен гранями и содержит точечные и протяженные дефекты. Дефекты (от лат. defectus — недостаток, изъян) – нарушения периодичности кристаллической структуры. Помимо статических дефектов, существуют отклонения от идеальной решётки другого рода, связанные с тепловыми колебаниями частиц, составляющих решётку (динамические дефекты). 28
 Классификация дефектов 1. Нульмерные (точечные) дефекты – вакансии, межузельные атомы, примеси, центры окраски и пр. 2. Одномерные (линейные) дефекты – цепочки точечных дефектов, дислокации 3. Двумерные (поверхностные) дефекты – дефекты упаковки, границы блоков мозаики, границы зерен, двойников, межфазные границы, сама поверхность кристалла 4. Трехмерные (объемные) дефекты – пустоты, включения второй фазы (по Ван-Бюрену) - Равновесные дефекты (термодинамика) – точечные (определенная концентрация и тип) - Неравновесные дефекты ( «предыстория» ) – дислокации (10 -100 э. В), блоки мозаики, границы зерен - Взаимодействие дефектов (дислокации и точечные дефекты) - Собственные и несобственные дефекты 29
Классификация дефектов 1. Нульмерные (точечные) дефекты – вакансии, межузельные атомы, примеси, центры окраски и пр. 2. Одномерные (линейные) дефекты – цепочки точечных дефектов, дислокации 3. Двумерные (поверхностные) дефекты – дефекты упаковки, границы блоков мозаики, границы зерен, двойников, межфазные границы, сама поверхность кристалла 4. Трехмерные (объемные) дефекты – пустоты, включения второй фазы (по Ван-Бюрену) - Равновесные дефекты (термодинамика) – точечные (определенная концентрация и тип) - Неравновесные дефекты ( «предыстория» ) – дислокации (10 -100 э. В), блоки мозаики, границы зерен - Взаимодействие дефектов (дислокации и точечные дефекты) - Собственные и несобственные дефекты 29
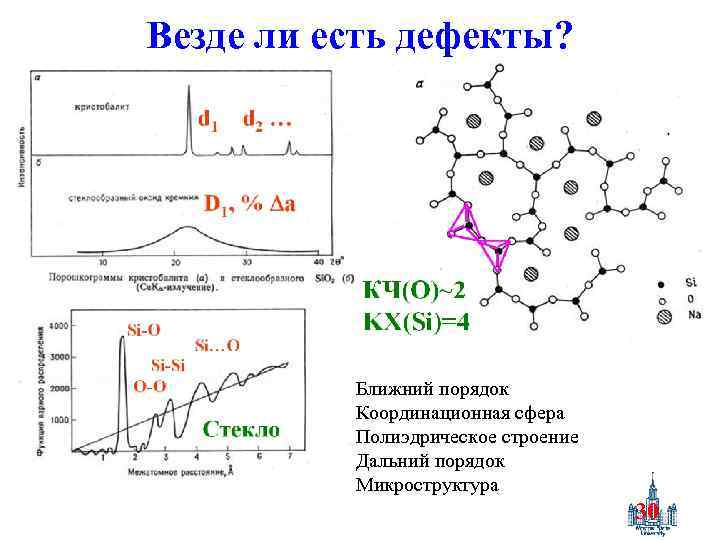 Везде ли есть дефекты? Ближний порядок Координационная сфера Полиэдрическое строение Дальний порядок Микроструктура 30
Везде ли есть дефекты? Ближний порядок Координационная сфера Полиэдрическое строение Дальний порядок Микроструктура 30
 Шкала размеров 31
Шкала размеров 31
 Иглы для атомно-силовой микроскопии Фотолитография + ПЖК 32
Иглы для атомно-силовой микроскопии Фотолитография + ПЖК 32
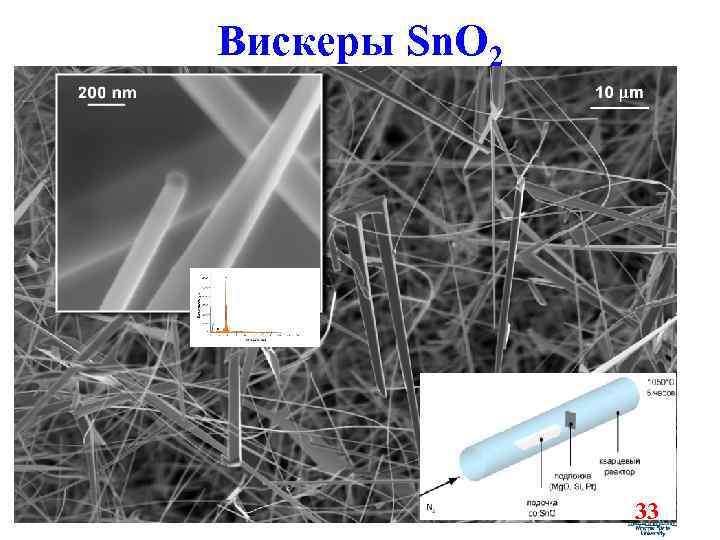 Вискеры Sn. O 2 33
Вискеры Sn. O 2 33
 Нитевидные кристаллы Si. O 2 Система Ga-N-Si-O (лит. данные) 34
Нитевидные кристаллы Si. O 2 Система Ga-N-Si-O (лит. данные) 34
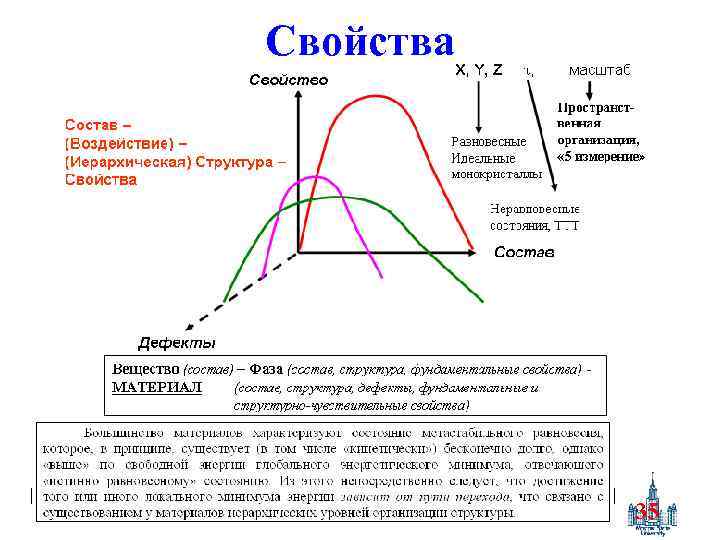 Свойства 35
Свойства 35
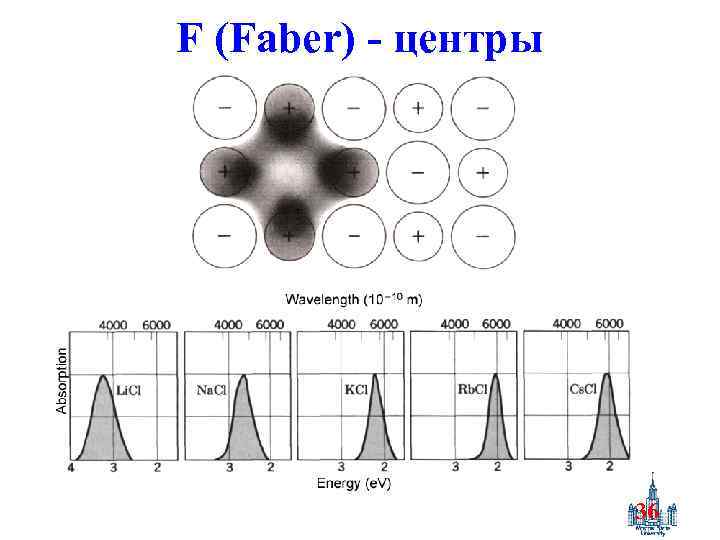 F (Faber) - центры 36
F (Faber) - центры 36
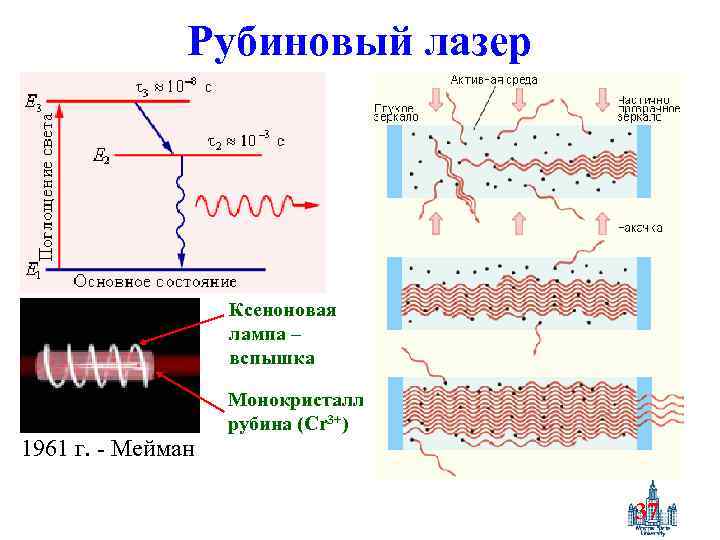 Рубиновый лазер Ксеноновая лампа – вспышка 1961 г. - Мейман Монокристалл рубина (Cr 3+) 37
Рубиновый лазер Ксеноновая лампа – вспышка 1961 г. - Мейман Монокристалл рубина (Cr 3+) 37
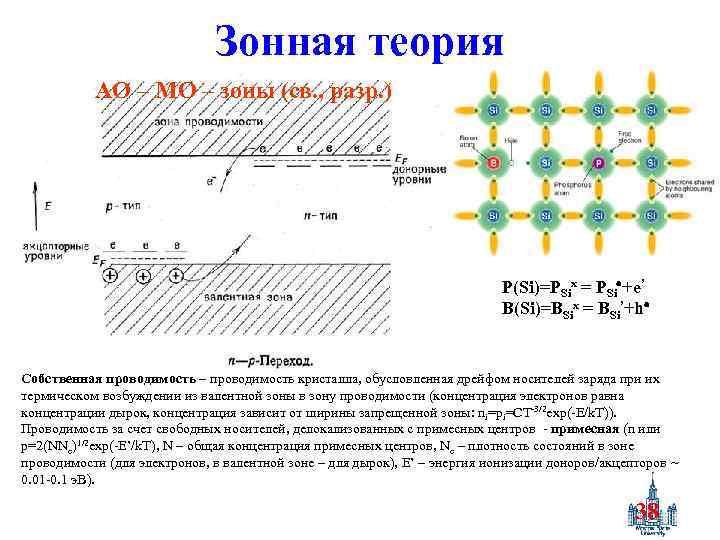 Зонная теория AO – MO – зоны (св. , разр. ) P(Si)=PSix = PSi +e’ B(Si)=BSix = BSi’+h Собственная проводимость – проводимость кристалла, обусловленная дрейфом носителей заряда при их термическом возбуждении из валентной зоны в зону проводимости (концентрация электронов равна концентрации дырок, концентрация зависит от ширины запрещенной зоны: ni=pi=CT-3/2 exp(-E/k. T)). Проводимость за счет свободных носителей, делокализованных с примесных центров - примесная (n или p=2(NNc)1/2 exp(-E’/k. T), N – общая концентрация примесных центров, Nc – плотность состояний в зоне проводимости (для электронов, в валентной зоне – для дырок), E’ – энергия ионизации доноров/акцепторов ~ 0. 01 -0. 1 э. В). 38
Зонная теория AO – MO – зоны (св. , разр. ) P(Si)=PSix = PSi +e’ B(Si)=BSix = BSi’+h Собственная проводимость – проводимость кристалла, обусловленная дрейфом носителей заряда при их термическом возбуждении из валентной зоны в зону проводимости (концентрация электронов равна концентрации дырок, концентрация зависит от ширины запрещенной зоны: ni=pi=CT-3/2 exp(-E/k. T)). Проводимость за счет свободных носителей, делокализованных с примесных центров - примесная (n или p=2(NNc)1/2 exp(-E’/k. T), N – общая концентрация примесных центров, Nc – плотность состояний в зоне проводимости (для электронов, в валентной зоне – для дырок), E’ – энергия ионизации доноров/акцепторов ~ 0. 01 -0. 1 э. В). 38
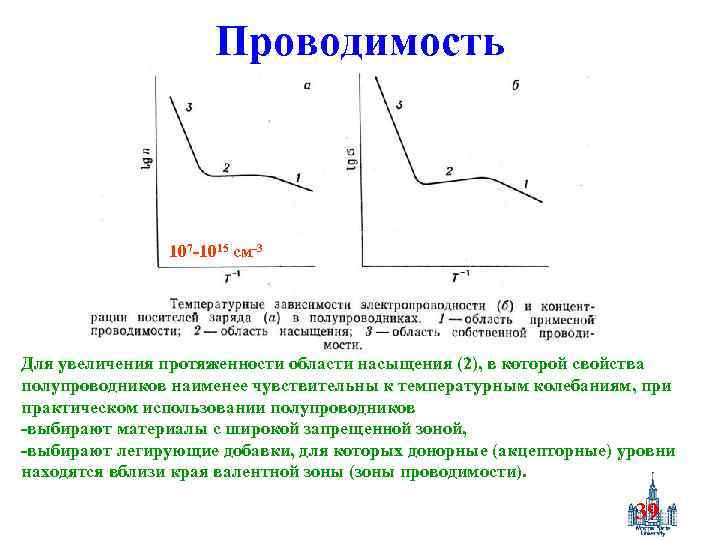 Проводимость 107 -1015 см-3 Для увеличения протяженности области насыщения (2), в которой свойства полупроводников наименее чувствительны к температурным колебаниям, при практическом использовании полупроводников -выбирают материалы с широкой запрещенной зоной, -выбирают легирующие добавки, для которых донорные (акцепторные) уровни находятся вблизи края валентной зоны (зоны проводимости). 39
Проводимость 107 -1015 см-3 Для увеличения протяженности области насыщения (2), в которой свойства полупроводников наименее чувствительны к температурным колебаниям, при практическом использовании полупроводников -выбирают материалы с широкой запрещенной зоной, -выбирают легирующие добавки, для которых донорные (акцепторные) уровни находятся вблизи края валентной зоны (зоны проводимости). 39
![Фотокатализ ] 01 [0 hν UV Ti. O 2 h+ e- OH OH H Фотокатализ ] 01 [0 hν UV Ti. O 2 h+ e- OH OH H](https://present5.com/presentation/3506544_176381504/image-40.jpg) Фотокатализ ] 01 [0 hν UV Ti. O 2 h+ e- OH OH H 2 O Ti 4+ O 2 CO 2 HO 2 40
Фотокатализ ] 01 [0 hν UV Ti. O 2 h+ e- OH OH H 2 O Ti 4+ O 2 CO 2 HO 2 40
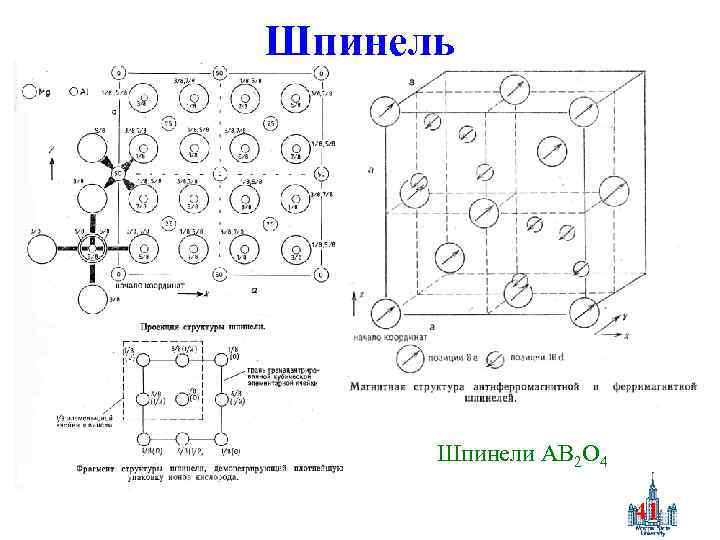 Шпинель Шпинели AB 2 O 4 41
Шпинель Шпинели AB 2 O 4 41
 Описание Кубические Fd 3 m, n = 8. КПУ кислорода, в пустотах: ½ окт – В, 1/8 тетр. – А. [A 1 -δB δ][AδB 2 -δ]o. O 4, δ – степень обращения γ-Fe 2 O 3: [Fe 3+]т[V 1/3 Fe 1 2/33+]O 4 Факторы распределения: 1. Ионные радикалы, электронное строение: Ni 2+, Cr 3+ - окт. , Mn 2+, Fe 3+, Mg 2+ - люб. , Cd 2+, Ga 3+ - тетр. 2. Электростатическая энергия – высокий заряд – октаэдр δ = f(T): δ(1+δ)/(1 -δ)2 = e-E/k. T E – энергия перераспределения октаэдр ↔ тетраэдр δ увеличивается с Т, ∟АОВ ≈ 125 о, ∟ВОВ ≈ 90 o A↑ B↓ B↓ μ = μB – μA (в магнетонах Бора, «μВ» ), μА = g. SA = n. A, μB = g. SB = n. B 42
Описание Кубические Fd 3 m, n = 8. КПУ кислорода, в пустотах: ½ окт – В, 1/8 тетр. – А. [A 1 -δB δ][AδB 2 -δ]o. O 4, δ – степень обращения γ-Fe 2 O 3: [Fe 3+]т[V 1/3 Fe 1 2/33+]O 4 Факторы распределения: 1. Ионные радикалы, электронное строение: Ni 2+, Cr 3+ - окт. , Mn 2+, Fe 3+, Mg 2+ - люб. , Cd 2+, Ga 3+ - тетр. 2. Электростатическая энергия – высокий заряд – октаэдр δ = f(T): δ(1+δ)/(1 -δ)2 = e-E/k. T E – энергия перераспределения октаэдр ↔ тетраэдр δ увеличивается с Т, ∟АОВ ≈ 125 о, ∟ВОВ ≈ 90 o A↑ B↓ B↓ μ = μB – μA (в магнетонах Бора, «μВ» ), μА = g. SA = n. A, μB = g. SB = n. B 42
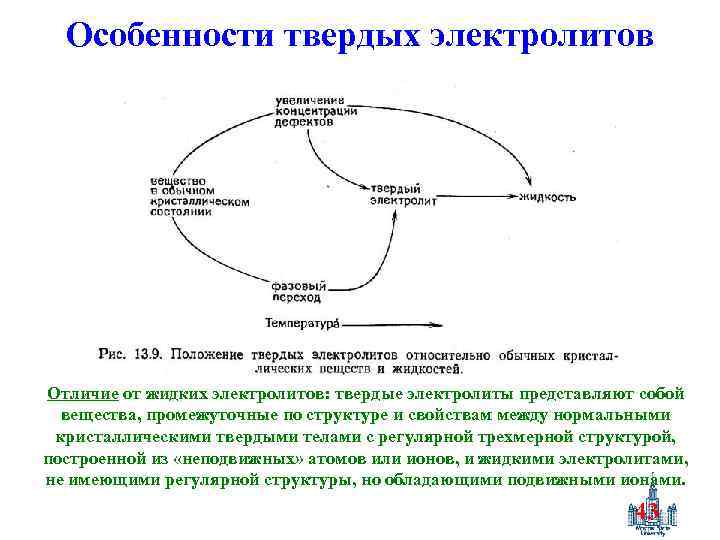 Особенности твердых электролитов Отличие от жидких электролитов: твердые электролиты представляют собой вещества, промежуточные по структуре и свойствам между нормальными кристаллическими твердыми телами с регулярной трехмерной структурой, построенной из «неподвижных» атомов или ионов, и жидкими электролитами, не имеющими регулярной структуры, но обладающими подвижными ионами. 43
Особенности твердых электролитов Отличие от жидких электролитов: твердые электролиты представляют собой вещества, промежуточные по структуре и свойствам между нормальными кристаллическими твердыми телами с регулярной трехмерной структурой, построенной из «неподвижных» атомов или ионов, и жидкими электролитами, не имеющими регулярной структуры, но обладающими подвижными ионами. 43
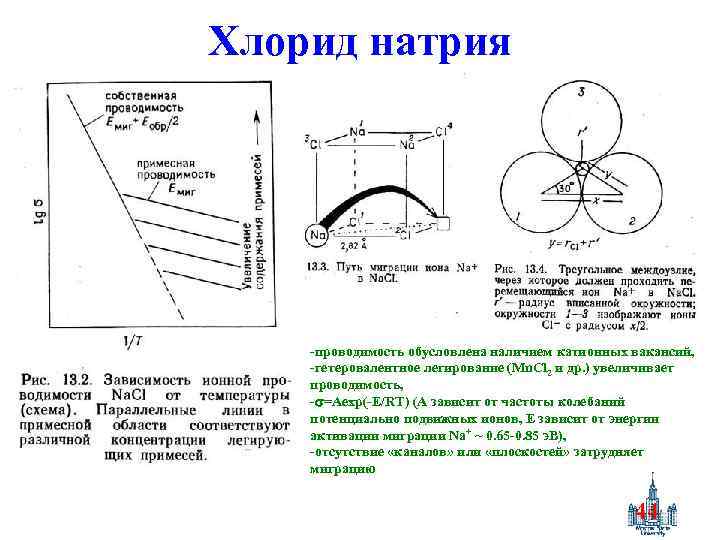 Хлорид натрия -проводимость обусловлена наличием катионных вакансий, -гетеровалентное легирование (Mn. Cl 2 и др. ) увеличивает проводимость, - =Aexp(-E/RT) (A зависит от частоты колебаний потенциально подвижных ионов, Е зависит от энергии активации миграции Na+ ~ 0. 65 -0. 85 э. В), -отсутствие «каналов» или «плоскостей» затрудняет миграцию 44
Хлорид натрия -проводимость обусловлена наличием катионных вакансий, -гетеровалентное легирование (Mn. Cl 2 и др. ) увеличивает проводимость, - =Aexp(-E/RT) (A зависит от частоты колебаний потенциально подвижных ионов, Е зависит от энергии активации миграции Na+ ~ 0. 65 -0. 85 э. В), -отсутствие «каналов» или «плоскостей» затрудняет миграцию 44
 Ag. Cl (механизм проводимости) Доминирующий тип дефектов – дефекты Френкеля (подвижные междоузельные ионы Ag+, связанные с катионными вакансиями). 45
Ag. Cl (механизм проводимости) Доминирующий тип дефектов – дефекты Френкеля (подвижные междоузельные ионы Ag+, связанные с катионными вакансиями). 45
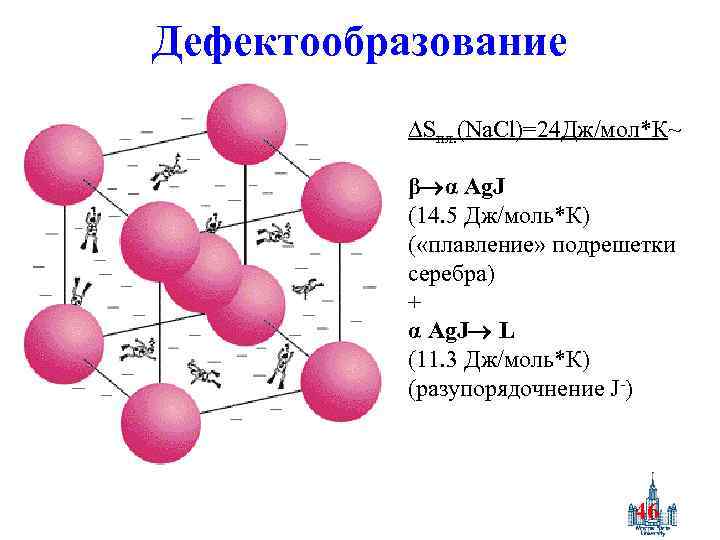 Дефектообразование Sпл. (Na. Cl)=24 Дж/мол*К~ β α Ag. J (14. 5 Дж/моль*К) ( «плавление» подрешетки серебра) + α Ag. J L (11. 3 Дж/моль*К) (разупорядочнение J-) 46
Дефектообразование Sпл. (Na. Cl)=24 Дж/мол*К~ β α Ag. J (14. 5 Дж/моль*К) ( «плавление» подрешетки серебра) + α Ag. J L (11. 3 Дж/моль*К) (разупорядочнение J-) 46
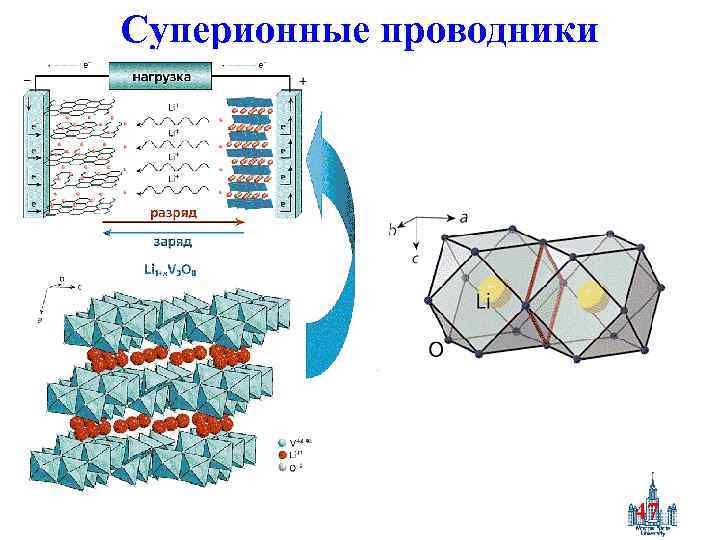 Суперионные проводники 47
Суперионные проводники 47
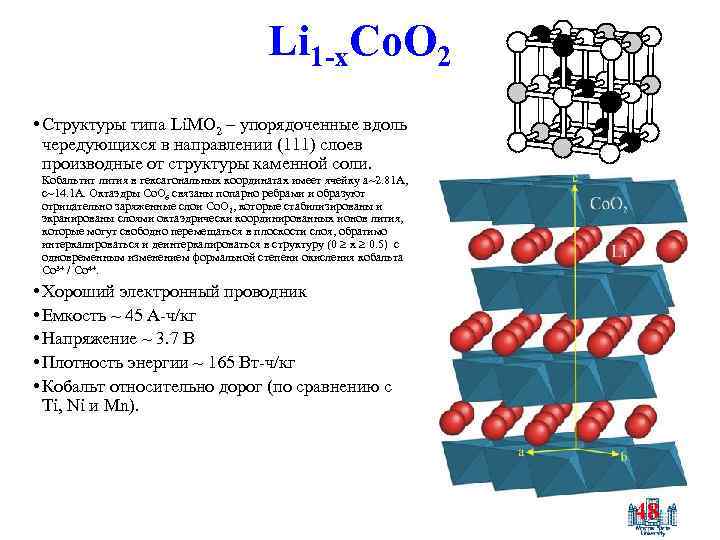 Li 1 -x. Co. O 2 • Структуры типа Li. MO 2 – упорядоченные вдоль чередующихся в направлении (111) слоев производные от структуры каменной соли. Кобальтит лития в гексагональных координатах имеет ячейку a~2. 81 A, c~14. 1 A. Октаэдры Co. O 6 связаны попарно ребрами и образуют отрицательно заряженные слои Co. O 2, которые стабилизированы и экранированы слоями октаэдрически координированных ионов лития, которые могут свободно перемещаться в плоскости слоя, обратимо интеркалироваться и деинтеркалироваться в структуру (0 x 0. 5) с одновременным изменением формальной степени окисления кобальта Co 3+ / Co 4+. • Хороший электронный проводник • Емкость ~ 45 А-ч/кг • Напряжение ~ 3. 7 В • Плотность энергии ~ 165 Вт-ч/кг • Кобальт относительно дорог (по сравнению с Ti, Ni и Mn). 48
Li 1 -x. Co. O 2 • Структуры типа Li. MO 2 – упорядоченные вдоль чередующихся в направлении (111) слоев производные от структуры каменной соли. Кобальтит лития в гексагональных координатах имеет ячейку a~2. 81 A, c~14. 1 A. Октаэдры Co. O 6 связаны попарно ребрами и образуют отрицательно заряженные слои Co. O 2, которые стабилизированы и экранированы слоями октаэдрически координированных ионов лития, которые могут свободно перемещаться в плоскости слоя, обратимо интеркалироваться и деинтеркалироваться в структуру (0 x 0. 5) с одновременным изменением формальной степени окисления кобальта Co 3+ / Co 4+. • Хороший электронный проводник • Емкость ~ 45 А-ч/кг • Напряжение ~ 3. 7 В • Плотность энергии ~ 165 Вт-ч/кг • Кобальт относительно дорог (по сравнению с Ti, Ni и Mn). 48
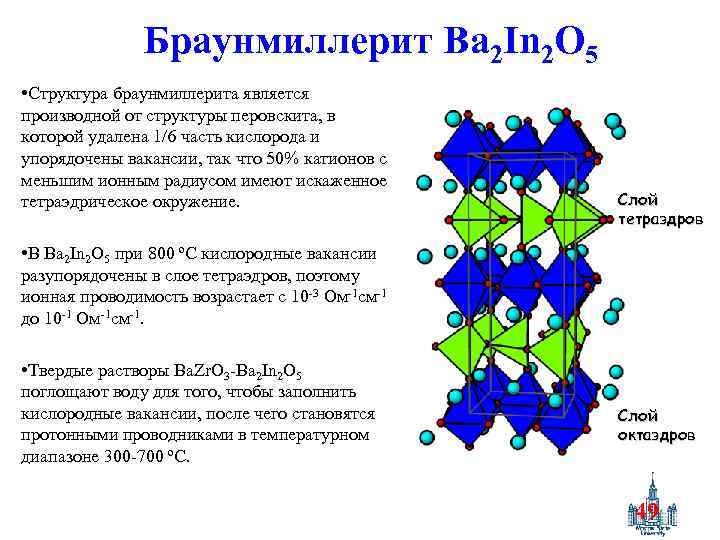 Браунмиллерит Ba 2 In 2 O 5 • Структура браунмиллерита является производной от структуры перовскита, в которой удалена 1/6 часть кислорода и упорядочены вакансии, так что 50% катионов с меньшим ионным радиусом имеют искаженное тетраэдрическое окружение. Слой тетраэдров • В Ba 2 In 2 O 5 при 800 ºC кислородные вакансии разупорядочены в слое тетраэдров, поэтому ионная проводимость возрастает с 10 -3 Ом-1 см-1 до 10 -1 Ом-1 см-1. • Твердые растворы Ba. Zr. O 3 -Ba 2 In 2 O 5 поглощают воду для того, чтобы заполнить кислородные вакансии, после чего становятся протонными проводниками в температурном диапазоне 300 -700 ºC. Слой октаэдров 49
Браунмиллерит Ba 2 In 2 O 5 • Структура браунмиллерита является производной от структуры перовскита, в которой удалена 1/6 часть кислорода и упорядочены вакансии, так что 50% катионов с меньшим ионным радиусом имеют искаженное тетраэдрическое окружение. Слой тетраэдров • В Ba 2 In 2 O 5 при 800 ºC кислородные вакансии разупорядочены в слое тетраэдров, поэтому ионная проводимость возрастает с 10 -3 Ом-1 см-1 до 10 -1 Ом-1 см-1. • Твердые растворы Ba. Zr. O 3 -Ba 2 In 2 O 5 поглощают воду для того, чтобы заполнить кислородные вакансии, после чего становятся протонными проводниками в температурном диапазоне 300 -700 ºC. Слой октаэдров 49
 Фазы Ауривиллиуса и Bi. Me. VOx • Фазы Ауривиллиуса (например, Bi 2 WO 6) содержат двумерные перовскитоподобные слои из соединяющихся по вершинам октаэдров, зажатых слоями типа Bi 2 O 22+. • (Bi 2 O 2)VO 3. 5 – представитель дефектных фаз Ауривиллиуса, в которых 1/8 часть ктслорода в перовскитном слое вакантна. Мобильны только ионы кислорода в перовскитных слоях. • Легирование V – позиций стабилизирует высокотемпературную модификацию с высокой проводимостью (Bi. Me. VOX). (Bi 2 O 2)Cu 0. 1 V 0. 9 O 3. 35 имеет проводимость порядка 0. 01 Ом-1 см-1 уже при 350 ºC. 50
Фазы Ауривиллиуса и Bi. Me. VOx • Фазы Ауривиллиуса (например, Bi 2 WO 6) содержат двумерные перовскитоподобные слои из соединяющихся по вершинам октаэдров, зажатых слоями типа Bi 2 O 22+. • (Bi 2 O 2)VO 3. 5 – представитель дефектных фаз Ауривиллиуса, в которых 1/8 часть ктслорода в перовскитном слое вакантна. Мобильны только ионы кислорода в перовскитных слоях. • Легирование V – позиций стабилизирует высокотемпературную модификацию с высокой проводимостью (Bi. Me. VOX). (Bi 2 O 2)Cu 0. 1 V 0. 9 O 3. 35 имеет проводимость порядка 0. 01 Ом-1 см-1 уже при 350 ºC. 50
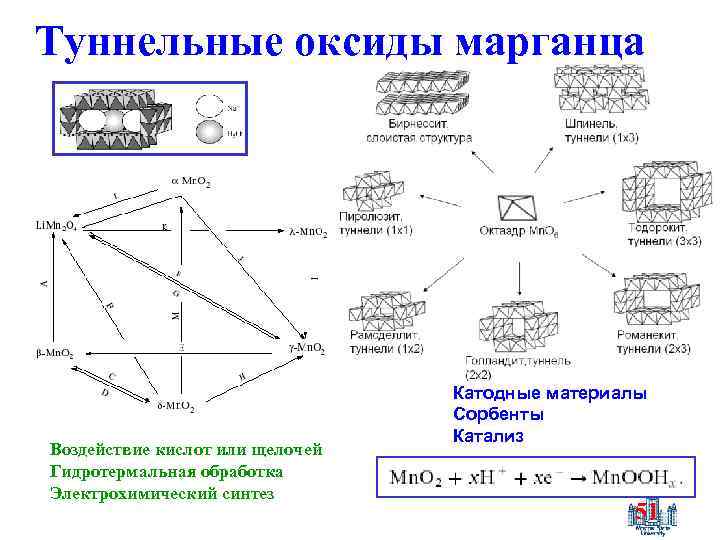 Туннельные оксиды марганца Воздействие кислот или щелочей Гидротермальная обработка Электрохимический синтез Катодные материалы Сорбенты Катализ 51
Туннельные оксиды марганца Воздействие кислот или щелочей Гидротермальная обработка Электрохимический синтез Катодные материалы Сорбенты Катализ 51
 Декорированные вискеры 52
Декорированные вискеры 52
 Иерарархические уровни структуры Увеличение площади поверхности до 16 м 2/г 53
Иерарархические уровни структуры Увеличение площади поверхности до 16 м 2/г 53
 Туннельные структуры R S D Ba 6 Mn 24 O 48 54
Туннельные структуры R S D Ba 6 Mn 24 O 48 54
 Морфология Н-формы вискеров Гор. конц. HNO 3, 5 часов 55
Морфология Н-формы вискеров Гор. конц. HNO 3, 5 часов 55
 Микроструктура Холодная конц. HNO 3, 9 дней 56
Микроструктура Холодная конц. HNO 3, 9 дней 56
 Композитный материал 57
Композитный материал 57
 Открытие ВТСП Е. В. Антипов, С. Н. Путилин и др. : Hg-ВТСП Tc ~ 4+130 K “химическая” J. G. Bednorz, K. A. Muller Nobel Prize 1987 эволюция Kamerling Onnes: Жидкий He, “плохой металл” Hg Tc ~ 4 K 58
Открытие ВТСП Е. В. Антипов, С. Н. Путилин и др. : Hg-ВТСП Tc ~ 4+130 K “химическая” J. G. Bednorz, K. A. Muller Nobel Prize 1987 эволюция Kamerling Onnes: Жидкий He, “плохой металл” Hg Tc ~ 4 K 58
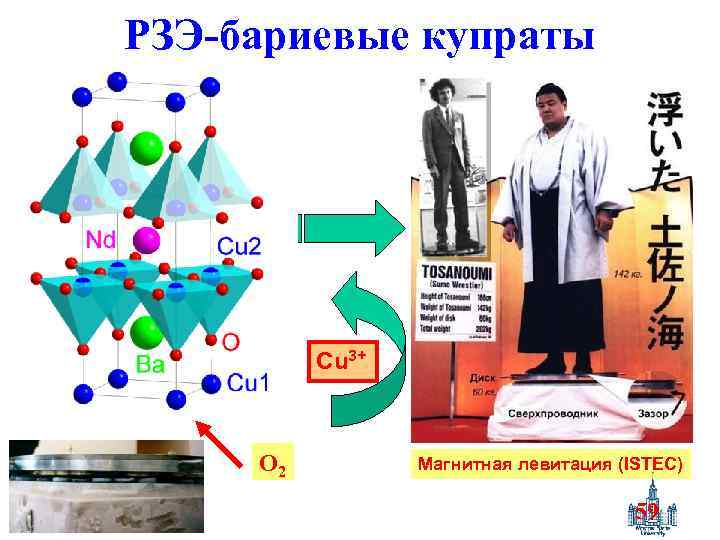 РЗЭ-бариевые купраты Cu 3+ O 2 Магнитная левитация (ISTEC) 59
РЗЭ-бариевые купраты Cu 3+ O 2 Магнитная левитация (ISTEC) 59
 Реальная структура 60
Реальная структура 60
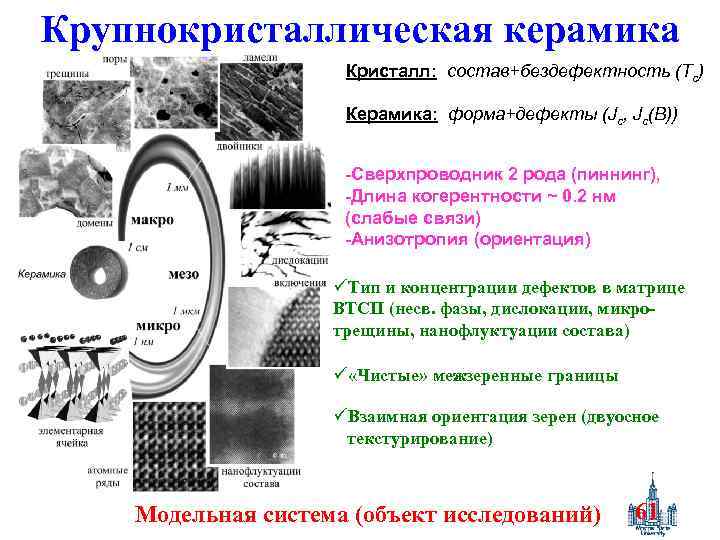 Крупнокристаллическая керамика Кристалл: состав+бездефектность (Тс) Керамика: форма+дефекты (Jc, Jc(B)) -Сверхпроводник 2 рода (пиннинг), -Длина когерентности ~ 0. 2 нм (слабые связи) -Анизотропия (ориентация) üТип и концентрации дефектов в матрице ВТСП (несв. фазы, дислокации, микротрещины, нанофлуктуации состава) ü «Чистые» межзеренные границы üВзаимная ориентация зерен (двуосное текстурирование) Модельная система (объект исследований) 61
Крупнокристаллическая керамика Кристалл: состав+бездефектность (Тс) Керамика: форма+дефекты (Jc, Jc(B)) -Сверхпроводник 2 рода (пиннинг), -Длина когерентности ~ 0. 2 нм (слабые связи) -Анизотропия (ориентация) üТип и концентрации дефектов в матрице ВТСП (несв. фазы, дислокации, микротрещины, нанофлуктуации состава) ü «Чистые» межзеренные границы üВзаимная ориентация зерен (двуосное текстурирование) Модельная система (объект исследований) 61
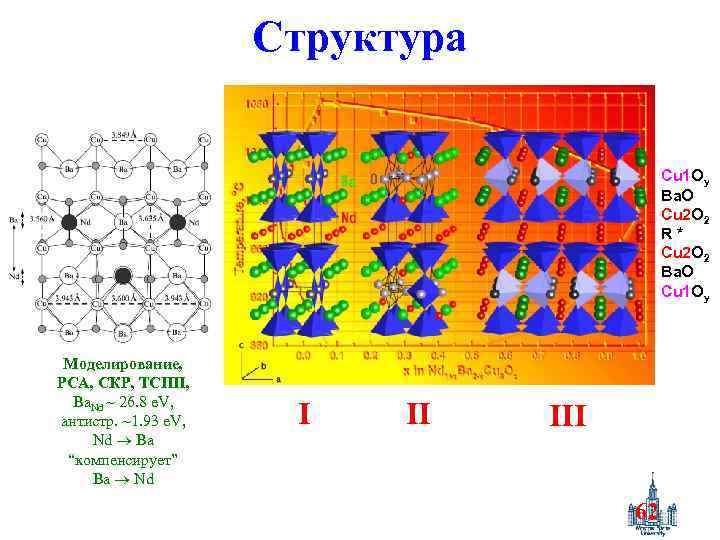 Структура Cu 1 Oy Ba. O Cu 2 O 2 R* Cu 2 O 2 Ba. O Cu 1 Oy Моделирование, РСА, СКР, ТСПП, Ba. Nd ~ 26. 8 e. V, антистр. ~1. 93 e. V, Nd Ba “компенсирует” Ba Nd I II III 62
Структура Cu 1 Oy Ba. O Cu 2 O 2 R* Cu 2 O 2 Ba. O Cu 1 Oy Моделирование, РСА, СКР, ТСПП, Ba. Nd ~ 26. 8 e. V, антистр. ~1. 93 e. V, Nd Ba “компенсирует” Ba Nd I II III 62
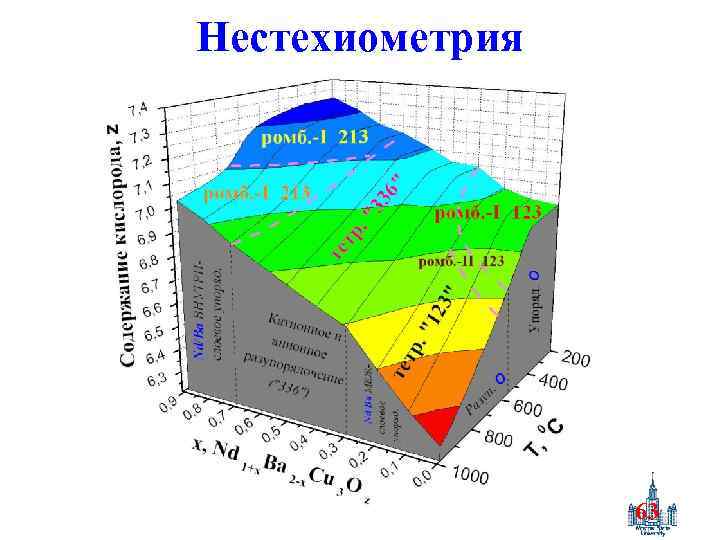 Нестехиометрия 63
Нестехиометрия 63
 Ртутные ВТСП - гомологи Hg. Ba 2 Can. Cun+1 Oz -оптимальная концентрация заряда в сверхпроводящих плоскостях, -оптимальное количество сверхпроводящих плоскостей. Многие ВТСП фазы имеют гомологи ( «вставка» СП-плоскостей): -Y 123, 247, 124, -Bi 2201, 2212, 2223, -… 64
Ртутные ВТСП - гомологи Hg. Ba 2 Can. Cun+1 Oz -оптимальная концентрация заряда в сверхпроводящих плоскостях, -оптимальное количество сверхпроводящих плоскостей. Многие ВТСП фазы имеют гомологи ( «вставка» СП-плоскостей): -Y 123, 247, 124, -Bi 2201, 2212, 2223, -… 64
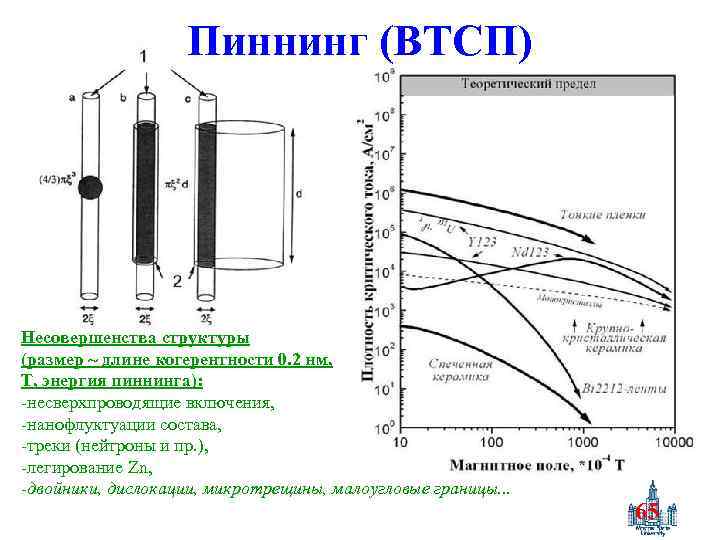 Пиннинг (ВТСП) Несовершенства структуры (размер ~ длине когерентности 0. 2 нм, T, энергия пиннинга): -несверхпроводящие включения, -нанофлуктуации состава, -треки (нейтроны и пр. ), -легирование Zn, -двойники, дислокации, микротрещины, малоугловые границы. . . 65
Пиннинг (ВТСП) Несовершенства структуры (размер ~ длине когерентности 0. 2 нм, T, энергия пиннинга): -несверхпроводящие включения, -нанофлуктуации состава, -треки (нейтроны и пр. ), -легирование Zn, -двойники, дислокации, микротрещины, малоугловые границы. . . 65
 Требуемая микроструктура взаимная ориентация ансамбля кристаллитов в поликристаллическом функциональном материале (максимум интегрированных свойств, баланс внутрикристаллитных свойств и межкристаллитных границ) Jc a’ a C Критично: двуосное текстурирование ( «сильные связи» для повышения Jc(B)) Разориентаци в 100 – падение тока на 1 -2 порядка 66
Требуемая микроструктура взаимная ориентация ансамбля кристаллитов в поликристаллическом функциональном материале (максимум интегрированных свойств, баланс внутрикристаллитных свойств и межкристаллитных границ) Jc a’ a C Критично: двуосное текстурирование ( «сильные связи» для повышения Jc(B)) Разориентаци в 100 – падение тока на 1 -2 порядка 66
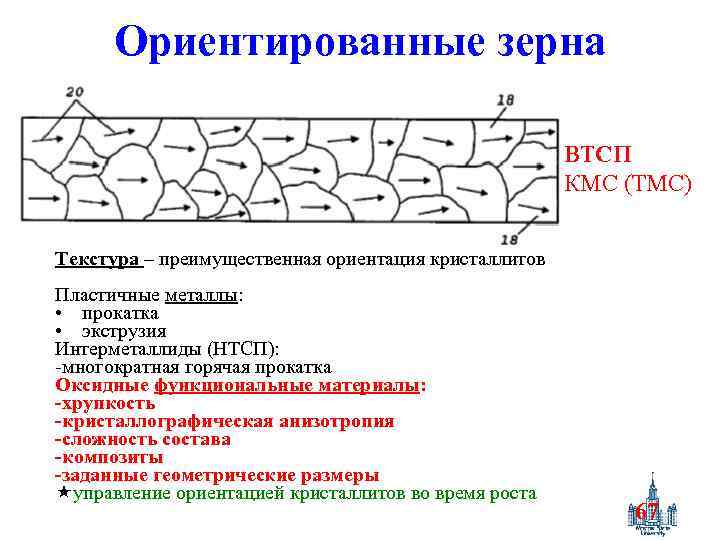 Ориентированные зерна Текстура – преимущественная ориентация кристаллитов Пластичные металлы: • прокатка • экструзия Интерметаллиды (НТСП): -многократная горячая прокатка Оксидные функциональные материалы: -хрупкость -кристаллографическая анизотропия -сложность состава -композиты -заданные геометрические размеры управление ориентацией кристаллитов во время роста 67
Ориентированные зерна Текстура – преимущественная ориентация кристаллитов Пластичные металлы: • прокатка • экструзия Интерметаллиды (НТСП): -многократная горячая прокатка Оксидные функциональные материалы: -хрупкость -кристаллографическая анизотропия -сложность состава -композиты -заданные геометрические размеры управление ориентацией кристаллитов во время роста 67
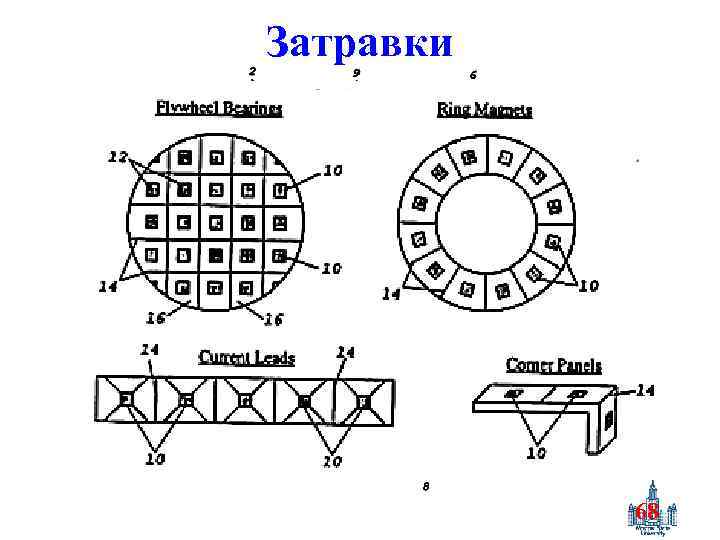 Затравки 68
Затравки 68
 Графоэпитаксиальное «дерево» Дендриты, дендримеры, фракталы 69
Графоэпитаксиальное «дерево» Дендриты, дендримеры, фракталы 69
 Ориентация кристаллитов ВТСП YBa 2 Cu 3 O 6. 5 1 мм Параллельные внутренние стенки канавок üСоответствующий по симметрии рельеф (ось второго порядка, пластинки), üСоответствие размеров кристаллов и элементов рельефа (около 100 мкм), üГеометрические ограничения роста (две параллельные стенки), üКонтроль зародышеобразования (вблизи элементов рельефа) a Двойники 70 b
Ориентация кристаллитов ВТСП YBa 2 Cu 3 O 6. 5 1 мм Параллельные внутренние стенки канавок üСоответствующий по симметрии рельеф (ось второго порядка, пластинки), üСоответствие размеров кристаллов и элементов рельефа (около 100 мкм), üГеометрические ограничения роста (две параллельные стенки), üКонтроль зародышеобразования (вблизи элементов рельефа) a Двойники 70 b
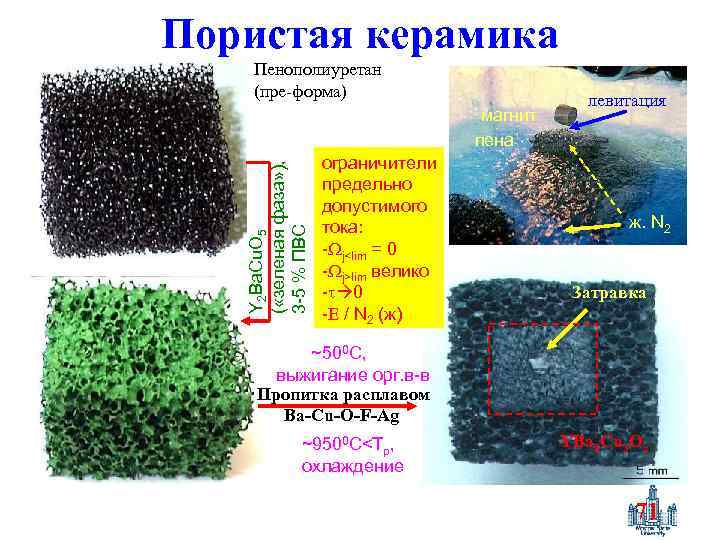 Пористая керамика Пенополиуретан (пре-форма) Y 2 Ba. Cu. O 5 ( «зеленая фаза» ), 3 -5 % ПВС магнит пена ограничители предельно допустимого тока: - j
Пористая керамика Пенополиуретан (пре-форма) Y 2 Ba. Cu. O 5 ( «зеленая фаза» ), 3 -5 % ПВС магнит пена ограничители предельно допустимого тока: - j
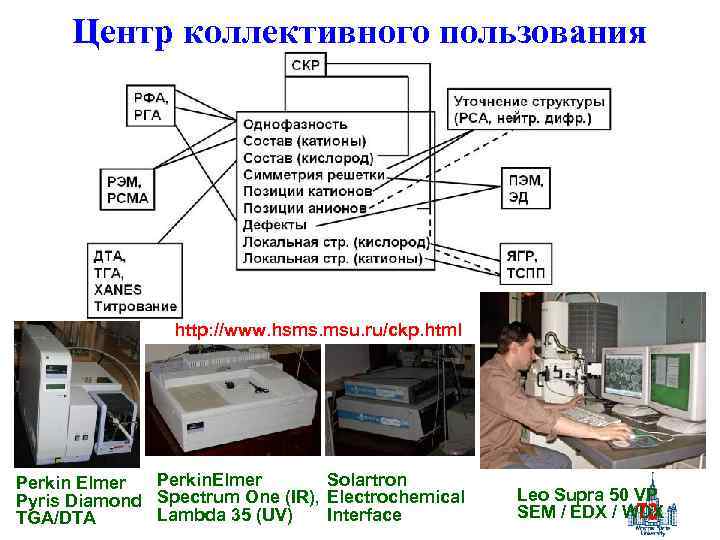 Центр коллективного пользования http: //www. hsms. msu. ru/ckp. html Perkin. Elmer Solartron Perkin Elmer Pyris Diamond Spectrum One (IR), Electrochemical Lambda 35 (UV) Interface TGA/DTA Leo Supra 50 VP SEM / EDX / WDX 72
Центр коллективного пользования http: //www. hsms. msu. ru/ckp. html Perkin. Elmer Solartron Perkin Elmer Pyris Diamond Spectrum One (IR), Electrochemical Lambda 35 (UV) Interface TGA/DTA Leo Supra 50 VP SEM / EDX / WDX 72
 Создание новых материалов 73
Создание новых материалов 73
 Основная литература 1. А. Вест. Химия твердого тела. М. : Мир, 1988, т. 1, 2. 2. Ю. Д. Третьяков, Х. Лепис. Химия и технология твердофазных материалов. М. : МГУ, 1985. 3. В. И. Фистуль. Физика и химия твердого тела, т. 1, 2. М. : Металлургия, 1995. 4. С. С. Горелик, М. Я. Дашевский. Материаловедение полупроводников и диэлектриков. М. : Металлургия, 1988. 5. В. И. Фистуль. Новые материалы. Состояние, проблемы, перспективы. М. : МИСИС, 1995. 6. Ч. Н. Р. Рао, Дж. Гополакришнан. Новые направления в химии твердого тела. Новосибирск: Наука, 1990. 7. Л. ван Флек. Теоретическое и прикладное материаловедение. М. : Атомиздат, 1975. 8. О. Уайэтт, Д. Дью-Хьюз, Металлы. Керамики. Полимеры. , М. : Атомиздат, 1979 9. У. Д. Кингери. Введение в керамику. М. : Изд-во лит-ры по строительству, 1967, 494 с. 74
Основная литература 1. А. Вест. Химия твердого тела. М. : Мир, 1988, т. 1, 2. 2. Ю. Д. Третьяков, Х. Лепис. Химия и технология твердофазных материалов. М. : МГУ, 1985. 3. В. И. Фистуль. Физика и химия твердого тела, т. 1, 2. М. : Металлургия, 1995. 4. С. С. Горелик, М. Я. Дашевский. Материаловедение полупроводников и диэлектриков. М. : Металлургия, 1988. 5. В. И. Фистуль. Новые материалы. Состояние, проблемы, перспективы. М. : МИСИС, 1995. 6. Ч. Н. Р. Рао, Дж. Гополакришнан. Новые направления в химии твердого тела. Новосибирск: Наука, 1990. 7. Л. ван Флек. Теоретическое и прикладное материаловедение. М. : Атомиздат, 1975. 8. О. Уайэтт, Д. Дью-Хьюз, Металлы. Керамики. Полимеры. , М. : Атомиздат, 1979 9. У. Д. Кингери. Введение в керамику. М. : Изд-во лит-ры по строительству, 1967, 494 с. 74
 Электронные источники http: //perst. isssph. kiae. ru/ (Перст – Перспективные Технологии) http: //www. rebco-effort. net/ (EFFORT) http: //www. materialstoday. com/home. htm (Materials Today!) http: //elibrary. ru/defaultx. asp, http: //lib. hsms. msu. ru/ (Электронная библиотека РФФИ и ФНМ) http: //www. superconductors. org/ (Популярные статьи по ВТСП) goodilin@inorg. chem. msu. ru (PDF – файлы) 75
Электронные источники http: //perst. isssph. kiae. ru/ (Перст – Перспективные Технологии) http: //www. rebco-effort. net/ (EFFORT) http: //www. materialstoday. com/home. htm (Materials Today!) http: //elibrary. ru/defaultx. asp, http: //lib. hsms. msu. ru/ (Электронная библиотека РФФИ и ФНМ) http: //www. superconductors. org/ (Популярные статьи по ВТСП) goodilin@inorg. chem. msu. ru (PDF – файлы) 75
 Анкета 1. Что такое материал (общее определение)? 2. Назовите химические соединения (1 -2 формулы), являющиеся типичными представителями: наноматериалов, катализаторов, стекол, диэлектриков, полупроводников, сверхпроводников, супериоников, магнитных и биоматериалов. 3. Какие науки вносят наибольший вклад в изучение материалов? 4. Какие существуют методы физико-химического исследования материалов? 76
Анкета 1. Что такое материал (общее определение)? 2. Назовите химические соединения (1 -2 формулы), являющиеся типичными представителями: наноматериалов, катализаторов, стекол, диэлектриков, полупроводников, сверхпроводников, супериоников, магнитных и биоматериалов. 3. Какие науки вносят наибольший вклад в изучение материалов? 4. Какие существуют методы физико-химического исследования материалов? 76
 «Реальная структура твердого тела» . Лекция 2. Метод апроксимации Броуэра. Лаборатория неорганического материаловедения, Химфак МГУ к. 548 goodilin@inorg. chem. msu. ru fmg. inorg. chem. msu. ru 939 -47 -29 Москва 2005 77
«Реальная структура твердого тела» . Лекция 2. Метод апроксимации Броуэра. Лаборатория неорганического материаловедения, Химфак МГУ к. 548 goodilin@inorg. chem. msu. ru fmg. inorg. chem. msu. ru 939 -47 -29 Москва 2005 77
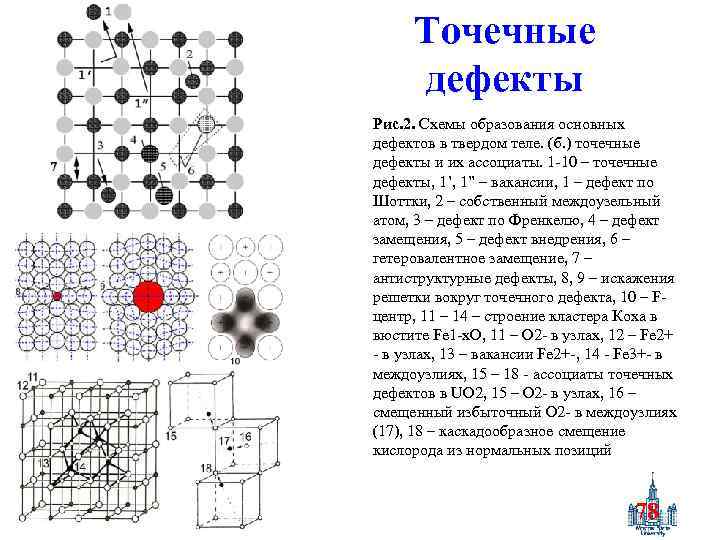 Точечные дефекты Рис. 2. Схемы образования основных дефектов в твердом теле. (б. ) точечные дефекты и их ассоциаты. 1 -10 – точечные дефекты, 1’, 1” – вакансии, 1 – дефект по Шоттки, 2 – собственный междоузельный атом, 3 – дефект по Френкелю, 4 – дефект замещения, 5 – дефект внедрения, 6 – гетеровалентное замещение, 7 – антиструктурные дефекты, 8, 9 – искажения решетки вокруг точечного дефекта, 10 – Fцентр, 11 – 14 – строение кластера Коха в вюстите Fe 1 -x. O, 11 – O 2 - в узлах, 12 – Fe 2+ - в узлах, 13 – вакансии Fe 2+-, 14 - Fe 3+- в междоузлиях, 15 – 18 - ассоциаты точечных дефектов в UO 2, 15 – O 2 - в узлах, 16 – смещенный избыточный O 2 - в междоузлиях (17), 18 – каскадообразное смещение кислорода из нормальных позиций 78
Точечные дефекты Рис. 2. Схемы образования основных дефектов в твердом теле. (б. ) точечные дефекты и их ассоциаты. 1 -10 – точечные дефекты, 1’, 1” – вакансии, 1 – дефект по Шоттки, 2 – собственный междоузельный атом, 3 – дефект по Френкелю, 4 – дефект замещения, 5 – дефект внедрения, 6 – гетеровалентное замещение, 7 – антиструктурные дефекты, 8, 9 – искажения решетки вокруг точечного дефекта, 10 – Fцентр, 11 – 14 – строение кластера Коха в вюстите Fe 1 -x. O, 11 – O 2 - в узлах, 12 – Fe 2+ - в узлах, 13 – вакансии Fe 2+-, 14 - Fe 3+- в междоузлиях, 15 – 18 - ассоциаты точечных дефектов в UO 2, 15 – O 2 - в узлах, 16 – смещенный избыточный O 2 - в междоузлиях (17), 18 – каскадообразное смещение кислорода из нормальных позиций 78
 Дефектность Идеальных кристаллов не существует. “Кристаллы как люди: именно несовершенства делают их интересными” (Colin Humphreys). Большинство свойств материалов определяются дефектами (частоискусственно введенными: полупроводники, суперионные проводники, ВТСП). 79
Дефектность Идеальных кристаллов не существует. “Кристаллы как люди: именно несовершенства делают их интересными” (Colin Humphreys). Большинство свойств материалов определяются дефектами (частоискусственно введенными: полупроводники, суперионные проводники, ВТСП). 79
 Квазихимические уравнения * закон сохранения массы, * закон сохранения (эффективного) заряда, * фиксированное соотношение между числом различных узлов решетки. 0 (стехиометрический кристалл) = Na (поверхность) + ½ Cl 2 (адс. ) + VNa’ + VCl , при поглощении кристаллами Na. Cl натрия образуются F-центры: 0 + Na(пар) = Na. Nax + VCl + e’ = Na. Nax + [VCl + e’]. La. F 3 = La. Cax + 2 FFx + Fix = La. Ca + 2 FFx + Fi’ (+Ca. F 2) 80
Квазихимические уравнения * закон сохранения массы, * закон сохранения (эффективного) заряда, * фиксированное соотношение между числом различных узлов решетки. 0 (стехиометрический кристалл) = Na (поверхность) + ½ Cl 2 (адс. ) + VNa’ + VCl , при поглощении кристаллами Na. Cl натрия образуются F-центры: 0 + Na(пар) = Na. Nax + VCl + e’ = Na. Nax + [VCl + e’]. La. F 3 = La. Cax + 2 FFx + Fix = La. Ca + 2 FFx + Fi’ (+Ca. F 2) 80
 81
81
 М. Планк (1911) показал, что энтропия идеального кристалла в состоянии равновесия стремится к нулю по мере приближения к абсолютному нулю температуры. Для реального кристалла при отличных от 0 К температурах происходит образование равновесных дефектов. Это термодинамически выгодный процесс, поскольку образование большинства дефектов невыгодно лишь энергетически, однако может быть выгодно с точки зрения общего уменьшения изобарно-изотермического потенциала системы из-за возрастания энтропии (Рис. 3. ). где G 0 – энергия Гиббса идеального кристалла, n g – потеря энергии при образовании n дефектов, Sc – конфигурационная энтропия при образовании дефектов, N – количество регулярных узлов образовании дефектов по Френкелю количество вариантов размещения дефектов и узлов составит по формуле Стирлинга 82
М. Планк (1911) показал, что энтропия идеального кристалла в состоянии равновесия стремится к нулю по мере приближения к абсолютному нулю температуры. Для реального кристалла при отличных от 0 К температурах происходит образование равновесных дефектов. Это термодинамически выгодный процесс, поскольку образование большинства дефектов невыгодно лишь энергетически, однако может быть выгодно с точки зрения общего уменьшения изобарно-изотермического потенциала системы из-за возрастания энтропии (Рис. 3. ). где G 0 – энергия Гиббса идеального кристалла, n g – потеря энергии при образовании n дефектов, Sc – конфигурационная энтропия при образовании дефектов, N – количество регулярных узлов образовании дефектов по Френкелю количество вариантов размещения дефектов и узлов составит по формуле Стирлинга 82
 83
83
 84
84
 85
85
 86
86
 Квазихимические приближения Прописная буква – тип дефекта: A, B, … – атомы, V – вакансия (h – дырка, e – электрон). Нижний индекс – в какой позиции находится дефект: AA – атом в регулярном узле, AB – атом в «чужой» подрешетке, Ai – атом в междоузлии, Vi – свободное междоузлие. Верхний индекс – (эффективный) заряд – заряд атомов или вакансий по отношению к нормальным составляющим решетки: x – нейтральный, - положительный, ‘ – отрицательный (количество надстрочных индексов соответствует величине заряда) Дефекты рассматриваются как квазичастицы, к которым применимы законы сохранения заряда, вещества и количества окружающих данную позицию «противо» узлов (образование вакансии катиона должно автоматически привести к эквивалентным изменениям в анионной подрешетке и наоборот). Дефекты Шоттки – вакансии (в катионной и анионной подрешктке), дефекты Френкеля – переход атома в междоузлие, антиструктурные дефекты – обмен эквивалентного атомов/ионов между подрешетками. 87
Квазихимические приближения Прописная буква – тип дефекта: A, B, … – атомы, V – вакансия (h – дырка, e – электрон). Нижний индекс – в какой позиции находится дефект: AA – атом в регулярном узле, AB – атом в «чужой» подрешетке, Ai – атом в междоузлии, Vi – свободное междоузлие. Верхний индекс – (эффективный) заряд – заряд атомов или вакансий по отношению к нормальным составляющим решетки: x – нейтральный, - положительный, ‘ – отрицательный (количество надстрочных индексов соответствует величине заряда) Дефекты рассматриваются как квазичастицы, к которым применимы законы сохранения заряда, вещества и количества окружающих данную позицию «противо» узлов (образование вакансии катиона должно автоматически привести к эквивалентным изменениям в анионной подрешетке и наоборот). Дефекты Шоттки – вакансии (в катионной и анионной подрешктке), дефекты Френкеля – переход атома в междоузлие, антиструктурные дефекты – обмен эквивалентного атомов/ионов между подрешетками. 87
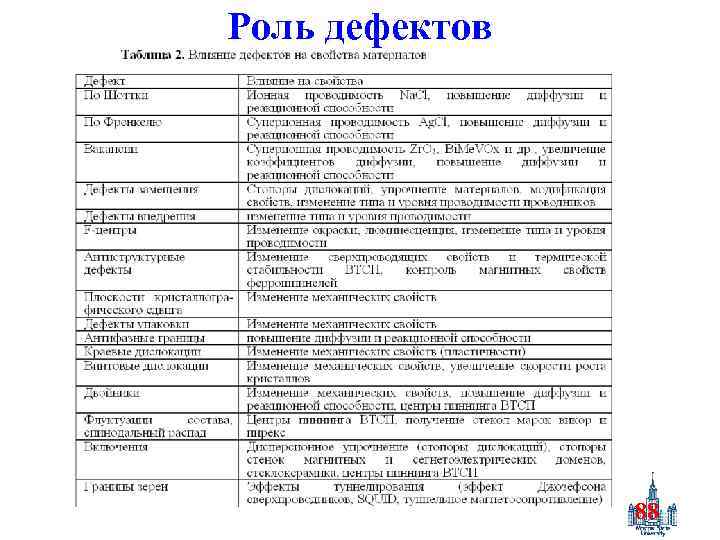 Роль дефектов 88
Роль дефектов 88
 Примеси 89
Примеси 89
 Законы Мерфи Следствия II з. т. : «чудес не бывает» «законы Мерфи» Закон Мэрфи Если какая-нибудь неприятность может произойти, она случается Следствия: 1. Из всех неприятностей произойдет именно та, ущерб от которой больше; 2. Предоставленные сами себе, события имеют тенденцию развиваться от плохого к худшему; 3. Если эксперимент удался, что-то здесь не так (первый закон Финэйгла) вероятность удачи < суммы вероятности неудач 90
Законы Мерфи Следствия II з. т. : «чудес не бывает» «законы Мерфи» Закон Мэрфи Если какая-нибудь неприятность может произойти, она случается Следствия: 1. Из всех неприятностей произойдет именно та, ущерб от которой больше; 2. Предоставленные сами себе, события имеют тенденцию развиваться от плохого к худшему; 3. Если эксперимент удался, что-то здесь не так (первый закон Финэйгла) вероятность удачи < суммы вероятности неудач 90
 Энтропия ( «вероятностное определение» ) Термодинамическая вероятность W состояния системы – это число способов, которыми может быть реализовано данное состояние макроскопической системы, или число микросостояний, осуществляющих данное макросостояние (W >> 1). Энтропия - мера статистического беспорядка в замкнутой термодинамической системе. Все самопроизвольно протекающие процессы в замкнутой системе, приближающие систему к состоянию равновесия и сопровождающиеся ростом энтропии, направлены в сторону увеличения вероятности состояния (Больцман). 91
Энтропия ( «вероятностное определение» ) Термодинамическая вероятность W состояния системы – это число способов, которыми может быть реализовано данное состояние макроскопической системы, или число микросостояний, осуществляющих данное макросостояние (W >> 1). Энтропия - мера статистического беспорядка в замкнутой термодинамической системе. Все самопроизвольно протекающие процессы в замкнутой системе, приближающие систему к состоянию равновесия и сопровождающиеся ростом энтропии, направлены в сторону увеличения вероятности состояния (Больцман). 91
 Вычисление энтропии S=kln. W, где k=1, 38· 10– 23 Дж/К (постоянная Больцмана) 1 моль газа, число N способов размещения молекулы по двум половинкам сосуда (микросостояний): 1/N 0 – молекулы только в одной половинке сосуда (одно из микросостояний). Наибольшее число микросостояний - молекулы равномерно распределены по всему объему. 92
Вычисление энтропии S=kln. W, где k=1, 38· 10– 23 Дж/К (постоянная Больцмана) 1 моль газа, число N способов размещения молекулы по двум половинкам сосуда (микросостояний): 1/N 0 – молекулы только в одной половинке сосуда (одно из микросостояний). Наибольшее число микросостояний - молекулы равномерно распределены по всему объему. 92
 Стратегия 93
Стратегия 93
 Правила 94
Правила 94
 Упрощения 95
Упрощения 95
 Реакция с газовой фазой 96
Реакция с газовой фазой 96
 Бинарный кристалл 97
Бинарный кристалл 97
 Комбинированные константы 98
Комбинированные константы 98
 Баланс зарядов 99
Баланс зарядов 99
 Алгоритм записи Тип кристалла: MX, MO 2, M 2 O и пр. Соотношение констант: Ki, KS, KF, KS’, KF’ и др. Участок: I, III, IV, V и др. Парциальное давление: низкое, среднее, высокое, … Квазихимическое уравнение: взаимодействие с газовой фазой Доминирующий тип дефекта: n, p, VX, VM, Mi, VX*, VM’, Mi*, … Уравнение электронейтральности: упрощение с учетом дом-го типа дефектов ----- Упрощенные уравнения концентраций дефектов для данного участка ----i- дефект: указание типа дефектов i-тангенс угла наклона: с учетом «+» или «-» , в логарифмических координатах Выводы о типах носителей заряда в зависимости от внешних условий 100
Алгоритм записи Тип кристалла: MX, MO 2, M 2 O и пр. Соотношение констант: Ki, KS, KF, KS’, KF’ и др. Участок: I, III, IV, V и др. Парциальное давление: низкое, среднее, высокое, … Квазихимическое уравнение: взаимодействие с газовой фазой Доминирующий тип дефекта: n, p, VX, VM, Mi, VX*, VM’, Mi*, … Уравнение электронейтральности: упрощение с учетом дом-го типа дефектов ----- Упрощенные уравнения концентраций дефектов для данного участка ----i- дефект: указание типа дефектов i-тангенс угла наклона: с учетом «+» или «-» , в логарифмических координатах Выводы о типах носителей заряда в зависимости от внешних условий 100
 Бинарный кристалл. Шоттки. 101
Бинарный кристалл. Шоттки. 101
 Соотношение констант 102
Соотношение констант 102
 Низкие р. X 2 (участок 1) 103
Низкие р. X 2 (участок 1) 103
 Аппроксимация 104
Аппроксимация 104
 Средние p. X 2 (участок 2) 105
Средние p. X 2 (участок 2) 105
 Высокие p. X 2 (участок 3) 106
Высокие p. X 2 (участок 3) 106
 Итоги n 107
Итоги n 107
 108
108
 Кристалл Mg. O 109
Кристалл Mg. O 109
 Взаимодействие с газовой фазой 110
Взаимодействие с газовой фазой 110
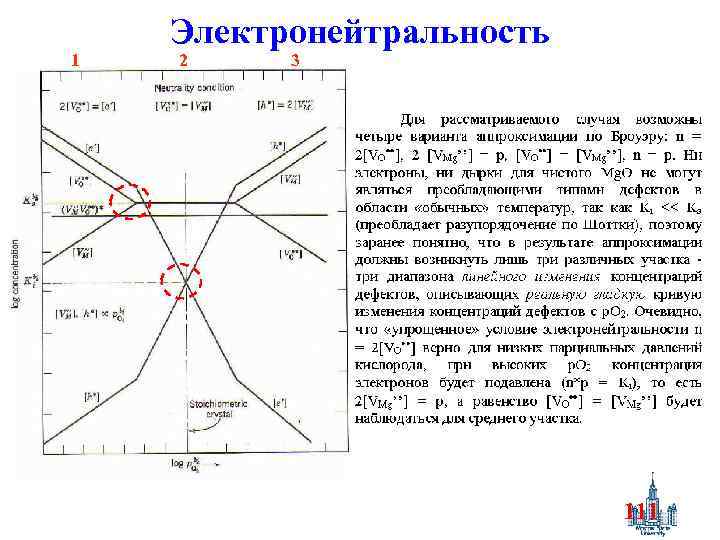 1 Электронейтральность 2 3 111
1 Электронейтральность 2 3 111
 Средний участок n: - ½ p: + ½ 112
Средний участок n: - ½ p: + ½ 112
![Восстановительная атмосфера n: - 1/3 [VO**]: - 1/3 [VMg’’]: + 1/3 p: + 1/3 Восстановительная атмосфера n: - 1/3 [VO**]: - 1/3 [VMg’’]: + 1/3 p: + 1/3](https://present5.com/presentation/3506544_176381504/image-113.jpg) Восстановительная атмосфера n: - 1/3 [VO**]: - 1/3 [VMg’’]: + 1/3 p: + 1/3 113
Восстановительная атмосфера n: - 1/3 [VO**]: - 1/3 [VMg’’]: + 1/3 p: + 1/3 113
![Окислительная атмосфера n: - 1/3 [VO**]: - 1/3 [VMg’’]: + 1/3 p: + 1/3 Окислительная атмосфера n: - 1/3 [VO**]: - 1/3 [VMg’’]: + 1/3 p: + 1/3](https://present5.com/presentation/3506544_176381504/image-114.jpg) Окислительная атмосфера n: - 1/3 [VO**]: - 1/3 [VMg’’]: + 1/3 p: + 1/3 114
Окислительная атмосфера n: - 1/3 [VO**]: - 1/3 [VMg’’]: + 1/3 p: + 1/3 114
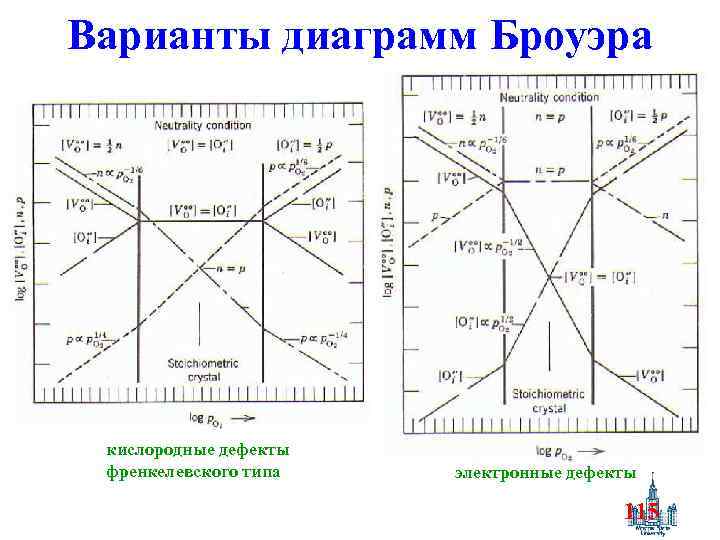 Варианты диаграмм Броуэра кислородные дефекты френкелевского типа электронные дефекты 115
Варианты диаграмм Броуэра кислородные дефекты френкелевского типа электронные дефекты 115
 116
116
![Кислородные сенсоры V = (RT/4 F) ln[{(PO 2(эталон)}/{(PO 2(образец)}] р. О 2 в анализируемой Кислородные сенсоры V = (RT/4 F) ln[{(PO 2(эталон)}/{(PO 2(образец)}] р. О 2 в анализируемой](https://present5.com/presentation/3506544_176381504/image-117.jpg) Кислородные сенсоры V = (RT/4 F) ln[{(PO 2(эталон)}/{(PO 2(образец)}] р. О 2 в анализируемой газовой атмосфере может быть определено из измеряемой э. д. с. по уравнению Нернста. Из-за низкой величины ионной проводимости диапазон рабочих температур может быть выше 650 ºC. 117
Кислородные сенсоры V = (RT/4 F) ln[{(PO 2(эталон)}/{(PO 2(образец)}] р. О 2 в анализируемой газовой атмосфере может быть определено из измеряемой э. д. с. по уравнению Нернста. Из-за низкой величины ионной проводимости диапазон рабочих температур может быть выше 650 ºC. 117
 Температурные диапазоны Легирование Zr. O 2 (Zr 1 -x. Yx. O 2 -x/2, Zr 1 -x. Cax. O 2 -x): -Рост концентрации анионных вакансий (низковалентный катион) -Стабилизация кубической модификации (крупные катионы) Возможно также замещение Zr на катион с большим ионным радиусом (Ce 4+) для стабилизации кубической структуры, или более низковалентным катионом (Bi 3+) для увеличения концентрации вакансий. Ca. O(Zr. O 2) = Ca. Zr’’ + Vo + Oox 15 мол. % Ca. O ti = i/( i + e + h) O=e’ + h (n~p. O 21/4) При низких р. О 2 O = 0. 5 O 2 + Vo + 2 e’ (n~p. O 2 -1/4) ti >0. 99, если lg(p. O 2(Па)) > -60500/T + 18. 5 118
Температурные диапазоны Легирование Zr. O 2 (Zr 1 -x. Yx. O 2 -x/2, Zr 1 -x. Cax. O 2 -x): -Рост концентрации анионных вакансий (низковалентный катион) -Стабилизация кубической модификации (крупные катионы) Возможно также замещение Zr на катион с большим ионным радиусом (Ce 4+) для стабилизации кубической структуры, или более низковалентным катионом (Bi 3+) для увеличения концентрации вакансий. Ca. O(Zr. O 2) = Ca. Zr’’ + Vo + Oox 15 мол. % Ca. O ti = i/( i + e + h) O=e’ + h (n~p. O 21/4) При низких р. О 2 O = 0. 5 O 2 + Vo + 2 e’ (n~p. O 2 -1/4) ti >0. 99, если lg(p. O 2(Па)) > -60500/T + 18. 5 118
 Анкета 1. 2. 3. 4. 5. Что такое материал (общее определение)? В чем разница между функциональными, конструкционными и интеллектуальными материалами? Назовите химические соединения (1 -2 формулы), являющиеся типичными представителями: наноматериалов, катализаторов, полупроводников, сверхпроводников, супериоников, магнитных и биоматериалов. Какие науки вносят наибольший вклад в изучение материалов? Какие существуют методы физико-химического исследования материалов? 119
Анкета 1. 2. 3. 4. 5. Что такое материал (общее определение)? В чем разница между функциональными, конструкционными и интеллектуальными материалами? Назовите химические соединения (1 -2 формулы), являющиеся типичными представителями: наноматериалов, катализаторов, полупроводников, сверхпроводников, супериоников, магнитных и биоматериалов. Какие науки вносят наибольший вклад в изучение материалов? Какие существуют методы физико-химического исследования материалов? 119
 120
120


