 РЕАКЦІЯ МІХАЕЛЯ Сучасні методи органічного синтезу
РЕАКЦІЯ МІХАЕЛЯ Сучасні методи органічного синтезу
 Реакція Міхаеля 2
Реакція Міхаеля 2
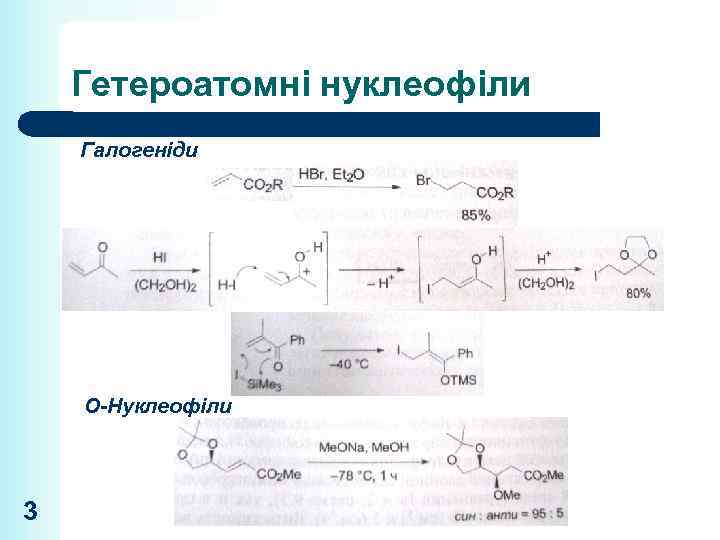 Гетероатомні нуклеофіли Галогеніди О-Нуклеофіли 3
Гетероатомні нуклеофіли Галогеніди О-Нуклеофіли 3
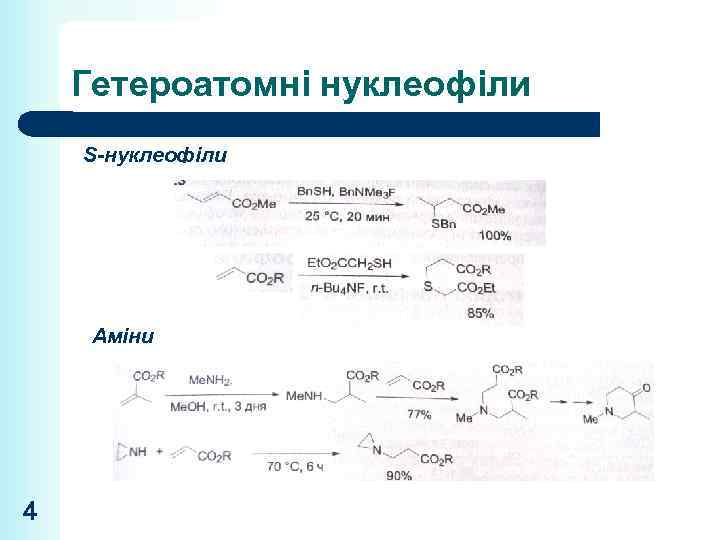 Гетероатомні нуклеофіли S-нуклеофіли Аміни 4
Гетероатомні нуклеофіли S-нуклеофіли Аміни 4
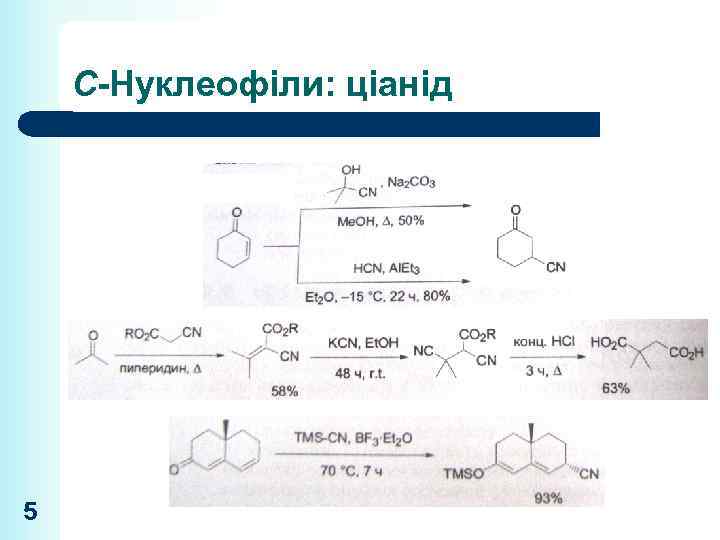 С-Нуклеофіли: ціанід 5
С-Нуклеофіли: ціанід 5
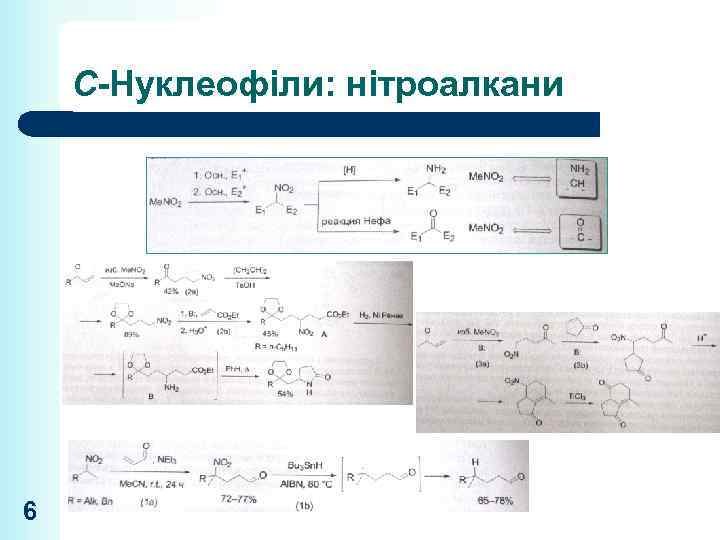 С-Нуклеофіли: нітроалкани 6
С-Нуклеофіли: нітроалкани 6
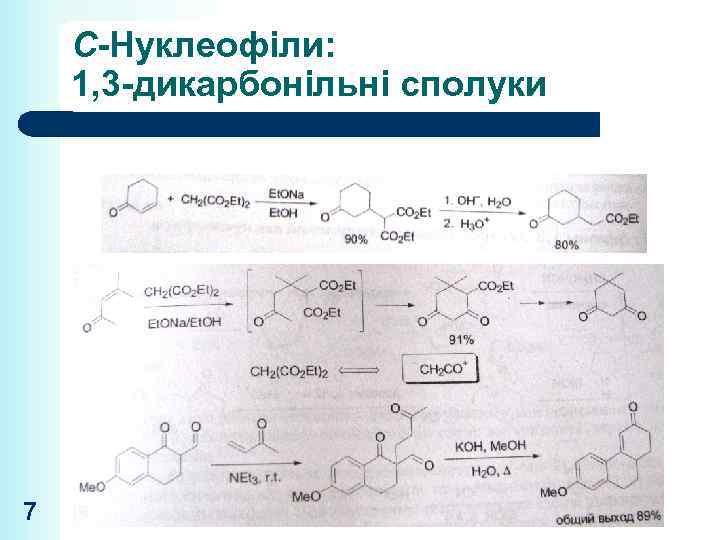 С-Нуклеофіли: 1, 3 -дикарбонільні сполуки 7
С-Нуклеофіли: 1, 3 -дикарбонільні сполуки 7
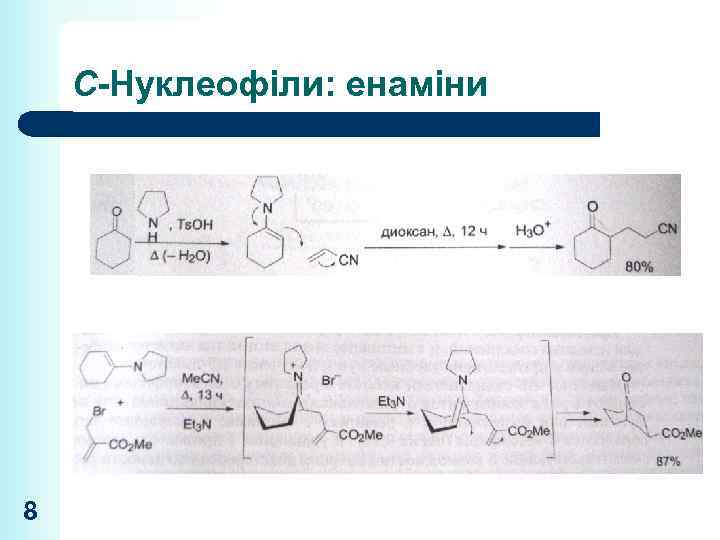 С-Нуклеофіли: енаміни 8
С-Нуклеофіли: енаміни 8
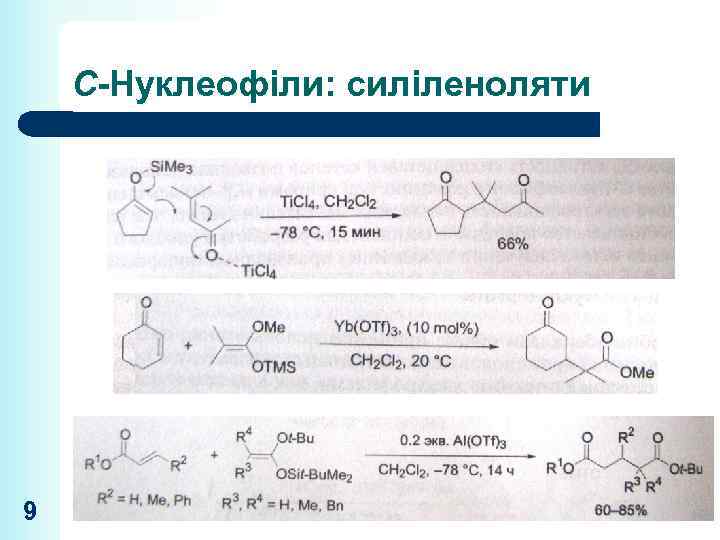 С-Нуклеофіли: силіленоляти 9
С-Нуклеофіли: силіленоляти 9
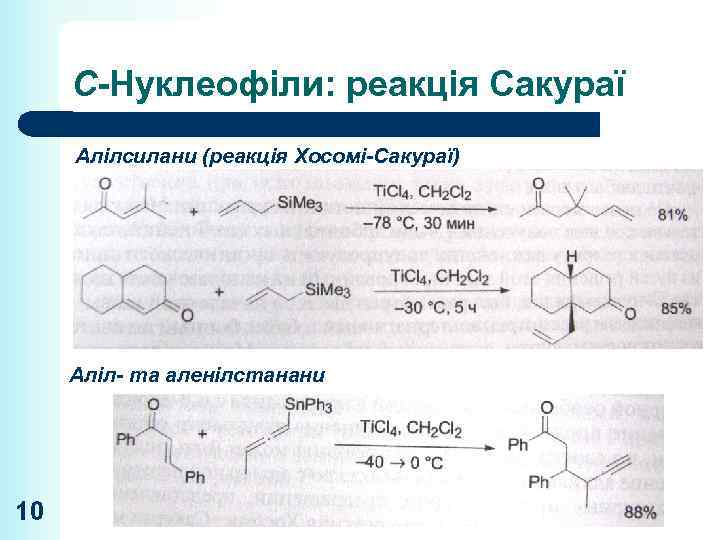 С-Нуклеофіли: реакція Сакураї Алілсилани (реакція Хосомі-Сакураї) Аліл- та аленілстанани 10
С-Нуклеофіли: реакція Сакураї Алілсилани (реакція Хосомі-Сакураї) Аліл- та аленілстанани 10
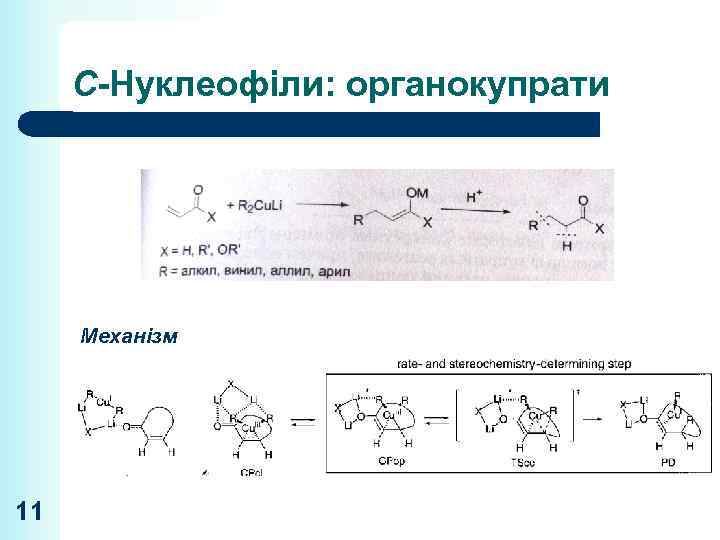 С-Нуклеофіли: органокупрати Механізм 11
С-Нуклеофіли: органокупрати Механізм 11
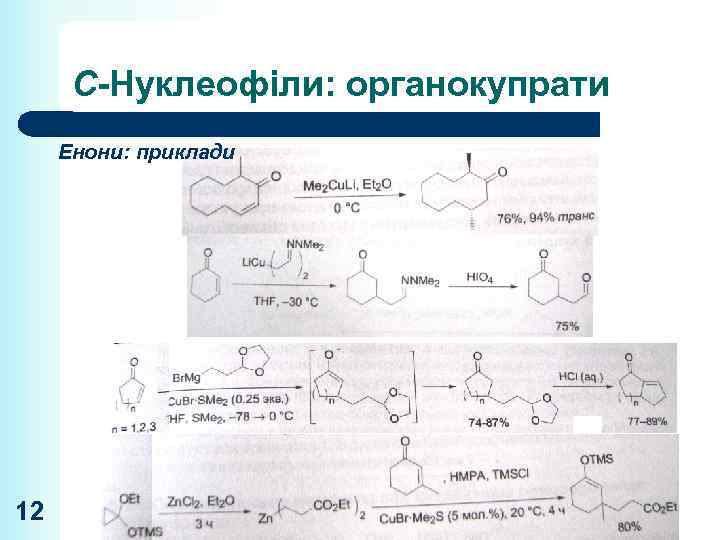 С-Нуклеофіли: органокупрати Енони: приклади 12
С-Нуклеофіли: органокупрати Енони: приклади 12
 С-Нуклеофіли: органокупрати Енони: приєдання-елімінування 13
С-Нуклеофіли: органокупрати Енони: приєдання-елімінування 13
 С-Нуклеофіли: органокупрати Силани як активатори Похідні , -ненасичених кислот 14
С-Нуклеофіли: органокупрати Силани як активатори Похідні , -ненасичених кислот 14
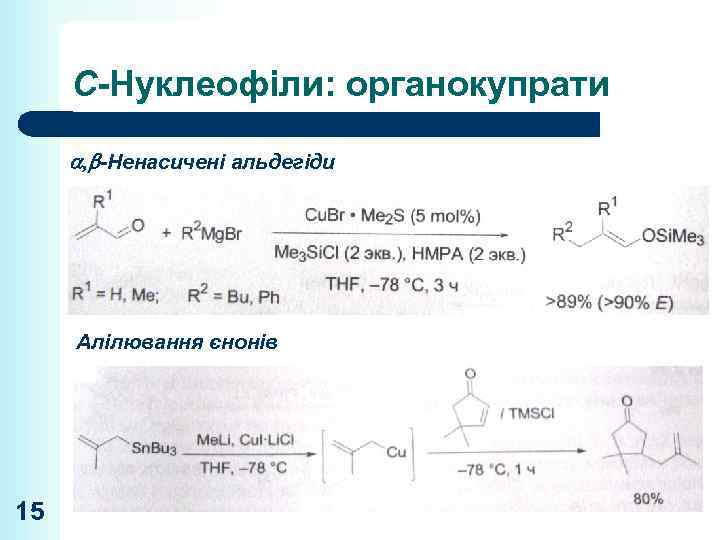 С-Нуклеофіли: органокупрати , -Ненасичені альдегіди Алілювання єнонів 15
С-Нуклеофіли: органокупрати , -Ненасичені альдегіди Алілювання єнонів 15
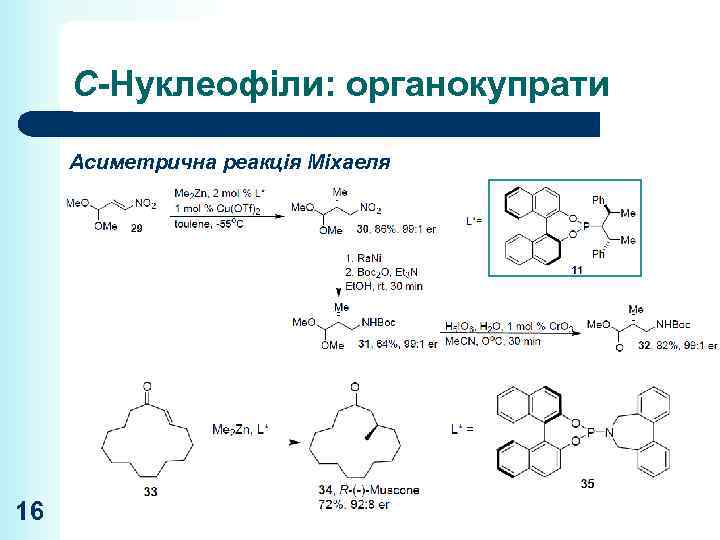 С-Нуклеофіли: органокупрати Асиметрична реакція Міхаеля 16
С-Нуклеофіли: органокупрати Асиметрична реакція Міхаеля 16
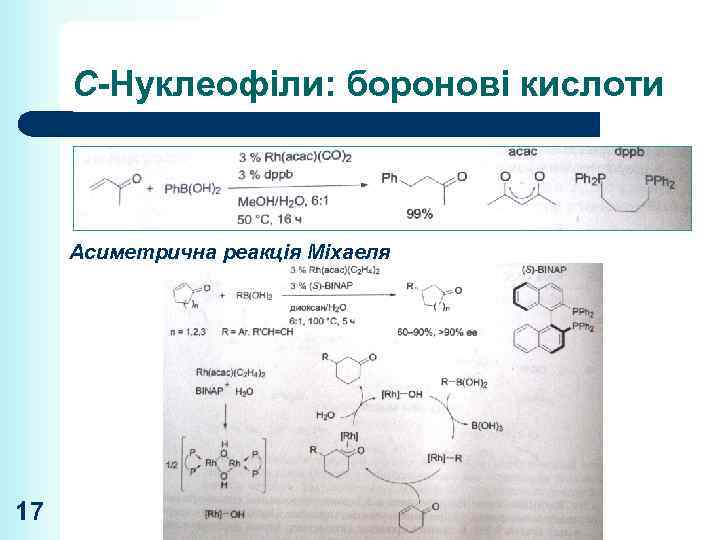 С-Нуклеофіли: боронові кислоти Асиметрична реакція Міхаеля 17
С-Нуклеофіли: боронові кислоти Асиметрична реакція Міхаеля 17
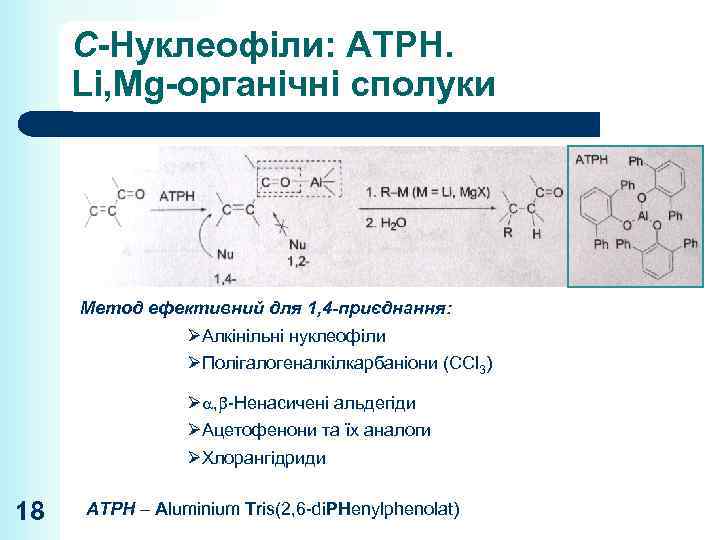 C-Нуклеофіли: ATPH. Li, Mg-органічні сполуки Метод ефективний для 1, 4 -приєднання: ØАлкінільні нуклеофіли ØПолігалогеналкілкарбаніони (CCl 3) Ø , -Ненасичені альдегіди ØАцетофенони та їх аналоги ØХлорангідриди 18 ATPH – Aluminium Tris(2, 6 -di. PНenylphenolat)
C-Нуклеофіли: ATPH. Li, Mg-органічні сполуки Метод ефективний для 1, 4 -приєднання: ØАлкінільні нуклеофіли ØПолігалогеналкілкарбаніони (CCl 3) Ø , -Ненасичені альдегіди ØАцетофенони та їх аналоги ØХлорангідриди 18 ATPH – Aluminium Tris(2, 6 -di. PНenylphenolat)
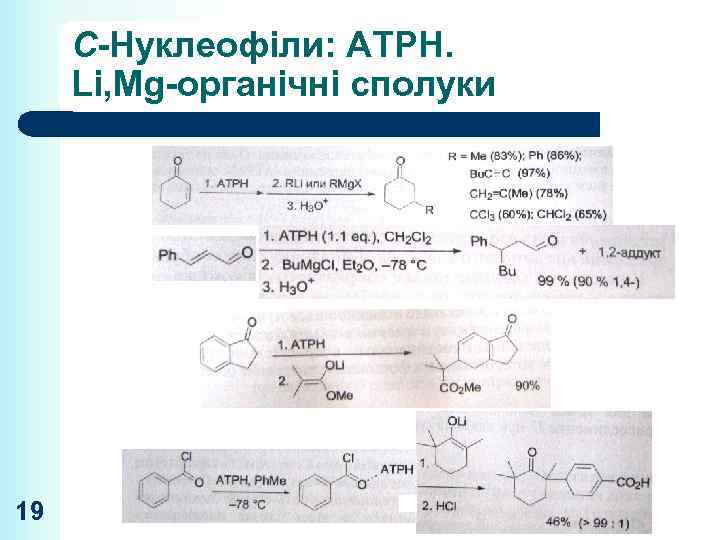 C-Нуклеофіли: ATPH. Li, Mg-органічні сполуки 19
C-Нуклеофіли: ATPH. Li, Mg-органічні сполуки 19
 Тандем приєднання алкілювання 20
Тандем приєднання алкілювання 20
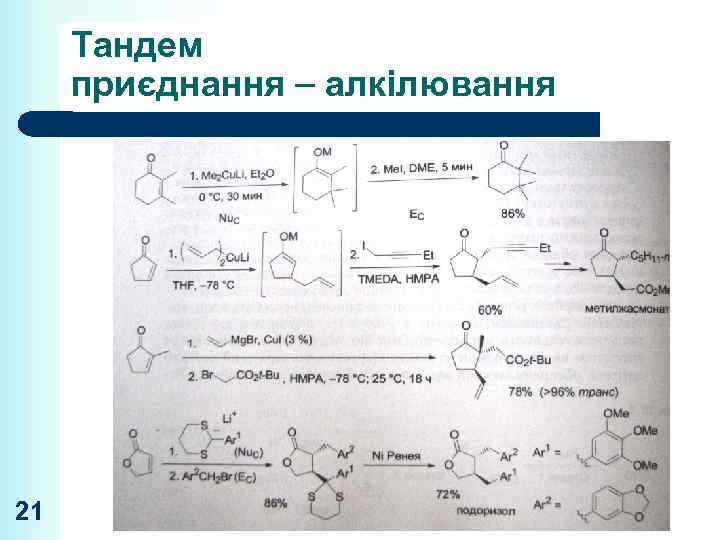 Тандем приєднання алкілювання 21
Тандем приєднання алкілювання 21
 Реакція Бейліса–Хілмана 22
Реакція Бейліса–Хілмана 22
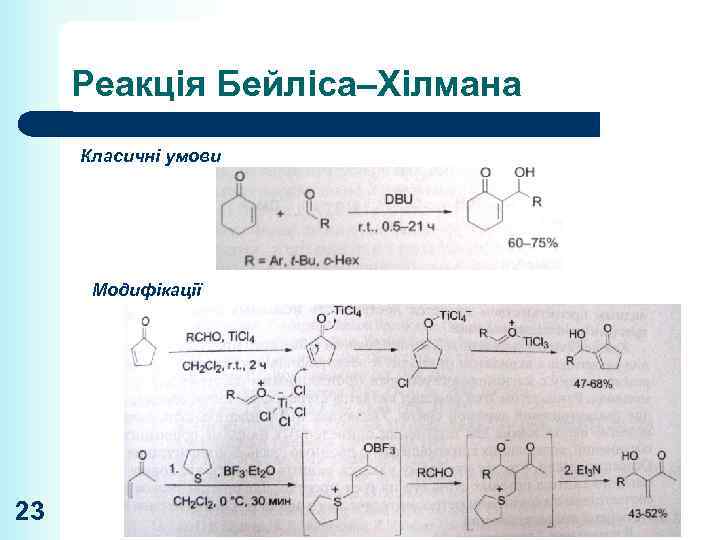 Реакція Бейліса–Хілмана Класичні умови Модифікації 23
Реакція Бейліса–Хілмана Класичні умови Модифікації 23
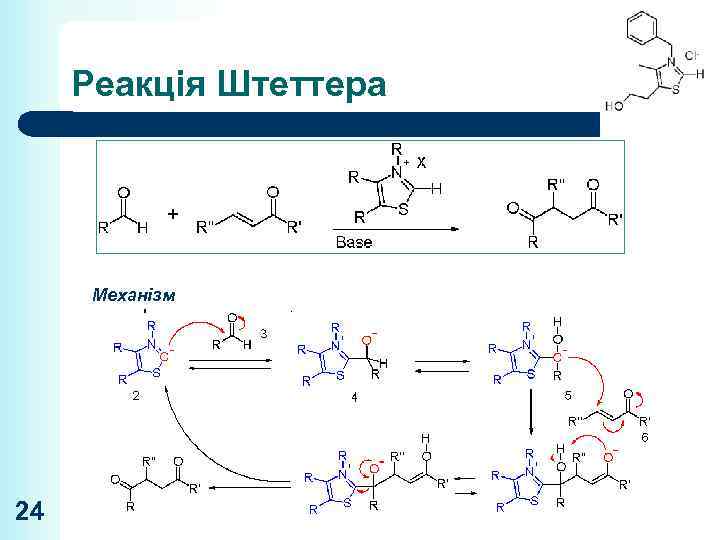 Реакція Штеттера Механізм 24
Реакція Штеттера Механізм 24