РЕАКЦИОННАЯ СПОСОБНОСТЬ УГЛЕВОДОРОДОВ.ppt
- Количество слайдов: 31

РЕАКЦИОННАЯ СПОСОБНОСТЬ УГЛЕВОДОРОДОВ Реакционная способность - способность вещества вступать в химическую реакцию и реагировать с определенной скоростью. Субстрат – вещество, которое подвергается воздействию. Содержит атом углерода, у которого происходит разрыв старой связи и образование новой. Реагент – вещество, действующее на субстрат.
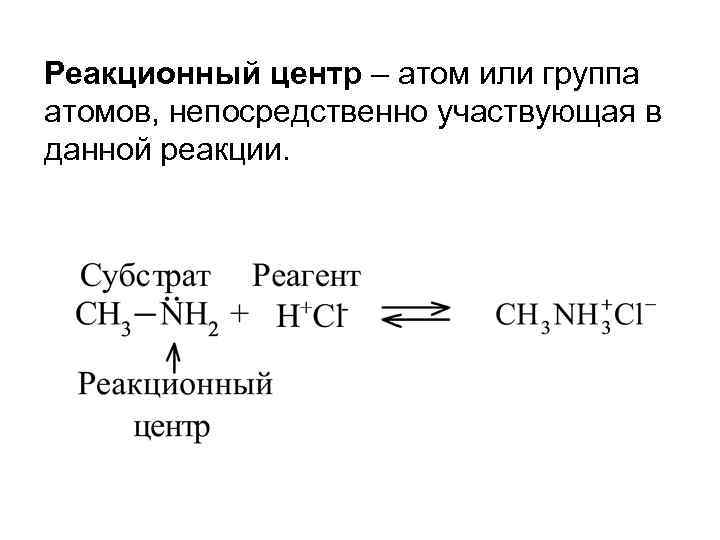
Реакционный центр – атом или группа атомов, непосредственно участвующая в данной реакции.

Классификация реакций По конечному результату Замещение – substitution (S) A–B + C → A–C + B - Замещение радикальное SR (алканы, циклоалканы) - Замещение электрофильное SE (ароматические соединения) - Замещение нуклеофильное SN (спирты, карбоновые кислоты)

Присоединение – addition (A) - Присоединение электрофильное AE (непредельные углеводороды) - Присоединение нуклеофильное AN (альдегиды и кетоны)
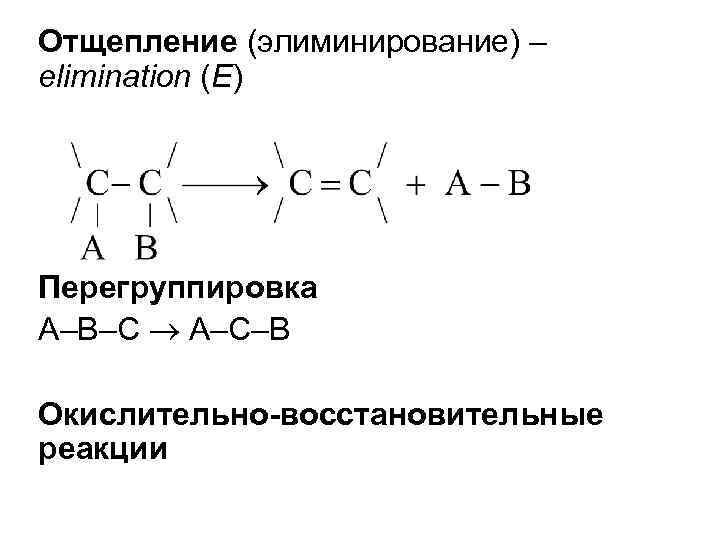
Отщепление (элиминирование) – elimination (E) Перегруппировка A–B–C A–C–B Окислительно-восстановительные реакции

По механизму разрыва связей в субстрате и реагенте Радикальные – radical (R) – гомолитические В этих реакциях действуют радикалы – свободные атомы или частицы с неспаренным электроном, которые образуются при гомолитическом разрыве связи под действием света (фотолизе), (пиролизе), при крекинге, в окислительно-восстановительных реакциях.

Ионные – гетеролитические. В этих реакциях участвуют ионы, которые образуются при гетеролитическом разрыве связи:

Электрофил (E+) – положительная частица имеет свободные орбитали (H+, Br+, NO 2+, R 3 C+). Нуклеофил (N–) – отрицательная частица содержит неподеленную пару электронов на внешнем уровне или pэлектроны кратной связи ( H–, Cl–, CH 2=CH 2, ).

Нуклеофильные AN – присоединение нуклеофильное (альдегиды, кетоны); SN – замещение нуклеофильное (спирты, карбоновые кислоты). Электрофильные AE – присоединение электрофильное (непредельные углеводороды); SE – замещение электрофильное (ароматические углеводороды).

Реакции радикального замещения SR Характерны для алканов и циклоалканов, имеющих неполярные σ-связи и атомы углерода в sp 3 -гибридизации. Галогенирование предельных углеводородов. хлорметан

Механизм реакции включает следующие стадии: I. Инициирование – образование свободных радикалов
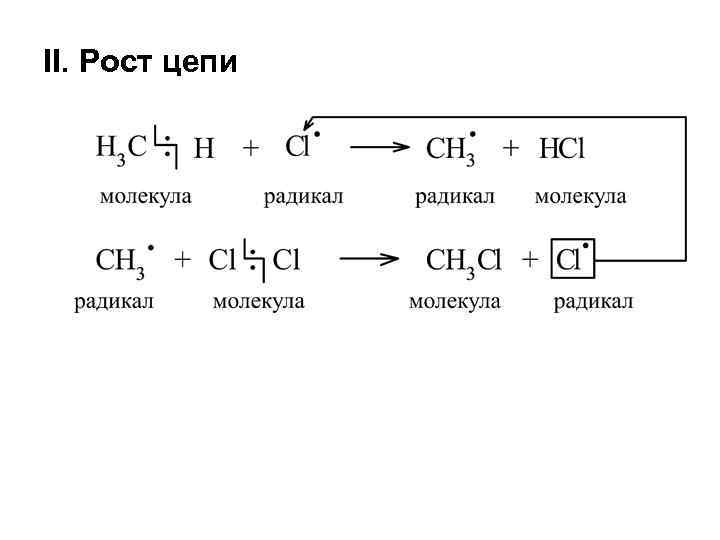
II. Рост цепи
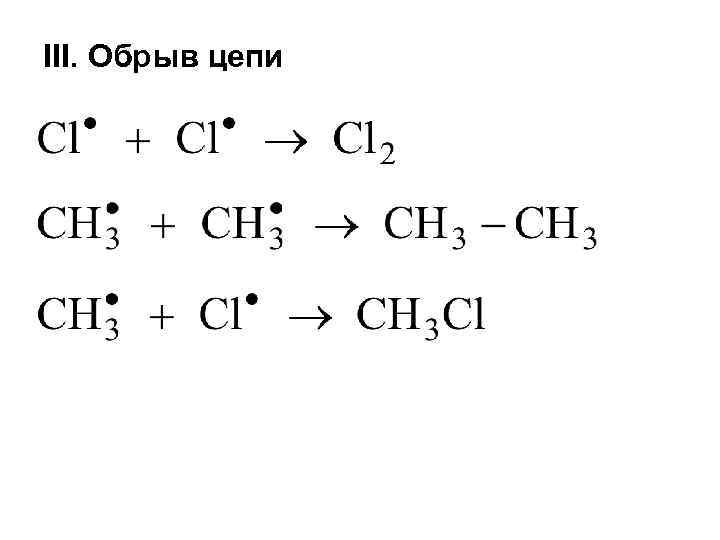
III. Обрыв цепи
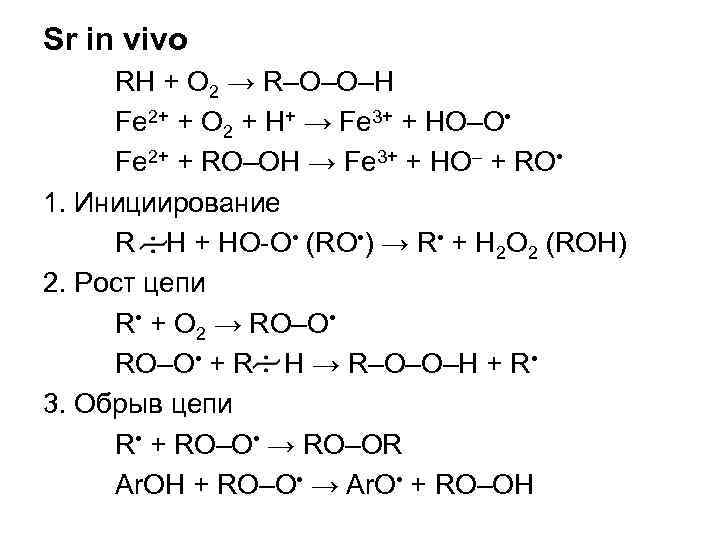
Sr in vivo RH + O 2 → R–O–O–H Fe 2+ + O 2 + H+ → Fe 3+ + HO–O • Fe 2+ + RO–OH → Fe 3+ + HO– + RO • 1. Инициирование R H + HO-O • (RO • ) → R • + H 2 O 2 (ROH) 2. Рост цепи R • + O 2 → RO–O • + R H → R–O–O–H + R • 3. Обрыв цепи R • + RO–O • → RO–OR Ar. OH + RO–O • → Ar. O • + RO–OH

Реакции электрофильного присоединения AE Реакции присоединения характерны для ненасыщенных углеводородов, имеющих двойные или тройные связи. Наиболее важной in vivo (в организме) является двойная связь. За счет электронов p-связи в молекулах алкенов имеется область повышенной электронной плотности, т. е. нуклеофильный центр, который может подвергаться атаке электрофильным реагентом. Поэтому реакции присоединения к алкенам протекают по механизму AE.
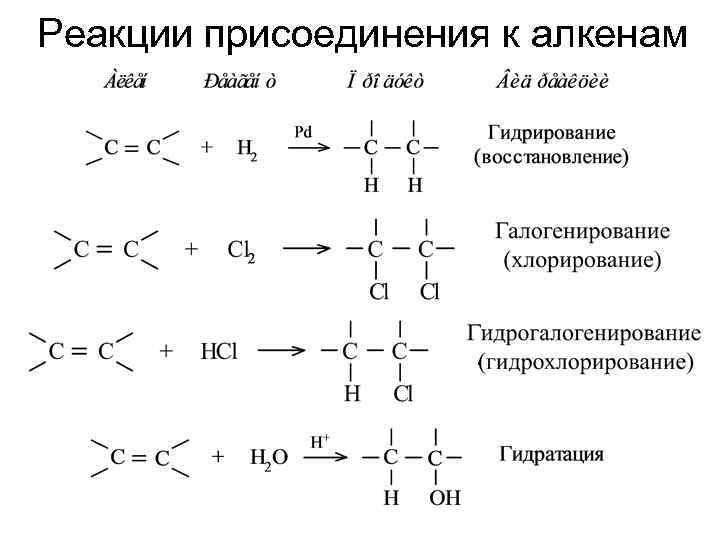
Реакции присоединения к алкенам
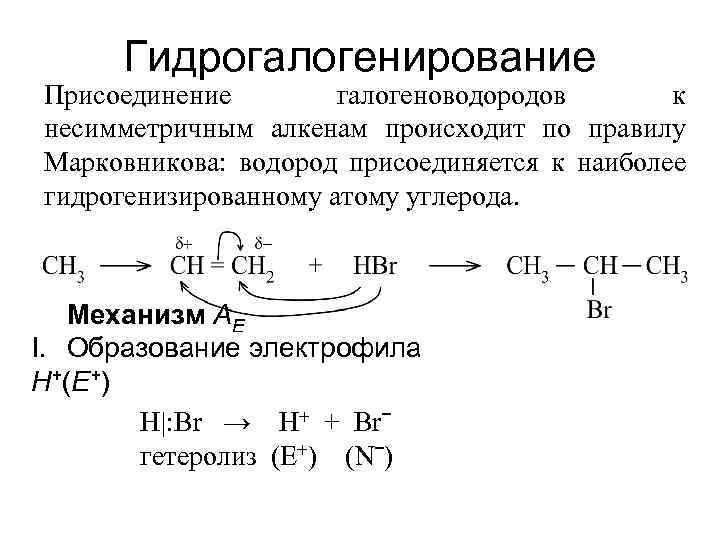
Гидрогалогенирование Присоединение галогеноводородов к несимметричным алкенам происходит по правилу Марковникова: водород присоединяется к наиболее гидрогенизированному атому углерода. Механизм AE I. Образование электрофила H+(E+) H|: Br → H+ + Brˉ гетеролиз (E+) (Nˉ)

II. Образование p-комплекса p - комплекс III. Образование s-комплекса (карбокатиона) s-комплекс IV. Образование продукта 2 -бромпропан
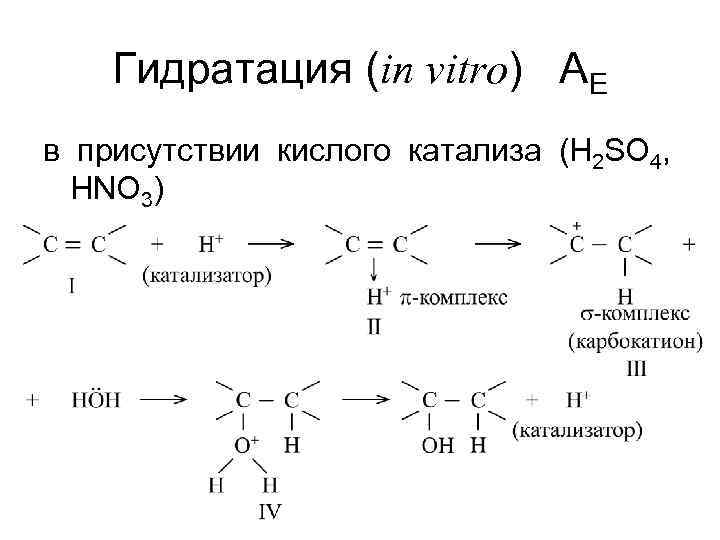
Гидратация (in vitro) AE в присутствии кислого катализа (H 2 SO 4, HNO 3)
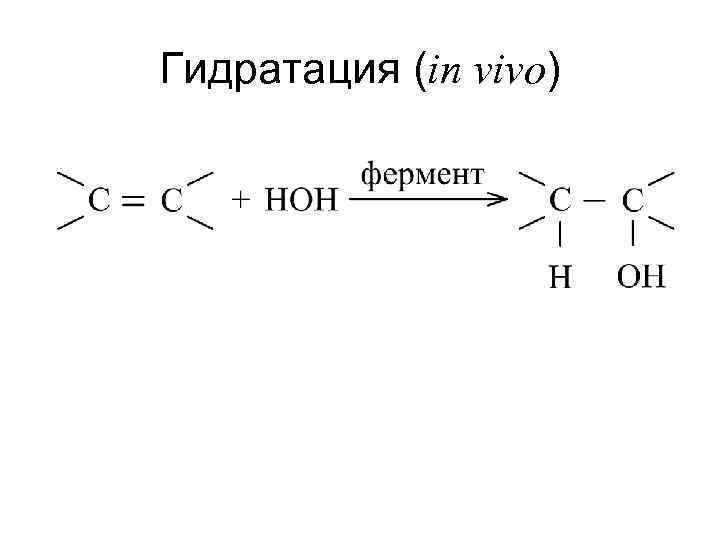
Гидратация (in vivo)

Присоединение к диеновым углеводородам В зависимости от условий возможны продукты 1 -2 и 1 -4 присоединения
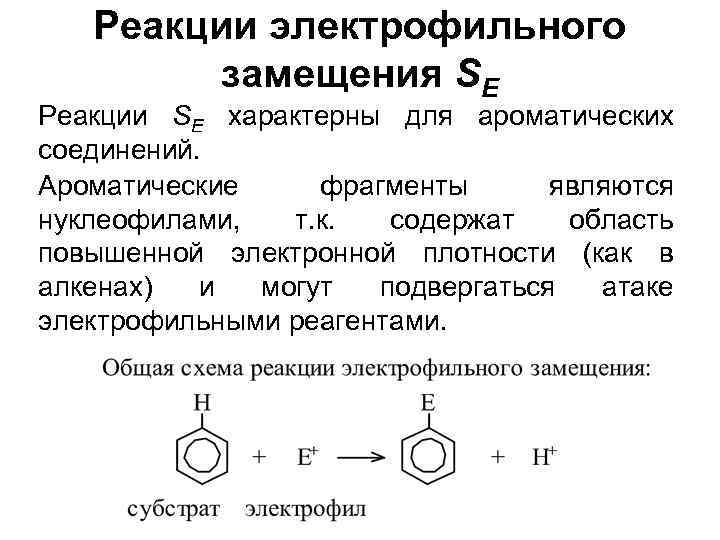
Реакции электрофильного замещения SE Реакции SE характерны для ароматических соединений. Ароматические фрагменты являются нуклеофилами, т. к. содержат область повышенной электронной плотности (как в алкенах) и могут подвергаться атаке электрофильными реагентами.

Механизм реакции SE I. Образование электрофильной частицы (E+) за счет поляризации связи в реагенте под действием катализатора. II. Образование p – комплекса. Электрофил образует нестойкий p-комплекс со всеми pэлектронами ароматической системы.
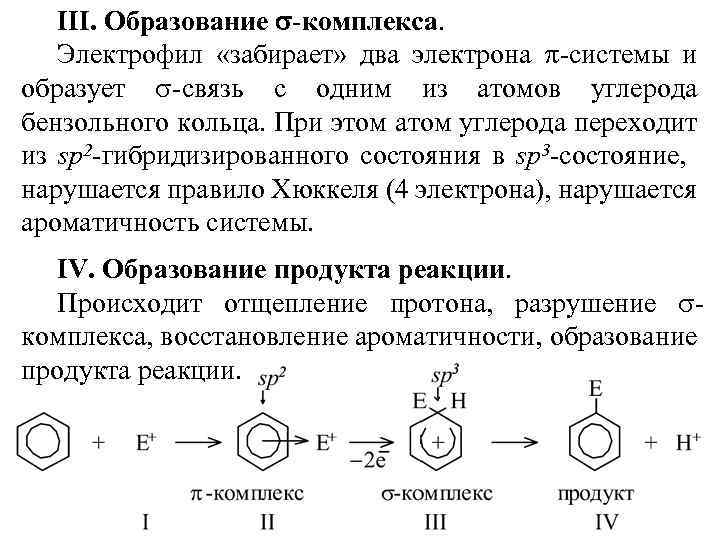
III. Образование s-комплекса. Электрофил «забирает» два электрона p-системы и образует s-связь с одним из атомов углерода бензольного кольца. При этом атом углерода переходит из sp 2 -гибридизированного состояния в sp 3 -состояние, нарушается правило Хюккеля (4 электрона), нарушается ароматичность системы. IV. Образование продукта реакции. Происходит отщепление протона, разрушение sкомплекса, восстановление ароматичности, образование продукта реакции.
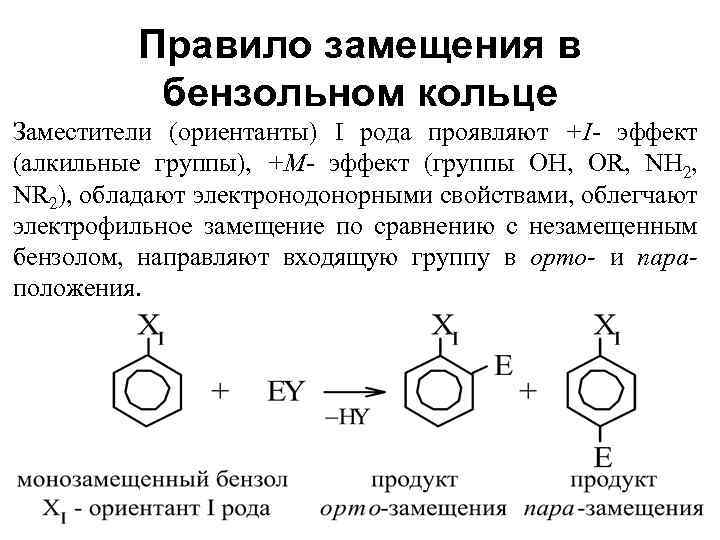
Правило замещения в бензольном кольце Заместители (ориентанты) I рода проявляют +I- эффект (алкильные группы), +М- эффект (группы OH, OR, NH 2, NR 2), обладают электронодонорными свойствами, облегчают электрофильное замещение по сравнению с незамещенным бензолом, направляют входящую группу в орто- и параположения.
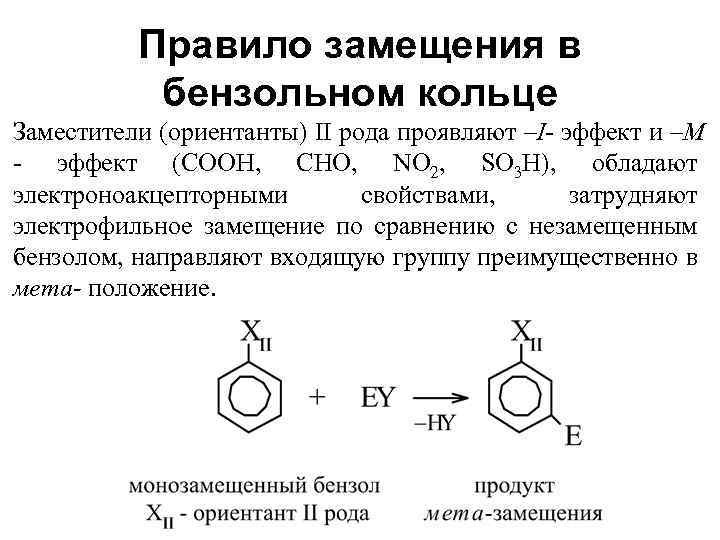
Правило замещения в бензольном кольце Заместители (ориентанты) II рода проявляют –I- эффект и –М - эффект (COOH, CHO, NO 2, SO 3 H), обладают электроноакцепторными свойствами, затрудняют электрофильное замещение по сравнению с незамещенным бензолом, направляют входящую группу преимущественно в мета- положение.
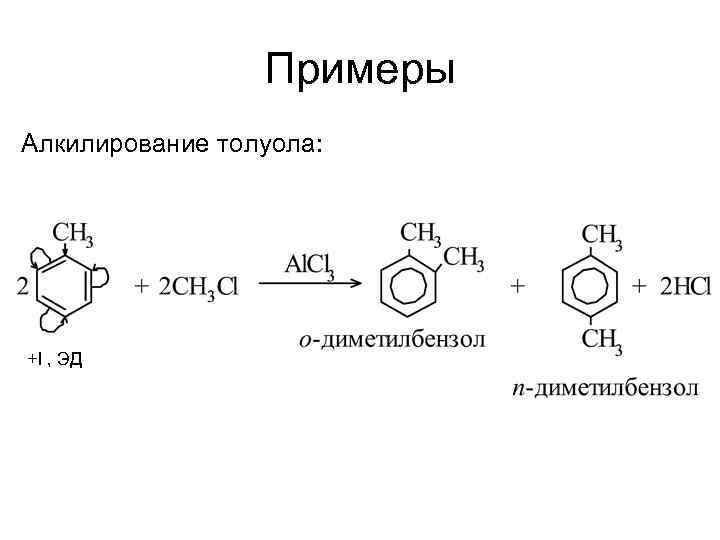
Примеры Алкилирование толуола: +I , ЭД
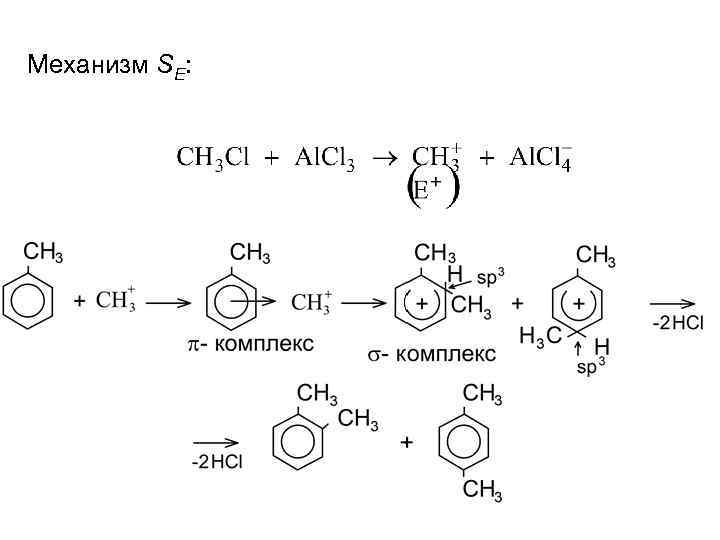
Механизм SE:
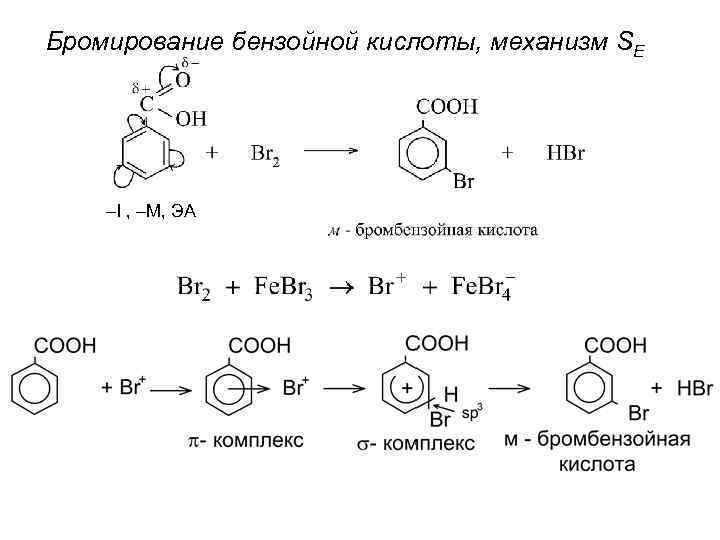
Бромирование бензойной кислоты, механизм SE –I , –М, ЭА
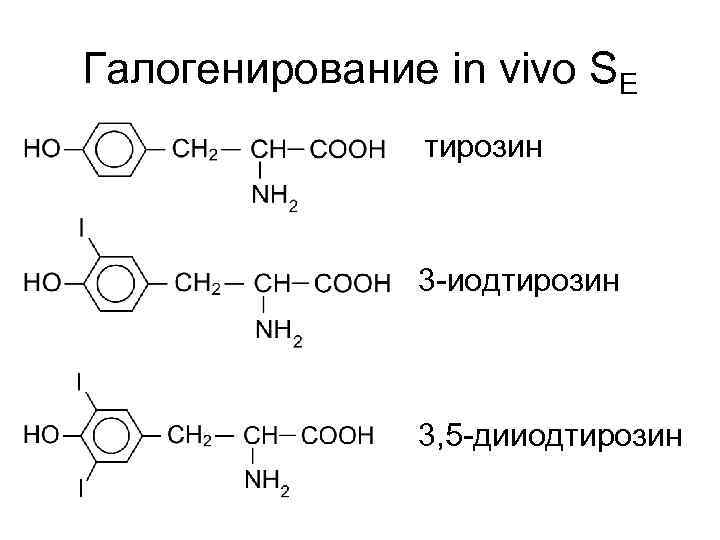
Галогенирование in vivo SE тирозин 3 -иодтирозин 3, 5 -дииодтирозин
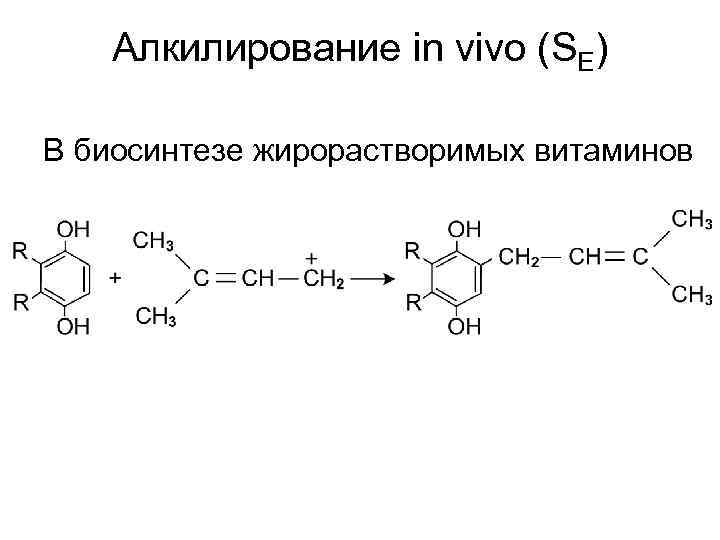
Алкилирование in vivo (SE) В биосинтезе жирорастворимых витаминов
РЕАКЦИОННАЯ СПОСОБНОСТЬ УГЛЕВОДОРОДОВ.ppt