Alken-2012.ppt
- Количество слайдов: 94

РЕАКЦИОННАЯ СПОСОБНОСТЬ УГЛЕВОДОРОДОВ (АЛКЕНЫ) 1

Сn. Н 2 n Алкены - ненасыщенные углеводороды, молекулы которых содержат одну двойную связь олефины этиленовые углеводороды
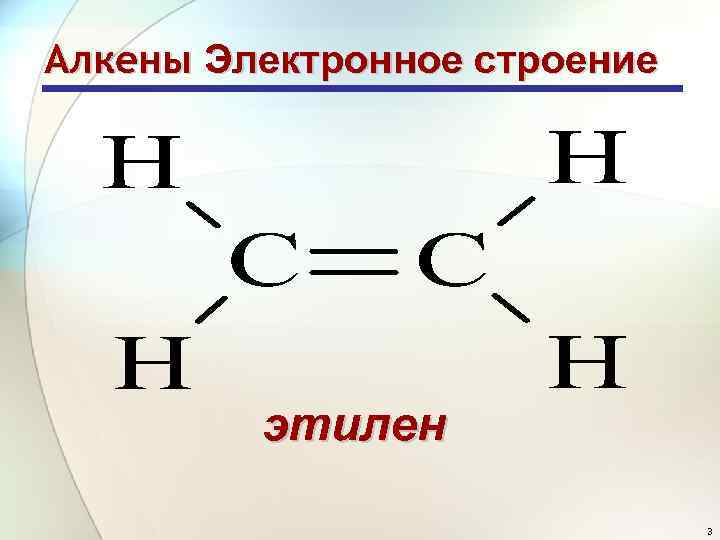
Алкены Электронное строение этилен 3
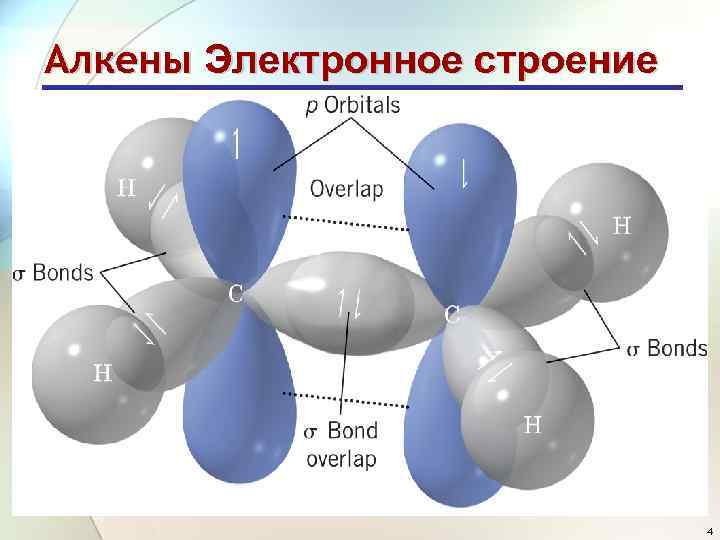
Алкены Электронное строение 4

Алкены Номенклатура • Нумерацию цепи производят с того конца, ближе к которому находится двойная связь • В названии алкана, соответствующего этой родоначальной структуре, суффикс -ан заменяется на –ен этилен пропилен гексен-2 5
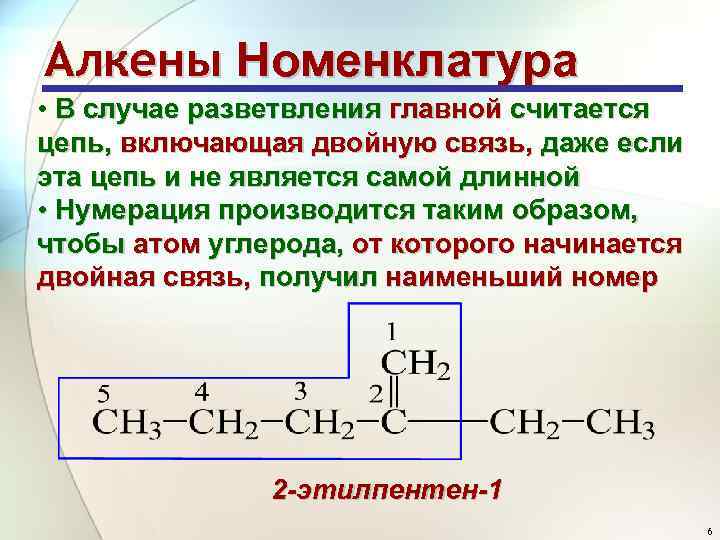
Алкены Номенклатура • В случае разветвления главной считается цепь, включающая двойную связь, даже если эта цепь и не является самой длинной • Нумерация производится таким образом, чтобы атом углерода, от которого начинается двойная связь, получил наименьший номер 2 -этилпентен-1 6

Алкены Номенклатура • Углеводородные заместители обозначаются префиксом • Заместители перечисляются в алфавитном порядке 2 -метилбутен-2 7

Алкены Номенклатура • В случае нескольких одинаковых углеводородных заместителей перед их названием ставится умножительная приставка ди-, три- и т. д. 2 -метилбутен-2 8

Алкены Номенклатура 2, 5 -диметилгексен-2 изобутилен 9

Алкены Номенклатура • Углеводородные радикалы, образованные от алкенов, получают суффикс –енил 10

Алкены Номенклатура • Для простейших аллильных радикалов вместо систематических названий разрешается использовать тривиальные: винил (этенил) 11
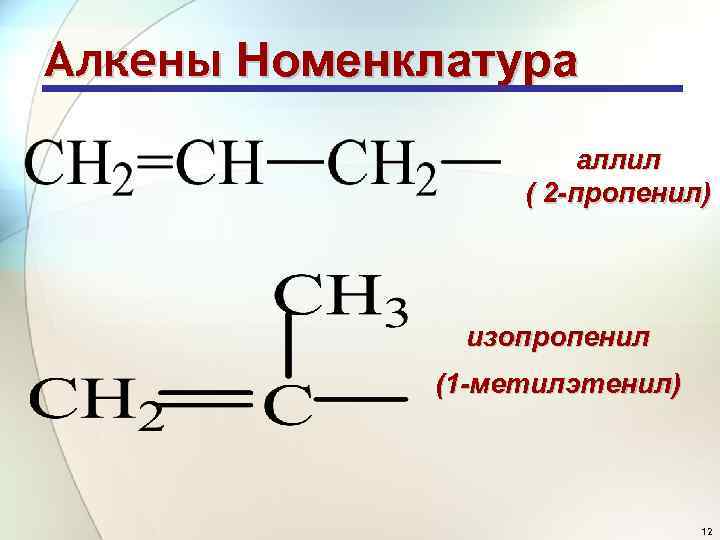
Алкены Номенклатура аллил ( 2 -пропенил) изопропенил (1 -метилэтенил) 12
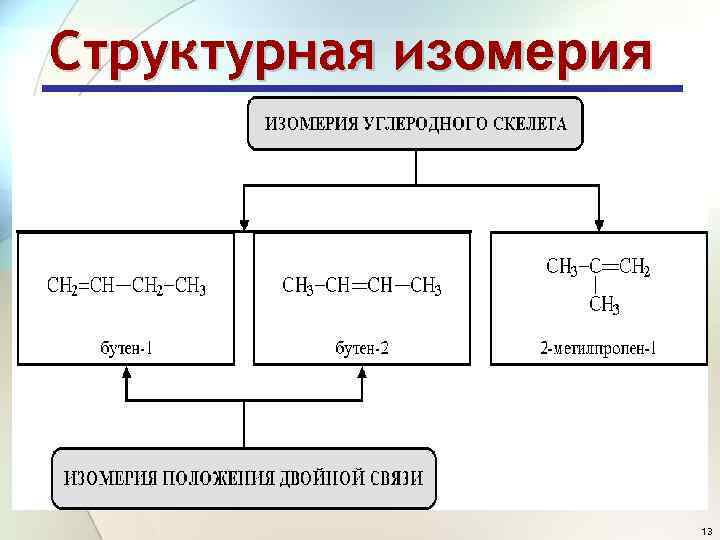
Структурная изомерия 13

Изомерия положения двойной связи 2 -метилбутен-2 2 -метилбутен-1 14
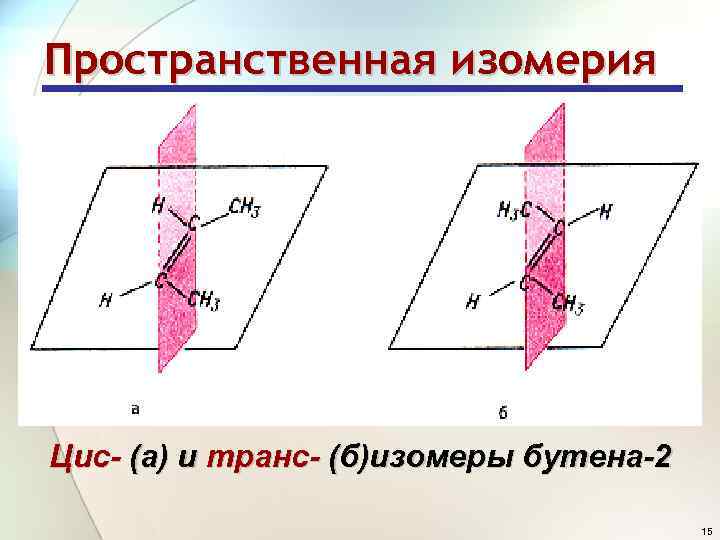
Пространственная изомерия Цис- (а) и транс- (б)изомеры бутена-2 15
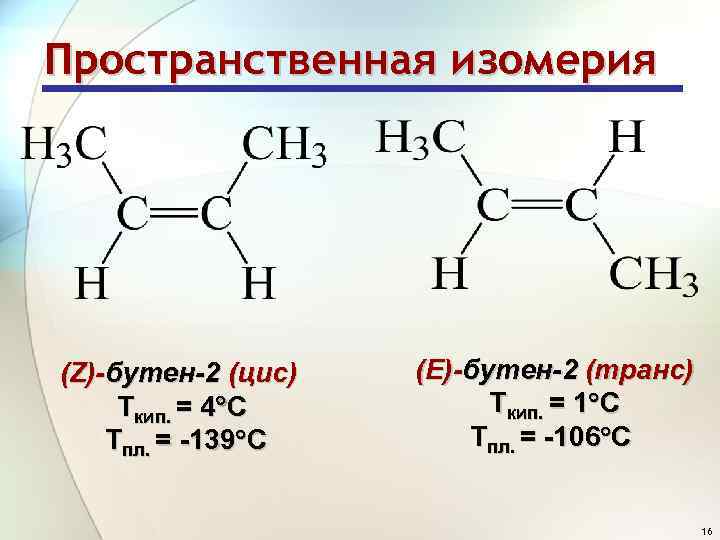
Пространственная изомерия (Z)-бутен-2 (цис) Ткип. = 4 С Тпл. = -139 С (Е)-бутен-2 (транс) Ткип. = 1 С Тпл. = -106 С 16
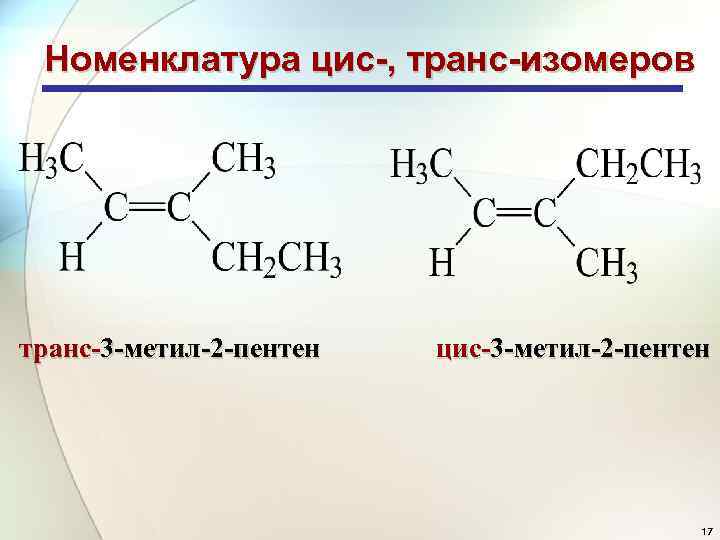
Номенклатура цис-, транс-изомеров транс-3 -метил-2 -пентен цис-3 -метил-2 -пентен 17
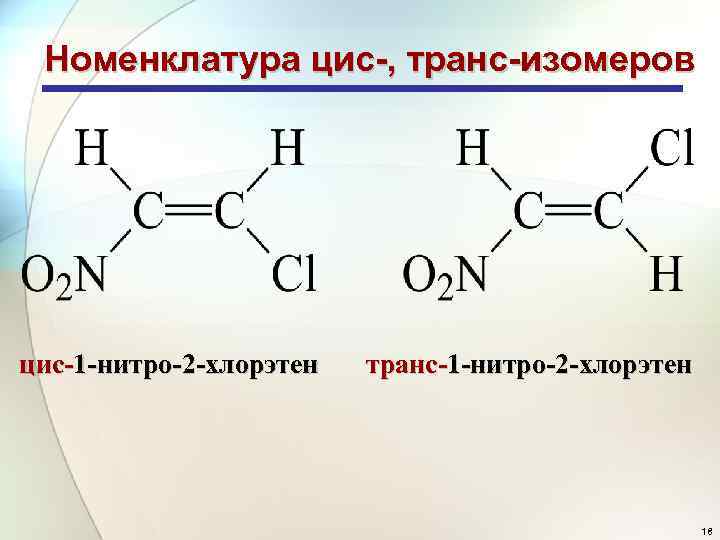
Номенклатура цис-, транс-изомеров цис-1 -нитро-2 -хлорэтен транс-1 -нитро-2 -хлорэтен 18

Номенклатура Кана–Ингольда–Прелога • Определяют сначала относительное старшинство заместителей, связанных с двойной связью, и дают им номера по старшинству 1 или 2 19

Номенклатура Кана–Ингольда–Прелога • Если две наиболее старшие группы расположены по одну сторону от плоскости связи, то конфигурация заместителей обозначается символом Z 20

Номенклатура Кана–Ингольда–Прелога • Если же эти группы находятся по разные стороны от плоскости связи, то конфигурация обозначается символом Е 21
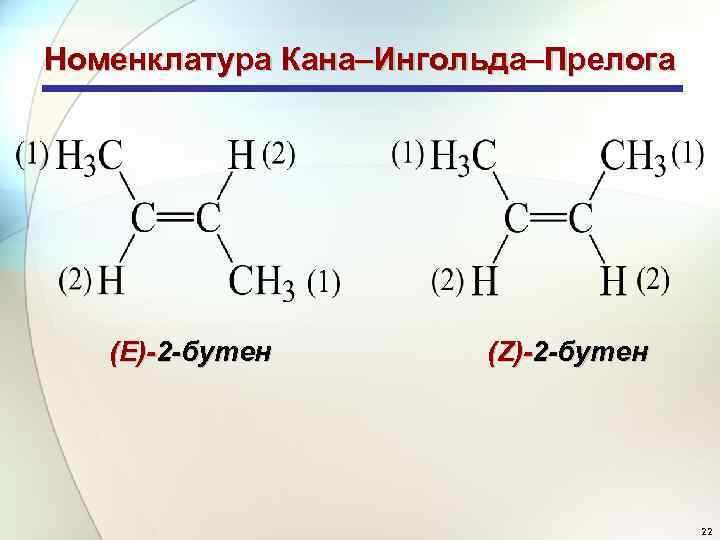
Номенклатура Кана–Ингольда–Прелога (Е)-2 -бутен (Z)-2 -бутен 22
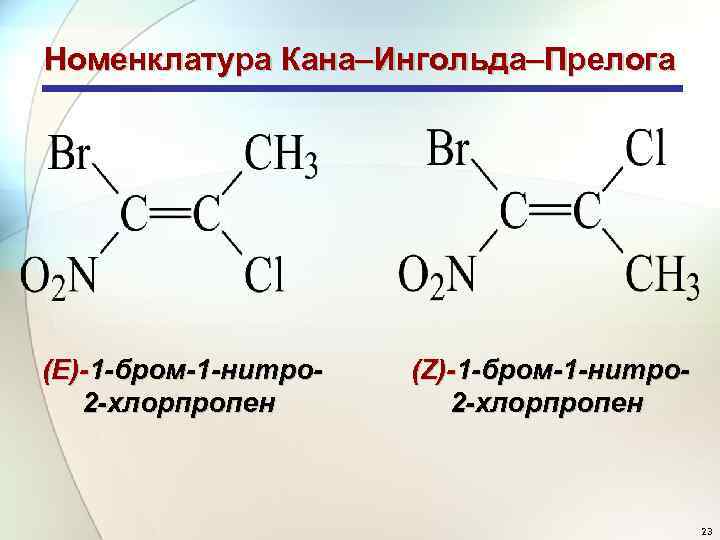
Номенклатура Кана–Ингольда–Прелога (Е)-1 -бром-1 -нитро 2 -хлорпропен (Z)-1 -бром-1 -нитро 2 -хлорпропен 23
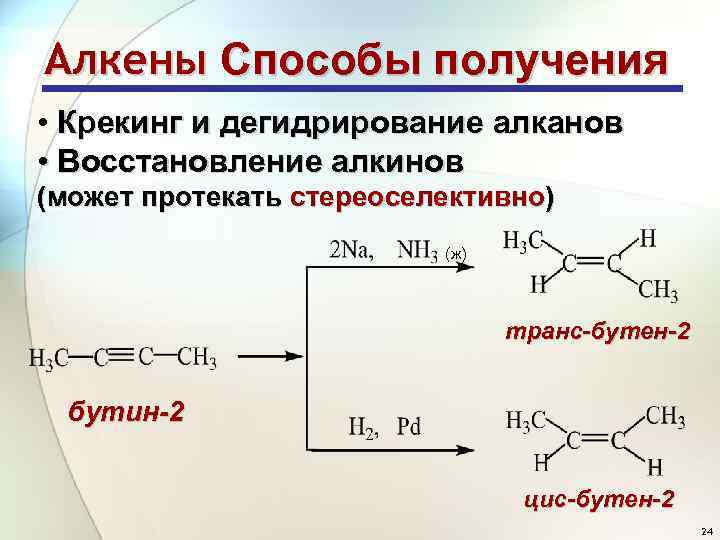
Алкены Способы получения • Крекинг и дегидрирование алканов • Восстановление алкинов (может протекать стереоселективно) (ж) транс-бутен-2 бутин-2 цис-бутен-2 24

Алкены Способы получения Реакции элиминирования • Элиминирование - отщепление двух атомов или групп атомов от соседних атомов углерода с образованием между ними связи 25
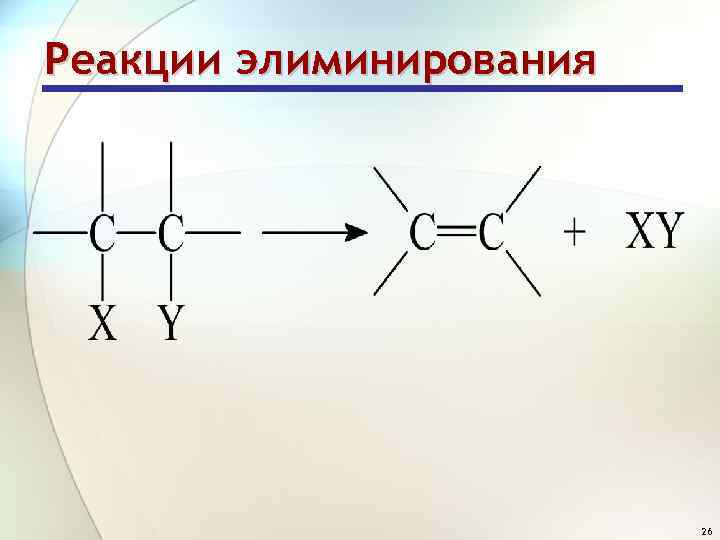
Реакции элиминирования 26
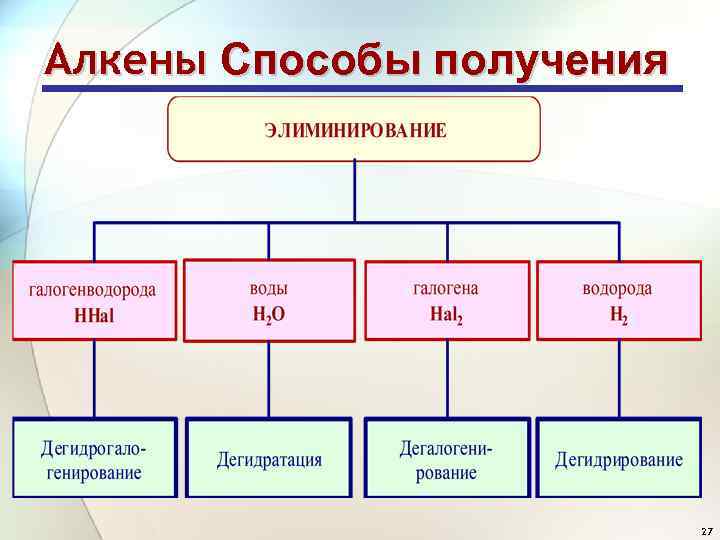
Алкены Способы получения 27

Алкены Способы получения Дегидрогалогенирование галогенуглеводородов Реакция осуществляется под действием сильных оснований в спиртовом растворе: 28

Алкены Способы получения • Дегидрогалогенирование галогенуглеводородов протекает по правилу Зайцева: В случае нессиметричных алкилгалогенидов отщепление атома водорода происходит от наименее гидрогенизированного атома углерода: 29

Алкены Способы получения ЗАЙЦЕВ Александр Михайлович (Россия) (2. VII. 1841 - 1. IX. 1910) 30

Алкены Способы получения Дегидратация спиртов 31

Алкены Способы получения • Легкость дегидратации спиртов изменяется в ряду: третичный › вторичный › первичный • Отщепление элементов воды от соседних атомов углерода также происходит по правилу Зайцева 32

Алкены Способы получения Дегалогенирование дигалогенопроизводных 33
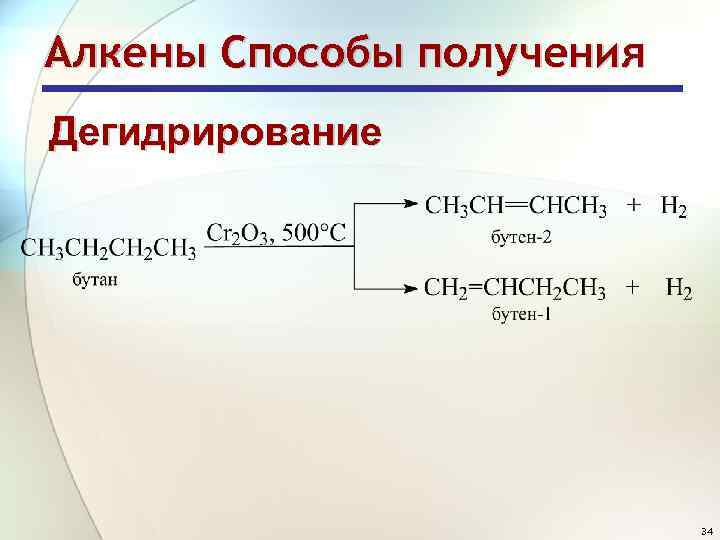
Алкены Способы получения Дегидрирование 34
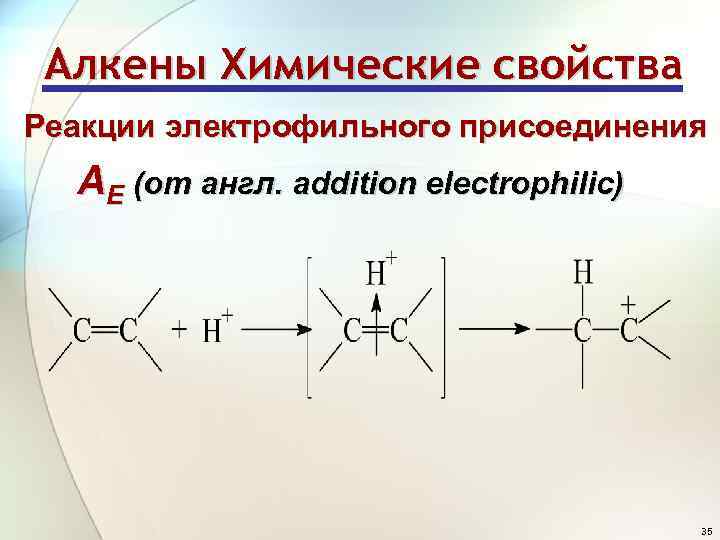
Алкены Химические свойства Реакции электрофильного присоединения АE (от англ. addition electrophilic) 35
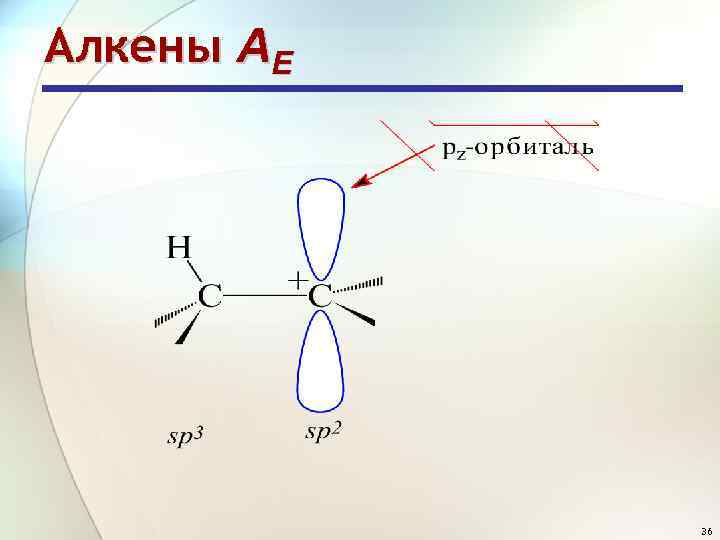
Алкены АE 36
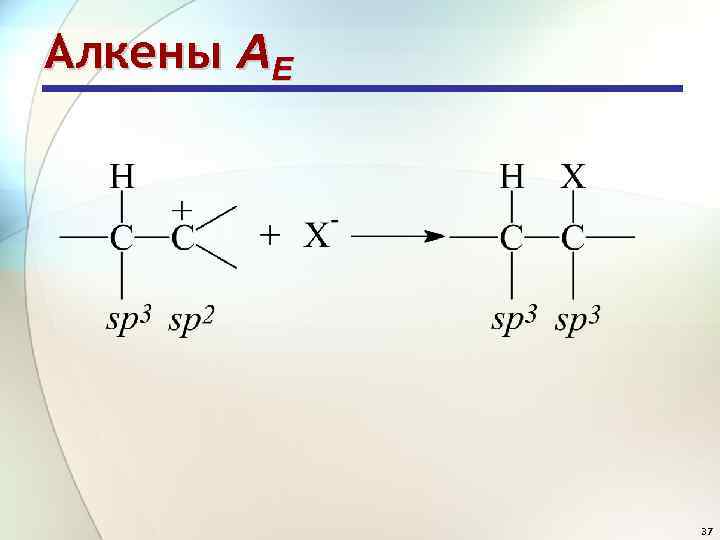
Алкены АE 37
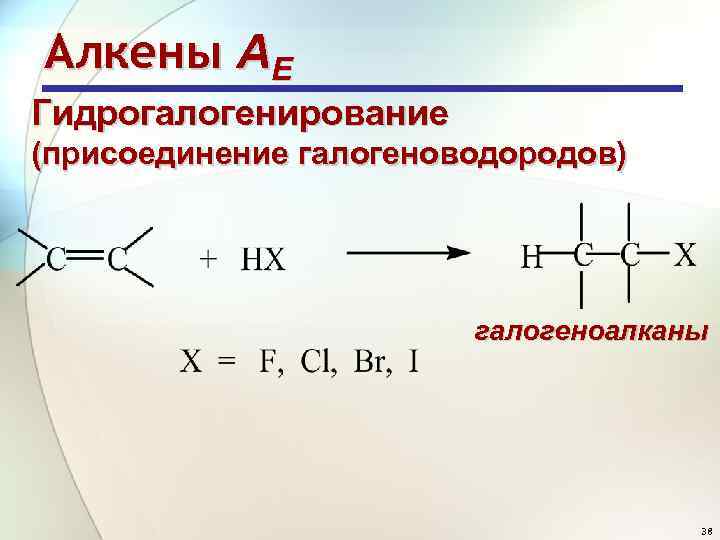
Алкены АE Гидрогалогенирование (присоединение галогеноводородов) галогеноалканы 38

Алкены АE Гидрогалогенирование 39
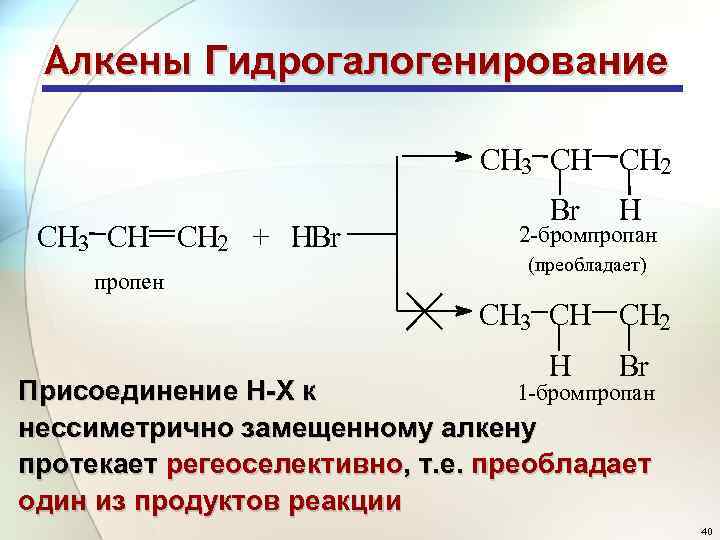
Алкены Гидрогалогенирование CH 3 CH CH 2 + HBr пропен Br H 2 -бромпропан (преобладает) CH 3 CH CH 2 H Br Присоединение H-X к 1 -бромпропан нессиметрично замещенному алкену протекает регеоселективно, т. е. преобладает один из продуктов реакции 40

Алкены Гидрогалогенирование Правило Марковникова: присоединении молекул типа НХ к несимметричным алкенам атом водорода присоединяется к более гидрогенизированному атому углерода двойной связи 41

Алкены Гидрогалогенирование МАРКОВНИКОВ Владимир Васильевич 13. 12. 1837 – 29. 01. 1904 (Россия) 42
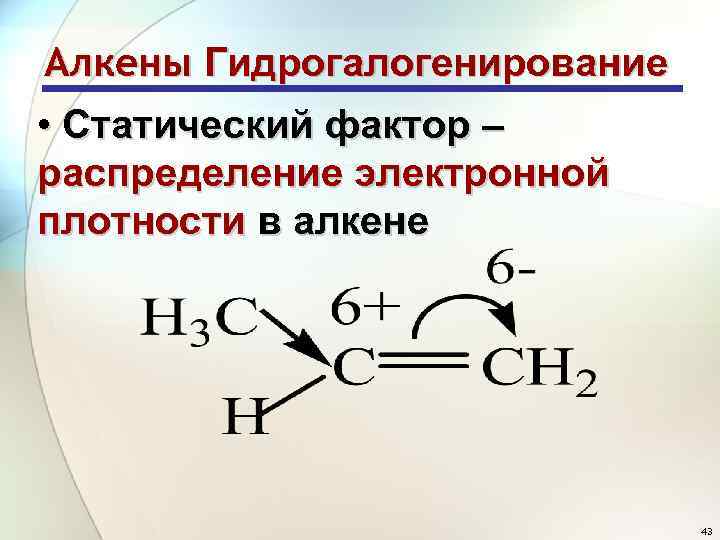
Алкены Гидрогалогенирование • Статический фактор – распределение электронной плотности в алкене 43
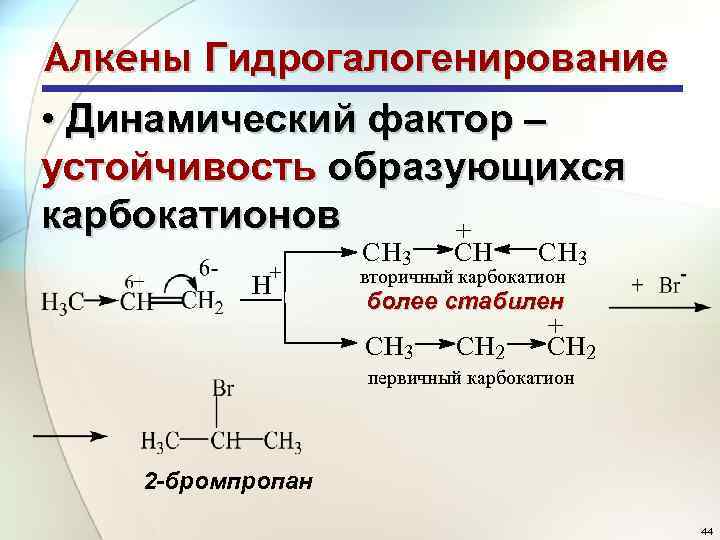
Алкены Гидрогалогенирование • Динамический фактор – устойчивость образующихся карбокатионов + + H CH 3 CH CH 3 вторичный карбокатион более стабилен CH 3 CH 2 + CH 2 первичный карбокатион 2 -бромпропан 44
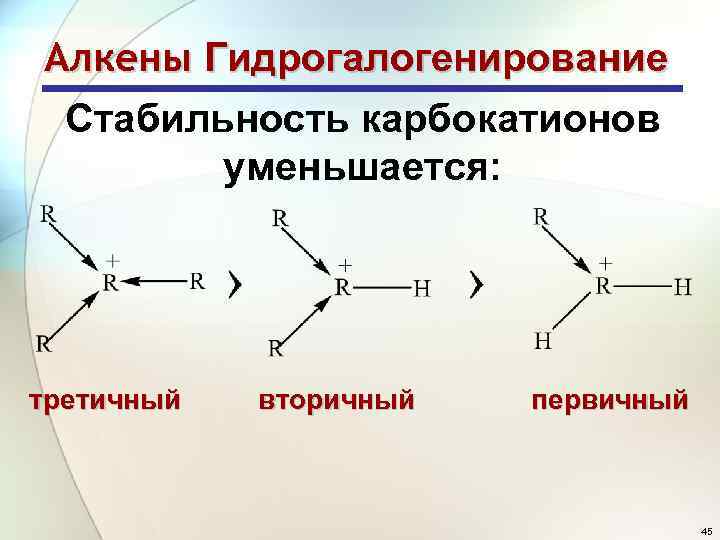
Алкены Гидрогалогенирование Стабильность карбокатионов уменьшается: третичный вторичный первичный 45

Алкены Гидрогалогенирование Правило Марковникова в современной интерпретации: направление присоединения реагентов типа НХ к непредельным соединениям определяется относительной устойчивостью образующихся карбокатионов 46
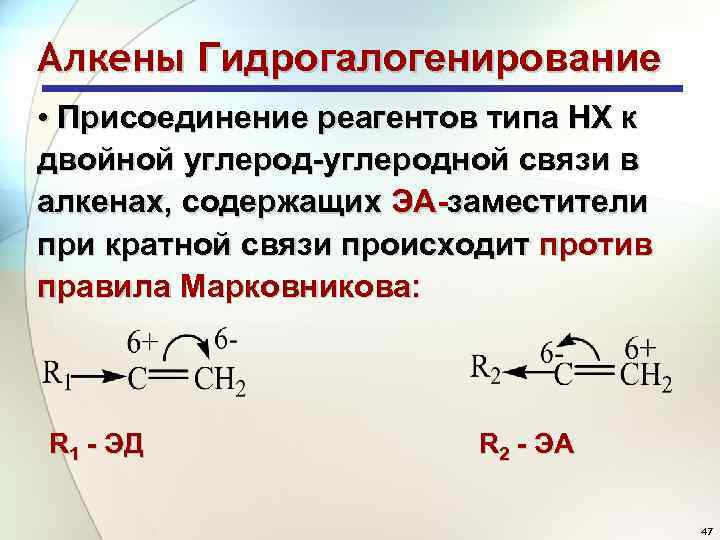
Алкены Гидрогалогенирование • Присоединение реагентов типа НХ к двойной углерод-углеродной связи в алкенах, содержащих ЭА-заместители при кратной связи происходит против правила Марковникова: R 1 - ЭД R 2 - ЭА 47
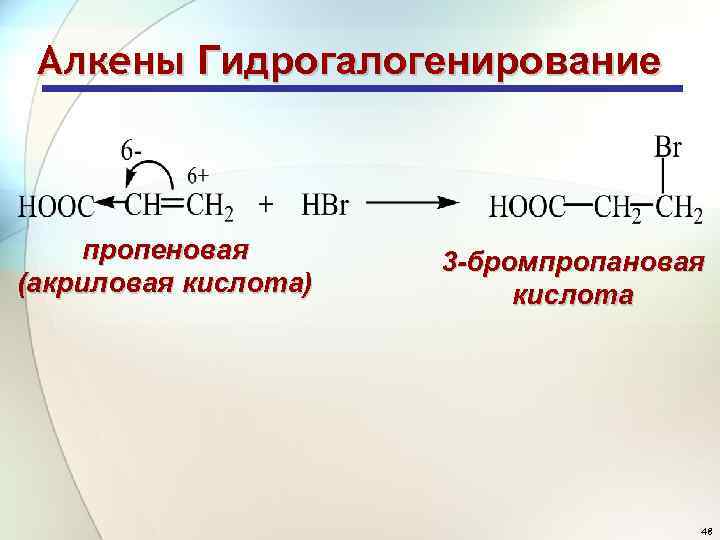
Алкены Гидрогалогенирование пропеновая (акриловая кислота) 3 -бромпропановая кислота 48
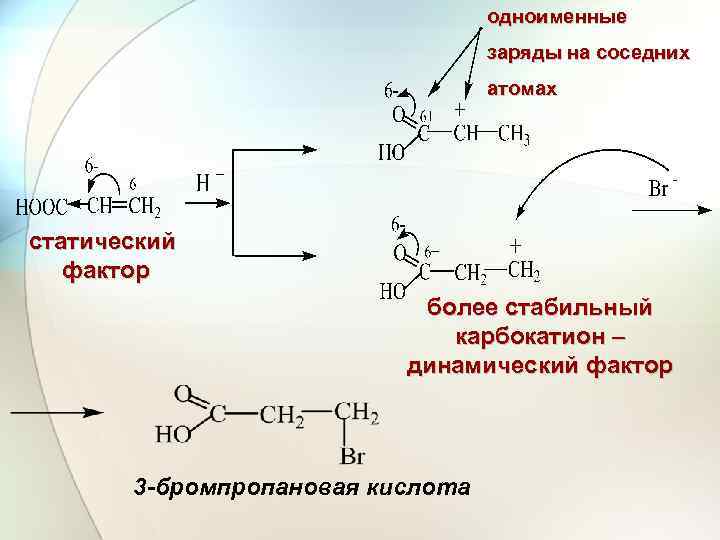
одноименные заряды на соседних атомах статический фактор более стабильный карбокатион – динамический фактор 3 -бромпропановая кислота
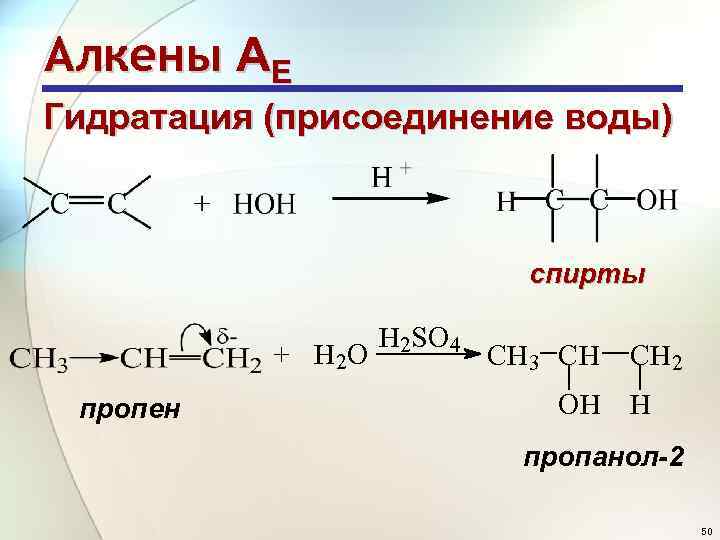
Алкены АE Гидратация (присоединение воды) спирты + H 2 O пропен H 2 SO 4 CH 3 CH CH 2 OH H пропанол-2 50
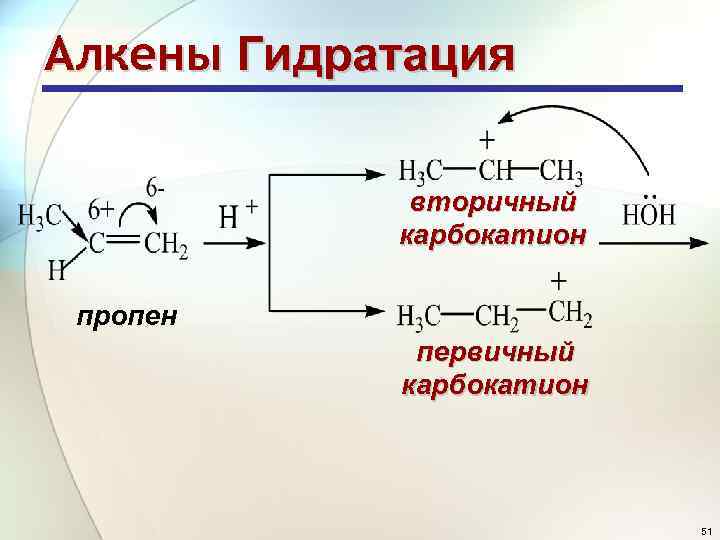
Алкены Гидратация вторичный карбокатион пропен первичный карбокатион 51
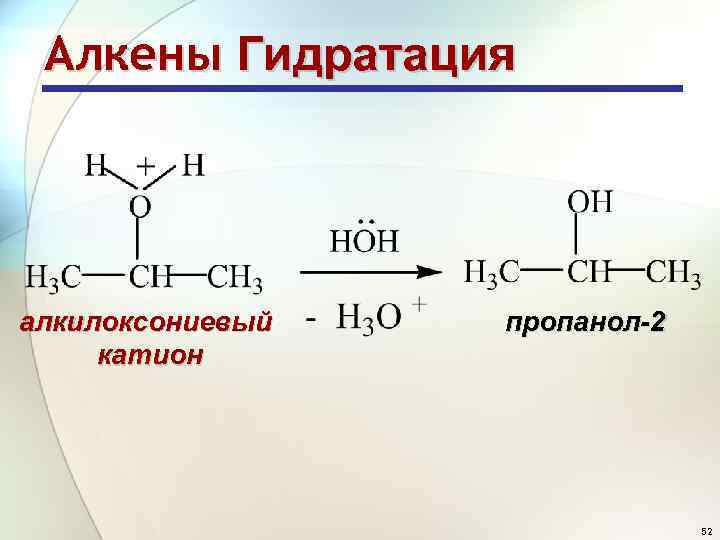
Алкены Гидратация алкилоксониевый катион пропанол-2 52
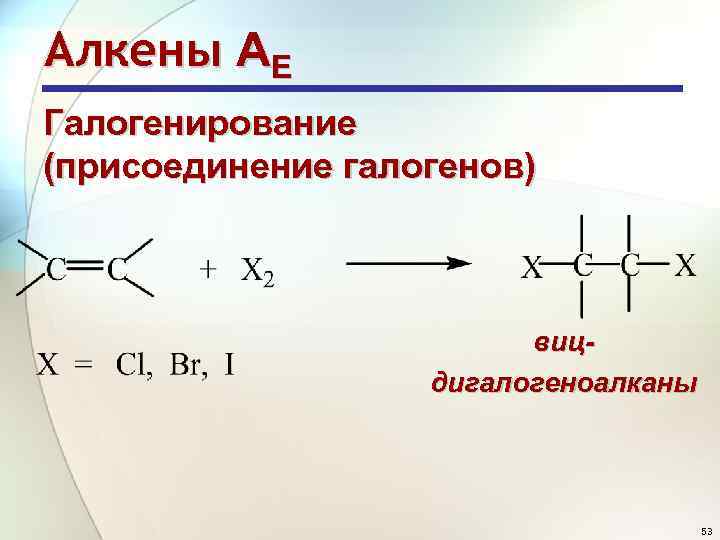
Алкены АE Галогенирование (присоединение галогенов) вицдигалогеноалканы 53

Алкены Галогенирование бутен-1 1, 2 -дибромбутан (99%) 54
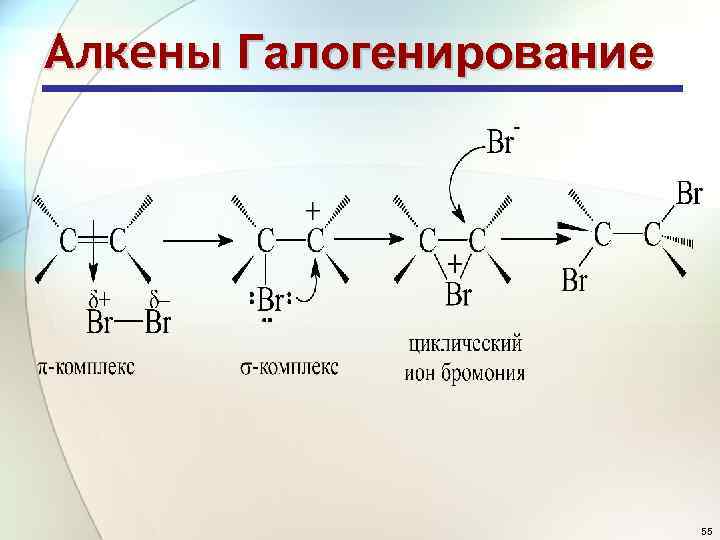
Алкены Галогенирование 55

Алкены Галогенирование • Раствор брома в воде или тетрахлорметане имеет бурую окраску, продукты присоединения брома бесцветны 56

Алкены Галогенирование • Быстрое обесцвечивание раствора брома используется как простой визуальный тест на ненасыщенность 57
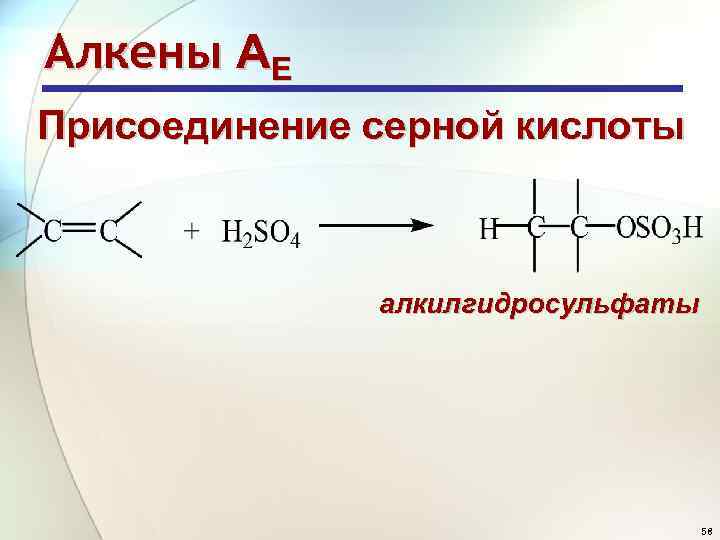
Алкены АE Присоединение серной кислоты алкилгидросульфаты 58

Алкены АE • Взаимодействие алкенов с Н 2 SO 4 широко используется для получения спиртов: этилгидросульфат этанол 59
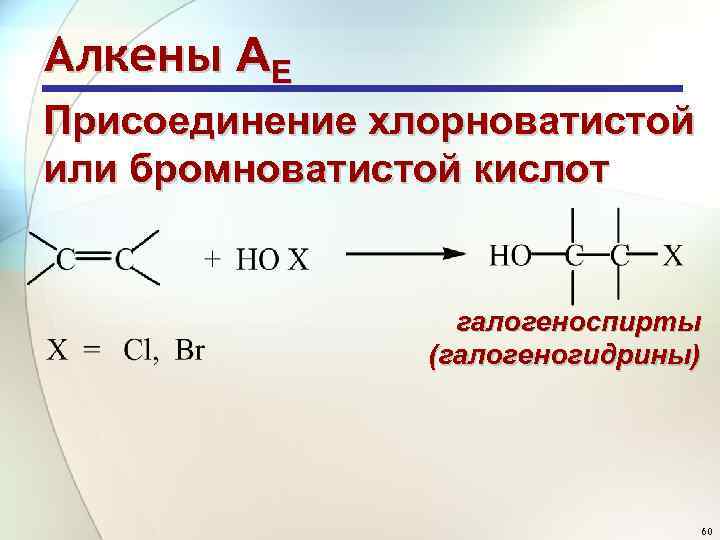
Алкены АE Присоединение хлорноватистой или бромноватистой кислот галогеноспирты (галогеногидрины) 60
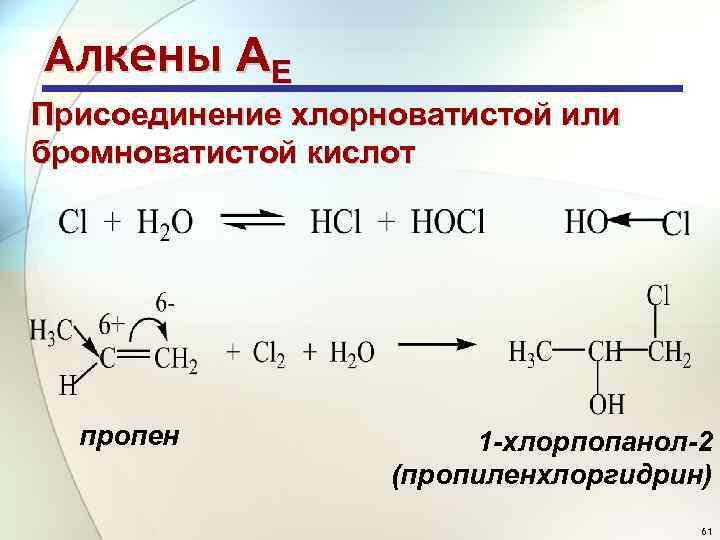
Алкены АE Присоединение хлорноватистой или бромноватистой кислот пропен 1 -хлорпопанол-2 (пропиленхлоргидрин) 61

Алкены АE • Реакции Ае протекают тем легче, чем большая электронная плотность (ЭП) сосредоточена между атомами углерода, образующими двойную связь 62

Алкены АE • ЭД увеличивают ЭП двойной связи, следовательно, ускоряют реакции Ае • ЭА уменьшают ЭП двойной связи, следовательно, замедляют реакции Ае 63

Алкены АE • Сопряжение двойной связи с бензольным кольцом ускоряет реакции Ае 64

Алкены АE • Чем меньше реакционная способность алкена в реакции с кислотными реагентами НХ, тем сильнее или концентрирование д. б. кислота 65

Алкены Химические свойства Реакции свободно-радикального присоединения АR • Свободные радикалы – электронодефицитные частицы 66

Алкены Химические свойства • Свободные радикалы могут атаковать π-электроны двойной связи и присоединяться к ней. Возникает новый радикал 67

Алкены АR • Новый радикал может оторвать атом водорода (или другой атом) от молекулы и реакция присоединения завершается 68

Алкены АR • Если новый радикал присоединяется к следующей молекуле алкена и далее, то образуются цепи различной длины – радикальная полимеризация 69

Алкены АR • Для предотвращения полимеризации алкен необходимо брать в недостатке 70
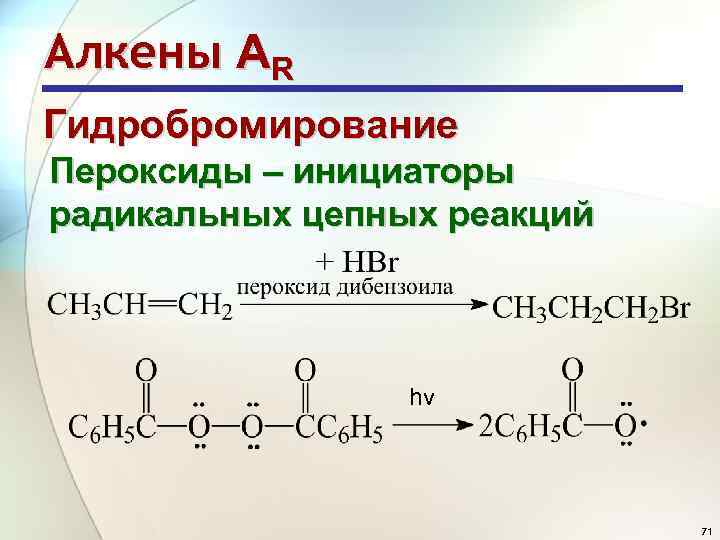
Алкены АR Гидробромирование Пероксиды – инициаторы радикальных цепных реакций hν 71

Алкены АR • Присоединение HBr против правила Марковникова происходит следующим образом: Br (а не Н ) реагирует в первую очередь с -системой и быстрее всего образуется наиболее стабильный радикал 72

Алкены АR «Пероксидный эффект» (эффект Хараша-Майо), 1993 73

Алкены АR • Направление присоединения определяется стабильностью алкильных радикалов: третичный вторичный первичный метильный 74
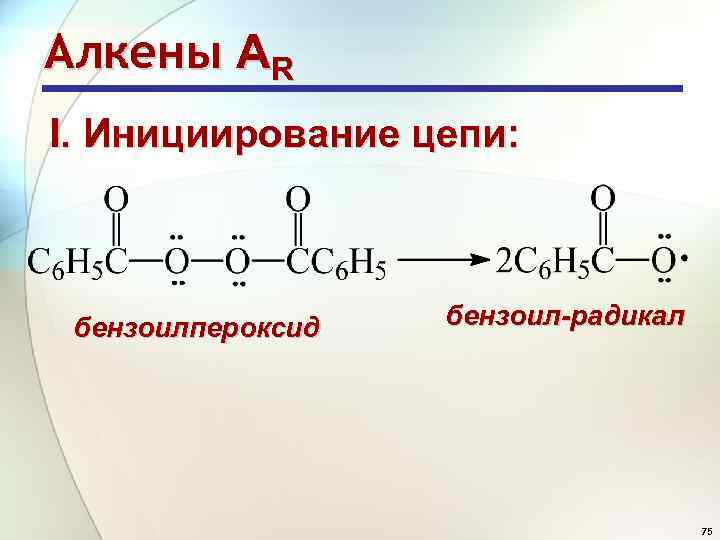
Алкены АR I. Инициирование цепи: бензоилпероксид бензоил-радикал 75

Алкены АR II. Рост цепи: вторичный радикал 76
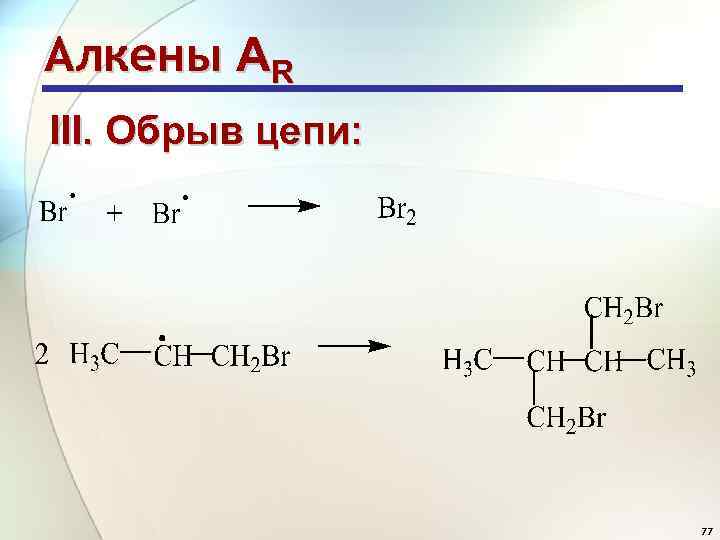
Алкены АR III. Обрыв цепи: 77

Алкены АR Аллильное замещение галогенами (замещение водорода на галоген в алкильной группе алкена) пропен аллилхлорид 78

Алкены АR • В алкенах наиболе легко замещаются атомы водорода в аллильном положении (у соседнего с двойной связью атома углерода) 79

Алкены АR • Селективность реакции обусловлена стабильностью радикала аллильного типа (за счет сопряжения с кратной связью): 80

Алкены Химические свойства Реакции окисления • Алкены легко окисляются многими окислителями • При мягком окислении алкенов разрывается π-связь, при глубоком окислении - π- и σ-связи и образуются новые связи с кислородом 81

Алкены Реакции окисления • Продуктами окисления алкенов в порядке увеличения степени окисления могут быть: - эпоксиды (оксираны) - винициальные диолы - альдегиды - кетоны - карбоновые кислоты - диоксид углерода 82
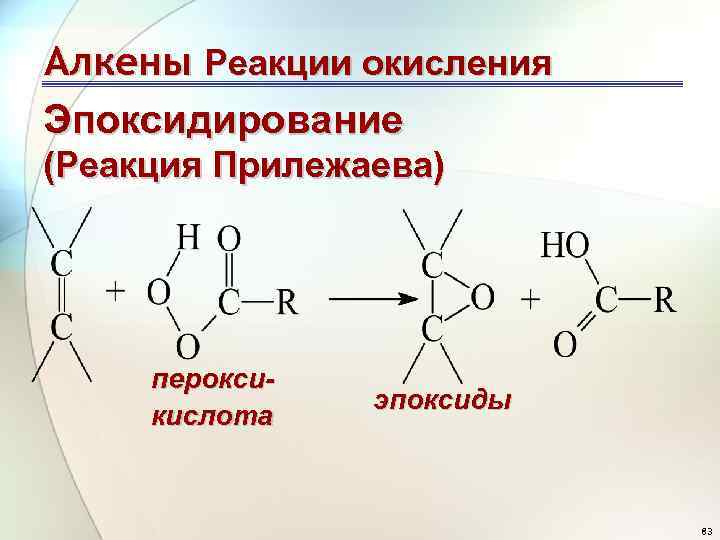
Алкены Реакции окисления Эпоксидирование (Реакция Прилежаева) пероксикислота эпоксиды 83

Алкены Реакции окисления Гидроксилирование (окисление по Вагнеру) ВАГНЕР Егорович (9. XII. 1849 – 27. XI. 1903) 84
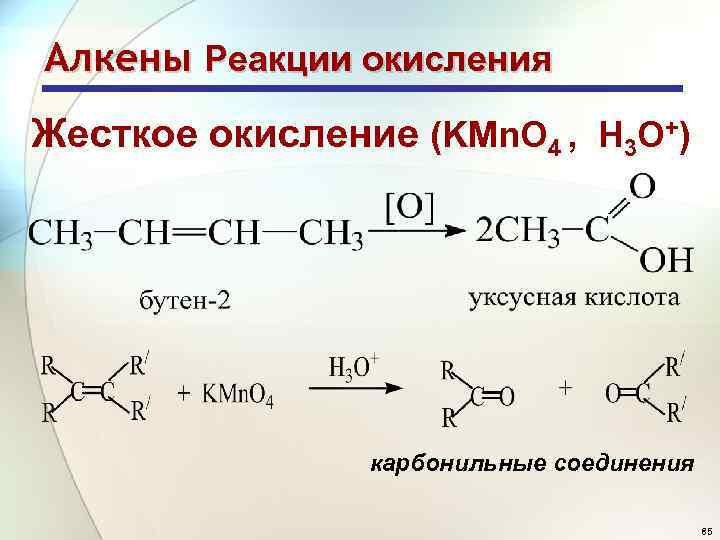
Алкены Реакции окисления Жесткое окисление (KMn. O 4 , H 3 O+) карбонильные соединения 85

Алкены Реакции окисления Горение C 2 H 4 + 3 O 2 2 CO 2 + 2 H 2 O 86
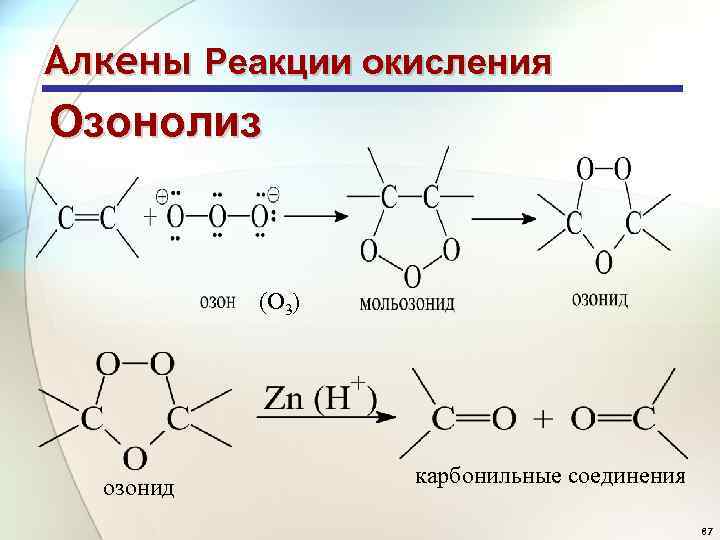
Алкены Реакции окисления Озонолиз (О 3) озонид карбонильные соединения 87
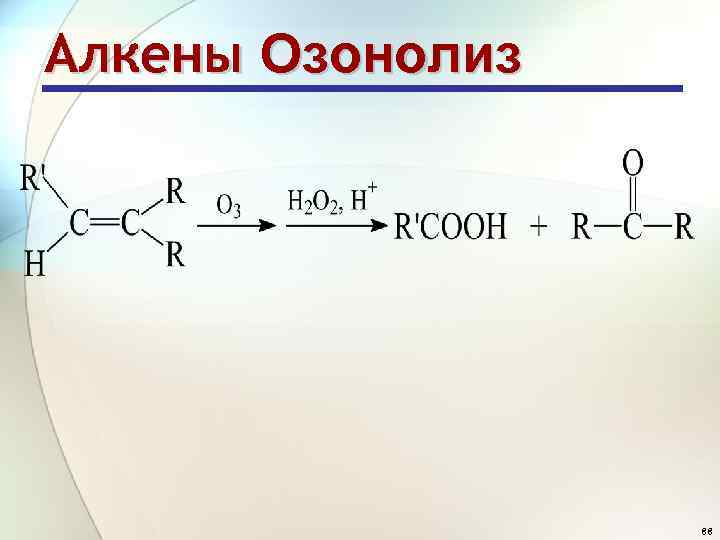
Алкены Озонолиз 88
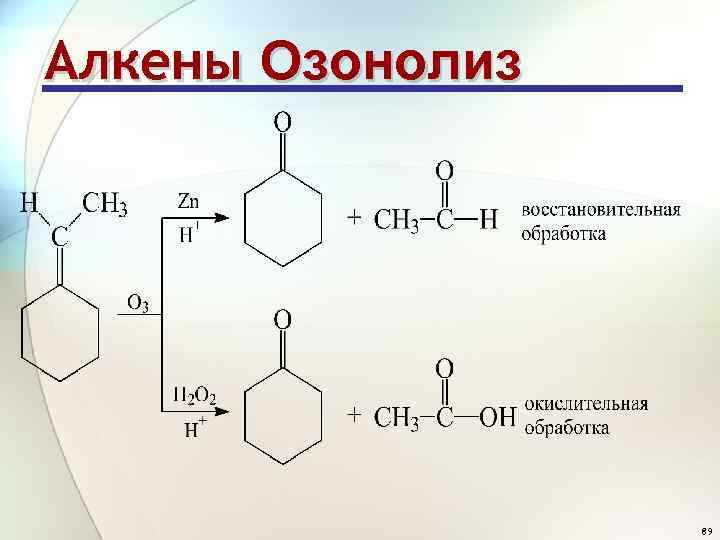
Алкены Озонолиз 89

Алкены Химические свойства Реакция восстановления (гидрирование) катализатор: Pt, Pd, Ni 90
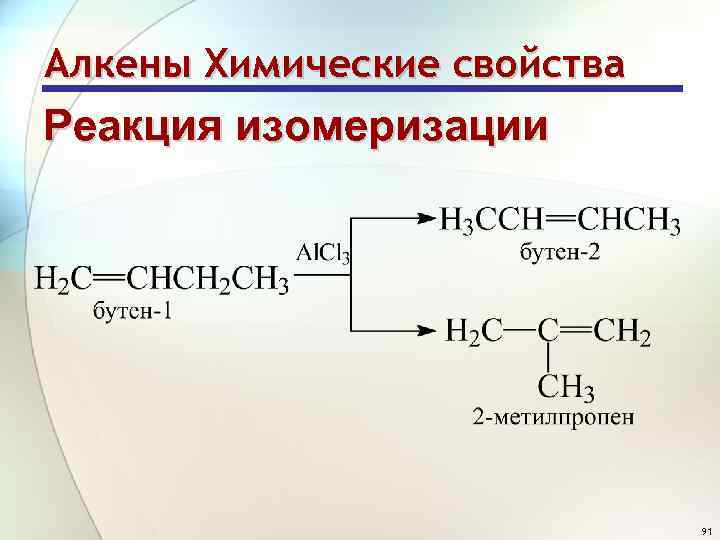
Алкены Химические свойства Реакция изомеризации 91

Алкены Химические свойства Реакция полимеризации – последовательное присоединение молекул ненасыщенных соединений друг к другу с образованием высокомолекулярного продукта – полимера 92
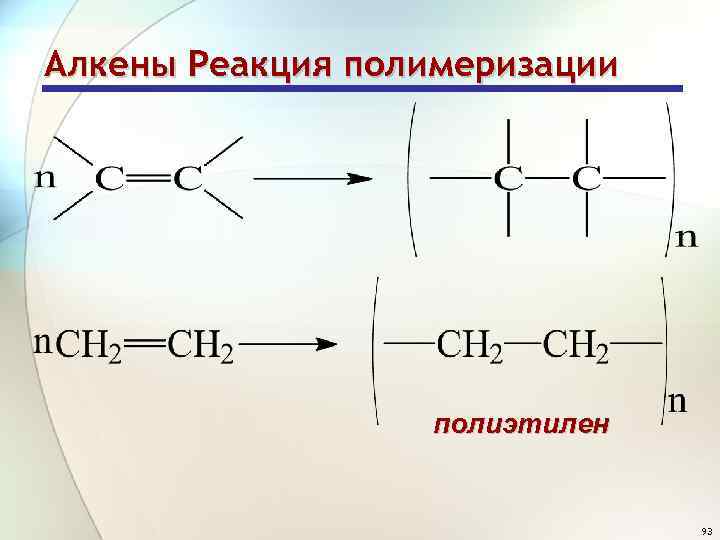
Алкены Реакция полимеризации полиэтилен 93
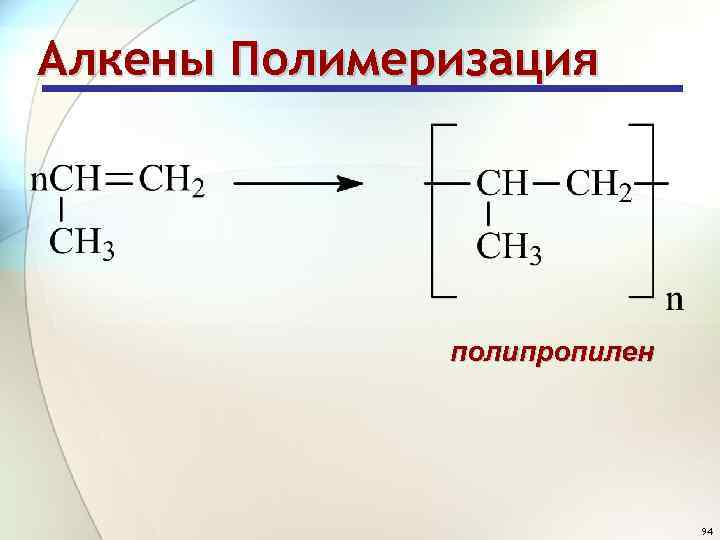
Алкены Полимеризация полипропилен 94
Alken-2012.ppt