Алканы.ppt
- Количество слайдов: 76

РЕАКЦИОННАЯ СПОСОБНОСТЬ УГЛЕВОДОРОДОВ (АЛКАНЫ) 1
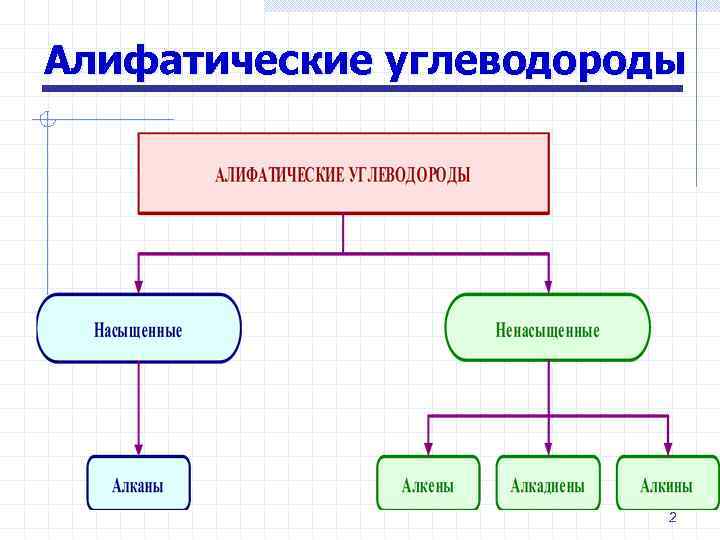
Алифатические углеводороды 2

Сn. Н 2 n+2 Алканы - насыщенные углеводороды, молекулы которых состоят из атомов углерода и водорода, связанных между собой только -связями
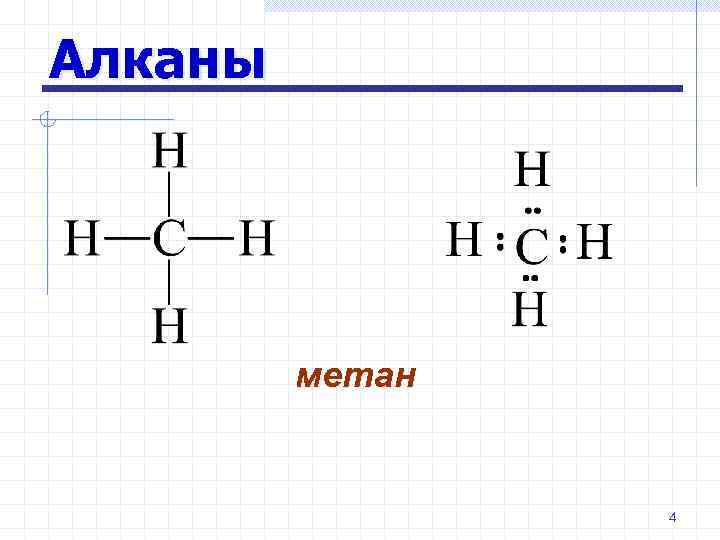
Алканы метан 4
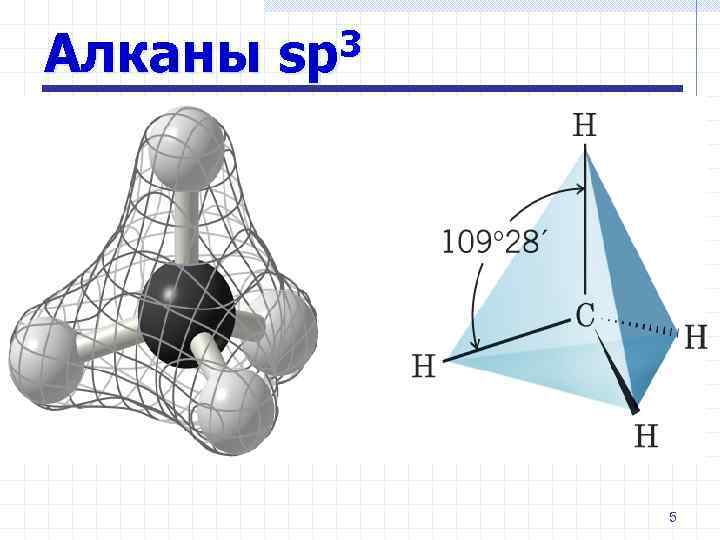
Алканы 3 sp 5
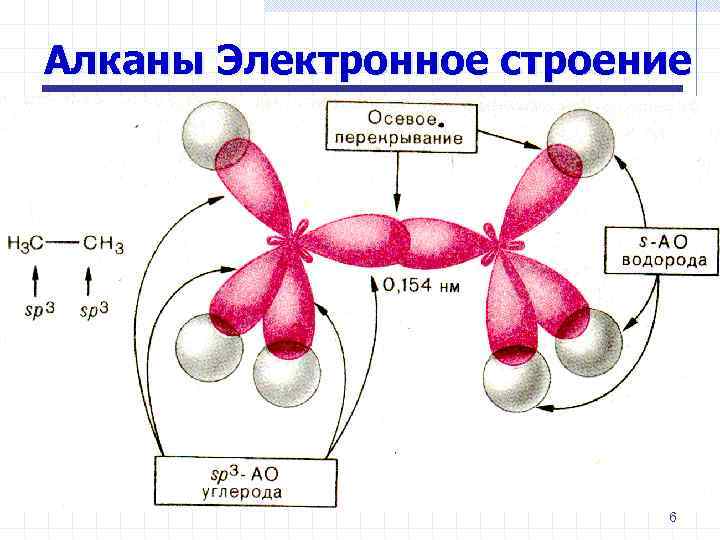
Алканы Электронное строение 6

Алканы Сn. Н 2 n+2 Гомологический ряд метана и т. д. В соответствии с общей формулой алканы образуют гомологический ряд в котором гомологи отличаются друг от друга на гомологическую разность СН 2 7

Алканы Сn. Н 2 n+2 Гомологический ряд изобутана 8
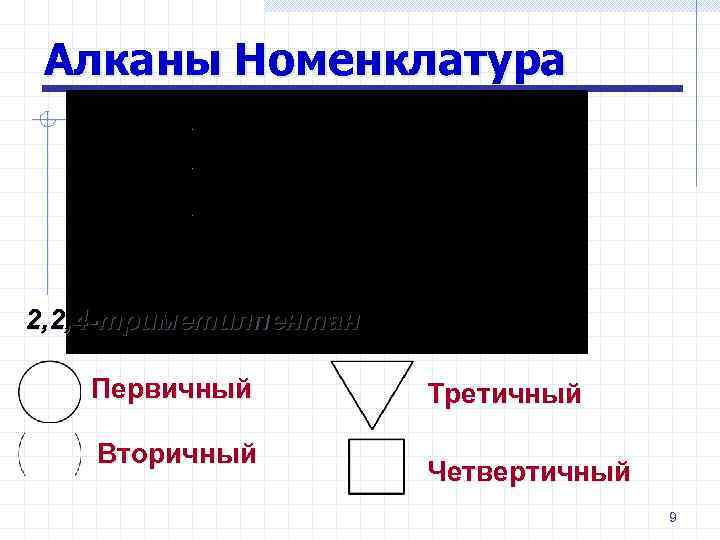
Алканы Номенклатура 2, 2, 4 -триметилпентан Первичный Вторичный Третичный Четвертичный 9

Алканы Номенклатура Систематическая номенклатура ИЮПАК 1) определяют самую длинную цепь атомов углерода. Число атомов углерода в этой цепи служит основой названия 2) нумеруют главную цепь с того конца, ближе к которому находится заместитель (углеводородный радикал) 10

Алканы Номенклатура 3) перед основой названия указывают цифровой номер того атома углерода в главной цепи, у которого находится заместитель, а затем в виде префикса называют этот заместитель 11

Алканы Номенклатура 4) при наличии двух и более заместителей их перечисляют в алфавитном порядке. Если заместители одинаковые, то к их названию добавляют умножительные приставки ди -, три-, тетра-, пента- и т. д. 12

Алканы Номенклатура 5) если в главной цепи на равном расстоянии от концов стоят одинаковые радикалы, то нумерацию производят таким образом, чтобы радикалы получили наименьшие номера 13
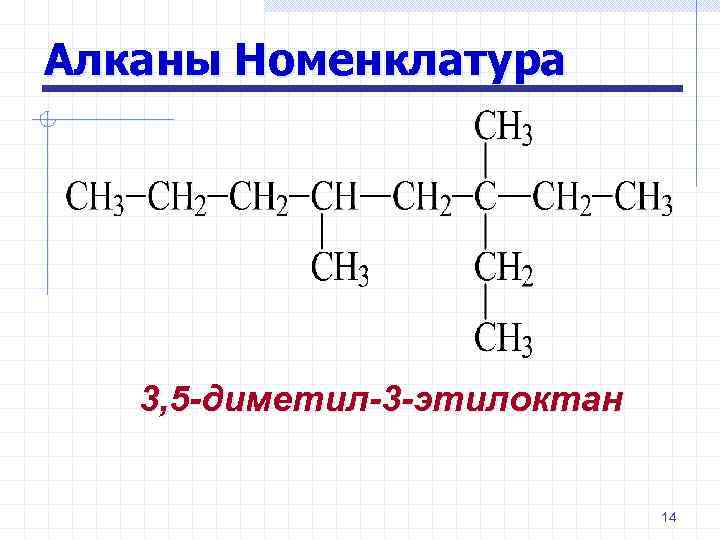
Алканы Номенклатура 3, 5 -диметил-3 -этилоктан 14

Алканы Номенклатура 2, 3, 4 -триметилпентан 15

Алканы Номенклатура 2, 3, 6 -триметилгептан 16

Рациональная Номенклатура тетраметилметан (2, 2 -диметилпропан) 17
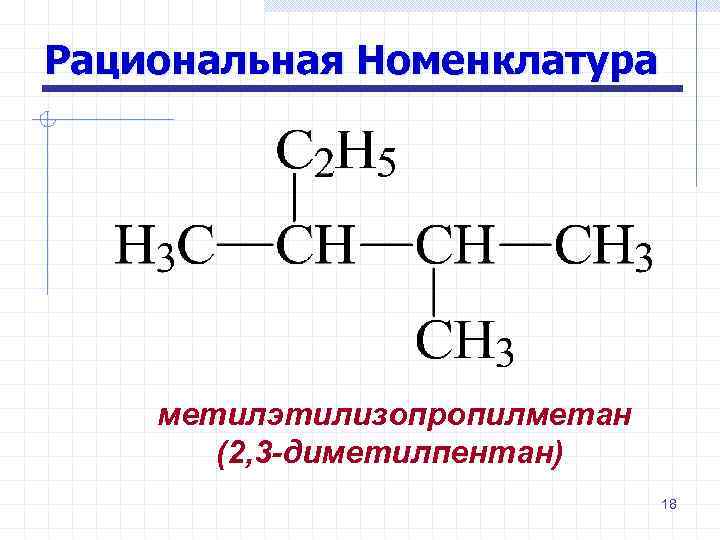
Рациональная Номенклатура метилэтилизопропилметан (2, 3 -диметилпентан) 18

Алканы Структурная изомерия • Для алканов, начиная с бутана, существуют структурные изомеры (изомеры строения), различающиеся порядком связывания между атомами углерода 19

Алканы Структурная изомерия С 4 Н 10 н-бутан Ткип= -0, 5 С изобутан Ткип= -11, 7 С 20
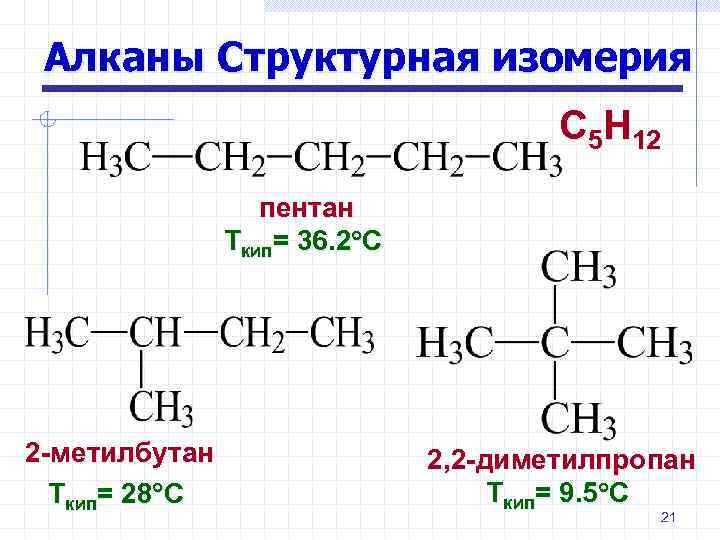
Алканы Структурная изомерия С 5 Н 12 пентан Ткип= 36. 2 С 2 -метилбутан Ткип= 28 С 2, 2 -диметилпропан Ткип= 9. 5 С 21

Алканы Физические свойства • При обычных условиях первые четыре члена гомологического ряда алканов - газы без запаха • Углеводороды, содержащие 5 -15 атомов углерода, - жидкости с характерным бензиновым запахом • Высшие алканы – твердые вещества без запаха 22
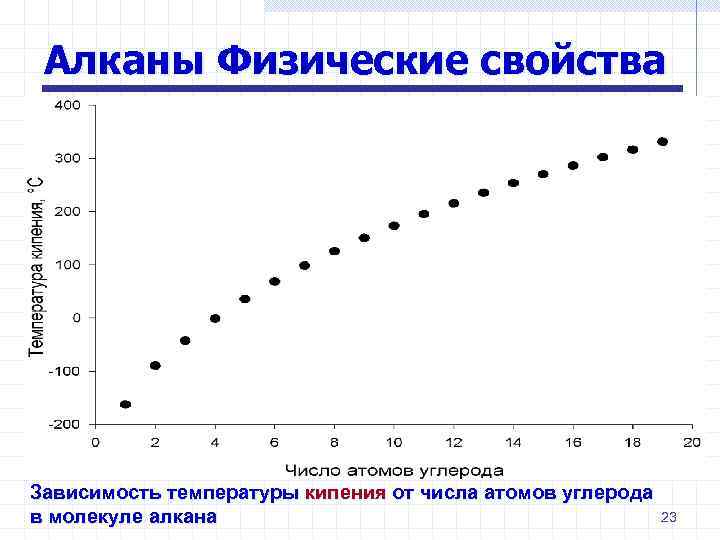
Алканы Физические свойства Зависимость температуры кипения от числа атомов углерода 23 в молекуле алкана
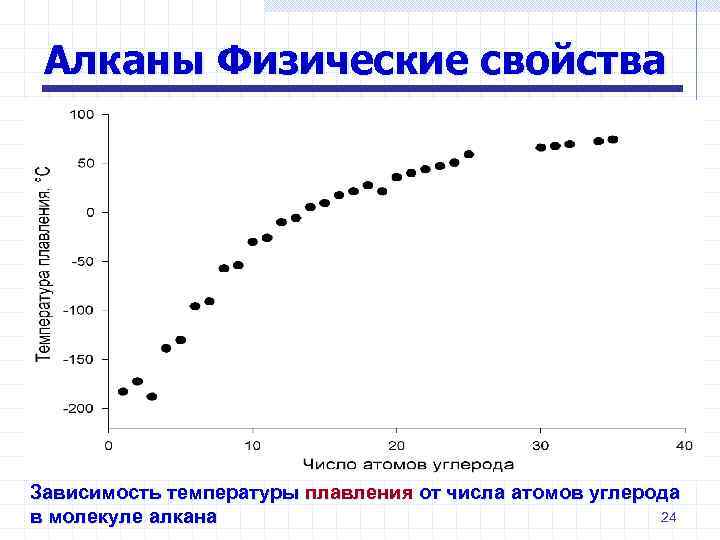
Алканы Физические свойства Зависимость температуры плавления от числа атомов углерода 24 в молекуле алкана
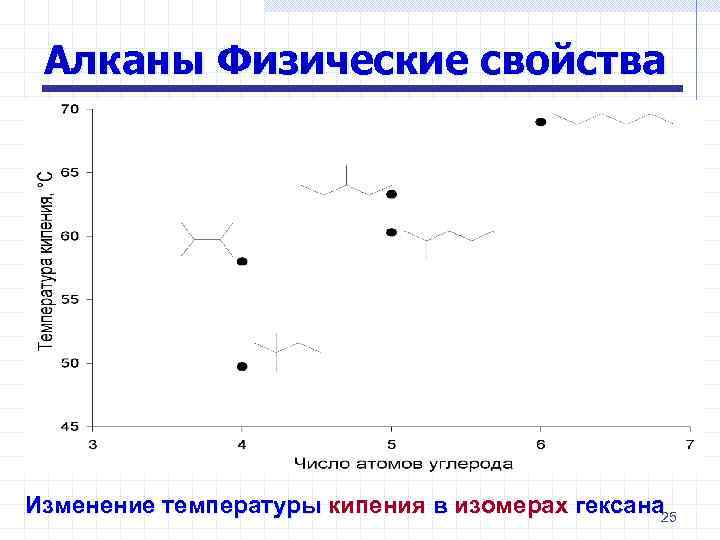
Алканы Физические свойства Изменение температуры кипения в изомерах гексана 25

Промышленные источники алканов • Природный газ • Нефть и ее фракции, перерабатываемые различными методами (крекинг, пиролиз, риформинг) 27

Синтетические способы получения алканов Газофикация угля (Бертло, 1869) 28

Синтетические способы получения алканов Метод Фишера-Тропша Синтетический бензин - «синтин» 29

Синтетические способы получения алканов Получение из ненасыщенных углеводородов (гидрирование алкенов и алкинов) 30

Алканы Получение из галогенопроизводных (при действии металлического натрия на моногалогенпроизводные) 31
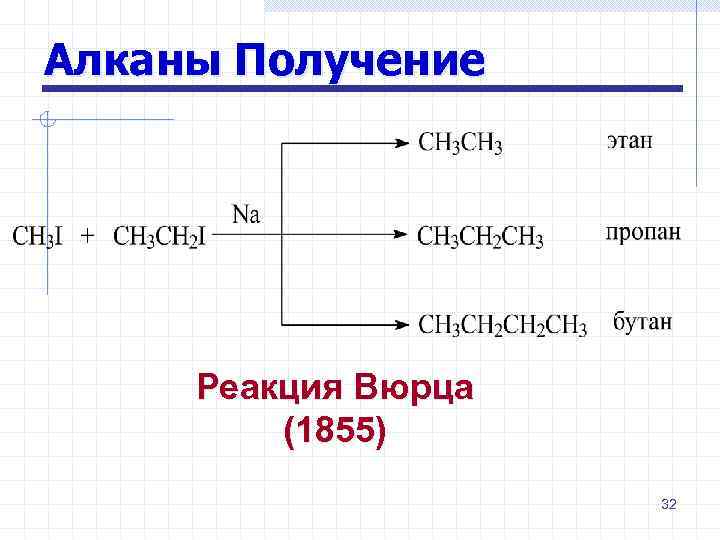
Алканы Получение Реакция Вюрца (1855) 32
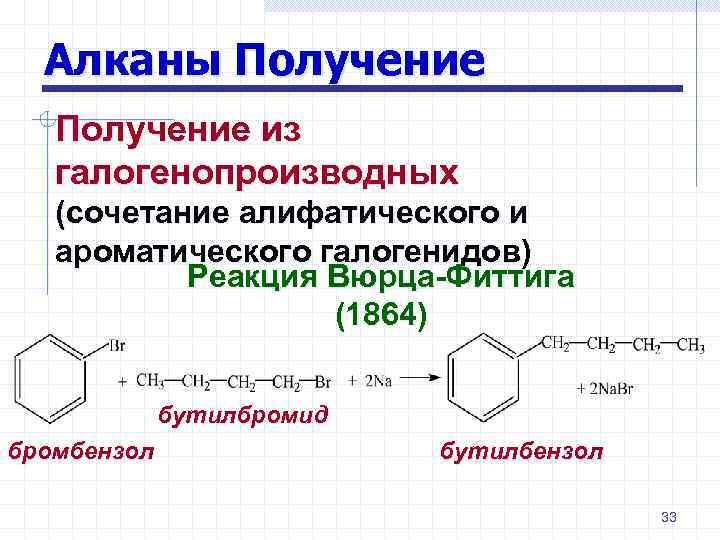
Алканы Получение из галогенопроизводных (сочетание алифатического и ароматического галогенидов) Реакция Вюрца-Фиттига (1864) бутилбромид бромбензол бутилбензол 33

Алканы Получение Восстановление галогеналканов • Li. Al. H 4 Na. BH 4 • Na или Li в трет-бутиловом спирте • Каталитическое восстановление водородом 34

Алканы Получение Алкилйодиды могут быть восстановлены путем нагревания с йодоводородной кислотой: 35

Алканы Получение из солей карбоновых кислот (сплавление солей карбоновых кислот со щелочью) 36

Алканы Получение Электролиз солей щелочных металлов и карбоновых кислот (анодный синтез алканов) Реакция Кольбе (1849) 37
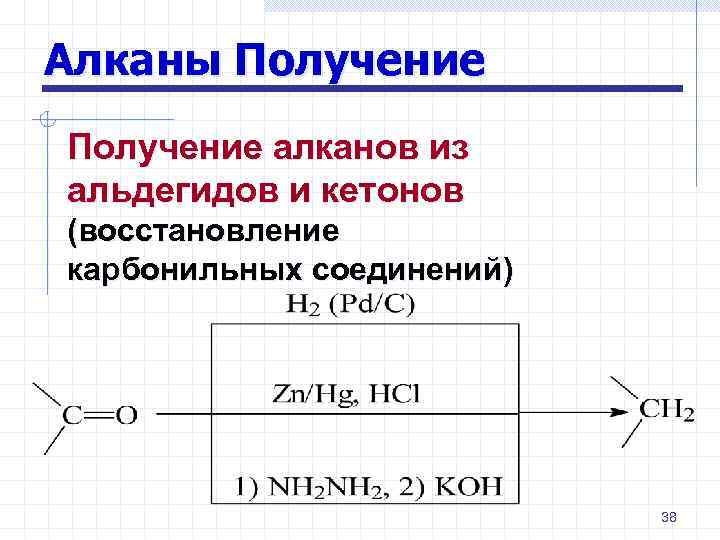
Алканы Получение алканов из альдегидов и кетонов (восстановление карбонильных соединений) 38

Алканы Получение Гидролиз карбидов металлов • Карбиды, при гидролизе, которых образуется метан карбиды алюминия и берилия Al 4 C 3, Be 2 C Al 4 C 3 + 12 H 2 O = 3 CH 4 + 4 Al(OH)3 39

Алканы Получение • Карбиды при гидролизе, которых образуется ацетилен Na 2 C 2 Ba. C 2 K 2 C 2 Cu 2 C 2 Ca. C 2 Ag 2 C 2 40

Алканы Получение • Карбиды при гидролизе, которых образуется смесь углеводородов (карбиды переходных металлов) Переработка отходов биологического происхождения 41

Алканы Химические свойства • Большая химическая инертность • Устойчивость к действию концентрированных кислот, щелочей и сильных окислителей • Устойчивость к действию ионных реагентов 42

Алканы Химические свойства • Не взаимодействуют со щелочными металлами • Характерны реакции при которых происходит замена атомов водорода на различные атомы и группы – реакции замещения 43

Реакции замещения водорода Алканы Химические свойства в алканах носят цепной характер и протекают по радикальному механизму (SR) 44
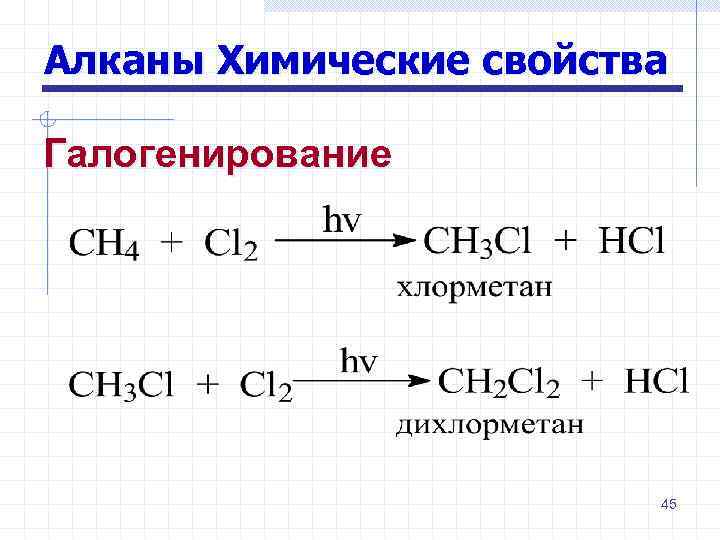
Алканы Химические свойства Галогенирование 45
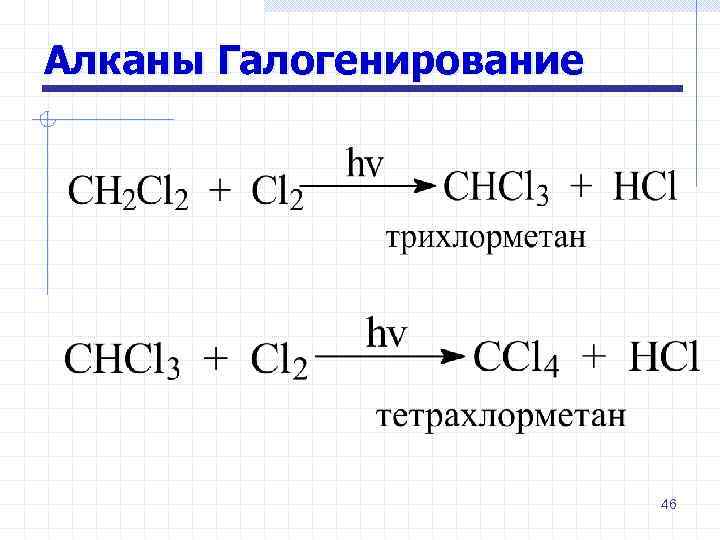
Алканы Галогенирование 46

Алканы Галогенирование Механизм реакции I. Инициирование: 47
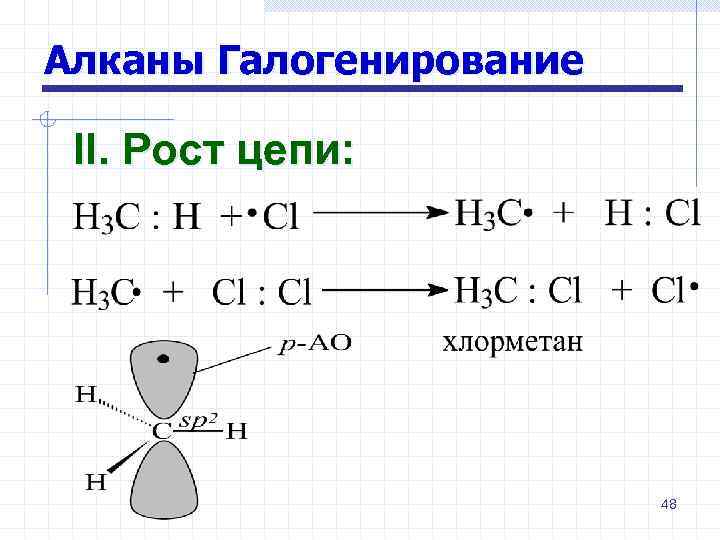
Алканы Галогенирование II. Рост цепи: 48
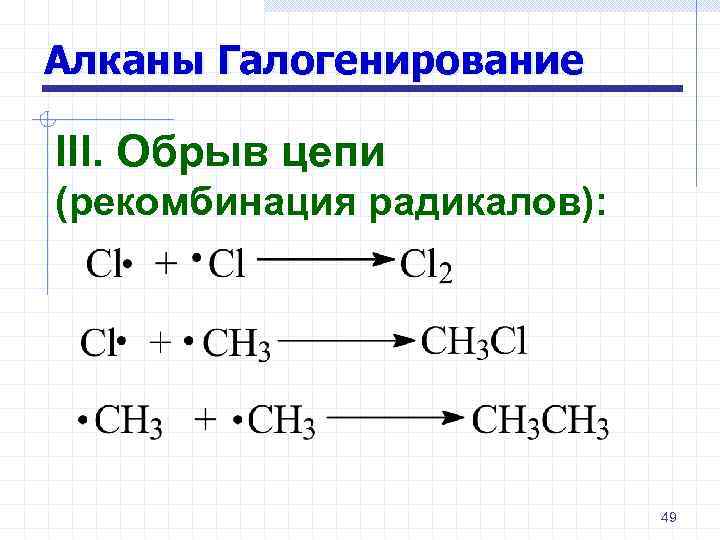
Алканы Галогенирование III. Обрыв цепи (рекомбинация радикалов): 49

Алканы Галогенирование • Галогенирование начинается только под действием инициатора радикальных реакций (УФ -облучение, радикальные реагенты, нагревание) 50

Алканы Галогенирование Реакционная способность в ряду галогенов уменьшается в ряду: F 2 > Cl 2 > Br 2 > I 2 51

Алканы Галогенирование • Галогенирование под действием фтора и хлора может выйти из под контроля и приобрести взрывной характер 52

Алканы SR • Легкость образования алкильных радикалов и их относительная устойчивость уменьшаются в следующем порядке: 53

Алканы SR вторичный метильный первичный третичный Чем стабильнее свободный радикал, тем легче и быстрее 54

Алканы Галогенирование 55

Алканы Химические свойства Сульфохлорирование (УФ-облучение, пероксиды) С 10 H 22 + SO 2 + Cl 2 C 10 H 21 SO 2 Cl + HCl декан сульфонилхлорид декана 56

Алканы Сульфохлорирование C 10 H 21 SO 2 Cl + 2 Na. OH C 10 H 21 SO 3 Na + Na. Cl + H 2 O алкилсульфонат (моющее средство) 57

Алканы Химические свойства С 10 H 22 + SO 2 + ½ О 2 C 10 H 21 SO 3 Н декансульфоновая кислота Сульфоокисление (УФ-облучение, пероксиды) 58

Алканы Химические свойства Нитрование . ) (нитроний-радикал NO 2 жидкофазное нитрование Реакция Коновалова (1888) 59
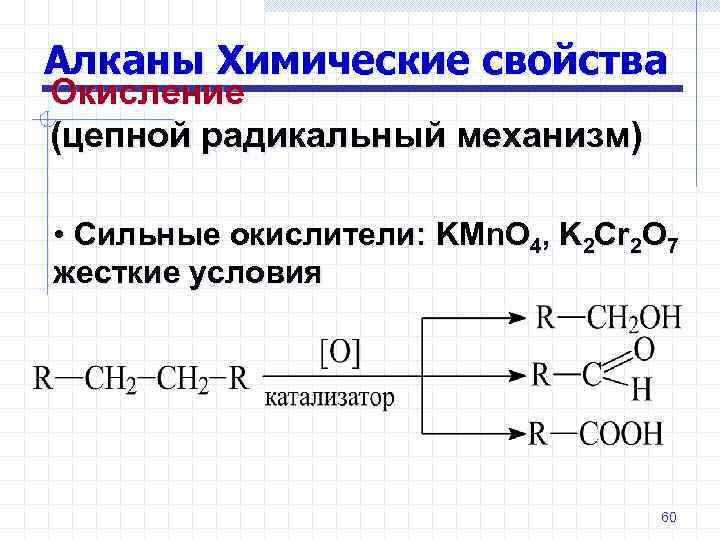
Алканы Химические свойства Окисление (цепной радикальный механизм) • Сильные окислители: KMn. O 4, K 2 Cr 2 O 7 жесткие условия 60

Алканы Окисление • Окисление в жидкой фазе – производство уксусной кислоты из бутана: 61

Алканы Окисление CH 4 + H 2 O CO + 3 H 2 CH 4 + ½O 2 CO + H 2 CH 4 + CO 2 2 CO + 2 H 2 CH 4 + 2 O 2 CO 2 + H 2 O + 890 к. Дж/моль (использование в энергетических целях) 62

Изомеризация Алканы Изомеризация (ионная цепная реакция) перестройка углеродного скелета молекулы • Нагревание с кислотами Льюиса (Аl. Cl 3, Al. Br 3), каталитических количеств алкена (R-CH=CH 2) и воды 63
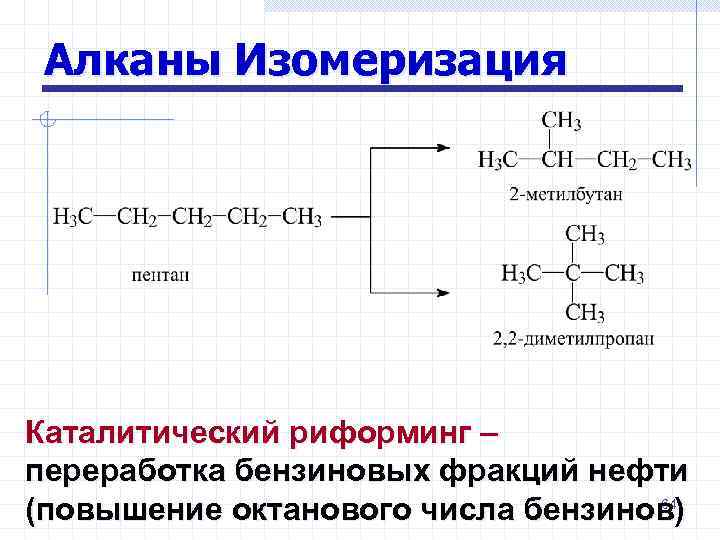
Алканы Изомеризация Каталитический риформинг – переработка бензиновых фракций нефти 64 (повышение октанового числа бензинов)

Дегидрирование - Алканы Химические свойства обратимый высокотемпературный каталитический процесс 65

Алканы Дегидрирование Температура: • при катализе оксидами – 50– 650°С; • при катализе металлами – около 300°С Катализаторы: Cr 2 O 2 Fe 2 O 3 Zn. O Pt Pd Ni Fe 66

Алканы Дегидрирование • Низшие алканы бутан превращаются в алкены: бутен-1 бутен-2 бутадиен-1, 3 67

Алканы Дегидрирование • Алканы, содержащие пять (но не более) атомов углерода в цепи подвергаются дегидроциклизации: 2, 4 -диметилпентан 1, 3 -диметилциклопентан 68

Алканы Дегидрирование • Алканы, содержащие шесть и более атомов углерода в цепи подвергаются дегидроциклизации и дальнейшему дегидрированию с образованием ароматического кольца 69
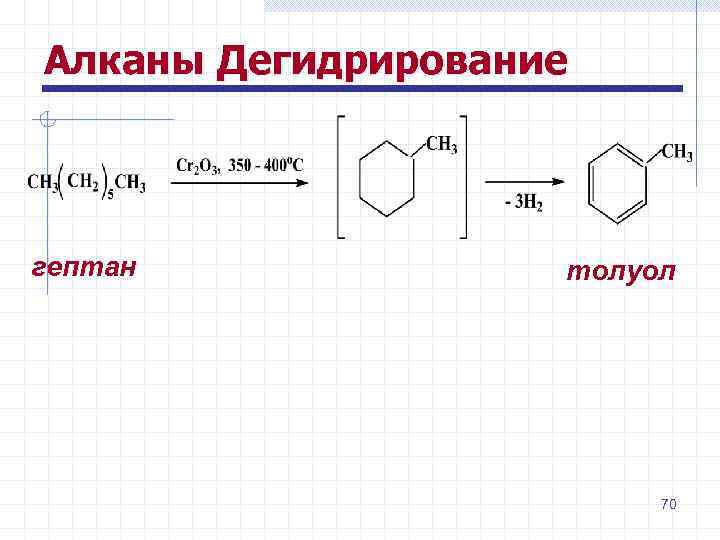
Алканы Дегидрирование гептан толуол 70

Алканы Крекинг - термическое расщепление углеводородов нефти Температура – 450– 650°С; Катализаторы – Al 2 O 3, Аl. Сl 3, Сr 2 О 3 71

Алканы Крекинг - важнейший метод химической переработки нефти • Крекинг сопровождается разрывом связей С-С и С-Н, что приводит к образованию смеси насыщенных и ненасыщенных углеводородов с меньшей длиной цепи 72

Алканы Крекинг • Параллельно протекают реакции изомеризации, ароматизации, циклизации, полимеризации, алкилирования • Состав продуктов крекинга зависит от исходного сырья, типа катализатора и технологического режима 73

Алканы Крекинг • Наиболее перспективны методы каталитического крекинга (алюмосиликаты), при котором образуются устойчивые третичные карбокатионы (сильно разветвленные алканы). Этот процесс приводит к получению бензинов с более высоким октановым числом 74

Алканы Крекинг CH 3 + H 2 C CH 2 H 2 C CH 3 CH 2 CH 3 CH CH 3 + CH 4 CH CH 2 CH 3 + H 3 C H 2 C CH CH CH 2 + 2 H 2 H 3 C CH 3 + CH 4 + CH 3 2 HC CH + 3 H 2 CH CH CH 3 + H 2 75

Алканы.ppt