Реакционная способность органических соединений Связь


Реакционная способность органических соединений Связь структура – свойства. Реакционная способность молекулы определяется прежде всего распределением и подвижностью электронов, т. е. структурой реагента либо промежуточного продукта реакции

Влияние строения на реакционную способность • эффект поля • резонансный (или мезомерный) эффект • пространственные эффекты.
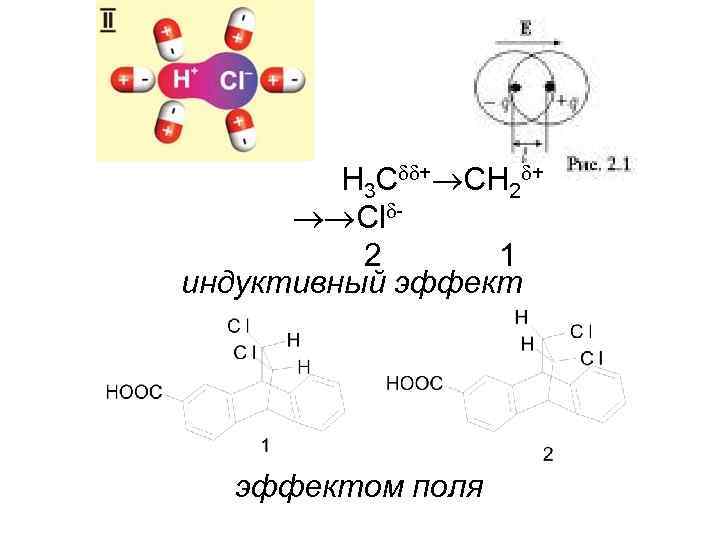
H 3 C + CH 2 + Cl 2 1 индуктивный эффектом поля

Механизмы органических реакций. • Ковалентная связь между атомами А и В может быть разорвана, во первых, гомолитически электронная пара делится между атомами, частицы А и В получают по одному электрону и становятся свободными радикалами: А В А + В

Механизмы органических реакций • Во вторых, гетеролитически, с образованием различных электронных структур ионов, в которых атом А лишился электрона и обрел положительный заряд (катион), а атом В захватил оба общих до того электрона и приобрел отрицательный заряд (анион). А В А+ + : В-

Механизмы органических реакций • Свободнорадикальные реакции: • 1) инициируются светом, высокой температурй или свободными радикалами, вводимыми или образующимися в реакции при разложении других веществ; • 2) тормозятся веществами, легко реагирующими со свободными радикалами, например, фенолы или амины; • 3) проходят в неполярных растворителях или в паровой фазе; • 4) часто имеют автокаталитический характер и индукционный период в начале реакции; • 5) в кинетическом отношении являются цепными.

Механизмы органических реакций • Ионные реакции • 1) катализируются кислотами или основаниями, свет и свободные радикалы не влияют на ход реакции; • 2) не подвержены влиянию акцепторов свободных радикалов; • 3) на ход реакции оказывает влияние природа растворителя; • 4) редко протекают в паровой фазе; • 5) кинетически являются большей частью реакциями первого или второго порядка.

Классификация органических реакций по характеру химических превращений. • 1. Реакции без изменения углеродного скелета • а) замещения • Реакции замещения могут протекать по ионному или радикальному механизму. Их обозначение: S (substitutio лат. ) замещение, SN – нуклеофильное замещение, SЕ – электрофильное замещение, SR радикальное замещение. • A B + C A + B C (SN), • A B + C+ A+ + B C (SE), • A B + C A + B C (SR)

Классификация органических реакций по характеру химических превращений. • 1. Реакции без изменения углеродного скелета • б) присоединения • Реакции присоединения также протекают или по ионному, или по радикальному механизму (АE, AN, AR): • А=В + C A B C (АN), • A=B + C+ A+ B C (АE), • A=B + C A B C (АR),

Классификация органических реакций по характеру химических превращений. • 1. Реакции без изменения углеродного скелета • в) элиминирования (отщепления) • X А В Y A=B + X Y • г) изомеризации • A=B C A B=C
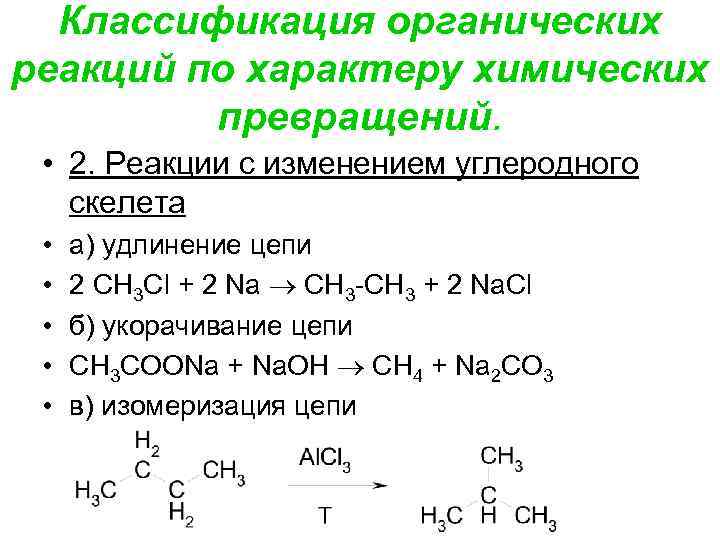
Классификация органических реакций по характеру химических превращений. • 2. Реакции с изменением углеродного скелета • а) удлинение цепи • 2 CH 3 Cl + 2 Na CH 3 + 2 Na. Cl • б) укорачивание цепи • CH 3 COONa + Na. OH CH 4 + Na 2 CO 3 • в) изомеризация цепи
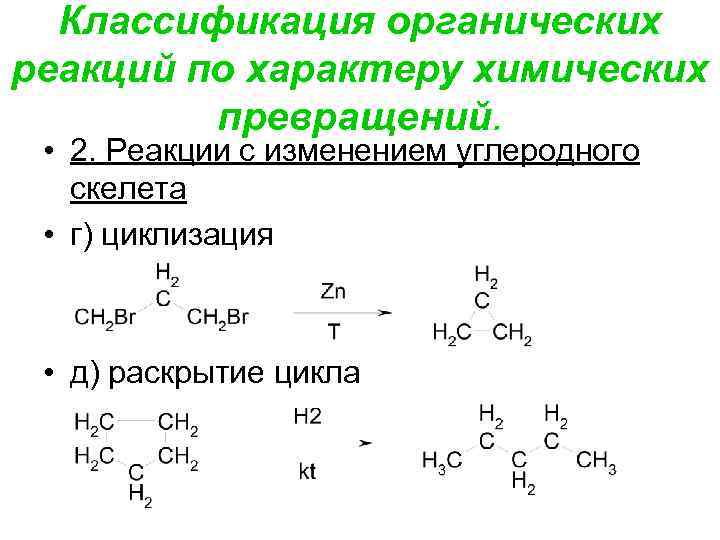
Классификация органических реакций по характеру химических превращений. • 2. Реакции с изменением углеродного скелета • г) циклизация • д) раскрытие цикла
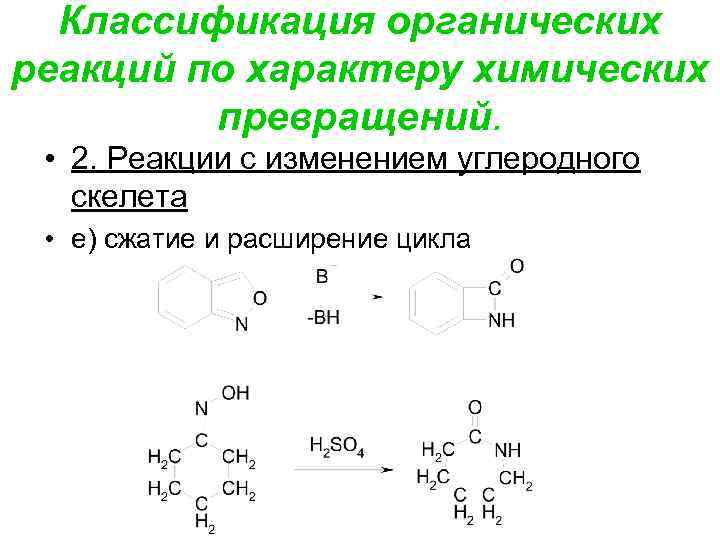
Классификация органических реакций по характеру химических превращений. • 2. Реакции с изменением углеродного скелета • е) сжатие и расширение цикла

Кислоты и основания в органической химии По Бренстеду Лоури, кислоты представляют собой вещества, способные отдавать протон, а основания вещества, присоединяющие протон. Согласно Бренстеду Лоури, для того чтобы быть кислотой, соединение должно иметь водород. За редким исключением почти все органические соединения отвечают этому условию. Поэтому все они являются потенциальными бренстедовскими кислотами. А вот сила этих кислот определяется конкретной структурой соединений.

Кислоты и основания в органической химии Степень кислотности определяется главным образом характером атома, с которым связан водород. Элемент и связанный с ним атом водорода называют кислотным центром. Кислотность соединения будет определяться как характером связи в кислотном центре (элемент водород) (статический фактор), так и способностью атома удерживать электронную пару после ухода иона водорода (динамический фактор). Способность удерживать электронную пару зависит от различных факторов, в том числе от электроотрицательности атомов и их размера. Таким образом, в периодах таблицы Менделеева кислотность возрастает с увеличением электроотрицательности. • Кислотность: Н СН 3 < Н NH 2 < Н ОН < Н F, H SH < H CI. • В группах кислотность возрастает с увеличением размеров атома: • Н F < Н С 1 < Н Вг < Н I, Н OH < H Se. H. По природе кислотного центра большинство бренстедовских кислот может быть представлено четырьмя типами: ОН кислоты (карбоновые кислоты, фенолы, спирты), SH кислоты (тиолы), NH кислоты (амины, амиды, имиды), СН кислоты (углеводороды и их производные).

Кислоты и основания в органической химии По Льюису, кислотные и основные свойства органических соединений оцениваются по способности принимать или предоставлять электронную пару с последующим образованием связи. Атом, принимающий электронную пару, является акцептором электронов, а соединение, содержащее такой атом, следует отнести к кислотам. Атом, предоставляющий электронную пару, является донором электронов, а соединение, содержащее такой атом, основанием. По сравнению с протонной теорией Бренстеда теория Льюиса носит более общий характер и охватывает более широкий круг соединений. При взаимодействии кислот и оснований Льюиса образуются донорно акцепторные (кислотно основные) комплексы самой различной природы.

Кислоты и основания в органической химии Кислотно основные отношения можно охарактеризовать как взаимодействие частиц, содержащих заполненную и вакантную орбитали. Легкость протекания кислотно основных реакций зависит не только от силы кислоты и основания, но и от другого свойства, учитывающего соответствие другу взаимодействующих (граничных) орбиталей. Учет этого свойства позволил Пирсону конкретизировать свойства льюисовских кислот и оснований, введя представление о жестких и мягких кислотах и основаниях (принцип ЖМКО или принцип Пирсона).

Кислоты и основания в органической химии • Жесткие кислоты Льюиса, в которых акцепторные атомы малы по размеру, обладают большим положительным зарядом, большой электроотрицательностью и низкой поляризуемостью. Молекулярная орбиталь жестких кислот, на которую переходят электроны донора, имеет низкий уровень энергии. • Мягкие кислоты - кислоты Льюиса, содержащие акцепторные атомы большого размера с малым положительным зарядом, с небольшой электроотрицательностью и высокой поляризуемостью. Молекулярная орбиталь мягких кислот, принимающая электроны донора, имеет высокий уровень энергии.

Кислоты и основания в органической химии • Жесткие основания - донорные частицы, в которых атомы доноры имеют высокую электроотрицательность и низкую поляризуемость. Валентные электроны удерживаются прочно, продукт окисляется с трудом. Орбиталь, пара электронов которой передается акцептору, имеет низкий уровень энергии. Донорными атомами в жестких основаниях могут быть кислород, азот, фтор, хлор. • Мягкие основания - донорные частицы, в которых атомы доноры имеют низкую электроотрицательность и высокую поляризуемость, они легко окисляются; валентные электроны удерживаются слабо. Орбиталь, пара электронов которой передается акцептору, обладает высоким уровнем энергии. Донорными атомами в мягких основаниях выступа ют атомы углерода, серы, йода. • Понятия жесткие и мягкие кислоты и основания неравноценны понятиям сильные и слабые кислоты и основания.

Кислоты и основания в органической химии Кислоты Основания Жесткие Мягкие Жесткие Мягкие H+, Li+, Na+, K+, Ag+, Cu+, Hg 2+, HO-, RO-, F-, Cl-, RSH, R 2 S, J-, Mg 2+, Ca 2+, Al 3+, RS+, J+, Br+, Pt 2+, RCOO-, NO 3 -, H-, R 3 C-, R 2 C=CR 2, Cr 3+, Fe 3+, BF 3, BH 3, карбены NH 3, RNH 2, H 2 O, C 6 H 6, R 3 P, (RO)3 P B(OR)3, Al. R 3, ROH, SO 42 -, CO 32 - Al. Cl 3, SO 3, , R 2 O, NR 2 -, NH 2 - RC+O, CO 2, RSO 2+ Промежуточные Cu 2+, Fe 2+, Zn 2+, SO 2, R 3 C+, C 6 H 5+, Br-, C 6 H 5 NH 2, NO 2 -, C 5 H 5 N NO+
органическая-химия-chem3.ppt
- Количество слайдов: 20

