алкены, алкины.ppt
- Количество слайдов: 44

Реакционная способность алкенов, алкадиенов и алкинов
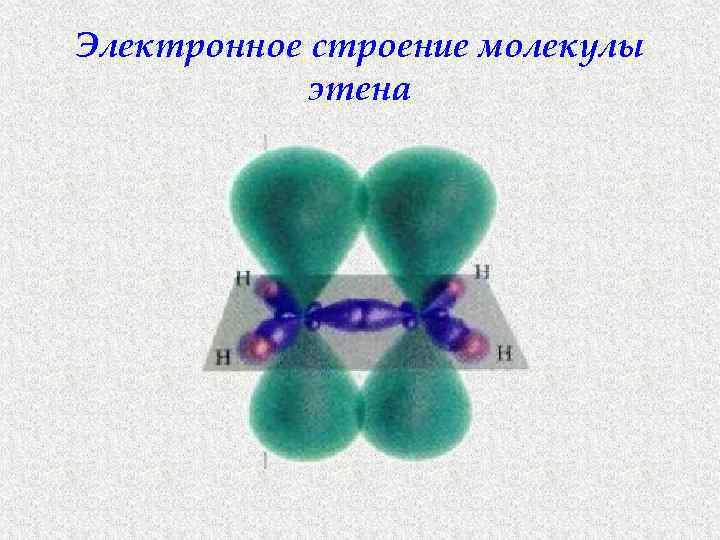
Электронное строение молекулы этена
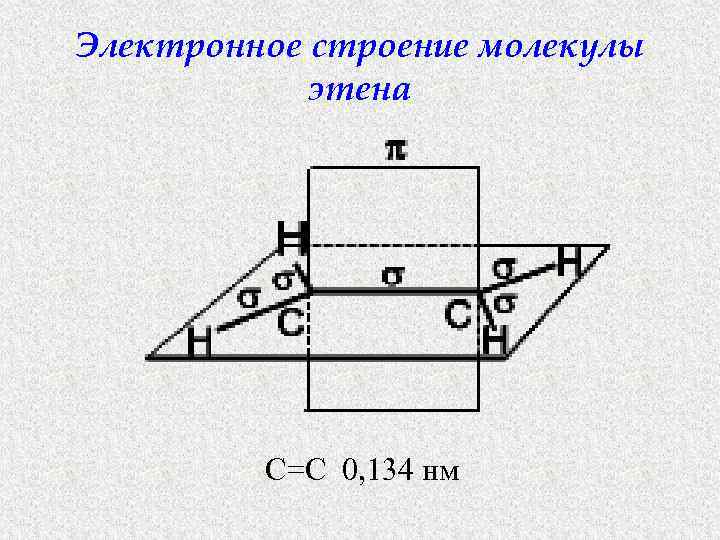
Электронное строение молекулы этена С=С 0, 134 нм
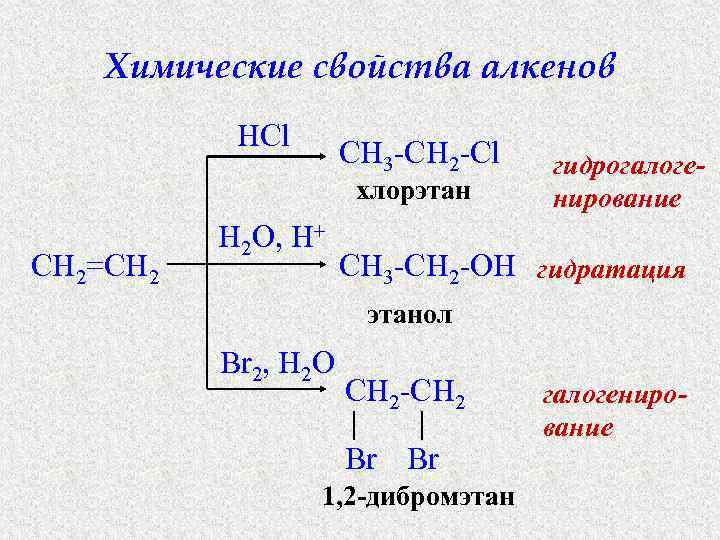
Химические свойства алкенов HCl CH 3 -CH 2 -Cl хлорэтан CH 2=CH 2 H 2 O, H+ гидрогалогенирование CH 3 -CH 2 -OH гидратация этанол Br 2, H 2 O CH 2 -CH 2 Br Br 1, 2 -дибромэтан галогенирование
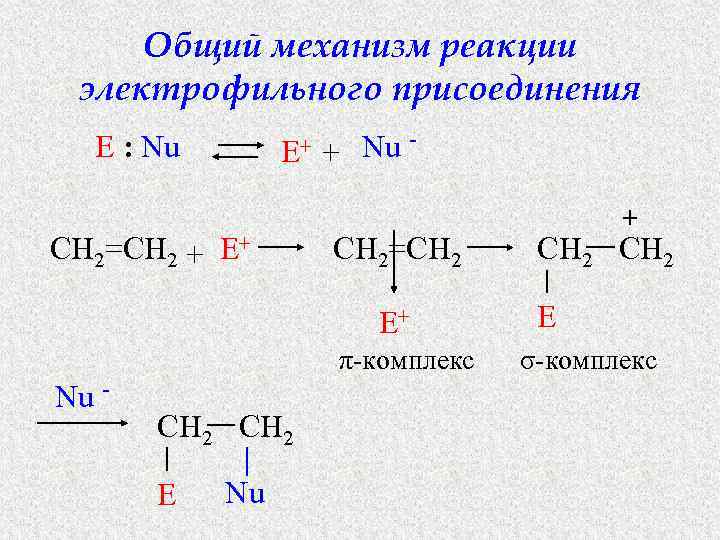
Общий механизм реакции электрофильного присоединения E : Nu E+ CH 2=CH 2 + E+ Nu + CH 2=CH 2 E+ Nu - π-комплекс CH 2 E Nu + CH 2 E σ-комплекс

Общий механизм реакции электрофильного присоединения CH 2 + CH 2 - + Nu : E
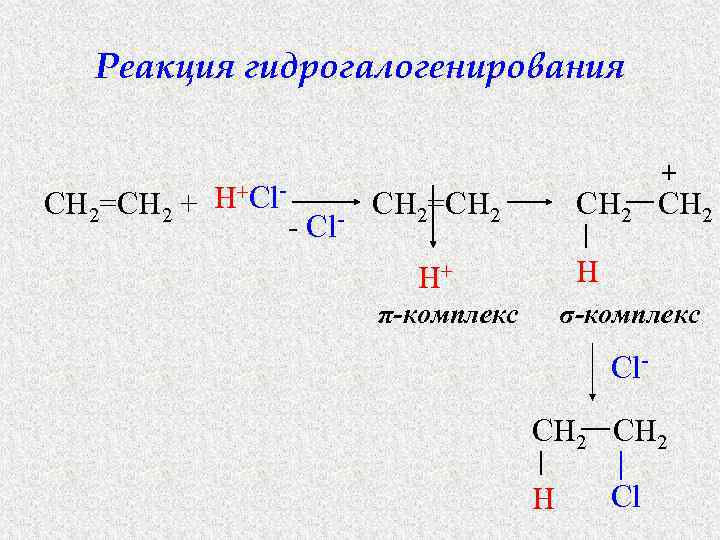
Реакция гидрогалогенирования H+Cl. CH 2=CH 2 + - Cl- + CH 2=CH 2 H H+ π-комплекс σ-комплекс Cl. CH 2 H Cl
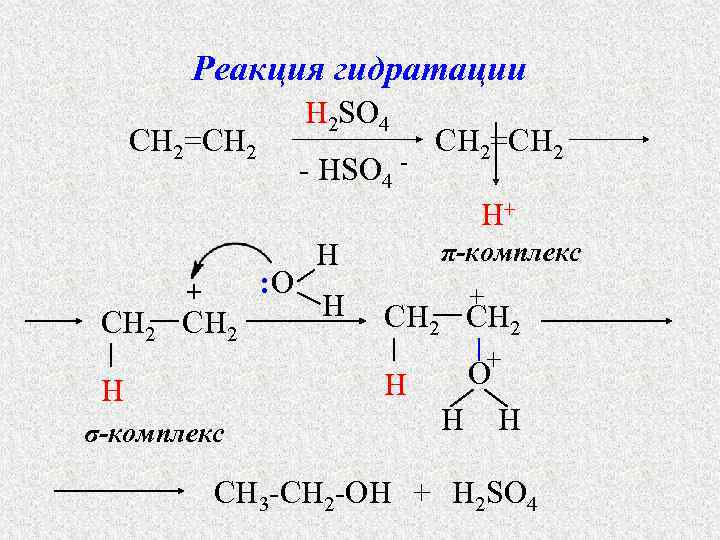
Реакция гидратации H 2 SO 4 CH 2=CH 2 - HSO 4 - CH 2=CH 2 H+ : O + CH 2 π-комплекс H H + CH 2 H H σ-комплекс O+ H H CH 3 -CH 2 -OH + H 2 SO 4
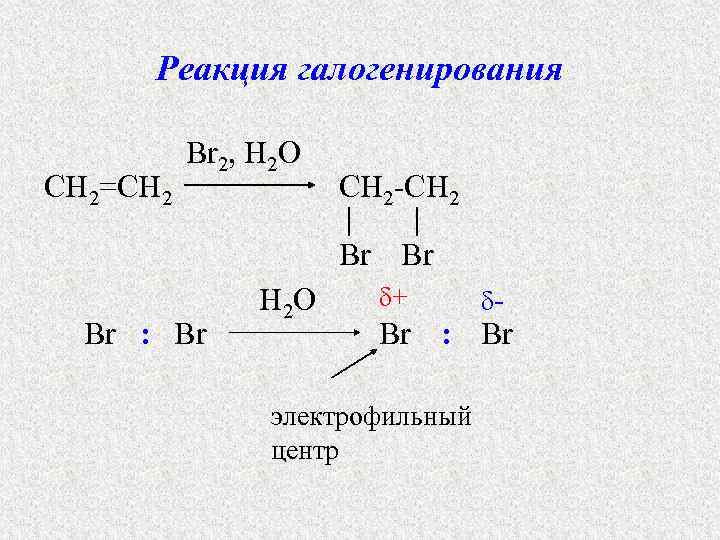
Реакция галогенирования CH 2=CH 2 Br 2, H 2 O CH 2 -CH 2 Br Br Br : Br H 2 O δ+ δ- Br : Br электрофильный центр
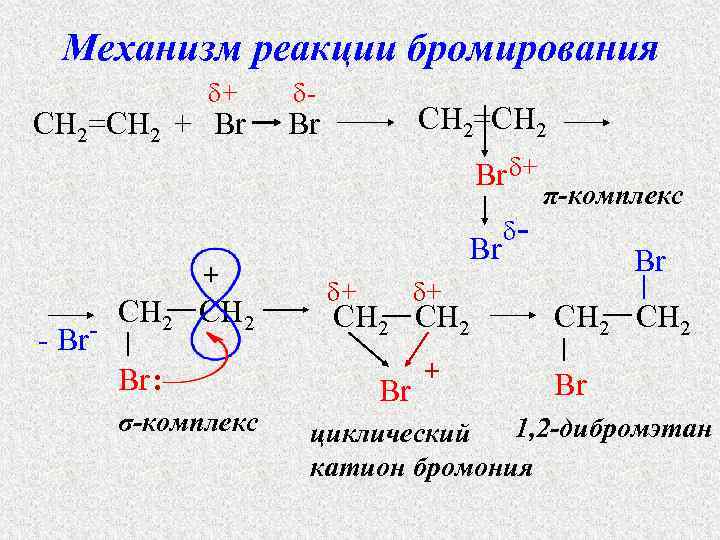
Механизм реакции бромирования δ+ CH 2=CH 2 + Br δ- CH 2=CH 2 Br Br δ+ + - Br- CH 2 Br : σ-комплекс Br δ+ δ+ CH 2 Br + δ- π-комплекс Br CH 2 Br 1, 2 -дибромэтан циклический катион бромония
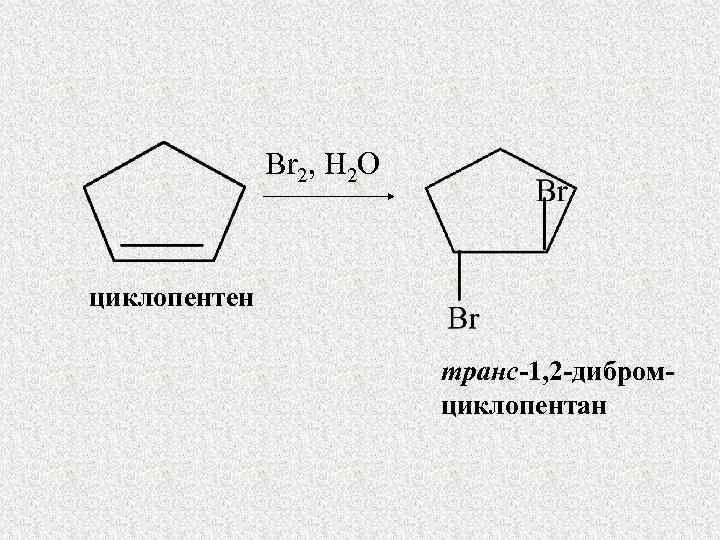
Br 2, H 2 O циклопентен транс-1, 2 -дибромциклопентан

Признаки качественных реакций • выпадение осадка • растворение осадка • изменение окраски • выделение пузырьков газа • появление характерного запаха
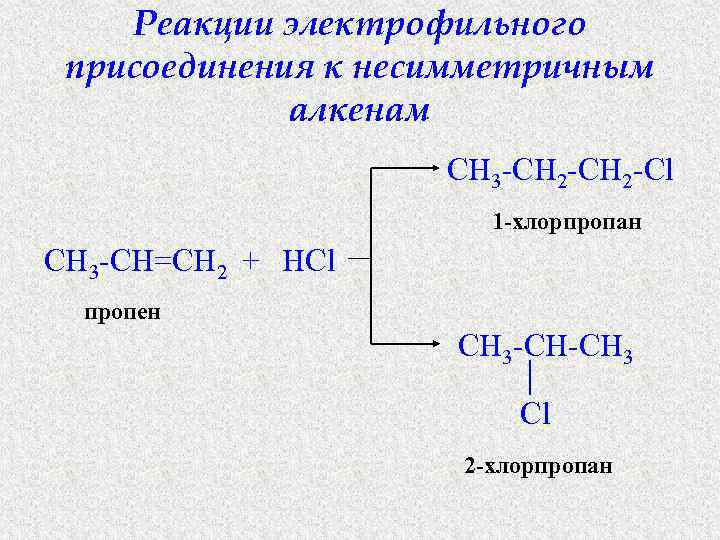
Реакции электрофильного присоединения к несимметричным алкенам CH 3 -CH 2 -Cl 1 -хлорпропан CH 3 -CH=CH 2 + HCl пропен CH 3 -CH-CH 3 Cl 2 -хлорпропан

Реакции электрофильного присоединения к несимметричным алкенам Правило Марковникова: При присоединении реагентов типа H+X- (HCl, HBr, HOH) к несимметричным алкенам протон водорода (H+) присоединяется к более гидрогенизированному атому углерода при двойной связи

Реакции электрофильного присоединения к несимметричным алкенам Статический фактор – это распределение электронной плотности в нереагирующей молекуле δ+ δ- CH 3 CH=CH 2 sp 3 sp 2

Реакции электрофильного присоединения к несимметричным алкенам Динамический фактор – это сравнение стабильности промежуточных частиц (карбокатионов). Чем стабильнее частица, тем больше вероятность ее образования.
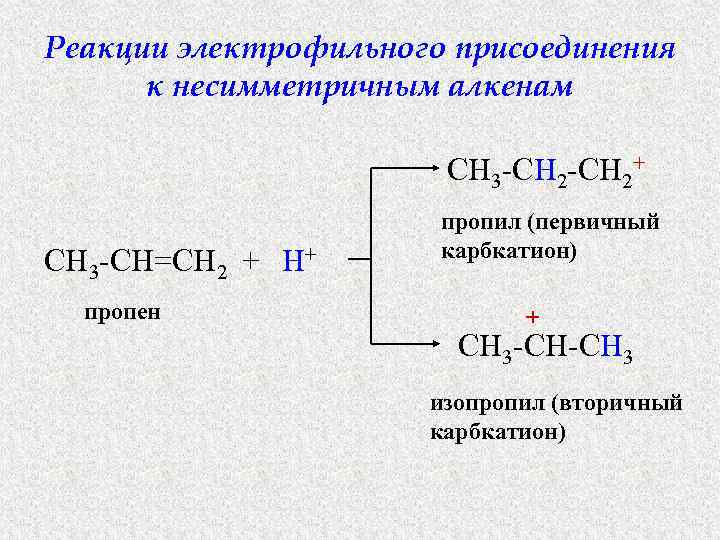
Реакции электрофильного присоединения к несимметричным алкенам CH 3 -CH 2+ CH 3 -CH=CH 2 + H+ пропен пропил (первичный карбкатион) + CH 3 -CH-CH 3 изопропил (вторичный карбкатион)
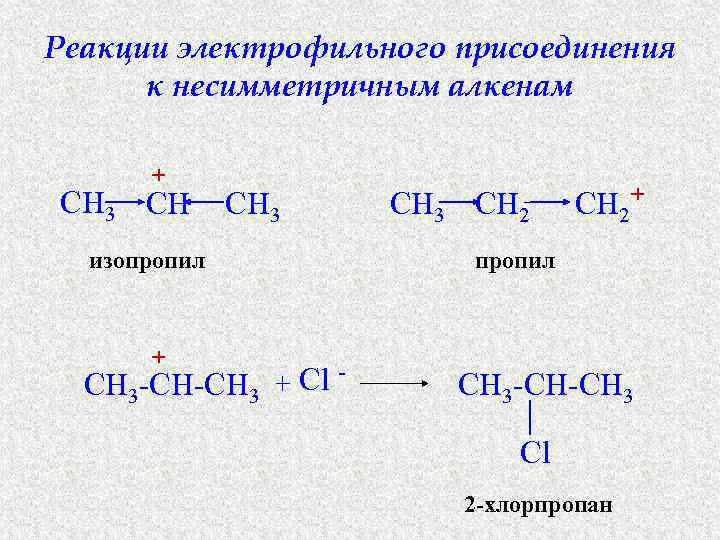
Реакции электрофильного присоединения к несимметричным алкенам + CH 3 CH CH 3 изопропил + Cl CH 3 -CH-CH 3 + CH 3 CH 2 + пропил CH 3 -CH-CH 3 Cl 2 -хлорпропан

Реакции электрофильного присоединения к несимметричным алкенам Современная интерпретация правила Марковникова: При присоединении реагентов типа H+X- (HCl, HBr, HOH) к несимметричным алкенам реакция протекает через образование наиболее стабильного карбкатиона.
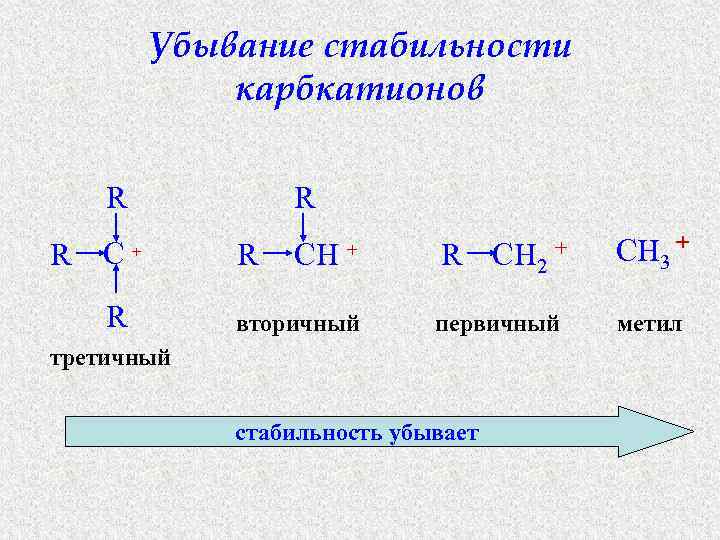
Убывание стабильности карбкатионов R R C R + R R CH + вторичный R CH 2 + первичный третичный стабильность убывает CH 3 + метил
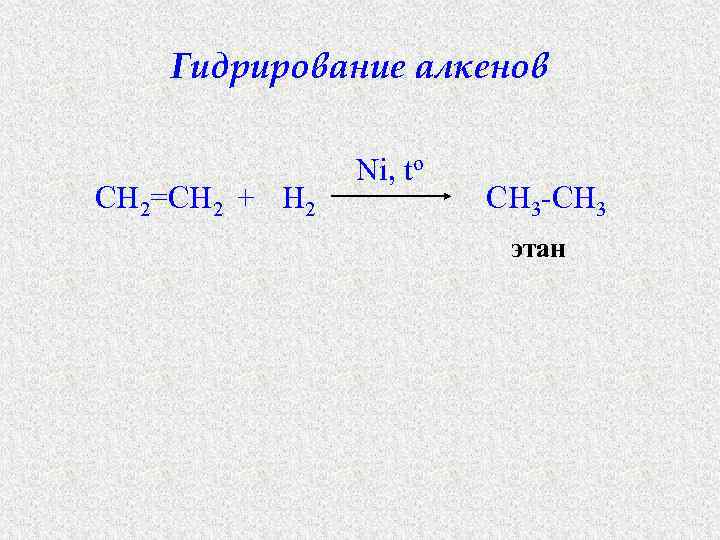
Гидрирование алкенов CH 2=CH 2 + H 2 Ni, to CH 3 -CH 3 этан
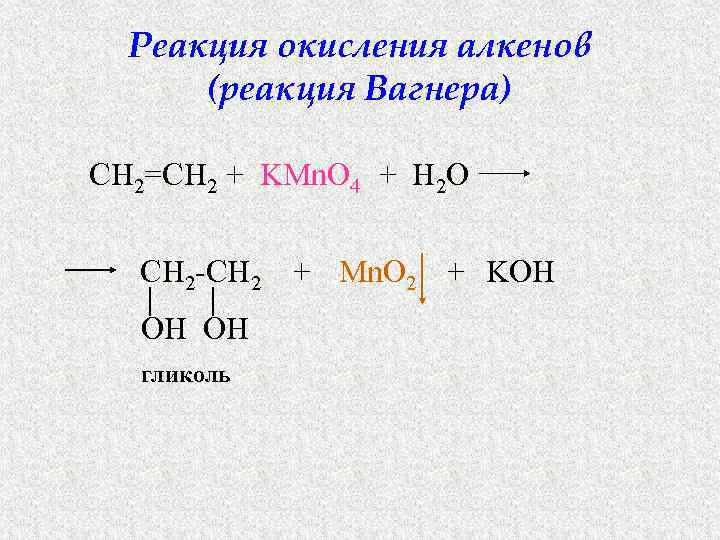
Реакция окисления алкенов (реакция Вагнера) CH 2=CH 2 + KMn. O 4 + H 2 O CH 2 -CH 2 OH OH гликоль + Mn. O 2 + KOH
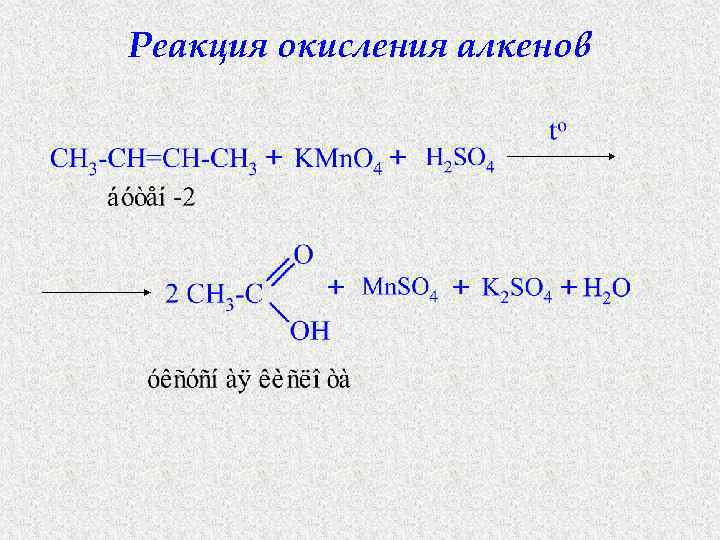
Реакция окисления алкенов
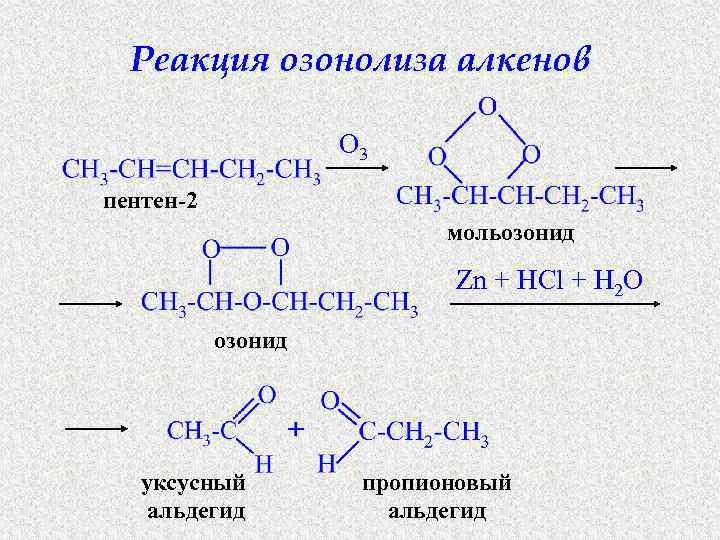
Реакция озонолиза алкенов O 3 пентен-2 мольозонид Zn + HCl + H 2 O озонид уксусный альдегид пропионовый альдегид
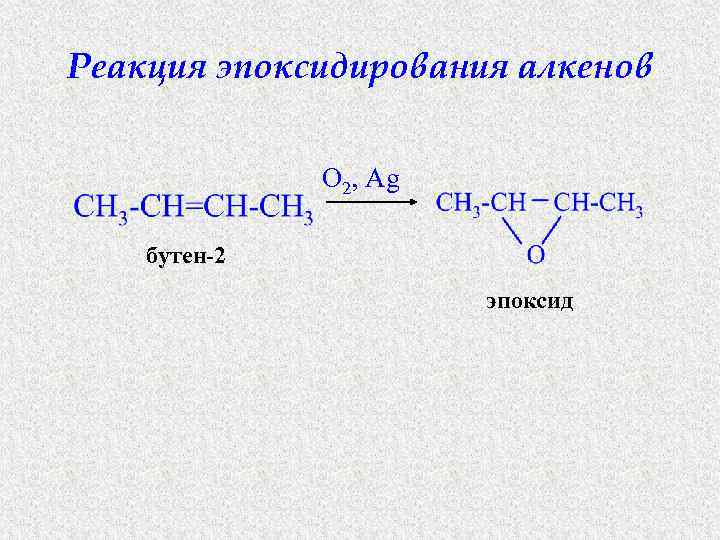
Реакция эпоксидирования алкенов O 2, Ag бутен-2 эпоксид
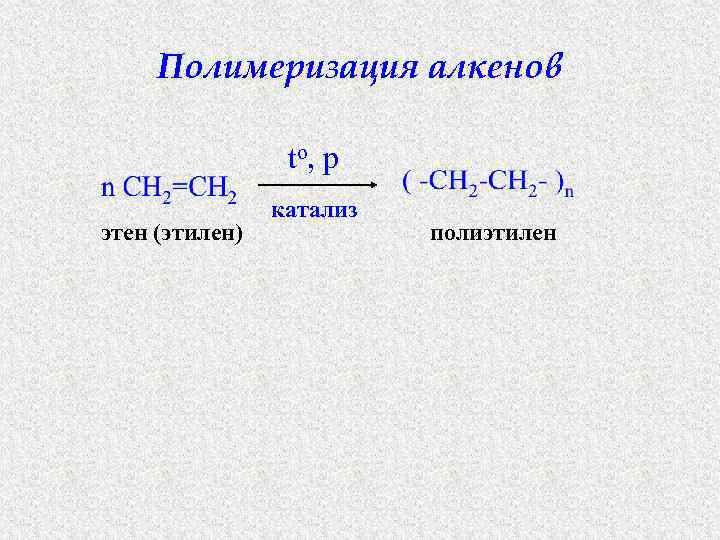
Полимеризация алкенов to, p этен (этилен) катализ полиэтилен
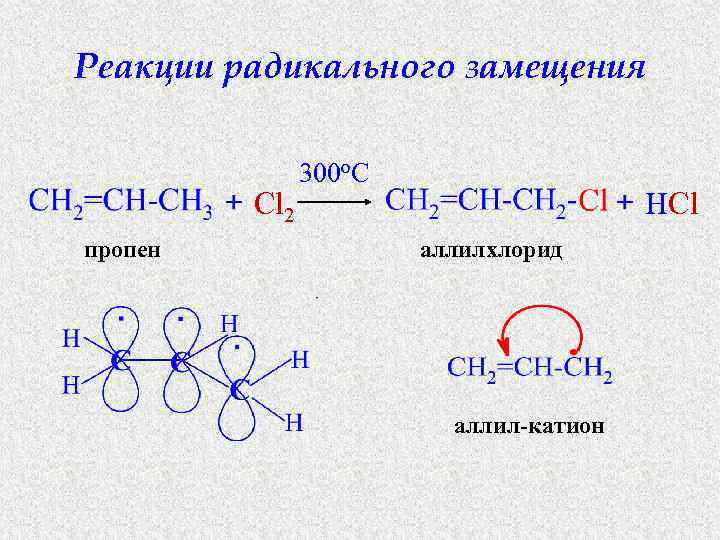
Реакции радикального замещения Cl 2 пропен 300 o. C HCl аллилхлорид аллил-катион

Синтезы на основе этилена

Реакционная способность алкинов
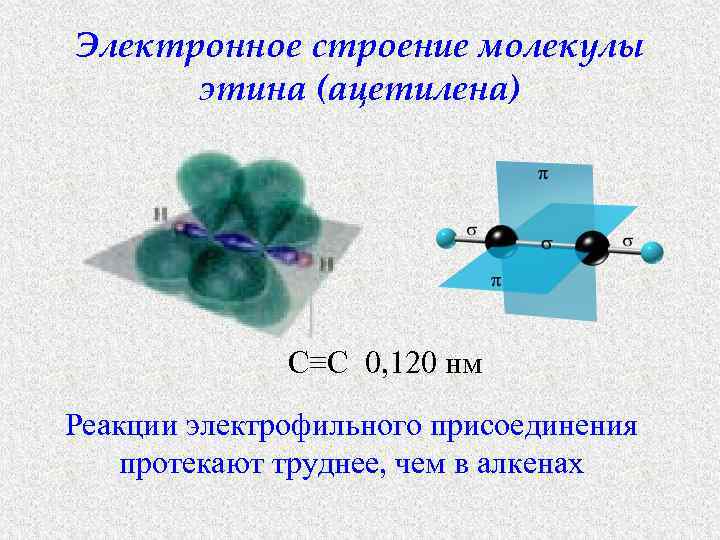
Электронное строение молекулы этина (ацетилена) С≡С 0, 120 нм Реакции электрофильного присоединения протекают труднее, чем в алкенах
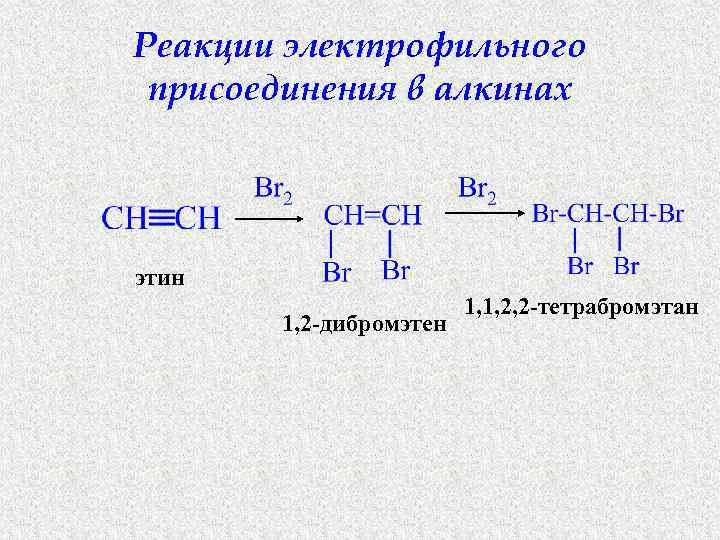
Реакции электрофильного присоединения в алкинах этин 1, 2 -дибромэтен 1, 1, 2, 2 -тетрабромэтан
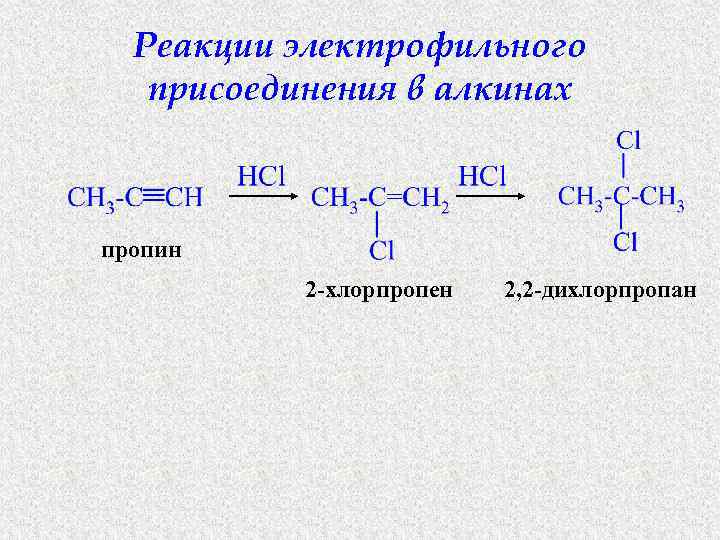
Реакции электрофильного присоединения в алкинах пропин 2 -хлорпропен 2, 2 -дихлорпропан
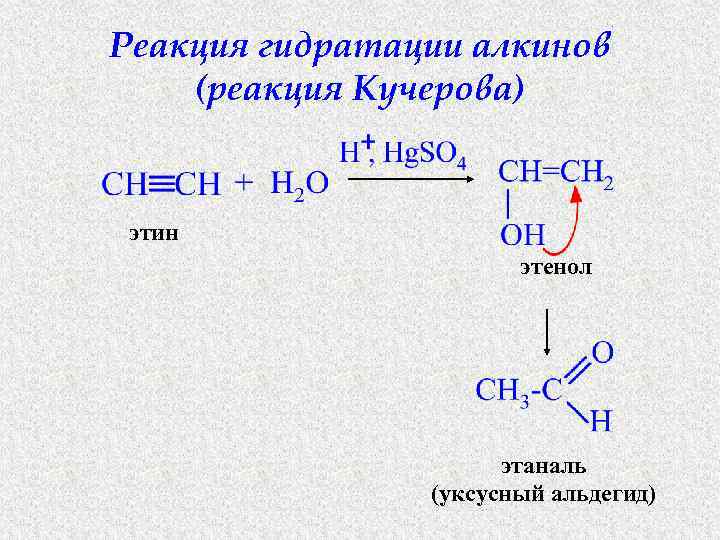
Реакция гидратации алкинов (реакция Кучерова) этин этенол этаналь (уксусный альдегид)
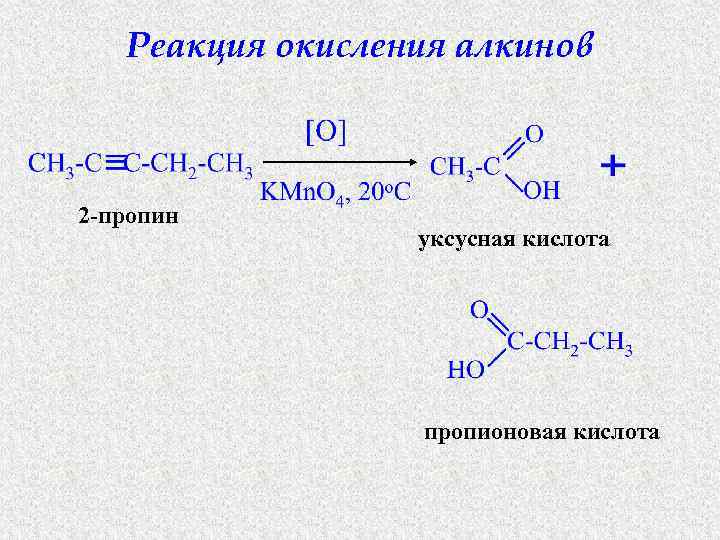
Реакция окисления алкинов 2 -пропин уксусная кислота пропионовая кислота
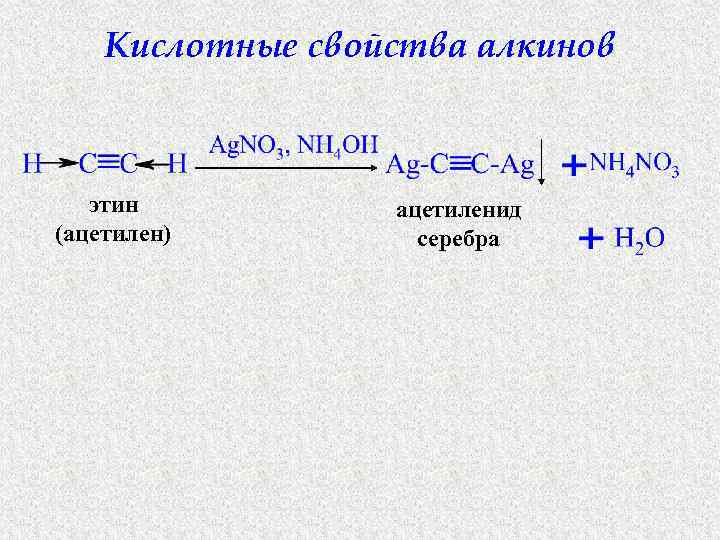
Кислотные свойства алкинов этин (ацетилен) ацетиленид серебра
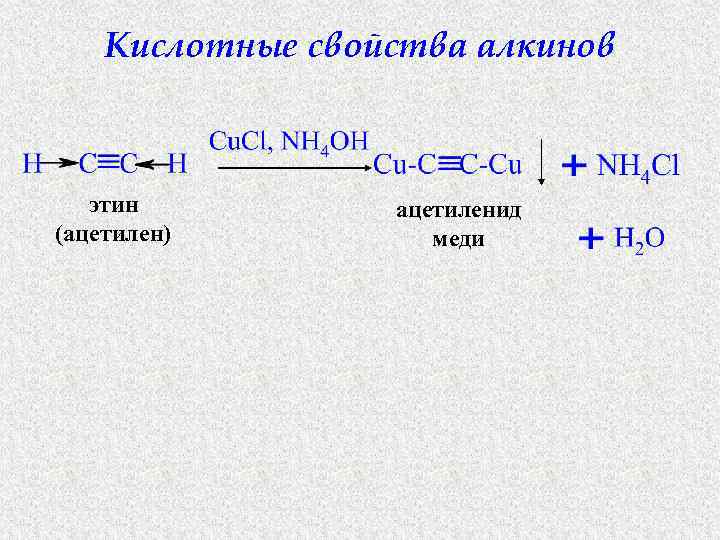
Кислотные свойства алкинов этин (ацетилен) ацетиленид меди
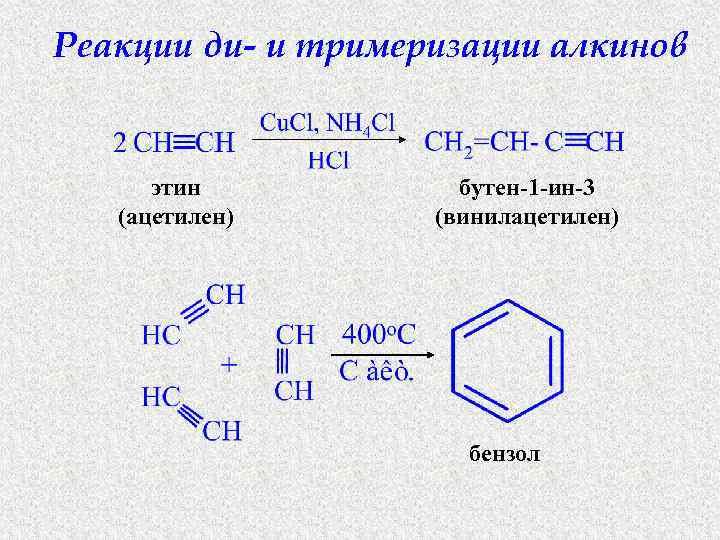
Реакции ди- и тримеризации алкинов этин (ацетилен) бутен-1 -ин-3 (винилацетилен) бензол
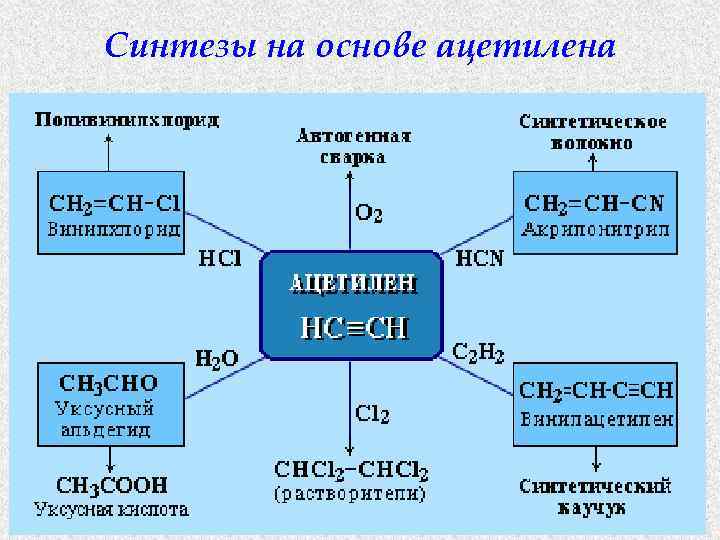
Синтезы на основе ацетилена

Реакционная способность алкадиенов
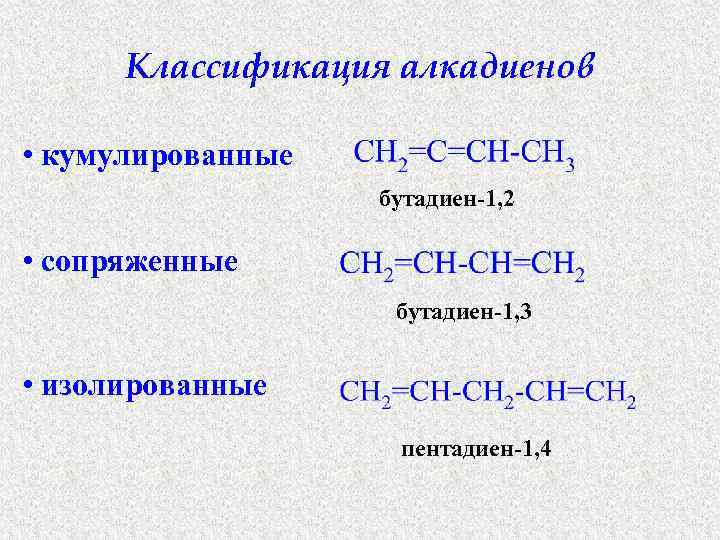
Классификация алкадиенов • кумулированные бутадиен-1, 2 • сопряженные бутадиен-1, 3 • изолированные пентадиен-1, 4
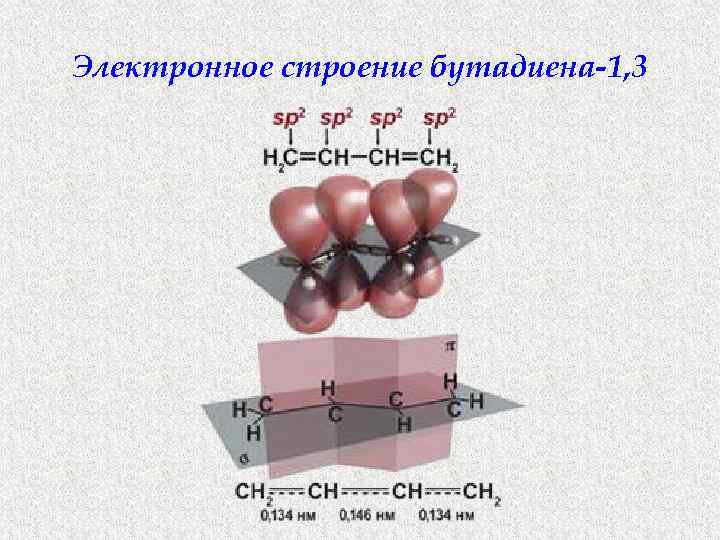
Электронное строение бутадиена-1, 3
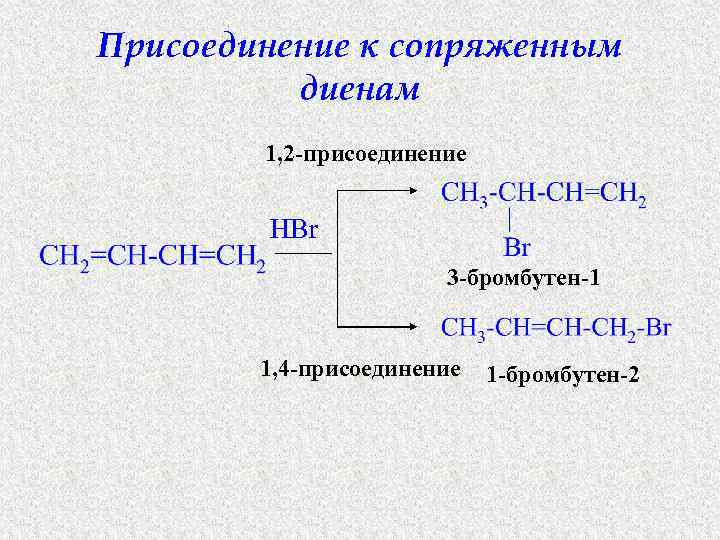
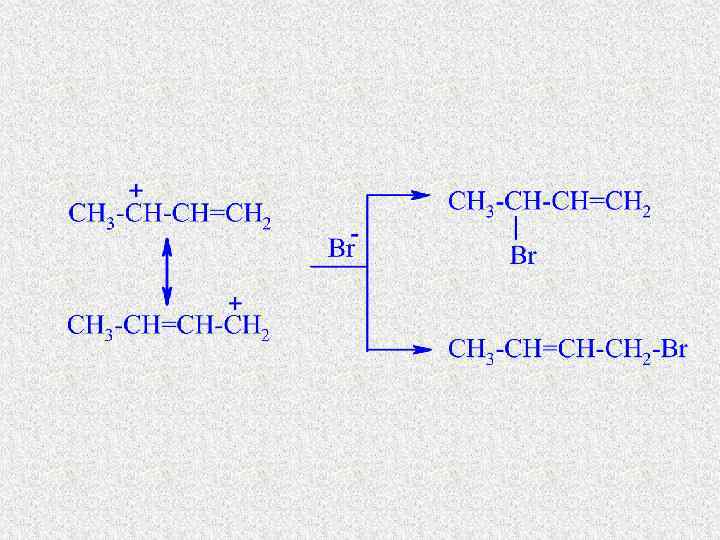
Присоединение к сопряженным диенам 1, 2 -присоединение HBr 3 -бромбутен-1 1, 4 -присоединение 1 -бромбутен-2
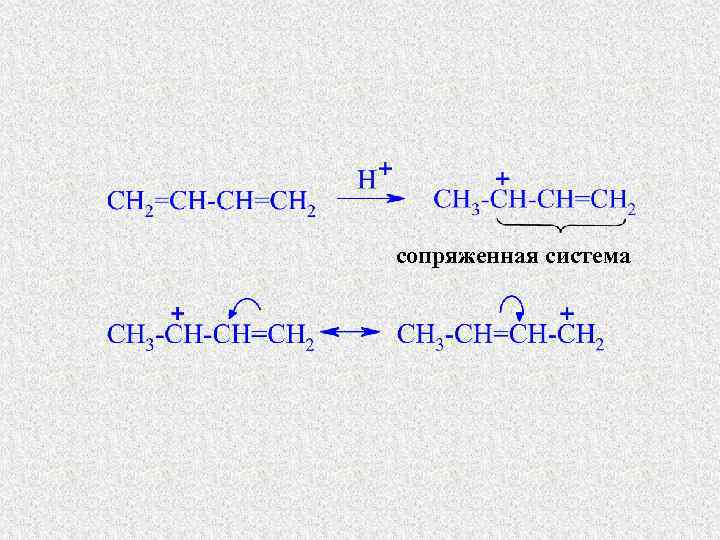
сопряженная система
алкены, алкины.ppt