Реакции замещения и реакции обмена.pptx
- Количество слайдов: 16

Реакции замещения и реакции обмена.

Вспомните, что такое реакции соединения и разложения? Fе(ОН)3 → Fе 2 O 3 + Н 2 O, Fе(ОН)3 + HCl → Fе. Сl 3 + Н 2 О, Li + O 2 → Li 2 O, Li 2 O + H 2 O → Li. OH, Cu. SO 4 + Fe → Fe. SO 4 + Cu, HNO 3 → H 2 O + NO 2 + O 2. Какие из этих реакций соединения? Какие разложения? С какими вы еще не знакомы?

Вспомните, что такое реакции соединения и разложения? Fе(ОН)3 → Fе 2 O 3 + Н 2 O, Fе(ОН)3 + HCl → Fе. Сl 3 + Н 2 О, Li + O 2 → Li 2 O, Li 2 O + H 2 O → Li. OH, Cu. SO 4 + Fe → Fe. SO 4 + Cu, HNO 3 → H 2 O + NO 2 + O 2. С какими вы еще не знакомы? Как вы думаете, какая реакция замещения? Почему?

Вспомните, что такое реакции соединения и разложения? Fе(ОН)3 → Fе 2 O 3 + Н 2 O, Fе(ОН)3 + HCl → Fе. Сl 3 + Н 2 О, Li + O 2 → Li 2 O, Li 2 O + H 2 O → Li. OH, Cu. SO 4 + Fe → Fe. SO 4 + Cu, HNO 3 → H 2 O + NO 2 + O 2. С какими вы еще не знакомы? Как вы думаете, какая реакция замещения? Почему?

Посмотрите реакцию взаимодействия цинка с соляной кислотой. Что наблюдаете? Zn + 2 HCl → Zn. Cl 2 + H 2↑ Теперь заменим Zn на Fe и Cu: Fe + 2 HCl → Fe. Cl 2 + H 2↑ (но медленнее) Cu + 2 HCl →

Возьмем вместо раствора кислоты, раствор солей и металлы: Cu. SO 4 + Fe → Cu↓ + Fe. SO 4 2 Ag. NO 3 + Cu → 2 Ag↓ + Cu(NO 3) 2 Pb(NO 3)2 + Zn → Pb↓ + Zn(NO 3)2 Реакции замещения – это реакции, в результате которых атомы простого вещества замещают атомы одного из химических элементов в сложном веществе.

Для прогнозирования возможного протекания реакции замещения используют ряд напряжений металлов: Тот металл, который располагается в ряду левее – вытесняет из соединений металл, который располагается правее.

Вспомните, что такое реакции соединения и разложения? Fе(ОН)3 → Fе 2 O 3 + Н 2 O, Fе(ОН)3 + HCl → Fе. Сl 3 + Н 2 О, Li + O 2 → Li 2 O, Li 2 O + H 2 O → Li. OH, Cu. SO 4 + Fe → Fe. SO 4 + Cu, HNO 3 → H 2 O + NO 2 + O 2. С какими вы еще не знакомы? Как вы думаете, какая реакция обмена? Почему?

Вспомните, что такое реакции соединения и разложения? Fе(ОН)3 → Fе 2 O 3 + Н 2 O, Fе(ОН)3 + HCl → Fе. Сl 3 + Н 2 О, Li + O 2 → Li 2 O, Li 2 O + H 2 O → Li. OH, Cu. SO 4 + Fe → Fe. SO 4 + Cu, HNO 3 → H 2 O + NO 2 + O 2. С какими вы еще не знакомы? Как вы думаете, какая реакция обмена? Почему?

Реакции обмена – Реакции, в результате которых два сложных вещества обмениваются своими составными частями.

1) Fе(ОН)3 + 3 HCl → Fе. Сl 3 + 3 НОН Н 2 О Продуктами реакции взаимодействия щелочи и кислоты являются соль и вода – реакция нейтрализации. Общая схема реакции: Me. OH + H(КО) → Me(КО) + Н 2 О

2) Cu. SO 4 + 2 Na. OH → Cu(OH)2↓ + Na 2 SO 4 При взаимодействии щелочи с солями образуются новая соль и новое основание. Me(KO) + Me. OH → Me(KO) + Me. OH 3) Cu(NO 3)2 + H 2 S → Cu. S↓ + 2 HNO 3 При взаимодействии соли с кислотой образуются новая соль и новая кислота: Me(KO) + H(KO) → Me(KO) + H(KO)

Напишите уравнение взаимодействия карбоната натрия с кислотой. Na 2 CO 3 + HCl → 2 Na. Cl + ?
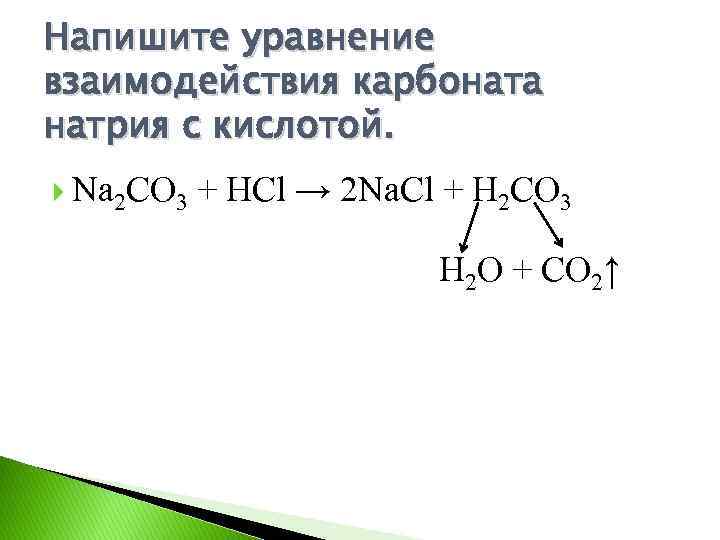
Напишите уравнение взаимодействия карбоната натрия с кислотой. Na 2 CO 3 + HCl → 2 Na. Cl + Н 2 СО 3 Н 2 О + СО 2↑

Реакции обмена, протекающие в растворах, идут до конца только в том случае, если в результате их образуется осадок, газ или вода. ↓ ↑ Н 2 О

Домашнее задание: § 31 -32, № 2, с. 164, № 4, 5, с. 168
Реакции замещения и реакции обмена.pptx