10 нуклеофильное замещение.ppt
- Количество слайдов: 16

Реакции нуклеофильного замещения у sp 3 -гибридизованного атома углерода. Y(нуклеофил) – анион или нейтральная молекула, имеющая хотя бы одну неподеленную электронную пару (основание Льюиса): Y = OH-, H 2 O, OR-, ROH, SH-, H 2 S, SR-, HSR, Hal-, CN-, NO 2 -, NH 3, …). Х (замещаемая группа, уходящая группа) – обычно обладает высокой электроотрицательностью и может уходить в виде аниона или электронейтральной молекулы, отщепляясь с электронами нарушающейся связи: X = Hal-, OH-, OR-, O-SO 2 R, O-COR, N+R 3, …). Реакции нуклеофильного замещения при атоме углерода в состоянии sp 3 -гибридизации Мономолекулярный (диссоциативный) механизм (SN 1) Бимолекулярный (синхронный) механизм (SN 2)
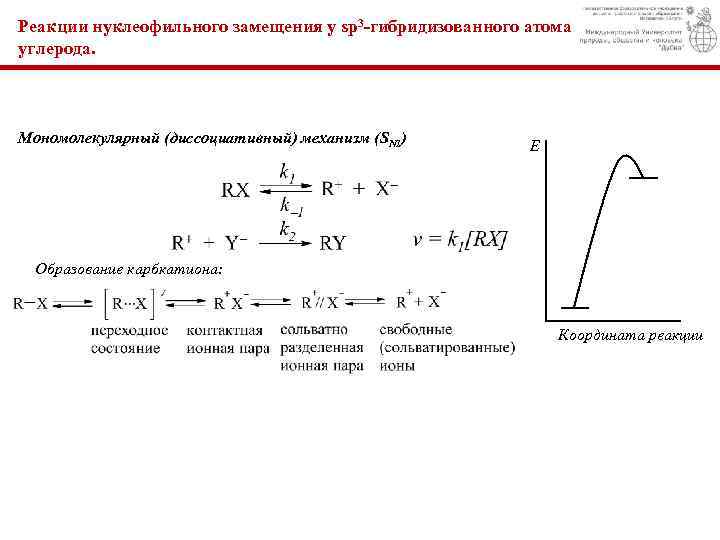
Реакции нуклеофильного замещения у sp 3 -гибридизованного атома углерода. Мономолекулярный (диссоциативный) механизм (SN 1) Е Образование карбкатиона: Координата реакции

Реакции нуклеофильного замещения у sp 3 -гибридизованного атома углерода. Мономолекулярный механизм Реакцию ускоряют ЭД заместители. Соединение kотн. (CH 3)2 CH–Cl 0, 1 (CH 3)3 C–Cl 4· 104 C 6 H 5 CH(CH 3)–Cl Влияние электронных факторов на скорость SN 1 реакций: 1. Природа карбкатиона. Факторы, стабилизирующие карбкатион, должны приводить к ускорению реакции. 8· 104 (C 6 H 5)2 CH–Cl 4· 107 (C 6 H 5)3 C–Cl 2· 1010 2. Природа уходящей группы. Введение в уходящую группу электроноакцепторных заместителей приводит к делокализации возникающего в ней отрицательного заряда и к увеличению скорости реакции. В ряду галогенов реакционная способность уменьшается в последовательности: C–I > C–Br > C–Cl >> C–F Увеличение энергии диссоциации связи 3. Природа нуклеофила. Так как нуклеофил не принимает участия в образовании переходного состояния, то можно считать, что он не влияет на скорость реакции.
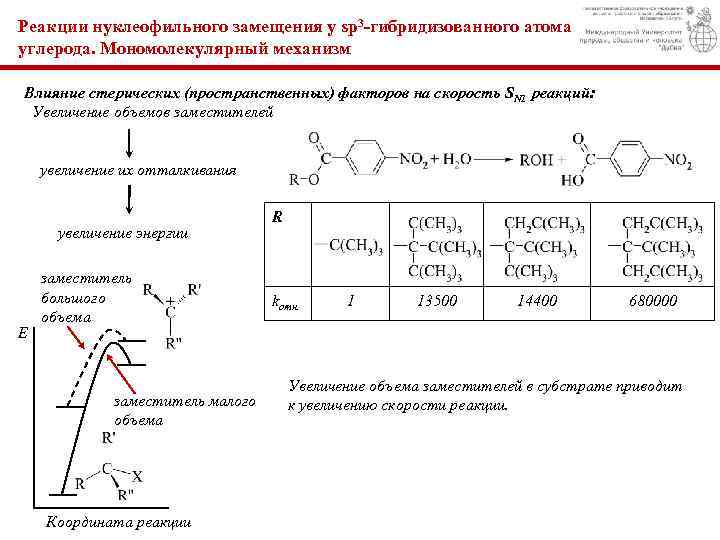
Реакции нуклеофильного замещения у sp 3 -гибридизованного атома углерода. Мономолекулярный механизм Влияние стерических (пространственных) факторов на скорость SN 1 реакций: Увеличение объемов заместителей увеличение их отталкивания увеличение энергии Е заместитель большого объема заместитель малого объема Координата реакции R kотн. 1 13500 14400 680000 Увеличение объема заместителей в субстрате приводит к увеличению скорости реакции.
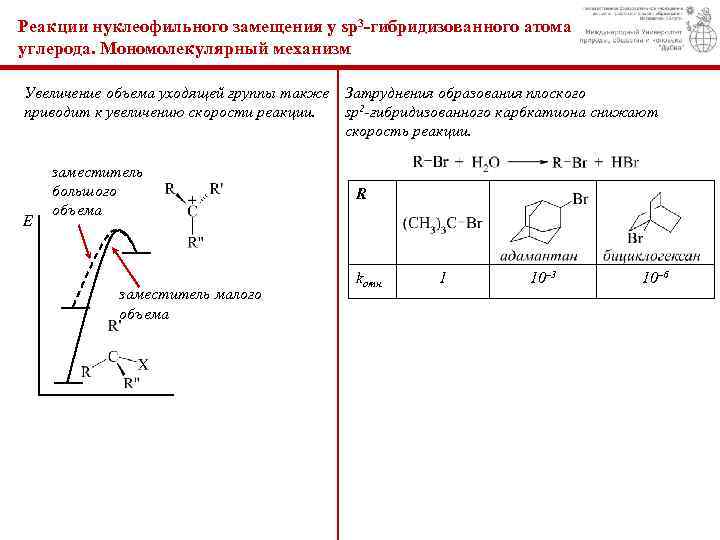
Реакции нуклеофильного замещения у sp 3 -гибридизованного атома углерода. Мономолекулярный механизм Увеличение объема уходящей группы также Затруднения образования плоского приводит к увеличению скорости реакции. sp 2 -гибридизованного карбкатиона снижают скорость реакции. Е заместитель большого объема заместитель малого объема R kотн. 1 10– 3 10– 6
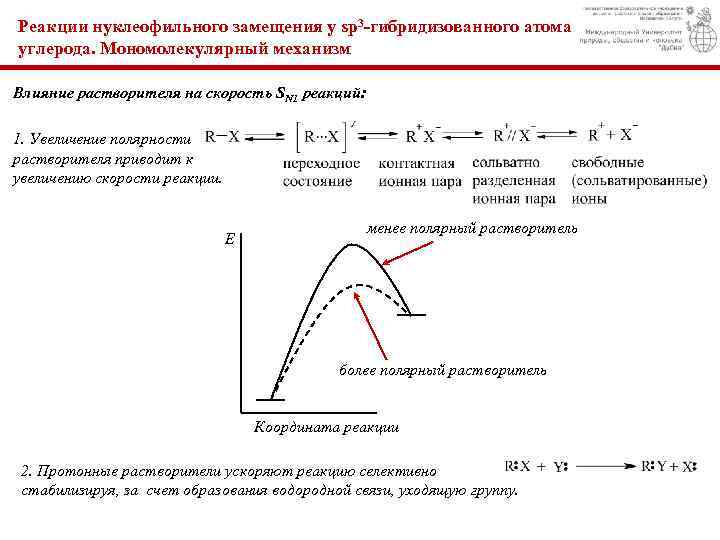
Реакции нуклеофильного замещения у sp 3 -гибридизованного атома углерода. Мономолекулярный механизм Влияние растворителя на скорость SN 1 реакций: 1. Увеличение полярности растворителя приводит к увеличению скорости реакции. Е менее полярный растворитель более полярный растворитель Координата реакции 2. Протонные растворители ускоряют реакцию селективно стабилизируя, за счет образования водородной связи, уходящую группу.
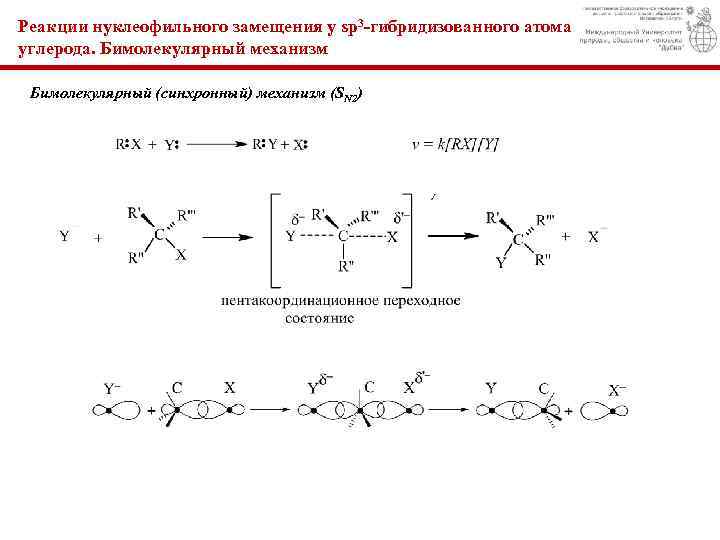
Реакции нуклеофильного замещения у sp 3 -гибридизованного атома углерода. Бимолекулярный механизм Бимолекулярный (синхронный) механизм (SN 2)

Реакции нуклеофильного замещения у sp 3 -гибридизованного атома углерода. Бимолекулярный механизм Влияние электронных факторов на скорость SN 2 реакций: 1. Природа субстрата. Случай А. Скорости разрыва «старой» связи и образования «новой» равны. «Центральное» переходное состояние. Скорость реакции не зависит от электронной природы заместителей. Случай Б. Разрыв «старой» связи обгоняет образование «новой» . «Рыхлое» переходное состояние. Скорость реакции увеличивается при введении в молекулу субстрата ЭД заместителей. Случай В. «Сжатое» переходное состояние. Разрыв «старой» связи отстает от образования «новой» . Скорость реакции увеличивается при введении в молекулу субстрата ЭА заместителей. Экспериментальные данные – реакция ускоряется при введение в молекулу субстрата ЭА заместителей.

Реакции нуклеофильного замещения у sp 3 -гибридизованного атома углерода. Бимолекулярный механизм 2. Природа уходящей группы. Так как уходящая группа несет отрицательный заряд, то, очевидно, что введение ЭА заместителей приводит к ее стабилизации и, следовательно, к ускорению реакции. В ряду галогенов реакционная способность уменьшается в последовательности: C–I > C–Br > C–Cl >> C–F Увеличение энергии диссоциации связи 3. Природа нуклеофила. Случай А. Отрицательный заряд на нуклеофиле уменьшается. Случай Б. На нуклеофиле появляется положительный заряд. Случай А. Е Введение ЭД заместителей увеличивает скорость реакции. Случай Б. Координата реакции
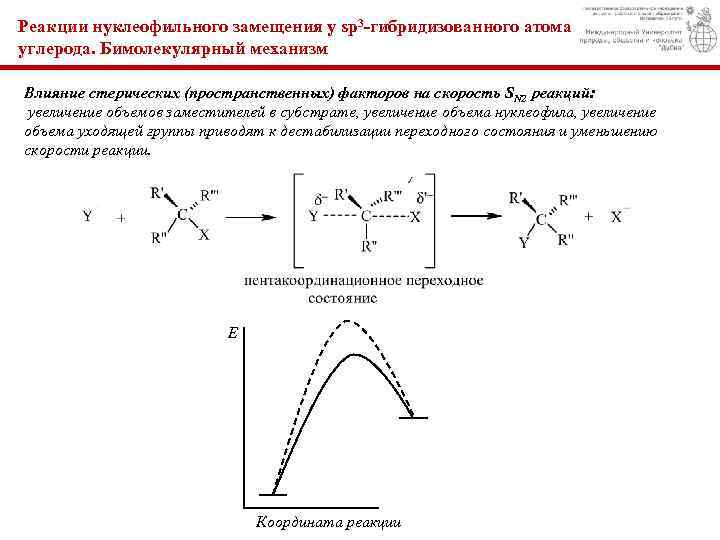
Реакции нуклеофильного замещения у sp 3 -гибридизованного атома углерода. Бимолекулярный механизм Влияние стерических (пространственных) факторов на скорость SN 2 реакций: увеличение объемов заместителей в субстрате, увеличение объема нуклеофила, увеличение объема уходящей группы приводят к дестабилизации переходного состояния и уменьшению скорости реакции. Е Координата реакции

Реакции нуклеофильного замещения у sp 3 -гибридизованного атома углерода. Бимолекулярный механизм Е Более полярный растворитель увеличивает скорость реакции Случай Б. Y- + RX [Yδ-···R···Xδ’-] – делокализация отрицательного заряда. Полярность переходного состояния меньше, чем исходного. Е Более полярный растворитель уменьшает скорость реакции Случай В. Y + RX+ [Yδ+···R···Xδ’+] – делокализация положительного заряда. Полярность переходного состояния меньше, чем исходного. Е Более полярный растворитель уменьшает скорость реакции Случай Г. Y- + RX+ [Yδ-···R···Xδ’+] – нейтрализация разноименных зарядов. Полярность переходного состояния меньше, чем исходного. Е Более полярный растворитель уменьшает скорость реакции Влияние растворителя на скорость SN 2 реакций: Случай А. Y + RX [Yδ+···R···Xδ-] – разделение зарядов. Полярность переходного состояния больше, чем исходного.

Реакции нуклеофильного замещения у sp 3 -гибридизованного атома углерода. Стереохимические особенности реакций нуклеофильного замещения у sp 3 -гибридизованного атома углерода. оптические антиподы (энантиомеры) Характеристикой оптической активности является удельное вращение — вращение плоскости поляризации плоскополяризованного света, приходящееся на единицу длины (дм) и единицу концентрации (г/мл). Эквимолекулярная смесь оптических антиподов называется рацемической смесью (рацематом) и не является оптически активной.
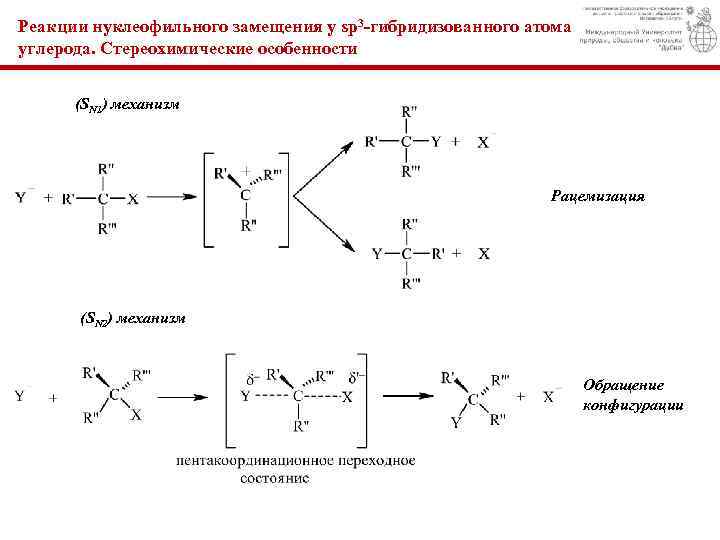
Реакции нуклеофильного замещения у sp 3 -гибридизованного атома углерода. Стереохимические особенности (SN 1) механизм Рацемизация (SN 2) механизм Обращение конфигурации
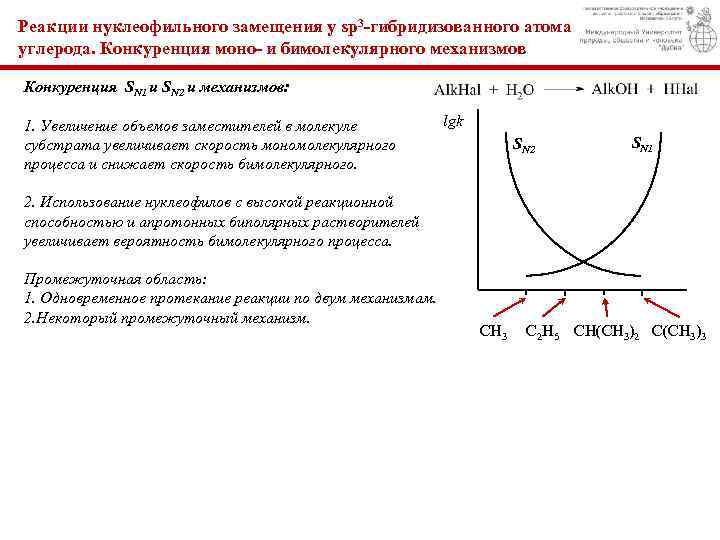
Реакции нуклеофильного замещения у sp 3 -гибридизованного атома углерода. Конкуренция моно- и бимолекулярного механизмов Конкуренция SN 1 и SN 2 и механизмов: 1. Увеличение объемов заместителей в молекуле субстрата увеличивает скорость мономолекулярного процесса и снижает скорость бимолекулярного. lgk SN 2 SN 1 2. Использование нуклеофилов с высокой реакционной способностью и апротонных биполярных растворителей увеличивает вероятность бимолекулярного процесса. Промежуточная область: 1. Одновременное протекание реакции по двум механизмам. 2. Некоторый промежуточный механизм. CH 3 C 2 H 5 CH(CH 3)2 C(CH 3)3
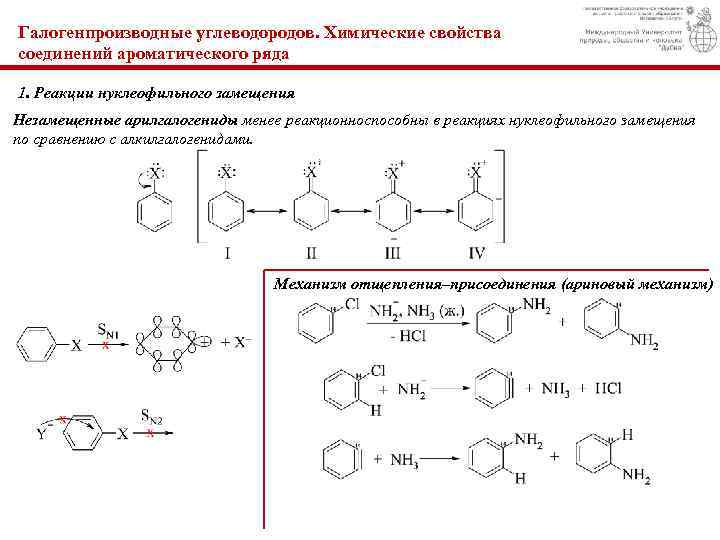
Галогенпроизводные углеводородов. Химические свойства соединений ароматического ряда 1. Реакции нуклеофильного замещения Незамещенные арилгалогениды менее реакционноспособны в реакциях нуклеофильного замещения по сравнению с алкилгалогенидами. Механизм отщепления–присоединения (ариновый механизм)
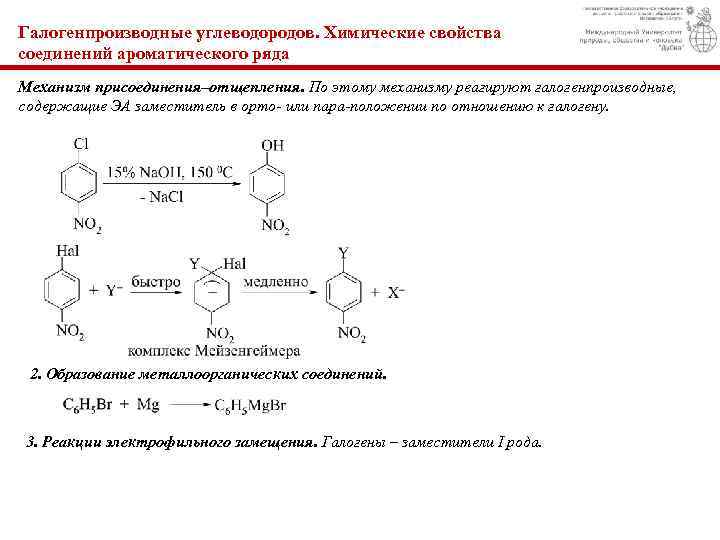
Галогенпроизводные углеводородов. Химические свойства соединений ароматического ряда Механизм присоединения–отщепления. По этому механизму реагируют галогенпроизводные, содержащие ЭА заместитель в орто- или пара-положении по отношению к галогену. 2. Образование металлоорганических соединений. 3. Реакции электрофильного замещения. Галогены – заместители I рода.
10 нуклеофильное замещение.ppt