Лекция 8-Комплекс 2012.ppt
- Количество слайдов: 19

Реакции комплексообразования в анализе 1. Применение реакций комплексообразования в анализе. Важнейшие комплексные соединения 2. Ступенчатый характер комплексообразования. Константы устойчивости. 3. Маскирование. Маскирующшие агенты. Закомплексованность. 4. Комплексонометрия. Металлохромные индикаторы
![Типы комплексных соединений Неорганические – образованы неорганическими лигандами: Сl- – хлоридные [Ag(Cl)2 ]- NH Типы комплексных соединений Неорганические – образованы неорганическими лигандами: Сl- – хлоридные [Ag(Cl)2 ]- NH](https://present5.com/presentation/3/19923136_132127816.pdf-img/19923136_132127816.pdf-2.jpg)
Типы комплексных соединений Неорганические – образованы неорганическими лигандами: Сl- – хлоридные [Ag(Cl)2 ]- NH 3 – аммиачные [Cu(NH 3 )4 ]2+ Н 2 О – аквакомплексы [Fe(H 2 O)6 ]3+ Органические – образованы органическими лигандами: Сit 3 - – цитратные С 2 О 42 - - оксалатные Насыщенные - внутренняя сфера занята только лигандами; [Fe(SCN)6 ]3 Ненасыщенные – внутренняя сфера занята лигандами и молекулами растворителя [Fe(H 2 O)3 (SCN)3 ]

Устойчивые и неустойчивые – по величине константы устойчивости: чем больше значение константы, тем устойчивее комплекс Инертные и лабильные – по скорости образования и разрушения Внутрикомплексные соединения - хелаты О = С__ ОI O = C__O- -О__С Zn+2 =О ( «хелат» (греч. ) - клешня) I -O__C =O Образование внутримолекулярных 5 - и 6 -членных циклов с участием комплексообразователя повышает прочность комплексов ( «ХЕЛАТОЭФФЕКТ» )
![Применение комплексных соединений в промышленности • Изготовление катализаторов. Раствор Н 2[Рt. Cl 4] (Н Применение комплексных соединений в промышленности • Изготовление катализаторов. Раствор Н 2[Рt. Cl 4] (Н](https://present5.com/presentation/3/19923136_132127816.pdf-img/19923136_132127816.pdf-4.jpg)
Применение комплексных соединений в промышленности • Изготовление катализаторов. Раствор Н 2[Рt. Cl 4] (Н 2[Рd. Cl 4]) наносят на основу катализатора, затем его высушивают и восстанавливают Pt в токе водорода. • Получение золота из руд. Руду растворяют в смеси азотной и соляной кислот (царская водка), в результате золото переходит в раствор в виде комплекса Н[Au. Cl 4], затем его восстанавливают перекисью водорода до. металлического. • Разделение смесей элементов, например, лантаноидов.

Применение реакций комплексообразования в анализе Fe +3 + 3 SCN- = Fe(SCN)3 1. В качественном анализе 2. Маскирование Fe +3 + 6 CN- = [Fe(CN)6]3 - 3. Изменение ок-восст. свойств 2 Fe +3 + 2 I- = 2 Fe+2 + I 2 2 [Fe(CN)6 ]3 - + 2 I- = реакция не идет 4. Изменение растворимости Ag+ + Cl- = Ag. Cl↓ В присутствии NH 3 осадок Ag. Cl+ 2 NH 3 = [Ag(NH 3)2]Cl растворяется 5. В инструментальных методах- фотометрическое определение катионов по интенсивности окраски раствора 6. В титриметрии – комплексометрическое титрование

Равновесие реакций комплексообразования Реакции комплексообразования с участием низкодентатных лиганд протекают ступенчато: Ступенчатые константы: М+R МR 2 + R МRn-1+R MR MR 2 MR 3 MRn Суммарные реакции: М+R MR М+2 R MR 2 М+3 R MR 3 М+ n. R MRn Общие константы:

Закомплексованность Общая характеристика процессов комплексообразования, протекающих в растворе с участием М – функция закомплексованности - Ф Ф принимает значения от 1 до б. б. значений ( вплоть до 1020) Закомплексованность металла зависит от констант устойчивости комплексов β и от избыточной концентрации лиганда. Закомплексованность НЕ ЗАВИСИТ от общей концентрации металла в растворе. При большом избытке R и образовании самого насыщенного комплекса:

Доминирование того или иного комплекса в растворе зависит от константы его устойчивости и от концентрации лиганда. С увеличением концентрации лиганда увеличивается доля более насыщенных комплексов Распределительные диаграммы – зависимость доли (α) каждой формы металла от концентрации лиганда R ( или p R). Их строят в координатах α = f (R) или α = f (p. R)
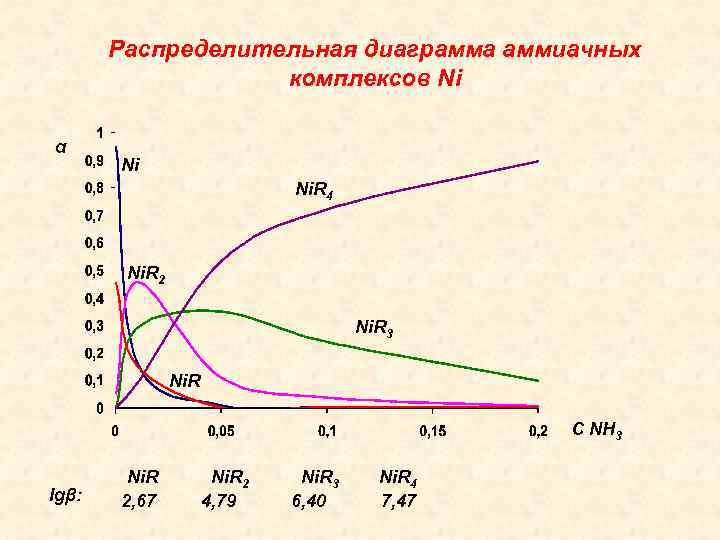
Распределительная диаграмма аммиачных комплексов Ni α Ni Ni. R 4 Ni. R 2 Ni. R 3 Ni. R С NH 3 lgβ: Ni. R 2, 67 Ni. R 2 4, 79 Ni. R 3 6, 40 Ni. R 4 7, 47

Маскирование 1. Для маскирования выбирают лиганд, который образует с металлами прочные бесцветные комплексы Примеры лиганд: цитраты, оксалаты, цианиды, ЭДТА, фосфаты 2. Общая концентрация металла в растворе должна быть примерно известна. Исходя из состава комплекса вычисляют концентрацию лиганда по уравнению реакции Ме + n. R = [Me. Rn ] 3. Задают закомплексованность Ф 4. Вычисляют равновесную избыточную концентрацию лиганда, необходимую для достижения Ф 5. Суммируют к-ции лиганда, вычисленные по уравнению реакции и избыточную

Термодинамические и условные константы устойчивости В справочниках приведены значения общих констант устойчивости или их логарифмы lgβТ n = lg k 1 +lgk 2 +…. lgn Чаще всего могут протекать побочные реакции: -протонирование лиганда - образование комплексов металлов с другими лигандами, присутствующими в растворе ( например, компоненты буферных систем), или образование осадков и т. п. Условные константы устойчивости выражают через общие концентрации М и R. Устойчивость комплексов при протекании побочных процессов снижается, условные константы устойчивости меньше термодинамических
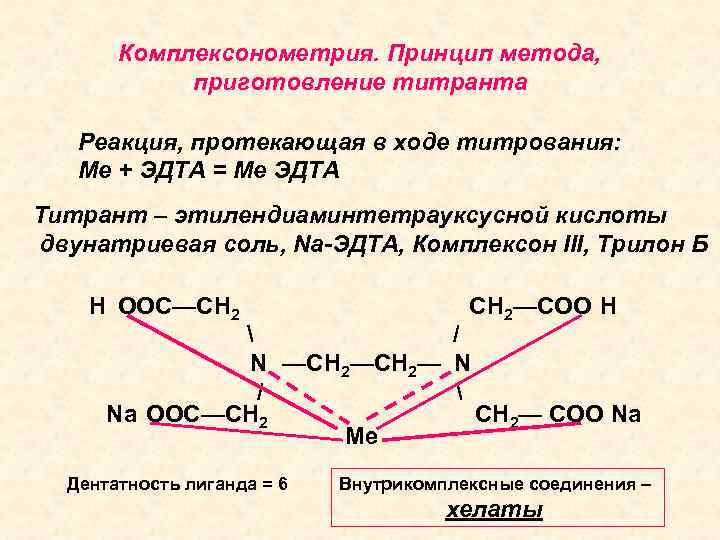
Комплексонометрия. Принцип метода, приготовление титранта Реакция, протекающая в ходе титрования: Ме + ЭДТА = Ме ЭДТА Титрант – этилендиаминтетрауксусной кислоты двунатриевая соль, Na-ЭДТА, Комплексон III, Трилон Б H OOC—CH 2—COO H / N —CH 2— N / Na OOC—CH 2— COO Na Ме Дентатность лиганда = 6 Внутрикомплексные соединения – хелаты

Прочность комплексонатов. Константы устойчивости. Ме + R = Ме R Состав комплексов любых металлов 1: 1 Устойчивость комплексов некоторых металлов с ЭДТА Металл lgβ Mg Ca Zn Cd Pb Ni Cu Cr (III) Fe(III) Co (III) 9, 1 10, 6 16, 3 16, 5 18, 0 18, 6 18, 8 23, 4 24, 2 40, 6

Состояние ЭДТА в растворе при разных р. Н H 6 R 2+ H 5 R+ 0 H 4 R H 3 R - H 2 R 2 - HR 3 - R 4 - 14 Me + HR 3 - = Me. R + H+ [R 4 -] = α Cобщ R Me + H 2 R 2 - = Me. R + 2 H+ Для поддержания р. Н применяют буферные растворы p. H Состояние катионов металлов в растворе при добавлении буферных растворов Me + NH 3 = [Me. NH 3] Me + OH- = [Me. OH-] [Me] =α lgβусл = lg βT – pαMe - pαR Cобщ Me

Титрование 0, 01 М растворов металлов с погрешностью не более 1% возможно, если значение lg βусл > 8 Выбор р. Н. Возможность раздельного титрования. lgβусл = lg βT – pαMe - pαR 8 = lg р. Н 1 pαR 17, 7 βT pαR = lg – pαR 3 4 5 13, 4 10, 6 8, 4 6, 5 4, 7 3, 3 2, 3 lg βT 10, 6 16, 3 18, 0 pαR 2, 6 8, 3 10 р. Нmin 8 4 3 Ni 18, 6 10, 6 Fe(III) 24, 2 16, 2 По таблице находят р. Н для pαR – 8 2 Ме Ca Zn Pb 6 βT 7 3 1, 5 8 9 10 11 12 13 1, 3 0, 5 0, 1 0, 07 0
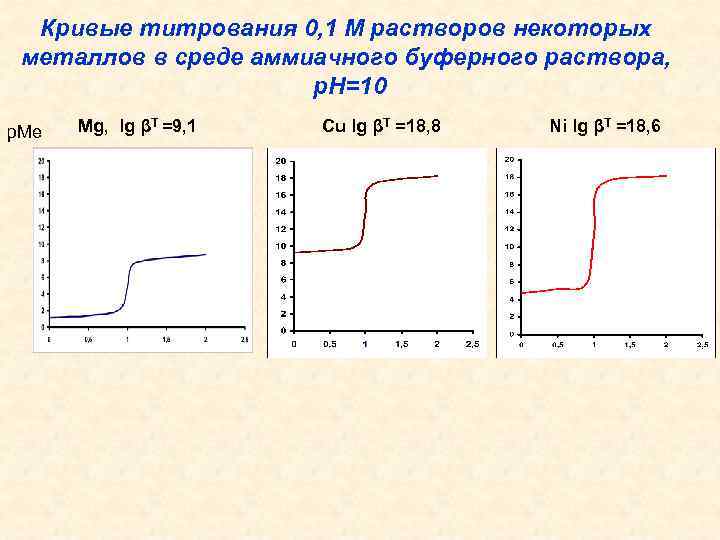
Кривые титрования 0, 1 М растворов некоторых металлов в среде аммиачного буферного раствора, р. Н=10 p. Me Mg, lg βT =9, 1 Cu lg βT =18, 8 Ni lg βT =18, 6

Высота скачка зависит: 1. От устойчивости комплекса Ме. ЭДТА : чем выше , тем больше высота скачка. 2. От концентрации титруемого раствора : чем она выше, тем больше высота скачка. 3. От природы и концентрации маскирующих веществ: чем прочнее комплексы металлов, тем меньше высота 4. От р. Н раствора: при уменьшении р. Н высота скачка уменьшается
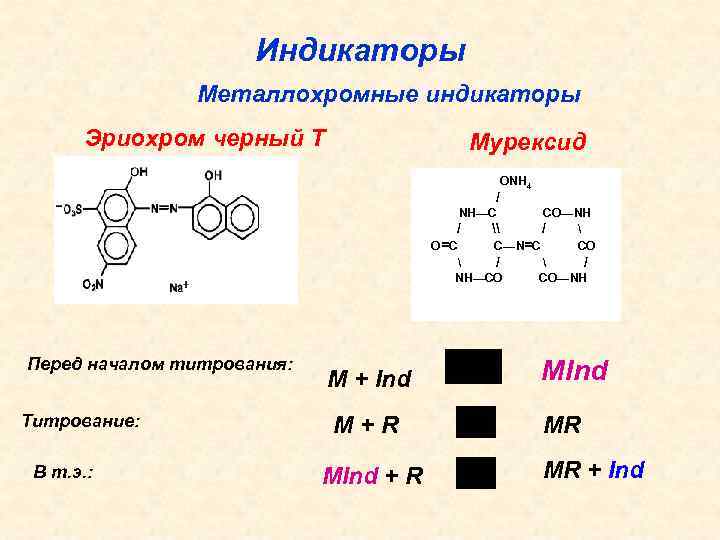
Индикаторы Металлохромные индикаторы Эриохром черный Т Мурексид / ОNН 4 NН—С СО—NН / \ / О =С С—N=С СО / NН—СО СО—NН Перед началом титрования: Титрование: В т. э. : М + Ind М+R МR МInd + R МR + Ind

Выбор индикатора Ме. Ind = Комплекс - красный Индикатор - синий Ширина интервала перехода окраски индикатора: р. Ме = lg Ме. Ind ± 1 1. Комплекс катиона металла с индикатором должен быть достаточно устойчивым, но менее прочным, чем комплекс этого металла с ЭДТА 2. Комплекс катиона металла с индикатором должен быстро образовываться и быстро разрушаться под действием ЭДТА Если комплекс катиона металла с индикатором излишне прочный - происходит «блокировка» индикатора 3. Интервал перехода индикатора должен входить в пределы скачка титрования 4. Окраски свободного индикатора и комплекса должны быть контрастными
Лекция 8-Комплекс 2012.ppt