занятие 9-10.ppt
- Количество слайдов: 54

Реакции клеток на облучение. Клеточная радиочувствительность u преходящие лучевые реакции клеток u летальные лучевые реакции клеток

Преходящие лучевые реакции клеток u Разнообразные реакции повреждения – задержка деления, угнетение синтеза ДНК, повреждение мембран и др. u Степень выраженности этих реакций зависит от того, на какой стадии жизненного цикла клетки произведено облучение
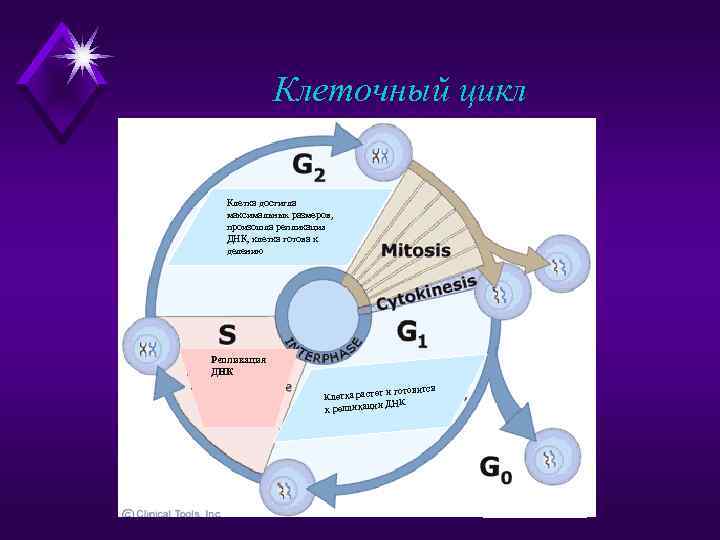
Клеточный цикл Клетка достигла максимальных размеров, произошла репликация ДНК, клетка готова к делению Репликация ДНК и готовится Клетка растет ДНК к репликации

Митотический цикл u u u М — митоз G 1 — предсинтетическнй период S — период синтеза ДНК G 2 — постсинтетический период Go — фаза покоя
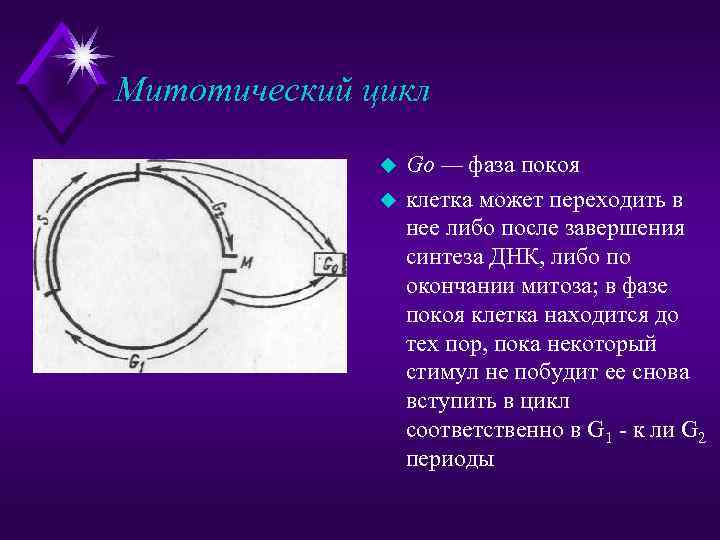
Митотический цикл u u Go — фаза покоя клетка может переходить в нее либо после завершения синтеза ДНК, либо по окончании митоза; в фазе покоя клетка находится до тех пор, пока некоторый стимул не побудит ее снова вступить в цикл соответственно в G 1 - к ли G 2 периоды

Митотический цикл u Продолжительность митотического цикла - время между двумя последовательными делениями клетки — слагается из отдельных стадий, длительность которых в разных тканях варьирует относительно друга по величине, располагаясь, как правило, следующим образом: М < G 2 < S< G 1

Преходящие лучевые реакции клеток Нарушение метаболизма: u Ингибирование нуклеинового обмена u Ингибирование окислительного фосфорилирования u Слипание хромосом и др.

Преходящие лучевые реакции клеток u Проявляются в ближайшие сроки после облучения u Исчезают с течением времени

Преходящие лучевые реакции клеток u Наиболее универсальная реакция – временная задержка (угнетение) клеточного деления (радиационный блок митоза) u данная реакция была открыта сразу после открытия рентгеновского излучения

Радиационный блок митоза u Длительность задержки деления зависит: - от дозы облучения - от свойств биологического объекта - в том числе от стадии клеточного цикла u проявляется у всех клеток облученной популяции не зависимо от их дальнейшей судьбы (погибнет/выживет)
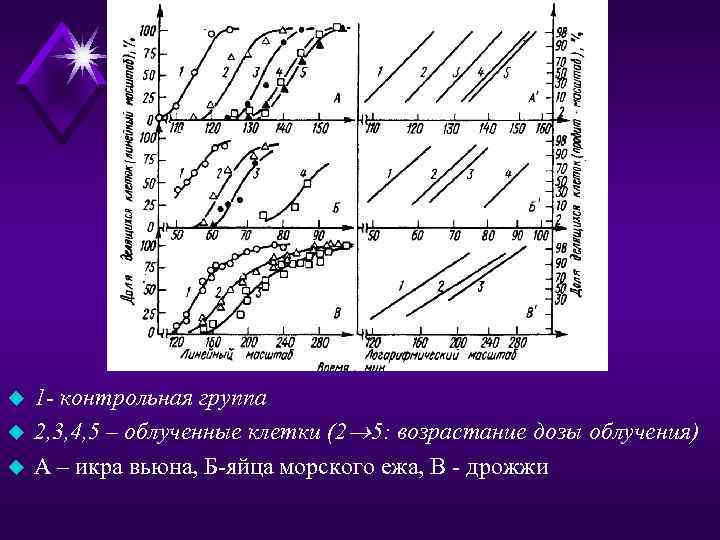
u u u 1 - контрольная группа 2, 3, 4, 5 – облученные клетки (2 5: возрастание дозы облучения) А – икра вьюна, Б-яйца морского ежа, В - дрожжи

Пояснения к графикам: u Во всех случаях после облучения деление клеток прекращалось и возобновлялось спустя некоторое время u У каждого объекта кривые первого послерадиационного деления имеют такую же форму, что и кривые контроля, но сдвинуты по оси абсцисс u Чем больше доза, тем больше сдвиг, т. е. тем больше продолжительность задержки митоза

Пояснения к графикам: u Многочисленные исследования показали, что для большинства изученных культур клеток задержка деления соответствует примерно 1 часу на каждый 1 Гр u Следовательно, эта реакция идентична у всех особей однородной популяции не только качественно, но и количественно u С увеличением дозы возрастает не доля реагирующих особей, а продолжительность задержки деления каждой облученной клетки.
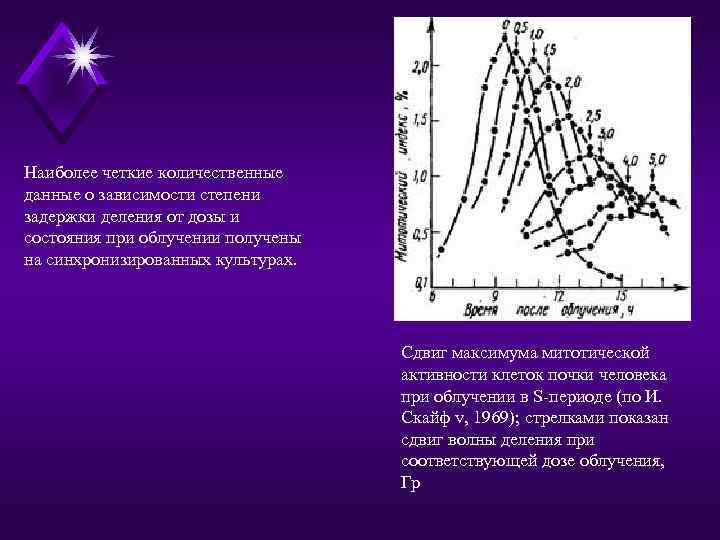
Наиболее четкие количественные данные о зависимости степени задержки деления от дозы и состояния при облучении получены на синхронизированных культурах. Сдвиг максимума митотической активности клеток почки человека при облучении в S-периоде (по И. Скайф v, 1969); стрелками показан сдвиг волны деления при соответствующей дозе облучения, Гр

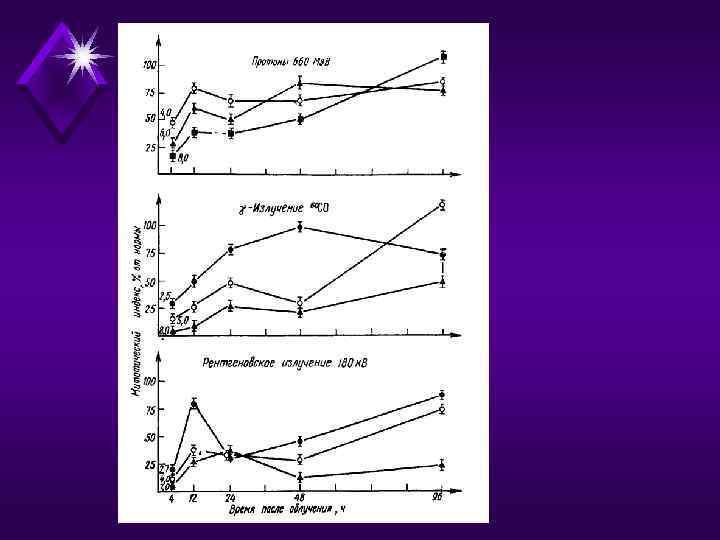
Радиационный блок митоза u u Время задержки деления клеток зависит и от стадии клеточного цикла, в которой находятся клетки при облучении; наиболее длительно оно в тех случаях, когда воздействию подвергаются клетки в стадии синтеза ДНК или в постсинтетической стадии, и самое короткое - при облучении в митозе, когда абсолютное большинство клеток, начав митоз, заканчивает его без задержки. Из-за различий в длительности задержки деления, наблюдающейся на отдельных стадиях клеточного цикла, восстановление митотической активности при облучении активно пролиферирующих тканей происходит волнообразно, так как эти ткани представляют собой асинхронную клеточную популяцию, т. е. состоящую из клеток, находящихся на разных стадиях жизненного цикла.
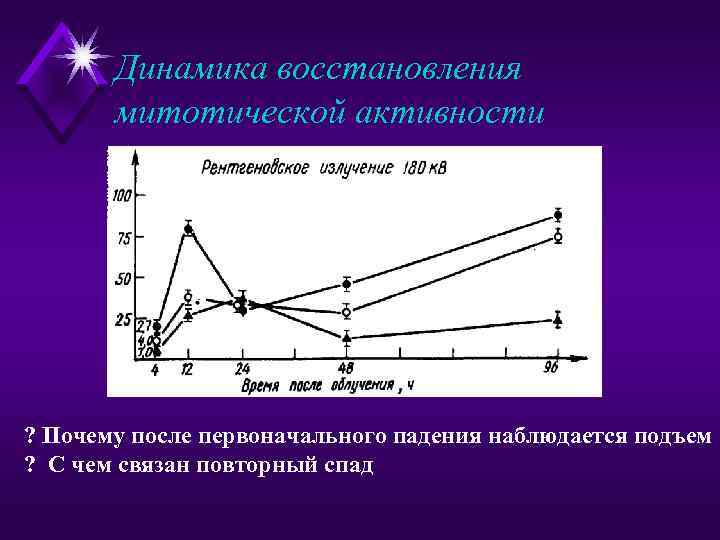
Динамика восстановления митотической активности ? Почему после первоначального падения наблюдается подъем ? С чем связан повторный спад
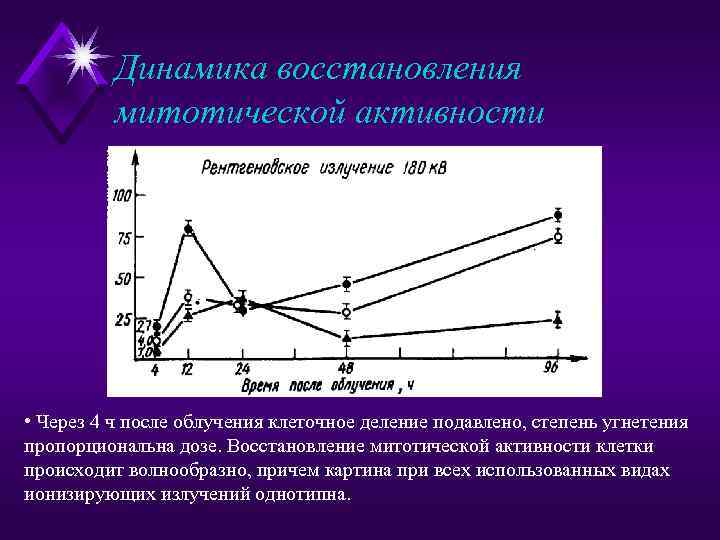
Динамика восстановления митотической активности • Через 4 ч после облучения клеточное деление подавлено, степень угнетения пропорциональна дозе. Восстановление митотической активности клетки происходит волнообразно, причем картина при всех использованных видах ионизирующих излучений однотипна.

Вскоре после первоначального падения митотический индекс достаточно резко повышается, иногда даже достигая исходного уровня, а затем вновь снижается. Это начальное повышение еще не является истинным увеличением количества митозов. Объяснением этому служит тот факт, что под влиянием облучения некоторые клетки запаздывают со вступлением в деление, что отражается в снижении митотического индекса сразу после облучения. Вероятно, эти клетки в момент облучения находились на наиболее чувствительной к излучению (по данному критерию) стадии интерфазы. Затем они начинают делиться, причем одновременно с клетками, которые к моменту облучения находились на менее чувствительной стадии, и потому вступили в митоз в обычное время. Так образуется компенсаторная волна увеличения митотического индекса, которая иногда может превышать исходные показатели. С увеличением дозы облучения и компенсаторная волна, и новое значение митотического индекса еще долго оказываются меньшими по сравнению с исходными, что объясняется подавлением способностей клеток к делению.

Механизм радиационной задержки деления Можно рассматривать задержку деления как проявление неспецифического компонента реакции клеток на облучение (тем более что она наблюдается в ответ на действие многих внешних факторов), имеющее защитно-приспособительный характер.

Механизм радиационной задержки деления Все сказанное относится к временной задержке первого пострадиационного деления, наблюдаемой после облучения в определенном, хоти и достаточно большом диапазоне доз (для большинства клеток млекопитающих в пределах 10 Гр). Еще менее изучен механизм задержки деления при повторных облучениях, а потому и более затруднена интерпретация.

Механизм радиационной задержки деления Описываемую реакцию задержки деления следует отличать от полного подавления митоза, наступающего после воздействия больших доз, когда клетка значительное время продолжает жизнь, но необратимо утрачивает способность к делению. В результате такой необратимой реакции на облучение часто образуются патологические формы гигантских клеток, иногда даже содержащие несколько наборов хромосом вследствие их редупликации в пределах одной и той же не разделившейся клетки (эндомитоз).

Летальные реакции клеток u Репродуктивные формы гибели u Гибель непосредственно при облучении

Репродуктивная гибель u Среди многих проявлений действия излучения на жизнедеятельность клетки подавление способности к делению является наиболее важным. В связи с этим под клеточной гибелью, или летальным эффектом облучения, в радиобиологии понимают утрату клеткой способности к пролиферации. Наоборот, выжившими клетками считают те, которые сохранили способность к неограниченному размножению, т. е. к клонообразованию. Таким образом, речь идет здесь о репродуктивной гибели клеток. Репродуктивная форма лучевой инактивации клеток наиболее распространена в природе, Она же и лучше изучена методами количественной радиобиологии в связи с тем, что ее можно наблюдать при культивировании клеток вне организма.

1 - гибель 2 - слияние u При наблюдении за облученными клетками линии L (мышиных фибробластов) было установлено, что их гибель происходит как в процессе 1 -го пострадиационного деления, так и во 2 -м, 3 -м и 4 -м митозах. Схематически показана судьба потомков одной клетки, облученной в дозе 2 Гр. Их гибель (фрагментация) наблюдалась только через 70 и 140 ч после облучения исходной клетки, т. е. соответственно после 2 -го и 3 -го деления. После облучения в дозе 4 Гр клетки линии L более чем в 80% случаев успешно заканчивали 1 -е пострадиационное деление, но зато вероятность деления дочерних клеток (1 -я генерация) и "внучек" (2 -я генерация) составляла около 30%; остальные 70 % клеток, начав деление, погибали

Репродуктивная гибель u Другая разновидность репродуктивной гибели потомков облученных клеток — формирование так называемых гигантских клеток возникающих в результате слияния двух соседних, чаще "сестринских" клеток. Такие клетки способны не более чем к 2— 3 делениям, после чего они погибают. Гигантские клетки могут возникнуть без слияния при длительной задержке истинного деления (эндомитоз) облученных клеток или их потомков. Такие клетки также нежизнеспособны.

интерфазная гибель u Другая форма радиационной инактивации клеток — интерфазная гибель — наступает до вступления клетки в митоз. При очень больших дозах облучения это происходит непосредственно "под лучом" или вскоре после облучения. В диапазоне умеренных доз (до 10 Гр) гибель наступает в первые часы после облучения и может быть зарегистрирована в виде различных дегенеративных изменений клетки; чаще всего под микроскопом через 2— 6 ч можно наблюдать клетки с резким пикнозом ядра и фрагментацией хроматина.

интерфазная гибель u Для размножающихся клеток в культуре ткани, а также для большинства клеток соматических тканей взрослых животных и человека интерфазная гибель регистрируется только после облучения при дозах в десятки и сотни грей. При меньших дозах наблюдается репродуктивная форма гибели, причиной которой, как упоминалось, в большинстве случаев являются структурные хромосомные повреждения.

Репродуктивная гибель u Какие же реакции приводят делящиеся и малодифференцированные клетки к гибели?

Летальные реакции u u Основной причиной репродуктивной гибели клеток являются структурные повреждения ДНК, возникающие под влиянием облучения. Они легко обнаруживаются, в частности, цитологическими методами в виде так называемых хромосомных перестроек или аберраций хромосом. При этом разорванные хромосомы могут соединяться неправильно, а очень часто отдельные фрагменты их просто теряются при делении.

Летальные реакции u u Возникающие хромосомные перестройки весьма разнообразны. Отметим лишь основные виды аберраций: - фрагментация хромосом - формирование хромосомных мостов - дицентриков - кольцевых хромосом - появление внутри- и меж хромосомных обменов и т. п.

Летальные реакции u Часть аберраций, как, например, мосты, механически препятствует делению клетки; появление обменов и ацентрических фрагментов приводит к неравномерному разделению хромосом и утрате генетического материала, вызывающей гибель клетки из-за нехватки метаболитов, синтез которых кодировался ДНК утраченной части хромосомы.

Летальные реакции u Долю клеток с хромосомными перестройками часто используют в качестве количественного показателя радиочувствительности, так как, с одной стороны, число таких перестроек четко зависит от дозы облучения, а с другой — они, отражая летальное действие излучений, хорошо коррелируют с выживаемостью клеток.

Критерий клеточной радиочувствительности – кривые выживания u Существует несколько методов оценки жизнеспособности облученных клеток, основанных на определении их способности к неограниченному размножению путем образования колоний или бляшек, возникающих из одиночных клеток

Определение выживаемости клеток in vitro u Количественный метод определения выживаемости клеток, млекопитающих после облучения впервые был разработан в 1956 г. Т. Паком и П. Маркусом для культуры клеток He. La.

Описание методики u Клетки снимают со стенок культурального сосуда раствором трипсина или версена, пипетируют до получения взвеси из строго одиночных клеток и рассеивают по чашкам Петри так, чтобы в каждую чашку попало заданное количество клеток. На каждую дозу облучения и контроль берут по 5— 8 чашек. После посева чашки с клетками облучают при нескольких дозах вплоть до 10— 20 Гр и выращивают в термостате 7— 14 дней до получения видимых невооруженным глазом колоний, содержащих не менее 50 клеток. Следовательно, облученная, но сохранившая жизнеспособность клетка и ее потомки должны совершить не менее шести последовательных делений. Выживаемость клеток при каждой дозе облучения определяют как отношение числа колоний, выросших в облученных чашках, к числу колоний, выросших в контроле.
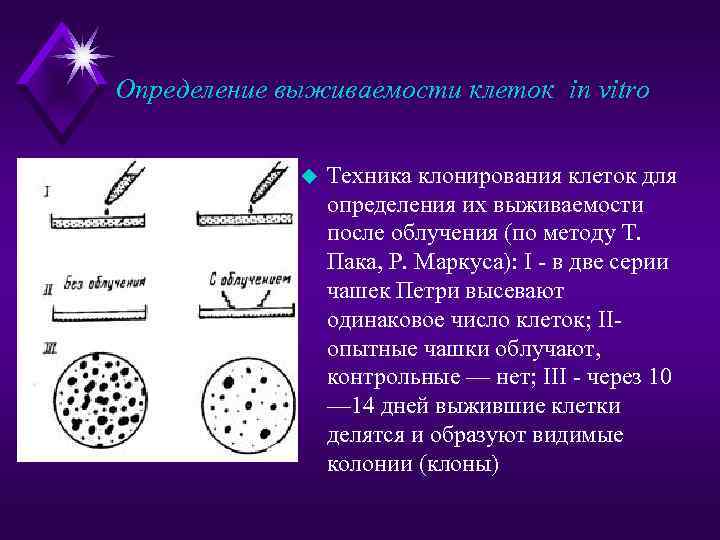
Определение выживаемости клеток in vitro u Техника клонирования клеток для определения их выживаемости после облучения (по методу Т. Пака, Р. Маркуса): I - в две серии чашек Петри высевают одинаковое число клеток; IIопытные чашки облучают, контрольные — нет; III - через 10 — 14 дней выжившие клетки делятся и образуют видимые колонии (клоны)
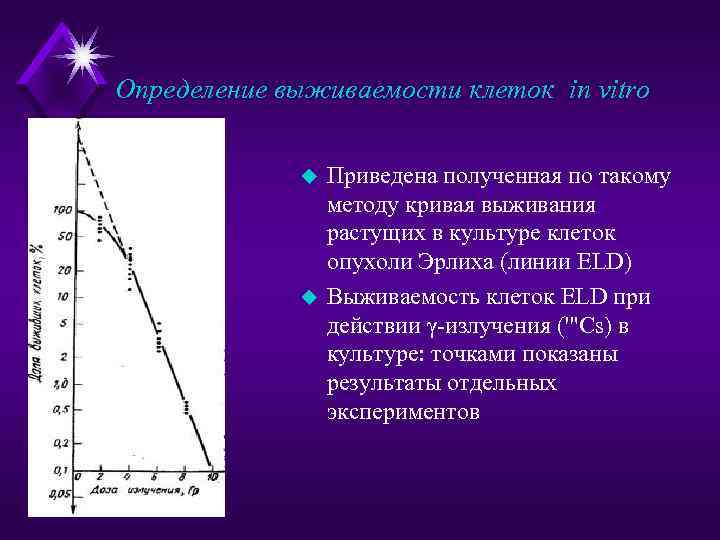
Определение выживаемости клеток in vitro u u Приведена полученная по такому методу кривая выживания растущих в культуре клеток опухоли Эрлиха (линии ELD) Выживаемость клеток ELD при действии γ-излучения ('"Cs) в культуре: точками показаны результаты отдельных экспериментов

Определение выживаемости клеток in vivo u u u В настоящее время радиобиологи имеют возможность в эксперименте количественно оценивать радиочувствительность многих тканей и опухолей, сравнивая кривые выживания клеток после облучения (в том числе in vivo). Используют клетки, выросшие in vivo, облученные in vivo, с последующей оценкой колониеобразования in vitro Кривые выживания самых различных клеток при действии рентгеновского, гамма- или любого другого редко ионизирующего излучения имеют форму, аналогичную приведенной на следующем рисунке
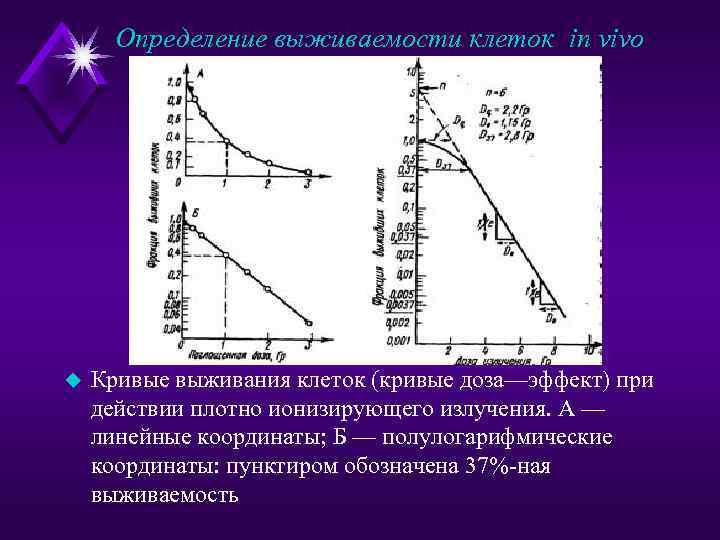
Определение выживаемости клеток in vivo u Кривые выживания клеток (кривые доза—эффект) при действии плотно ионизирующего излучения. А — линейные координаты; Б — полулогарифмические координаты: пунктиром обозначена 37%-ная выживаемость
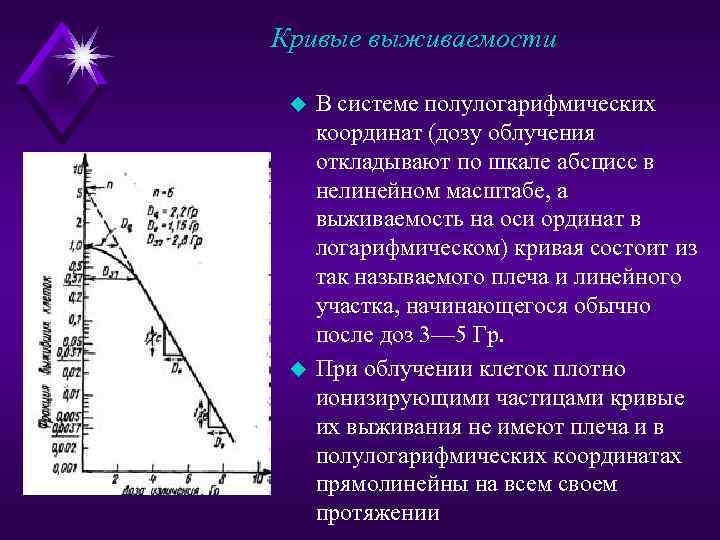
Кривые выживаемости u u В системе полулогарифмических координат (дозу облучения откладывают по шкале абсцисс в нелинейном масштабе, а выживаемость на оси ординат в логарифмическом) кривая состоит из так называемого плеча и линейного участка, начинающегося обычно после доз 3— 5 Гр. При облучении клеток плотно ионизирующими частицами кривые их выживания не имеют плеча и в полулогарифмических координатах прямолинейны на всем своем протяжении

Кривые выживаемости u Такая зависимость хорошо описывается уравнением вида где N — число выживших клеток из общего их числа, D — любая доза облучения, D 0 — доза, при которой доля живых клеток уменьшается в сравнении с исходной в е раз: N/N 0 = е-1 = 1/2, 71 = 0, 367. Таким образом, при дозе облучения, равной D 0, выживает ~37%, а погибает ~63 % клеток.
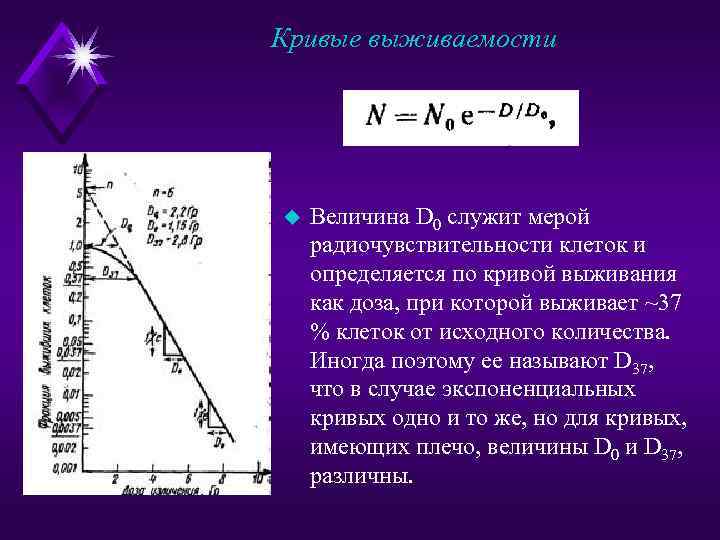
Кривые выживаемости u Величина D 0 служит мерой радиочувствительности клеток и определяется по кривой выживания как доза, при которой выживает ~37 % клеток от исходного количества. Иногда поэтому ее называют D 37, что в случае экспоненциальных кривых одно и то же, но для кривых, имеющих плечо, величины D 0 и D 37, различны.

Кривые выживаемости u Кривые, имеющие плечо, кроме величины D 0, определяющей наклон ее линейного участка, характеризуются еще и так называемым экстраполяционным числом n. Оно определяется в месте пересечения ординаты экстраполированным прямолинейным участком кривой выживания. Здесь величина D 0 определяется как инкремент (приращение) дозы, снижающей выживаемость в е раз на прямолинейном участке кривой выживания.

Кривые выживаемости u Мерой способности клеток к репарации является величина плеча, оцениваемая квазипороговой дозой Dq. Она измеряется длиной отрезка прямой, параллельной оси абсцисс, проведенной на уровне 100%-ной выживаемости от оси ординат до точки пересечения с экстраполированным участком кривой выживания

Кривые выживаемости u u Летальные реакции клеток имеют специфическую особенность, отличающую их от рассмотренных выше обратимых преходящих клеточных эффектов. Эта особенность состоит в том, что с увеличением дозы облучения увеличивается не только (и даже не столько) степень поражения всех облученных клеток, как это имеет место, например, в отношении задержки деления, сколько доля пораженных, т. е. погибших, клеток. Иными словами, с одной стороны, даже при самых малых дозах может быть зарегистрирован экстремальный эффект - гибель клетки (разумеется, с малой вероятностью), с другой - и при очень больших дозах (опять же с малой вероятностью) могут сохраниться отдельные жизнеспособные клетки.

Аберрации хромосом - критерий летального поражения клеток u Одним из часто используемых количественных методов оценки летального поражения пролиферирующих клеток служит подсчет числа клеток с аберрациями хромосом. u В конце 50 -х годов было установлено, что между числом выживающих после облучения клеток и числом клеток без хромосомных перестроек существует тесная корреляция
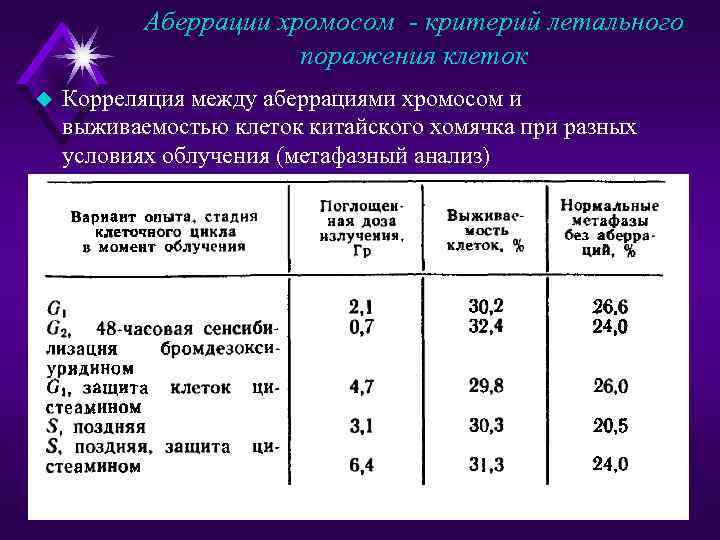
Аберрации хромосом - критерий летального поражения клеток u Корреляция между аберрациями хромосом и выживаемостью клеток китайского хомячка при разных условиях облучения (метафазный анализ)

Аберрации хромосом - критерий летального поражения клеток u u Согласно данным метафазного анализа существует полный параллелизм в изменении выживаемости клеток и долей безаберрантных клеток при облучении клеточной культуры, синхронизированной на отдельных периодах интерфазы, а также в условиях защиты или сенсибилизации. При дозах облучения, различающихся даже в 9 раз, но вызывающих одно и то же подавление жизнеспособности клеток, одинаковой оказывается и доля безаберрантных клеток.

Аберрации хромосом - критерий летального поражения клеток u Доля клеток без хромосомных аберраций несколько меньше доли выживших клеток, способных к образованию колоний. Это может быть объяснено тем, что некоторые аберрации обусловливают гибель только одного из потомков облученной клетки, вызывая образование неполноценных абортивных колоний. Близкое соответствие кривых гибели и снижения числа клеток аберраций хромосом наблюдается и при учете аберраций не в метафазе, а в анафазе
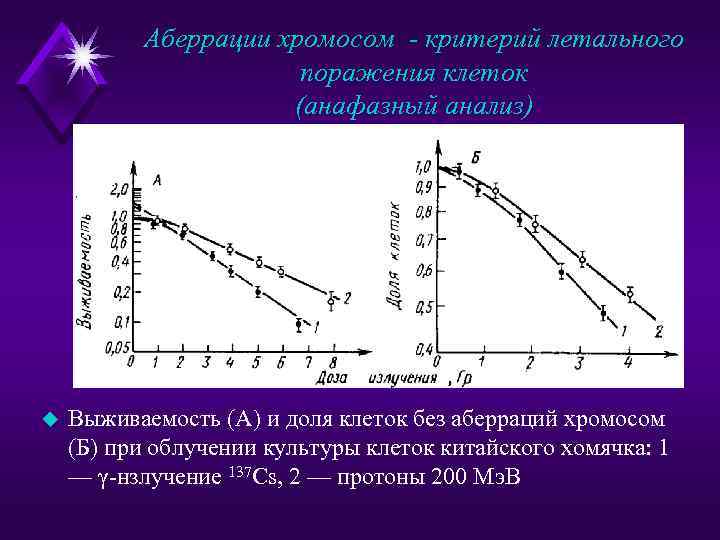
Аберрации хромосом - критерий летального поражения клеток (анафазный анализ) u Выживаемость (A) и доля клеток без аберраций хромосом (Б) при облучении культуры клеток китайского хомячка: 1 — γ-нзлучение 137 Cs, 2 — протоны 200 Мэ. В

Аберрации хромосом - критерий летального поражения клеток (анафазный анализ) u число клеток без аберраций здесь несколько больше числа выживших клеток. Это определяется тем, что анафазный метод выявляет не все аберрации (по некоторым данным, в два раза меньше, чем метафазный), например, потому, что фрагменты увлекаются расходящимися хромосомами в анафазные "шапки", где их нельзя обнаружить. Но и в этом случае существует соответствие характера кривых, а одинаковое снижение эффекта облучения при переходе от γ-излучения к протонам высоких энергий, выявляемое по обоим критериям, также свидетельствует о связи аберраций хромосом с клеточной гибелью.

Аберрации хромосом - критерий летального поражения клеток (анафазный анализ) u Отсутствие полного соответствия между выживаемостью клеток и возникновением аберраций (во многих работах отмечено 20 — 30%-ное расхождение между уровнем погибших и аберрантных клеток) не умаляет роли аберраций хромосом в качестве пригодного количественного критерия клеточной радиочувствительности.

Аберрации хромосом - критерий летального поражения клеток (анафазный анализ) u Отсутствие полного соответствия между выживаемостью клеток и возникновением аберраций (во многих работах отмечено 20 — 30%-ное расхождение между уровнем погибших и аберрантных клеток) не умаляет роли аберраций хромосом в качестве пригодного количественного критерия клеточной радиочувствительности.
занятие 9-10.ppt