Лекция по органике 9.ppt
- Количество слайдов: 37

Реакции карбоновых кислот и их производных Лекция 9
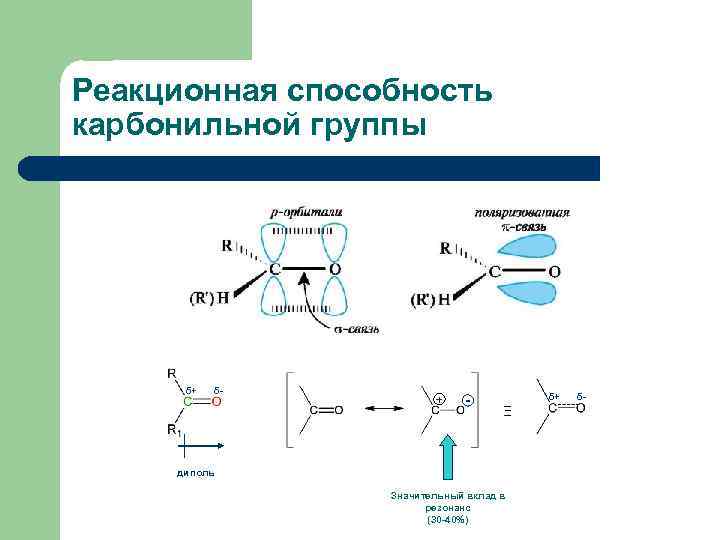
Реакционная способность карбонильной группы δ+ δ- + - δ+ Ξ диполь Значительный вклад в резонанс (30 -40%) δ-
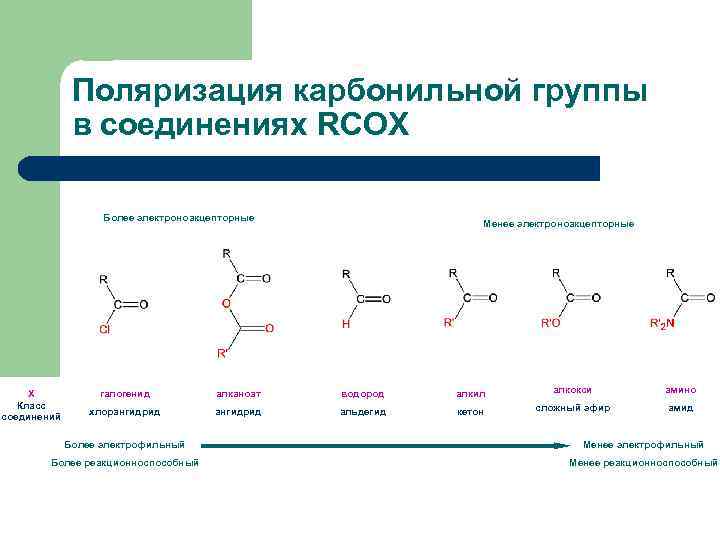
Поляризация карбонильной группы в соединениях RCOX Более электроноакцепторные Х Класс соединений Менее электроноакцепторные галогенид алканоат водород алкил алкокси амино хлорангидрид альдегид кетон сложный эфир амид Более электрофильный Менее электрофильный Более реакционноспособный Менее реакционноспособный
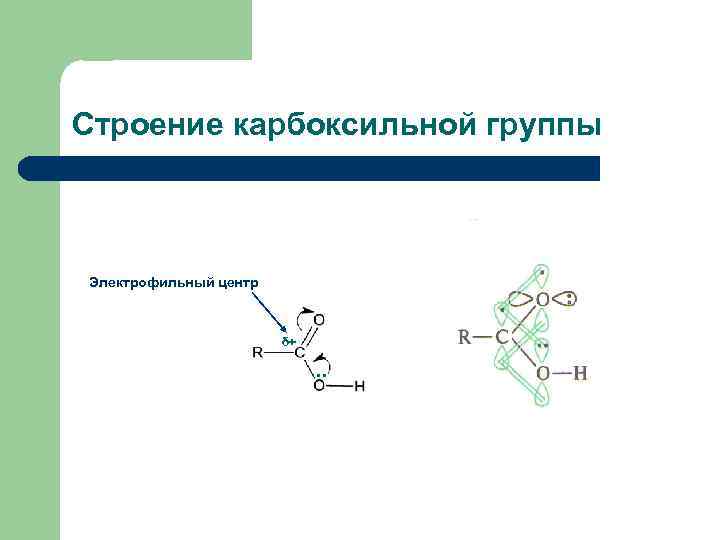
Строение карбоксильной группы Электрофильный центр δ+ . .
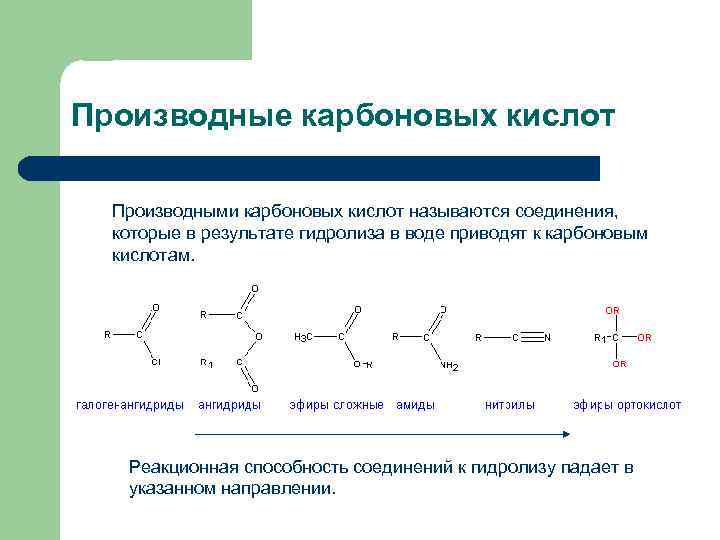
Производные карбоновых кислот Производными карбоновых кислот называются соединения, которые в результате гидролиза в воде приводят к карбоновым кислотам. Реакционная способность соединений к гидролизу падает в указанном направлении.
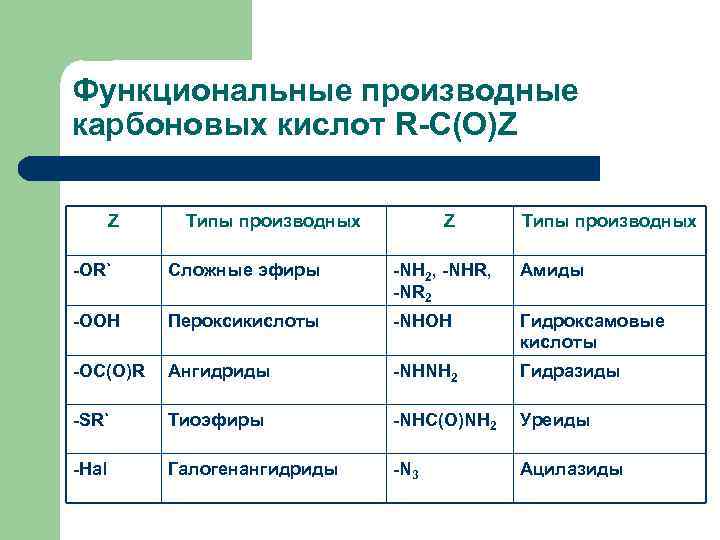
Функциональные производные карбоновых кислот R-C(O)Z Z Типы производных -OR` Сложные эфиры -NH 2, -NHR, -NR 2 Амиды -OOH Пероксикислоты -NHOH Гидроксамовые кислоты -OC(O)R Ангидриды -NHNH 2 Гидразиды -SR` Тиоэфиры -NHC(O)NH 2 Уреиды -Hal Галогенангидриды -N 3 Ацилазиды

Номенклатура IUPAC При наименованиях карбоновых кислот выделяют самую длинную цепь углерода, включающую карбоксил. Атому углерода карбоксильной группы присваивается номер 1 и от него начинается нумерация цепи. Название формируется перечислением номеров и наименований заместителей и названия углеводорода, соответствующего общему числу атомов углерода в цепи с добавлением окончания – овая кислота.
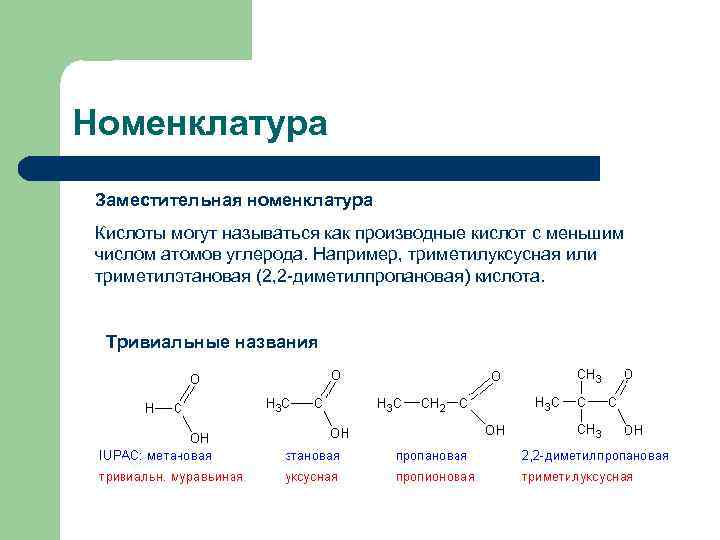
Номенклатура Заместительная номенклатура Кислоты могут называться как производные кислот с меньшим числом атомов углерода. Например, триметилуксусная или триметилэтановая (2, 2 -диметилпропановая) кислота. Тривиальные названия
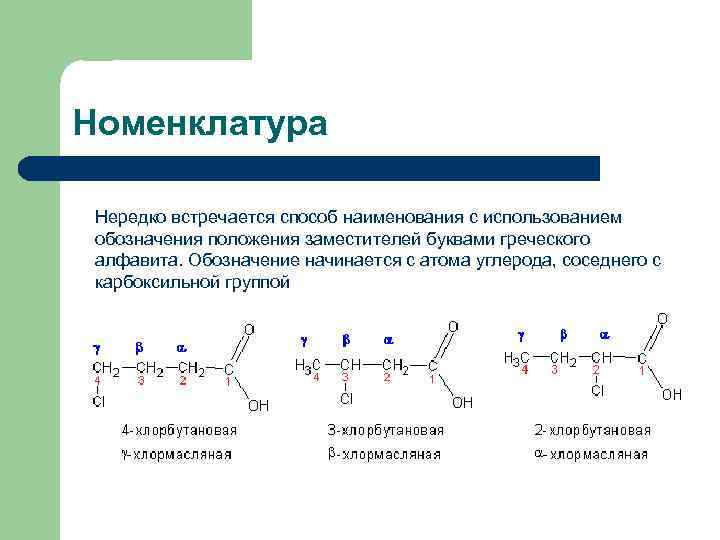
Номенклатура Нередко встречается способ наименования с использованием обозначения положения заместителей буквами греческого алфавита. Обозначение начинается с атома углерода, соседнего с карбоксильной группой
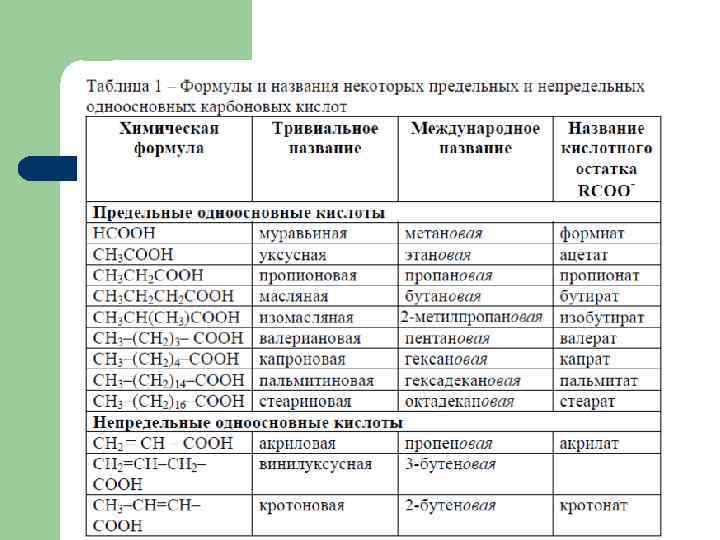
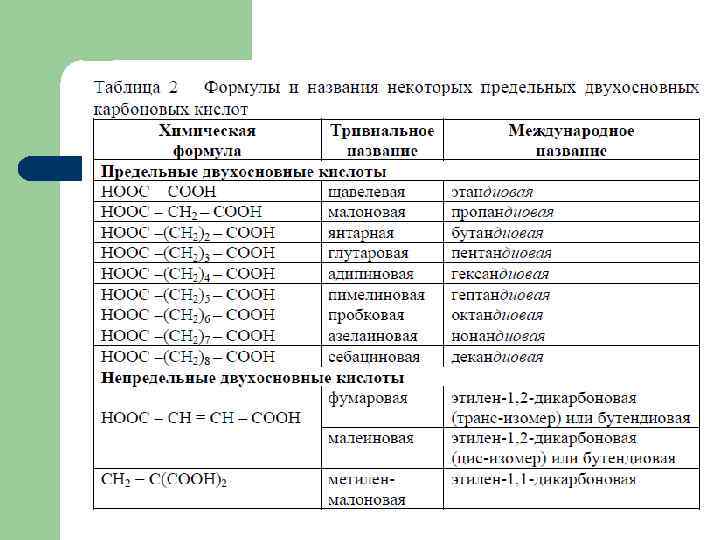
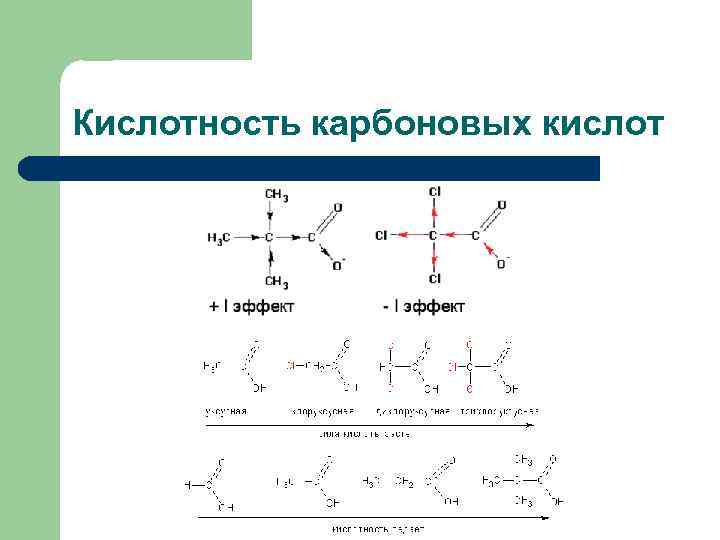
Кислотность карбоновых кислот
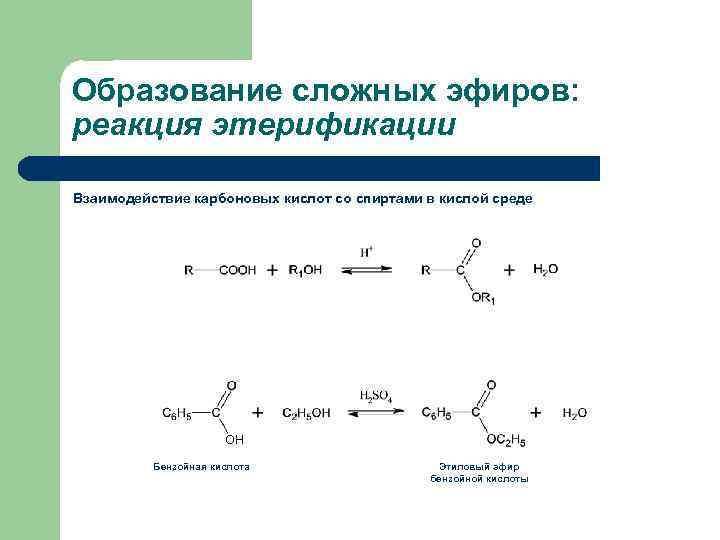
Образование сложных эфиров: реакция этерификации Взаимодействие карбоновых кислот со спиртами в кислой среде OH Бензойная кислота Этиловый эфир бензойной кислоты
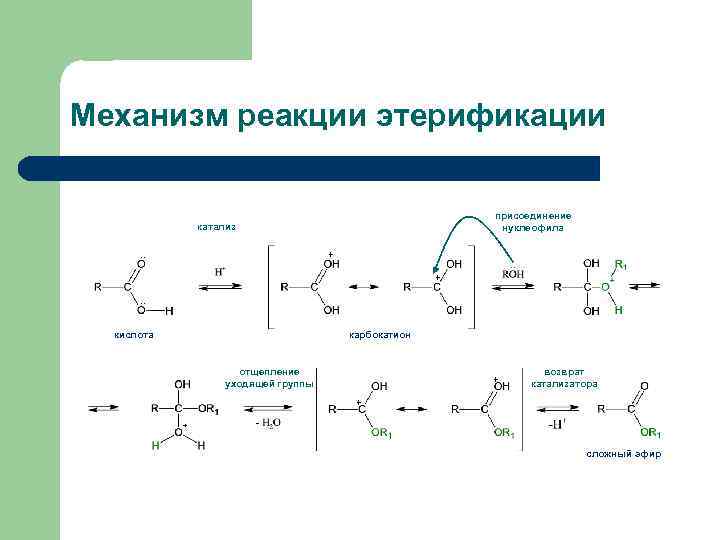
Механизм реакции этерификации присоединение нуклеофила катализ. . + . . кислота карбокатион отщепление уходящей группы + возврат катализатора + сложный эфир
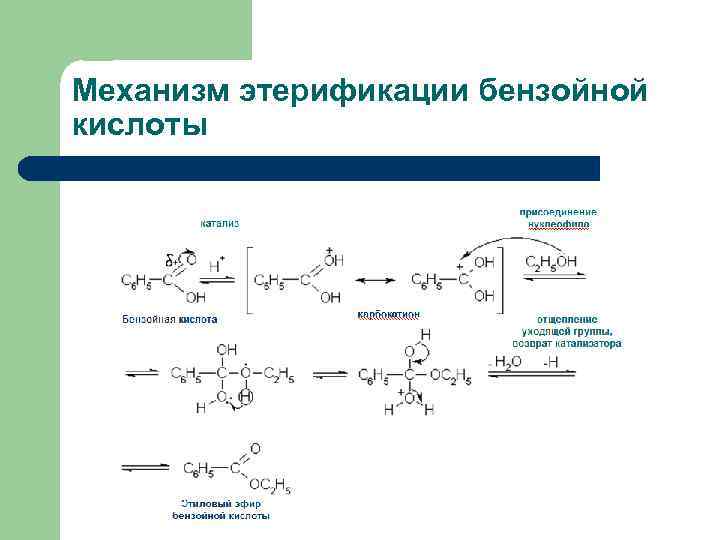
Механизм этерификации бензойной кислоты

Смещение равновесия в реакции этерификации Смещение равновесия вправо достигается: 1) Удаление воды (осушители, азеотропная отгонка) 2) Избыток одного из реагентов (обычно спирт) 3) Отгонка образующегося сложного эфира
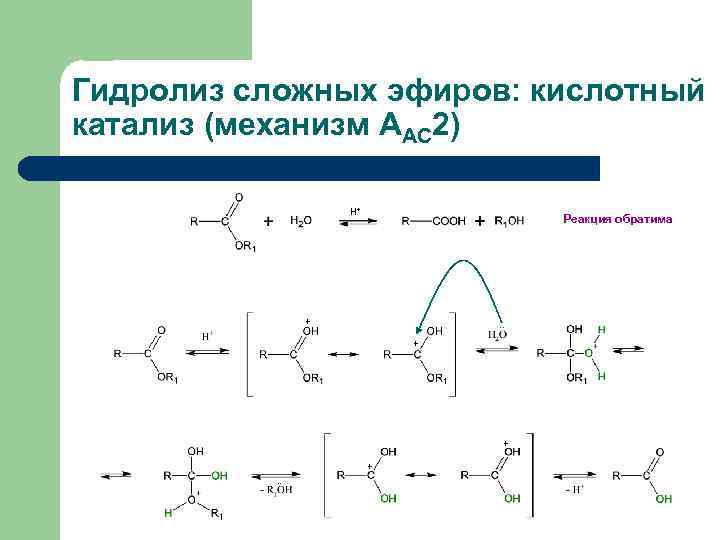
Гидролиз сложных эфиров: кислотный катализ (механизм ААС 2) Н+ Реакция обратима + . . + + +. .
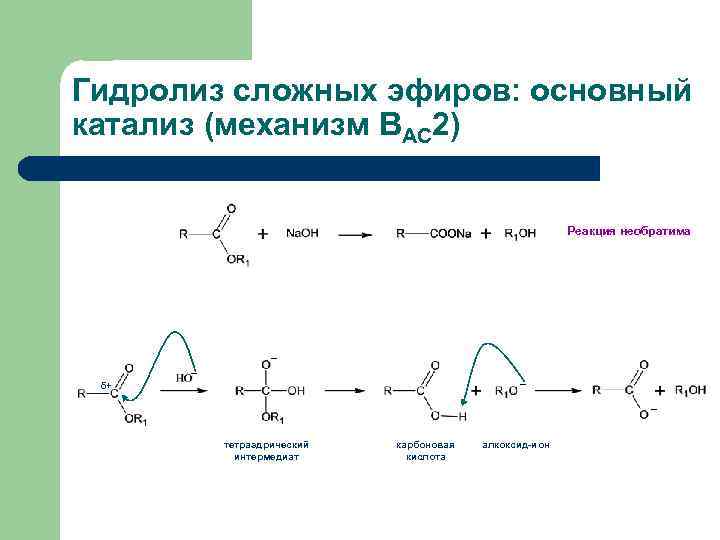
Гидролиз сложных эфиров: основный катализ (механизм ВАС 2) Реакция необратима _ _ _ δ+ _ тетраэдрический интермедиат карбоновая кислота алкоксид-ион

Скорость реакции гидролиза сложных эфиров l Бимолекулярный гидролиз, катализируемый кислотами (ААС 2): Скорость реакции = k[RCO 2 R`][H 2 O] l Бимолекулярный гидролиз, катализируемый основаниями (ВАС 2): Скорость реакции = k[RCO 2 R`][HO-]
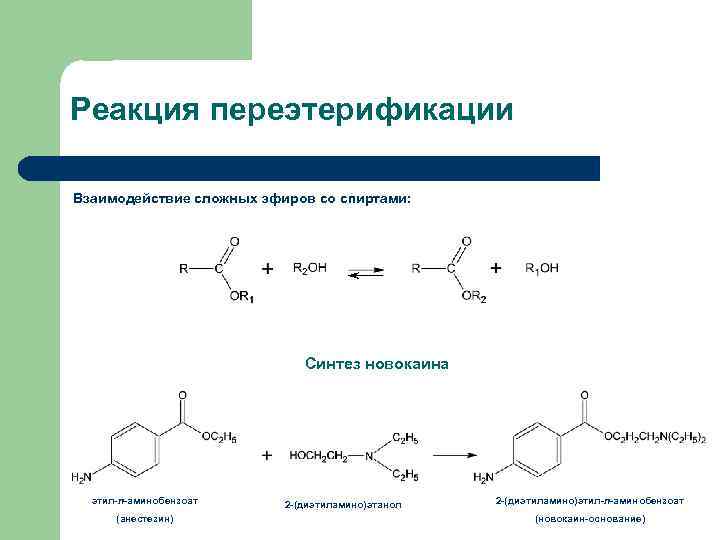
Реакция переэтерификации Взаимодействие сложных эфиров со спиртами: Синтез новокаина этил-п-аминобензоат (анестезин) 2 -(диэтиламино)этанол 2 -(диэтиламино)этил-п-аминобензоат (новокаин-основание)
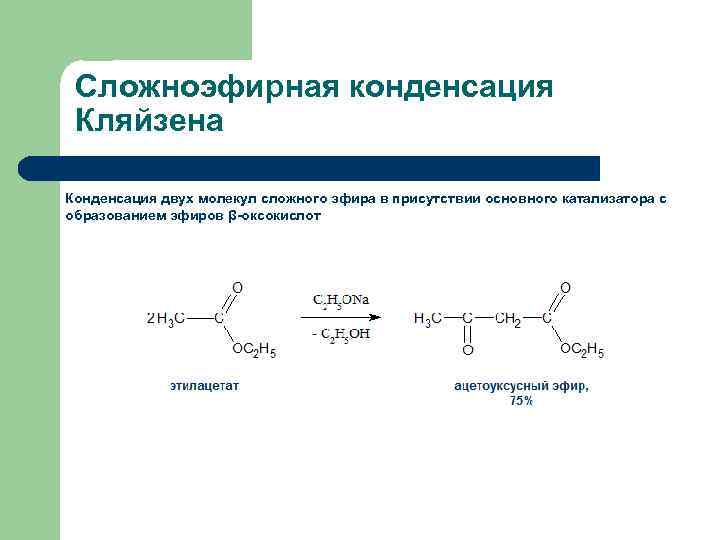
Сложноэфирная конденсация Кляйзена Конденсация двух молекул сложного эфира в присутствии основного катализатора с образованием эфиров β-оксокислот
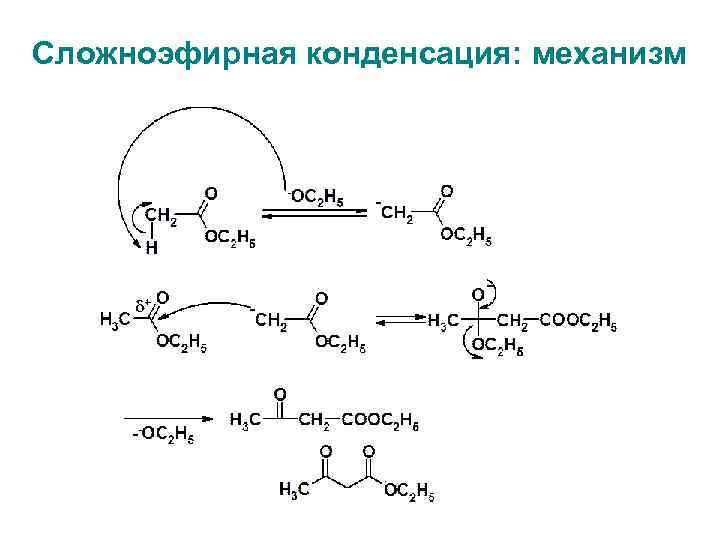
Сложноэфирная конденсация: механизм

Взаимодействие функциональных производных карбоновых кислот с реактивами Гриньяра
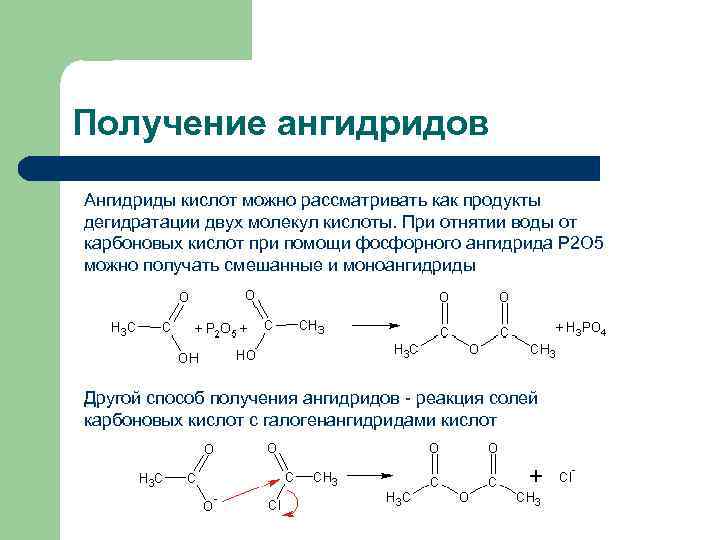
Получение ангидридов Ангидриды кислот можно рассматривать как продукты дегидратации двух молекул кислоты. При отнятии воды от карбоновых кислот при помощи фосфорного ангидрида Р 2 О 5 можно получать смешанные и моноангидриды Другой способ получения ангидридов - реакция солей карбоновых кислот с галогенангидридами кислот
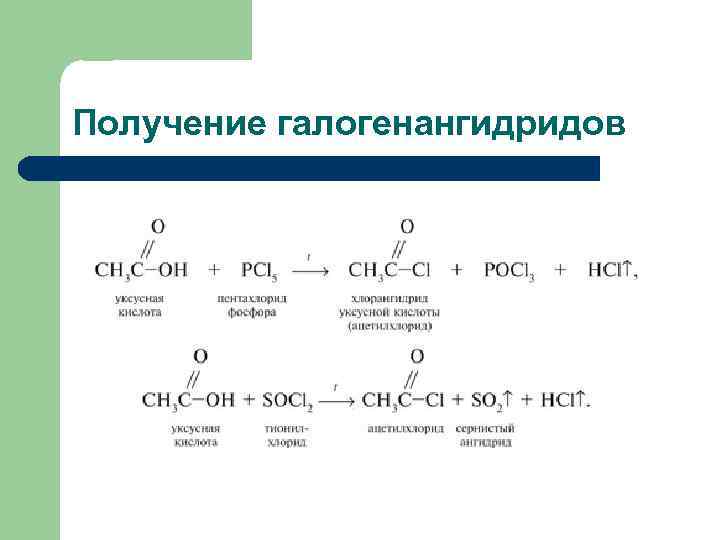
Получение галогенангидридов

Получение α-галогенпроизводных Вследствие электроноакцепторного влияния карбоксильной группы атомы водорода при углероде в α-положении довольно подвижные и могут замещаться на атомы хлора или брома
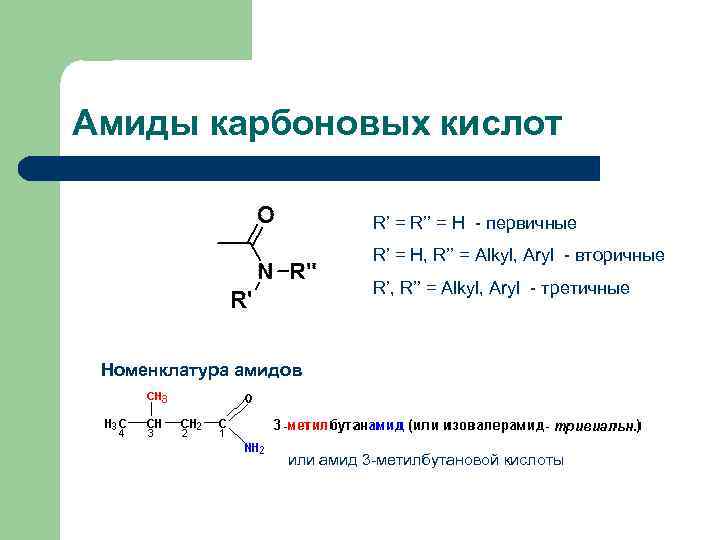
Амиды карбоновых кислот R’ = R’’ = H - первичные R’ = H, R’’ = Alkyl, Aryl - вторичные R’, R’’ = Alkyl, Aryl - третичные Номенклатура амидов или амид 3 -метилбутановой кислоты
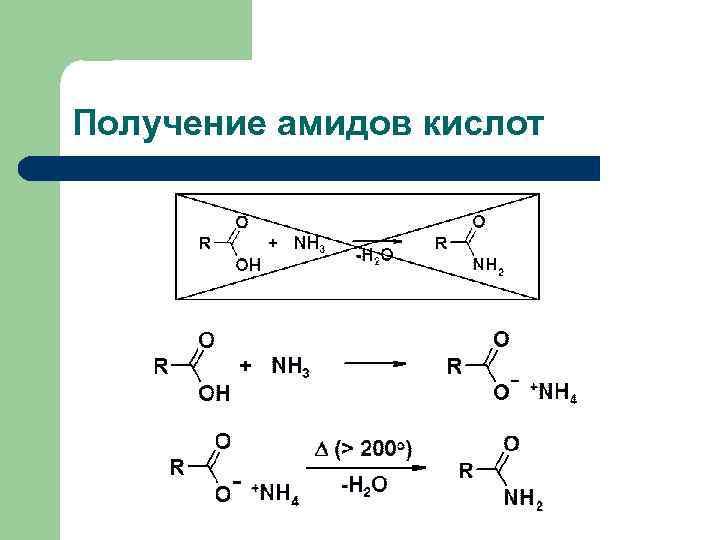
Получение амидов кислот
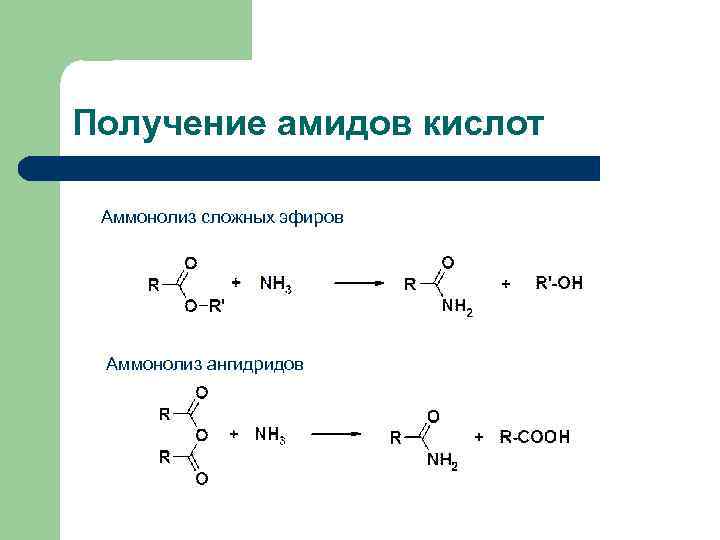
Получение амидов кислот Аммонолиз сложных эфиров Аммонолиз ангидридов
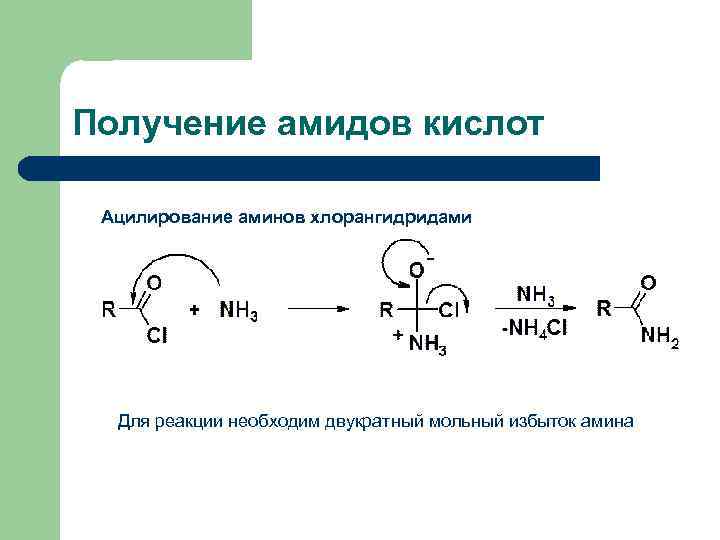
Получение амидов кислот Ацилирование аминов хлорангидридами Для реакции необходим двукратный мольный избыток амина
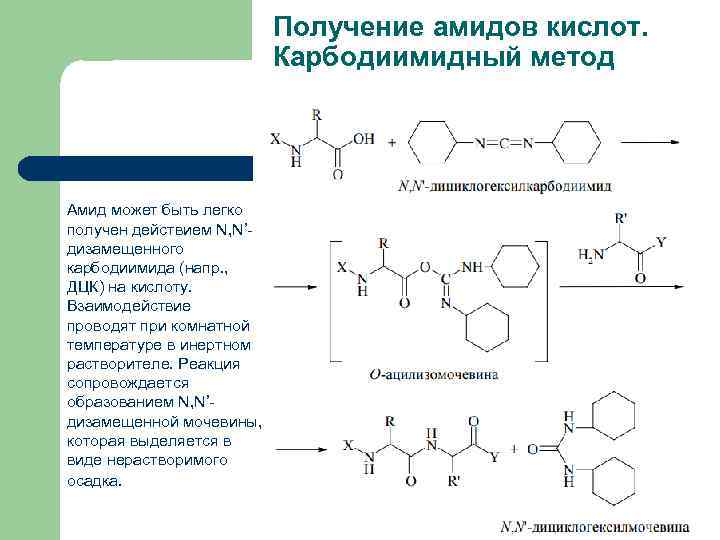
Получение амидов кислот. Карбодиимидный метод Амид может быть легко получен действием N, N’дизамещенного карбодиимида (напр. , ДЦК) на кислоту. Взаимодействие проводят при комнатной температуре в инертном растворителе. Реакция сопровождается образованием N, N’дизамещенной мочевины, которая выделяется в виде нерастворимого осадка.
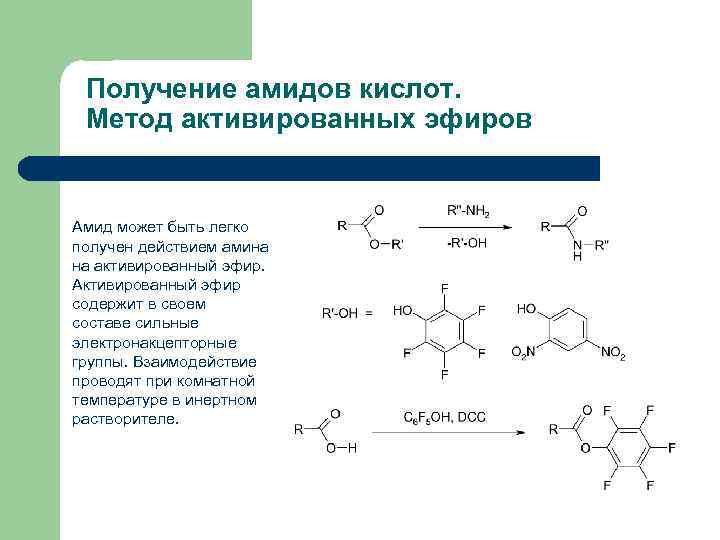
Получение амидов кислот. Метод активированных эфиров Амид может быть легко получен действием амина на активированный эфир. Активированный эфир содержит в своем составе сильные электронакцепторные группы. Взаимодействие проводят при комнатной температуре в инертном растворителе.
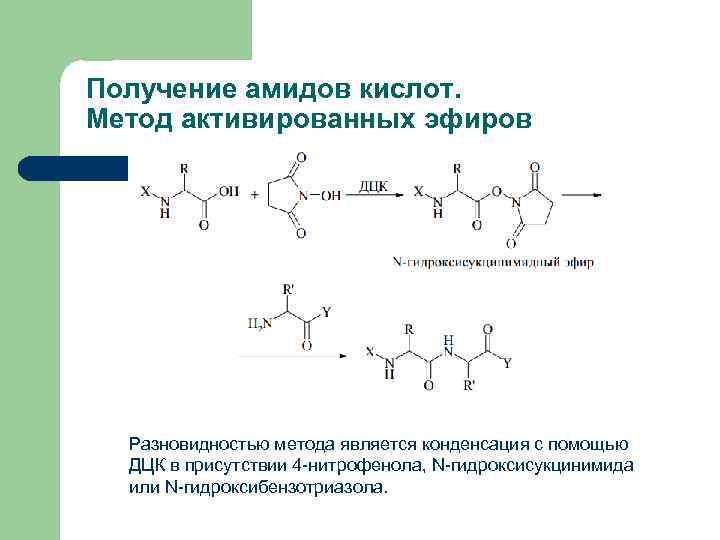
Получение амидов кислот. Метод активированных эфиров Разновидностью метода является конденсация с помощью ДЦК в присутствии 4 -нитрофенола, N-гидроксисукцинимида или N-гидроксибензотриазола.
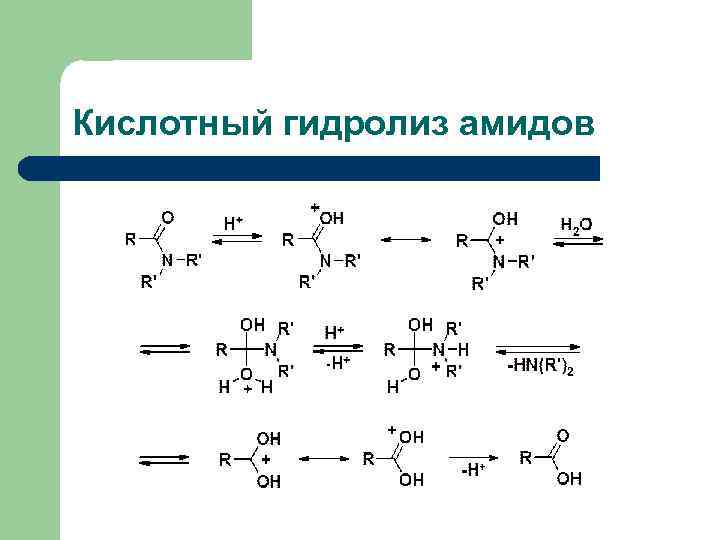
Кислотный гидролиз амидов
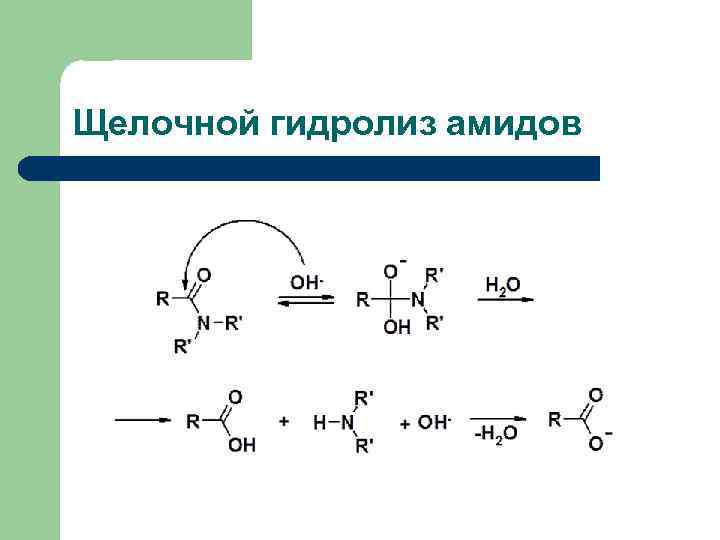
Щелочной гидролиз амидов
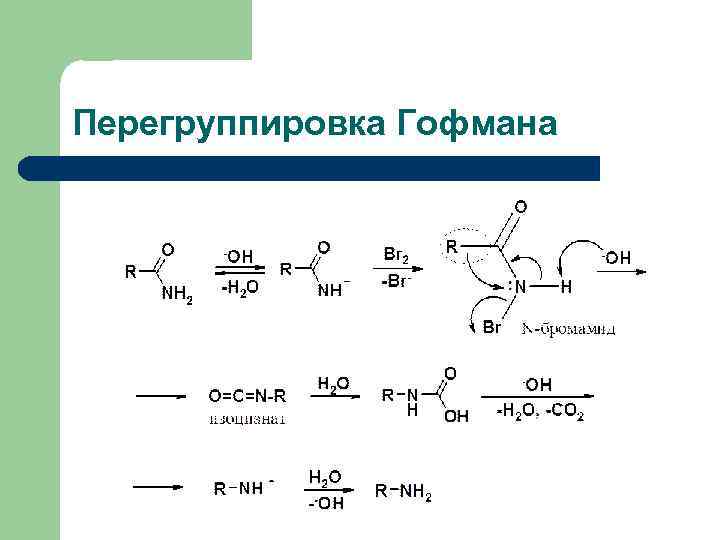
Перегруппировка Гофмана

Благодарю за внимание!
Лекция по органике 9.ppt