Лекция по органике_10.ppt
- Количество слайдов: 40

Реакции β-элиминирования Лекция 10

Реакции элиминирования (отщепления) – реакции, при которых происходит расщепление тех или иных связей в молекуле с образованием новых устойчивых молекул, стабильных или нестабильных частиц, например, ненасыщенных соединений, циклов, радикалов, бирадикалов и др.
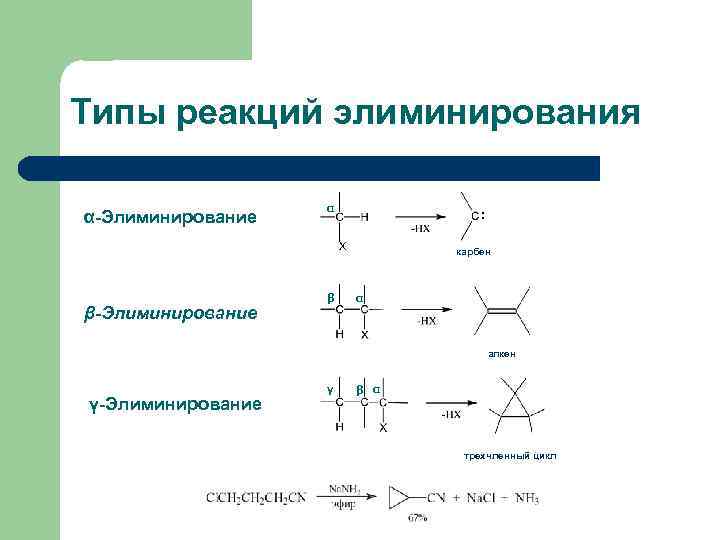
Типы реакций элиминирования α-Элиминирование α : X β-Элиминирование β карбен α алкен γ-Элиминирование γ β α трехчленный цикл

β-Элиминирование - β-Элиминирование (Е) – отщепление протона и группы Х от соседних атомов углерода с образованием кратной углеродной связи β α Атом углерода, от которого отщепляется группа Х - α-атом Атом углерода, от которого отщепляется протон – β-атом

Электронные переходы при βэлиминировании 1 2 3 Y: • Мономолекулярный механизм Е 1 – двухстадийный процесс, переход 3 осуществляется раньше переходов 1 и 2 • Бимолекулярный механизм Е 2 – одновременные электронные переходы • Мономолекулярное отщепление по сопряженному основанию Е 1 с. В – двухстадийный процесс, переход 1 предшествует переходам 2 и 3
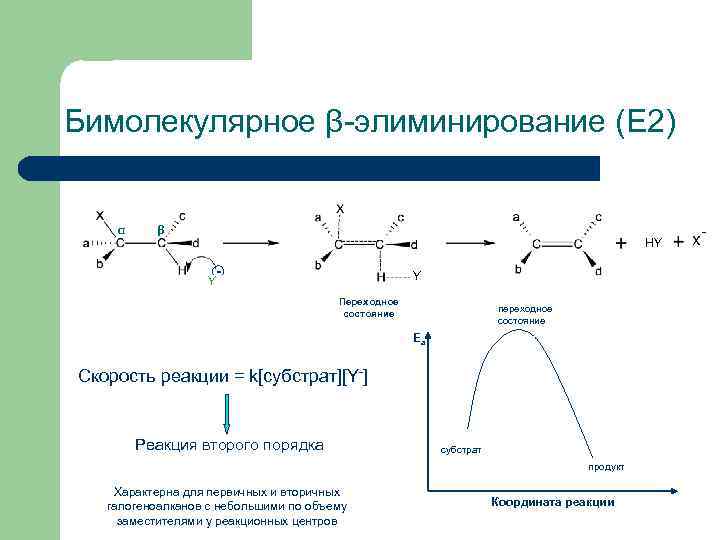
Бимолекулярное β-элиминирование (E 2) α β HY - Y Y Переходное состояние переходное состояние Еа Скорость реакции = k[субстрат][Y-] Реакция второго порядка субстрат продукт Характерна для первичных и вторичных галогеноалканов с небольшими по объему заместителями у реакционных центров Координата реакции -
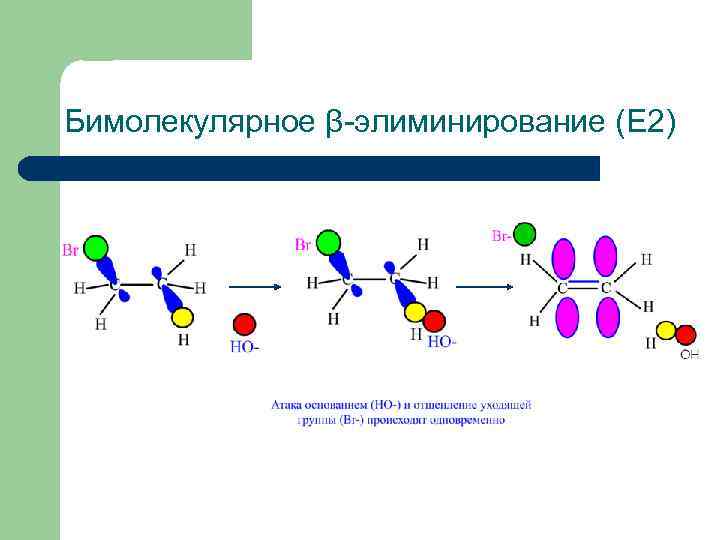
Бимолекулярное β-элиминирование (E 2)
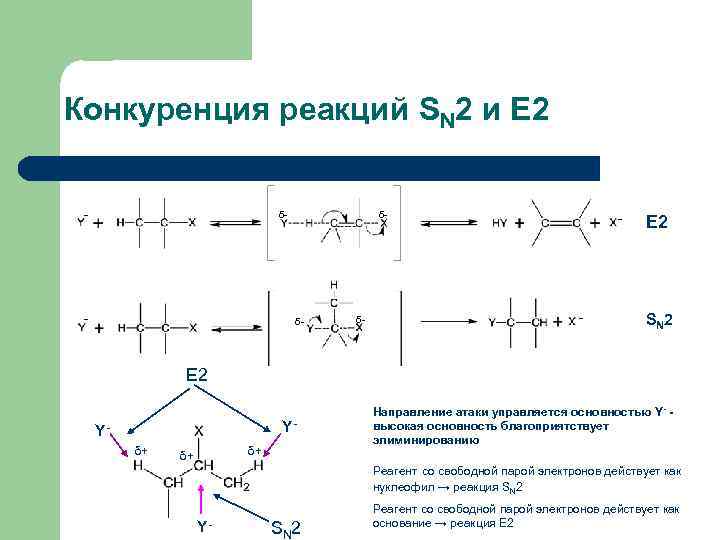
Конкуренция реакций SN 2 и Е 2 - δ- δ- δ- - - E 2 S N 2 E 2 Y- Yδ+ δ+ δ+ Направление атаки управляется основностью Y- - высокая основность благоприятствует элиминированию Реагент со свободной парой электронов действует как нуклеофил → реакция SN 2 Y- SN 2 Реагент со свободной парой электронов действует как основание → реакция E 2

Конкуренция реакций SN 2 и Е 2
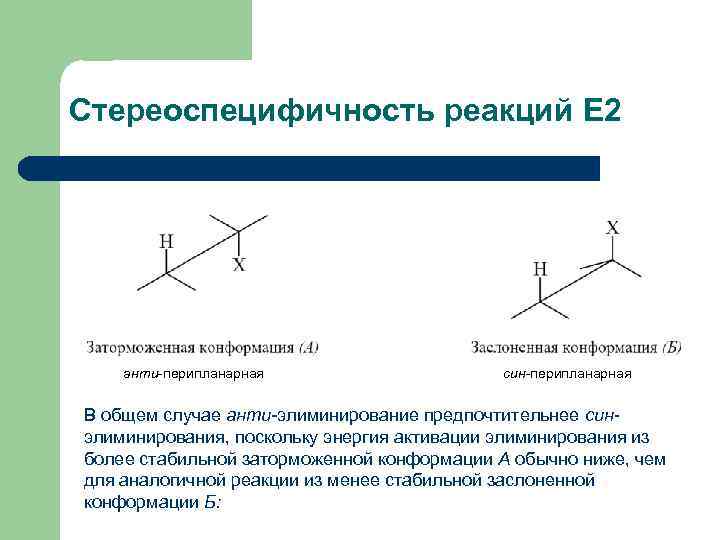
Стереоспецифичность реакций Е 2 анти-перипланарная син-перипланарная В общем случае анти-элиминирование предпочтительнее синэлиминирования, поскольку энергия активации элиминирования из более стабильной заторможенной конформации А обычно ниже, чем для аналогичной реакции из менее стабильной заслоненной конформации Б:
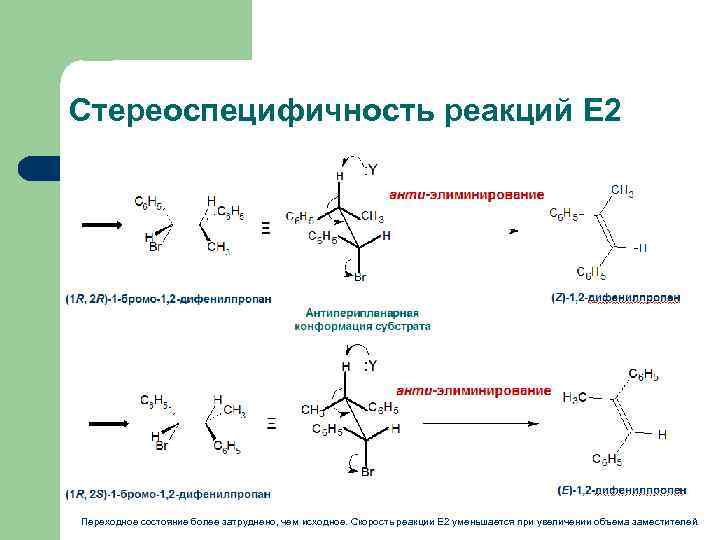
Стереоспецифичность реакций Е 2 Переходное состояние более затруднено, чем исходное. Скорость реакции Е 2 уменьшается при увеличении объема заместителей.
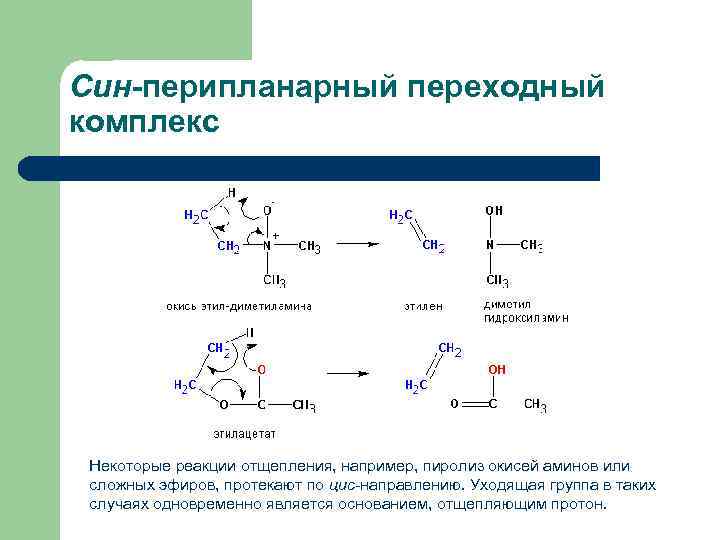
Син-перипланарный переходный комплекс Некоторые реакции отщепления, например, пиролиз окисей аминов или сложных эфиров, протекают по цис-направлению. Уходящая группа в таких случаях одновременно является основанием, отщепляющим протон.
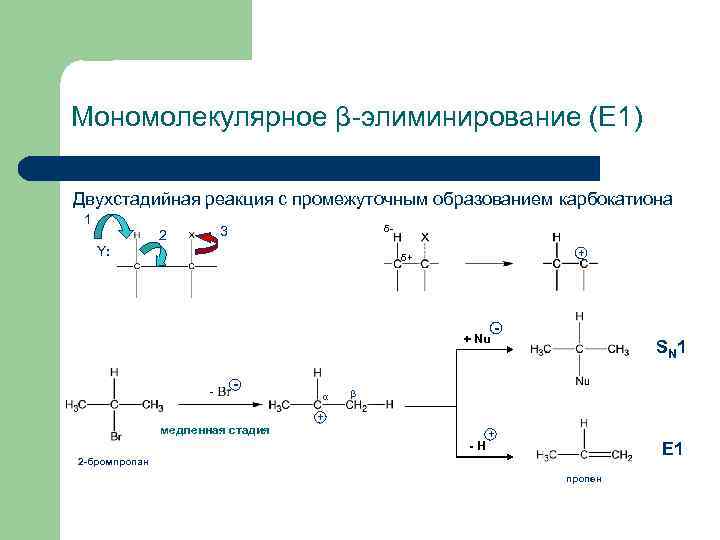
Мономолекулярное β-элиминирование (E 1) Двухстадийная реакция с промежуточным образованием карбокатиона 1 2 δ- 3 Y: + δ+ + Nu медленная стадия α - SN 1 β + - H + E 1 2 -бромпропан пропен

Мономолекулярное β-элиминирование (E 1) Схема реакции совпадает со схемой мономолекулярного замещения SN 1 до момента образования карбокатиона: Но далее, в зависимости от среды и атакующей частицы, протекает либо реакция замещения (SN 1), либо отщепление протона и образование продукта элиминирования (Е 1):
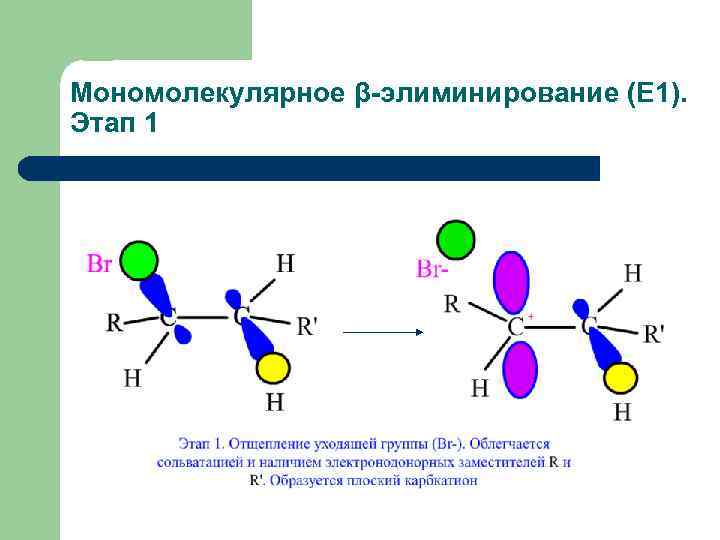
Мономолекулярное β-элиминирование (E 1). Этап 1
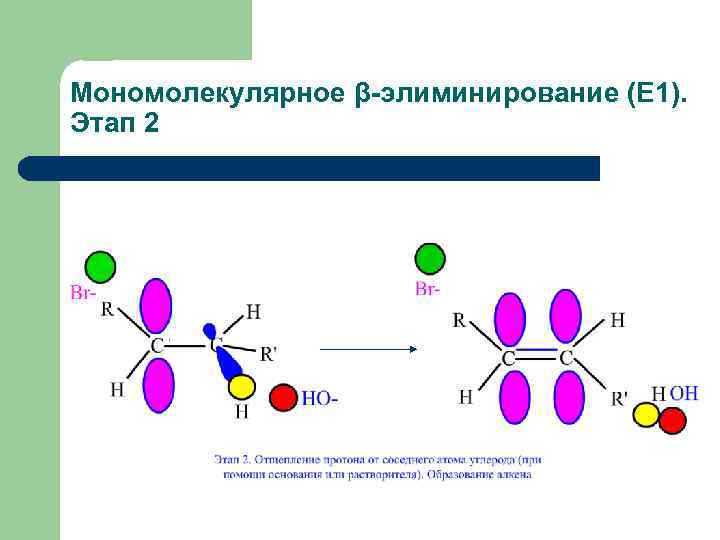
Мономолекулярное β-элиминирование (E 1). Этап 2
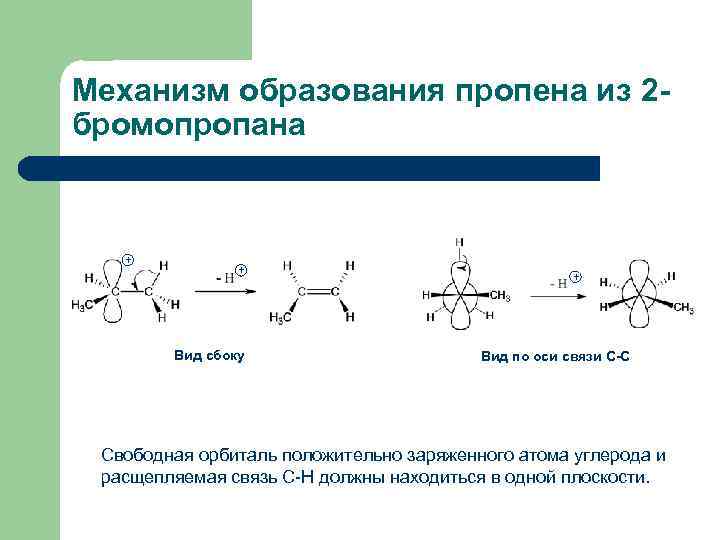
Механизм образования пропена из 2 бромопропана + + Вид сбоку + Вид по оси связи С-С Свободная орбиталь положительно заряженного атома углерода и расщепляемая связь С-Н должны находиться в одной плоскости.
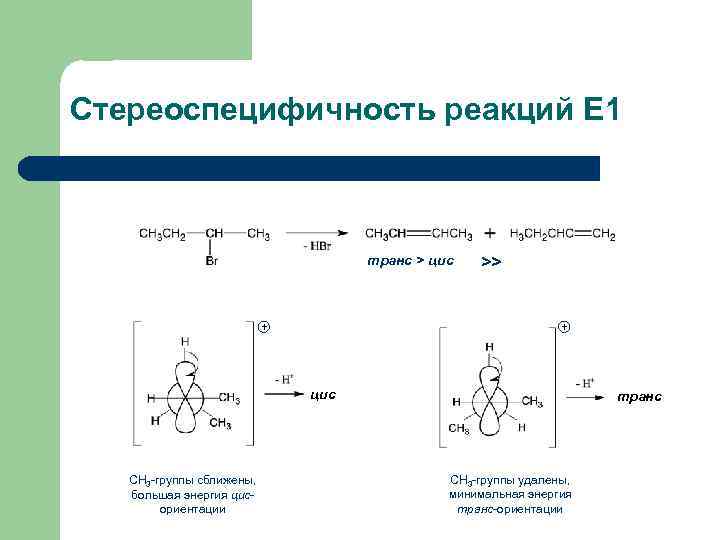
Стереоспецифичность реакций Е 1 транс > цис + >> + цис СН 3 -группы сближены, большая энергия цисориентации транс СН 3 -группы удалены, минимальная энергия транс-ориентации
![Энергетическая диаграмма реакции Е 1 + Еа Скорость реакции = k[субстрат] Еа 2 Еа Энергетическая диаграмма реакции Е 1 + Еа Скорость реакции = k[субстрат] Еа 2 Еа](https://present5.com/presentation/3/-76738116_384698759.pdf-img/-76738116_384698759.pdf-19.jpg)
Энергетическая диаграмма реакции Е 1 + Еа Скорость реакции = k[субстрат] Еа 2 Еа 1 карбокатион Реакция первого порядка Скорость реакции не зависит от концентрации основания Координата реакции
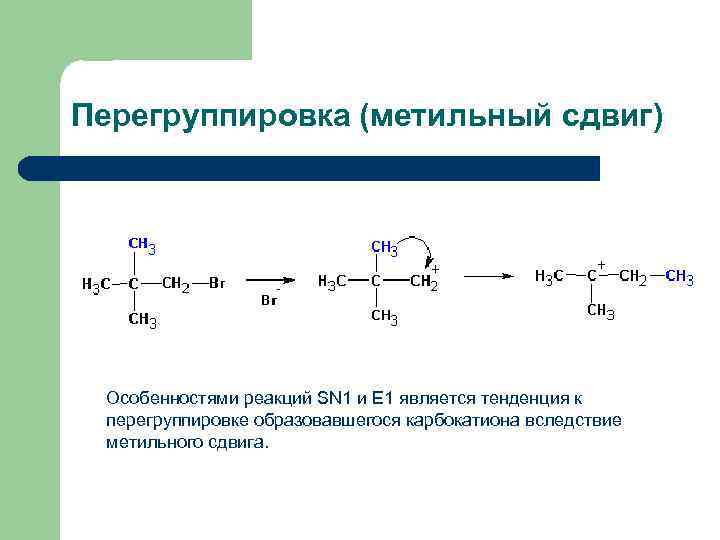
Перегруппировка (метильный сдвиг) Особенностями реакций SN 1 и Е 1 является тенденция к перегруппировке образовавшегося карбокатиона вследствие метильного сдвига.

Региоспецифичность реакций βэлиминирования I Правило Зайцева: В большинстве реакций дегидрогалогенирования атом водорода отщепляется преимущественно от соседнего наименее гидрогенизированного атома углерода атака по Сβ-Н Продукт по Зайцеву 2 -бутен 81% β’ β атака по Сβ’-Н 2 -бромобутан Продукт по Гофману 1 -бутен 19% Увеличение числа алкильных групп при двойной связи повышает ее стабильность. Поэтому в тех случаях, когда выполняется правило Зайцева, следует ожидать образования наиболее замещенного алкена

Региоспецифичность реакций βэлиминирования В случае алкилгалогенидов с различными алкильными остатками существует возможность образования двух алкенов: Для большинства реакций отщепления типа Е 2 характерно образование наиболее замещенного алкена типа II (по Зайцеву). Однако в том случае, когда уходящая группа имеет большой объем или обладает сильными электроноакцепторными свойствами, а также если атакующее основание имеет большой объем, может оказаться более благоприятным образование наименее стабильного (наименее замещенного) алкена (по Гофману).
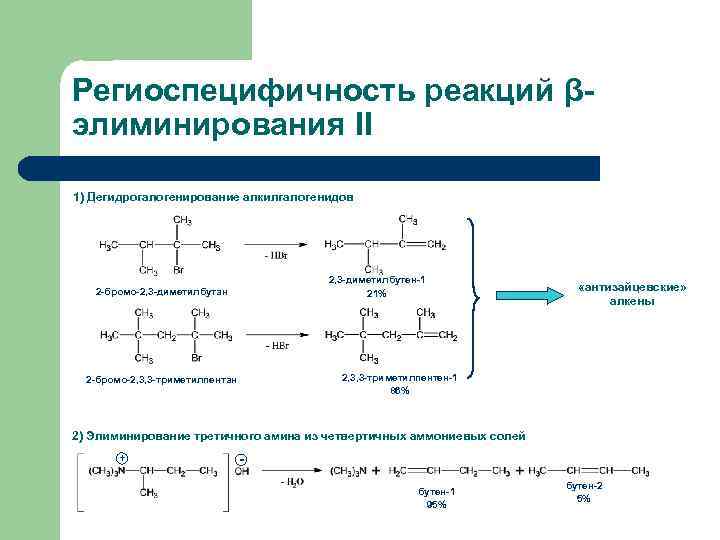
Региоспецифичность реакций βэлиминирования II 1) Дегидрогалогенирование алкилгалогенидов 2, 3 -диметилбутен-1 21% 2 -бромо-2, 3 -диметилбутан «антизайцевские» алкены 2, 3, 3 -триметилпентен-1 86% 2 -бромо-2, 3, 3 -триметилпентан 2) Элиминирование третичного амина из четвертичных аммониевых солей + бутен-1 95% бутен-2 5%

Региоспецифичность реакций βэлиминирования Е 2 Правила Зайцева и Гофмана очерчивают крайние границы в направлении E 2 -элиминирования. Реальное соотношение изомерных продуктов элиминирования, различающихся положением двойной связи, зависит главным образом от природы уходящей группы в субстрате, природы основания и пространственных факторов в субстрате.

Региоспецифичность реакций βэлиминирования: влияние размера основания 19% или 53% Увеличение объема основания приводит к увеличению доли наименее замещенного алкена в продуктах дегидрогалогенирования
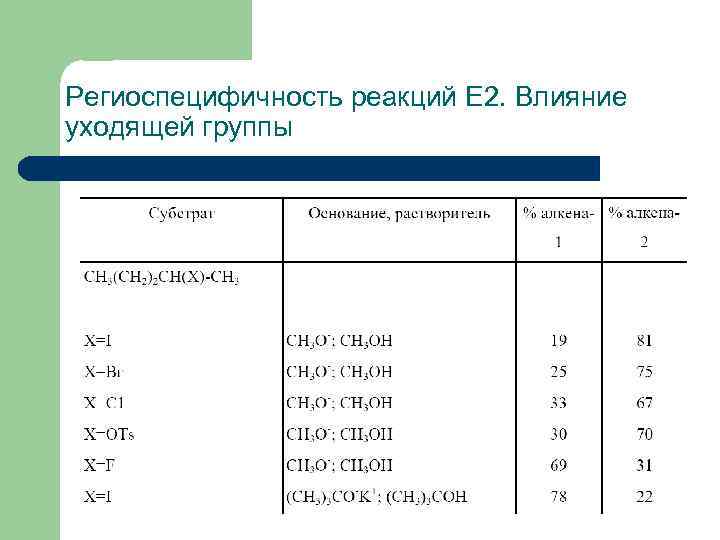
Региоспецифичность реакций Е 2. Влияние уходящей группы
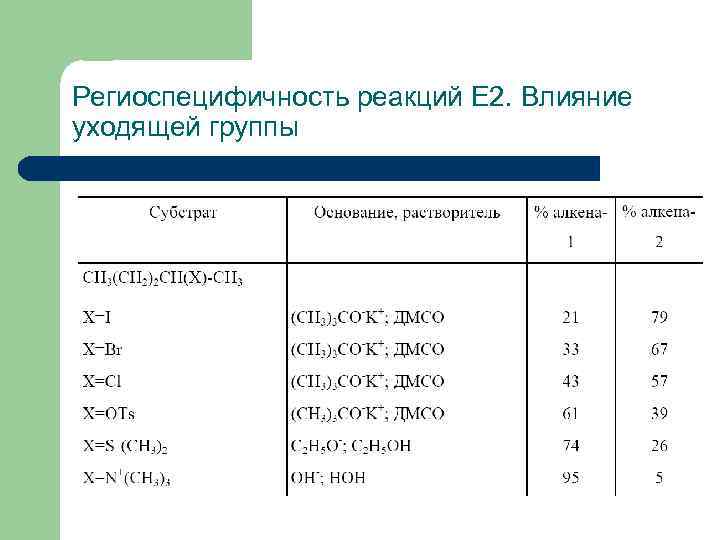
Региоспецифичность реакций Е 2. Влияние уходящей группы

Зайцев или Гофман? Доля олефина с концевой двойной связью при элиминировании в ряду втор-алкилгалогенидов возрастает в ряду: т. е. по мере того, как уходящая группа становится более электронакцепторной. Электронoакцепторные группы за счет своего (-I)-эффекта вызывают более сильную поляризацию связи βуглеродного атома с водородом, что облегчает отщепление его в виде протона при действии сильных оснований. Переходное состояние E 2 -элиминирования при наличии сильных электроотрицательных уходящих групп: F, N+R 3, S+R 2 и сильных оснований имеет явно выраженный Е 1 с. B-характер, и направление элиминирования соответствует правилу Гофмана.
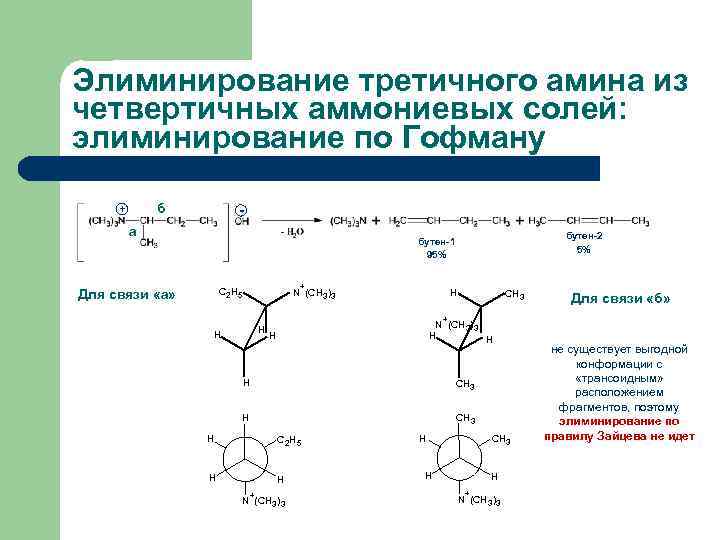
Элиминирование третичного амина из четвертичных аммониевых солей: элиминирование по Гофману б + - а бутен-2 5% бутен-1 95% Для связи «а» + C 2 H 5 N (CH 3)3 H CH 3 Для связи «б» + H H N (CH 3)3 H H CH 3 H C 2 H 5 H H + N (CH 3)3 H CH 3 H H + N (CH 3)3 не существует выгодной конформации с «трансоидным» расположением фрагментов, поэтому элиминирование по правилу Зайцева не идет
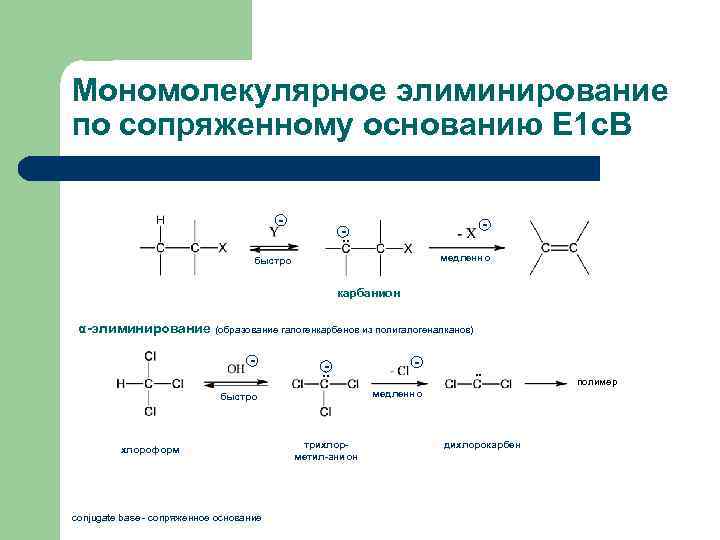
Мономолекулярное элиминирование по сопряженному основанию Е 1 c. B - - . . медленно быстро карбанион α-элиминирование (образование галогенкарбенов из полигалогеналканов) - . . conjugate base - сопряженное основание . . медленно быстро хлороформ - трихлорметил-анион дихлорокарбен полимер

Региоспецифичность реакций Е 1 c. B Реакции, протекающие по Е 1 с. В-механизму, преимущественно ограничены такими субстратами, которые содержат электроноакцепторные заместители при β-углеродном атоме, стабилизирующие промежуточно образующийся карбанион. - В реакциях Е 1 с. В образуется алкен, двойная связь которого сопряжена с двойной связью стабилизирующей группы (обладает –М-эффектом) С другой стороны, Е 1 с. B-механизм следует ожидать для субстратов, содержащих сильную электроноакцепторную уходящую группу: F; N+(CH 3)3; ОSО 2 СF 3 и др.

Факторы, влияющие на скорость реакций β-элиминирования 1) Строение субстрата 2) Свойства уходящей группы 3) Свойства основания 4) Полярность растворителя

Влияние строения субстрата на скорость β-элиминирования 1) Реакции Е 1 Заместители с +I при Сα или Сβ ускоряют Е 1 β α + Заместители с +М при Сα ускоряют Е 1 Заместители с +М, -I при Сβ замедляют Е 1 (не могут сопрягаться с вакантной р-орбиталью карбокатиона и дестабилизируют карбокатион) 2) Реакции Е 1 с. В Заместители с -I (особенно при Сβ) ускоряют Е 1 с. В . . β Заместители с -М при Сβ сильно ускоряют Е 1 с. В (сопряжение со свободной электронной α парой карбаниона) Заместители с -М при Сα слабо ускоряют Е 1 с. В 3) Реакции Е 2 1 Карбокатионный характер переходного состояния см. Е 1 β α Карбанионный характер переходного состояния см. Е 1 с. В 2 Y: 3
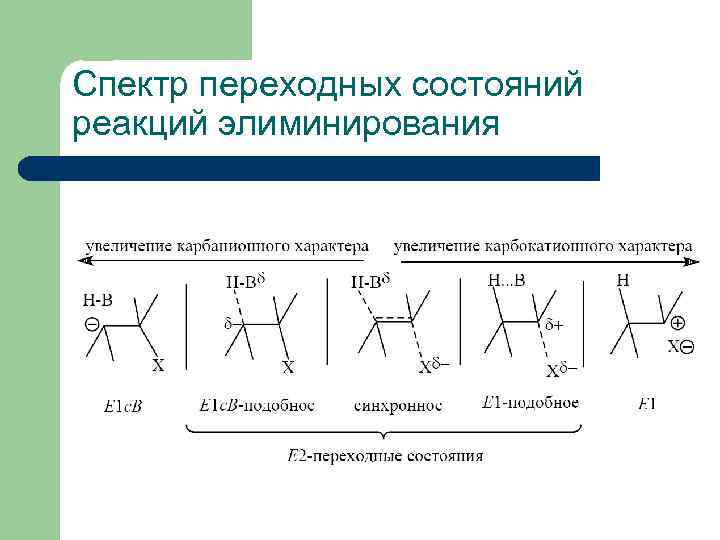
Спектр переходных состояний реакций элиминирования

Влияние уходящей группы и основания на скорость β-элиминирования 1) Влияние уходящей группы Чем легче отщепляется уходящая группа Х (т. е. чем слабее основание Х -), тем быстрее протекают реакции β-элиминирования. Пример: для органических галогенидов скорость отщепления меняется в зависимости от уходящей группы (Х) в следующем порядке: J > Br > Cl > F. Ускорение уменьшается в ряду механизмов: Е 1 > Е 2 >> Е 1 с. В 2) Влияние основания Е 1: не зависит от природы и концентрации основания (не участвует в скорость лимитирующей стадии реакции) Е 2: ускорение при увеличении силы основания Е 1 с. В: варьирование (от сильной (самая медленная стадия – первая) до слабой (скорости стадий близки между собой)) обеих

Влияние полярности растворителя на скорость β-элиминирования Если в переходном состоянии заряды более локализованы, чем в исходном, то увеличение полярности растворителя ускоряет реакцию Механизм Исходное состояние Переходное состояние Локализация зарядов Увеличение полярности растворителя Е 2 Y + RX δ- δ- Уменьшение Слабое замедление Е 2 Y + RX δ+ δ- Увеличение Сильное ускорение Е 2 + Y + RX δ- δ+ Уменьшение Сильное замедление Е 2 Y + RX + δ+ δ+ Уменьшение Слабое замедление Е 1 RX δ+ RX + δ- Увеличение Сильное ускорение δ+ δ+ Уменьшение Слабое замедление

Реакции нуклеофильного замещения и β-элиминирования в сравнении 1) Элиминированию благоприятствуют высокая температура и сильные основания - (например, -NH 2). Предпочтительным оказываются Е 2 и Е 1 с. В механизмы. 2) Замещению благоприятствуют хорошие нуклеофуги: RSO 3 3) В более полярных растворителях предпочтительно протекают реакции SN 2 по сравнению с Е 2: в Е 2 -реакциях используют спиртовой раствор КОН, в SN 2 – водный раствор КОН 4) Карбокатионы неизменно дают большее количество продукта замещения, чем элиминирования (SN 1>Е 1), и это соотношение нельзя изменить путем замены растворителя 5) Замещение при Сα способствует реакции Е 2 в большей степени, чем SN 2. Замещение при Сβ способствует элиминированию. Электроноакцепторные группы (например, Br и CN) в положении повышают кислотность водорода, связанного с Сβ и способствуют протеканию реакций Е 2 (Е 1 с. В).

Важнейшие реакции β-элиминирования 1) Дегидратация спиртов . . β α + β’ быстро медленно . . + . . Дегидратация вторичных и третичных спиртов: Е 1 Дегидратация первичных спиртов: Е 1. Для спиртов с доступным для атаки α-атомом углерода не исключен Е 2.

Важнейшие реакции β-элиминирования 2) Дегидрогалогенирование - 3) Расщепление четвертичных аммониевых оснований по Гофману +

Благодарю за внимание!
Лекция по органике_10.ppt