Дейнеко_Генериум_last.ppt
- Количество слайдов: 33

РАЗРАБОТКА СЪЕДОБНЫХ ВАКЦИН НА ОСНОВЕ ГЕНЕТИЧЕСКИ МОДИФИЦИРОВАННЫХ РАСТЕНИЙ д. б. н. , проф. Дейнеко Елена Викторовна зав. лабораторией биоинженерии растений ФГБУН Институт цитологии и генетики, Сибирское отделение РАН, Новосибирск

Производство лекарственных препаратов для фармацевтики важнейшая и динамично развивающуюся часть мировой индустрии. 2013 г. – объём фармацевтического рынка составил около 975 млрд. дол. США, с тенденцией к росту около 1, 2 трлн. дол. США к 2015 г. 2011 г. - объём биотехнологического сектора составил более 145 млрд. дол. США, с перспективой роста до 167 млрд. дол. США к 2015 г. «IMS Health»
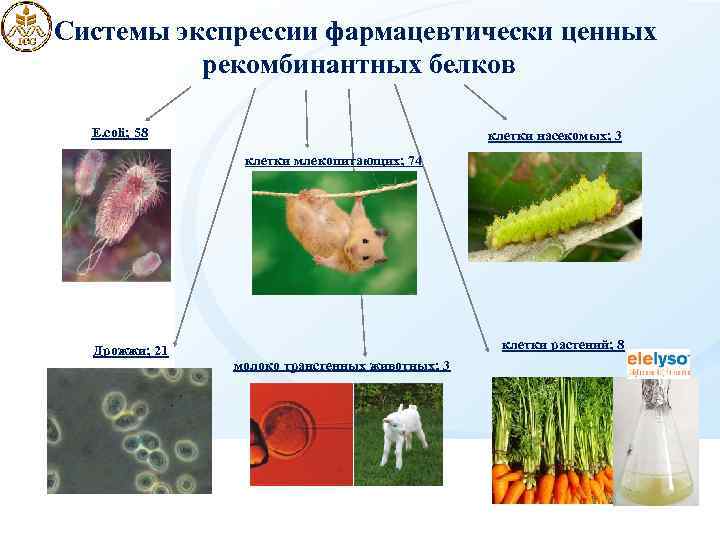
Системы экспрессии фармацевтически ценных рекомбинантных белков E. coli; 58 клетки насекомых; 3 клетки млекопитающих; 74 Дрожжи; 21 клетки растений; 8 молоко трансгенных животных; 3
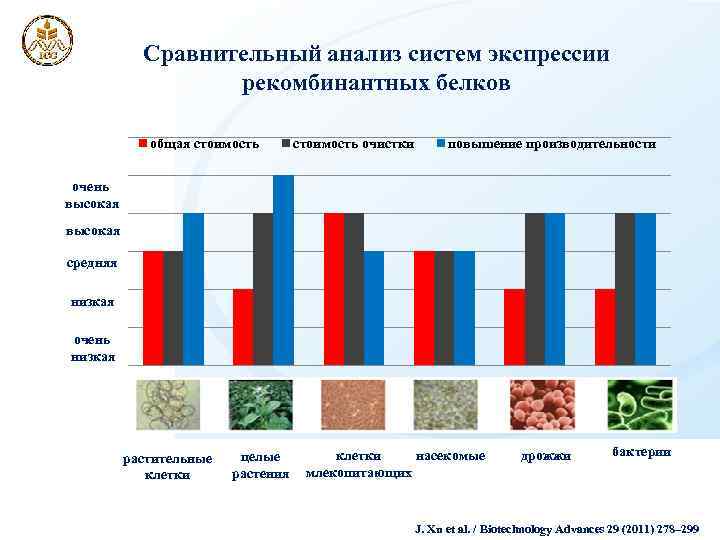
Сравнительный анализ систем экспрессии рекомбинантных белков общая стоимость очистки повышение производительности очень высокая средняя низкая очень низкая растительные клетки целые растения насекомые клетки млекопитающих дрожжи бактерии J. Xu et al. / Biotechnology Advances 29 (2011) 278– 299
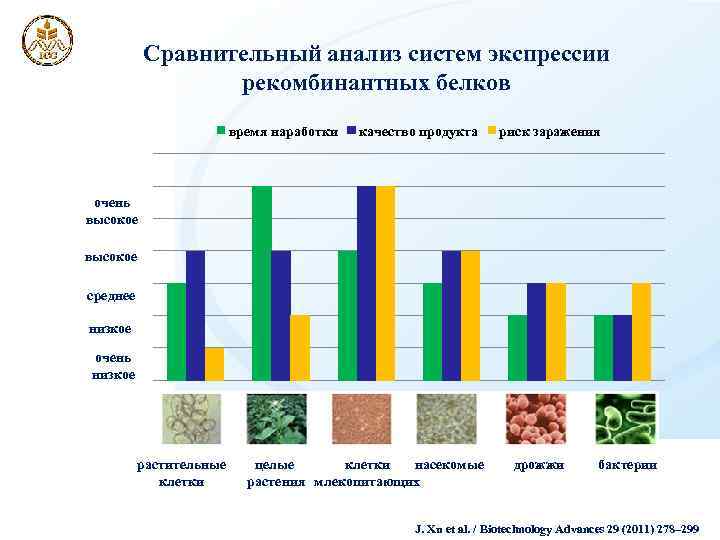
Сравнительный анализ систем экспрессии рекомбинантных белков время наработки качество продукта риск заражения очень высокое среднее низкое очень низкое растительные клетки насекомые целые растения млекопитающих дрожжи бактерии J. Xu et al. / Biotechnology Advances 29 (2011) 278– 299

Трансгенные растения – продуценты рекомбинантных белков для медицины: преимущества и недостатки
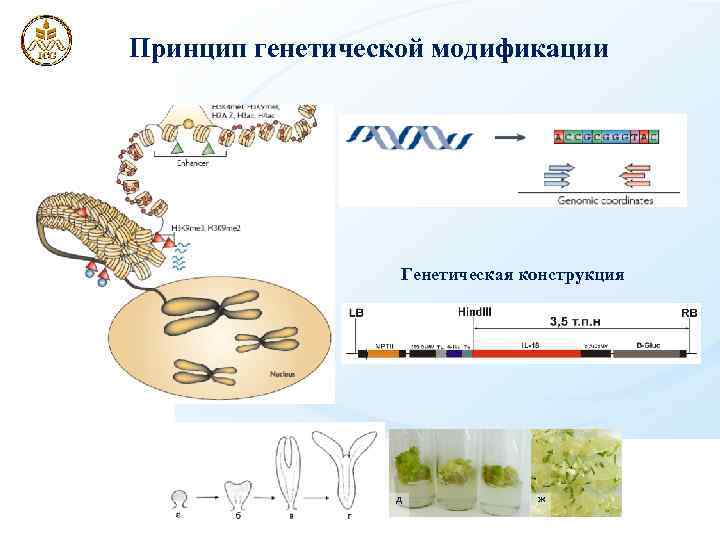
Принцип генетической модификации Генетическая конструкция д ж
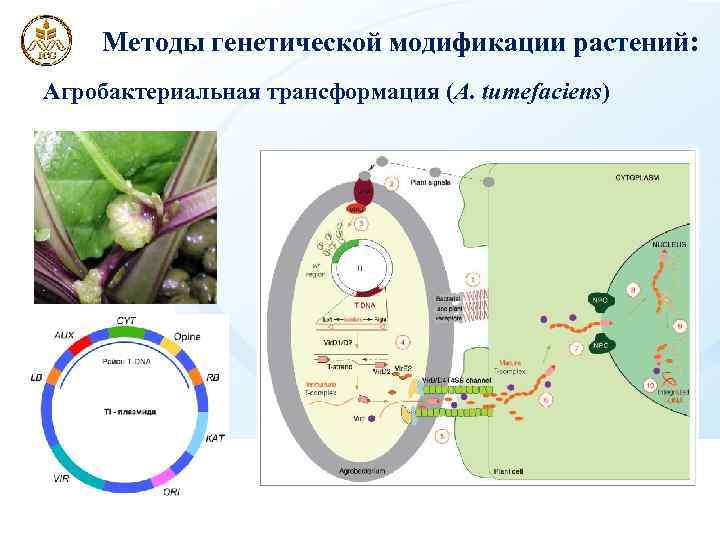
Методы генетической модификации растений: Агробактериальная трансформация (A. tumefaciens)
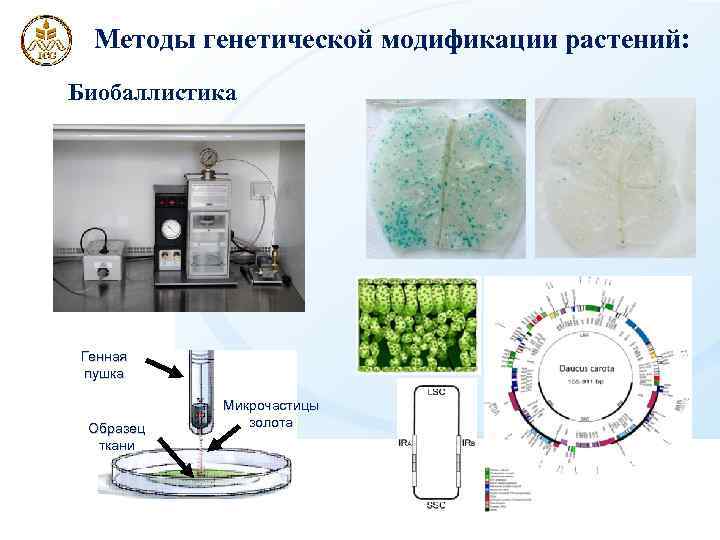
Методы генетической модификации растений: Биобаллистика Генная пушка Образец ткани Микрочастицы золота
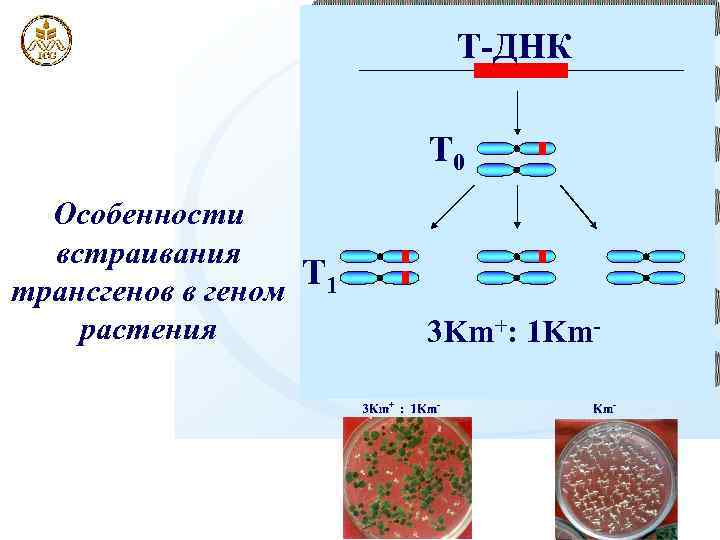
Т-ДНК Т 0 Особенности встраивания Т 1 трансгенов в геном растения 3 Km+: 1 Km-

Преимущества и недостатки растений по сравнению с другими системами экспрессии. vне содержат патогенных для человека вирусов и прионов vнет необходимости в дорогостоящем оборудовании для культивирования v разработанные системы агротехники vгликозилирование и фолдинг белков v. Способы доставки – «съедобные вакцины» vнизкий уровень экспрессии Авидин – 1 бушель (25 кг) кукурузы = 1 т белков куриных яиц авидин из кукурузы = 0, 5% от стоимости авидина из куриных яиц α-интерферон человека – в хлоропластах табака = 20% ОРБ = 3 мг/г сырой массы
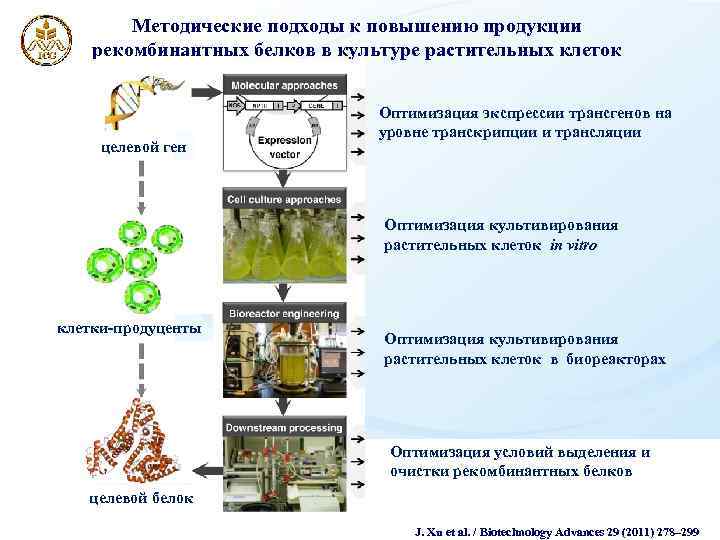
Методические подходы к повышению продукции рекомбинантных белков в культуре растительных клеток целевой ген Оптимизация экспрессии трансгенов на уровне транскрипции и трансляции Оптимизация культивирования растительных клеток in vitro клетки-продуценты Оптимизация культивирования растительных клеток в биореакторах Оптимизация условий выделения и очистки рекомбинантных белков целевой белок J. Xu et al. / Biotechnology Advances 29 (2011) 278– 299
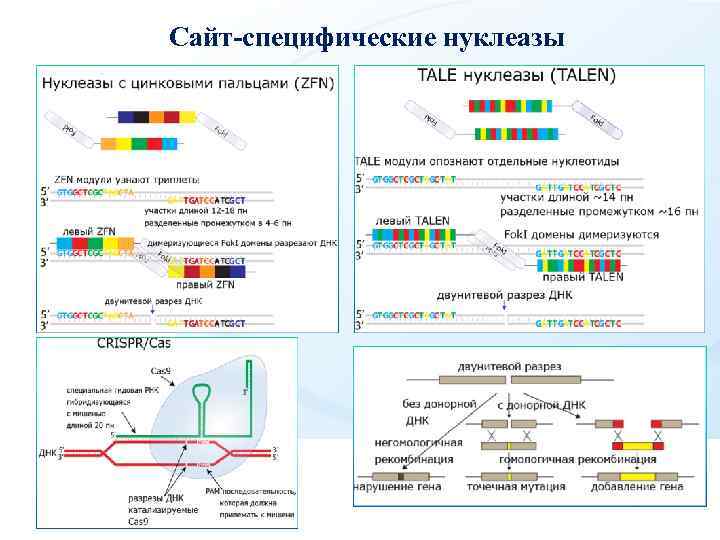
Сайт-специфические нуклеазы

Перспективные системы экспрессии в растительных клетках Ряска: горбатая - Lemna gibba; малая - L. minor “Biolex”, США Агроинфильтрация растений Nicotiana benthamiana “Bayer”, Германия Суспензионные клеточные культуры клеточная культура моркови “Protalix”, Израиль клеточная культура табака “Dow Agro. Sciences”, США

Получение рекомбинантного апротинина (ингибитор фибринолиза) на основе ГМ растений люцерна – ядерная трансформация – 0, 1% ОРБ (5 мг/кг биомассы), “Medicago”, Канада ряска – ядерная трансформация – 1, 9 -3, 7% ОРБ (0, 67 мг/л в среде), “Lemna Gene”, Франция зёрно кукурузы – ядерная трансформация – 8, 9% ОРБ, “Prody. Gene”, Люксембург табак (Nicotiana benthamiana) – агроинфильтрация – 2, 04, 2% ОРБ (до 400 мг/кг сырой массы за 7 дней), “LSBC”, США

Cостояние рынка рекомбинантных фармацевтически ценных белков, полученных на основе трансгенных растений
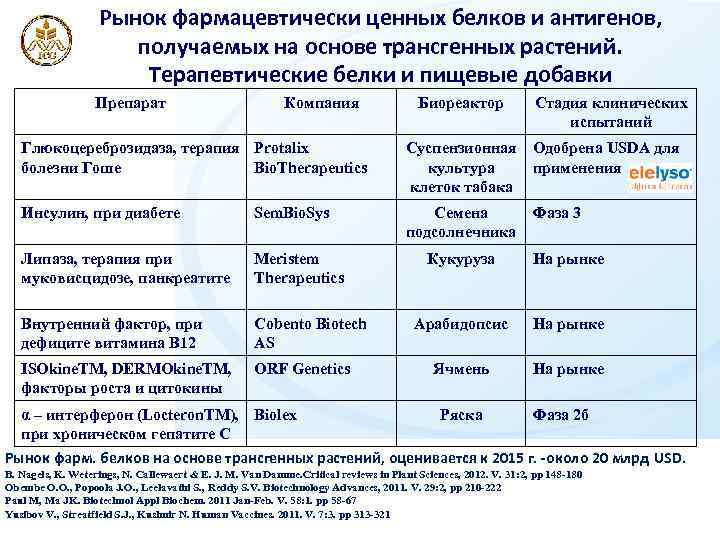
Рынок фармацевтически ценных белков и антигенов, получаемых на основе трансгенных растений. Терапевтические белки и пищевые добавки Препарат Компания Биореактор Стадия клинических испытаний Глюкоцереброзидаза, терапия Protalix болезни Гоше Bio. Therapeutics Суспензионная культура клеток табака Одобрена USDA для применения Инсулин, при диабете Sem. Bio. Sys Семена подсолнечника Фаза 3 Липаза, терапия при муковисцидозе, панкреатите Meristem Therapeutics Внутренний фактор, при дефиците витамина В 12 Cobento Biotech AS ISOkine. TM, DERMOkine. TM, факторы роста и цитокины ORF Genetics α – интерферон (Locteron. TM), Biolex при хроническом гепатите С Кукуруза На рынке Арабидопсис На рынке Ячмень На рынке Ряска Фаза 2 б Рынок фарм. белков на основе трансгенных растений, оценивается к 2015 г. -около 20 млрд USD. B. Nagels, K. Weterings, N. Callewaert & E. J. M. Van Damme. Critical reviews in Plant Sciences, 2012. V. 31: 2, pp 148 -180 Obembe O. O. , Popoola J. O. , Leelavathi S. , Reddy S. V. Biotechnology Advances, 2011. V. 29: 2, pp 210 -222 Paul M, Ma JK. Biotechnol Appl Biochem. 2011 Jan-Feb. V. 58: 1. pp 58 -67 Yusibov V. , Streatfield S. J. , Kushnir N. Human Vaccines. 2011. V. 7: 3. pp 313 -321
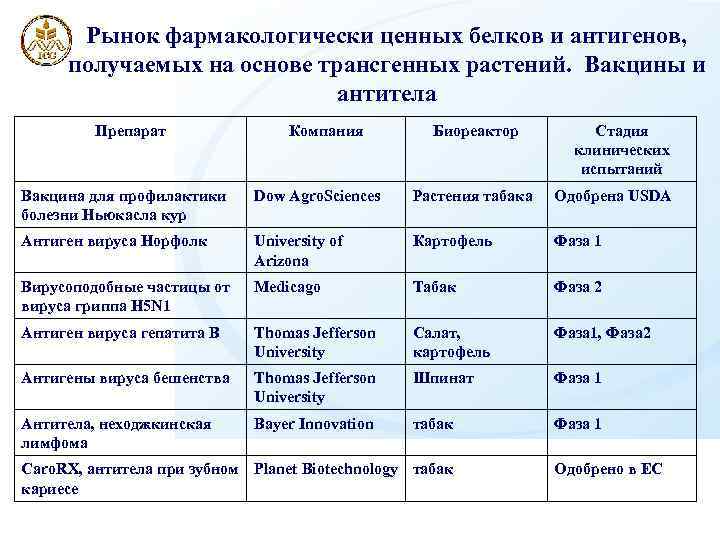
Рынок фармакологически ценных белков и антигенов, получаемых на основе трансгенных растений. Вакцины и антитела Препарат Компания Биореактор Стадия клинических испытаний Вакцина для профилактики болезни Ньюкасла кур Dow Agro. Sciences Растения табака Одобрена USDA Антиген вируса Норфолк University of Arizona Картофель Фаза 1 Вирусоподобные частицы от вируса гриппа H 5 N 1 Medicago Табак Фаза 2 Антиген вируса гепатита В Thomas Jefferson University Салат, картофель Фаза 1, Фаза 2 Антигены вируса бешенства Thomas Jefferson University Шпинат Фаза 1 Антитела, неходжкинская лимфома Bayer Innovation табак Фаза 1 Caro. RX, антитела при зубном Planet Biotechnology табак кариесе Одобрено в ЕС
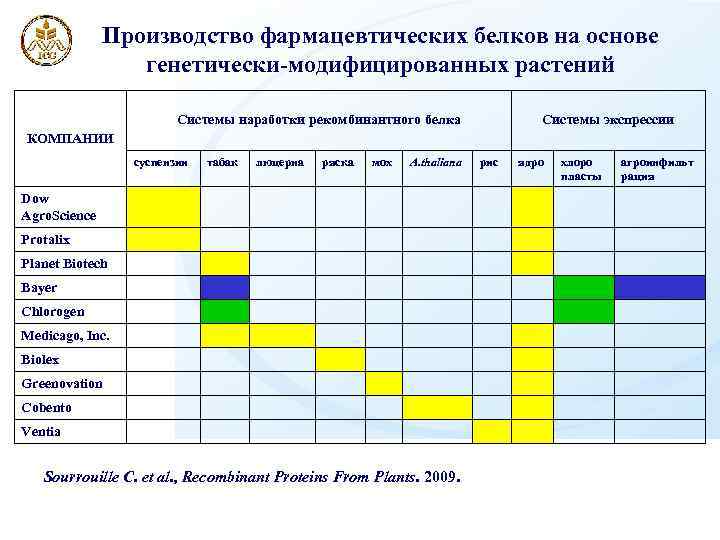
Производство фармацевтических белков на основе генетически-модифицированных растений Системы наработки рекомбинантного белка Системы экспрессии КОМПАНИИ суспензии табак люцерна ряска мох A. thaliana Dow Agro. Science Protalix Planet Biotech Bayer Chlorogen Medicago, Inc. Biolex Greenovation Cobento Ventia Sourrouille C. et al. , Recombinant Proteins From Plants. 2009. рис ядро хлоро пласты агроинфильт рация

• Затраты на производство 1 г антигена: - клетки млекопитающих – 367 -618 USD -клетки растений – 39 -125 USD Kaufmann S. , 2013 • Лигнин, фенольные соединения, протеазы, пигменты • Большие вложения в процесс сертификации продукта.

Трансгенные растения моркови – продуценты антигенов Mycobacterium tuberculosis
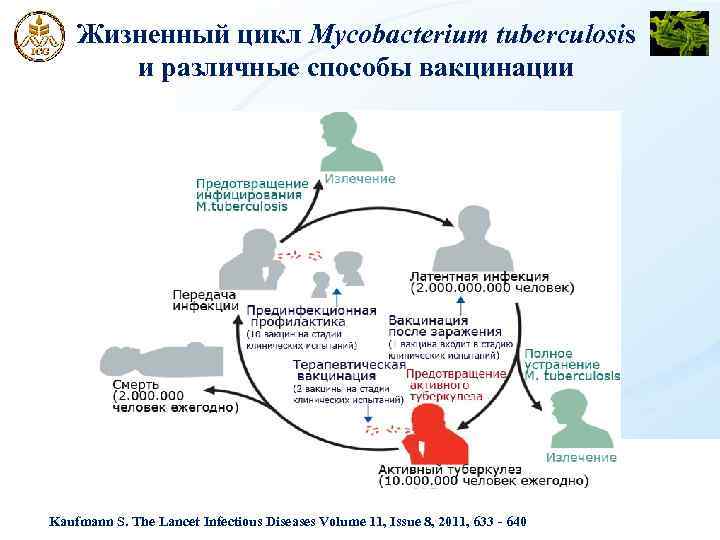
Жизненный цикл Mycobacterium tuberculosis и различные способы вакцинации Kaufmann S. The Lancet Infectious Diseases Volume 11, Issue 8, 2011, 633 - 640

Испытания новых вакцин против туберкулеза Фаза II Ad. Ag 85 A M 72+AS 01 Mc. Master University GSK, Aeras Hybrid-I+CAF 01 VPM 1002 SSI, TBVI H 56+IC 31 SSI, Aeras, Intercell Hyvac 4/ AERAS-404 +IC 31 SSI, sanofi-pasteur, Aeras, Intercell Max Planck, Vakzine Projekt Mgmt, TBVI Hybrid-1+IC 31 SSI, TBVI, EDCTP, Intercell RUTI Archivel Farma, S. L. ID 93/GLA-SE Infectious Disease Research Institute, Aeras Типы ТБ вакцин Основанные на вирусных векторах: MVA 85 A, AERAS-402, Ad. Ag 85 A Белок в сочетании с адьювантом: M 72, Hybrid-1, Hyvac 4, H 56, ID 93 r. BCG: VPM 1002 Убитые вакцины : Mw, RUTI Source: Tuberculosis Vaccine Candidates – 2011 Фаза IIб MVA 85 A/ AERAS-485 Oxford-Emergent Tuberculosis Consortium, Aeras, EDCTP, Wellcome Trust Фаза III Mw [M. indicus pranii (MIP)] Dept of Biotechnology (India), M/s. Cadila AERAS-402/ Crucell Ad 35 Crucell, Aeras, EDCTP, NIH SSI - Statens Serum Institute TBVI -Tuberculosis Vaccine Initiative GSK - Glaxo. Smith. Kline EDCTP - European and Developing Countries Clinical Trials первичная бустерная пост-инфекционная иммунотерапевтичческая
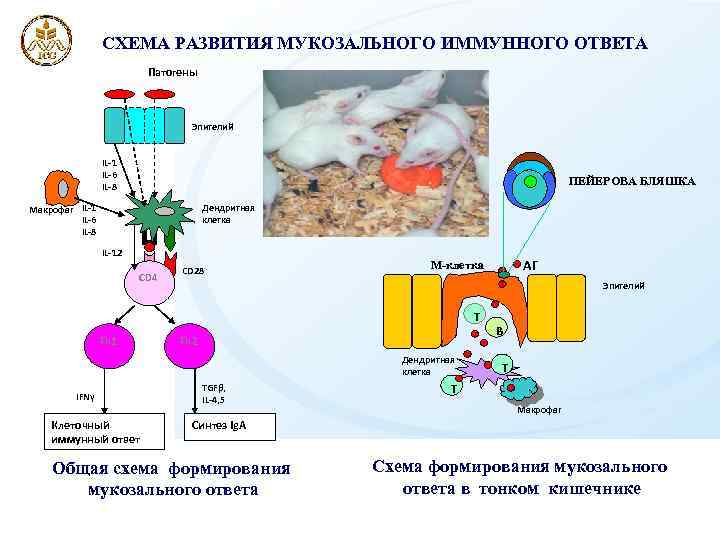
СХЕМА РАЗВИТИЯ МУКОЗАЛЬНОГО ИММУННОГО ОТВЕТА Патогены Эпителий IL-1 IL-6 IL-8 ПЕЙЕРОВА БЛЯШКА Макрофаг IL-1 IL-6 IL-8 Дендритная клетка IL-12 CD 4 CD 28 Эпителий Т Th 1 Th 2 Дендритная клетка IFNγ Клеточный иммунный ответ АГ М-клетка TGFβ, IL-4, 5 Т В Т Макрофаг Синтез Ig. A Общая схема формирования мукозального ответа Схема формирования мукозального ответа в тонком кишечнике

Концепция «съедобной вакцины» • чужеродные белки способны синтезироваться в клетках трансгенных растений в их природной, иммунологически активной форме • антигены (природный и синтезируемый трансгенными растениями) вызывают однотипные иммунологические реакции • при пероральной доставке антигены способны проходить через желудочно-кишечный тракт теплокровных • адаптивный мукозный иммунитет • стабильность целевого иммуногена при хранении • стандартизация иммуногена
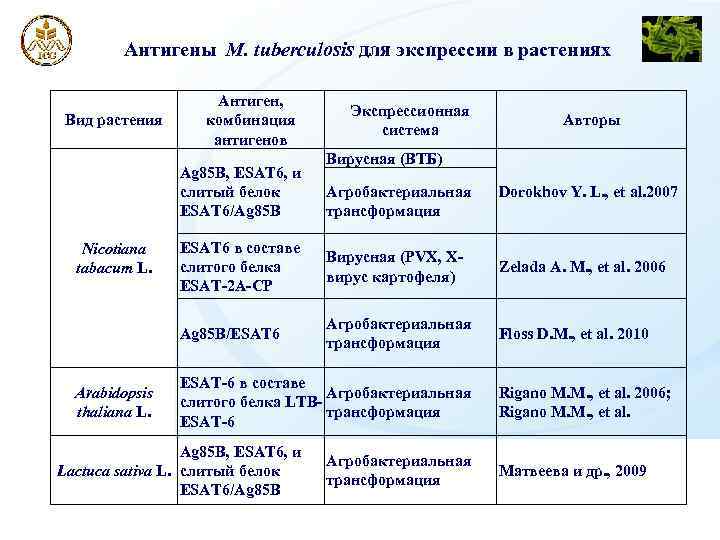
Антигены M. tuberculosis для экспрессии в растениях Вид растения Антиген, комбинация антигенов Ag 85 B, ESAT 6, и слитый белок ESAT 6/Ag 85 B Экспрессионная система Авторы Вирусная (ВТБ) Агробактериальная трансформация Dorokhov Y. L. , et al. 2007 Arabidopsis thaliana L. ESAT 6 в составе слитого белка ESAT-2 A-CP Вирусная (PVX, Хвирус картофеля) Zelada A. M. , et al. 2006 Ag 85 B/ESAT 6 Nicotiana tabacum L. Агробактериальная трансформация Floss D. M. , et al. 2010 ESAT-6 в составе Агробактериальная слитого белка LTBтрансформация ESAT-6 Ag 85 B, ESAT 6, и Lactuca sativa L. слитый белок ESAT 6/Ag 85 B Агробактериальная трансформация Rigano M. M. , et al. 2006; Rigano M. M. , et al. Матвеева и др. , 2009
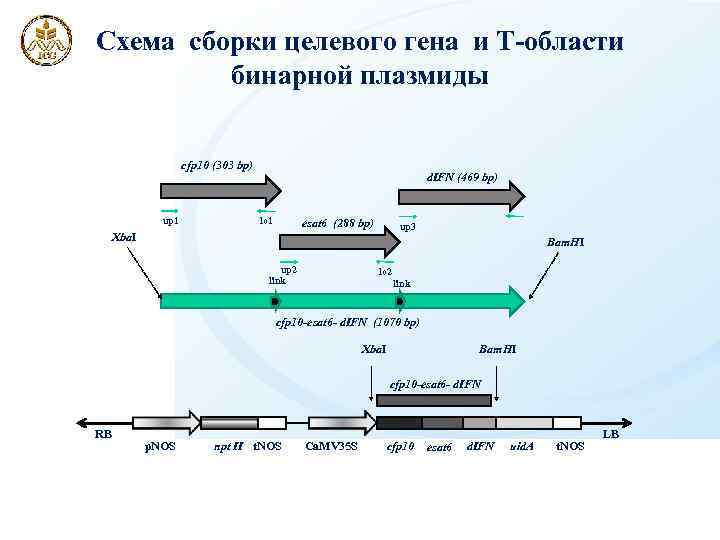
Схема сборки целевого гена и Т-области бинарной плазмиды cfp 10 (303 bp) up 1 d. IFN (469 bp) lo 1 esat 6 (288 bp) up 3 Xba. I Bam. HI up 2 link lo 2 link cfp 10 -esat 6 - d. IFN (1070 bp) Xba. I Bam. HI cfp 10 -esat 6 - d. IFN RB p. NOS npt II t. NOS Ca. MV 35 S cfp 10 esat 6 d. IFN uid. A t. NOS LB
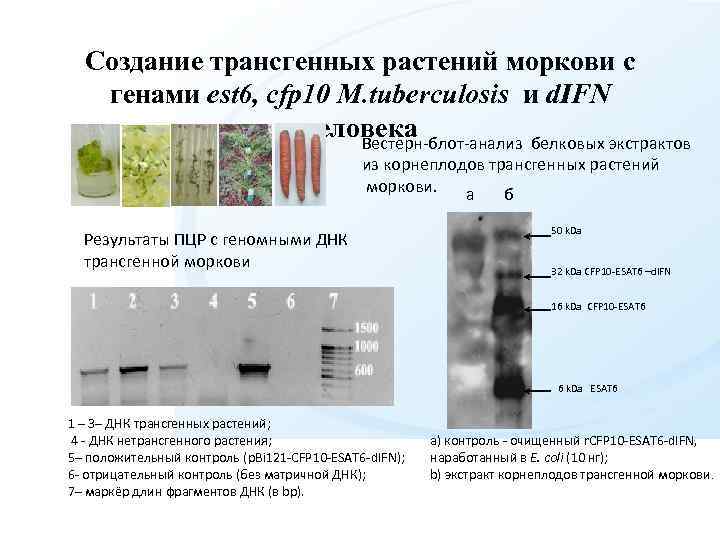
Создание трансгенных растений моркови с генами est 6, cfp 10 M. tuberculosis и d. IFN человека Вестерн-блот-анализ белковых экстрактов из корнеплодов трансгенных растений моркови. а б Результаты ПЦР с геномными ДНК трансгенной моркови 50 k. Da 32 k. Da CFP 10 -ESAT 6 –d. IFN 16 k. Da CFP 10 -ESAT 6 6 k. Da ESAT 6 1 – 3– ДНК трансгенных растений; 4 - ДНК нетрансгенного растения; 5– положительный контроль (p. Bi 121 -CFP 10 -ESAT 6 -d. IFN); 6 - отрицательный контроль (без матричной ДНК); 7– маркёр длин фрагментов ДНК (в bp). а) контроль - очищенный r. CFP 10 -ESAT 6 -d. IFN, наработанный в E. сoli (10 нг); b) экстракт корнеплодов трансгенной моркови.
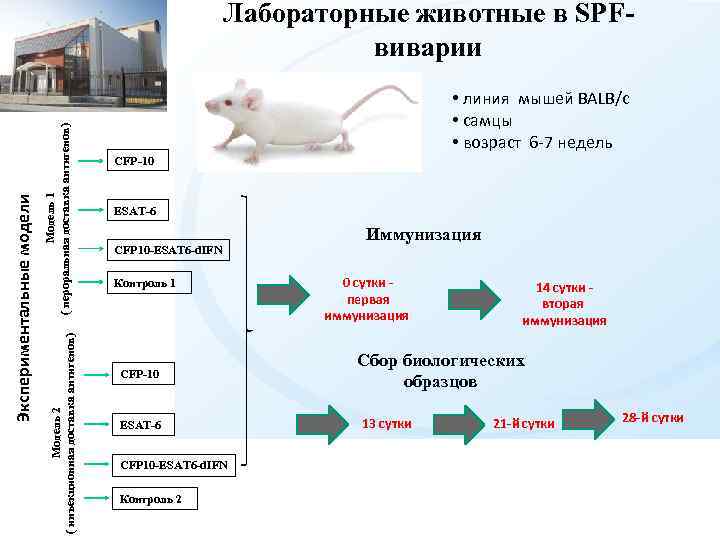
Модель 1 ( пероральная доставка антигенов) Модель 2 ( инъекционная доставка антигенов) Экспериментальные модели Лабораторные животные в SPFвиварии • линия мышей BALB/c • самцы • возраст 6 -7 недель CFP-10 ESAT-6 CFP 10 -ESAT 6 -d. IFN Контроль 1 CFP-10 ESAT-6 CFP 10 -ESAT 6 -d. IFN Контроль 2 Иммунизация 0 сутки первая иммунизация 14 сутки вторая иммунизация Сбор биологических образцов 13 сутки 21 -й сутки 28 -й сутки
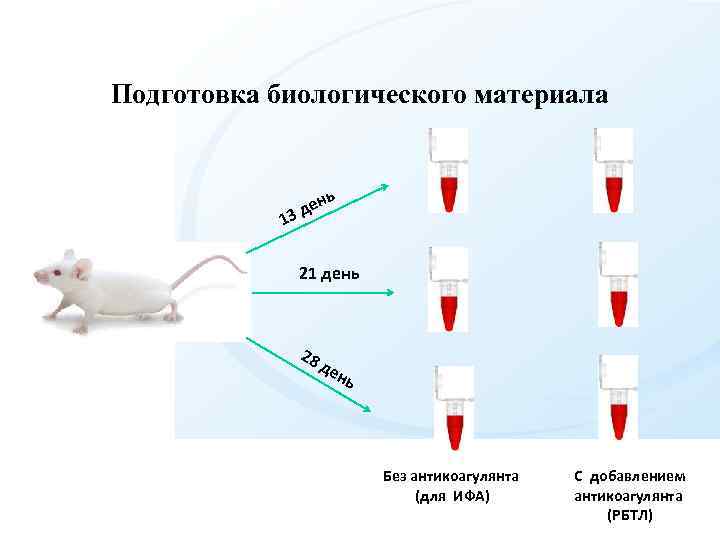
Подготовка биологического материала ь н де 3 1 21 день 28 д ен ь Без антикоагулянта (для ИФА) С добавлением антикоагулянта (РБТЛ)
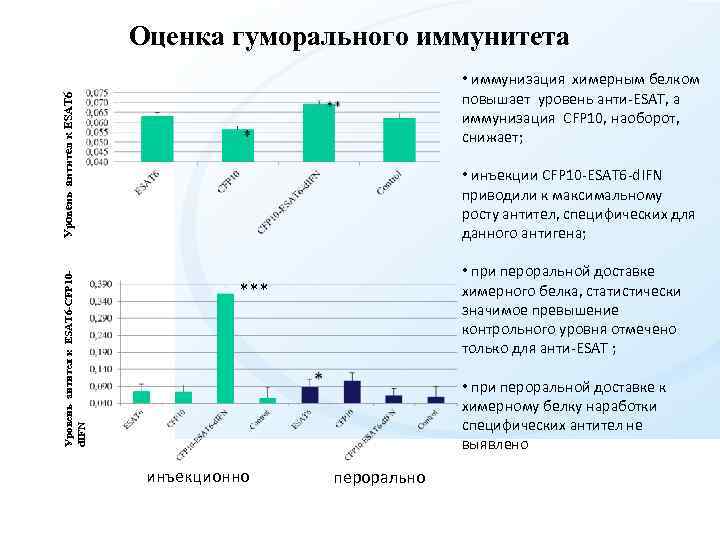
Оценка гуморального иммунитета Уровень антител к ESAT 6 -CFP 10 d. IFN Уровень антител к ESAT 6 • иммунизация химерным белком повышает уровень анти-ESAT, а иммунизация CFP 10, наоборот, снижает; • инъекции CFP 10 -ESAT 6 -d. IFN приводили к максимальному росту антител, специфических для данного антигена; • при пероральной доставке химерного белка, статистически значимое превышение контрольного уровня отмечено только для анти-ESAT ; *** • при пероральной доставке к химерному белку наработки специфических антител не выявлено инъекционно перорально
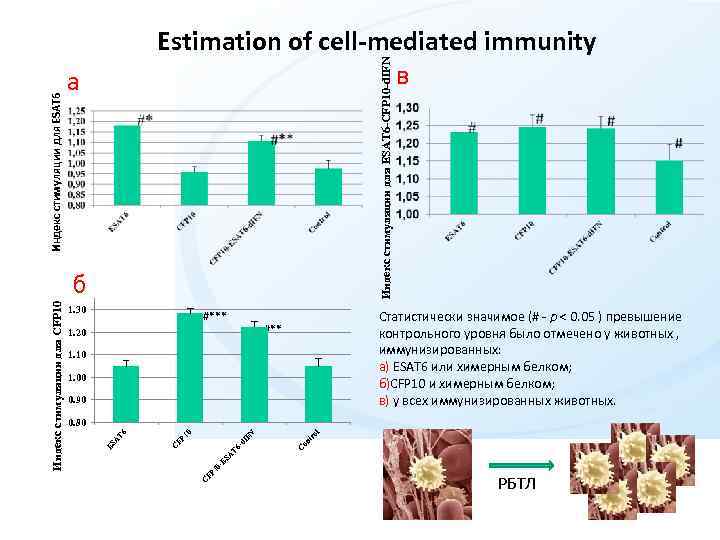
Индекс стимуляции для ESAT 6 -CFP 10 -d. IFN Индекс стимуляции для ESAT 6 Estimation of cell-mediated immunity в а 1. 30 #*** Статистически значимое (# - p < 0. 05 ) превышение контрольного уровня было отмечено у животных , иммунизированных: а) ESAT 6 или химерным белком; б)CFP 10 и химерным белком; в) у всех иммунизированных животных. #** 1. 20 1. 10 1. 00 0. 90 l on C -d IF C FP 10 -E SA T 6 tr o N 0 FP 1 C A T 6 0. 80 ES Индекс стимуляции для CFP 10 б РБТЛ

Спасибо за внимание!
Дейнеко_Генериум_last.ppt