Оптическая диагностика.ppt
- Количество слайдов: 63

Раздел: Оптическая биомедицинская диагностика (по В. В. Тучину) Неинвазивная медицинская спектрофотометрия (НМС) (по Д. А. Рогаткину) Noninvasive medical spectrophotometry (NMS) http: //page-nii-r 2. narod. ru/cr_r_bmt. htm
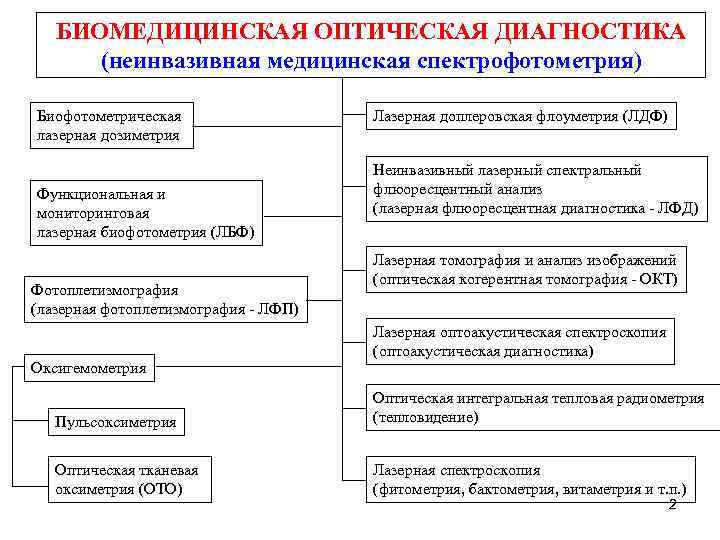
БИОМЕДИЦИНСКАЯ ОПТИЧЕСКАЯ ДИАГНОСТИКА (неинвазивная медицинская спектрофотометрия) Биофотометрическая лазерная дозиметрия Функциональная и мониторинговая лазерная биофотометрия (ЛБФ) Фотоплетизмография (лазерная фотоплетизмография - ЛФП) Оксигемометрия Лазерная доплеровская флоуметрия (ЛДФ) Неинвазивный лазерный спектральный флюоресцентный анализ (лазерная флюоресцентная диагностика - ЛФД) Лазерная томография и анализ изображений (оптическая когерентная томография - ОКТ) Лазерная оптоакустическая спектроскопия (оптоакустическая диагностика) Пульсоксиметрия Оптическая интегральная тепловая радиометрия (тепловидение) Оптическая тканевая оксиметрия (ОТО) Лазерная спектроскопия (фитометрия, бактометрия, витаметрия и т. п. ) 2

Предметом исследования неинвазивной медицинской спектрофотометрии (НМС) являются прижизненные уровни накопления различных биохимических веществ в толще ткани, а также их динамика во времени. Среди наиболее достоверно определяемых компонентов крови и клеточных биологических тканей сегодня в НМС рассматриваются: общий гемоглобин крови микроциркуляторного русла (Hbt), часто именуемый тканевым или транскутанным гематокритом (Htt), его аналог – объемное кровенаполнение (Vb) в зоне обследования, перфузия тканей кровью - индекс микроциркуляции, определяемый доплеровским методом (Im), процентное функциональное содержание (сатурация, SO 2) оксигенированной фракции гемоглобина (Hb. O 2) в артериальной (артериальная сатурация Sa. O 2) или в смешанной крови микроциркуляторного русла (тканевая, транскутанная сатурация St. O 2), меланин кожи, билирубин, жир, вода и ряд других молекул и веществ.
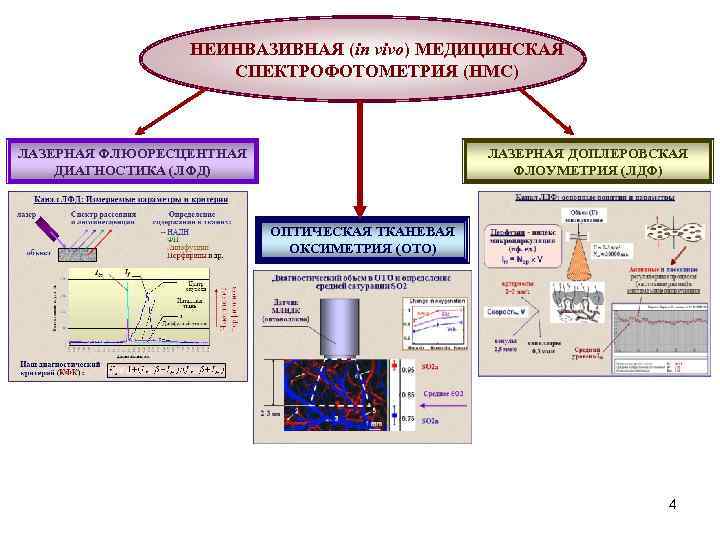
НЕИНВАЗИВНАЯ (in vivo) МЕДИЦИНСКАЯ СПЕКТРОФОТОМЕТРИЯ (НМС) ЛАЗЕРНАЯ ФЛЮОРЕСЦЕНТНАЯ ДИАГНОСТИКА (ЛФД) ЛАЗЕРНАЯ ДОПЛЕРОВСКАЯ ФЛОУМЕТРИЯ (ЛДФ) ОПТИЧЕСКАЯ ТКАНЕВАЯ ОКСИМЕТРИЯ (ОТО) 4
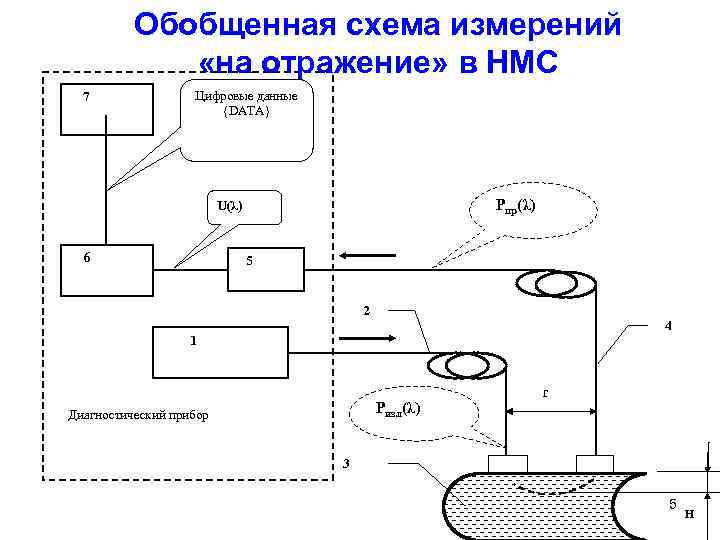
Обобщенная схема измерений «на отражение» в НМС 7 Цифровые данные {DATA} Pпр(λ) U(λ) 6 5 2 4 1 Pизл(λ) Диагностический прибор r 3 5 H

В диагностическом приборе излучение с длиной волны λ мощностью Pизл(λ) от источника излучения 1, который в зависимости от выбранного метода диагностики может представлять собой как один монохроматический источник света (лазер), так и набор разных источников с разным спектром излучения, включая источники смешанного (белого) света, доставляется посредством оптической системы освещения 2, например, посредством оптического волокна, к обследуемому биологическому объекту (БО) 3. Внутри БО попадающее туда излучение претерпевает многократные рассеяния (переотражения) на границах неоднородностей анатомической и клеточной структуры тканей и частично поглощается наполняющими ткань веществами: водой, меланином, гемоглобином крови и т. д. Часть излучения, ослабленная за счет поглощения и рассеяния, вследствие многократных актов рассеяния снова выходит наружу БО, составляя так называемый от БО поток обратно рассеянного излучения FBS. С помощью системы сбора и транспортировки излучения 4 от БО поток оптического излучения мощностью Pпр(λ)< Pизл(λ) доставляется в блок регистрации диагностического прибора и, в общем упрощенном случае, направляется на фотоприемник 5 - первичный измерительный преобразователь (ПИП). Он осуществляет, как правило, линейное преобразование оптического сигнала Pпр(λ) в напряжение U(λ). Далее полезный электрический сигнал U(λ) проходит аналоговую обработку (усиление, фильтрацию и т. п. ) в электронном блоке 6, оцифровывается и передается в компьютер 7 для последующих математических вычислений. В ряде случаев, как, например, в методах пульсоксиметрии, источники излучения - светодиоды и фотоприемник могут располагаться непосредственно на поверхности обследуемой ткани, т. е. могут отсутствовать системы транспортировки излучения 2 и 4, но общности приведенных выше рассуждений это не меняет.
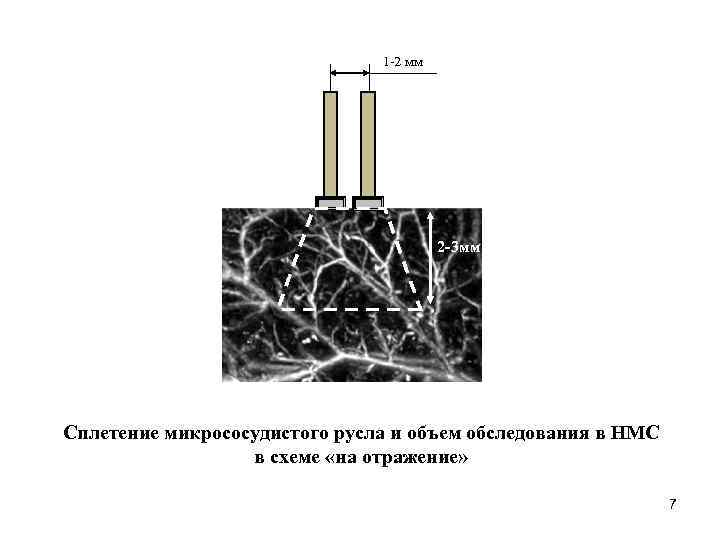
1 -2 мм 2 -3 мм Сплетение микрососудистого русла и объем обследования в НМС в схеме «на отражение» 7
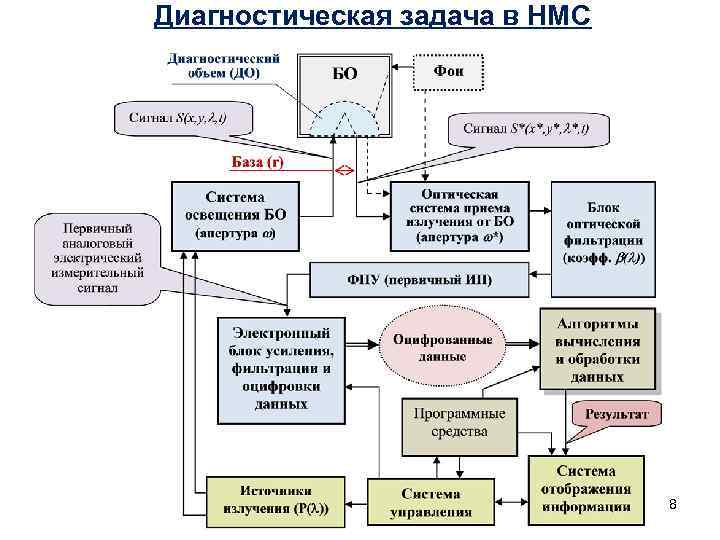
Диагностическая задача в НМС 8

Тестируемый БО с точки зрения структурно-функциональной модели диагностического процесса может быть представлен в этой схеме спектральнонелинейным оптическим фильтром, который преобразует падающую на него мощность Pизл(λ) в мощность вторичного излучения Pпр(λ), что математически равнозначно умножению исходного оптического сигнала на некоторую безразмерную функцию кодирования В(λ), зависящую от оптико-физических и медико-биологических параметров (МБП) БО, а также от условий освещения и приема излучения. В качестве примера В(λ) можно привести известное выражение, полученное на основе диффузионного приближения для полубесконечной среды: где: - эффективная длина, A – площадь детектора, r – расстояние между источником и приемником (так называемая база измерений), , , g=g(λ) – фактор анизотропии, s= s(λ) и a= a(λ) – транспортные коэффициенты рассеяния и поглощения соответственно. Зависимость g, s и a от МБП позволяет, определяя В(λ) на разных длинах волн, оценивать разные МБП у испытуемого. Такая оценка может выполняться и по результатам динамических наблюдений В(λ) при изменении МБП, скажем, в процессе выполнения функциональных нагрузочных тестов и проб.

Непосредственно измеряемой прибором НМС первичной физической величиной является безразмерная функция кодирования сигнала В(λ). Ее измерение (в отн. ед. ) обычно выполняется методом сравнения Pпр(λ) с аналогичным потоком, регистрируемым с «эталонной» светорассеивающей меры с известной В(λ). Косвенно измеряемой исходной физической величиной может считаться и поток Pпр(λ), если в приборе производится вычисление, документирование и хранение размерной величины Pпр(λ). Измеряемой вторичной измерительной схемой внутри диагностического прибора вторичной физической величиной является напряжение U(λ) - выходной сигнал ПИП. Полученному массиву U (λ) в памяти компьютера соответствует массив размерных цифровых данных {DATA}, а все конечные МБП БО определяются на заключительном этапе измерений по {DATA} уже исключительно расчетным путем с использованием вычислительных и интерпретирующих алгоритмов, реализуемых программно. Т. е. в НМС по способу получения конечного диагностического результата мы имеем дело с классическими косвенными совокупными или совместными измерениями, которым из-за сложности их реализации всегда присущи достаточно большие погрешности.

ЛАЗЕРНАЯ ДОПЛЕРОВСКАЯ ФЛОУМЕТРИЯ Laser Doppler Flowmetry (LDF) Для диагностики применяется зондирование ткани лазерным излучением; обработка отраженного от ткани излучения основана на выделении из зарегистрированного сигнала доплеровского сдвига частоты отраженного сигнала, пропорционального скорости движения эритроцитов; в ходе проводимых исследований обеспечивается регистрация изменения потока крови в микроциркуляторном русле – флоуметрия.

ЛДФ: основные понятия и параметры Объем (U) зондирования Перфузия - индекс микроциркуляции (пф. ед. ) Im = Nэр V U 2 -3 мм 3 Ner 30000 шт. Активные и пассивные регуляторные процессы (частотные ритмы) в системе микроциркуляции артериолы 2– 3 мм/с Скорость, V венулы 2, 5 мм/с капилляры 0, 3 мм/с Средний уровень Im

Схема зондирования ткани лазерным излучением при ЛДФ При взаимодействии лазерного излучения с тканью отраженный сигнал имеет две составляющие: постоянную и переменную. Постоянный сигнал обусловлен отражением от неподвижных структур зондируемой ткани. Переменный сигнал связан с движущимися частицами – эритроцитами. 13
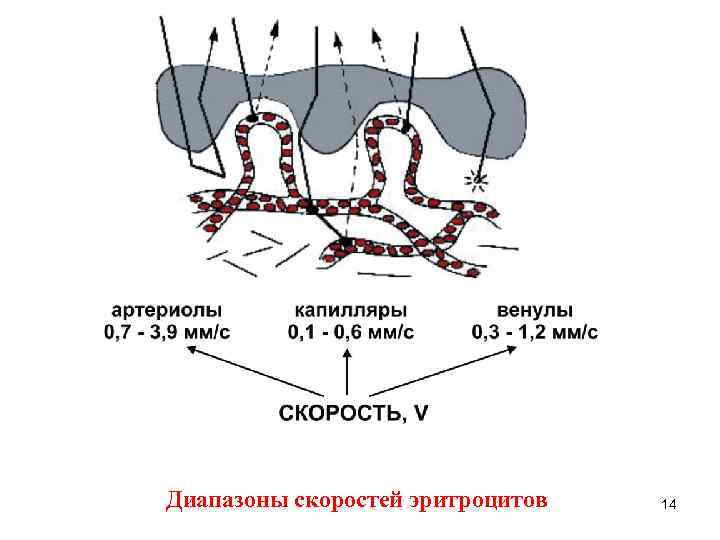
Диапазоны скоростей эритроцитов 14

ФИЗИЧЕСКИЕ ОСНОВЫ МЕТОДА ЛДФ Движущийся объект облучают пучком лазерного излучения от неподвижного источника. Это излучение отражается от объекта и регистрируется неподвижным приемником. Вследствие эффекта Доплера (изменение частоты и длины волн, регистрируемых приёмником, вызванное движением их источника и/или движением приёмника), частота излучения, попадающего на приемник, будет отличаться от частоты излучения неподвижного источника на некоторую величину, пропорциональную скорости движения объекта относительно источника и приемника. При взаимодействии лазерного излучения с неподвижной тканью рассеянное излучение имеет ту же частоту, что и зондирующее излучение, при взаимодействии с движущимися эритроцитами частота рассеянного излучения отличается от частоты падающего излучения в соответствии с доплеровским эффектом. Доплеровский сдвиг частоты связан со скоростью эритроцитов известным выражением: Δf = 2 n. V/λ где: Δf – доплеровский сдвиг частоты, n – показатель преломления излучения в ткани, V – скорость эритроцитов, λ – длина волны зондирующего излучения.

Кровеносные сосуды микроциркуляторного русла могут быть ориентированы по отношению к фронту волны зондирующего излучения под разными углами. Максимальная частота допплеровского сдвига возникает, когда векторы направления распространения фронта волны излучения и скорости движения эритроцита параллельны. Этой ситуации соответствует частотный сдвиг около 4, 4 к. Гц для скорости эритроцитов 1 мм/с и длины волны гелий-неонового лазера 0, 638 мкм при показателе преломления ткани 1, 4. Для эритроцитов, которые движутся под углом к направлению зондирующего излучения, величина доплеровского сдвига частоты уменьшается пропорционально значению косинуса этого угла. В зависимости от задач исследования микроциркуляции крови применяются лазерные источники мощностью 1 -2 м. Вт, излучающие в диапазоне от зеленой до ближней инфракрасной длины волны. Глубина зондирующего слоя зависит от длины волны: чем короче длина волны, тем тоньше слой. Это обстоятельство объясняется различным поглощением излучения в биологических тканях молекулами меланина, гемоглобина, бетакаротина и билирубина. Поглощение излучения молекулами гемоглобина является наиболее значительным для коротковолнового излучения – это приводит к уменьшению величины детектируемого рассеянного излучения. Для указанного диапазона от зеленой до инфракрасной длины волны толщина зондируемого слоя ткани может составлять от 0, 5 до 2 мм.

Глубина проникновения излучения в ткань определяется поглощением и рассеянием вперед от лазерного источника. Когда излучение распространяется в биологической ткани, только незначительная часть (около 3 -7%) отражается назад. Наибольшая величина мощности излучения частично поглощается или рассеивается вперед в соответствии с законом Дебая-Релея. Объем зондируемой ткани в методе ЛДФ определяется геометрией и оптическими параметрами световодного зонда и составляет, как правило, около 1 мм 3 для излучения в красной видимой области спектра. Указанный объем ткани кожи может содержать зону, включающую восходящую из глубины дермы артериолу, от которой отходят до пяти ответвлений, множество капилляров и сопутствующую нисходящую венулу с девятью сходящими посткапиллярными венулами. В этом объеме эритроциты движутся с разными линейными скоростями: от 0, 68 до 3, 87 мм/с в артериолах; от 0, 1 до 0, 6 мм/с в капиллярах и от 0, 32 до 1, 21 мм/с в венулах. Число эритроцитов в объеме 1 мм 3 может достигать несколько десятков тысяч.

Следовательно, амплитуда отраженного сигнала формируется в результате отражения излучения от ансамбля эритроцитов, движущихся с разными скоростями и по-разному количественно распределенных в артериолах, капиллярах, венулах и артериоловенулярных анастомозах. Поэтому в методе ЛДФ применяется алгоритм усреднения, который позволяет получить средний доплеровский сдвиг частоты по всей совокупности эритроцитов, попадающих в зондируемую область. В результате такого усреднения методом ЛДФ оценивается изменение потока эритроцитов. Для этого проводят обработку отраженного сигнала электронным путем, осуществляя усреднение по скоростям (доплеровским сдвигам частоты). Очевидно, что мощность отраженного излучения складывается из отдельных актов отражения излучения на каждом эритроците и, следовательно, зависит от их концентрации. На выходе прибора формируется результат флоуметрии - сигнал, амплитуда которого пропорциональна скорости и количеству эритроцитов.

Получив в результате преобразования Фурье частотную характеристику исследуемого сигнала, становится возможным определить соответствующие скорости движения эритроцитов. Для исследования целесообразно иметь информацию об усредненной скорости движения, то есть скорости, с которой в данный момент времени движется наибольшее количество эритроцитов. Считая, что все эритроциты в исследуемом объеме находятся в равных условиях, полагаем, что амплитуда той или иной частотной составляющей сигнала пропорциональна числу эритроцитов, движущихся с соответствующей скоростью. Получив в результате преобразования Фурье частотную характеристику исследуемого сигнала, возможно определить соответствующие скорости движения эритроцитов. Считая, что все эритроциты в исследуемом объеме находятся в равных условиях, полагаем, что амплитуда той или иной частотной составляющей сигнала пропорциональна числу эритроцитов, движущихся с соответствующей скоростью. Показатель микроциркуляции находят как: где ПМ – показатель микроциркуляции; К – коэффициент пропорциональности; V – скорость движения i-ого ансамбля эритроцитов; A – амплитуда i-ой частотной составляющей (гармоники спектра); N – количество вычисленных частотных составляющих спектра.

Поскольку капилляры ориентированы перпендикулярно к поверхности дермы следует полагать, что вектор скорости совпадет с направлением «локаторчастица» . В этом случае скорость i-ого ансамбля эритроцитов связана со значением частоты соответствующей ему i-ой гармоники доплеровского сдвига выражением: где Vi – скорость частицы; fi – доплеровская частота сдвига; n – показатель преломления среды (для плазмы крови n = 1, 4). Однако такой подход применим (и то с определенными допущениями) лишь для капиллярных петель. Направление движения эритроцитов в артериолах и венулах носит случайный характер и в общем случае не совпадает с направлением «локатор-частица» . Таким образом, показатель микроциркуляции представляет собой усредненный параметр, не позволяющий судить об абсолютных скоростях движения эритроцитов.
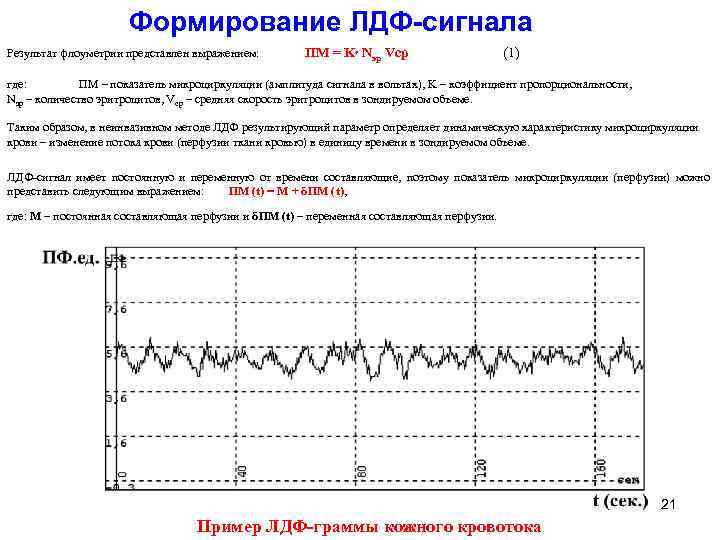
Формирование ЛДФ-сигнала Результат флоуметрии представлен выражением: ПМ = K Nэр Vср (1) где: ПМ – показатель микроциркуляции (амплитуда сигнала в вольтах), K – коэффициент пропорциональности, Nэр – количество эритроцитов, Vср – средняя скорость эритроцитов в зондируемом объеме. Таким образом, в неинвазивном методе ЛДФ результирующий параметр определяет динамическую характеристику микроциркуляции крови – изменение потока крови (перфузии ткани кровью) в единицу времени в зондируемом объеме. ЛДФ-сигнал имеет постоянную и переменную от времени составляющие, поэтому показатель микроциркуляции (перфузии) можно представить следующим выражением: ПМ (t) = М + δПМ (t), где: М – постоянная составляющая перфузии и δПМ (t) – переменная составляющая перфузии. 21 Пример ЛДФ-граммы кожного кровотока
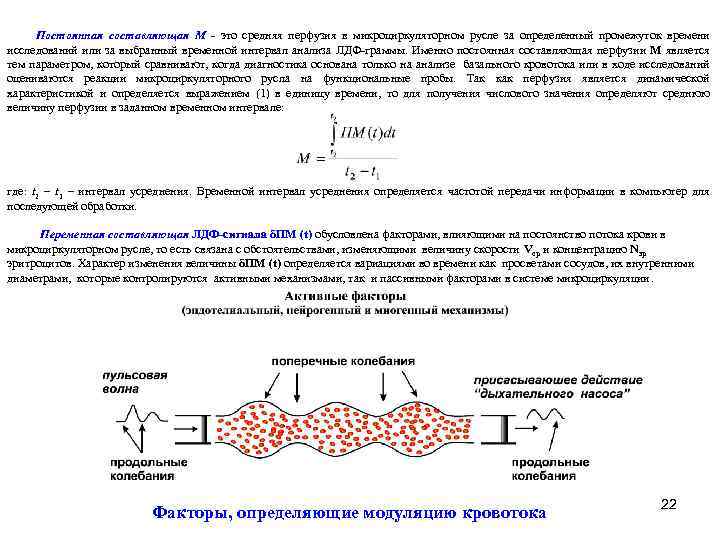
Постоянная составляющая М - это средняя перфузия в микроциркуляторном русле за определенный промежуток времени исследований или за выбранный временной интервал анализа ЛДФ-граммы. Именно постоянная составляющая перфузии М является тем параметром, который сравнивают, когда диагностика основана только на анализе базального кровотока или в ходе исследований оцениваются реакции микроциркуляторного русла на функциональные пробы. Так как перфузия является динамической характеристикой и определяется выражением (1) в единицу времени, то для получения числового значения определяют среднюю величину перфузии в заданном временном интервале: где: t 2 – t 1 – интервал усреднения. Временной интервал усреднения определяется частотой передачи информации в компьютер для последующей обработки. Переменная составляющая ЛДФ-сигнала δПМ (t) обусловлена факторами, влияющими на постоянство потока крови в микроциркуляторном русле, то есть связана с обстоятельствами, изменяющими величину скорости Vср и концентрацию Nэр эритроцитов. Характер изменения величины δПМ (t) определяется вариациями во времени как просветами сосудов, их внутренними диаметрами, которые контролируются активными механизмами, так и пассивными факторами в системе микроциркуляции. Факторы, определяющие модуляцию кровотока 22
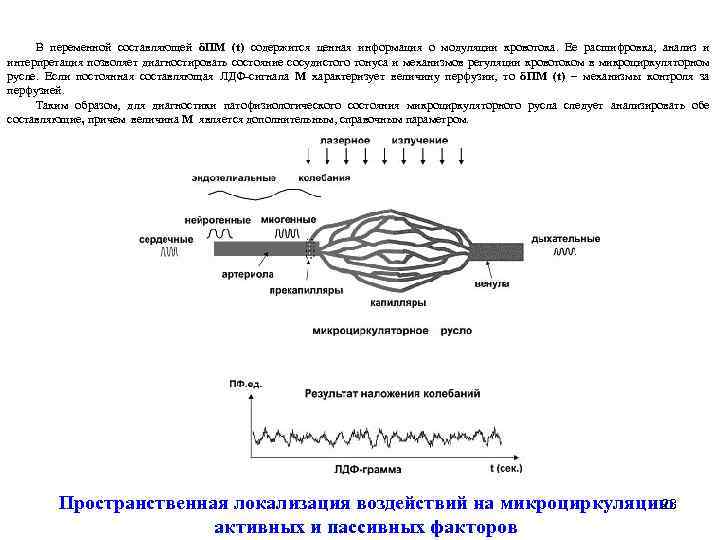
В переменной составляющей δПМ (t) содержится ценная информация о модуляции кровотока. Ее расшифровка, анализ и интерпретация позволяет диагностировать состояние сосудистого тонуса и механизмов регуляции кровотоком в микроциркуляторном русле. Если постоянная составляющая ЛДФ-сигнала М характеризует величину перфузии, то δПМ (t) – механизмы контроля за перфузией. Таким образом, для диагностики патофизиологического состояния микроциркуляторного русла следует анализировать обе составляющие, причем величина М является дополнительным, справочным параметром. Пространственная локализация воздействий на микроциркуляцию 23 активных и пассивных факторов

Методы регистрации доплеровского сдвига оптического излучения Информацию о движении объекта, содержащуюся в рассеянном им свете, можно извлечь, подвергнув его спектральному анализу. Большие доплеровские сдвиги можно легко обнаружить, проводя анализ на оптических частотах при помощи узкополосных фильтров. Малые доплеровские сдвиги обнаруживаются только при анализе на частотах радиодиапазона, для чего частота рассеянного света должна быть сдвинута в этот диапазон с помощью нелинейного смешения. Для регистрации доплеровского сдвига ОИ широкое применение нашли методы на основе эффекта фотосмешения, при которых на поверхность фотоприемника направляются две волны; реакция его квадратична относительно напряженности поля, поэтому если две волны имеют различные частоты, то выходной ток приемника содержит составляющую на разностной частоте. Опорной волной, относительно которой отсчитывают доплеровский сдвиг частоты, является часть излучения лазера, зондирующего исследуемый объект, что связано с нестабильностью частоты излучения лазера.

При оптическом фотосмешении необходимо, чтобы рассеянное излучение смешивалось на поверхности фотокатода с частью нерассеянного излучения лазера. Если излучение линейно поляризовано и не учитывается деполяризация при рассеянии, то мгновенное значение поля на фотокатоде можно выразить скалярной величиной Ε(t). Фототок приемника в любой момент времени t без учета шумов пропорционален квадрату падающего поля: где E(t) – напряженность электрического поля. Полное поле Ε(t) является суммой полей рассеянного Eв(t) и опорного Ео(t) пучков. Следовательно, Обычно наблюдаемой величиной является спектр мощности S(ω) фототока, равный преобразованию Фурье его автокорреляционной функции:

Используется несколько типовых структурных схем, реализующих метод фотосмешения, для регистрации доплеровского сдвига лазерного излучения при измерении скоростей движения в жидкостных двухфазных системах, к которым относится кровь. Рассмотрим наиболее простые: - одноканальная схема с фотосмешением отраженного и опорного потоков; - дифференциальная схема с фотосмешением отраженного и опорного потоков.
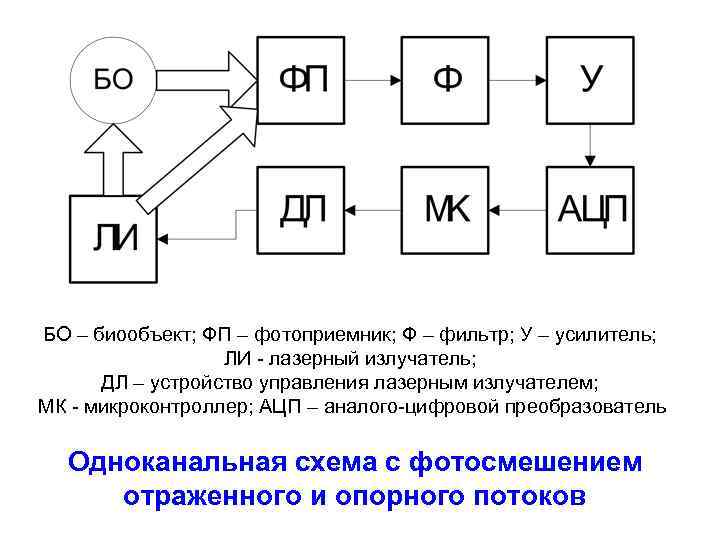
БО – биообъект; ФП – фотоприемник; Ф – фильтр; У – усилитель; ЛИ - лазерный излучатель; ДЛ – устройство управления лазерным излучателем; МК - микроконтроллер; АЦП – аналого-цифровой преобразователь Одноканальная схема с фотосмешением отраженного и опорного потоков

Одноканальная упрощенная схема, реализующая смешение отраженного и опорного потоков на фотоприемнике ФП. Лазерное излучение от лазерного излучателя ЛИ по оптоволокну подается непосредственно на поверхность ткани, перфузию кровью которой необходимо определить. По другому оптоволокну отраженный и рассеянный свет подается на фотоприемник. Одновременно на фотоприемник подается и часть светового потока непосредственно с лазерного излучателя, формирующая опорный поток. Опорный и отраженный потоки смешиваются на фотоприемнике и преобразуются в фототок. Электрический сигнал с фотоприемника поступает на фильтр Ф, где выделяется разностная частота доплеровского сдвига. Отфильтрованный сигнал усиливается усилителем У и преобразуется в цифровой код с помощью АЦП. Микроконтроллер МК анализирует спектр мощности сигнала и вычисляет перфузию кровью исследуемого участка ткани. К недостаткам данной схемы можно отнести подверженность к артефактам, вызванным движением оптоволокна и пациента, так как такие движения будут вносить большой вклад в переменную составляющую фототока.

БО – биообъект; ФП 1, ФП 2 – фотоприемники; Ф 1, Ф 2 – фильтры; ДУ – дифференциальный усилитель; ЛИ - лазерный излучатель Дифференциальная схема с фотосмешением отраженного и опорного потоков

В данном случае изменение светового потока, вызванное движением пациента или излучающей головки на конце оптоволокна, является синфазным для двух каналов и удаляется после дифференциального усилителя. Информативный же сигнал слабо коррелирует в двух каналах, и поэтому дифференциальным усилителем не подавляется. После усилителя сигнал оцифровывается и анализируется микроконтроллером.

Аппарат ЛДФ: серия ЛАКК www. lazma. ru Общий вид анализатора ЛАКК-02– исполнение 1 1 – блок анализатора, 2 – базовый зонд для исследования микроциркуляции, 3 – белый диск из фторопласта для проверки нулевого показания каналов, 4 – ручка установки нулевого положения, 5 – кнопка увеличения показателей микроциркуляции в 3 раза, 6 – кнопка вывода среднего значения показателя микроциркуляции за интервал времени 2 мин. на индикаторное табло. Общий вид анализатора ЛАКК-02 – исполнение 2 1 – блок анализатора, 2 – световодный зонд (2 штуки), световодный зонд 1 канала имеет маркировку красного цвета, световодный зонд 2 канала имеет маркировку черного цвета, 3 – ручки установки нулевого положения соответственно 1 и 2 каналов, 4 – белый диск из фторопласта для проверки нулевого показания каналов, 5 – кнопка увеличения показателей микроциркуляции в 3 раза, 6 – тумблер переключения каналов, 7 – кнопка вывода на индикаторные панели средних значений показателей микроциркуляции по обоим каналам за интервал времени 2 мин. , 8 – кнопка вывода на индикаторные панели разности значений показателей микроциркуляции между 1 -ым и 2 -ым каналами в процентах. За 100 принимается наибольшее значение показателей микроциркуляции. 31

АППАРАТУРА «ЛАКК-ТЕСТ» 32 Предназначена для осуществления избирательных функциональных нагрузок на систему микроциркуляции.

Аппаратура «ЛАКК-ТЕСТ» состоит из двух блоков: «ЛАКК-ТЕСТ (Т)» и «ЛАККТЕСТ (Э)» , с помощью которых возможно организовать следующие функциональные нагрузки: температурный тест (5 – 50 С), ионофоретический тест – диффузный ввод лекарств, электростимуляционный тест – вазодилатация в результате активации сенсорной регуляции. В состав блока «ЛАККТЕСТ (Т) входит пробник для измерения температуры кожи. 33
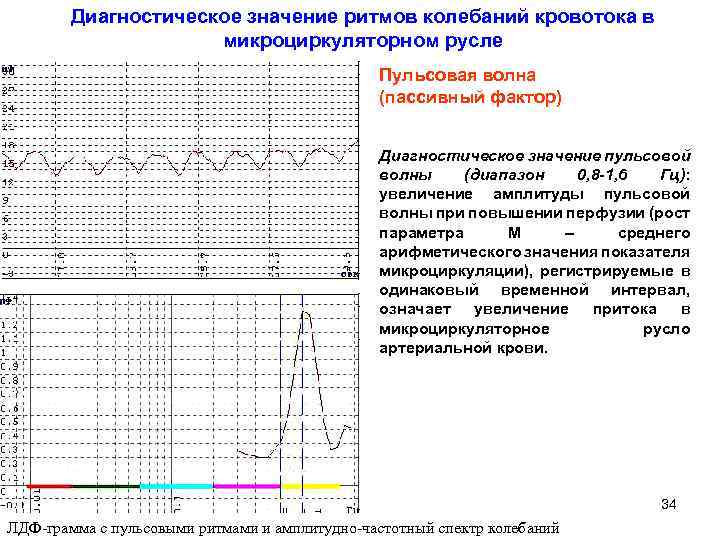
Диагностическое значение ритмов колебаний кровотока в микроциркуляторном русле Пульсовая волна (пассивный фактор) Диагностическое значение пульсовой волны (диапазон 0, 8 -1, 6 Гц): увеличение амплитуды пульсовой волны при повышении перфузии (рост параметра М – среднего арифметического значения показателя микроциркуляции), регистрируемые в одинаковый временной интервал, означает увеличение притока в микроциркуляторное русло артериальной крови. 34 ЛДФ-грамма с пульсовыми ритмами и амплитудно-частотный спектр колебаний
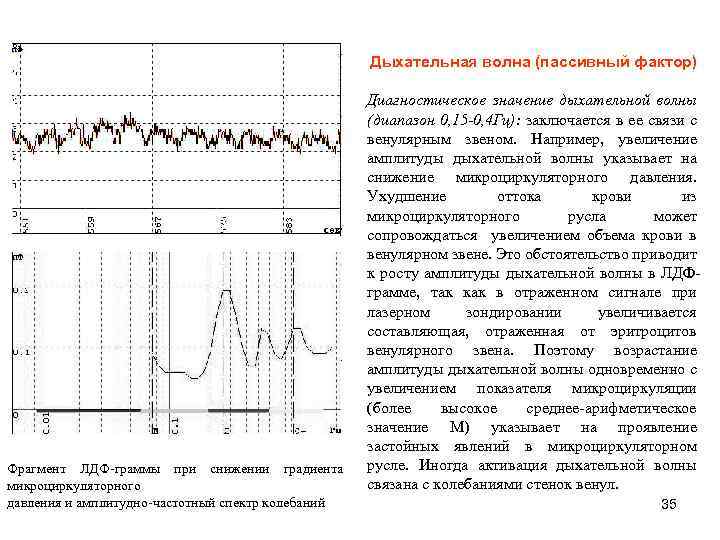
Дыхательная волна (пассивный фактор) Фрагмент ЛДФ-граммы при снижении градиента микроциркуляторного давления и амплитудно-частотный спектр колебаний Диагностическое значение дыхательной волны (диапазон 0, 15 -0, 4 Гц): заключается в ее связи с венулярным звеном. Например, увеличение амплитуды дыхательной волны указывает на снижение микроциркуляторного давления. Ухудшение оттока крови из микроциркуляторного русла может сопровождаться увеличением объема крови в венулярном звене. Это обстоятельство приводит к росту амплитуды дыхательной волны в ЛДФграмме, так как в отраженном сигнале при лазерном зондировании увеличивается составляющая, отраженная от эритроцитов венулярного звена. Поэтому возрастание амплитуды дыхательной волны одновременно с увеличением показателя микроциркуляции (более высокое среднее-арифметическое значение М) указывает на проявление застойных явлений в микроциркуляторном русле. Иногда активация дыхательной волны связана с колебаниями стенок венул. 35
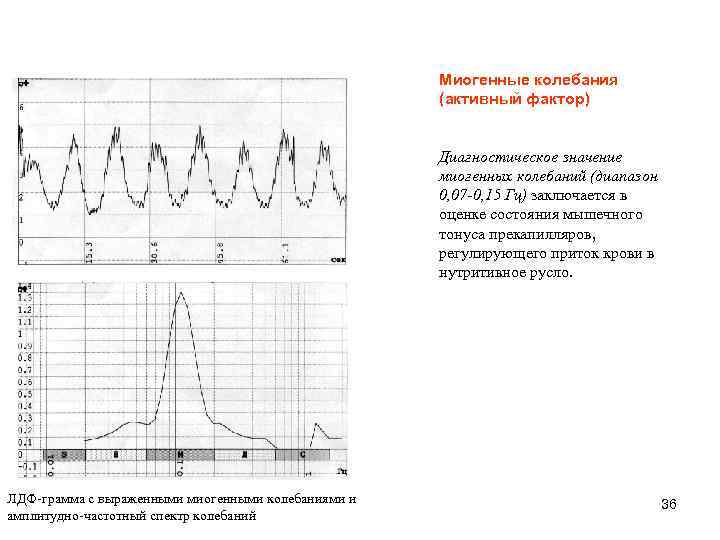
Миогенные колебания (активный фактор) Диагностическое значение миогенных колебаний (диапазон 0, 07 -0, 15 Гц) заключается в оценке состояния мышечного тонуса прекапилляров, регулирующего приток крови в нутритивное русло. ЛДФ-грамма с выраженными миогенными колебаниями и амплитудно-частотный спектр колебаний 36
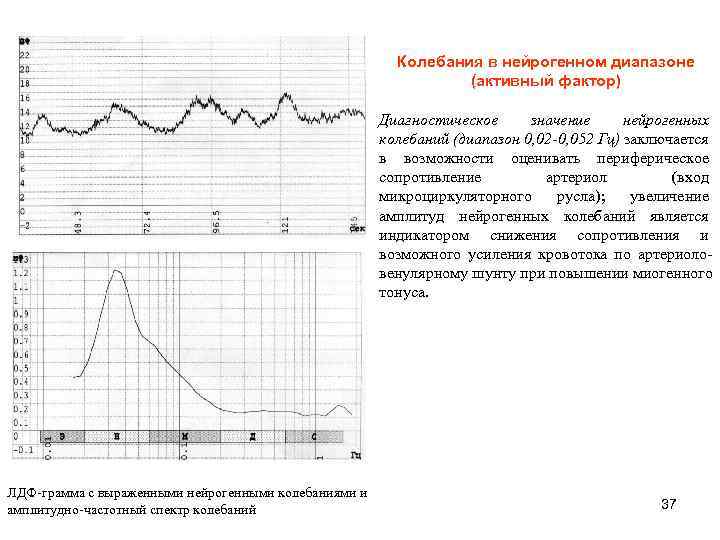
Колебания в нейрогенном диапазоне (активный фактор) Диагностическое значение нейрогенных колебаний (диапазон 0, 02 -0, 052 Гц) заключается в возможности оценивать периферическое сопротивление артериол (вход микроциркуляторного русла); увеличение амплитуд нейрогенных колебаний является индикатором снижения сопротивления и возможного усиления кровотока по артериоловенулярному шунту при повышении миогенного тонуса. ЛДФ-грамма с выраженными нейрогенными колебаниями и амплитудно-частотный спектр колебаний 37
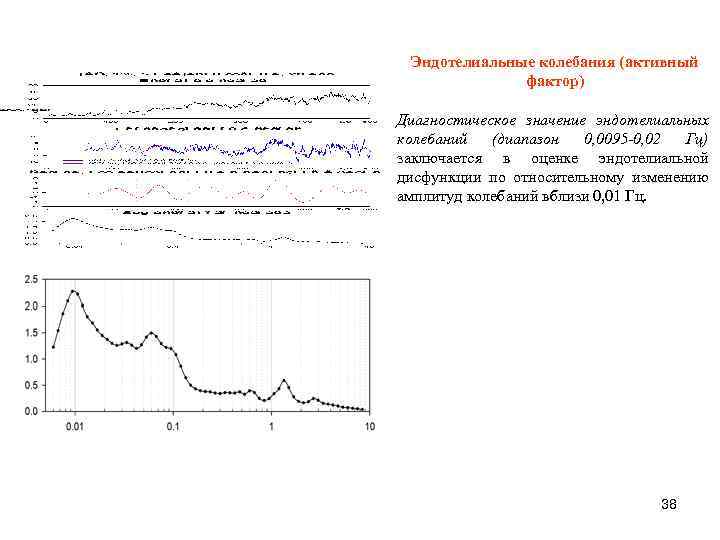
Эндотелиальные колебания (активный фактор) Диагностическое значение эндотелиальных колебаний (диапазон 0, 0095 -0, 02 Гц) заключается в оценке эндотелиальной дисфункции по относительному изменению амплитуд колебаний вблизи 0, 01 Гц. 38
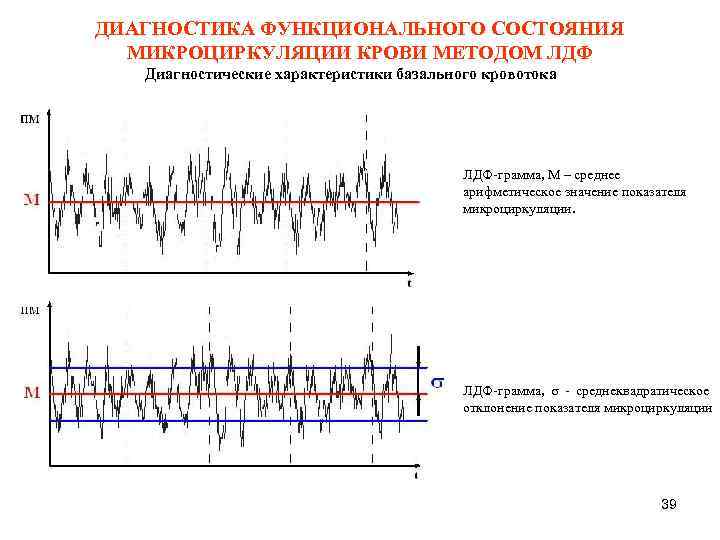
ДИАГНОСТИКА ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ МИКРОЦИРКУЛЯЦИИ КРОВИ МЕТОДОМ ЛДФ Диагностические характеристики базального кровотока ЛДФ-грамма, М – среднее арифметическое значение показателя микроциркуляции. ЛДФ-грамма, - среднеквадратическое отклонение показателя микроциркуляции 39

Очевидно, что изменение значений М и σ связаны. Например, повышение перфузии при ослаблении сосудистого тонуса приводит к увеличению М в результате увеличения объема кровотока в артериолах, и вместе с тем может привести к увеличению σ из-за повышения амплитуды сердечного ритма, который привносится из артерий большим количеством эритроцитов, поступающих в артериолы. Аналогично, при явлениях застоя крови в венулах увеличивается число эритроцитов в венулярном звене, что в случае снижения перфузионного давления приводит к увеличению амплитуды дыхательного ритма, и, как следствие, к росту М и σ. Поэтому в анализе расчетных параметров целесообразно ориентироваться на соотношение величин М и σ, то есть на коэффициент вариации: Кv = σ/М · 100% Увеличение величины Кv отражает улучшение состояния микроциркуляции, так как увеличение этого коэффициента связано с повышением σ в результате активации эндотелиальной секреции, нейрогенного и миогенного механизмов контроля при практически не изменяющейся величине М. Увеличение амплитуд сердечного и иногда дыхательного ритмов сопровождается повышением параметра средней перфузии М и при нормировке σ/М влияние изменений последних ритмов нивелируется. Расчетные параметры М, σ и Kv дают общую оценку состояния микроциркуляции крови. Более детальный анализ функционирования микроциркуляторного русла может быть проведен на втором этапе обработки ЛДФ-грамм базального кровотока при исследовании структуры ритмов колебаний перфузии крови. На втором этапе анализируется амплитудно-частотный спектр (АЧС) колебаний перфузии. По величинам амплитуд колебаний микрокровотока в конкретных частотных диапазонах возможно оценивать состояние функционирования определенных механизмов контроля перфузии. 40
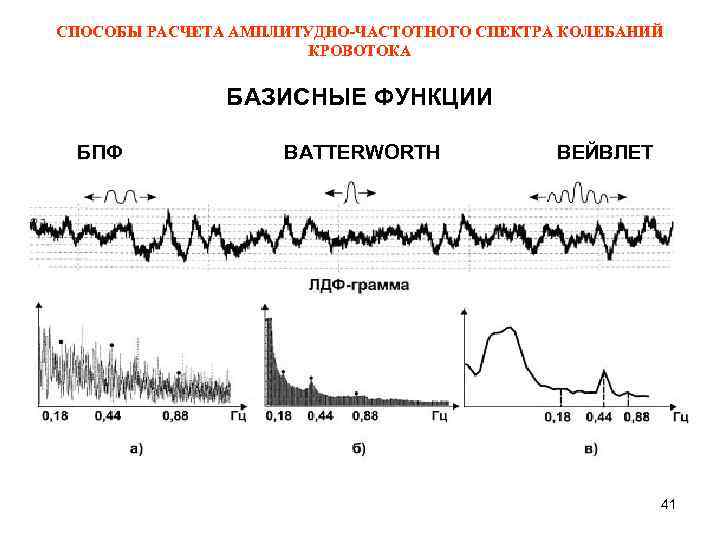
СПОСОБЫ РАСЧЕТА АМПЛИТУДНО-ЧАСТОТНОГО СПЕКТРА КОЛЕБАНИЙ КРОВОТОКА БАЗИСНЫЕ ФУНКЦИИ БПФ BATTERWORTH ВЕЙВЛЕТ 41
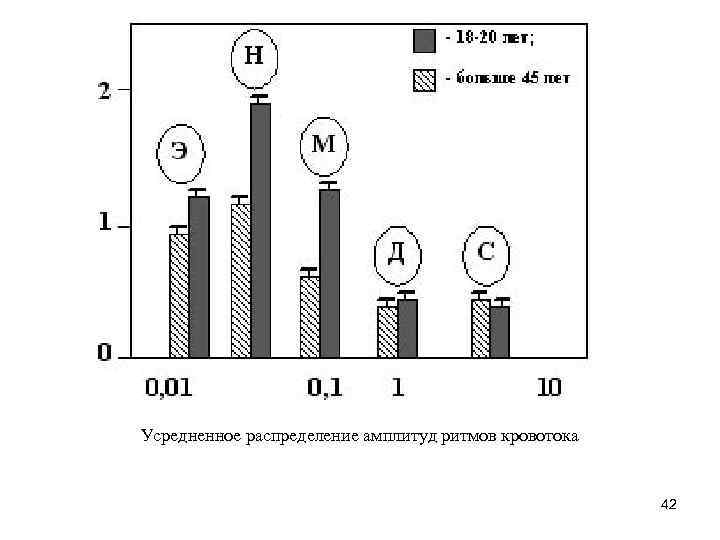
Усредненное распределение амплитуд ритмов кровотока 42
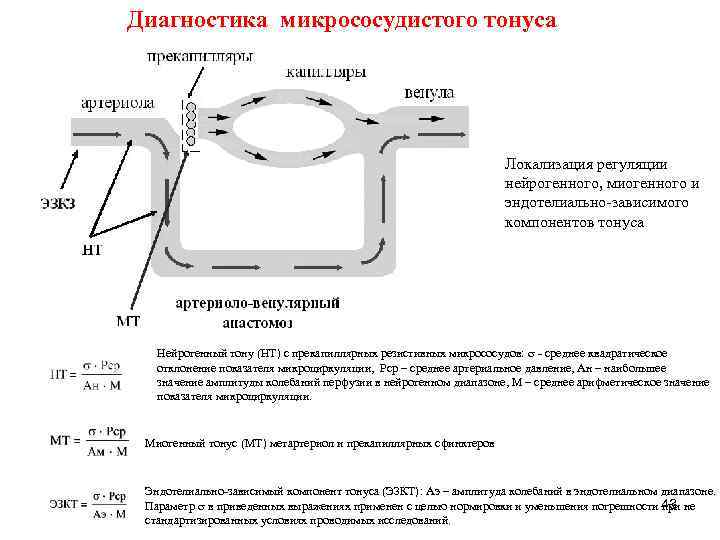
Диагностика микрососудистого тонуса Локализация регуляции нейрогенного, миогенного и эндотелиально-зависимого компонентов тонуса Нейрогенный тону (НТ) с прекапиллярных резистивных микрососудов: - среднее квадратическое отклонение показателя микроциркуляции, Рср – среднее артериальное давление, Ан – наибольшее значение амплитуды колебаний перфузии в нейрогенном диапазоне, М – среднее арифметическое значение показателя микроциркуляции. Миогенный тонус (МТ) метартериол и прекапиллярных сфинктеров Эндотелиально-зависимый компонент тонуса (ЭЗКТ): Аэ – амплитуда колебаний в эндотелиальном диапазоне. 43 Параметр в приведенных выражениях применен с целью нормировки и уменьшения погрешности при не стандартизированных условиях проводимых исследований.
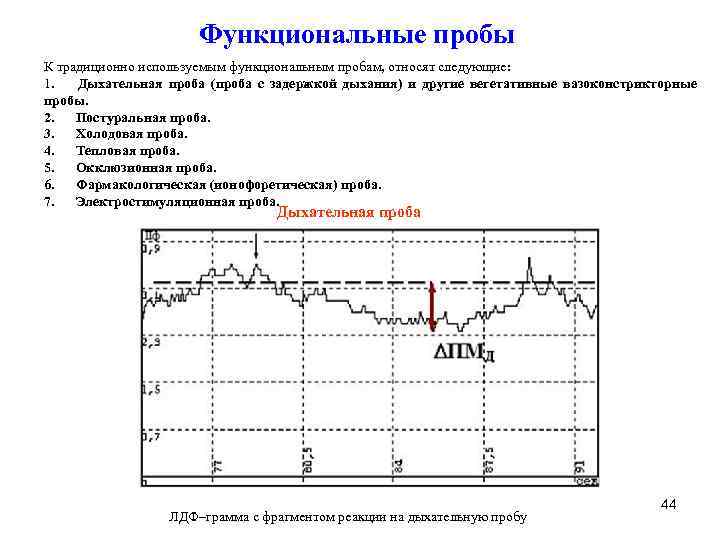
Функциональные пробы К традиционно используемым функциональным пробам, относят следующие: 1. Дыхательная проба (проба с задержкой дыхания) и другие вегетативные вазоконстрикторные пробы. 2. Постуральная проба. 3. Холодовая проба. 4. Тепловая проба. 5. Окклюзионная проба. 6. Фармакологическая (ионофоретическая) проба. 7. Электростимуляционная проба. Дыхательная проба ЛДФ–грамма с фрагментом реакции на дыхательную пробу 44

Постуральная (ортостатическая) проба Постуральная проба здорового человека 45
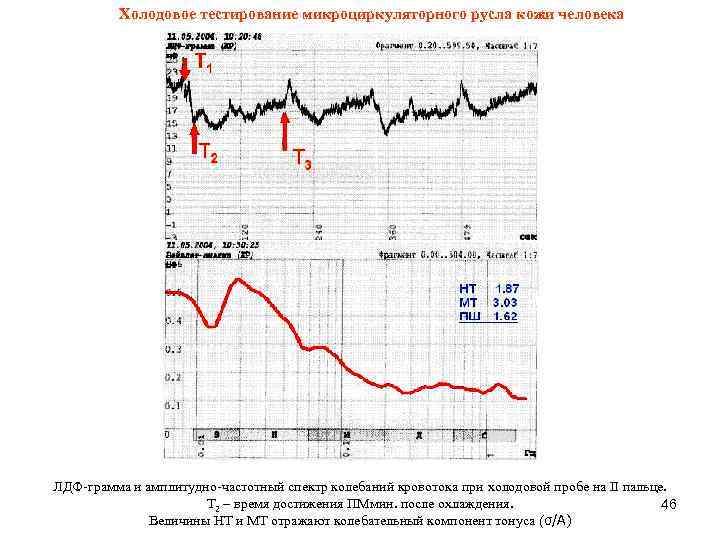
Холодовое тестирование микроциркуляторного русла кожи человека ЛДФ-грамма и амплитудно-частотный спектр колебаний кровотока при холодовой пробе на II пальце. Т 2 – время достижения ПМмин. после охлаждения. 46 Величины НТ и МТ отражают колебательный компонент тонуса (σ/А)
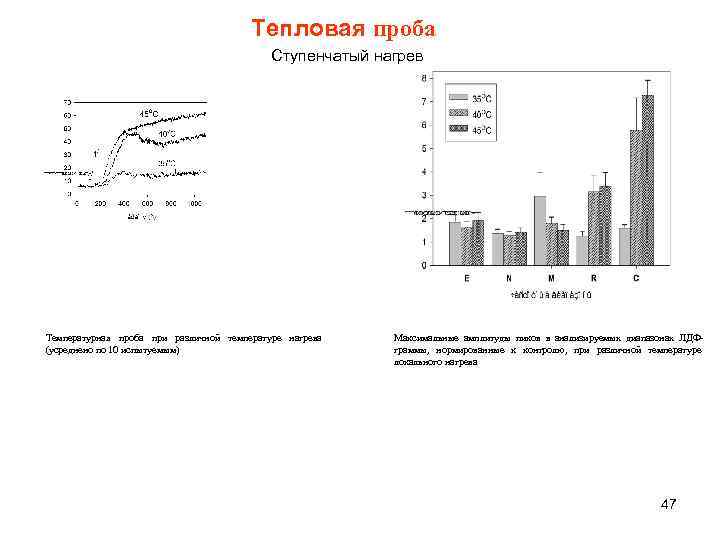
Тепловая проба Ступенчатый нагрев Температурная проба при различной температуре нагрева (усреднено по 10 испытуемым) Максимальные амплитуды пиков в анализируемых диапазонах ЛДФграммы, нормированные к контролю, при различной температуре локального нагрева 47
Линейный нагрев Зависимость показателя микроциркуляции от времени (А) и температуры нагрева (Б). 48
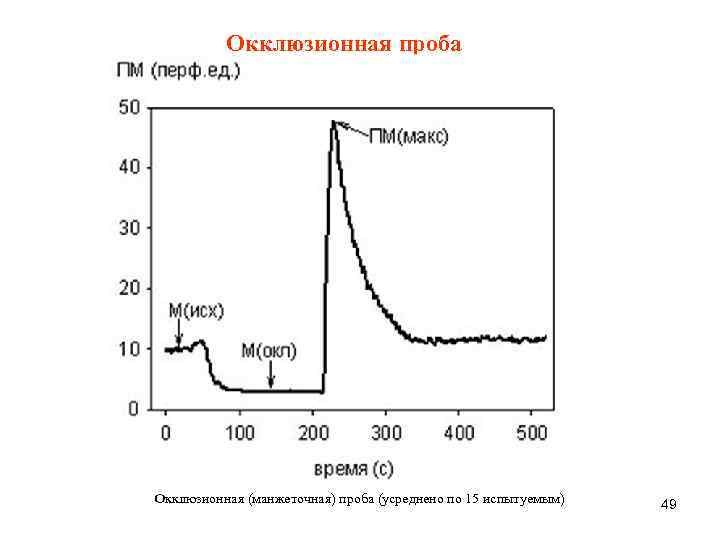
Окклюзионная проба Окклюзионная (манжеточная) проба (усреднено по 15 испытуемым) 49
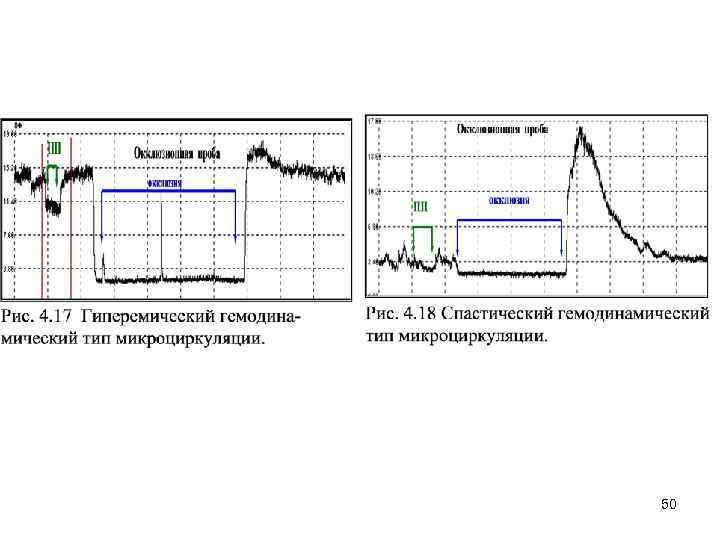
50
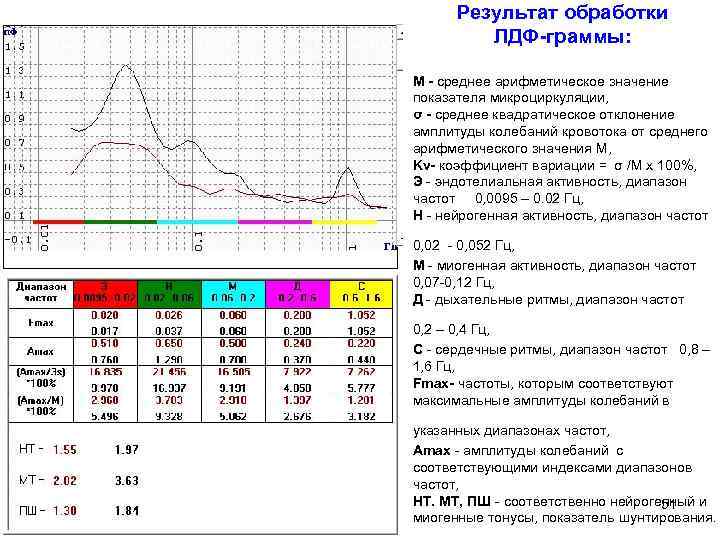
Результат обработки ЛДФ-граммы: М - среднее арифметическое значение показателя микроциркуляции, σ - среднее квадратическое отклонение амплитуды колебаний кровотока от среднего арифметического значения М, Kv- коэффициент вариации = σ /М х 100%, Э - эндотелиальная активность, диапазон частот 0, 0095 – 0. 02 Гц, Н - нейрогенная активность, диапазон частот 0, 02 - 0, 052 Гц, М - миогенная активность, диапазон частот 0, 07 -0, 12 Гц, Д - дыхательные ритмы, диапазон частот 0, 2 – 0, 4 Гц, С - сердечные ритмы, диапазон частот 0, 8 – 1, 6 Гц, Fmax- частоты, которым соответствуют максимальные амплитуды колебаний в указанных диапазонах частот, Amax - амплитуды колебаний с соответствующими индексами диапазонов частот, НТ. МТ, ПШ - соответственно нейрогенный и 51 миогенные тонусы, показатель шунтирования.

Многофункциональные неинвазивные спектрофотометрические диагностические системы Многофункциональные лазерные диагностические комплексы (МЛДК)

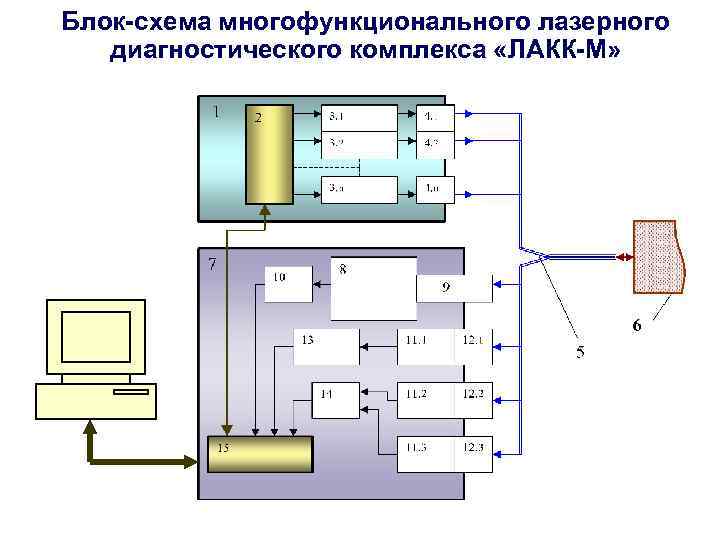
МЛДК предназначены для реализации на нескольких (например, 12) длинах волн одновременно таких методов НМС как ЛФД, ЛДФ, ФПГ, ОТО и др. при разрешении одновременно двух слоев биоткани. С целью сбора необходимого массива данных для решения обратной задачи в конструкции МЛДК предусмотрена возможность сбора оптических сигналов по поверхности тестируемой области. Для этого излучение от набора лазеров 1 доставляется по световоду 2 к локальному участку обследуемой ткани 3, а вышедшее из ткани вторичное оптическое излучение (обратно рассеянное, флюоресцентное и т. п. ) одновременно регистрируется в нескольких (не менее 2) пространственных точках на поверхности биоткани световодами 4 а, 4 б и т. д. на разном расстоянии от участка освещения так, чтобы зарегистрировать тенденцию в изменении параметров вторичного излучения на каждой воздействующей длине волны за счет разницы в длине пути вторичного излучения внутри биоткани от участка воздействия до точек регистрации. При этом оптико-электронная система регистрации и выделния полезных сигналов 5 выполнена, соответственно, в виде двух или более одинаковых спектральных оптических блоков (6 а, 6 б и т. д. , регистрирующих доставляемое к ним излучение. Получаемая в результате диагностическая информация с учетом разных длин волн и создает необходимый массив данных для решения обратной задачи в ПК 7.
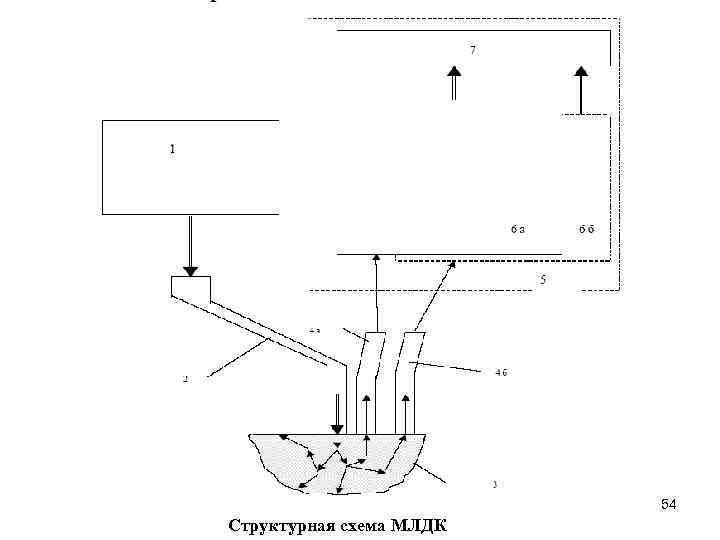
54 Структурная схема МЛДК

Оптико-электронная система регистрации 5 представляет собой устройство, производящее оптическую фильтрацию и селекцию регист-рируемых сигналов, преобразование оптических сигналов в электрические, электронное усиление и фильтрацию электрических сигналов, их оцифровку и передачу в ПК. Пришедшее от биоткани излучение в распределительном узле 10 посредством отвода от общего оптического жгута части его приемных волокон распределяется по спектральным оптическим блокам (СОБ) 11 и 12. СОБ 11 реализует динамическую, с разрешением по времени до 10(-6) с, регистрацию пришедших сигналов основного спектра (на длинах волн источников излучения) с целью реализации методик ЛДФ и ФПГ. Для этого он содержит «n» быстродействующих фотодиодов 13 а, 13 б …. 13 n, излучение на которые из основного потока отводится селективными по спектру зеркалами 14. Электрические сигналы с фотодиодов поступают на блок предварительного усиления 15, представляющий собой набор из «n» широкополосных усилителей. После усиления сигналы поступают в блок 16 для выделения и усиления для каждого сигнала отдельно его высокочастотной переменной, а также постоянной и низкочастотной переменной составляющих. После разделения все сигналы поступают на блок 17 для оцифровки, коммутации и передачи дальше в ПК. СОБ 12 реализует выделение и статическую регистрацию сигналов флюоресценции. Он выполнен по традиционной схеме полихроматора с дифракционной решеткой 18 и оптической схемой формирования луча 19 на основе зеркальной оптики. На входе полихроматора устанавливается набор сменных фильтров 20, гасящих до необходимого уровня излучение на длинах волн источников. Разложенное в спектр излучение попадает на матрицу высокочувствительных (до 10(-12)Вт) фотоприемников 21 на основе ПЗС структур. Далее электрический сигнал подается на блок усиления, оцифровки и коммутации сигналов 22 и передается в ПК. Смена фильтров 20 осуществляется шаговым двигателем в зависимости от выбранной длины волны и необходимого коэффициента ослабления β. Электронное управление работой всех узлов и блоков, анализ и обработка первичных сигналов и результатов диагностики в целом производятся управляющим ПК.
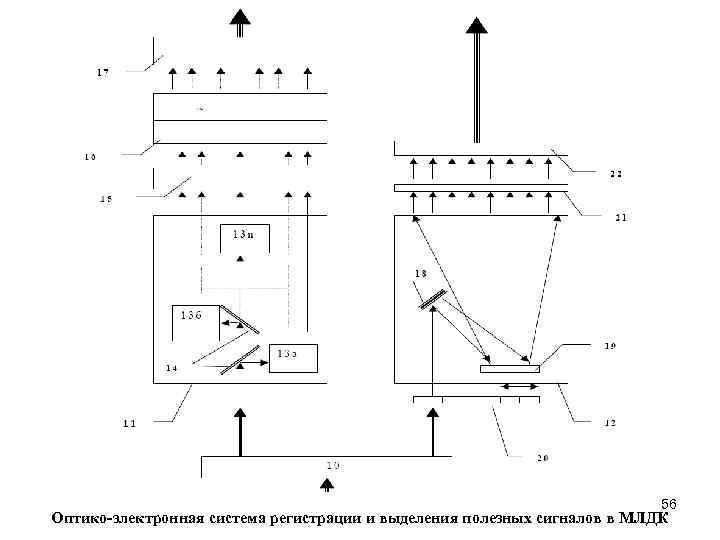
56 Оптико-электронная система регистрации и выделения полезных сигналов в МЛДК

Опытный макет многофункционального лазерного диагностического комплекса «ЛАКК-М» Оптический зонд для наружных и эндоскопических процедур
Блок-схема многофункционального лазерного диагностического комплекса «ЛАКК-М»
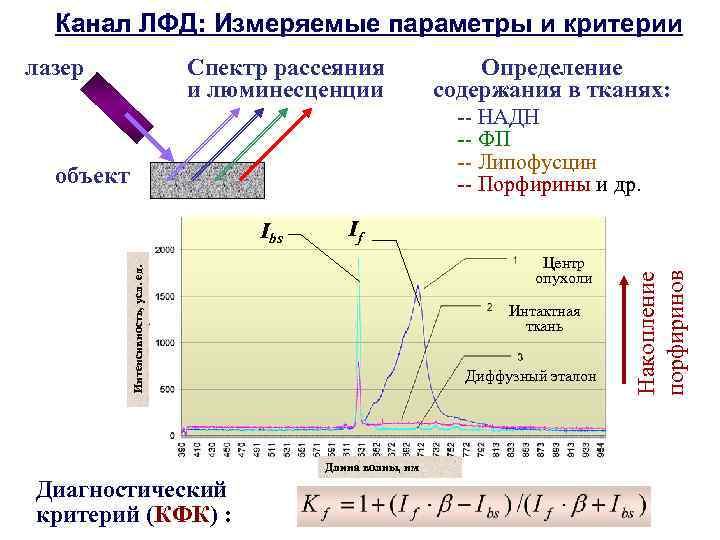
Канал ЛФД: Измеряемые параметры и критерии лазер Спектр рассеяния и люминесценции Определение содержания в тканях: -- НАДН -- ФП -- Липофусцин -- Порфирины и др. объект Центр опухоли Интактная ткань Диффузный эталон Длина волны, нм Диагностический критерий (КФК) : Накопление порфиринов If Интенсивность, усл. ед. Ibs
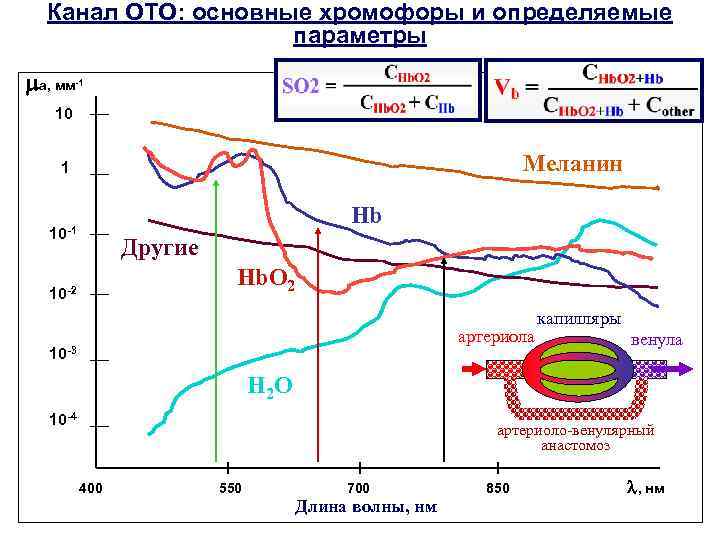
Канал ОТО: основные хромофоры и определяемые параметры a, мм -1 10 Меланин 1 Hb 10 -1 Другие Hb. O 2 10 -2 артериола 10 -3 капилляры венула H 2 O 10 -4 артериоло-венулярный анастомоз 400 550 700 Длина волны, нм 850 , нм

Диагностический объем в ОТО и определение средней сатурации SO 2 Датчик (оптоволокно) SO 2 a Среднее SO 2 2 -3 мм SO 2 в

Многофункциональный лазерный диагностический комплекс ЛАКК-М (исполнение 1) Основной вариант поставки: - доплеровский канал с лазером на длину волны 0, 8 мкм; - спектрофотометрический канал с лазерами на длины волн 0, 53 мкм и 0, 63 мкм; -флуоресцентный канал с излучателями на длины волн 0, 37 мкм, 0, 53 мкм и 0, 63 мкм; - пульоксиметрический канал; - составной световодный зонд для доставки зондирующего излучения и приема отраженного от ткани излучения; - программное обеспечение.

Многофункциональный лазерный диагностический комплекс ЛАКК-М (исполнение 2) МЛДК ЛАКК-М (исполнение 2) обеспечивает одновременные измерения перфузии ткани кровью, сатурации гемоглобина кислородом (SO 2) и объем фракции гемоглобина (Vr) в зондируемой области исследования. Оценка перфузии осуществляется методом лазерной допплеровской флоуметрии (ЛДФ), а вычисление SO 2 и Vr производится по методологии абсорбционной спектроскопии. SO 2 определяется на основе разных оптических свойств оксигенированных (Hb. O 2) и дезоксигенированных (Hb) фракций гемоглобина, содержащихся в тестируемом объеме крови в биоткани. Для оценки параметров Vr и SO 2 используется разница в регистрируемых сигналах при зондировании биоткани в красном и зеленом спектральных диапазонах длин волн.
Оптическая диагностика.ppt