4-5Молекулярная биофизика.ppt
- Количество слайдов: 92

Раздел: Молекулярная биофизика Тема: Пространственная организация биополимеров
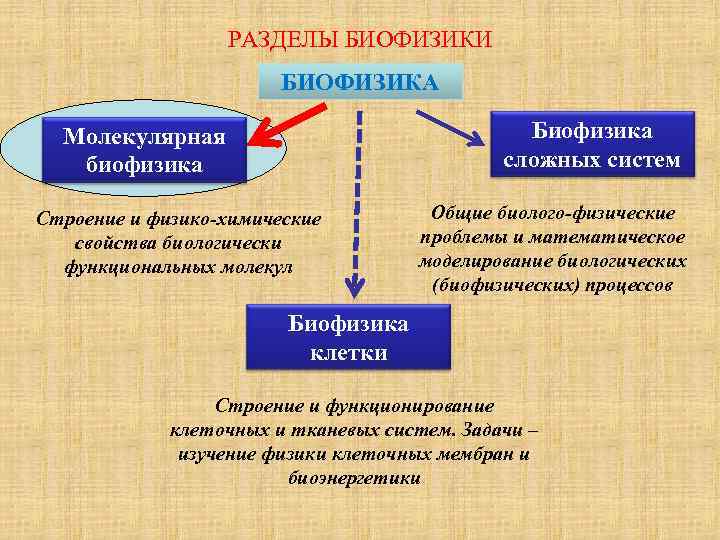
РАЗДЕЛЫ БИОФИЗИКИ БИОФИЗИКА Биофизика сложных систем Молекулярная биофизика Строение и физико-химические свойства биологически функциональных молекул Общие биолого-физические проблемы и математическое моделирование биологических (биофизических) процессов Биофизика клетки Строение и функционирование клеточных и тканевых систем. Задачи – изучение физики клеточных мембран и биоэнергетики

Молекулярная биология (развитие генетики и цитологии) • Объекты исследования: биологические молекулы (белки и нуклеиновые кислоты), их строение и свойства • Методы исследования: - Биологические - Физические - Химические
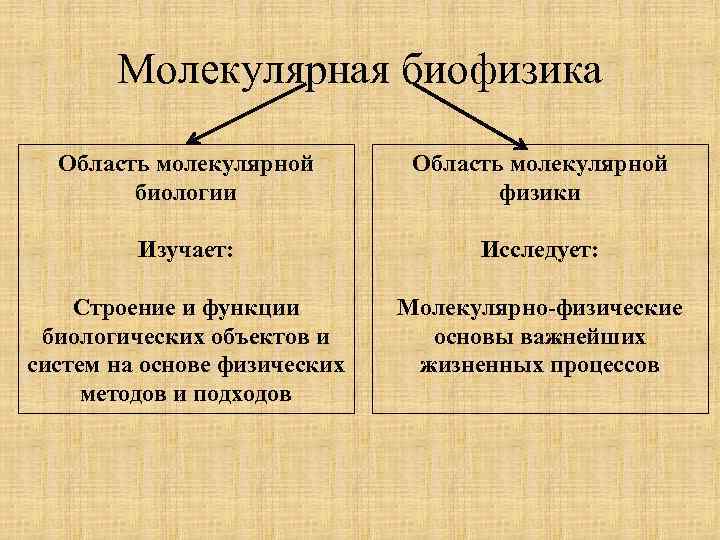
Молекулярная биофизика Область молекулярной биологии Область молекулярной физики Изучает: Исследует: Строение и функции биологических объектов и систем на основе физических методов и подходов Молекулярно-физические основы важнейших жизненных процессов

Гибкость полимерной цепи Какова характерная форма молекулярной цепи в различных полимерных веществах (какова конформация)? Прямолинейная конформация Конформация запутанного клубка

Модели гибкости полимерных цепей • Персистентная модель (червеобразная) • Свободно сочлененная модель
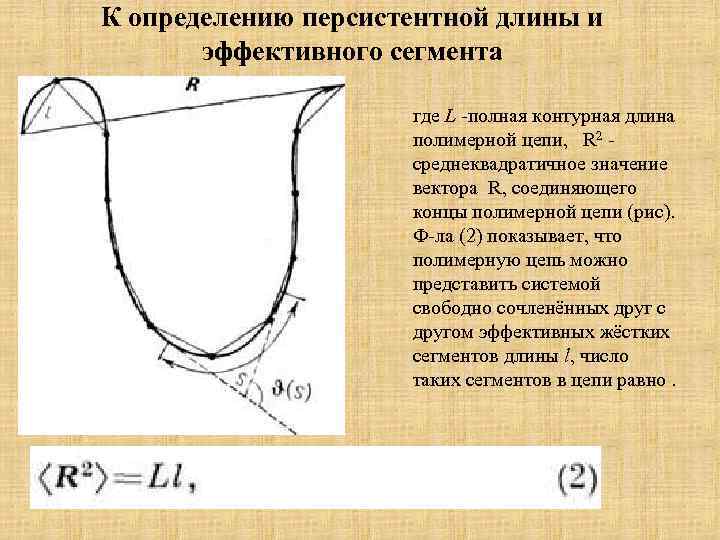
К определению персистентной длины и эффективного сегмента где L -полная контурная длина полимерной цепи, R 2 среднеквадратичное значение вектора R, соединяющего концы полимерной цепи (рис). Ф-ла (2) показывает, что полимерную цепь можно представить системой свободно сочленённых друг с другом эффективных жёстких сегментов длины l, число таких сегментов в цепи равно.
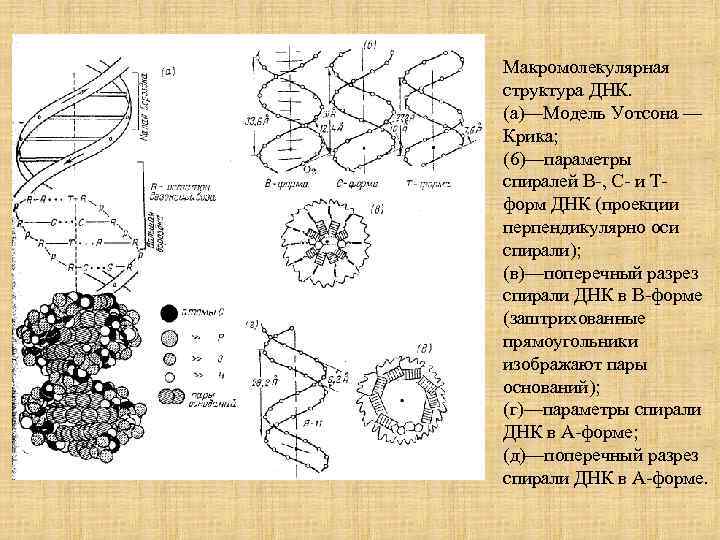
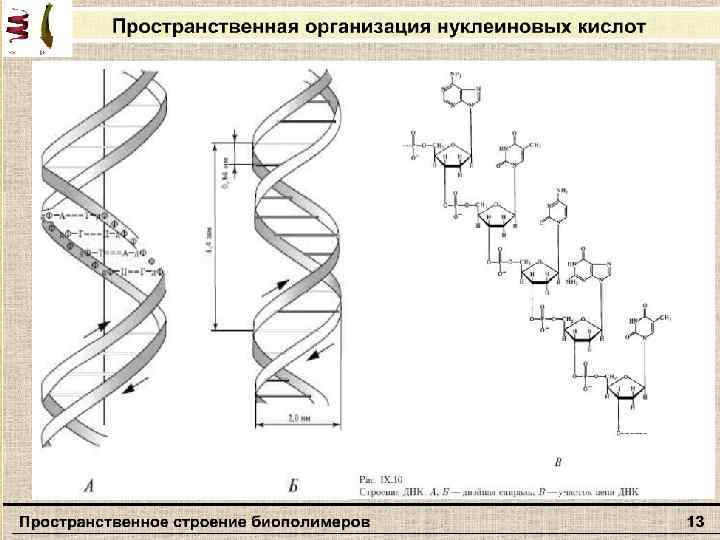
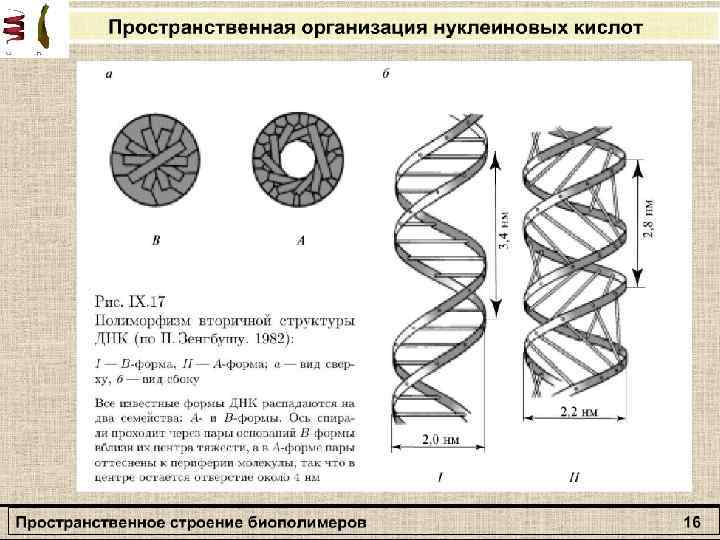
Макромолекулярная структура ДНК. (а)—Модель Уотсона — Крика; (6)—параметры спиралей В-, С- и Тформ ДНК (проекции перпендикулярно оси спирали); (в)—поперечный разрез спирали ДНК в В-форме (заштрихованные прямоугольники изображают пары оснований); (г)—параметры спирали ДНК в А-форме; (д)—поперечный разрез спирали ДНК в А-форме.
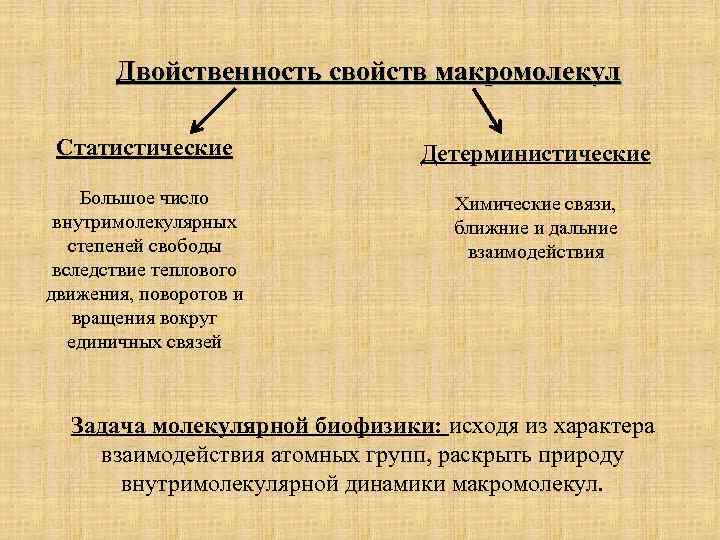
Двойственность свойств макромолекул Статистические Детерминистические Большое число внутримолекулярных степеней свободы вследствие теплового движения, поворотов и вращения вокруг единичных связей Химические связи, ближние и дальние взаимодействия Задача молекулярной биофизики: исходя из характера взаимодействия атомных групп, раскрыть природу внутримолекулярной динамики макромолекул.

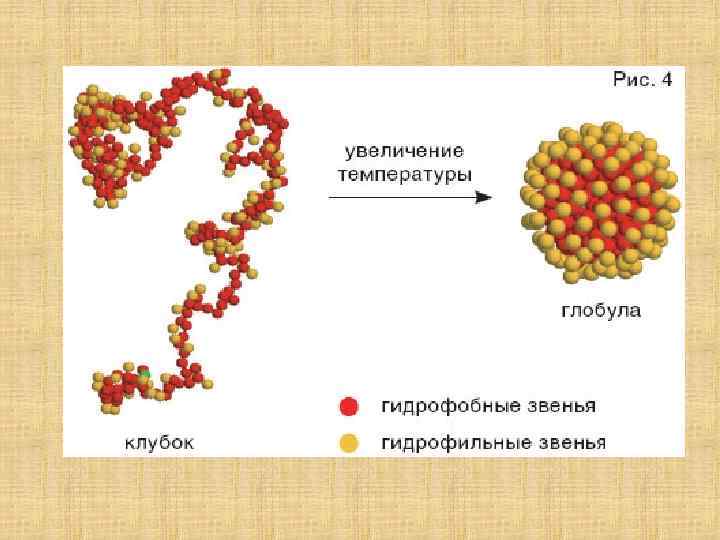

Полимерная цепь, где взаимодействуют только соседние звенья Клубок Свойства клубка ØПереход между конформациями в результате микроброуновского движения частей цепи. ØHe обладает внутренней структурой, все время «дышит» с амплитудой порядка размера клубка. ØВзаимное положение отдельных частей подчиняется статистическим закономерностям.

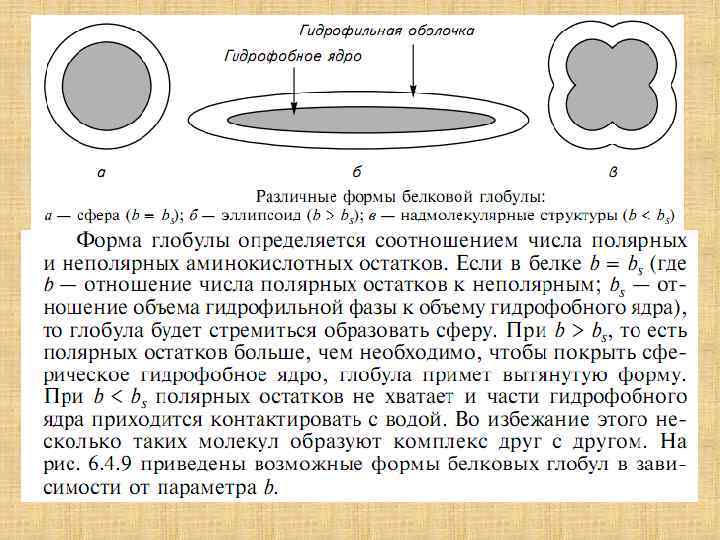
Полимерная цепь, где имеются объемные взаимодействия между атомами, далеко отстоящими друг от друга в цепи Глобула с плотной сердцевиной Свойства глобулы ØИмеет структуру ØСердцевина большой глобулы пространственно однородна с постоянной концентрацией звеньев (большей по сравнению с наружными слоями) Распределение плотности звеньев в глобуле в зависимости от расстояния от центра глобулы R 0 — радиус глобулы, n 0 — число звеньев

Переходы глобула-клубок (порядок-беспорядок) ØПроисходят в относительно малом интервале температур – подобны фазовым переходам 1 -го рода (напр. лед-вода) ØСопровождаются значительным изменением теплоемкости макромолекулы – структурные перестройки
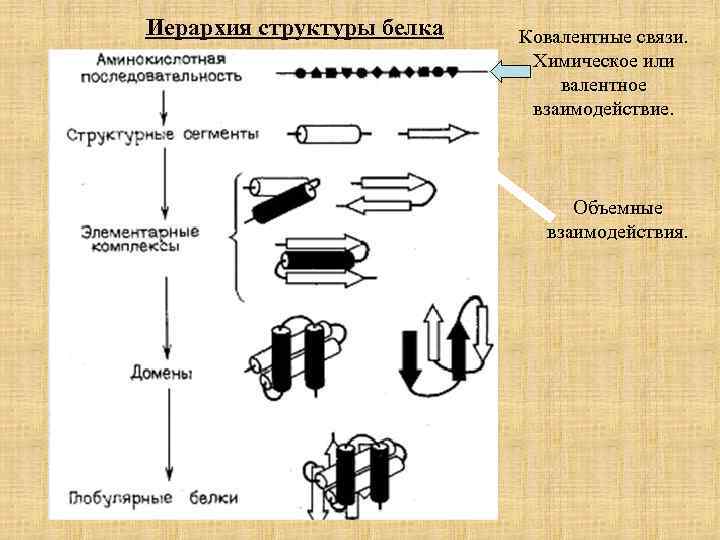
Иерархия структуры белка Ковалентные связи. Химическое или валентное взаимодействие. Объемные взаимодействия.
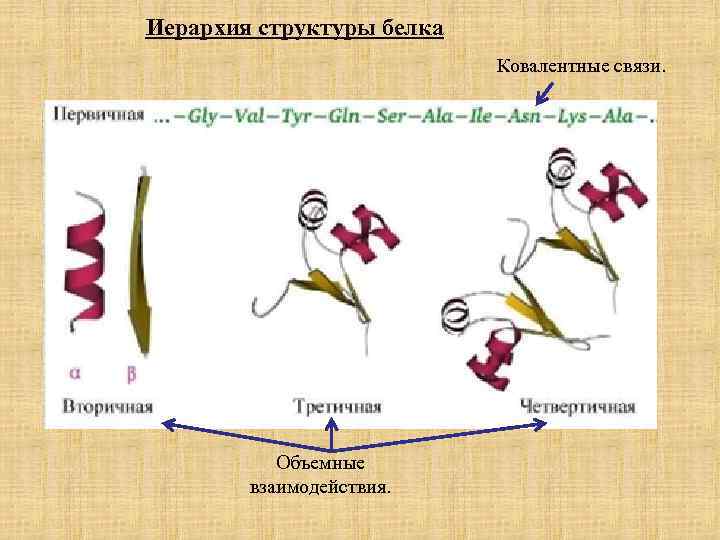
Иерархия структуры белка Ковалентные связи. Объемные взаимодействия.

Типы объемных взаимодействий 1 Ближние все типы взаимодействий на расстоянии 1 -4 а. о. 2 Средние – все типы взаимодействий на расстоянии 5 -15 а. о. 3 Дальние – все типы взаимодействий на расстоянии >15 а. о.




Конформация - такое распределение атомов в пространстве, которое можно изменить вращением вокруг одинарных связей (возможен разрыв и образование водородных связей). Конфигурация - такое распределение атомов в пространстве, которое можно изменить только за счет разрыва и образования химических связей.
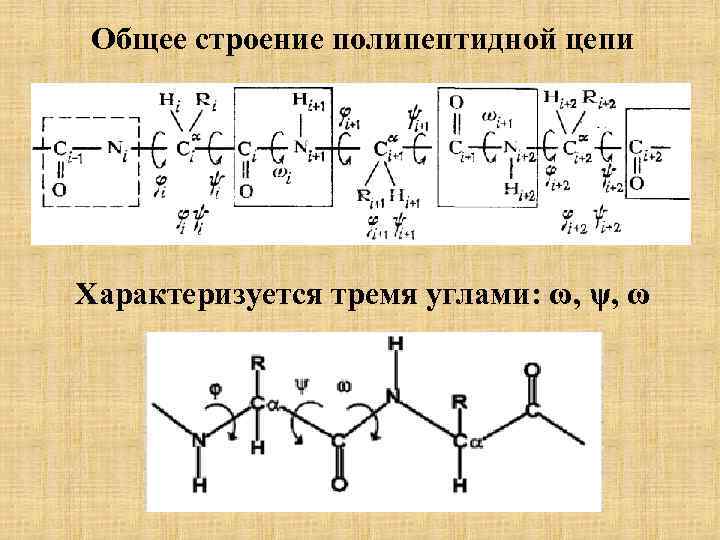
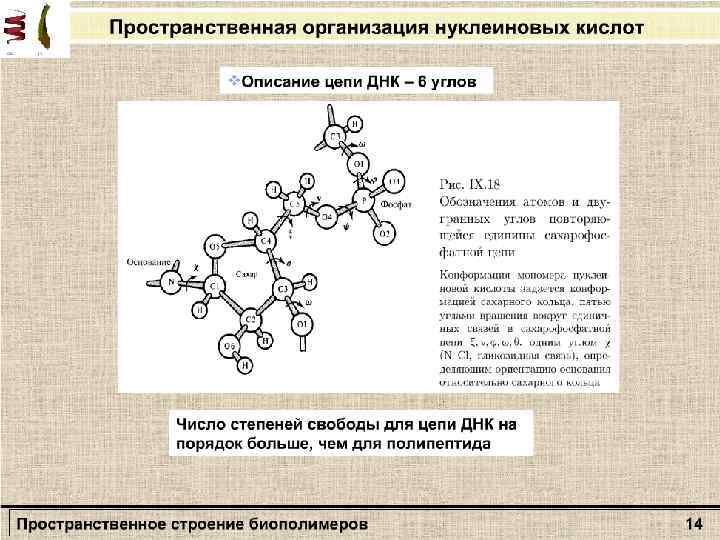
Общее строение полипептидной цепи Характеризуется тремя углами: ω, ψ, ω
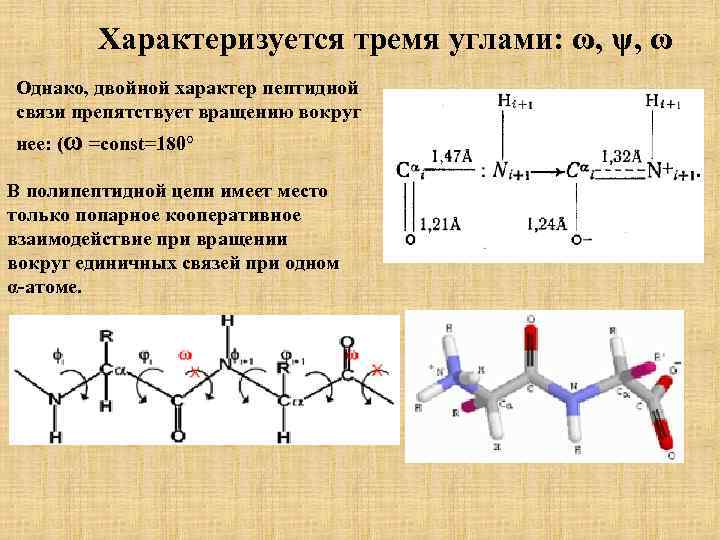
Характеризуется тремя углами: ω, ψ, ω Однако, двойной характер пептидной связи препятствует вращению вокруг нее: (ω =const=180° В полипептидной цепи имеет место только попарное кооперативное взаимодействие при вращении вокруг единичных связей при одном α-атоме.

Общее строение полипептидной цепи Общее выражение для конформационной энергии

Вопросы для самоконтроля 1. Чем отличаются свойства биополимера в состоянии клубка от свойств в состоянии глобулы? 2. Какими взаимодействиями удерживается первичная структура биополимеров? Вторичная? Третичная? 3. Какие взаимодействия являются причиной появления сил Ван-дер-Ваальса? Между какими группами они возникают? 4. Что такое конформация биополимера? Конфигурация? 5. Вращение вокруг каких связей определяет конформационную энергию полипептидной цепи?

Раздел: Молекулярная биофизика Тема: Взаимодействия в макромолекулах
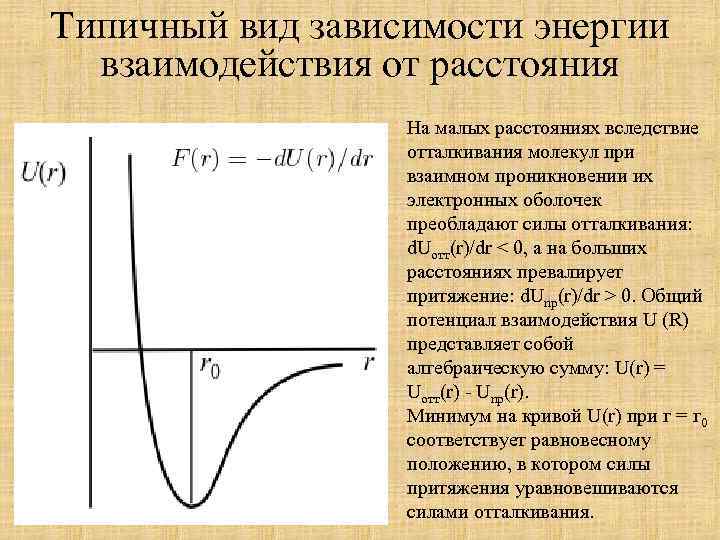
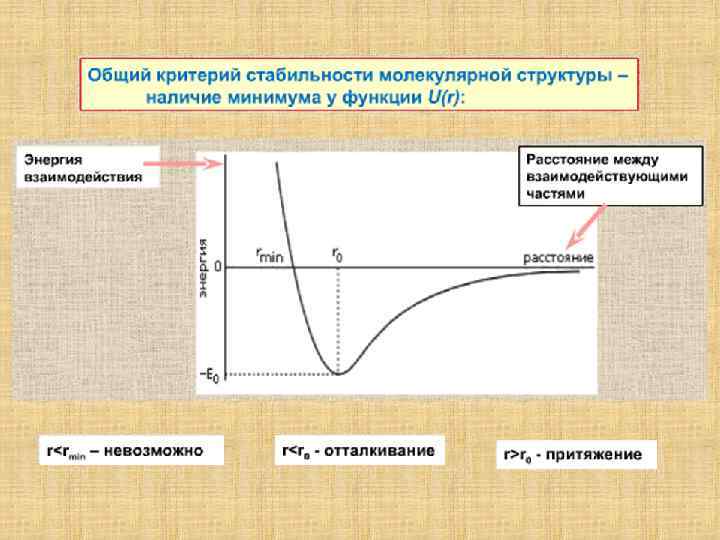
Типичный вид зависимости энергии взаимодействия от расстояния На малых расстояниях вследствие отталкивания молекул при взаимном проникновении их электронных оболочек преобладают силы отталкивания: d. Uотт(r)/dr < 0, а на больших расстояниях превалирует притяжение: d. Unp(r)/dr > 0. Общий потенциал взаимодействия U (R) представляет собой алгебраическую сумму: U(r) = Uотт(r) - Unp(r). Минимум на кривой U(r) при г = г 0 соответствует равновесному положению, в котором силы притяжения уравновешиваются силами отталкивания.









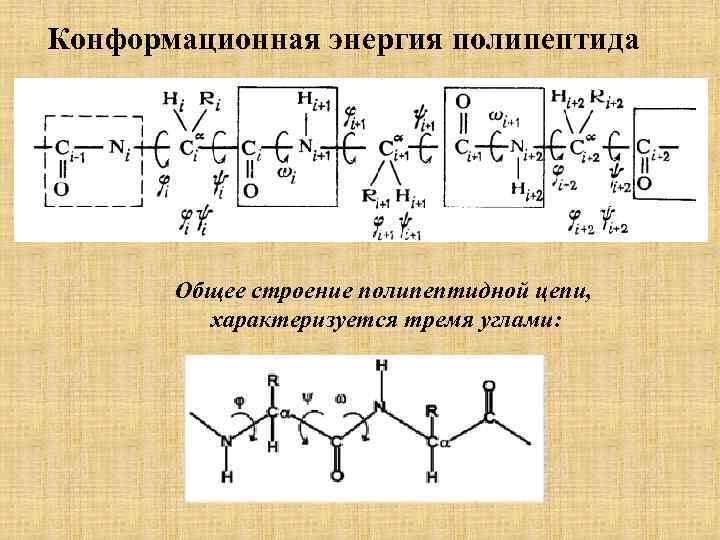
Конформационная энергия полипептида Общее строение полипептидной цепи, характеризуется тремя углами:
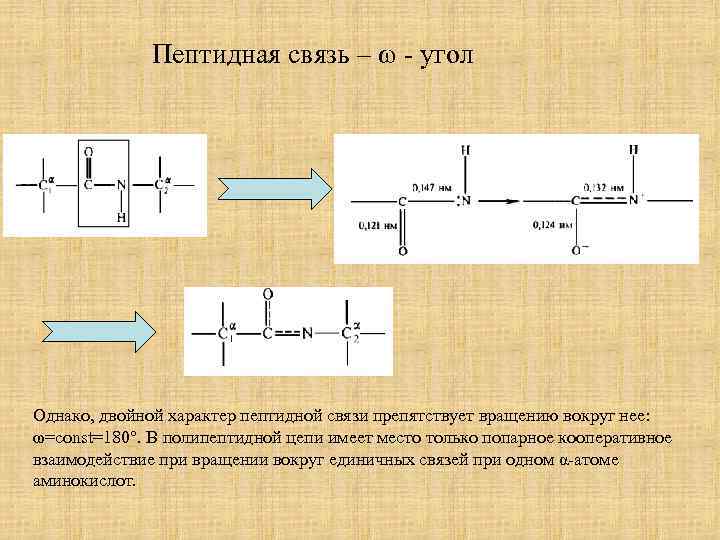
Пептидная связь – ω - угол Однако, двойной характер пептидной связи препятствует вращению вокруг нее: ω=const=180°. В полипептидной цепи имеет место только попарное кооперативное взаимодействие при вращении вокруг единичных связей при одном α-атоме аминокислот.
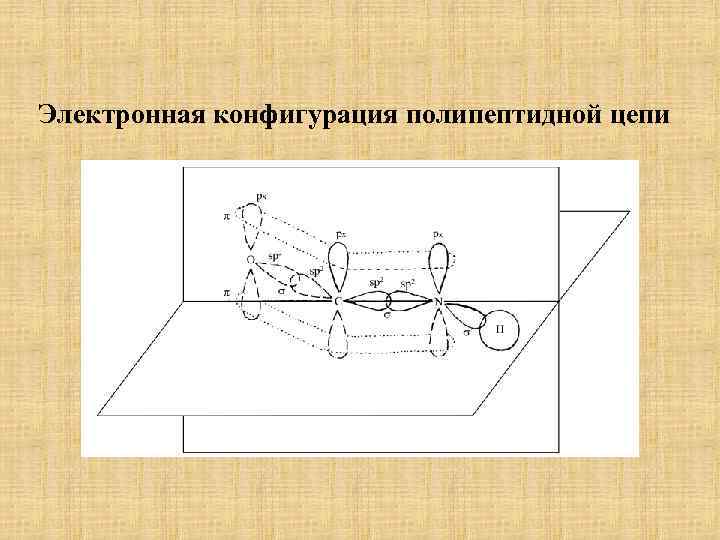
Электронная конфигурация полипептидной цепи
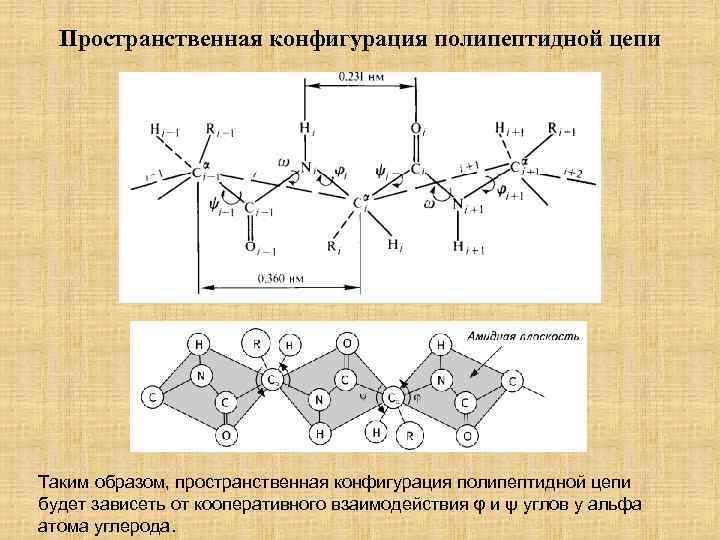
Пространственная конфигурация полипептидной цепи Таким образом, пространственная конфигурация полипептидной цепи будет зависеть от кооперативного взаимодействия φ и ψ углов у альфа атома углерода.

Стерическая карта Рамачандрана для поли-L-аланина. Сплошные линии обозначают границы полностью разрешенных областей; пунктирные - частично разрешенных. На карте указаны области значений углов ψ и φ для параллельной (βп„) и антипараллельной (βа) β-форм, спирали белка коллагена (К), правой (αR) и левой (αL) α спиралей. Не все значения углов ψ и φ допустимы вследствие возможного стерического несоответствия двух соседних аминокислотных остатков. Индийский ученый Г. Рамачандран рассчитал допустимые значения углов ψ и φ (углы отсчитываются от плоской транс-конформации полипептидной цени) и построил стерические карты, на которых но оси абсцисс откладываются значения углов φ от 0 до 360°, а по оси ординат - значения углов ψ. На карте отмечаются полностью разрешенные (при обычных межатомных расстояниях) и частично разрешенные (при минимальных межатомных расстояниях) области значений этих углов.
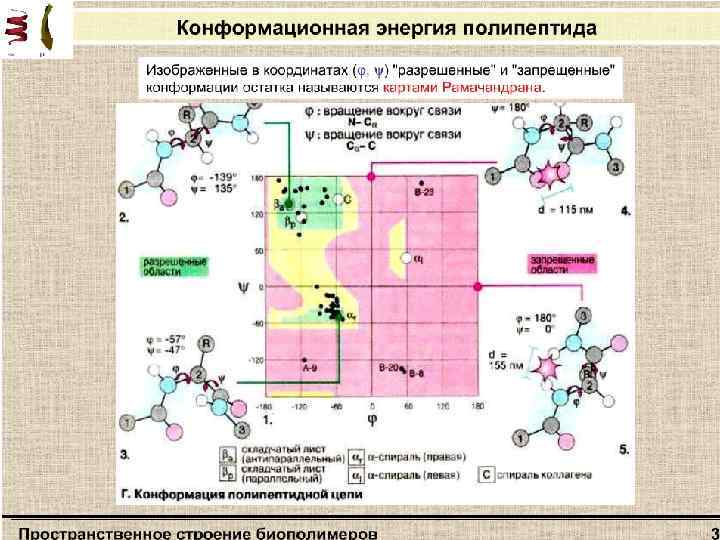



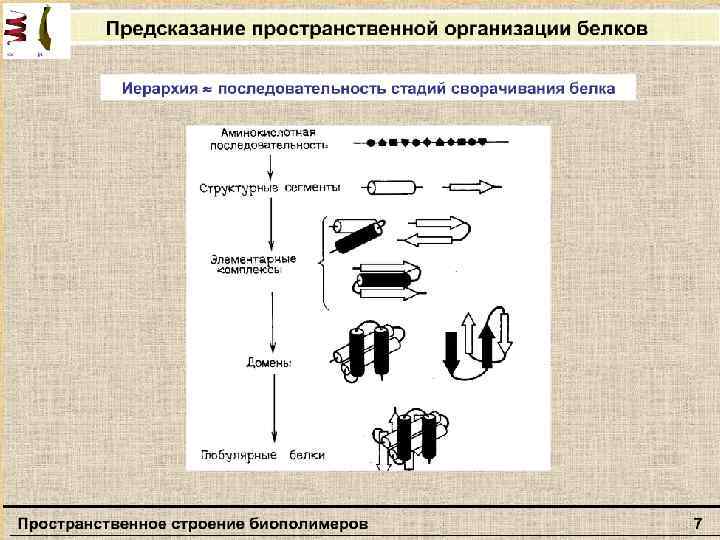
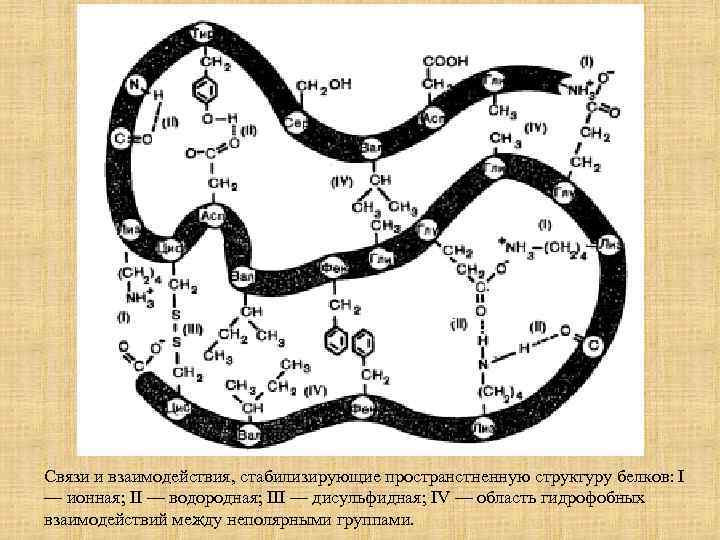
Связи и взаимодействия, стабилизирующие пространстненную структуру белков: I — ионная; II — водородная; III — дисульфидная; IV — область гидрофобных взаимодействий между неполярными группами.
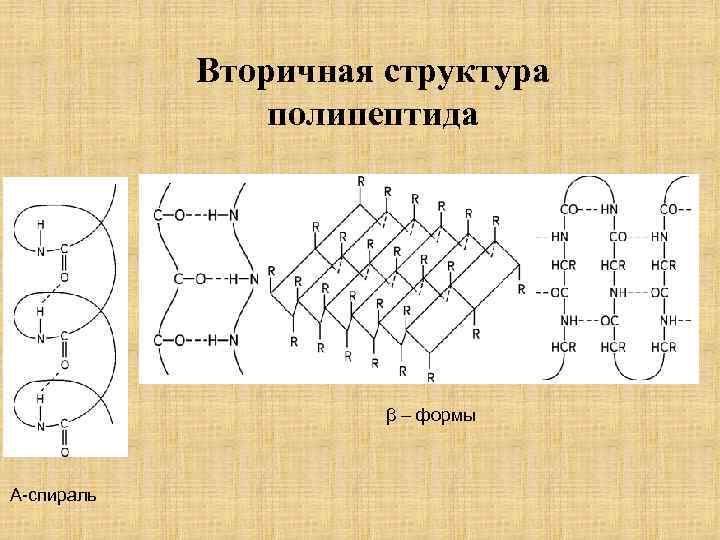
Вторичная структура полипептида β – формы Α-спираль




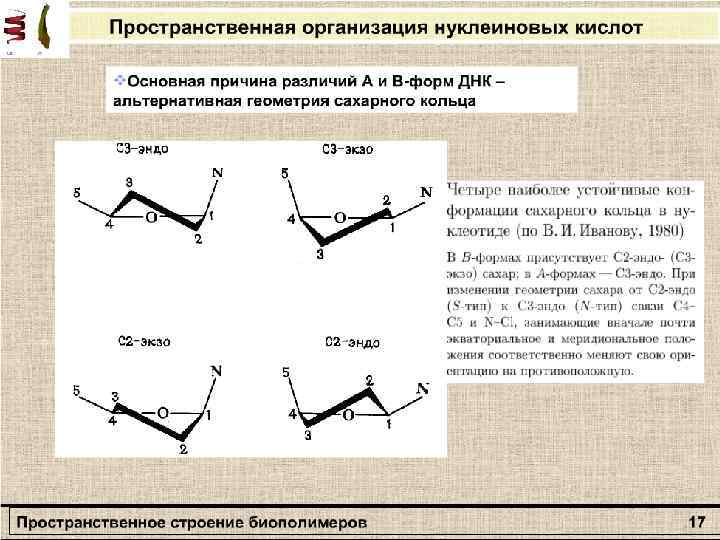
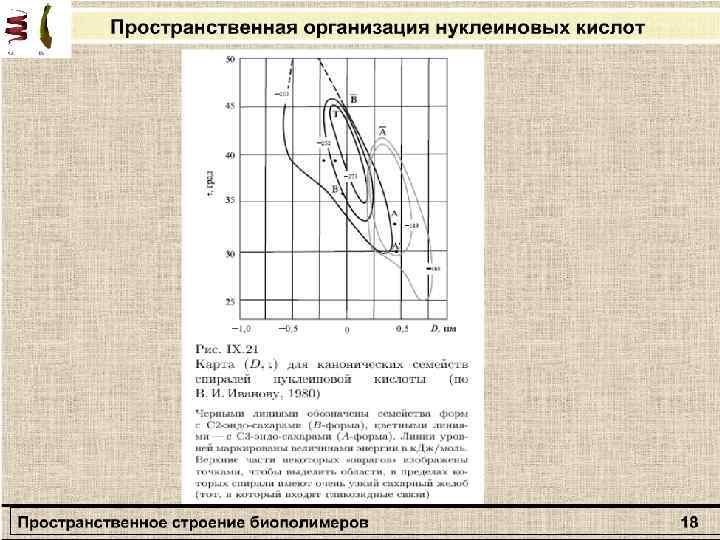


Молекулярная биофизика Динамика макромолекул

Пространственная структура миоглобина (кашалота) в проекции ху Миоглобин (переносчик кислорода в мышцах) содержит один гем и одну полипептидную цепь, включающую 153 остатка, которые распределены в основном по 8 а-спиральным участкам (А — Н). Гем, в центре которого расположен атом Fe, находится между спиралями Е и F.

Расщепление d-орбиталей в октаэдрическом комплексе (I): и распределение d-электронов по орбиталям высокоспинового (расщепление Δ мало) и низко спинового (расщепление Δ велико) состояний иона Fe 2+ (II)
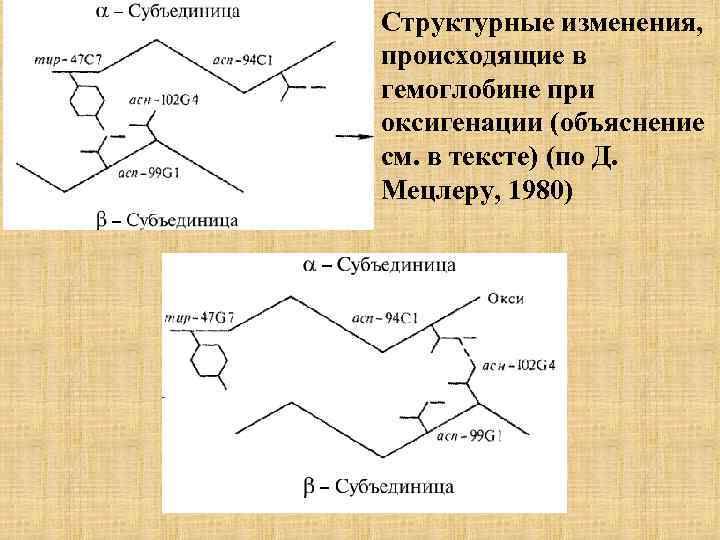
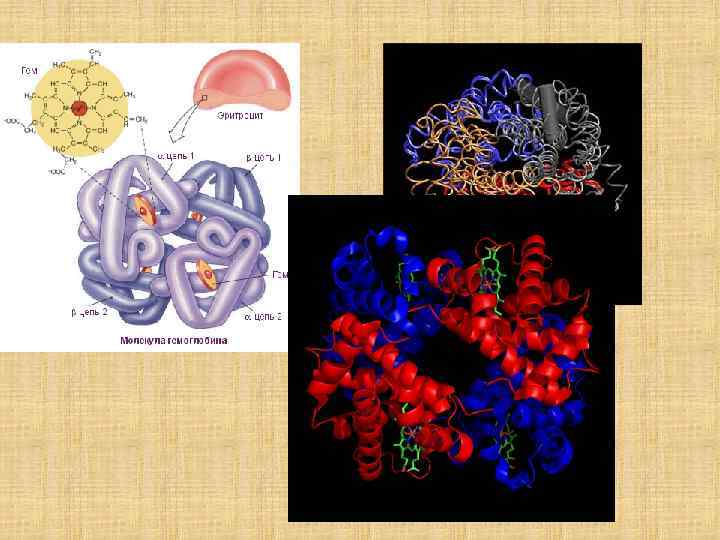
Структурные изменения, происходящие в гемоглобине при оксигенации (объяснение см. в тексте) (по Д. Мецлеру, 1980)

Методы изучения подвижности белков Люминесцентные методы ЭПР ЯМР ЯГР спектроскопия Метод изотопного обмена
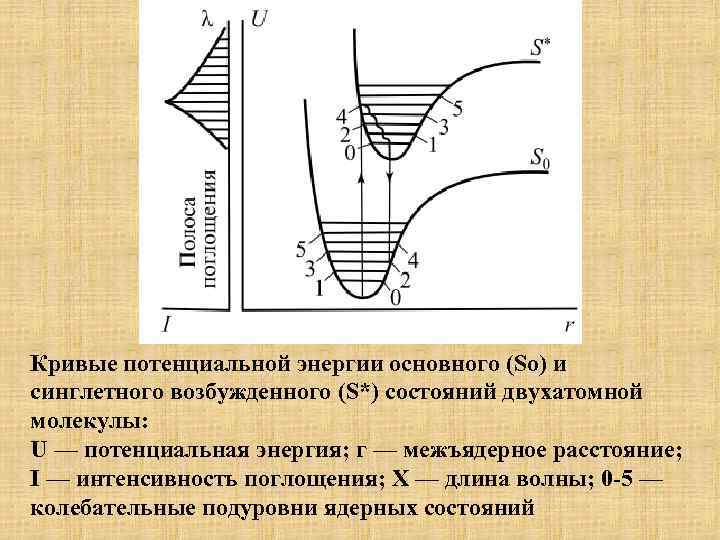
Кривые потенциальной энергии основного (So) и синглетного возбужденного (S*) состояний двухатомной молекулы: U — потенциальная энергия; г — межъядерное расстояние; I — интенсивность поглощения; X — длина волны; 0 -5 — колебательные подуровни ядерных состояний

Электронные уровни органической молекулы и переходы между ними (схема Яблонского): р — вероятность переходов в единицу времени на основной уровень с испусканием флуорисценции, qi—то же, без излучения; г — вероятность конверсии и триплетное состояние. Молекула обладает системой триплетных T 1, Т 2, . . . и синглетных возбужденных уровней S 1, S 2, . . . , Sn. При переходе на один из высших возбужденных синглетных уровней избыток энергии быстро (10 -12 с) диссипирует; молекула попадает на низший возбужденный синглетный уровень S 1, с которого и происходит переход (S 1 → S 0) или внутримолекулярная конверсия (S 1 → Т 1). Суммарная вероятность (P) дезактивации определяется суммой величину, qi, r: Р = р + qi + r

Люминесцентные методы • Измерение внутримолекулярной подвижности белка по зависимости положения максимума люминесценции метки, введенной в белок, либо собственной люминисценции триптофана белка от температуры • Характеристика подвижности окружения метки • t=10 -2 -10 -6 c • =10 -1 -10 -2 c • *=10 -8 -10 -9 c
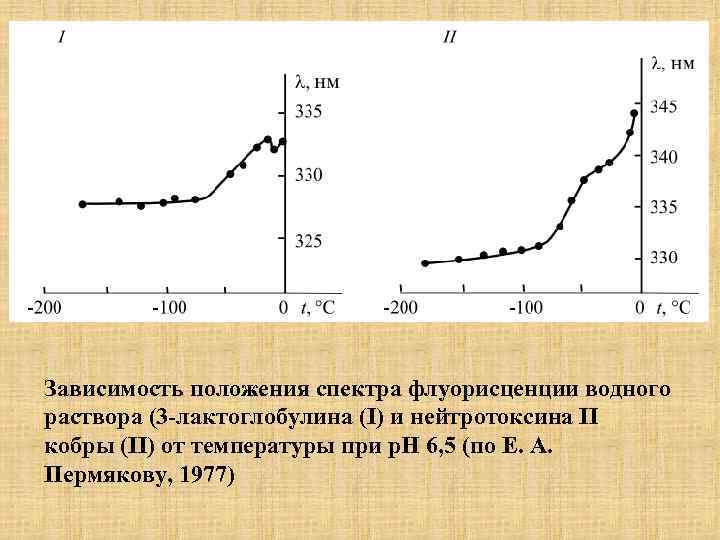
Зависимость положения спектра флуорисценции водного раствора (3 -лактоглобулина (I) и нейтротоксина II кобры (II) от температуры при р. Н 6, 5 (по Е. А. Пермякову, 1977)
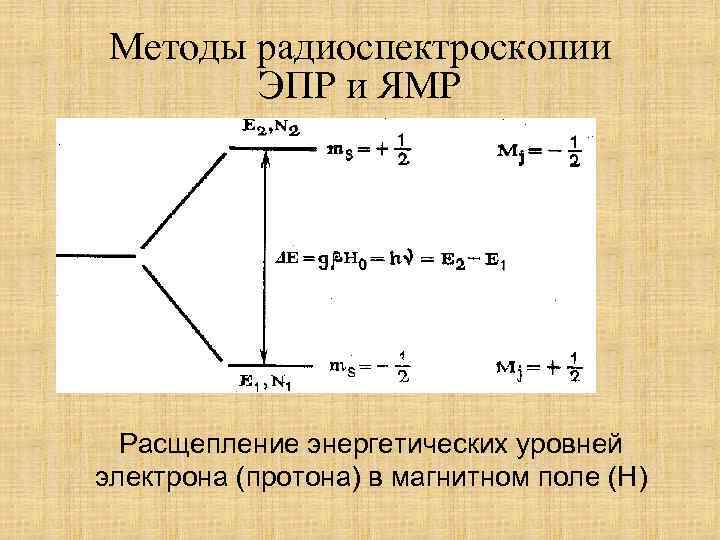
Методы радиоспектроскопии ЭПР и ЯМР Расщепление энергетических уровней электрона (протона) в магнитном поле (Н)
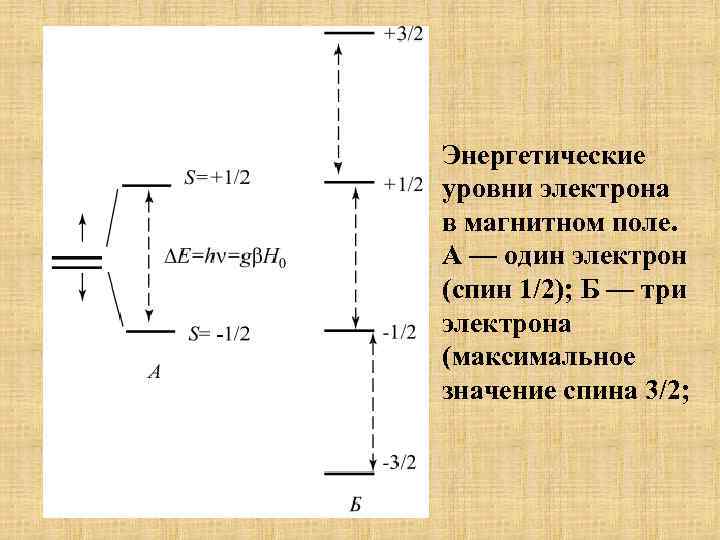
Энергетические уровни электрона в магнитном поле. А — один электрон (спин 1/2); Б — три электрона (максимальное значение спина 3/2;
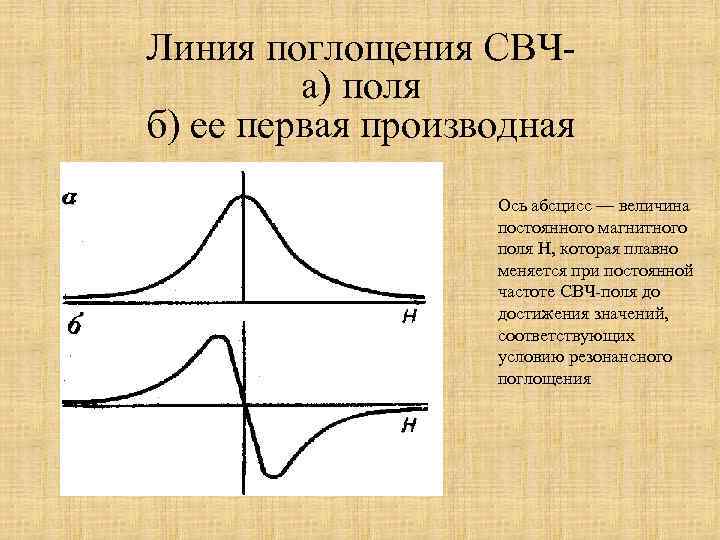
Линия поглощения СВЧа) поля б) ее первая производная Ось абсцисс — величина постоянного магнитного поля Н, которая плавно меняется при постоянной частоте СВЧ-поля до достижения значений, соответствующих условию резонансного поглощения

Линия резонанса ЭПР • Ширина: • Т 1 – время передачи энергии окружающей среде • Т 2 – время спин-спинового взаимодействия Для свободных радикалов: Т 1 >> Т 2
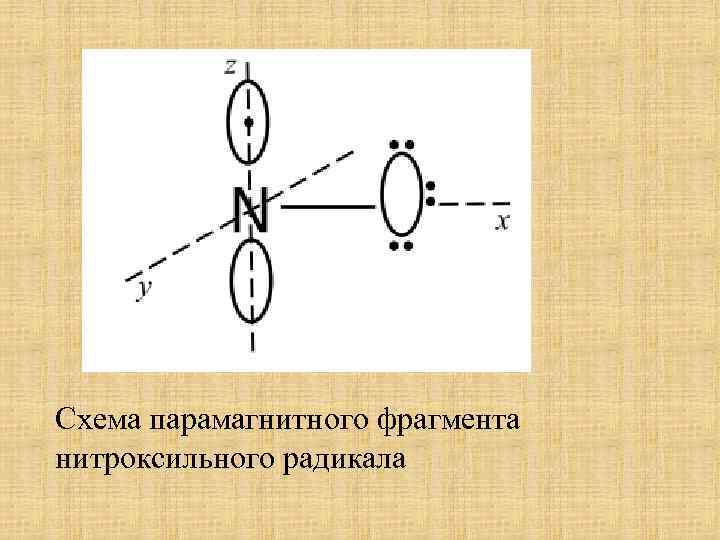
Схема парамагнитного фрагмента нитроксильного радикала
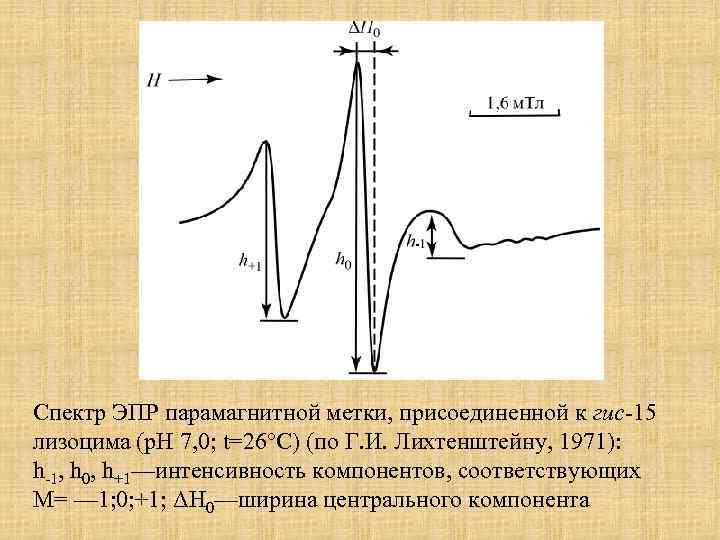
Спектр ЭПР парамагнитной метки, присоединенной к гис-15 лизоцима (р. Н 7, 0; t=26°C) (по Г. И. Лихтенштейну, 1971): h-1, h 0, h+1—интенсивность компонентов, соответствующих M= — 1; 0; +1; ΔH 0—ширина центрального компонента

ЯМР-спектроскопия • Измерение времени релаксации Т 1 и Т 2 по ширине линии резонанса. • Определение времени вращения метки, на которой наблюдается резонанс • Оценка подвижности белковых структур в состав которых входят «резонирующие» протоны • Изучение некоторых видов внутримолекулярного движения в белках • Информация о химической структуре молекулы
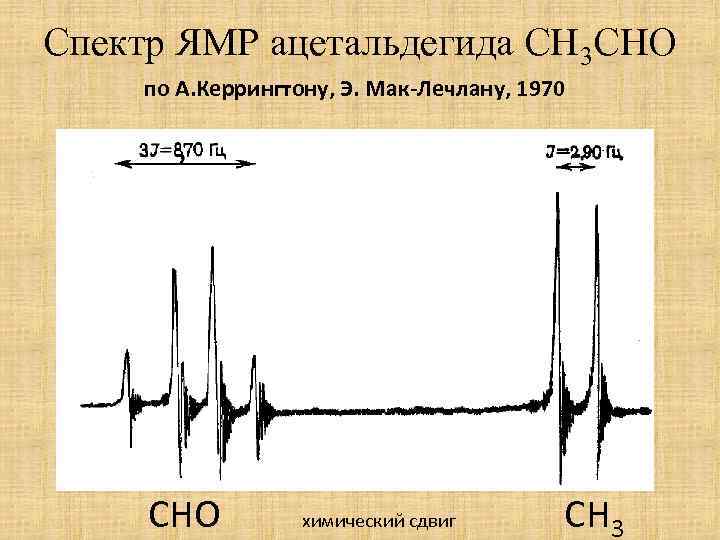
Спектр ЯМР ацетальдегида СН 3 СНО по А. Керрингтону, Э. Мак-Лечлану, 1970 СНО химический сдвиг СН 3

ЯГР спектроскопия • Дает информацию не только о временных, а также амплитудных характеристиках движений в белке (средние величины смещений атомов в структуре белка за t=10 -7 -10 -9 c) Основан на резонансном поглощении квантов тяжелым ядром атома Эффект Мёссбауэра
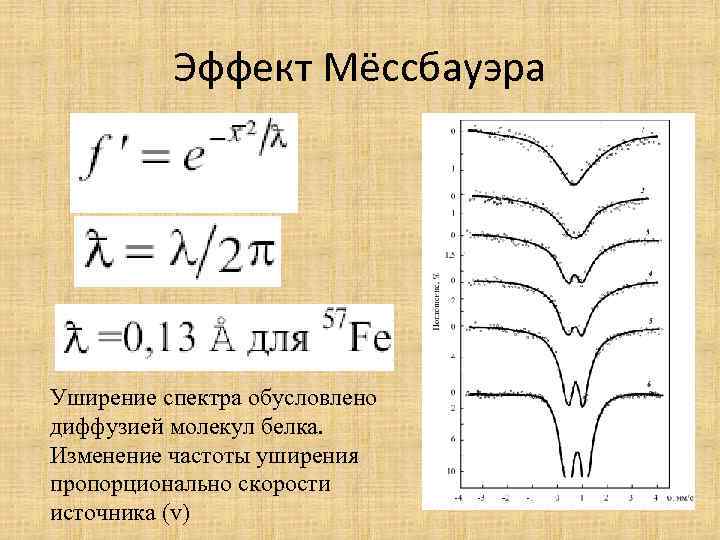
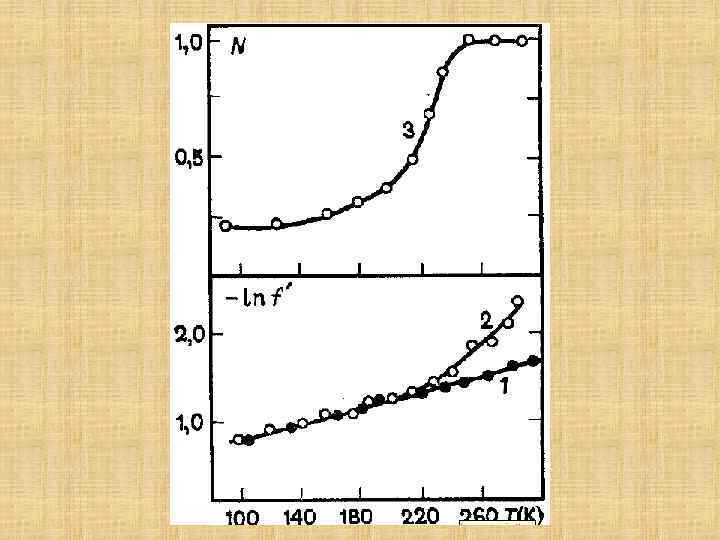
Эффект Мёссбауэра Уширение спектра обусловлено диффузией молекул белка. Изменение частоты уширения пропорционально скорости источника (v)


Picture of G-Protein Receptor Family 7 TM Transmembrane Domains
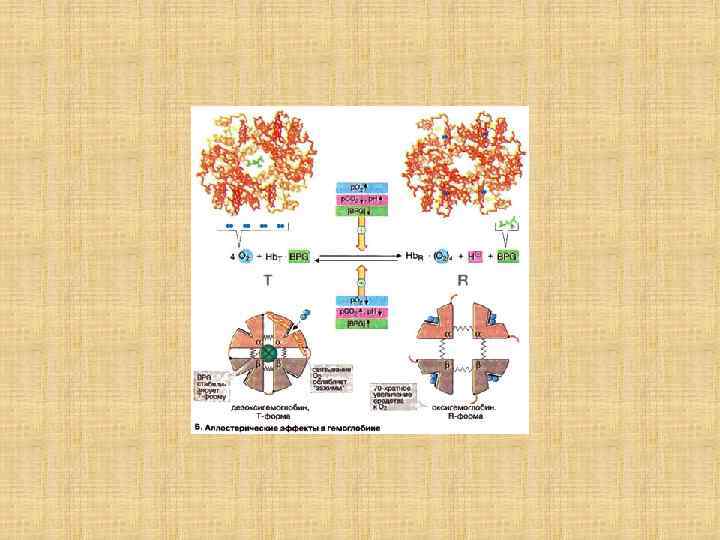

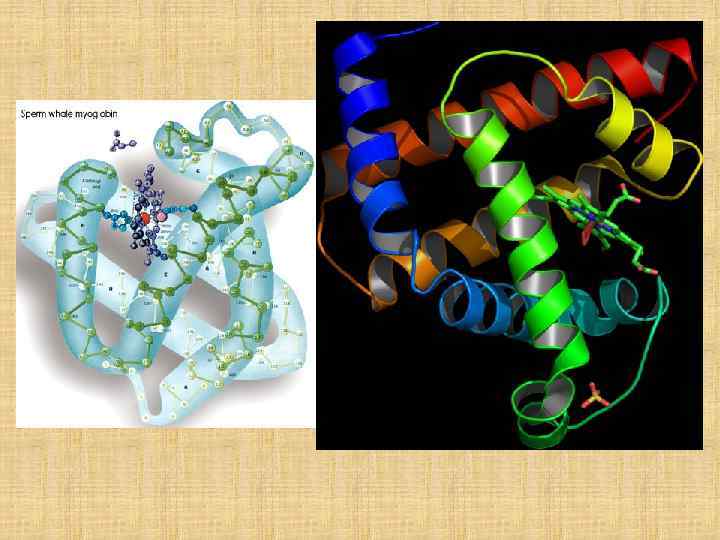
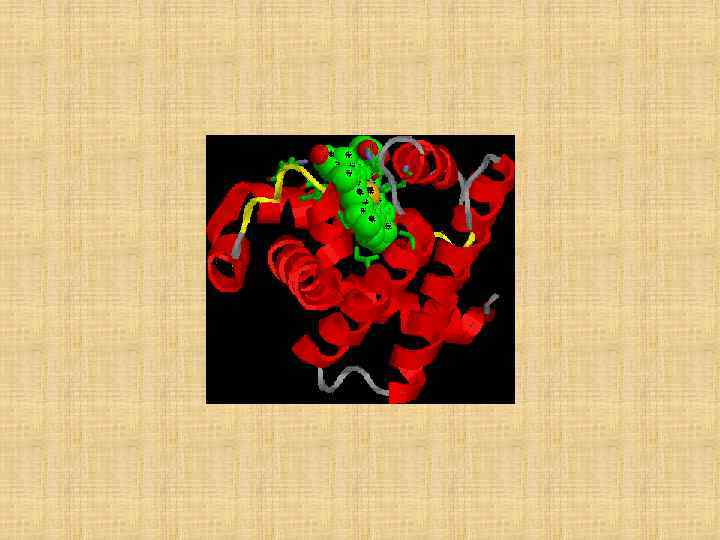
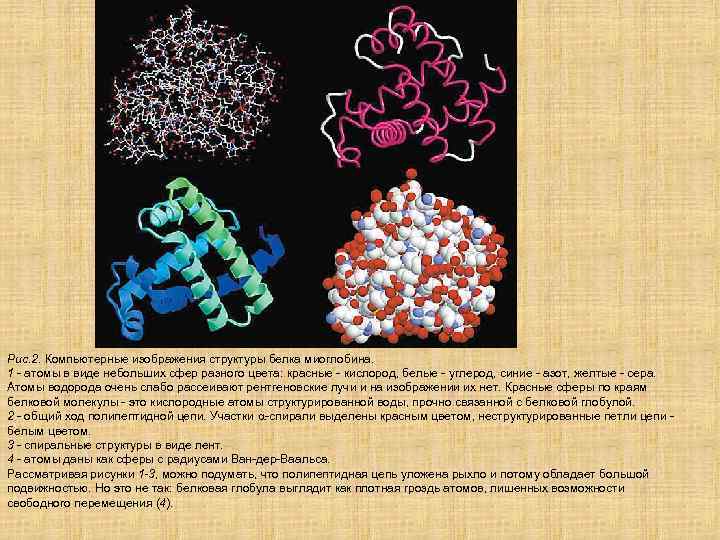
Рис. 2. Компьютерные изображения структуры белка миоглобина. 1 - атомы в виде небольших сфер разного цвета: красные - кислород, белые - углерод, синие - азот, желтые - сера. Атомы водорода очень слабо рассеивают рентгеновские лучи и на изображении их нет. Красные сферы по краям белковой молекулы - это кислородные атомы структурированной воды, прочно связанной с белковой глобулой. 2 - общий ход полипептидной цепи. Участки a-спирали выделены красным цветом, неструктурированные петли цепи белым цветом. 3 - спиральные структуры в виде лент. 4 - атомы даны как сферы с радиусами Ван-дер-Ваальса. Рассматривая рисунки 1 -3, можно подумать, что полипептидная цепь уложена рыхло и потому обладает большой подвижностью. Но это не так: белковая глобула выглядит как плотная гроздь атомов, лишенных возможности свободного перемещения (4).
4-5Молекулярная биофизика.ppt