Razdel3_Prez_4.ppt
- Количество слайдов: 62
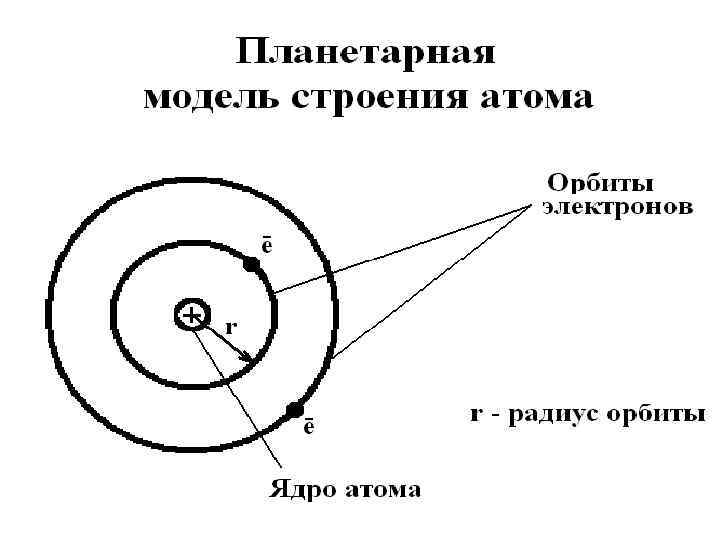
 Раздел 3. Строение атомов. Тема 3. 1. Основные сведения о строении атома § 1. Модели строения атомов Первая модель строения атома была предложена Э. Резерфордом в 1911 г. Она получила название «планетарной» . В планетарной модели электрон – частица. Предполагалось, что движение электрона вокруг ядра по орбите можно описать законами механики И. Ньютона. Чем больше радиус орбиты электрона, тем выше энергия электрона в атоме.
Раздел 3. Строение атомов. Тема 3. 1. Основные сведения о строении атома § 1. Модели строения атомов Первая модель строения атома была предложена Э. Резерфордом в 1911 г. Она получила название «планетарной» . В планетарной модели электрон – частица. Предполагалось, что движение электрона вокруг ядра по орбите можно описать законами механики И. Ньютона. Чем больше радиус орбиты электрона, тем выше энергия электрона в атоме.
 В 1924 г. Луи де Бройль показал, что электроны и другие частицы проявляют дуализм и обладают свойствами как волны, так и частицы. Математически эта гипотеза выражается в следующей форме: где h – постоянная Планка; m – масса тела; v – скорость тела. Произведение mv представляет импульс (количество движения) тела.
В 1924 г. Луи де Бройль показал, что электроны и другие частицы проявляют дуализм и обладают свойствами как волны, так и частицы. Математически эта гипотеза выражается в следующей форме: где h – постоянная Планка; m – масса тела; v – скорость тела. Произведение mv представляет импульс (количество движения) тела.
 Волновые свойства электронов экспериментально подтверждены их дифракцией (1927 г. ), которая имеет чисто волновую природу. Создание электронного микроскопа (1933 г. ) явилось шагом к сознательному практическому использованию волновой природы электрона. Далее были предложены математические уравнения, позволяющие описать энергию и характер движения электронов в атоме. Получила развитие наука КВАНТОВАЯ МЕХАНИКА.
Волновые свойства электронов экспериментально подтверждены их дифракцией (1927 г. ), которая имеет чисто волновую природу. Создание электронного микроскопа (1933 г. ) явилось шагом к сознательному практическому использованию волновой природы электрона. Далее были предложены математические уравнения, позволяющие описать энергию и характер движения электронов в атоме. Получила развитие наука КВАНТОВАЯ МЕХАНИКА.
 Квантовая механика, или волновая механика – это область теоретической физики, которая математически описывает волновые свойства субмикроскопических частиц. Квант – это минимальное количество, на которое может изменяться дискретная по своей природе физическая величина. Например, квант энергии электромагнитного излучения: где h – постоянная Планка; ν – частота волны электромагнитного излучения.
Квантовая механика, или волновая механика – это область теоретической физики, которая математически описывает волновые свойства субмикроскопических частиц. Квант – это минимальное количество, на которое может изменяться дискретная по своей природе физическая величина. Например, квант энергии электромагнитного излучения: где h – постоянная Планка; ν – частота волны электромагнитного излучения.
 Фактически, с 1924 г. развивается квантовомеханическая модель строения атома, основные постулаты которой следующие: 1) Электрон – частица - волна. 2) Невозможно знать с высокой точностью одновременно координаты и импульс электрона (Принцип неопределённости Гейзенберга, 1927 г. ). Это означает, что движение электрона в атоме имеет «вероятностный характер» .
Фактически, с 1924 г. развивается квантовомеханическая модель строения атома, основные постулаты которой следующие: 1) Электрон – частица - волна. 2) Невозможно знать с высокой точностью одновременно координаты и импульс электрона (Принцип неопределённости Гейзенберга, 1927 г. ). Это означает, что движение электрона в атоме имеет «вероятностный характер» .
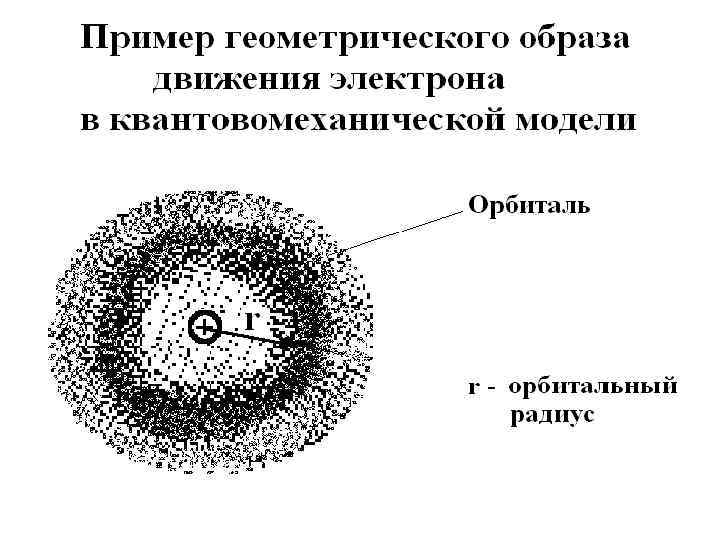
 Геометрическим образом характера движения электрона в атоме является не орбита, а ОРБИТАЛЬ. Орбиталь – совокупность наиболее вероятных состояний электрона в атоме в соответствии с его свойствами. Форма и ориентация орбитали в пространстве зависит от свойств (состояния) электрона.
Геометрическим образом характера движения электрона в атоме является не орбита, а ОРБИТАЛЬ. Орбиталь – совокупность наиболее вероятных состояний электрона в атоме в соответствии с его свойствами. Форма и ориентация орбитали в пространстве зависит от свойств (состояния) электрона.
 ВАЖНЫЕ ДЛЯ ХИМИИ следствия из математического аппарата квантовой механики: 1) E (энергия электрона квантована): E 1 = n 1 hν; E 2 = n 2 hν; ∆E = (n 2 - n 1)hν; n = 1, 2, 3, …. 2) Состояние электрона в атоме можно охарактеризовать пятью квантовыми числами.
ВАЖНЫЕ ДЛЯ ХИМИИ следствия из математического аппарата квантовой механики: 1) E (энергия электрона квантована): E 1 = n 1 hν; E 2 = n 2 hν; ∆E = (n 2 - n 1)hν; n = 1, 2, 3, …. 2) Состояние электрона в атоме можно охарактеризовать пятью квантовыми числами.
 § 2. Квантовые числа электронов 1. Главное квантовое число. Обозначение: n. Может принимать значения из натурального ряда чисел: n = 1, 2, 3 …. ∞. Определяет главную часть полной энергии электрона в атоме: E = nhν. Чем больше n, тем выше энергия электрона. При n = ∞ энергия электрона настолько высока, что он преодолевает силы притяжения ядра и покидает пределы атома.
§ 2. Квантовые числа электронов 1. Главное квантовое число. Обозначение: n. Может принимать значения из натурального ряда чисел: n = 1, 2, 3 …. ∞. Определяет главную часть полной энергии электрона в атоме: E = nhν. Чем больше n, тем выше энергия электрона. При n = ∞ энергия электрона настолько высока, что он преодолевает силы притяжения ядра и покидает пределы атома.
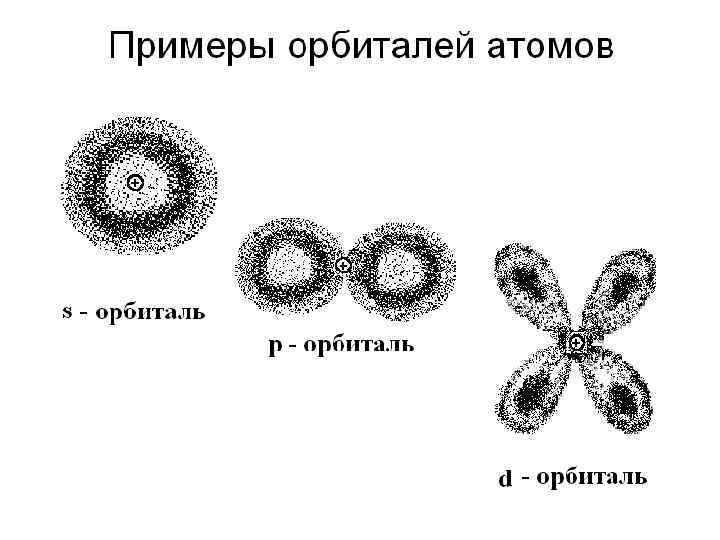
 2. Орбитальное (побочное) квантовое число. Обозначение: Может принимать значения: = 0, 1, 2, 3 …. (n - 1). Состояния электрона буквамис различными принято обозначать латинского алфавита: : 0 1 2 3 4 Значения Обозначение состояния: s p d f g Каждое из этих состояний характеризуется формой орбитали.
2. Орбитальное (побочное) квантовое число. Обозначение: Может принимать значения: = 0, 1, 2, 3 …. (n - 1). Состояния электрона буквамис различными принято обозначать латинского алфавита: : 0 1 2 3 4 Значения Обозначение состояния: s p d f g Каждое из этих состояний характеризуется формой орбитали.
 3. Магнитное квантовое число. Обозначение: ml. Может принимать значения: ml = от – l до + l, включая 0. Всего (2 l + 1) значений. Определяет магнитные свойства электрона при движении его по орбитали. А более конкретно: ориентацию орбитали в пространстве в среде с источником магнитного поля. ПРИМЕР: l = 2 (d-орбиталь); ml = -2; -1; 0; +1; +2 (всего пять значений). Это означает, что dорбиталь может быть ориентирована в пространстве пятью различными способами.
3. Магнитное квантовое число. Обозначение: ml. Может принимать значения: ml = от – l до + l, включая 0. Всего (2 l + 1) значений. Определяет магнитные свойства электрона при движении его по орбитали. А более конкретно: ориентацию орбитали в пространстве в среде с источником магнитного поля. ПРИМЕР: l = 2 (d-орбиталь); ml = -2; -1; 0; +1; +2 (всего пять значений). Это означает, что dорбиталь может быть ориентирована в пространстве пятью различными способами.
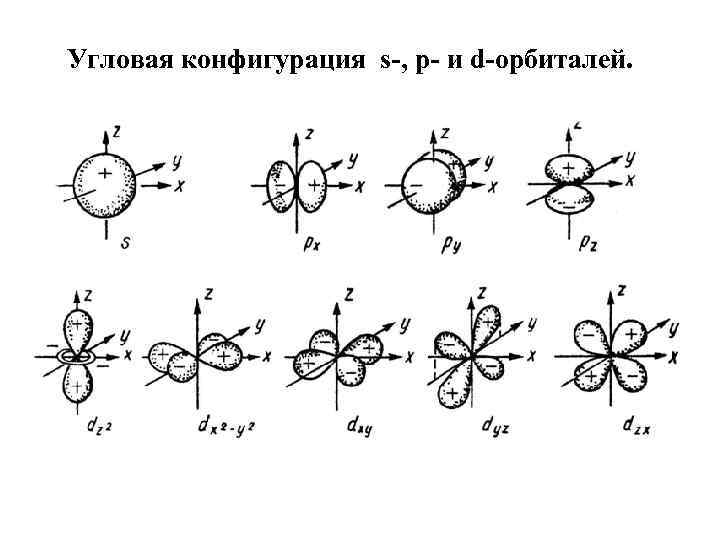 Угловая конфигурация s-, p- и d-орбиталей.
Угловая конфигурация s-, p- и d-орбиталей.
 4. Спин электрона. Обозначение: s. Спин (spin – «волчок» ) элементарной частицы – это момент импульса частицы при её вращательном движении вокруг «собственной оси» . Для электрона:
4. Спин электрона. Обозначение: s. Спин (spin – «волчок» ) элементарной частицы – это момент импульса частицы при её вращательном движении вокруг «собственной оси» . Для электрона:
 5. Проекция спина. Обозначение: ms. Определяет взаимодействие вращающейся вокруг собственной оси заряженной частицы в среде с источником магнитного поля с полем. Может принимать два значения: ms = +1/2 (при вращательном движении частицы по часовой стрелке). ms = -1/2 (при вращательном движении частицы против часовой стрелки).
5. Проекция спина. Обозначение: ms. Определяет взаимодействие вращающейся вокруг собственной оси заряженной частицы в среде с источником магнитного поля с полем. Может принимать два значения: ms = +1/2 (при вращательном движении частицы по часовой стрелке). ms = -1/2 (при вращательном движении частицы против часовой стрелки).
 Отметим, что из пяти квантовых чисел электронов изменяются четыре: n, , ml, ms. Эти квантовые числа являются величинами безразмерными.
Отметим, что из пяти квантовых чисел электронов изменяются четыре: n, , ml, ms. Эти квантовые числа являются величинами безразмерными.
 Тема 3. 2. Принципы заполнения электронных оболочек атомов § 1. Принципы построения атомных орбиталей, подуровней и уровней Электроны могут переходить от одного атома к другому или от одной группы атомов к другой. Эти переходы сопровождаются образованием новых простых и сложных веществ. Важно знать и понимать свойства электронов в атоме.
Тема 3. 2. Принципы заполнения электронных оболочек атомов § 1. Принципы построения атомных орбиталей, подуровней и уровней Электроны могут переходить от одного атома к другому или от одной группы атомов к другой. Эти переходы сопровождаются образованием новых простых и сложных веществ. Важно знать и понимать свойства электронов в атоме.
 ПРИНЦИП ПАУЛИ В атоме химического элемента не может быть двух электронов с одинаковым набором всех четырёх изменяющихся квантовых чисел. Принцип Паули – это принцип запрета! Но электроны с одинаковыми n, l, ml могут быть. Таких электронов 2. Один с ms = +1/2, а второй с ms = -1/2. Электроны с одинаковыми n, l, ml составляют атомную орбиталь.
ПРИНЦИП ПАУЛИ В атоме химического элемента не может быть двух электронов с одинаковым набором всех четырёх изменяющихся квантовых чисел. Принцип Паули – это принцип запрета! Но электроны с одинаковыми n, l, ml могут быть. Таких электронов 2. Один с ms = +1/2, а второй с ms = -1/2. Электроны с одинаковыми n, l, ml составляют атомную орбиталь.
 На электронной схеме атома атомные орбитали обозначаются как квадрат: - свободная атомная орбиталь. Обозначение электронов: ↑ - электрон с проекцией спина ms = +1/2, ↓ - электрон с проекцией спина ms = -1/2. ↑ ↓ - полностью занятая орбиталь со спаренными электронами. ↑ -орбиталь с неспаренным электроном.
На электронной схеме атома атомные орбитали обозначаются как квадрат: - свободная атомная орбиталь. Обозначение электронов: ↑ - электрон с проекцией спина ms = +1/2, ↓ - электрон с проекцией спина ms = -1/2. ↑ ↓ - полностью занятая орбиталь со спаренными электронами. ↑ -орбиталь с неспаренным электроном.
 Максимальное число электронов на атомной орбитали равно 2.
Максимальное число электронов на атомной орбитали равно 2.
 Если электроны имеют одинаковые n и l, но отличаются ml, то они образуют атомный подуровень. Подуровни состоят из атомных орбиталей. Свойства подуровня и количество орбиталей на подуровне определяется значением l и числом возможных значений ml приданном l. Рассмотрим структуру некоторых подуровней:
Если электроны имеют одинаковые n и l, но отличаются ml, то они образуют атомный подуровень. Подуровни состоят из атомных орбиталей. Свойства подуровня и количество орбиталей на подуровне определяется значением l и числом возможных значений ml приданном l. Рассмотрим структуру некоторых подуровней:
 l = 0. Это s – подуровень. ml принимает значение 0. Только одно значение. Вывод: s-подуровень состоит только из одной орбитали. Изображение s-подуровня на электронной схеме атома: s
l = 0. Это s – подуровень. ml принимает значение 0. Только одно значение. Вывод: s-подуровень состоит только из одной орбитали. Изображение s-подуровня на электронной схеме атома: s
 l =1. Это p – подуровень. ml принимает значения -1, 0, +1. Только три значения. Вывод: p-подуровень состоит из трёх орбиталей. Изображение p-подуровня на электронной схеме атома: p px py pz
l =1. Это p – подуровень. ml принимает значения -1, 0, +1. Только три значения. Вывод: p-подуровень состоит из трёх орбиталей. Изображение p-подуровня на электронной схеме атома: p px py pz
 l = 2. Это d – подуровень. ml принимает значения -2, -1, 0, +1, +2. Всего пять значений. Вывод: d-подуровень состоит из пяти орбиталей. Изображение d-подуровня на электронной схеме атома: d
l = 2. Это d – подуровень. ml принимает значения -2, -1, 0, +1, +2. Всего пять значений. Вывод: d-подуровень состоит из пяти орбиталей. Изображение d-подуровня на электронной схеме атома: d
 Общее (максимальное) число электронов на подуровне можно рассчитать по формуле:
Общее (максимальное) число электронов на подуровне можно рассчитать по формуле:
 Если электроны имеют одинаковые n , но отличаются l, то они образуют атомный уровень (или атомную оболочку). Уровни состоят из атомных подуровней (а свойства подуровней мы уже знаем). Свойства уровня и количество подуровней на уровне определяется значением n и числом возможных значений l при данном n. Рассмотрим структуру некоторых уровней:
Если электроны имеют одинаковые n , но отличаются l, то они образуют атомный уровень (или атомную оболочку). Уровни состоят из атомных подуровней (а свойства подуровней мы уже знаем). Свойства уровня и количество подуровней на уровне определяется значением n и числом возможных значений l при данном n. Рассмотрим структуру некоторых уровней:
 n = 1. Это первый уровень. При n = 1 квантовое число l принимает только одно значение: l = 0, что соответствует s-подуровню. Вывод: Первый уровень состоит только из одного подуровня. Это s-подуровень. Изображение первого уровня в электронной схеме атома: 1 s
n = 1. Это первый уровень. При n = 1 квантовое число l принимает только одно значение: l = 0, что соответствует s-подуровню. Вывод: Первый уровень состоит только из одного подуровня. Это s-подуровень. Изображение первого уровня в электронной схеме атома: 1 s
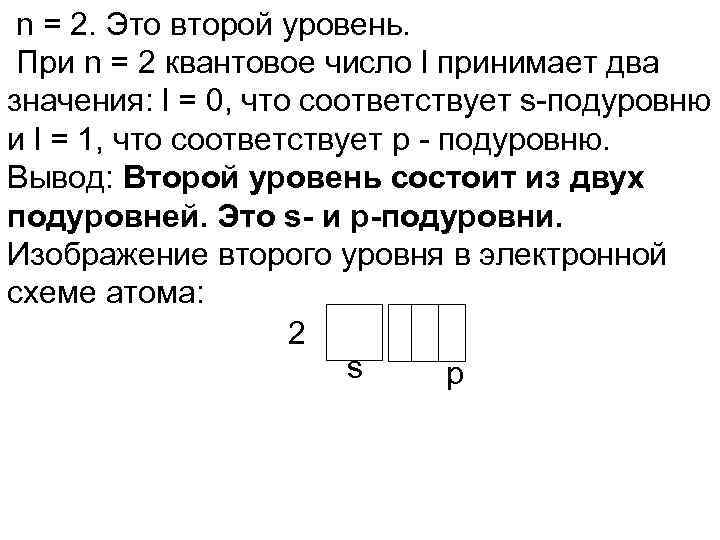 n = 2. Это второй уровень. При n = 2 квантовое число l принимает два значения: l = 0, что соответствует s-подуровню и l = 1, что соответствует p - подуровню. Вывод: Второй уровень состоит из двух подуровней. Это s- и p-подуровни. Изображение второго уровня в электронной схеме атома: 2 s p
n = 2. Это второй уровень. При n = 2 квантовое число l принимает два значения: l = 0, что соответствует s-подуровню и l = 1, что соответствует p - подуровню. Вывод: Второй уровень состоит из двух подуровней. Это s- и p-подуровни. Изображение второго уровня в электронной схеме атома: 2 s p
 Подсчитаем число электронов, которые могут располагаться на уровне с главным квантовым числом n:
Подсчитаем число электронов, которые могут располагаться на уровне с главным квантовым числом n:
 ПРИНЦИП НАИМЕНЬШЕЙ ЭНЕРГИИ В первую очередь электроны занимают в атоме состояния, которым отвечает как минимум энергии самого электрона, так и всего атома в целом. Таким состояниям согласно правилу Клечковского отвечает минимум суммы квантовых чисел n и l: Если для двух состояний эта сумма оказывается одинаковой, то более предпочтительным является состояние с меньшим n.
ПРИНЦИП НАИМЕНЬШЕЙ ЭНЕРГИИ В первую очередь электроны занимают в атоме состояния, которым отвечает как минимум энергии самого электрона, так и всего атома в целом. Таким состояниям согласно правилу Клечковского отвечает минимум суммы квантовых чисел n и l: Если для двух состояний эта сумма оказывается одинаковой, то более предпочтительным является состояние с меньшим n.
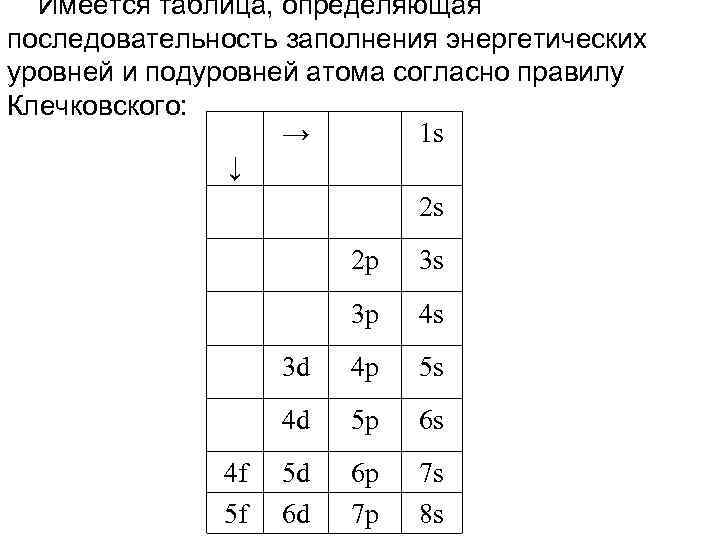 Имеется таблица, определяющая последовательность заполнения энергетических уровней и подуровней атома согласно правилу Клечковского: → 1 s ↓ 2 s 2 p 3 p 4 s 3 d 4 p 5 s 4 d 4 f 5 f 3 s 5 p 6 s 5 d 6 d 6 p 7 p 7 s 8 s
Имеется таблица, определяющая последовательность заполнения энергетических уровней и подуровней атома согласно правилу Клечковского: → 1 s ↓ 2 s 2 p 3 p 4 s 3 d 4 p 5 s 4 d 4 f 5 f 3 s 5 p 6 s 5 d 6 d 6 p 7 p 7 s 8 s
 § 2. Электронные конфигурации атомов химических элементов Электронной конфигурацией атома называется обозначение того, как электроны распределяются по энергетическим уровням, подуровням и орбиталям. Электронную конфигурацию атома составляют следующим образом: записывают главное квантовое число цифрой, затем букву латинского алфавита, соответствующую квантовому числу l, и далее указывают в виде надстрочного индекса справа у латинской буквы число электронов на подуровне. Например: 1 s 22 p 4. Никаких разделительных знаков при записи электронной конфигурации не ставят!
§ 2. Электронные конфигурации атомов химических элементов Электронной конфигурацией атома называется обозначение того, как электроны распределяются по энергетическим уровням, подуровням и орбиталям. Электронную конфигурацию атома составляют следующим образом: записывают главное квантовое число цифрой, затем букву латинского алфавита, соответствующую квантовому числу l, и далее указывают в виде надстрочного индекса справа у латинской буквы число электронов на подуровне. Например: 1 s 22 p 4. Никаких разделительных знаков при записи электронной конфигурации не ставят!
 Если хотят показать число электронов не только на подуровне, но и на орбиталях, то представляют орбитальную диаграмму или схему электронной конфигурации. При этом для изображения орбиталей и электронов используются символы, использованные ранее: □, ↑, ↓.
Если хотят показать число электронов не только на подуровне, но и на орбиталях, то представляют орбитальную диаграмму или схему электронной конфигурации. При этом для изображения орбиталей и электронов используются символы, использованные ранее: □, ↑, ↓.
 Составим электронные конфигурации атомов химических элементов и их схемы в порядке возрастания атомных номеров элементов на единицу. Такой ряд получил название «Менделеевский ряд элементов» .
Составим электронные конфигурации атомов химических элементов и их схемы в порядке возрастания атомных номеров элементов на единицу. Такой ряд получил название «Менделеевский ряд элементов» .
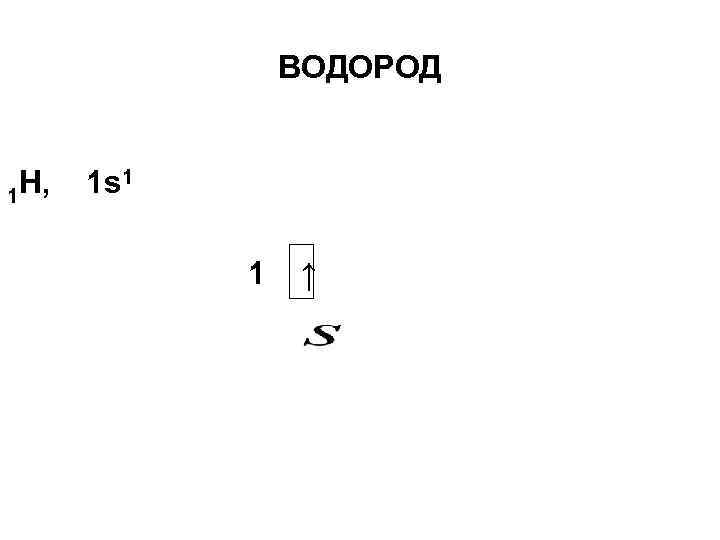 ВОДОРОД 1 H, 1 s 1 1 ↑
ВОДОРОД 1 H, 1 s 1 1 ↑
 ГЕЛИЙ He, 1 s 2. Возможности первого уровня 2 исчерпаны. Полностью заполненный первый уровень энергии – «ДУБЛЕТ» . 1 ↑ ↓
ГЕЛИЙ He, 1 s 2. Возможности первого уровня 2 исчерпаны. Полностью заполненный первый уровень энергии – «ДУБЛЕТ» . 1 ↑ ↓
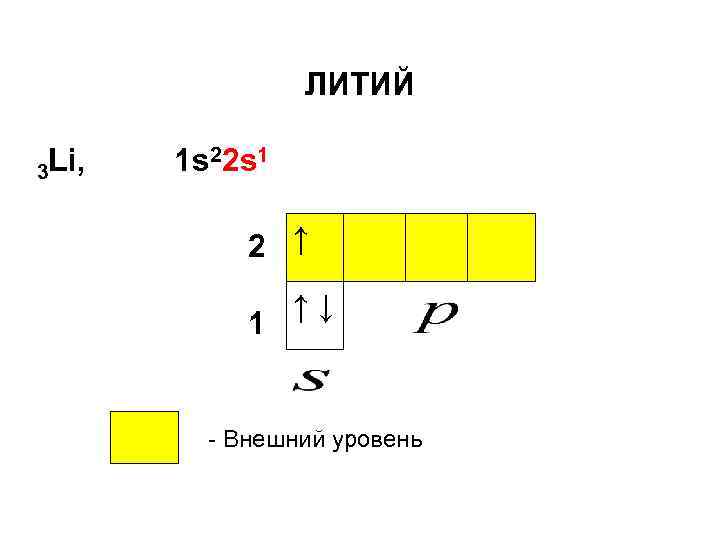 ЛИТИЙ 3 Li, 1 s 22 s 1 2 ↑ 1 ↑↓ - Внешний уровень
ЛИТИЙ 3 Li, 1 s 22 s 1 2 ↑ 1 ↑↓ - Внешний уровень
 Заметим, что по строению внешнего электронного уровня элемент Li является аналогом элемента H.
Заметим, что по строению внешнего электронного уровня элемент Li является аналогом элемента H.
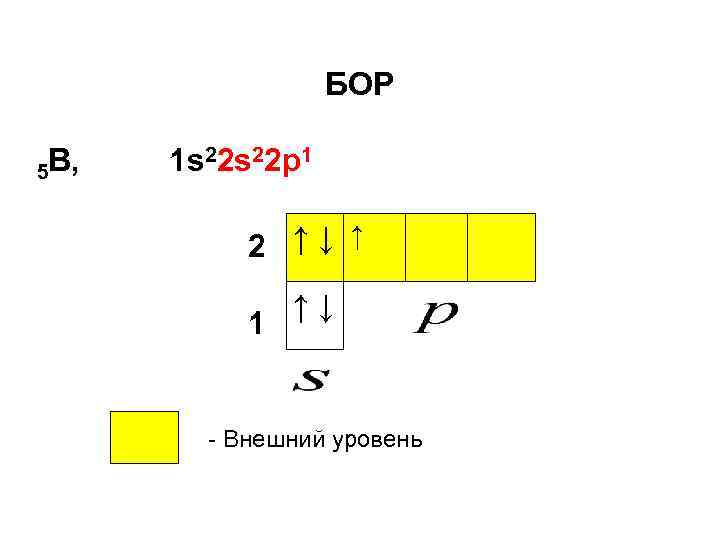 БОР 5 B, 1 s 22 p 1 2 ↑↓ ↑ 1 ↑↓ - Внешний уровень
БОР 5 B, 1 s 22 p 1 2 ↑↓ ↑ 1 ↑↓ - Внешний уровень
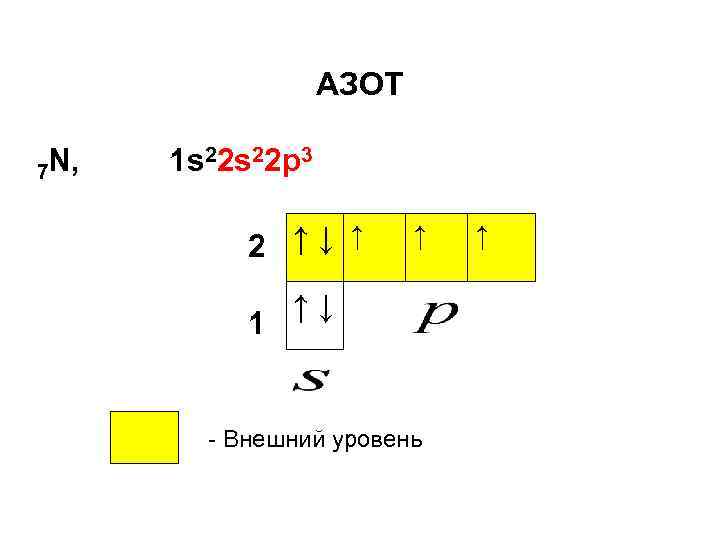 AЗОТ 7 N, 1 s 22 p 3 2 ↑↓ ↑ 1 ↑ ↑↓ - Внешний уровень ↑
AЗОТ 7 N, 1 s 22 p 3 2 ↑↓ ↑ 1 ↑ ↑↓ - Внешний уровень ↑
 То, что в атоме элемента азота (и других элементов) электроны располагаются именно таким образом не является очевидным, а следует из правила Гунда: В пределах подуровня электроны располагаются таким образом, чтобы суммарный спин конфигурации был максимальным. где S∑ -суммарный спин конфигурации; ms – проекции спинов электронов, образующих конфигурацию.
То, что в атоме элемента азота (и других элементов) электроны располагаются именно таким образом не является очевидным, а следует из правила Гунда: В пределах подуровня электроны располагаются таким образом, чтобы суммарный спин конфигурации был максимальным. где S∑ -суммарный спин конфигурации; ms – проекции спинов электронов, образующих конфигурацию.
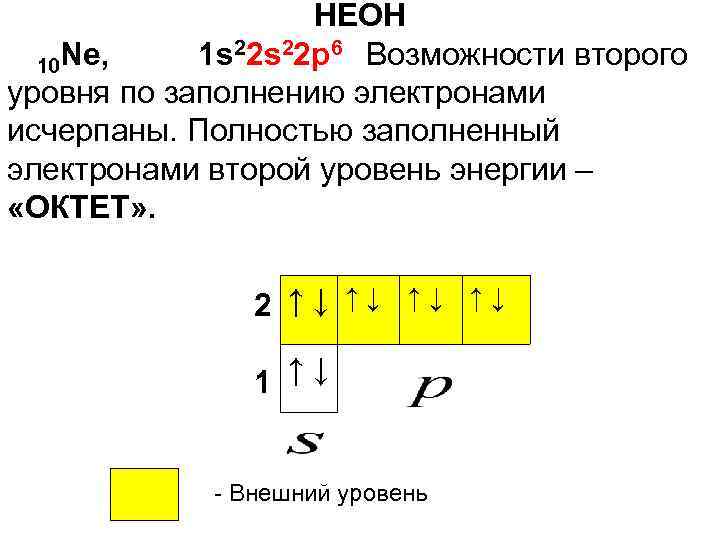 НЕОН Ne, 1 s 22 p 6 Возможности второго 10 уровня по заполнению электронами исчерпаны. Полностью заполненный электронами второй уровень энергии – «ОКТЕТ» . 2 ↑↓ ↑↓ ↑↓ 1 - Внешний уровень
НЕОН Ne, 1 s 22 p 6 Возможности второго 10 уровня по заполнению электронами исчерпаны. Полностью заполненный электронами второй уровень энергии – «ОКТЕТ» . 2 ↑↓ ↑↓ ↑↓ 1 - Внешний уровень
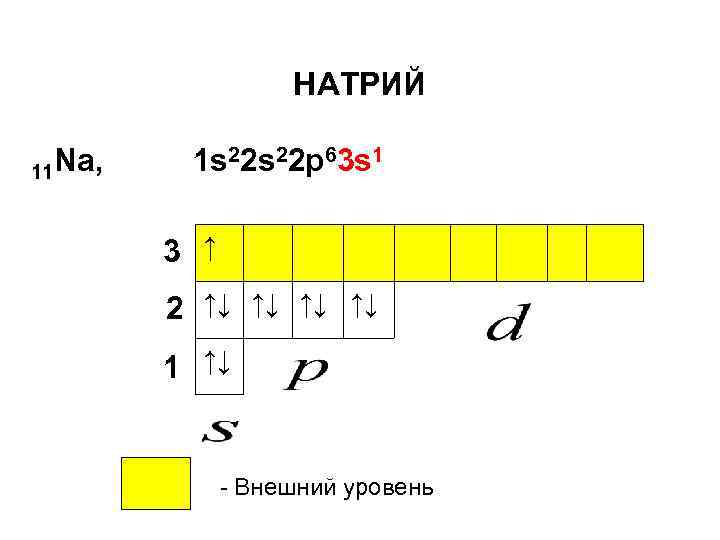 НAТРИЙ 11 Na, 1 s 22 p 63 s 1 3 ↑ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
НAТРИЙ 11 Na, 1 s 22 p 63 s 1 3 ↑ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
 Отметим, что по строению внешнего электронного уровня атом Na является аналогом атомов Li (2 s 1) и H (1 s 1).
Отметим, что по строению внешнего электронного уровня атом Na является аналогом атомов Li (2 s 1) и H (1 s 1).
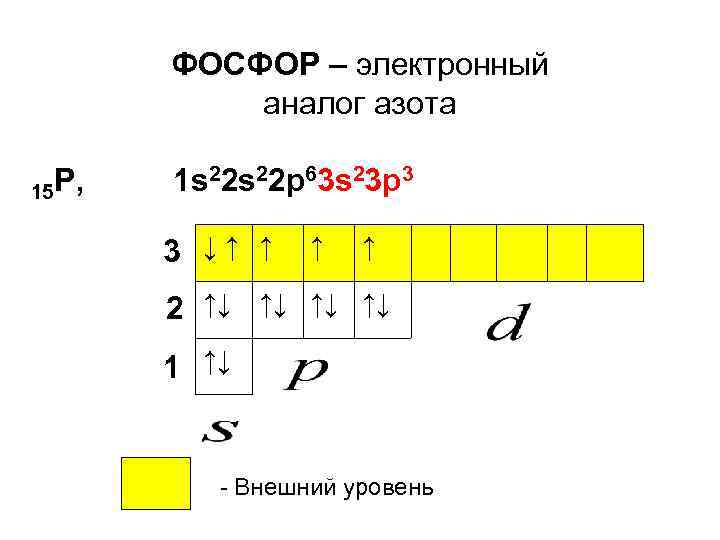 ФОСФОР – электронный аналог азота 15 P, 1 s 22 p 63 s 23 p 3 3 ↓↑ ↑ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
ФОСФОР – электронный аналог азота 15 P, 1 s 22 p 63 s 23 p 3 3 ↓↑ ↑ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
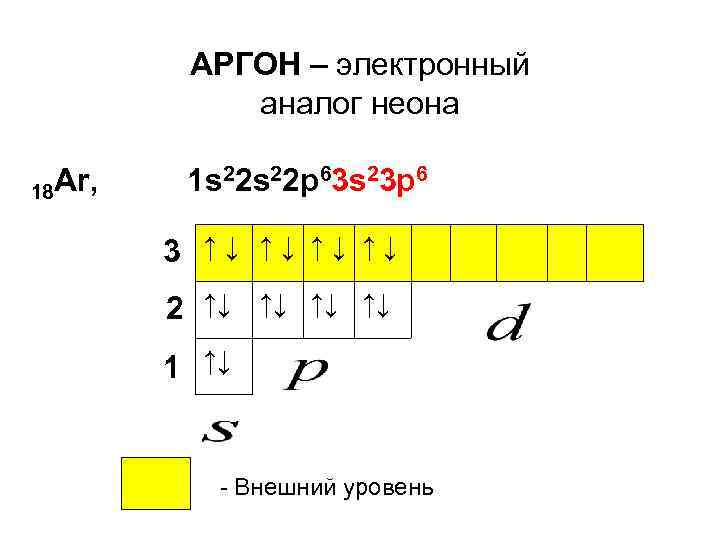 АРГОН – электронный аналог неона 18 Ar, 1 s 22 p 63 s 23 p 6 3 ↑↓ ↑↓ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
АРГОН – электронный аналог неона 18 Ar, 1 s 22 p 63 s 23 p 6 3 ↑↓ ↑↓ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
 По правилу Клечковсого 19 – ый электрон атома элемента K попадает на 4 s – орбиталь:
По правилу Клечковсого 19 – ый электрон атома элемента K попадает на 4 s – орбиталь:
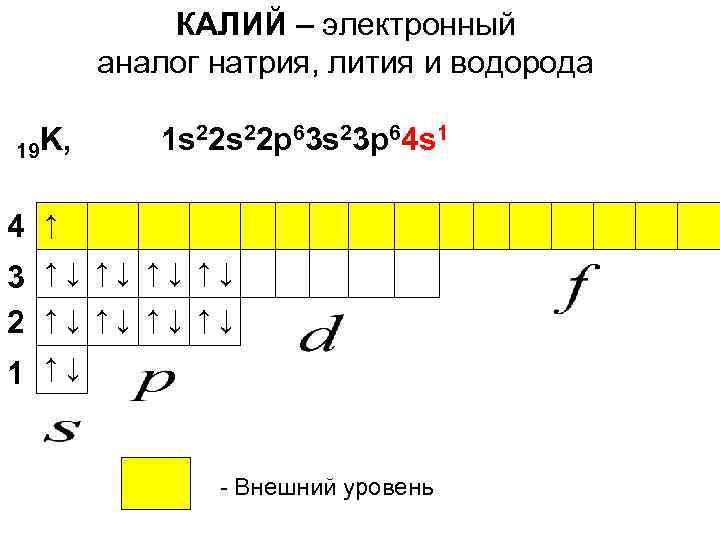 КАЛИЙ – электронный аналог натрия, лития и водорода 19 K, 1 s 22 p 63 s 23 p 64 s 1 4 ↑ 3 ↑↓ ↑↓ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
КАЛИЙ – электронный аналог натрия, лития и водорода 19 K, 1 s 22 p 63 s 23 p 64 s 1 4 ↑ 3 ↑↓ ↑↓ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
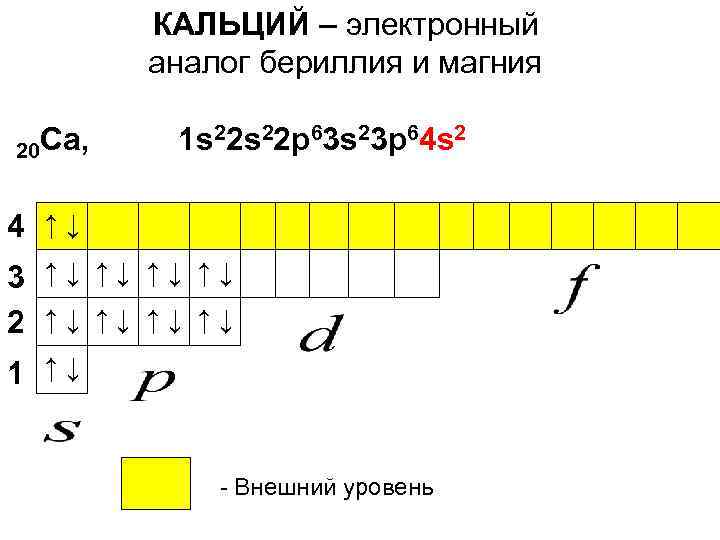 КАЛЬЦИЙ – электронный аналог бериллия и магния 20 Ca, 1 s 22 p 63 s 23 p 64 s 2 4 ↑↓ 3 ↑↓ ↑↓ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
КАЛЬЦИЙ – электронный аналог бериллия и магния 20 Ca, 1 s 22 p 63 s 23 p 64 s 2 4 ↑↓ 3 ↑↓ ↑↓ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
 21 – ый электрон атома элемента скандия, согласно правилу Клечковского попадает на теперь уже внутреннюю 3 d-орбиталь. Среди предыдущих элементов Менделеевского ряда у скандия нет аналогов по электронной конфигурации:
21 – ый электрон атома элемента скандия, согласно правилу Клечковского попадает на теперь уже внутреннюю 3 d-орбиталь. Среди предыдущих элементов Менделеевского ряда у скандия нет аналогов по электронной конфигурации:
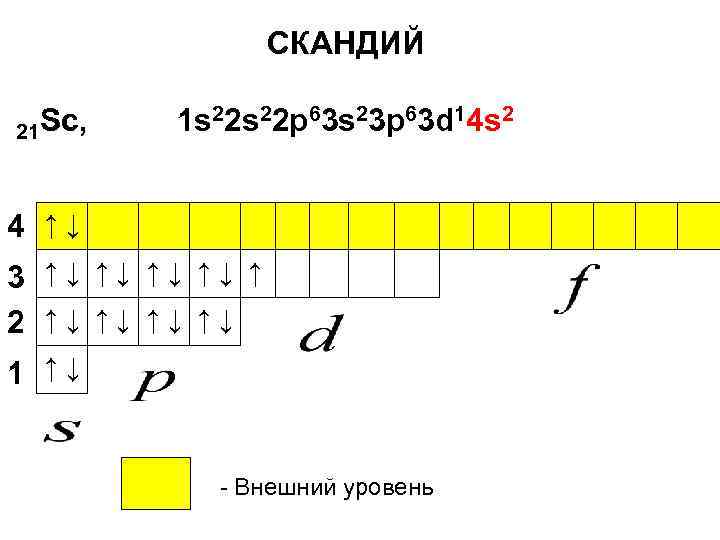 CКАНДИЙ 21 Sc, 1 s 22 p 63 s 23 p 63 d 14 s 2 4 ↑↓ 3 ↑↓ ↑↓ ↑ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
CКАНДИЙ 21 Sc, 1 s 22 p 63 s 23 p 63 d 14 s 2 4 ↑↓ 3 ↑↓ ↑↓ ↑ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
 У следующих за скандием элементов продолжает заполняться электронами 3 -d подуровень в соответствии с правилом Гунда. Однако, особенность проявляется у атома элемента хрома Cr:
У следующих за скандием элементов продолжает заполняться электронами 3 -d подуровень в соответствии с правилом Гунда. Однако, особенность проявляется у атома элемента хрома Cr:
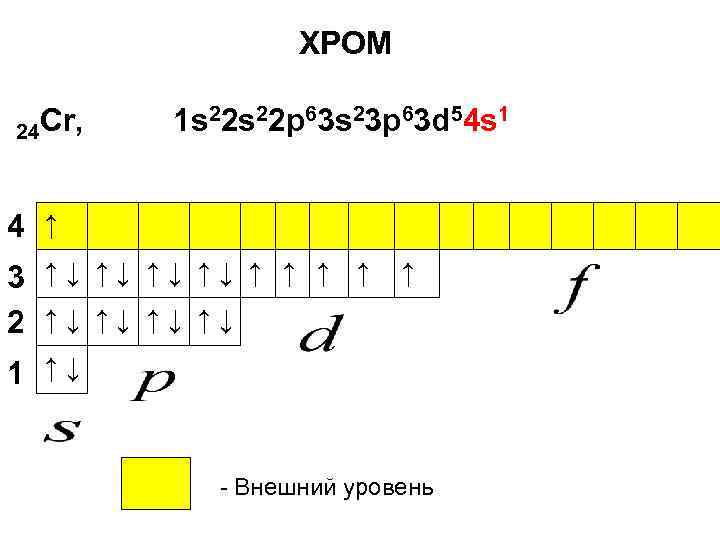 ХРОМ 24 Cr, 1 s 22 p 63 s 23 p 63 d 54 s 1 4 ↑ 3 ↑↓ ↑↓ ↑ ↑ ↑ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
ХРОМ 24 Cr, 1 s 22 p 63 s 23 p 63 d 54 s 1 4 ↑ 3 ↑↓ ↑↓ ↑ ↑ ↑ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
 Такие локальные переходы электронов между уровнями с близкими значениями энергии объясняются особой устойчивостью (минимумами) некоторых электронных конфигураций d- и f-подуровней: d 0 d 5 d 10 f 7 f 14
Такие локальные переходы электронов между уровнями с близкими значениями энергии объясняются особой устойчивостью (минимумами) некоторых электронных конфигураций d- и f-подуровней: d 0 d 5 d 10 f 7 f 14
 У элемента марганца Mn 25 – ый электрон идёт на 4 -s подуровень:
У элемента марганца Mn 25 – ый электрон идёт на 4 -s подуровень:
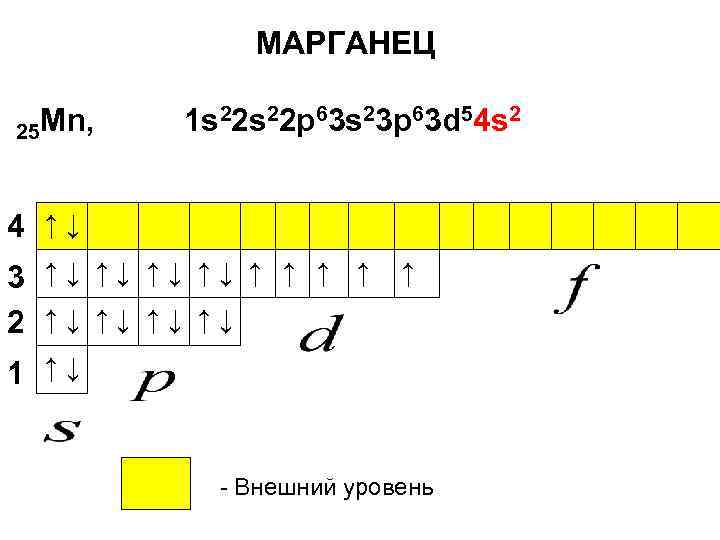 МАРГАНЕЦ 25 Mn, 1 s 22 p 63 s 23 p 63 d 54 s 2 4 ↑↓ 3 ↑↓ ↑↓ ↑ ↑ ↑ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
МАРГАНЕЦ 25 Mn, 1 s 22 p 63 s 23 p 63 d 54 s 2 4 ↑↓ 3 ↑↓ ↑↓ ↑ ↑ ↑ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
 У следующих за марганцем элементов Fe, Co, Ni, Cu, Zn электроны последовательно добавляются на 3 d-подуровень (с локальным переходом 4 s → 3 d на меди). У элемента галлия Ga начинает заполняться электронами 4 p-подуровень:
У следующих за марганцем элементов Fe, Co, Ni, Cu, Zn электроны последовательно добавляются на 3 d-подуровень (с локальным переходом 4 s → 3 d на меди). У элемента галлия Ga начинает заполняться электронами 4 p-подуровень:
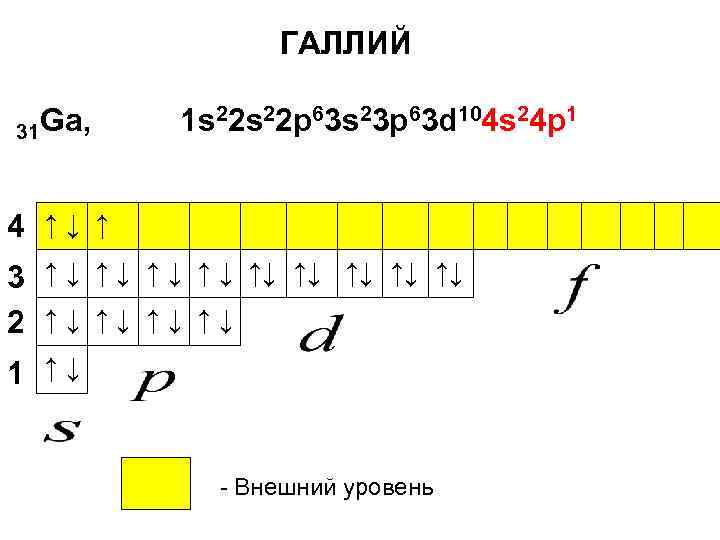 ГАЛЛИЙ 31 Ga, 1 s 22 p 63 s 23 p 63 d 104 s 24 p 1 4 ↑↓ ↑ 3 ↑ ↓ ↑ ↓ ↑↓ ↑↓ ↑↓ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
ГАЛЛИЙ 31 Ga, 1 s 22 p 63 s 23 p 63 d 104 s 24 p 1 4 ↑↓ ↑ 3 ↑ ↓ ↑ ↓ ↑↓ ↑↓ ↑↓ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
 Полностью 4 p-подуровень заполняется у благородного газа криптона Kr:
Полностью 4 p-подуровень заполняется у благородного газа криптона Kr:
 КРИПТОН 36 Kr, 1 s 22 p 63 s 23 p 63 d 104 s 24 p 6 - ОКТЕТ 4 ↑↓ ↑↓ 3 ↑ ↓ ↑ ↓ ↑↓ ↑↓ ↑↓ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
КРИПТОН 36 Kr, 1 s 22 p 63 s 23 p 63 d 104 s 24 p 6 - ОКТЕТ 4 ↑↓ ↑↓ 3 ↑ ↓ ↑ ↓ ↑↓ ↑↓ ↑↓ 2 ↑↓ ↑↓ 1 ↑↓ - Внешний уровень
 В заключение отметим, что максимальное главное квантовое число, имеющееся в электронной конфигурации атома данного элемента определяет «ГЛАВНОЕ КВАНТОВОЕ ЧИСЛО ЭЛЕМЕНТА»
В заключение отметим, что максимальное главное квантовое число, имеющееся в электронной конфигурации атома данного элемента определяет «ГЛАВНОЕ КВАНТОВОЕ ЧИСЛО ЭЛЕМЕНТА»


