ХИМИЯ- лекция 1-Растворы.ppt
- Количество слайдов: 43
 РАСТВОРЫ составитель: доцент кафедры химии и физики Закаева Р. Ш.
РАСТВОРЫ составитель: доцент кафедры химии и физики Закаева Р. Ш.
 План 1. 2. 3. 4. 5. Классификация дисперсных систем. Растворы, их характеристики. Классификации растворов. Вода. Растворение как физико-химический процесс. Растворимость веществ. 6. Свойства растворов. Осмос, законы Рауля.
План 1. 2. 3. 4. 5. Классификация дисперсных систем. Растворы, их характеристики. Классификации растворов. Вода. Растворение как физико-химический процесс. Растворимость веществ. 6. Свойства растворов. Осмос, законы Рауля.
 Дисперсные системы – гетерогенные системы, в которых в одном веществе (дисперсионной среде) распределено (диспергированно) в виде очень мелких частиц другое вещество (дисперсная фаза).
Дисперсные системы – гетерогенные системы, в которых в одном веществе (дисперсионной среде) распределено (диспергированно) в виде очень мелких частиц другое вещество (дисперсная фаза).
 Классификация дисперсных систем (по степени дисперсности) Система r, см Примеры Грубодисперсные r > 10 -5 Взвеси Гетерогенные системы Тонкодисперсные (коллоидные) 10 -5 > r > 10 -7 Молоко Гели, золи Гомогенные системы (растворы) r < 10 -7 Cu. SO 4 в воде
Классификация дисперсных систем (по степени дисперсности) Система r, см Примеры Грубодисперсные r > 10 -5 Взвеси Гетерогенные системы Тонкодисперсные (коллоидные) 10 -5 > r > 10 -7 Молоко Гели, золи Гомогенные системы (растворы) r < 10 -7 Cu. SO 4 в воде
 Классификация дисперсных систем (по агрегатному состоянию) Т(фаза)-Т(среда) Твердые р-ры Тв. золи (рубин) Ж-Т Твердая эмульсия (жемчуг) Г-Т Твердая пена (пемза) Н 2 в Pd Т-Ж Взвеси, золи (глина в воде) Истинные р-ры Ж-Ж Эмульсии (молоко) Жидкие р-ры Г-Ж Пена (мыльная пена) О 2 в воде Т-Г Аэрозоли (дым) Ж-Г Аэрозоли (туман) Г-Г Газовые смеси
Классификация дисперсных систем (по агрегатному состоянию) Т(фаза)-Т(среда) Твердые р-ры Тв. золи (рубин) Ж-Т Твердая эмульсия (жемчуг) Г-Т Твердая пена (пемза) Н 2 в Pd Т-Ж Взвеси, золи (глина в воде) Истинные р-ры Ж-Ж Эмульсии (молоко) Жидкие р-ры Г-Ж Пена (мыльная пена) О 2 в воде Т-Г Аэрозоли (дым) Ж-Г Аэрозоли (туман) Г-Г Газовые смеси
 Растворы Раствор – дисперсная система, состоящая из двух или боле компонентов, состав которой можно изменять в определенных пределах без нарушения однородности. Растворитель- компонент не меняющий своего агрегатного состояния при образовании раствора. В случаях систем Т-Т, Ж-Ж, Г-Г - растворитель - компонент, количество которого больше.
Растворы Раствор – дисперсная система, состоящая из двух или боле компонентов, состав которой можно изменять в определенных пределах без нарушения однородности. Растворитель- компонент не меняющий своего агрегатного состояния при образовании раствора. В случаях систем Т-Т, Ж-Ж, Г-Г - растворитель - компонент, количество которого больше.
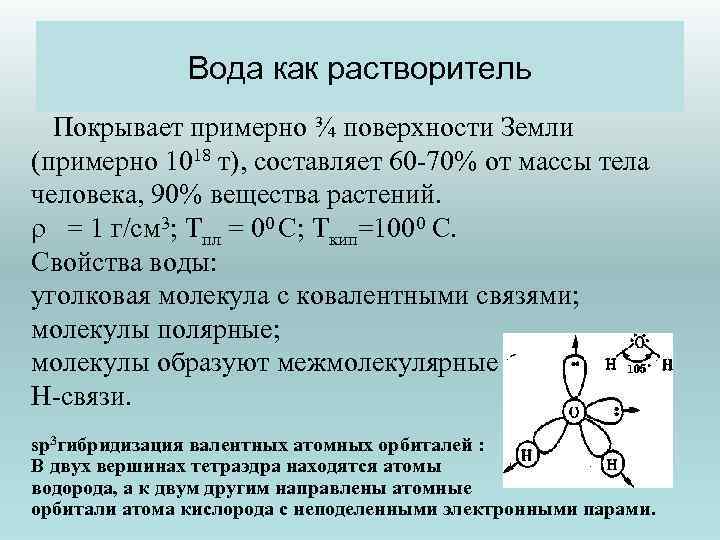 Вода как растворитель Покрывает примерно ¾ поверхности Земли (примерно 1018 т), составляет 60 -70% от массы тела человека, 90% вещества растений. r = 1 г/см 3; Тпл = 00 С; Ткип=1000 С. Свойства воды: уголковая молекула с ковалентными связями; молекулы полярные; молекулы образуют межмолекулярные Н-связи. sp 3 гибридизация валентных атомных орбиталей : В двух вершинах тетраэдра находятся атомы водорода, а к двум другим направлены атомные орбитали атома кислорода с неподеленными электронными парами.
Вода как растворитель Покрывает примерно ¾ поверхности Земли (примерно 1018 т), составляет 60 -70% от массы тела человека, 90% вещества растений. r = 1 г/см 3; Тпл = 00 С; Ткип=1000 С. Свойства воды: уголковая молекула с ковалентными связями; молекулы полярные; молекулы образуют межмолекулярные Н-связи. sp 3 гибридизация валентных атомных орбиталей : В двух вершинах тетраэдра находятся атомы водорода, а к двум другим направлены атомные орбитали атома кислорода с неподеленными электронными парами.
 Уникальные свойства воды • высокая теплоемкость (75, 3 Дж/моль • К) и • большая теплота испарения (40, 8 к. Дж/моль) обеспечивают термостатирование нашего организма. • способствует растворению и диссоциации на ионы, что обуславливает: • высокие скорости протекания биохимических реакций, • быструю миграцию ионов через биологические мембраны • практически мгновенную передачу нервных импульсов.
Уникальные свойства воды • высокая теплоемкость (75, 3 Дж/моль • К) и • большая теплота испарения (40, 8 к. Дж/моль) обеспечивают термостатирование нашего организма. • способствует растворению и диссоциации на ионы, что обуславливает: • высокие скорости протекания биохимических реакций, • быструю миграцию ионов через биологические мембраны • практически мгновенную передачу нервных импульсов.
![• Наше тело [по массе] на 70% состоит из воды; минимальная потеря воды • Наше тело [по массе] на 70% состоит из воды; минимальная потеря воды](https://present5.com/presentation/-58367693_219752903/image-9.jpg) • Наше тело [по массе] на 70% состоит из воды; минимальная потеря воды за сутки 1700 мл, • причём 50% воды выделяется из организма почками, • 5% — кишечником, • 13% — лёгкими, остальная вода выделяется кожей. За всю жизнь человек выпивает около 25 тонн воды; • вода поступает с продуктами, • часть воды образуется при обмене веществ как конечный продукт. При окислении • 100 г жира образуется 107 мл воды; • 100 г углеводов — 55 мл воды; • 100 г белка — 41 мл воды.
• Наше тело [по массе] на 70% состоит из воды; минимальная потеря воды за сутки 1700 мл, • причём 50% воды выделяется из организма почками, • 5% — кишечником, • 13% — лёгкими, остальная вода выделяется кожей. За всю жизнь человек выпивает около 25 тонн воды; • вода поступает с продуктами, • часть воды образуется при обмене веществ как конечный продукт. При окислении • 100 г жира образуется 107 мл воды; • 100 г углеводов — 55 мл воды; • 100 г белка — 41 мл воды.
 Роль воды – • Составная часть всех клеток и тканей организма. • Средой, в которой протекают все химические превращения. • Вода — источник минеральных солей, поступающих в организм. • Транспортировка элементов питания и продуктов обмена происходит по водным магистралям. • Вода — не только индифферентный растворитель, но и активный участник многих реакций обмена [например, реакций гидролиза]. • Механическая роль — вода облегчает скольжение трущихся поверхностей [суставов, связок, мышц и т. д. ]. • Испарение воды кожей — мощный фактор терморегуляции организма. • С водой связаны осмотические явления. • Только в водной среде сохраняется коллоидное состояние протоплазмы.
Роль воды – • Составная часть всех клеток и тканей организма. • Средой, в которой протекают все химические превращения. • Вода — источник минеральных солей, поступающих в организм. • Транспортировка элементов питания и продуктов обмена происходит по водным магистралям. • Вода — не только индифферентный растворитель, но и активный участник многих реакций обмена [например, реакций гидролиза]. • Механическая роль — вода облегчает скольжение трущихся поверхностей [суставов, связок, мышц и т. д. ]. • Испарение воды кожей — мощный фактор терморегуляции организма. • С водой связаны осмотические явления. • Только в водной среде сохраняется коллоидное состояние протоплазмы.
![• В организме различают две формы воды: внутриклеточную и внеклеточную. Общая вода [70%] • В организме различают две формы воды: внутриклеточную и внеклеточную. Общая вода [70%]](https://present5.com/presentation/-58367693_219752903/image-11.jpg) • В организме различают две формы воды: внутриклеточную и внеклеточную. Общая вода [70%] Внутриклеточная [50%] Интерстициальная [15%] Внеклеточная [20%] Внутрисосудистая [5%] • Внутриклеточная вода —связанная вода протоплазмы, вода притяжения на поверхности коллоидных мицелл и вода капиллярности (в ней растворены электролиты). • Интерстициальная жидкость окружает непосредственно клетки. • Внутрисосудистая жидкость — плазма крови, ликвор, лимфа (содержит белок).
• В организме различают две формы воды: внутриклеточную и внеклеточную. Общая вода [70%] Внутриклеточная [50%] Интерстициальная [15%] Внеклеточная [20%] Внутрисосудистая [5%] • Внутриклеточная вода —связанная вода протоплазмы, вода притяжения на поверхности коллоидных мицелл и вода капиллярности (в ней растворены электролиты). • Интерстициальная жидкость окружает непосредственно клетки. • Внутрисосудистая жидкость — плазма крови, ликвор, лимфа (содержит белок).
 Растворение Процесс растворения – сложный, наблюдаются физические явления (например, диффузия) и химические (образованием связей между растворяемым веществом и растворителем, процесс этот называется сольватацией (гидратацией). Доказательством химического взаимодействия является: • тепловые эффекты (КОН –выделяется, Na. Cl поглощается); Теплоту, выделяемую или поглощаемую при растворении 1 моль вещества, называют теплотой растворения Qраств. • изменение цвета - (Cu. SO 4 - с белого на голубой).
Растворение Процесс растворения – сложный, наблюдаются физические явления (например, диффузия) и химические (образованием связей между растворяемым веществом и растворителем, процесс этот называется сольватацией (гидратацией). Доказательством химического взаимодействия является: • тепловые эффекты (КОН –выделяется, Na. Cl поглощается); Теплоту, выделяемую или поглощаемую при растворении 1 моль вещества, называют теплотой растворения Qраств. • изменение цвета - (Cu. SO 4 - с белого на голубой).
 Растворимость РАСТВОРИМОСТЬЮ называется способность вещества растворяться в том или ином растворителе. Мерой растворимости вещества при данных условиях является его содержание в насыщенном растворе. Растворимость, выраженная при помощи массы вещества, которое может раствориться в 100 г воды при данной температуре, называют также коэффициентом растворимости. • P - хорошо растворимые (более 1, 0 г на 100 г воды); • M - малорастворимые (0, 1 г - 1, 0 г на 100 г воды); • Н - нерастворимые (менее 0, 1 г на 100 г воды).
Растворимость РАСТВОРИМОСТЬЮ называется способность вещества растворяться в том или ином растворителе. Мерой растворимости вещества при данных условиях является его содержание в насыщенном растворе. Растворимость, выраженная при помощи массы вещества, которое может раствориться в 100 г воды при данной температуре, называют также коэффициентом растворимости. • P - хорошо растворимые (более 1, 0 г на 100 г воды); • M - малорастворимые (0, 1 г - 1, 0 г на 100 г воды); • Н - нерастворимые (менее 0, 1 г на 100 г воды).
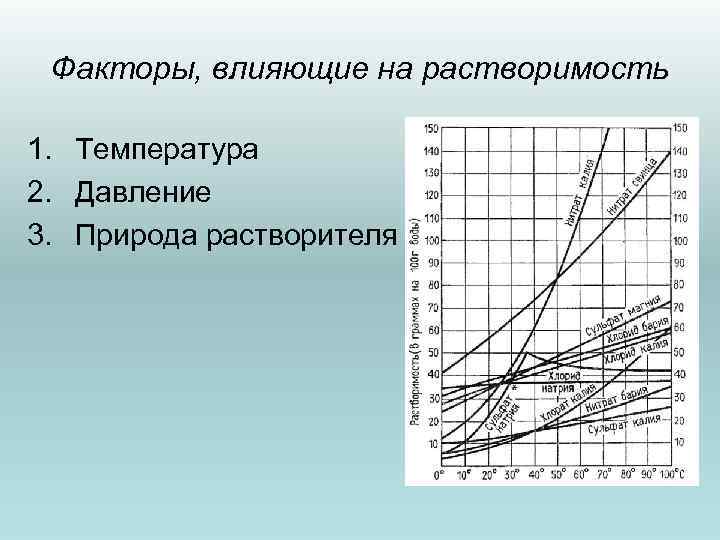 Факторы, влияющие на растворимость 1. Температура 2. Давление 3. Природа растворителя
Факторы, влияющие на растворимость 1. Температура 2. Давление 3. Природа растворителя
 Взаимная растворимость веществ Растворимость газа в жидкости Г + Ж раствор + Q Принцип Ле Шателье: увеличение р ; увеличение t ∙ С повышением давления растворимость газов в жидкостях увеличивается, а с понижением уменьшается. ∙ Растворимость газов с увеличением температуры уменьшается. Это связано прежде всего с тем, что молекулы газов при тепловом движении способны покидать раствор гораздо легче, чем молекулы твердых веществ.
Взаимная растворимость веществ Растворимость газа в жидкости Г + Ж раствор + Q Принцип Ле Шателье: увеличение р ; увеличение t ∙ С повышением давления растворимость газов в жидкостях увеличивается, а с понижением уменьшается. ∙ Растворимость газов с увеличением температуры уменьшается. Это связано прежде всего с тем, что молекулы газов при тепловом движении способны покидать раствор гораздо легче, чем молекулы твердых веществ.
 Растворимость газов: Х(г) ↔ Хр + Q, Закон Генри (1803 г. ): количество газа, растворенного при данной температуре в определенном объеме жидкости, при равновесии прямо пропорционально давлению газа С(Х) = Кг(Х)Р(Х), где С(Х) –концентрация газа в насыщенном растворе, моль/л; Кг(Х) – постоянная Генри для газа Х, моль∙лˉ¹∙Паˉ¹; Р(Х) – давление газа Х над раствором. Закон Генри справедлив лишь для разбавленных растворов при невысоких давлениях при условии отсутствия взаимодействия между растворителем и раствором.
Растворимость газов: Х(г) ↔ Хр + Q, Закон Генри (1803 г. ): количество газа, растворенного при данной температуре в определенном объеме жидкости, при равновесии прямо пропорционально давлению газа С(Х) = Кг(Х)Р(Х), где С(Х) –концентрация газа в насыщенном растворе, моль/л; Кг(Х) – постоянная Генри для газа Х, моль∙лˉ¹∙Паˉ¹; Р(Х) – давление газа Х над раствором. Закон Генри справедлив лишь для разбавленных растворов при невысоких давлениях при условии отсутствия взаимодействия между растворителем и раствором.
 Закон Дальтона Растворимость каждого из компонентов газовой смеси при постоянной температуре пропорциональна парциальному давлению компонента над жидкостью и не зависит от общего давления смеси и других компонентов Рi = Робщ Х(Хi), где Рi – парциальное давление компонента Хi; Робщ – общее давление газовой смеси; Х(Хi)- мольная доля I –компонента.
Закон Дальтона Растворимость каждого из компонентов газовой смеси при постоянной температуре пропорциональна парциальному давлению компонента над жидкостью и не зависит от общего давления смеси и других компонентов Рi = Робщ Х(Хi), где Рi – парциальное давление компонента Хi; Робщ – общее давление газовой смеси; Х(Хi)- мольная доля I –компонента.
 Закон Сеченова В присутствии электролитов растворимость газов в жидкостях понижается происходит высаливание растворов. С(Х)= Со (Х) е -Кс. Сэ где С(Х) - растворимость газа в присутствии электролита; со(Х) - растворимость газа в чистом растворителе; сэ - концентрация электролита; Кс - константа Сеченова, зависящая от природы газа, электролита и Т.
Закон Сеченова В присутствии электролитов растворимость газов в жидкостях понижается происходит высаливание растворов. С(Х)= Со (Х) е -Кс. Сэ где С(Х) - растворимость газа в присутствии электролита; со(Х) - растворимость газа в чистом растворителе; сэ - концентрация электролита; Кс - константа Сеченова, зависящая от природы газа, электролита и Т.
 Применение законов Генри и Дальтона • Кессонная болезнь- газы, закупоривают мелкие сосуды. • Для лечения барокамеры – при повышенном давлении увеличивается концентрация кислорода в крови –залечивание гангрен , сосудистая реабилитация после инсультов.
Применение законов Генри и Дальтона • Кессонная болезнь- газы, закупоривают мелкие сосуды. • Для лечения барокамеры – при повышенном давлении увеличивается концентрация кислорода в крови –залечивание гангрен , сосудистая реабилитация после инсультов.
 Растворимость жидкости в жидкости Ж 1 + Ж 2 раствор Принцип Ле Шателье: р – не влияет на равновесие; увеличение t (как правило) - ограниченная и неограниченная растворимость; В зависимости от природы жидкости могут смешиваться в любых соотношениях (в этом случае говорят о неограниченной взаимной растворимости), быть практически нерастворимыми друг в друге либо обладать ограниченной растворимостью. Повышение температуры приводит к увеличению взаимной растворимости и при некоторой температуре, называемой критической температурой растворения, взаимная растворимость ограничено растворимых жидкостей становится неограниченной. - несмешивающиеся жидкости; - «Подобное растворяется в подобном»
Растворимость жидкости в жидкости Ж 1 + Ж 2 раствор Принцип Ле Шателье: р – не влияет на равновесие; увеличение t (как правило) - ограниченная и неограниченная растворимость; В зависимости от природы жидкости могут смешиваться в любых соотношениях (в этом случае говорят о неограниченной взаимной растворимости), быть практически нерастворимыми друг в друге либо обладать ограниченной растворимостью. Повышение температуры приводит к увеличению взаимной растворимости и при некоторой температуре, называемой критической температурой растворения, взаимная растворимость ограничено растворимых жидкостей становится неограниченной. - несмешивающиеся жидкости; - «Подобное растворяется в подобном»
 Растворимость твердого вещества в жидкости Растворение физико химический процесс, включающий в себя: 1) разрушение кристаллической решетки; 2) сольватацию (гидратацию); 3) диффузию. ∙ Для большинства твердых веществ характерно увеличение растворимости при нагревании. ∙ Давление не оказывает заметного влияния на растворимость твердых веществ, потому что при растворении не происходит заметного изменения объема системы.
Растворимость твердого вещества в жидкости Растворение физико химический процесс, включающий в себя: 1) разрушение кристаллической решетки; 2) сольватацию (гидратацию); 3) диффузию. ∙ Для большинства твердых веществ характерно увеличение растворимости при нагревании. ∙ Давление не оказывает заметного влияния на растворимость твердых веществ, потому что при растворении не происходит заметного изменения объема системы.
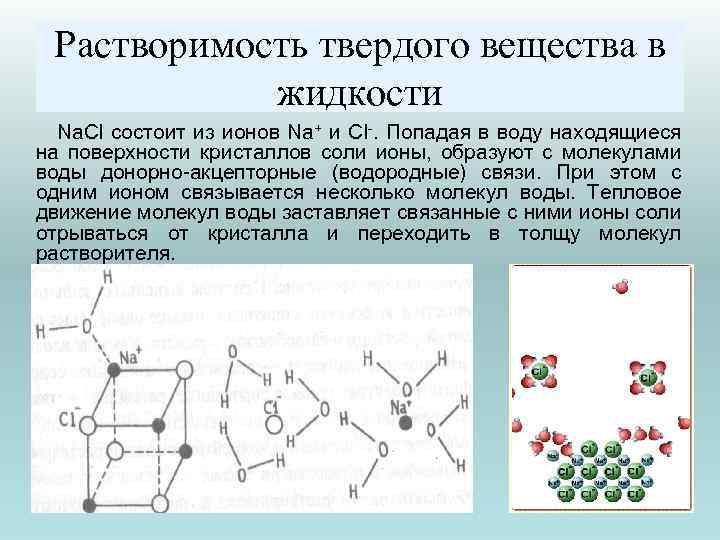 Растворимость твердого вещества в жидкости Na. Cl состоит из ионов Na+ и Cl-. Попадая в воду находящиеся на поверхности кристаллов соли ионы, образуют с молекулами воды донорно-акцепторные (водородные) связи. При этом с одним ионом связывается несколько молекул воды. Тепловое движение молекул воды заставляет связанные с ними ионы соли отрываться от кристалла и переходить в толщу молекул растворителя.
Растворимость твердого вещества в жидкости Na. Cl состоит из ионов Na+ и Cl-. Попадая в воду находящиеся на поверхности кристаллов соли ионы, образуют с молекулами воды донорно-акцепторные (водородные) связи. При этом с одним ионом связывается несколько молекул воды. Тепловое движение молекул воды заставляет связанные с ними ионы соли отрываться от кристалла и переходить в толщу молекул растворителя.
 Растворимость твердого вещества в жидкости G = H - T S H – энтальпийный фактор; T S – энтропийный фактор растворения. При растворении S > 0. H может быть или >0 или <0.
Растворимость твердого вещества в жидкости G = H - T S H – энтальпийный фактор; T S – энтропийный фактор растворения. При растворении S > 0. H может быть или >0 или <0.
 Способы выражения концентрации растворов 1) Массовая доля (ω) – показывает сколько грамм растворенного вещества растворено в 100 г раствора, выражается в долях или процентах (доли умножаются на 100 %) m вещества- масса растворенного в растворе вещества, грамм m вещества – масса раствора, грамм
Способы выражения концентрации растворов 1) Массовая доля (ω) – показывает сколько грамм растворенного вещества растворено в 100 г раствора, выражается в долях или процентах (доли умножаются на 100 %) m вещества- масса растворенного в растворе вещества, грамм m вещества – масса раствора, грамм
 2) Молярная концентрация (См, М) – показывает сколько моль растворенного вещества содержится в 1 литре раствора m - масса растворенного в растворе вещества, г; М – молярная масса растворенного вещества, г/моль V - объем раствора, л
2) Молярная концентрация (См, М) – показывает сколько моль растворенного вещества содержится в 1 литре раствора m - масса растворенного в растворе вещества, г; М – молярная масса растворенного вещества, г/моль V - объем раствора, л
 3) Молярная концентрация эквивалента вещества (эквивалентная, нормальность) (Сн, Н, СN, N) – показывает сколько моль эквивалентов вещества растворено в 1 литре раствора m - масса растворенного в растворе вещества, г; Мэк– молярная масса эквивалента растворенного вещества, г/моль; V - объем раствора, л
3) Молярная концентрация эквивалента вещества (эквивалентная, нормальность) (Сн, Н, СN, N) – показывает сколько моль эквивалентов вещества растворено в 1 литре раствора m - масса растворенного в растворе вещества, г; Мэк– молярная масса эквивалента растворенного вещества, г/моль; V - объем раствора, л
 4) Титр (Т) - количество граммов растворенного вещества в 1 мл раствора (г/мл). m T = -----V 5) Мольная доля χ - показывает отношение молей одного из компонентов раствора к сумме молей всех компонентов раствора
4) Титр (Т) - количество граммов растворенного вещества в 1 мл раствора (г/мл). m T = -----V 5) Мольная доля χ - показывает отношение молей одного из компонентов раствора к сумме молей всех компонентов раствора
 6) Моляльность (Сm) – показывает сколько моль растворенного вещества растворено в 1 кг растворителя m 1 - масса растворенного в растворе вещества, г; М – молярная масса растворенного вещества, г/моль; m 2 – масса растворителя, г.
6) Моляльность (Сm) – показывает сколько моль растворенного вещества растворено в 1 кг растворителя m 1 - масса растворенного в растворе вещества, г; М – молярная масса растворенного вещества, г/моль; m 2 – масса растворителя, г.
 Коллигативные свойства растворов Коллигативными свойствами называются свойства растворов, не зависящие от природы частиц растворенного вещества, а зависящие только от концентрации частиц в растворе. К ним принадлежат: • Диффузия • Осмотическое давление • Понижение упругости пара растворителя над раствором • Повышение температуры кипения растворов • Понижение температуры замерзания растворов
Коллигативные свойства растворов Коллигативными свойствами называются свойства растворов, не зависящие от природы частиц растворенного вещества, а зависящие только от концентрации частиц в растворе. К ним принадлежат: • Диффузия • Осмотическое давление • Понижение упругости пара растворителя над раствором • Повышение температуры кипения растворов • Понижение температуры замерзания растворов
 Диффузия Диффузией в растворе называется самопроизвольный направленный процесс переноса частиц растворенного вещества и растворителя, который приводит к выравниванию концентрации растворенного вещества в результате хаотического теплового движения частичек раствора скорость диффузии вещества пропорциональна площади поверхности, через которую переносится вещество, и градиент концентрации этого вещества В 1855 г. Фик вывел закон: ∆n/∆t = -DS ∆C/∆x, где ∆n/∆t - скорость диффузии; D - коэффициент диффузии; S - площадь сечения; ∆C/∆x- градиент концентрации.
Диффузия Диффузией в растворе называется самопроизвольный направленный процесс переноса частиц растворенного вещества и растворителя, который приводит к выравниванию концентрации растворенного вещества в результате хаотического теплового движения частичек раствора скорость диффузии вещества пропорциональна площади поверхности, через которую переносится вещество, и градиент концентрации этого вещества В 1855 г. Фик вывел закон: ∆n/∆t = -DS ∆C/∆x, где ∆n/∆t - скорость диффузии; D - коэффициент диффузии; S - площадь сечения; ∆C/∆x- градиент концентрации.
 Коэффициент диффузии , • А. Эйнштейн и независимо от него М. Смолуховский вывели следующее уравнение для коэффициента диффузии:
Коэффициент диффузии , • А. Эйнштейн и независимо от него М. Смолуховский вывели следующее уравнение для коэффициента диффузии:
 ОСМОС Осмос - односторонняя диффузия через полунепроницаемую перегородку (мембрану). 1 – Сосуд с водой 2 – Сосуд с полупроницаемыми стенками 3 - трубка
ОСМОС Осмос - односторонняя диффузия через полунепроницаемую перегородку (мембрану). 1 – Сосуд с водой 2 – Сосуд с полупроницаемыми стенками 3 - трубка
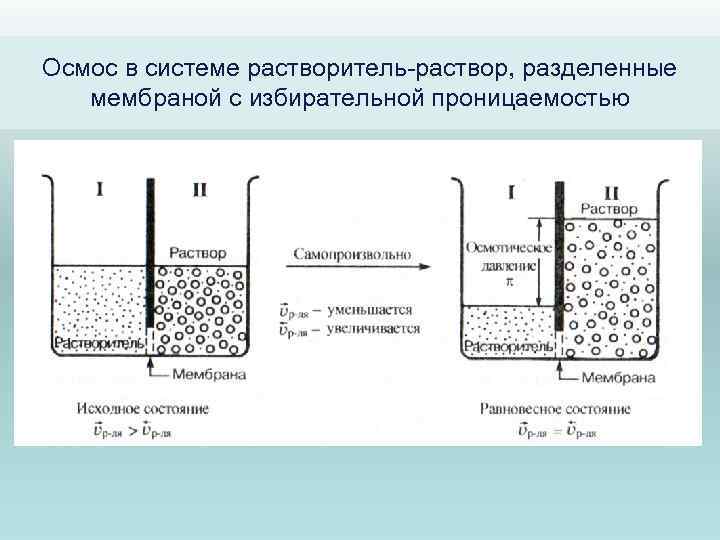 Осмос в системе растворитель-раствор, разделенные мембраной с избирательной проницаемостью
Осмос в системе растворитель-раствор, разделенные мембраной с избирательной проницаемостью
 ОСМОС • Осмотическое давление равно тому давлению, которое нужно приложить к раствору, чтобы прекратить осмос. πосм = (С, t 0), πосм (природы вещества и природы растворителя). Вант-Гофф (1886, Голландия) для разбавленных растворов неэлектролитов πосм = СМRT или πосм. V = RT, где СМ - мольная концентрация (моль/л); R = 8, 31 Дж/моль К; Т- температура, К; Р - давление, к. Па.
ОСМОС • Осмотическое давление равно тому давлению, которое нужно приложить к раствору, чтобы прекратить осмос. πосм = (С, t 0), πосм (природы вещества и природы растворителя). Вант-Гофф (1886, Голландия) для разбавленных растворов неэлектролитов πосм = СМRT или πосм. V = RT, где СМ - мольная концентрация (моль/л); R = 8, 31 Дж/моль К; Т- температура, К; Р - давление, к. Па.
 3 типа растворов по отношению к данному раствору: с меньшим осмотическим давлением – гипотонический; с бóльшим – гипертонический; с одинаковым осмотическим давлением- изотонический. В медицинской практике изотоническими растворами называются растворы, осмотическое давление которых равно осмотическому давлению крови = 7, 7 атм. 0, 9% раствор хлорида натрия и 4, 5 -5, 0% раствор глюкозы называемые физиологическими растворами. - π онкотич = 0, 03 - 0, 04 атм создается белками крови (7 -8 %) - π осм. мочи = 8 - 25 атм
3 типа растворов по отношению к данному раствору: с меньшим осмотическим давлением – гипотонический; с бóльшим – гипертонический; с одинаковым осмотическим давлением- изотонический. В медицинской практике изотоническими растворами называются растворы, осмотическое давление которых равно осмотическому давлению крови = 7, 7 атм. 0, 9% раствор хлорида натрия и 4, 5 -5, 0% раствор глюкозы называемые физиологическими растворами. - π онкотич = 0, 03 - 0, 04 атм создается белками крови (7 -8 %) - π осм. мочи = 8 - 25 атм
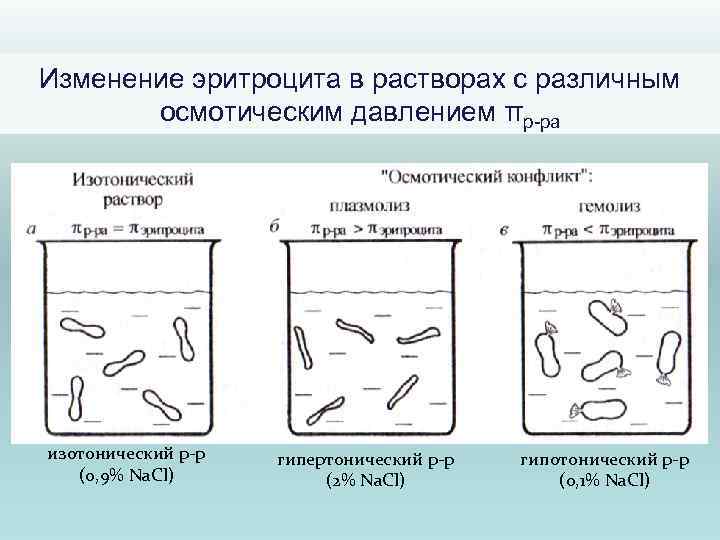 Изменение эритроцита в растворах с различным осмотическим давлением πр-ра изотонический р-р (0, 9% Na. Cl) гипертонический р-р (2% Na. Cl) гипотонический р-р (0, 1% Na. Cl)
Изменение эритроцита в растворах с различным осмотическим давлением πр-ра изотонический р-р (0, 9% Na. Cl) гипертонический р-р (2% Na. Cl) гипотонический р-р (0, 1% Na. Cl)
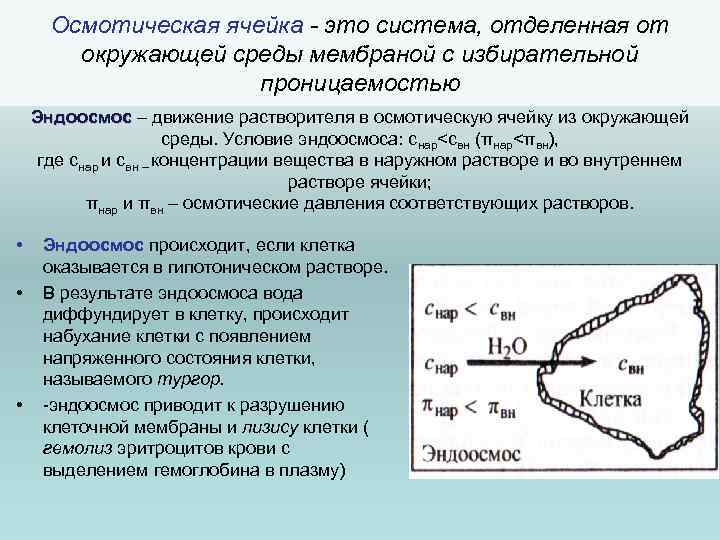 Осмотическая ячейка это система, отделенная от окружающей среды мембраной с избирательной проницаемостью Эндоосмос – движение растворителя в осмотическую ячейку из окружающей Эндоосмос среды. Условие эндоосмоса: снар<свн (πнар<πвн), где снар и свн – концентрации вещества в наружном растворе и во внутреннем растворе ячейки; πнар и πвн – осмотические давления соответствующих растворов. • • • Эндоосмос происходит, если клетка оказывается в гипотоническом растворе. В результате эндоосмоса вода диффундирует в клетку, происходит набухание клетки с появлением напряженного состояния клетки, называемого тургор. -эндоосмос приводит к разрушению клеточной мембраны и лизису клетки ( гемолиз эритроцитов крови с выделением гемоглобина в плазму)
Осмотическая ячейка это система, отделенная от окружающей среды мембраной с избирательной проницаемостью Эндоосмос – движение растворителя в осмотическую ячейку из окружающей Эндоосмос среды. Условие эндоосмоса: снар<свн (πнар<πвн), где снар и свн – концентрации вещества в наружном растворе и во внутреннем растворе ячейки; πнар и πвн – осмотические давления соответствующих растворов. • • • Эндоосмос происходит, если клетка оказывается в гипотоническом растворе. В результате эндоосмоса вода диффундирует в клетку, происходит набухание клетки с появлением напряженного состояния клетки, называемого тургор. -эндоосмос приводит к разрушению клеточной мембраны и лизису клетки ( гемолиз эритроцитов крови с выделением гемоглобина в плазму)
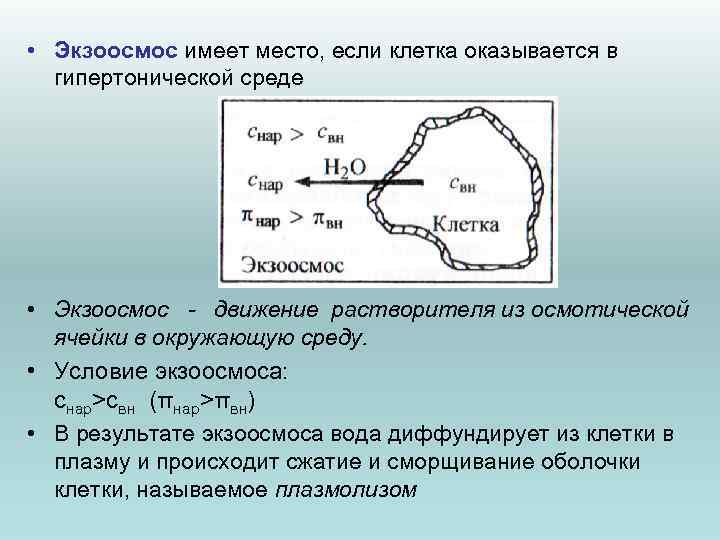 • Экзоосмос имеет место, если клетка оказывается в гипертонической среде • Экзоосмос движение растворителя из осмотической ячейки в окружающую среду. • Условие экзоосмоса: снар>свн (πнар>πвн) • В результате экзоосмоса вода диффундирует из клетки в плазму и происходит сжатие и сморщивание оболочки клетки, называемое плазмолизом
• Экзоосмос имеет место, если клетка оказывается в гипертонической среде • Экзоосмос движение растворителя из осмотической ячейки в окружающую среду. • Условие экзоосмоса: снар>свн (πнар>πвн) • В результате экзоосмоса вода диффундирует из клетки в плазму и происходит сжатие и сморщивание оболочки клетки, называемое плазмолизом
 • При приготовлении физиологических растворов необходимо учитывать их осмотические свойства, поэтому их концентрацию выражают через осмолярную концентрацию (осмолярность). • Осмолярная концентрация суммарное молярное количество всех кинетически активных, т. е. способных к самостоятельному движению, частиц, содержащихся в 1 литре раствора, независимо от их формы, размера и природы. • Осмотическому давлению крови человека соответствует осмолярная концентрация частиц от 275 до 300 м. Осм/л.
• При приготовлении физиологических растворов необходимо учитывать их осмотические свойства, поэтому их концентрацию выражают через осмолярную концентрацию (осмолярность). • Осмолярная концентрация суммарное молярное количество всех кинетически активных, т. е. способных к самостоятельному движению, частиц, содержащихся в 1 литре раствора, независимо от их формы, размера и природы. • Осмотическому давлению крови человека соответствует осмолярная концентрация частиц от 275 до 300 м. Осм/л.
 Первый закон Рауля Давление насыщенного пара раствора, содержащего нелетучее растворенное вещество прямо пропорционально его молярной доле растворителя: Р = Крх(Х 1), где Р - давление насыщенного. пара над раствором, Па; х(Х 1) - молярная доля растворителя Х 1; Кр – константа Рауля, Па.
Первый закон Рауля Давление насыщенного пара раствора, содержащего нелетучее растворенное вещество прямо пропорционально его молярной доле растворителя: Р = Крх(Х 1), где Р - давление насыщенного. пара над раствором, Па; х(Х 1) - молярная доля растворителя Х 1; Кр – константа Рауля, Па.
 Температура кипения растворов нелетучего вещества всегда выше, чем температура кипения чистого растворителя при том же давлении. II закон Рауля: Повышение температуры кипения или понижение температуры, замерзания идеальных растворов нелетучих веществ прямо пропорционально моляльной концентра ции раствора: Tк = Kэb(Х), Tз = Kкb(Х), где Kэ - эбулиоскопическая постоянная растворителя (от лат. «ebbulire» - выкипать ); КЭ для воды равна 0, 52 кг∙К∙мольˉ¹ Kк – криоскопическая постоянная растворителя (от греч. «криос» - холод). КК[вода] = 1, 86 кг∙К∙мольˉ¹. Т- температура кипения и замерзания раствора; Т 0 – температура кипения и замерзания чистого растворителя.
Температура кипения растворов нелетучего вещества всегда выше, чем температура кипения чистого растворителя при том же давлении. II закон Рауля: Повышение температуры кипения или понижение температуры, замерзания идеальных растворов нелетучих веществ прямо пропорционально моляльной концентра ции раствора: Tк = Kэb(Х), Tз = Kкb(Х), где Kэ - эбулиоскопическая постоянная растворителя (от лат. «ebbulire» - выкипать ); КЭ для воды равна 0, 52 кг∙К∙мольˉ¹ Kк – криоскопическая постоянная растворителя (от греч. «криос» - холод). КК[вода] = 1, 86 кг∙К∙мольˉ¹. Т- температура кипения и замерзания раствора; Т 0 – температура кипения и замерзания чистого растворителя.
 Формулы для определения молярной массы растворенного вещества:
Формулы для определения молярной массы растворенного вещества:
 СПАСИБО ЗА ВНИМАНИЕ!
СПАСИБО ЗА ВНИМАНИЕ!


