РАСТВОРЫ.ppt
- Количество слайдов: 21
 РАСТВОРЫ
РАСТВОРЫ
 Растворы электролитов Электролиты – вещества с ионной проводимостью. Это растворы солей, кислоты, оснований, расплавы солей. I – закон Рауля для электролитов:
Растворы электролитов Электролиты – вещества с ионной проводимостью. Это растворы солей, кислоты, оснований, расплавы солей. I – закон Рауля для электролитов:
 II закон Рауля ∆Tкип =i. Em ∆Tзам=i. Km Закон Вант-Гоффа ∆Pосм=ic. RT
II закон Рауля ∆Tкип =i. Em ∆Tзам=i. Km Закон Вант-Гоффа ∆Pосм=ic. RT
 i – поправочный коэффициент изотонический i – зависит от: - природы раствора - концентрации раствора i>1 для растворов солей, кислот и оснований
i – поправочный коэффициент изотонический i – зависит от: - природы раствора - концентрации раствора i>1 для растворов солей, кислот и оснований
 Теория электролитической диссоциации Аррениуса Распад молекул электролитов на ионы в среде растворителя под действием молекул растворителя. Na. Cl → Na+ + Cl. Количество частиц при диссоциации увеличивается.
Теория электролитической диссоциации Аррениуса Распад молекул электролитов на ионы в среде растворителя под действием молекул растворителя. Na. Cl → Na+ + Cl. Количество частиц при диссоциации увеличивается.
 Количественная характеристика процесса диссоциации выражается степенью электролитической диссоциации – α.
Количественная характеристика процесса диссоциации выражается степенью электролитической диссоциации – α.
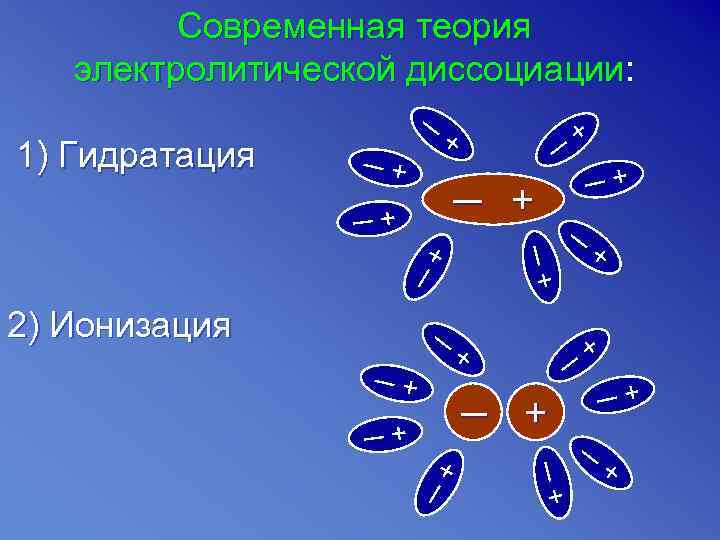 Современная теория электролитической диссоциации: 1) Гидратация ─ ─+ + ─ ─ + ─+ ─+ ─ + ─+ 2) Ионизация ─ ─+ + ─+ ─ ─ + ─+ ─+ ─ + + + ─ ─+ +
Современная теория электролитической диссоциации: 1) Гидратация ─ ─+ + ─ ─ + ─+ ─+ ─ + ─+ 2) Ионизация ─ ─+ + ─+ ─ ─ + ─+ ─+ ─ + + + ─ ─+ +
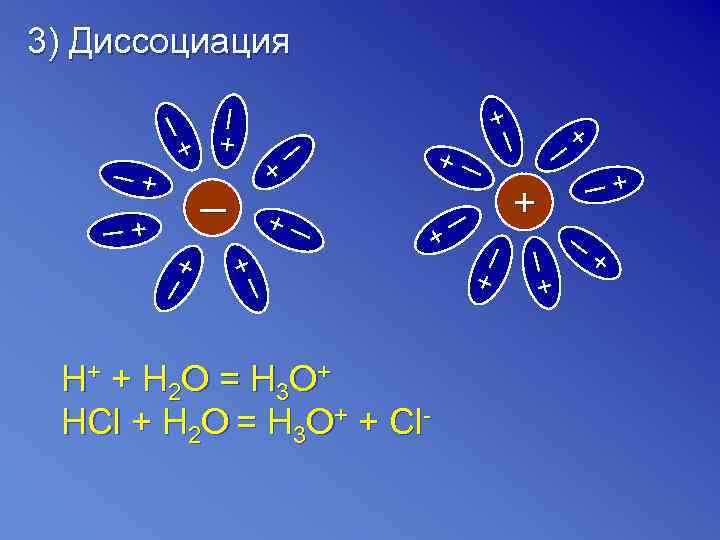 + ─+ ─+ + + ─+ ─ + ─ ─ ─ H + + H 2 O = H 3 O + HCl + H 2 O = H 3 O+ + Cl- ─ + ─+ ─+ ─+ 3) Диссоциация + ─ ─+ +
+ ─+ ─+ + + ─+ ─ + ─ ─ ─ H + + H 2 O = H 3 O + HCl + H 2 O = H 3 O+ + Cl- ─ + ─+ ─+ ─+ 3) Диссоциация + ─ ─+ +
 Способность гидратироваться зависит: - от природы ионов - от заряда иона - от размера иона - от строения электронной оболочки Al 3+ > Cr 3+ > Zn 2+ > Na+ Энтальпия гидратации ионов: ∆Hгид. соли = ∆H+гид+ ∆Н-гид ∆S>0 Гидратация сопровождается значительным разрушением структуры ∆S<0 если структура растворителя упорядочивается
Способность гидратироваться зависит: - от природы ионов - от заряда иона - от размера иона - от строения электронной оболочки Al 3+ > Cr 3+ > Zn 2+ > Na+ Энтальпия гидратации ионов: ∆Hгид. соли = ∆H+гид+ ∆Н-гид ∆S>0 Гидратация сопровождается значительным разрушением структуры ∆S<0 если структура растворителя упорядочивается
 По степени диссоциации: Сильные электролиты – α > 50% все соли, неорганические кислоты, гидроксиды щёлочных и щелочноземельных металлов: HCl, H 2 SO 4, HNO 3 Слабые электролиты – α < 50% Н 2 S, H 2 Si. O 3, H 2 CO 3, CH 3 COOH, гидрооксиды d – элементов (нерастворимые вещества), NH 4 OH.
По степени диссоциации: Сильные электролиты – α > 50% все соли, неорганические кислоты, гидроксиды щёлочных и щелочноземельных металлов: HCl, H 2 SO 4, HNO 3 Слабые электролиты – α < 50% Н 2 S, H 2 Si. O 3, H 2 CO 3, CH 3 COOH, гидрооксиды d – элементов (нерастворимые вещества), NH 4 OH.
 Растворы слабых электролитов AB диссоциация ассоциация A+ + B - Чем больше Кд тем диссоциирует электролит. NH 4 OH = NH 4+ + OH- сильнее
Растворы слабых электролитов AB диссоциация ассоциация A+ + B - Чем больше Кд тем диссоциирует электролит. NH 4 OH = NH 4+ + OH- сильнее
 Закон разбавления Освальда α<<1, то С – разбавлением раствора степень диссоциации увеличивается. с – молярная концентрация электролита сα – концентрация каждого из ионов с(1 -α) – концентрация недиссоциирующих частиц.
Закон разбавления Освальда α<<1, то С – разбавлением раствора степень диссоциации увеличивается. с – молярная концентрация электролита сα – концентрация каждого из ионов с(1 -α) – концентрация недиссоциирующих частиц.
 Растворы сильных электролитов Na. Cl i≈2 Na. Cl → Na+ + Cl- от наличия одноимённых ионов I. СН 3 COOH ↔ H+ + CH 3 COOII. СН 3 COONa → CH 3 COO- + Na+ III. - от температуры, увеличение t° вызывает ассоциацию ионов.
Растворы сильных электролитов Na. Cl i≈2 Na. Cl → Na+ + Cl- от наличия одноимённых ионов I. СН 3 COOH ↔ H+ + CH 3 COOII. СН 3 COONa → CH 3 COO- + Na+ III. - от температуры, увеличение t° вызывает ассоциацию ионов.
 1907 Льюис → активность (а) → эффективная концентрация ионов. а = f·c; f=1 a=c Активность отражает: 1. Неполную диссоциацию молекул 2. Взаимное притяжение разноименных ионов 3. Влияние гидратации ионов 4. Взаимодействия между молекулами растворителя.
1907 Льюис → активность (а) → эффективная концентрация ионов. а = f·c; f=1 a=c Активность отражает: 1. Неполную диссоциацию молекул 2. Взаимное притяжение разноименных ионов 3. Влияние гидратации ионов 4. Взаимодействия между молекулами растворителя.
 Коэффициент активности зависит от ионной силы раствора (J). А – коэффициент пропор. , зависит от вида растворителя. Кислоты – диссоциируют на катионы H+ и анион кислотного остатка HCl → H+ + Cl. Н 3 РО 4 ↔ [H+][H 2 PO 4]-
Коэффициент активности зависит от ионной силы раствора (J). А – коэффициент пропор. , зависит от вида растворителя. Кислоты – диссоциируют на катионы H+ и анион кислотного остатка HCl → H+ + Cl. Н 3 РО 4 ↔ [H+][H 2 PO 4]-
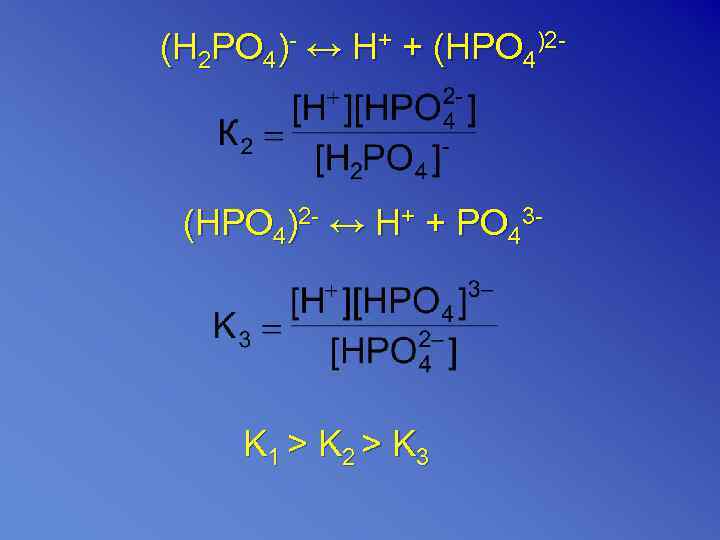 (H 2 PO 4)- ↔ H+ + (HPO 4)2 - ↔ H+ + PO 43 - K 1 > K 2 > K 3
(H 2 PO 4)- ↔ H+ + (HPO 4)2 - ↔ H+ + PO 43 - K 1 > K 2 > K 3
 Ионное произведение воды. p. H – растворов. Н 2 О ↔ H+ + ОН- K´воды = [H+][OH-] – ионное произведение воды Kводы = [H+][OH-] = 1, 1 10 -14 г-ион/л – увеличивается с ростом температуры. [H+][OH-] = 1 10 -14 тогда [H+] = [OH-] = = 10 -7 г-ион/л
Ионное произведение воды. p. H – растворов. Н 2 О ↔ H+ + ОН- K´воды = [H+][OH-] – ионное произведение воды Kводы = [H+][OH-] = 1, 1 10 -14 г-ион/л – увеличивается с ростом температуры. [H+][OH-] = 1 10 -14 тогда [H+] = [OH-] = = 10 -7 г-ион/л
![Нейтральный раствор [H+] = 10 -7 г-ион/л [OH-] = 10 -7 г-ион/л Кислый раствор Нейтральный раствор [H+] = 10 -7 г-ион/л [OH-] = 10 -7 г-ион/л Кислый раствор](https://present5.com/presentation/52606873_265452974/image-18.jpg) Нейтральный раствор [H+] = 10 -7 г-ион/л [OH-] = 10 -7 г-ион/л Кислый раствор [H+] > 10 -7 г-ион/л [OH-] < 10 -7 г-ион/л Щелочной раствор [H+] < 10 -7 г-ион/л [OH-] > 10 -7 г-ион/л Водородный показатель -Lg[H+] = p. H
Нейтральный раствор [H+] = 10 -7 г-ион/л [OH-] = 10 -7 г-ион/л Кислый раствор [H+] > 10 -7 г-ион/л [OH-] < 10 -7 г-ион/л Щелочной раствор [H+] < 10 -7 г-ион/л [OH-] > 10 -7 г-ион/л Водородный показатель -Lg[H+] = p. H
![В нейтральной среде: [H+] = 10 -7 -Lg[10 -7] = 7 → p. H В нейтральной среде: [H+] = 10 -7 -Lg[10 -7] = 7 → p. H](https://present5.com/presentation/52606873_265452974/image-19.jpg) В нейтральной среде: [H+] = 10 -7 -Lg[10 -7] = 7 → p. H = 7 В кислой среде: [H+] = 10 -5 -Lg[10 -5] = 5 → p. H = 5 p. H < 7 ([Н+] < 10 -7) В щелочной среде: [H+] = 10 -9 -Lg[10 -9] = 9 → p. H = 9 p. H > 7 ([Н+] > 10 -7)
В нейтральной среде: [H+] = 10 -7 -Lg[10 -7] = 7 → p. H = 7 В кислой среде: [H+] = 10 -5 -Lg[10 -5] = 5 → p. H = 5 p. H < 7 ([Н+] < 10 -7) В щелочной среде: [H+] = 10 -9 -Lg[10 -9] = 9 → p. H = 9 p. H > 7 ([Н+] > 10 -7)
![Пример 1: [OH-] = 10 -11 p. H = ? [H+][OH-] = 10 -14 Пример 1: [OH-] = 10 -11 p. H = ? [H+][OH-] = 10 -14](https://present5.com/presentation/52606873_265452974/image-20.jpg) Пример 1: [OH-] = 10 -11 p. H = ? [H+][OH-] = 10 -14 x 10 -11 = 10 -14 [H+] = 10 -3 г-ион/л -Lg[10 -3] = 3 p. H = 3 (кислая среда)
Пример 1: [OH-] = 10 -11 p. H = ? [H+][OH-] = 10 -14 x 10 -11 = 10 -14 [H+] = 10 -3 г-ион/л -Lg[10 -3] = 3 p. H = 3 (кислая среда)
![Пример 2: p. H = 2 [OH-] = ? [H+] = 10 -2 x Пример 2: p. H = 2 [OH-] = ? [H+] = 10 -2 x](https://present5.com/presentation/52606873_265452974/image-21.jpg) Пример 2: p. H = 2 [OH-] = ? [H+] = 10 -2 x = 10 -14 [OH-] = 10 -12 г-ион/л
Пример 2: p. H = 2 [OH-] = ? [H+] = 10 -2 x = 10 -14 [OH-] = 10 -12 г-ион/л


