4._Растворы.pptx
- Количество слайдов: 21
 Растворы Раствор - однородная система, которая состоит из двух или более компонентов. Компоненты раствора - растворитель и растворенное вещество. mр-ра = mв-ва + р-ля В зависимости от вида растворителя растворы могут быть газообразные, жидкие или твердые По степени дисперсности системы делятся на: взвеси, эмульсии - r > 100 нм коллоидные растворы - r > 1 нм растворы (истинные) - r < 1 нм
Растворы Раствор - однородная система, которая состоит из двух или более компонентов. Компоненты раствора - растворитель и растворенное вещество. mр-ра = mв-ва + р-ля В зависимости от вида растворителя растворы могут быть газообразные, жидкие или твердые По степени дисперсности системы делятся на: взвеси, эмульсии - r > 100 нм коллоидные растворы - r > 1 нм растворы (истинные) - r < 1 нм
 Концентрация растворов Концентрация показывает отношение массы или количества растворенного вещества к массе, объёму или количеству раствора или растворителя. Массовая доля вещества в растворе w равна отношению массы растворенного вещества к массе раствора: w = mв-ва/mр-ра или w = mв-ва/(V r), так как mр-ра = Vр-ра Молярная концентрация с равна отношению числа моль растворенного вещества к объёму раствора: с = n(моль)/V(л) или с = m/(M V(л))
Концентрация растворов Концентрация показывает отношение массы или количества растворенного вещества к массе, объёму или количеству раствора или растворителя. Массовая доля вещества в растворе w равна отношению массы растворенного вещества к массе раствора: w = mв-ва/mр-ра или w = mв-ва/(V r), так как mр-ра = Vр-ра Молярная концентрация с равна отношению числа моль растворенного вещества к объёму раствора: с = n(моль)/V(л) или с = m/(M V(л))
 Моль - это количество вещества, содержащее 6, 02 1023 структурных единиц (атомов, молекул, ионов). n = m/M =V/VM = N/NA n - количество вещества (моль), N - число частиц, NА = 6, 02 1023 частиц/моль - постоянная Авогадро, m - масса вещества (г), М – молярная масса (г/моль), V - объема газа (л), VМ= 22, 4 л/моль – молярный объем газа (н. у. )
Моль - это количество вещества, содержащее 6, 02 1023 структурных единиц (атомов, молекул, ионов). n = m/M =V/VM = N/NA n - количество вещества (моль), N - число частиц, NА = 6, 02 1023 частиц/моль - постоянная Авогадро, m - масса вещества (г), М – молярная масса (г/моль), V - объема газа (л), VМ= 22, 4 л/моль – молярный объем газа (н. у. )
 Эквивалент - реальная или условная частица, эквивалентная одному атому водорода. ЭО – 1/2 атома О. ЭAl = 1/3 атома алюминия. Молярная масса эквивалентов МЭ - отношение массы вещества к количеству эквивалентов этого вещества: МЭ = m/n(экв). В реакциях обмена зарядов МЭ ( Аnm+Вmn- ) с молярной массой М равна: МЭ = М/(n m). В окислительно-восстановительных реакциях МЭ вещества с молярной массой М равна: МЭ = М/n(ē), где п(ē) - число переданных электронов.
Эквивалент - реальная или условная частица, эквивалентная одному атому водорода. ЭО – 1/2 атома О. ЭAl = 1/3 атома алюминия. Молярная масса эквивалентов МЭ - отношение массы вещества к количеству эквивалентов этого вещества: МЭ = m/n(экв). В реакциях обмена зарядов МЭ ( Аnm+Вmn- ) с молярной массой М равна: МЭ = М/(n m). В окислительно-восстановительных реакциях МЭ вещества с молярной массой М равна: МЭ = М/n(ē), где п(ē) - число переданных электронов.
 Концентрация растворов Молярная концентрация эквивалентов (нормальная или эквивалентная концентрация) с. Э равна отношению числа моль эквивалентов растворенного вещества к объёму раствора: с. Э = n(моль экв)/V(л) с. Э = m/(MЭ V(л))
Концентрация растворов Молярная концентрация эквивалентов (нормальная или эквивалентная концентрация) с. Э равна отношению числа моль эквивалентов растворенного вещества к объёму раствора: с. Э = n(моль экв)/V(л) с. Э = m/(MЭ V(л))
 Закон эквивалентов – количества вещества эквивалентов реагентов равны другу nэ1 = nэ2 m 1/MЭ 1 = m 2/МЭ 2 V 1/Vэ1 = V 2/Vэ2 Для растворов закон эквивалентов может быть записан в виде: с. Э 1 V 1 = с. Э 2 V 2 где, с. Э 1, с. Э 2 и V 1 и V 2 - молярные концентрации эквивалентов и объёмы растворов этих двух веществ.
Закон эквивалентов – количества вещества эквивалентов реагентов равны другу nэ1 = nэ2 m 1/MЭ 1 = m 2/МЭ 2 V 1/Vэ1 = V 2/Vэ2 Для растворов закон эквивалентов может быть записан в виде: с. Э 1 V 1 = с. Э 2 V 2 где, с. Э 1, с. Э 2 и V 1 и V 2 - молярные концентрации эквивалентов и объёмы растворов этих двух веществ.
 Электролитическая диссоциация Электролиты - соединения, растворы или расплавы которых проводят электрический ток. Например: соли, щелочи, кислоты. Неэлектролиты - соединения, растворы или расплавы которых не проводят электрический ток. Например: сахар. Электролитическая диссоциация - это распад электролита на катионы и анионы под действием полярных молекул растворителя.
Электролитическая диссоциация Электролиты - соединения, растворы или расплавы которых проводят электрический ток. Например: соли, щелочи, кислоты. Неэлектролиты - соединения, растворы или расплавы которых не проводят электрический ток. Например: сахар. Электролитическая диссоциация - это распад электролита на катионы и анионы под действием полярных молекул растворителя.
 Степень диссоциации - - это отношение концентрации диссоциированных молекул (сдисс) к общей концентрации растворенных молекул (соб): = сдисс/соб. Если = 0, то нет диссоциации; если = 1, то полная диссоциация; если 0 1, то частичная диссоциация. Электролиты можно разделить на сильные ( 1) и слабые ( <<1)
Степень диссоциации - - это отношение концентрации диссоциированных молекул (сдисс) к общей концентрации растворенных молекул (соб): = сдисс/соб. Если = 0, то нет диссоциации; если = 1, то полная диссоциация; если 0 1, то частичная диссоциация. Электролиты можно разделить на сильные ( 1) и слабые ( <<1)
 Электролиты • • • Сильные электролиты (для них 1) соли, растворимые в воде и основания, растворимые в воде кислоты: HNO 3, HCl, H 2 SO 4, HI, HBr, HCl. O 4 и др. Слабые электролиты (для них <<1) H 2 O, NH 4 OH, малорастворимые основания и соли многие кислоты: HNO 2, HF, H 2 SO 3, H 3 PO 4, H 2 CO 3, H 2 S, CH 3 COOH и другие.
Электролиты • • • Сильные электролиты (для них 1) соли, растворимые в воде и основания, растворимые в воде кислоты: HNO 3, HCl, H 2 SO 4, HI, HBr, HCl. O 4 и др. Слабые электролиты (для них <<1) H 2 O, NH 4 OH, малорастворимые основания и соли многие кислоты: HNO 2, HF, H 2 SO 3, H 3 PO 4, H 2 CO 3, H 2 S, CH 3 COOH и другие.
 Ионные уравнения реакций В ионных уравнениях реакций сильные электролиты записываются в виде ионов, а слабые электролиты, малорастворимые вещества и газы - в виде молекул. Например: Ca. CO 3 + 2 HCl = Ca. Cl 2 + H 2 O + CO 2 Ca. CO 3 + 2 H+ + 2 Cl- = Ca 2+ + 2 Cl- + H 2 O + CO 2 Ca. CO 3 + 2 H+ = Ca 2+ + H 2 O + CO 2 Реакции между ионами идут в сторону получения вещества, образующего меньше ионов, то есть в сторону более слабого электролита или менее растворимого вещества
Ионные уравнения реакций В ионных уравнениях реакций сильные электролиты записываются в виде ионов, а слабые электролиты, малорастворимые вещества и газы - в виде молекул. Например: Ca. CO 3 + 2 HCl = Ca. Cl 2 + H 2 O + CO 2 Ca. CO 3 + 2 H+ + 2 Cl- = Ca 2+ + 2 Cl- + H 2 O + CO 2 Ca. CO 3 + 2 H+ = Ca 2+ + H 2 O + CO 2 Реакции между ионами идут в сторону получения вещества, образующего меньше ионов, то есть в сторону более слабого электролита или менее растворимого вещества
 Закон действия масс •
Закон действия масс •
 Константа равновесия - это мера протекания прямой реакции. К = 0 - прямая реакция не идет К = ∞ - прямая реакция идет до конца К > 1 - равновесие сдвинуто вправо К < 1 - равновесие сдвинуто влево ΔG = -RTln. K или ΔG = -2, 3 RTlg. K • Если К>1, то lg. K>0 и ΔG <0, равновесие сдвинуто вправо, реакция идет вправо самопроизвольно. • Если К<1, то lg. K<0 и ΔG >0 равновесие сдвинуто влево, то реакция самопроизвольно вправо не идет
Константа равновесия - это мера протекания прямой реакции. К = 0 - прямая реакция не идет К = ∞ - прямая реакция идет до конца К > 1 - равновесие сдвинуто вправо К < 1 - равновесие сдвинуто влево ΔG = -RTln. K или ΔG = -2, 3 RTlg. K • Если К>1, то lg. K>0 и ΔG <0, равновесие сдвинуто вправо, реакция идет вправо самопроизвольно. • Если К<1, то lg. K<0 и ΔG >0 равновесие сдвинуто влево, то реакция самопроизвольно вправо не идет
 Диссоциация слабых электролитов •
Диссоциация слабых электролитов •
 Диссоциация многоосновных кислот •
Диссоциация многоосновных кислот •
 Закон разбавления Оствальда •
Закон разбавления Оствальда •
 Влияние общего иона на диссоциацию слабого электролита •
Влияние общего иона на диссоциацию слабого электролита •
 Диссоциация сильных электролитов Активность иона - это концентрация иона, проявляющаяся в его свойствах. Коэффициент активности f - это отношение активности иона a к концентрации с: f = a/c или a = fc. Если f = 1, то ионы свободны и не взаимодействуют между собой. Если f < 1, то ионы взаимодействуют между собой. Чем меньше f, тем больше взаимодействие между ионами. Взаимодействие данного иона с раствором зависит от заряда иона z и ионной силы раствора I.
Диссоциация сильных электролитов Активность иона - это концентрация иона, проявляющаяся в его свойствах. Коэффициент активности f - это отношение активности иона a к концентрации с: f = a/c или a = fc. Если f = 1, то ионы свободны и не взаимодействуют между собой. Если f < 1, то ионы взаимодействуют между собой. Чем меньше f, тем больше взаимодействие между ионами. Взаимодействие данного иона с раствором зависит от заряда иона z и ионной силы раствора I.
 Ионная сила раствора I зависит от зарядов z и концентраций с ионов: I = 0, 5 Sci·zi 2 Для электролитов концентрации c ионная сила I равна в зависимости от типа электролита: A+B- (Na. OH, HCl) I = 1/2(c 12 + c 12) = c A 2+B 2 - (H 2 SO 4, Mg. Cl 2) I = 1/2(2 c 12 + c 22) = 3 c A 2+B 2 - Cu. SO 4, Mg. SO 4) I = 1/2(c 22 + c 22) = 4 c A 3+B 3 - (Al. Cl 3, Na 3 PO 4) I = 1/2(c 32 + 3 c 12) = 6 c
Ионная сила раствора I зависит от зарядов z и концентраций с ионов: I = 0, 5 Sci·zi 2 Для электролитов концентрации c ионная сила I равна в зависимости от типа электролита: A+B- (Na. OH, HCl) I = 1/2(c 12 + c 12) = c A 2+B 2 - (H 2 SO 4, Mg. Cl 2) I = 1/2(2 c 12 + c 22) = 3 c A 2+B 2 - Cu. SO 4, Mg. SO 4) I = 1/2(c 22 + c 22) = 4 c A 3+B 3 - (Al. Cl 3, Na 3 PO 4) I = 1/2(c 32 + 3 c 12) = 6 c
 Коэффициент активности •
Коэффициент активности •
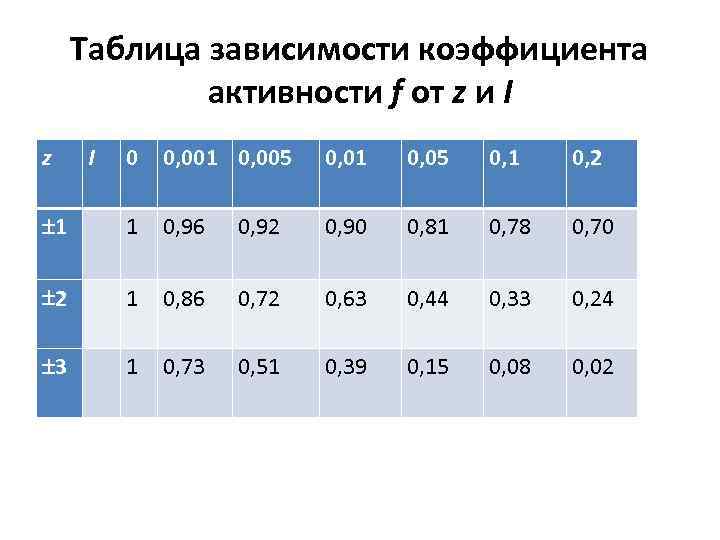 Таблица зависимости коэффициента активности f от z и I z I 0 0, 001 0, 005 0, 01 0, 05 0, 1 0, 2 1 1 0, 96 0, 92 0, 90 0, 81 0, 78 0, 70 2 1 0, 86 0, 72 0, 63 0, 44 0, 33 0, 24 3 1 0, 73 0, 51 0, 39 0, 15 0, 08 0, 02
Таблица зависимости коэффициента активности f от z и I z I 0 0, 001 0, 005 0, 01 0, 05 0, 1 0, 2 1 1 0, 96 0, 92 0, 90 0, 81 0, 78 0, 70 2 1 0, 86 0, 72 0, 63 0, 44 0, 33 0, 24 3 1 0, 73 0, 51 0, 39 0, 15 0, 08 0, 02
 Задача. Найти активности ионов в 0, 025 М Cu. SO 4. Решение: Cu. SO 4 ⇄ Cu 2+ + SO 420, 025 М I = 0, 5 Sci·zi = 0, 5(0, 025 22 + 0, 025 22) = 0, 1; По таблице: f(Cu 2+) = f(SO 42 -) = 0, 33; a(Cu 2+) = a(SO 42 -) = f c = 0, 025 0, 33 = 8, 25 10 -3 M
Задача. Найти активности ионов в 0, 025 М Cu. SO 4. Решение: Cu. SO 4 ⇄ Cu 2+ + SO 420, 025 М I = 0, 5 Sci·zi = 0, 5(0, 025 22 + 0, 025 22) = 0, 1; По таблице: f(Cu 2+) = f(SO 42 -) = 0, 33; a(Cu 2+) = a(SO 42 -) = f c = 0, 025 0, 33 = 8, 25 10 -3 M


