7 Растворы.ppt
- Количество слайдов: 13
 РАСТВОРЫ Раствор - гомогенная система, состоящая из двух или более компонентов, имеющих молекулярную, ионную или атомную степень раздробленности. 1. ЖИДКИЕ, ТВЕРДЫЕ, ГАЗООБРАЗНЫЕ РАСТВОРЫ N 2, 78% сплав металлов Водный раствор соли O 2, 21% воздух Ar, 0. 96% Au, Ag CO 2, 0. 036% Жидкий раствор: Твердый раствор: Газообразный раствор: молекулярная и ионная степень раздробленности атомная и молекулярная степень раздробленности
РАСТВОРЫ Раствор - гомогенная система, состоящая из двух или более компонентов, имеющих молекулярную, ионную или атомную степень раздробленности. 1. ЖИДКИЕ, ТВЕРДЫЕ, ГАЗООБРАЗНЫЕ РАСТВОРЫ N 2, 78% сплав металлов Водный раствор соли O 2, 21% воздух Ar, 0. 96% Au, Ag CO 2, 0. 036% Жидкий раствор: Твердый раствор: Газообразный раствор: молекулярная и ионная степень раздробленности атомная и молекулярная степень раздробленности
![2. КОНЦЕНТРАЦИЯ РАСТВОРА Молярность М или с [моль/л] равна отношению количества растворенного вещества (n, 2. КОНЦЕНТРАЦИЯ РАСТВОРА Молярность М или с [моль/л] равна отношению количества растворенного вещества (n,](https://present5.com/presentation/20845113_52262710/image-2.jpg) 2. КОНЦЕНТРАЦИЯ РАСТВОРА Молярность М или с [моль/л] равна отношению количества растворенного вещества (n, моль) к объему раствора (V, л): или Молярная доля N (безразмерная величина) – равна отношению количества растворенного вещества ( моль) к суммарному количеству всех веществ ( моль), составляющих раствор: Массовая доля (безразмерная величина) равна отношению массы растворенного вещества (mi кг) к массе раствора ( кг): Массовый процент: 100%
2. КОНЦЕНТРАЦИЯ РАСТВОРА Молярность М или с [моль/л] равна отношению количества растворенного вещества (n, моль) к объему раствора (V, л): или Молярная доля N (безразмерная величина) – равна отношению количества растворенного вещества ( моль) к суммарному количеству всех веществ ( моль), составляющих раствор: Массовая доля (безразмерная величина) равна отношению массы растворенного вещества (mi кг) к массе раствора ( кг): Массовый процент: 100%
 3. ПРИМЕРЫ ВЫЧИСЛЕНИЯ КОНЦЕНТРАЦИИ РАСТВОРА 1) В мерную колбу на 1 литр насыпали m = 34. 23 г сахарозы С 12 Н 22 О 11 (М = 342. 3 г/моль), растворили в воде и добавили воды до метки, соответствующей объему, равному 1 л. Вычислить молярную концентрацию раствора сахарозы Решение
3. ПРИМЕРЫ ВЫЧИСЛЕНИЯ КОНЦЕНТРАЦИИ РАСТВОРА 1) В мерную колбу на 1 литр насыпали m = 34. 23 г сахарозы С 12 Н 22 О 11 (М = 342. 3 г/моль), растворили в воде и добавили воды до метки, соответствующей объему, равному 1 л. Вычислить молярную концентрацию раствора сахарозы Решение
 2) 34. 23 г сахарозы С 12 Н 22 О 11 (М = 342. 3 г/моль), растворили в 180 г воды. Вычислить мольную долю сахарозы и воды в растворе Решение
2) 34. 23 г сахарозы С 12 Н 22 О 11 (М = 342. 3 г/моль), растворили в 180 г воды. Вычислить мольную долю сахарозы и воды в растворе Решение
 3) 34. 23 г сахарозы С 12 Н 22 О 11 (М = 342. 3 г/моль), растворили в 180 г воды. Вычислить массовую долю и процентную долю сахарозы и воды в растворе Решение или 16% сахарозы в водном растворе или 84% воды в водном растворе
3) 34. 23 г сахарозы С 12 Н 22 О 11 (М = 342. 3 г/моль), растворили в 180 г воды. Вычислить массовую долю и процентную долю сахарозы и воды в растворе Решение или 16% сахарозы в водном растворе или 84% воды в водном растворе
 4. ФИЗИЧЕСКИЕ СВОЙСТВА РАСТВОРОВ ЗАКОН РАУЛЯ Давление пара растворителя над раствором равно давлению пара чистого растворителя, умноженному на мольную долю растворителя в растворе Характер изменения давления водяного пара P 1 над раствором нелетучего вещества (например, Na. Cl) N 1 -мольная доля растворителя (воды) Р 1 – давление водяного пара над раствором о Р 1 – 0 N 1 1 давление водяного пара над чистым растворителем
4. ФИЗИЧЕСКИЕ СВОЙСТВА РАСТВОРОВ ЗАКОН РАУЛЯ Давление пара растворителя над раствором равно давлению пара чистого растворителя, умноженному на мольную долю растворителя в растворе Характер изменения давления водяного пара P 1 над раствором нелетучего вещества (например, Na. Cl) N 1 -мольная доля растворителя (воды) Р 1 – давление водяного пара над раствором о Р 1 – 0 N 1 1 давление водяного пара над чистым растворителем
 ОПЫТЫ ПОДТВЕРЖДАЮЩИЕ ЗАКОН РАУЛЯ Р 1>P 2 Р 1 Р 2 Низкая концентрация соли в водном растворе – высокое давление водяного пара Высокая концентрация соли в водном растворе – низкое давление водяного пара
ОПЫТЫ ПОДТВЕРЖДАЮЩИЕ ЗАКОН РАУЛЯ Р 1>P 2 Р 1 Р 2 Низкая концентрация соли в водном растворе – высокое давление водяного пара Высокая концентрация соли в водном растворе – низкое давление водяного пара
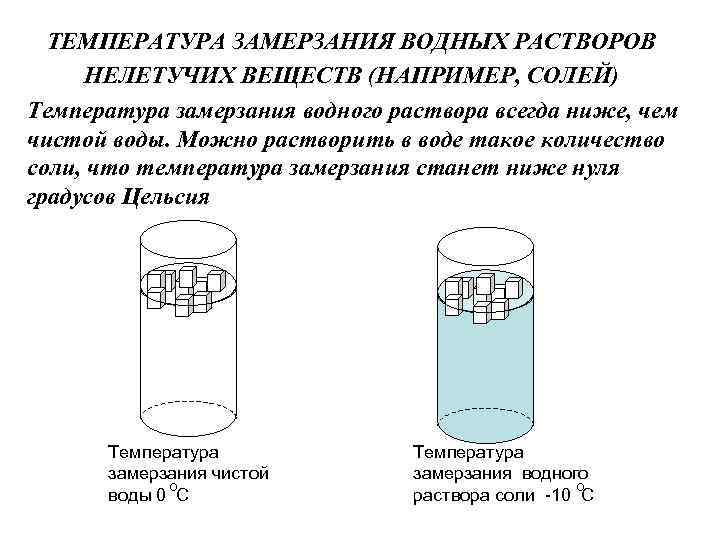 ТЕМПЕРАТУРА ЗАМЕРЗАНИЯ ВОДНЫХ РАСТВОРОВ НЕЛЕТУЧИХ ВЕЩЕСТВ (НАПРИМЕР, СОЛЕЙ) Температура замерзания водного раствора всегда ниже, чем чистой воды. Можно растворить в воде такое количество соли, что температура замерзания станет ниже нуля градусов Цельсия Температура замерзания чистой о воды 0 С Температура замерзания водного о раствора соли -10 С
ТЕМПЕРАТУРА ЗАМЕРЗАНИЯ ВОДНЫХ РАСТВОРОВ НЕЛЕТУЧИХ ВЕЩЕСТВ (НАПРИМЕР, СОЛЕЙ) Температура замерзания водного раствора всегда ниже, чем чистой воды. Можно растворить в воде такое количество соли, что температура замерзания станет ниже нуля градусов Цельсия Температура замерзания чистой о воды 0 С Температура замерзания водного о раствора соли -10 С
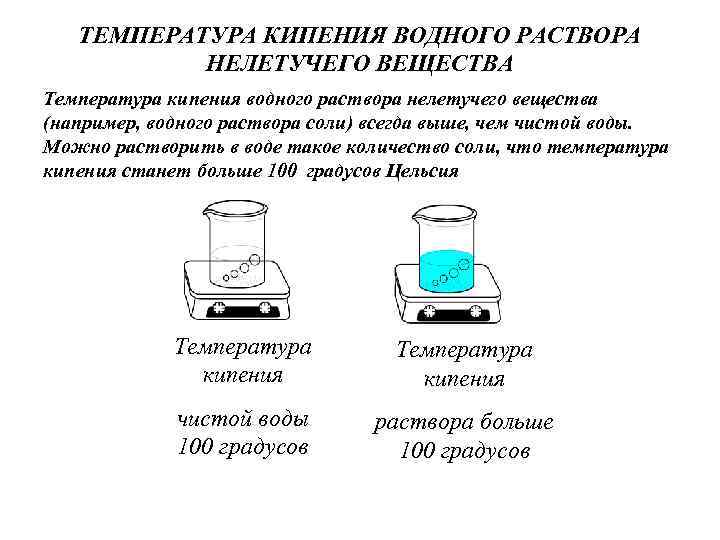 ТЕМПЕРАТУРА КИПЕНИЯ ВОДНОГО РАСТВОРА НЕЛЕТУЧЕГО ВЕЩЕСТВА Температура кипения водного раствора нелетучего вещества (например, водного раствора соли) всегда выше, чем чистой воды. Можно растворить в воде такое количество соли, что температура кипения станет больше 100 градусов Цельсия Температура кипения чистой воды 100 градусов раствора больше 100 градусов
ТЕМПЕРАТУРА КИПЕНИЯ ВОДНОГО РАСТВОРА НЕЛЕТУЧЕГО ВЕЩЕСТВА Температура кипения водного раствора нелетучего вещества (например, водного раствора соли) всегда выше, чем чистой воды. Можно растворить в воде такое количество соли, что температура кипения станет больше 100 градусов Цельсия Температура кипения чистой воды 100 градусов раствора больше 100 градусов
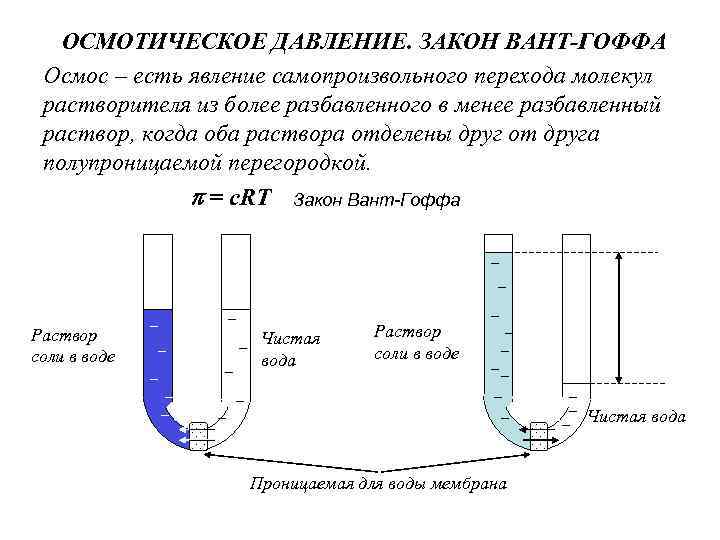 ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ. ЗАКОН ВАНТ-ГОФФА Осмос – есть явление самопроизвольного перехода молекул растворителя из более разбавленного в менее разбавленный раствор, когда оба раствора отделены друг от друга полупроницаемой перегородкой. = с. RT Закон Вант-Гоффа Раствор соли в воде Чистая вода Проницаемая для воды мембрана
ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ. ЗАКОН ВАНТ-ГОФФА Осмос – есть явление самопроизвольного перехода молекул растворителя из более разбавленного в менее разбавленный раствор, когда оба раствора отделены друг от друга полупроницаемой перегородкой. = с. RT Закон Вант-Гоффа Раствор соли в воде Чистая вода Проницаемая для воды мембрана
 РАСТВОРИМОСТЬ ГАЗОВ В ВОДЕ 1) С увеличением температуры растворимость газов в воде уменьшается. о Растворимость О 2 в воде при парциальном давлении, соответствующем его содержанию в атмосфере Т С S мг/л 0 5 14. 7 12. 8 10 11. 3 15 10. 2 20 9. 2 25 8. 4 29 7. 6 2) С увеличением давления растворимость газов в воде увеличивается. Закон Генри: N = K p где N – молярная доля газа в водном растворе; К – коэффициент пропорциональности; р – парциальное давление газа над раствором Растворимость газа в жидкости прямо пропорционально давлению газа над жидкостью
РАСТВОРИМОСТЬ ГАЗОВ В ВОДЕ 1) С увеличением температуры растворимость газов в воде уменьшается. о Растворимость О 2 в воде при парциальном давлении, соответствующем его содержанию в атмосфере Т С S мг/л 0 5 14. 7 12. 8 10 11. 3 15 10. 2 20 9. 2 25 8. 4 29 7. 6 2) С увеличением давления растворимость газов в воде увеличивается. Закон Генри: N = K p где N – молярная доля газа в водном растворе; К – коэффициент пропорциональности; р – парциальное давление газа над раствором Растворимость газа в жидкости прямо пропорционально давлению газа над жидкостью
 РАСТВОРИМОСТЬ ТВЕРДЫХ ВЕЩЕСТВ В ВОДЕ Растворимость твердых веществ в воде с увеличением температуры увеличивается S г/100 г Н 2 О 100 Ca. Cl 2 80 Mg. Cl 2 60 Na. Cl 40 20 Na 2 SO 4 0 0 10 20 30 о С
РАСТВОРИМОСТЬ ТВЕРДЫХ ВЕЩЕСТВ В ВОДЕ Растворимость твердых веществ в воде с увеличением температуры увеличивается S г/100 г Н 2 О 100 Ca. Cl 2 80 Mg. Cl 2 60 Na. Cl 40 20 Na 2 SO 4 0 0 10 20 30 о С
 Т 0 С Область раствора 16 0 14 0 12 0 10 0 80 Область двухфазной системы соль – раствор 60 40 Область двухфазной системы лед – раствор f а 20 b 2 d Область двухфазной системы соль – лед с 4 0 10 100 Н 2 О 20 30 40 50 c. Na. Cl, масс. % 60 70 80 90 Na. Cl
Т 0 С Область раствора 16 0 14 0 12 0 10 0 80 Область двухфазной системы соль – раствор 60 40 Область двухфазной системы лед – раствор f а 20 b 2 d Область двухфазной системы соль – лед с 4 0 10 100 Н 2 О 20 30 40 50 c. Na. Cl, масс. % 60 70 80 90 Na. Cl


