9. Физика_термодинамика растворов-1.ppt
- Количество слайдов: 16
 Растворы полимеров Термодинамика растворов
Растворы полимеров Термодинамика растворов
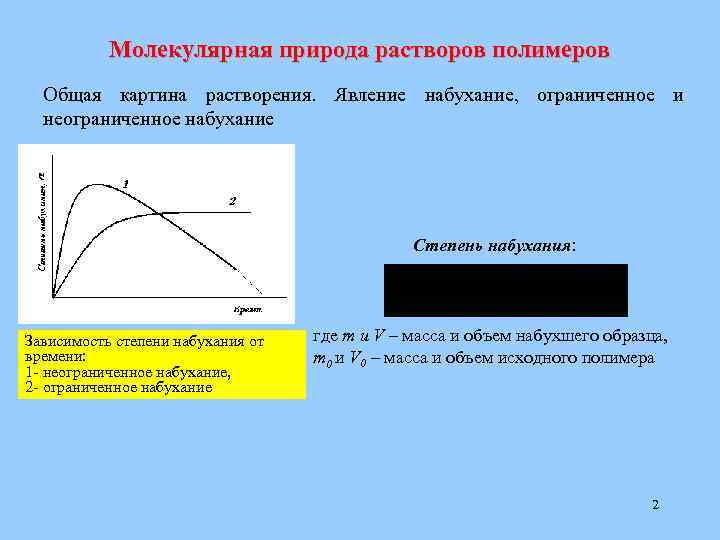 Молекулярная природа растворов полимеров Общая картина растворения. Явление набухание, ограниченное и неограниченное набухание Степень набухания: где m и V – масса и объем набухшего образца, Зависимость степени набухания от времени: 0 и V 0 – масса и объем исходного полимера m 1 - неограниченное набухание, 2 - ограниченное набухание 2
Молекулярная природа растворов полимеров Общая картина растворения. Явление набухание, ограниченное и неограниченное набухание Степень набухания: где m и V – масса и объем набухшего образца, Зависимость степени набухания от времени: 0 и V 0 – масса и объем исходного полимера m 1 - неограниченное набухание, 2 - ограниченное набухание 2
 Растворы полимеров являются истинными молекулярными растворами. Критерии истинности раствора: - термодинамическая устойчивость и и применимость правила фаз, - самопроизвольность образования, - постоянство концентрации во времени, - однофазность. выраженную способность к неравновесности (влияние на свойства раствора способа изготовления, термической предыстории и др. ). Причины неравновесности связаны с длительностью перехода к равновесному состоянию. В некоторых случаях равновесное состояние не достигается в связи с существованием больших энергетических барьеров. 3
Растворы полимеров являются истинными молекулярными растворами. Критерии истинности раствора: - термодинамическая устойчивость и и применимость правила фаз, - самопроизвольность образования, - постоянство концентрации во времени, - однофазность. выраженную способность к неравновесности (влияние на свойства раствора способа изготовления, термической предыстории и др. ). Причины неравновесности связаны с длительностью перехода к равновесному состоянию. В некоторых случаях равновесное состояние не достигается в связи с существованием больших энергетических барьеров. 3
 Простейшие диаграммы состояния растворов полимеров Применимость правила фаз к растворам полимеров: Ф = n 2 r, где Ф –количество степеней свободы, n – количество компонентов, r – количество фаз. При P сonst, Ф = n 1 r Предел совместимости – максимальное количество растворителя, которое можно ввести в полимер без изменения однофазного состояния. Бинодаль (бинодальная кривая) – геометрическое мест точек, характеризующих составы сосуществующих фаз. Типичные диаграммы состояния систем полимер – растворитель: 1 - область однофазных растворов, 2 - область двухфазных растворов, 4
Простейшие диаграммы состояния растворов полимеров Применимость правила фаз к растворам полимеров: Ф = n 2 r, где Ф –количество степеней свободы, n – количество компонентов, r – количество фаз. При P сonst, Ф = n 1 r Предел совместимости – максимальное количество растворителя, которое можно ввести в полимер без изменения однофазного состояния. Бинодаль (бинодальная кривая) – геометрическое мест точек, характеризующих составы сосуществующих фаз. Типичные диаграммы состояния систем полимер – растворитель: 1 - область однофазных растворов, 2 - область двухфазных растворов, 4
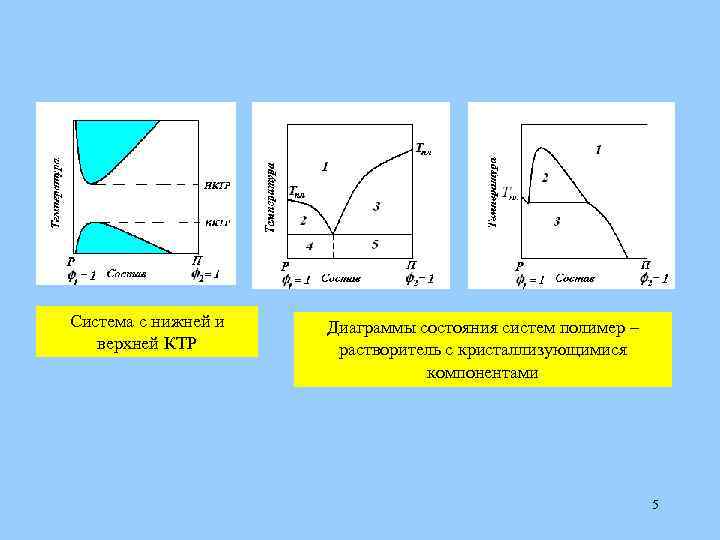 Система с нижней и верхней КТР Диаграммы состояния систем полимер – растворитель с кристаллизующимися компонентами 5
Система с нижней и верхней КТР Диаграммы состояния систем полимер – растворитель с кристаллизующимися компонентами 5
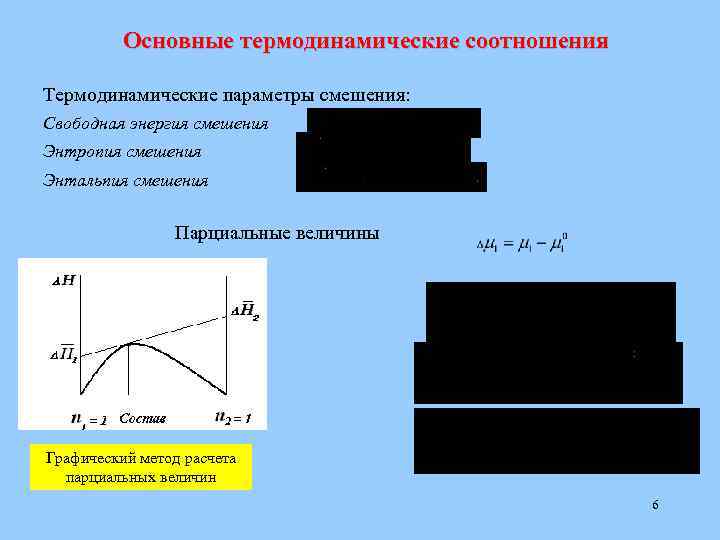 Основные термодинамические соотношения Термодинамические параметры смешения: Свободная энергия смешения Энтропия смешения Энтальпия смешения Парциальные величины Графический метод расчета парциальных величин 6
Основные термодинамические соотношения Термодинамические параметры смешения: Свободная энергия смешения Энтропия смешения Энтальпия смешения Парциальные величины Графический метод расчета парциальных величин 6
 Условия самопроизвольного растворения 7
Условия самопроизвольного растворения 7
 Факторы, влияющие на тепловой эффект растворения Величина HМ определяется соотношением величин энергий межмолекулярного взаимодействия: НМ = к (Е 1 -1 +Е 2 -2 2 Е 1 -2) 2 Е 1 -2 > Е 1 -1 +Е 2 -2 HM 0 2 Е 1 -2 < Е 1 -1 +Е 2 -2 2 Е 1 -2 Е 1 -1 +Е 2 -2 H M 0 HM 0 - экзотермическое растворение - эндотермическое растворение - атермическое растворение 8
Факторы, влияющие на тепловой эффект растворения Величина HМ определяется соотношением величин энергий межмолекулярного взаимодействия: НМ = к (Е 1 -1 +Е 2 -2 2 Е 1 -2) 2 Е 1 -2 > Е 1 -1 +Е 2 -2 HM 0 2 Е 1 -2 < Е 1 -1 +Е 2 -2 2 Е 1 -2 Е 1 -1 +Е 2 -2 H M 0 HM 0 - экзотермическое растворение - эндотермическое растворение - атермическое растворение 8
 Теория регулярных растворов Модель регулярного раствора Гильдебранда: Н 0, отсутствие ассоциации компонентов и их случайное распределение в объеме, отсутствие объемных эффектов. где. V – мольный объем раствора, 1 и 2 – объемные доли компонентов, Е 10 , Е 20, и V 1, V 2 - энергия межмолекулярного взаимодействия и мольный объем компонентов. 9
Теория регулярных растворов Модель регулярного раствора Гильдебранда: Н 0, отсутствие ассоциации компонентов и их случайное распределение в объеме, отсутствие объемных эффектов. где. V – мольный объем раствора, 1 и 2 – объемные доли компонентов, Е 10 , Е 20, и V 1, V 2 - энергия межмолекулярного взаимодействия и мольный объем компонентов. 9
 Параметры растворимости Важное следствие из теории регулярных растворов: Условие максимального энергетического сродства компонентов раствора (минимум Н) выполняется при равенстве величин параметров растворимости (В 0). «Подобное растворяется в подобном» Параметр растворимости (параметр растворимости Гильдебранда) и плотность энергии когезии являются важными физико-химическими характеристиками веществ, отражающими влияние строения молекул на величину энергии межмолекулярного взаимодействия. 10
Параметры растворимости Важное следствие из теории регулярных растворов: Условие максимального энергетического сродства компонентов раствора (минимум Н) выполняется при равенстве величин параметров растворимости (В 0). «Подобное растворяется в подобном» Параметр растворимости (параметр растворимости Гильдебранда) и плотность энергии когезии являются важными физико-химическими характеристиками веществ, отражающими влияние строения молекул на величину энергии межмолекулярного взаимодействия. 10
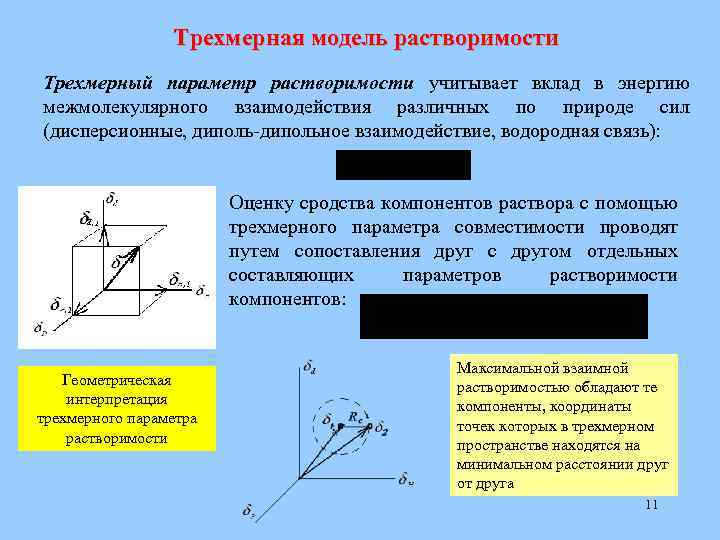 Трехмерная модель растворимости Трехмерный параметр растворимости учитывает вклад в энергию межмолекулярного взаимодействия различных по природе сил (дисперсионные, диполь-дипольное взаимодействие, водородная связь): Оценку сродства компонентов раствора с помощью трехмерного параметра совместимости проводят путем сопоставления друг с другом отдельных составляющих параметров растворимости компонентов: Геометрическая интерпретация трехмерного параметра растворимости Максимальной взаимной растворимостью обладают те компоненты, координаты точек которых в трехмерном пространстве находятся на минимальном расстоянии друг от друга 11
Трехмерная модель растворимости Трехмерный параметр растворимости учитывает вклад в энергию межмолекулярного взаимодействия различных по природе сил (дисперсионные, диполь-дипольное взаимодействие, водородная связь): Оценку сродства компонентов раствора с помощью трехмерного параметра совместимости проводят путем сопоставления друг с другом отдельных составляющих параметров растворимости компонентов: Геометрическая интерпретация трехмерного параметра растворимости Максимальной взаимной растворимостью обладают те компоненты, координаты точек которых в трехмерном пространстве находятся на минимальном расстоянии друг от друга 11
 Двухмерная модель растворимости Так как дисперсионные составляющие параметра растворимости различных веществ практически одинаковы, то можно пренебречь третьим членом уравнения для Rc: Вещества, находящиеся в плоской модели на одинаковом расстоянии друг от друга (сравниваемые пары имеют одинаковое значение Rc), характеризуются близким по величине энергетическим взаимодействием. 12
Двухмерная модель растворимости Так как дисперсионные составляющие параметра растворимости различных веществ практически одинаковы, то можно пренебречь третьим членом уравнения для Rc: Вещества, находящиеся в плоской модели на одинаковом расстоянии друг от друга (сравниваемые пары имеют одинаковое значение Rc), характеризуются близким по величине энергетическим взаимодействием. 12
 Методы определения параметров растворимости Параметр растворимости Гильдебранда можно рассчитать с помощью соотношения: где Е 0= Н 0 RT, Н 0 – скрытая энтальпия испарения. Этот способ расчета применим только для низкомолекулярных веществ. Величину Е 0 можно рассчитать по данным о температуре кипения вещества с помощью эмпирических уравнений вида: - Е 0 = 23, 7 Ткип + 0, 02 Т 2 кип – 2950 13
Методы определения параметров растворимости Параметр растворимости Гильдебранда можно рассчитать с помощью соотношения: где Е 0= Н 0 RT, Н 0 – скрытая энтальпия испарения. Этот способ расчета применим только для низкомолекулярных веществ. Величину Е 0 можно рассчитать по данным о температуре кипения вещества с помощью эмпирических уравнений вида: - Е 0 = 23, 7 Ткип + 0, 02 Т 2 кип – 2950 13
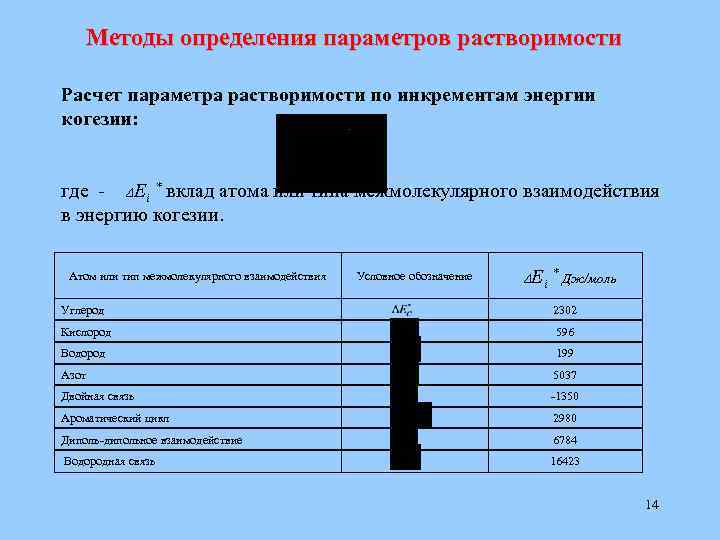 Методы определения параметров растворимости Расчет параметра растворимости по инкрементам энергии когезии: где - Еi * вклад атома или типа межмолекулярного взаимодействия в энергию когезии. Атом или тип межмолекулярного взаимодействия Условное обозначение Еi * Дж/моль Углерод 2302 Кислород 596 Водород 199 Азот 5037 Двойная связь -1350 Ароматический цикл 2980 Диполь-дипольное взаимодействие 6784 Водородная связь 16423 14
Методы определения параметров растворимости Расчет параметра растворимости по инкрементам энергии когезии: где - Еi * вклад атома или типа межмолекулярного взаимодействия в энергию когезии. Атом или тип межмолекулярного взаимодействия Условное обозначение Еi * Дж/моль Углерод 2302 Кислород 596 Водород 199 Азот 5037 Двойная связь -1350 Ароматический цикл 2980 Диполь-дипольное взаимодействие 6784 Водородная связь 16423 14
 Методы определения параметров растворимости Расчет полярной и Н-составляющих параметра растворимости: 15
Методы определения параметров растворимости Расчет полярной и Н-составляющих параметра растворимости: 15
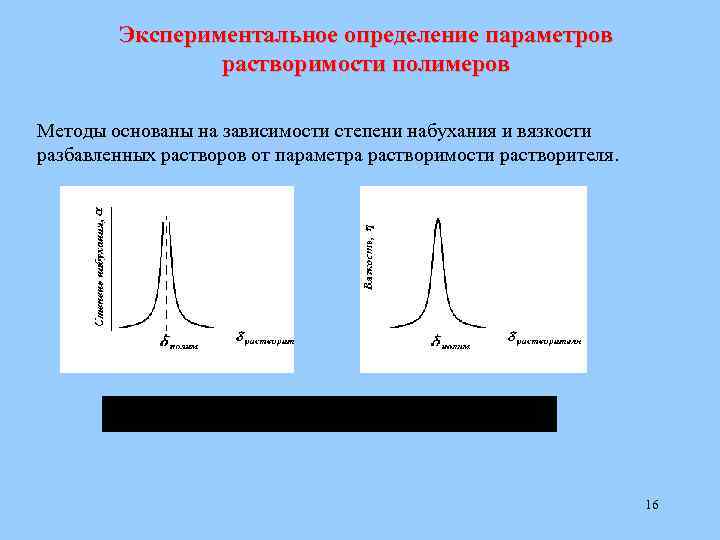 Экспериментальное определение параметров растворимости полимеров Методы основаны на зависимости степени набухания и вязкости разбавленных растворов от параметра растворимости растворителя. 16
Экспериментальное определение параметров растворимости полимеров Методы основаны на зависимости степени набухания и вязкости разбавленных растворов от параметра растворимости растворителя. 16


