10. Термодинамика растворов-2.ppt
- Количество слайдов: 16
 Растворы полимеров Термодинамика растворов ч. 2
Растворы полимеров Термодинамика растворов ч. 2
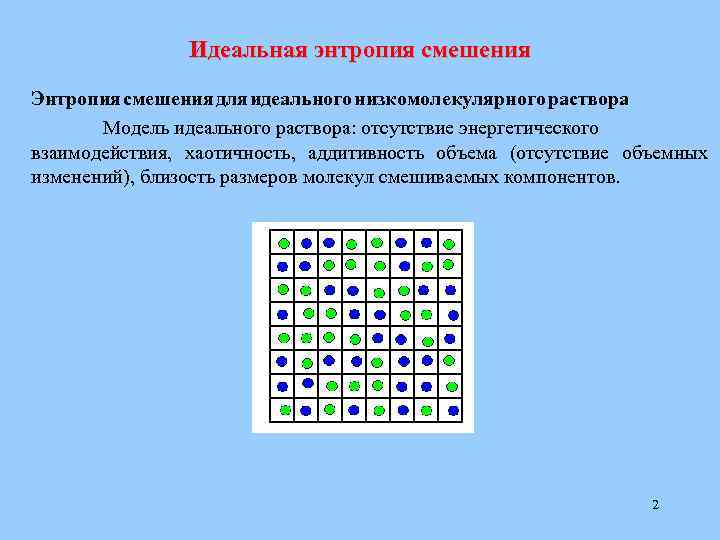 Идеальная энтропия смешения Энтропия смешения для идеального низкомолекулярного раствора Модель идеального раствора: отсутствие энергетического взаимодействия, хаотичность, аддитивность объема (отсутствие объемных изменений), близость размеров молекул смешиваемых компонентов. 2
Идеальная энтропия смешения Энтропия смешения для идеального низкомолекулярного раствора Модель идеального раствора: отсутствие энергетического взаимодействия, хаотичность, аддитивность объема (отсутствие объемных изменений), близость размеров молекул смешиваемых компонентов. 2
 3
3
 4
4
 Теория Флори – Хаггинса Модель раствора. Раствор является регулярным, а звенья цепей распределены равномерно по объему. В каждой ячейке квазикристаллической решетки может находится либо молекула растворителя, либо сегмент макромолекулы. Объем сегмента равен объему молекулы растворителя. Объем смешения Vсм = 0. Решеточная модель раствора Общее количество ячеек в решетке равно N 1+r. N 2 , где N 1= n 1 NA , N 2= n 2 NA , n 1 и n 2 – число молей молекул растворителя и полимера; - степень полимеризации (число сегментов) цепи. Каждая ячейка окружена определенным числом ближайших ячеек (координационное число Z). Доля ячеек, занятых молекулами полимера: , где - i молекул N 2. Рассмотрим число возможных способов размещения молекулы, последовательно заполняя ячейки сегментами. Первый сегмент может быть помещен в любую свободную ячейку, т. е. способами. Второй сегмент необходимо поместить в одну из Z ячеек, окружающих первый сегмент. Третий сегмент необходимо поместить в Z-1 ячейку из окружающих второй сегмент. Число способов размещения всех остальных сегментов цепи, начиная с третьего не 5 изменяется и равно , где y не зависит от гибкости цепи.
Теория Флори – Хаггинса Модель раствора. Раствор является регулярным, а звенья цепей распределены равномерно по объему. В каждой ячейке квазикристаллической решетки может находится либо молекула растворителя, либо сегмент макромолекулы. Объем сегмента равен объему молекулы растворителя. Объем смешения Vсм = 0. Решеточная модель раствора Общее количество ячеек в решетке равно N 1+r. N 2 , где N 1= n 1 NA , N 2= n 2 NA , n 1 и n 2 – число молей молекул растворителя и полимера; - степень полимеризации (число сегментов) цепи. Каждая ячейка окружена определенным числом ближайших ячеек (координационное число Z). Доля ячеек, занятых молекулами полимера: , где - i молекул N 2. Рассмотрим число возможных способов размещения молекулы, последовательно заполняя ячейки сегментами. Первый сегмент может быть помещен в любую свободную ячейку, т. е. способами. Второй сегмент необходимо поместить в одну из Z ячеек, окружающих первый сегмент. Третий сегмент необходимо поместить в Z-1 ячейку из окружающих второй сегмент. Число способов размещения всех остальных сегментов цепи, начиная с третьего не 5 изменяется и равно , где y не зависит от гибкости цепи.
 Число способов размещения макромолекулы в решетке пропорционально произведению чисел способов размещения последовательно связанных сегментов: . Множитель ½ вводится в связи с тем, что концы макромолекулы неразличимы, а при данном способе расчета каждая макромолекула помещается в решетку два раза, начиная с одного и другого конца. После заполнения ячеек молекулами полимера на оставшиеся места (свободные ячейки) помещаются молекулы растворителя. Так как молекулы растворителя не отличаются друг от друга, имеется лишь один способ их размещения. В итоге общее число возможных вариантов размещения сегментов в растворе, т. е. Число микросостояний выразится произведением: Член введен для того, чтобы учесть перестановки макромолекул между собой, которые не влияют на W. После логарифмирования последнего уравнения и преобразований с использованием уравнения Стирлинга получаем: 6
Число способов размещения макромолекулы в решетке пропорционально произведению чисел способов размещения последовательно связанных сегментов: . Множитель ½ вводится в связи с тем, что концы макромолекулы неразличимы, а при данном способе расчета каждая макромолекула помещается в решетку два раза, начиная с одного и другого конца. После заполнения ячеек молекулами полимера на оставшиеся места (свободные ячейки) помещаются молекулы растворителя. Так как молекулы растворителя не отличаются друг от друга, имеется лишь один способ их размещения. В итоге общее число возможных вариантов размещения сегментов в растворе, т. е. Число микросостояний выразится произведением: Член введен для того, чтобы учесть перестановки макромолекул между собой, которые не влияют на W. После логарифмирования последнего уравнения и преобразований с использованием уравнения Стирлинга получаем: 6
 Так как Уравнение для свободной энергии смешения Для учета энергетического взаимодействия вводится полуэмпирический параметр 1 (параметр взаимодействия Флори - Хаггинса): 1 равен энергии, необходимой для переноса одной молекулы или одного моля растворителя из чистого растворителя в полимер, отнесенной к тепловой энергии k. T или RT. С учетом этого, Для парциальной свободной энергии смешения 7
Так как Уравнение для свободной энергии смешения Для учета энергетического взаимодействия вводится полуэмпирический параметр 1 (параметр взаимодействия Флори - Хаггинса): 1 равен энергии, необходимой для переноса одной молекулы или одного моля растворителя из чистого растворителя в полимер, отнесенной к тепловой энергии k. T или RT. С учетом этого, Для парциальной свободной энергии смешения 7
 Виды уравнений Флори- Хаггинса 8
Виды уравнений Флори- Хаггинса 8
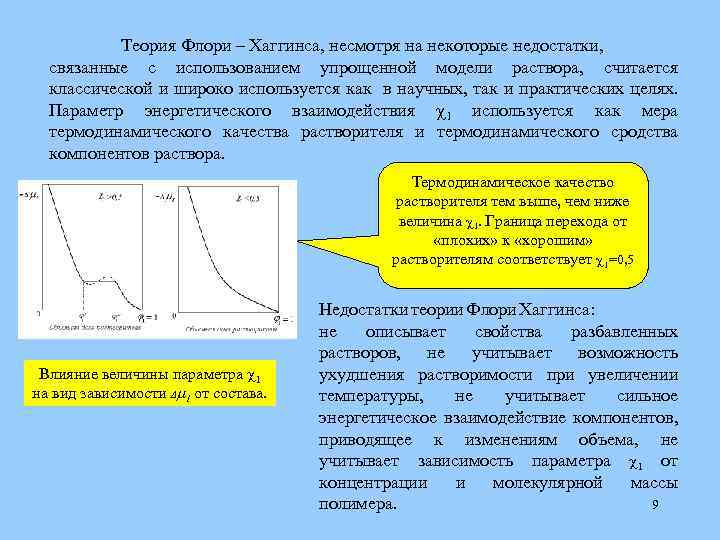 Теория Флори – Хаггинса, несмотря на некоторые недостатки, связанные с использованием упрощенной модели раствора, считается классической и широко используется как в научных, так и практических целях. Параметр энергетического взаимодействия 1 используется как мера термодинамического качества растворителя и термодинамического сродства компонентов раствора. Термодинамическое качество растворителя тем выше, чем ниже величина 1. Граница перехода от «плохих» к «хорошим» растворителям соответствует 1=0, 5 Влияние величины параметра 1 на вид зависимости 1 от состава. Недостатки теории Флори Хаггинса: не описывает свойства разбавленных растворов, не учитывает возможность ухудшения растворимости при увеличении температуры, не учитывает сильное энергетическое взаимодействие компонентов, приводящее к изменениям объема, не учитывает зависимость параметра 1 от концентрации и молекулярной массы 9 полимера.
Теория Флори – Хаггинса, несмотря на некоторые недостатки, связанные с использованием упрощенной модели раствора, считается классической и широко используется как в научных, так и практических целях. Параметр энергетического взаимодействия 1 используется как мера термодинамического качества растворителя и термодинамического сродства компонентов раствора. Термодинамическое качество растворителя тем выше, чем ниже величина 1. Граница перехода от «плохих» к «хорошим» растворителям соответствует 1=0, 5 Влияние величины параметра 1 на вид зависимости 1 от состава. Недостатки теории Флори Хаггинса: не описывает свойства разбавленных растворов, не учитывает возможность ухудшения растворимости при увеличении температуры, не учитывает сильное энергетическое взаимодействие компонентов, приводящее к изменениям объема, не учитывает зависимость параметра 1 от концентрации и молекулярной массы 9 полимера.
 Теория набухания сетчатых полимеров Набухание сетчатого полимера в растворителе сопровождается, как и в случае линейного полимера, возрастанием энтропии смешения. Одновременно с этим, в результате увеличения объема сетки и расстояния между её узлами, происходит уменьшение эластической составляющей энтропии: Д ля парциальной свободной энергии смешения: где 2 –плотность полимера, - парциальный объем растворителя, f – функциональность сетки. Уравнение Флори - Ренера 10
Теория набухания сетчатых полимеров Набухание сетчатого полимера в растворителе сопровождается, как и в случае линейного полимера, возрастанием энтропии смешения. Одновременно с этим, в результате увеличения объема сетки и расстояния между её узлами, происходит уменьшение эластической составляющей энтропии: Д ля парциальной свободной энергии смешения: где 2 –плотность полимера, - парциальный объем растворителя, f – функциональность сетки. Уравнение Флори - Ренера 10
 Уравнение Флори – Ренера для активности растворителя: В некоторых случаях формирование пространственной сетки проводят путем сшивания линейного полимера в растворе. Полученные таким образом сетки, содержащие растворитель, называют сетками второго типа ( в отличие от сеток первого типа, не содержащих растворитель). Набухание сеток 2 типа описывается уравнением Флори – Ренера, содержащим поправку на количество растворителя, присутствовавшего в растворе в момент сшивания макромолекул: 11
Уравнение Флори – Ренера для активности растворителя: В некоторых случаях формирование пространственной сетки проводят путем сшивания линейного полимера в растворе. Полученные таким образом сетки, содержащие растворитель, называют сетками второго типа ( в отличие от сеток первого типа, не содержащих растворитель). Набухание сеток 2 типа описывается уравнением Флори – Ренера, содержащим поправку на количество растворителя, присутствовавшего в растворе в момент сшивания макромолекул: 11
 Основные следствия из уравнения Флори - Ренера: - набухание сетчатого полимера всегда ограниченно, - степень набухания сетчатого полимера зависит от термодинамического сродства компонентов и плотности сетки, - увеличение плотности сетки приводит к уменьшению степени набухания. Метод Флори – Ренера для измерения плотности сетки Образец сетчатого полимера подвергают набуханию в избытке растворителя. После завершения набухания весовым или объемным методом измеряют равновесную степень набухания, и рассчитывают состав набухшего сетчатого полимера. При термодинамическом равновесии фазы набухшего полимера с фазой свободного растворителя 1=0. Приравнивают правую часть уравнения Флори - Ренера нулю: По известным значениям 1, 2, f и экспериментально измеренному значению 2 рассчитывают величину Мс. 12
Основные следствия из уравнения Флори - Ренера: - набухание сетчатого полимера всегда ограниченно, - степень набухания сетчатого полимера зависит от термодинамического сродства компонентов и плотности сетки, - увеличение плотности сетки приводит к уменьшению степени набухания. Метод Флори – Ренера для измерения плотности сетки Образец сетчатого полимера подвергают набуханию в избытке растворителя. После завершения набухания весовым или объемным методом измеряют равновесную степень набухания, и рассчитывают состав набухшего сетчатого полимера. При термодинамическом равновесии фазы набухшего полимера с фазой свободного растворителя 1=0. Приравнивают правую часть уравнения Флори - Ренера нулю: По известным значениям 1, 2, f и экспериментально измеренному значению 2 рассчитывают величину Мс. 12
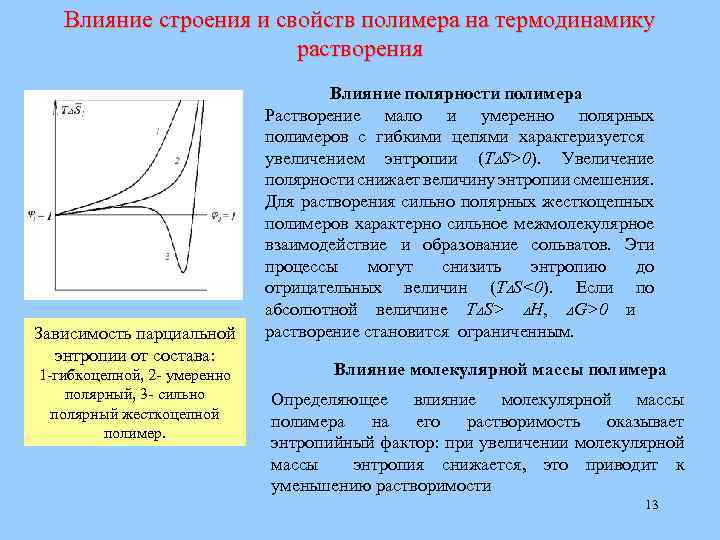 Влияние строения и свойств полимера на термодинамику растворения Зависимость парциальной энтропии от состава: 1 -гибкоцепной, 2 - умеренно полярный, 3 - сильно полярный жесткоцепной полимер. Влияние полярности полимера Растворение мало и умеренно полярных полимеров с гибкими цепями характеризуется увеличением энтропии (Т S>0). Увеличение полярности снижает величину энтропии смешения. Для растворения сильно полярных жесткоцепных полимеров характерно сильное межмолекулярное взаимодействие и образование сольватов. Эти процессы могут снизить энтропию до отрицательных величин (Т S<0). Если по абсолютной величине Т S> H, G>0 и растворение становится ограниченным. Влияние молекулярной массы полимера Определяющее влияние молекулярной массы полимера на его растворимость оказывает энтропийный фактор: при увеличении молекулярной массы энтропия снижается, это приводит к уменьшению растворимости 13
Влияние строения и свойств полимера на термодинамику растворения Зависимость парциальной энтропии от состава: 1 -гибкоцепной, 2 - умеренно полярный, 3 - сильно полярный жесткоцепной полимер. Влияние полярности полимера Растворение мало и умеренно полярных полимеров с гибкими цепями характеризуется увеличением энтропии (Т S>0). Увеличение полярности снижает величину энтропии смешения. Для растворения сильно полярных жесткоцепных полимеров характерно сильное межмолекулярное взаимодействие и образование сольватов. Эти процессы могут снизить энтропию до отрицательных величин (Т S<0). Если по абсолютной величине Т S> H, G>0 и растворение становится ограниченным. Влияние молекулярной массы полимера Определяющее влияние молекулярной массы полимера на его растворимость оказывает энтропийный фактор: при увеличении молекулярной массы энтропия снижается, это приводит к уменьшению растворимости 13
 Растворение кристаллических полимеров Растворение кристалла сопровождается разрушением (плавлением) кристаллической решетки. На разрушение кристаллической решетки затрачивается энергия, равная теплоте плавления. Парциальная энтальпия растворения является суммой энтальпий плавления и смешения: Первый член этого уравнения всегда положителен, а второй может иметь разные знаки. Изменение энтропии также зависит от соотношения величин энтропии плавления и энтропии смешения. При растворении кристаллических полимеров определяющее значение имеет энергетическое взаимодействие растворителя с полимером и температура растворения. Увеличение температуры повышению растворимости кристаллических полимеров. Зависимость температуры плавления полимера от концентрации раствора имеет вид: где и - температура плавления в растворе и равновесная температура плавления полимера, V 2 и V 1 - молярные объемы мономерного звена полимера и растворителя, H - энтальпия плавления полимера. Из этого уравнения видно, что растворимость полимера зависит от термодинамического сродства компонентов, 14 температуры и энтальпии плавления.
Растворение кристаллических полимеров Растворение кристалла сопровождается разрушением (плавлением) кристаллической решетки. На разрушение кристаллической решетки затрачивается энергия, равная теплоте плавления. Парциальная энтальпия растворения является суммой энтальпий плавления и смешения: Первый член этого уравнения всегда положителен, а второй может иметь разные знаки. Изменение энтропии также зависит от соотношения величин энтропии плавления и энтропии смешения. При растворении кристаллических полимеров определяющее значение имеет энергетическое взаимодействие растворителя с полимером и температура растворения. Увеличение температуры повышению растворимости кристаллических полимеров. Зависимость температуры плавления полимера от концентрации раствора имеет вид: где и - температура плавления в растворе и равновесная температура плавления полимера, V 2 и V 1 - молярные объемы мономерного звена полимера и растворителя, H - энтальпия плавления полимера. Из этого уравнения видно, что растворимость полимера зависит от термодинамического сродства компонентов, 14 температуры и энтальпии плавления.
 Фазовое равновесие в растворах полимеров. Самопроизвольно образующийся раствор может быть однофазным или двухфазным. При образовании однофазного раствора во всей области составов (неограниченная совместимость компонентов) зависимость от состава раствора имеет вид монотонной вогнутой кривой, расположенной в области отрицательных значений (кривая 3). В этом случае Зависимость изменения свободной энергии от состава : 1 и 2 – ограниченная растворимость, 3 – неограниченная растворимость, 4 - бинодаль, 5 – спинодаль Если зависимость G от состава имеет переменный знак кривизны (кривые 1 и 2), то раствор, в соответствии с требованием минимизации свободной энергии, разделяется на две фазы. Состав этих фаз определяется общими точками вогнутых участков кривой и касательной, проведенной к вогнутым участкам. Так как , то составы, соответствующие точкам минимумов , имеют одинаковое значение химических потенциалов (условие равновесия фаз). 15
Фазовое равновесие в растворах полимеров. Самопроизвольно образующийся раствор может быть однофазным или двухфазным. При образовании однофазного раствора во всей области составов (неограниченная совместимость компонентов) зависимость от состава раствора имеет вид монотонной вогнутой кривой, расположенной в области отрицательных значений (кривая 3). В этом случае Зависимость изменения свободной энергии от состава : 1 и 2 – ограниченная растворимость, 3 – неограниченная растворимость, 4 - бинодаль, 5 – спинодаль Если зависимость G от состава имеет переменный знак кривизны (кривые 1 и 2), то раствор, в соответствии с требованием минимизации свободной энергии, разделяется на две фазы. Состав этих фаз определяется общими точками вогнутых участков кривой и касательной, проведенной к вогнутым участкам. Так как , то составы, соответствующие точкам минимумов , имеют одинаковое значение химических потенциалов (условие равновесия фаз). 15
 Система термодинамически стабильна в областях концентраций левее и правее точек минимумов. В этих областях кривая вогнута и. Геометрическое место точек, соответствующих положению минимумов при различных температурах, образует пограничную кривую – бинодаль, разделяющую области однофазных устойчивых и двухфазных термодинамически неустойчивых растворов. Внутри бинодальной кривой находится спинодаль – геометрическое место точек перегибов (b) на зависимостях G. Область внутри спинодали – область абсолютно неустойчивых растворов. Между бинодалью и спинодалью находится область метастабильных растворов. Фазовый распад в метастабильной области может быть заторможен в связи с малой скоростью образования зародышей новых фаз 16
Система термодинамически стабильна в областях концентраций левее и правее точек минимумов. В этих областях кривая вогнута и. Геометрическое место точек, соответствующих положению минимумов при различных температурах, образует пограничную кривую – бинодаль, разделяющую области однофазных устойчивых и двухфазных термодинамически неустойчивых растворов. Внутри бинодальной кривой находится спинодаль – геометрическое место точек перегибов (b) на зависимостях G. Область внутри спинодали – область абсолютно неустойчивых растворов. Между бинодалью и спинодалью находится область метастабильных растворов. Фазовый распад в метастабильной области может быть заторможен в связи с малой скоростью образования зародышей новых фаз 16


