ОБЩАЯ 4 растворы.pptx
- Количество слайдов: 18
 РАСТВОРЫ Лекция 5
РАСТВОРЫ Лекция 5
 • Сложные химические системы могут быть получены из чистых химических веществ в результате дробления и перемешивания исходных фаз (диспергирования). • Дисперсные системы – это системы, состоящие из сплошной среды (называемой дисперсионной средой) с распределенным в ней веществом (дисперсной фазой), которое состоит из отдельных частиц с большой удельной поверхностью. • Растворы – это гомогенные системы переменного состава, образованные не менее чем двумя компонентами • Растворитель - тот компонент, который находится в жидкой фазе и, как правило, превалирует количественно • Образование раствора является самопроизвольным процессом, неизбежно протекающем при контакте фаз. Это - принципиальное следствие Второго Начала термодинамики, поскольку общая энтропия при смешении растет • Энергетической характеристикой процесса растворения является изменение энергии Гиббса в ходе этого процесса. Процессы при растворении Отрицательна при любом значении энтальпии. может быть как положительной, так и отрицательной. абсолютно нерастворимых веществ нет Положительна и очень велика эндотермический процесс разрушения связей в растворяемом веществе экзотермический процесс образования сольватов
• Сложные химические системы могут быть получены из чистых химических веществ в результате дробления и перемешивания исходных фаз (диспергирования). • Дисперсные системы – это системы, состоящие из сплошной среды (называемой дисперсионной средой) с распределенным в ней веществом (дисперсной фазой), которое состоит из отдельных частиц с большой удельной поверхностью. • Растворы – это гомогенные системы переменного состава, образованные не менее чем двумя компонентами • Растворитель - тот компонент, который находится в жидкой фазе и, как правило, превалирует количественно • Образование раствора является самопроизвольным процессом, неизбежно протекающем при контакте фаз. Это - принципиальное следствие Второго Начала термодинамики, поскольку общая энтропия при смешении растет • Энергетической характеристикой процесса растворения является изменение энергии Гиббса в ходе этого процесса. Процессы при растворении Отрицательна при любом значении энтальпии. может быть как положительной, так и отрицательной. абсолютно нерастворимых веществ нет Положительна и очень велика эндотермический процесс разрушения связей в растворяемом веществе экзотермический процесс образования сольватов
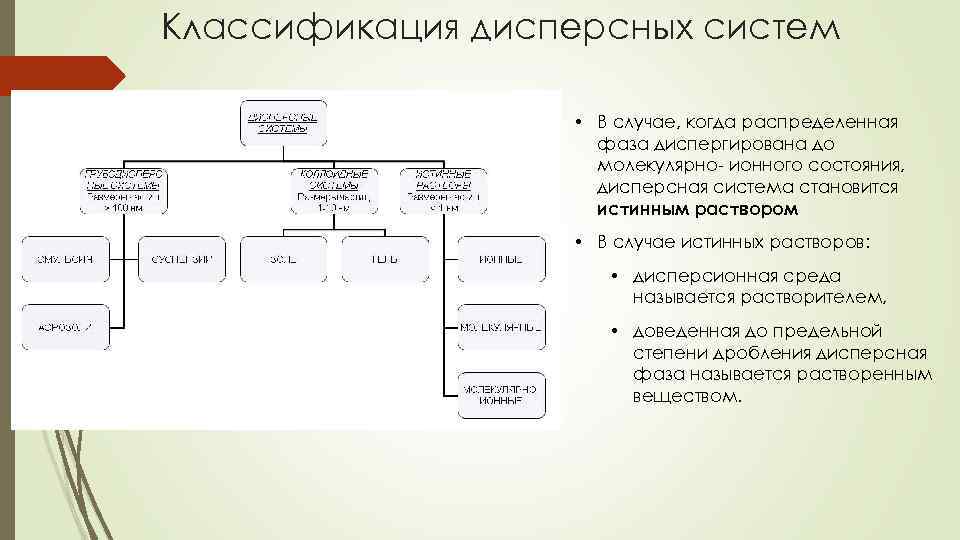 Классификация дисперсных систем • В случае, когда распределенная фаза диспергирована до молекулярно- ионного состояния, дисперсная система становится истинным раствором • В случае истинных растворов: • дисперсионная среда называется растворителем, • доведенная до предельной степени дробления дисперсная фаза называется растворенным веществом.
Классификация дисперсных систем • В случае, когда распределенная фаза диспергирована до молекулярно- ионного состояния, дисперсная система становится истинным раствором • В случае истинных растворов: • дисперсионная среда называется растворителем, • доведенная до предельной степени дробления дисперсная фаза называется растворенным веществом.
 Дисперсные системы Суспензии (suspensio) — это такие системы, которые состоят из раздробленного твердого вещества и жидкой фазы. Размер частиц в них колеблется от 0, 1 до 50 мкм и более (грубодисперсные системы). Суспензии гетерогенны, но в отличие от коллоидных растворов это мутные жидкости, частицы которых видны под обычным микроскопом. Эти жидкости седиментируют, их частицы задерживаются даже крупнопористыми фильтрующими материалами. Они не склонны к диализу и диффузии. Эмульсии (emulsus) представляют собой дисперсные системы, в которых и дисперсная фаза, и дисперсионная среда представлены взаимонерастворимыми или мало взаиморастворимыми жидкостями. Эмульсии относятся к грубодисперсным системам, в которых размер дисперсных частиц (капелек) колеблется в пределах от 1 до 150 мкм, но в некоторых случаях они бывают и более высокодисперсными Золи - жидкая (лиозоль) или газообразная (аэрозоль) дисперсионная среда, в объеме которой распределена другая (дисперсная) фаза в виде капелек жидкости, пузырьков газа или мелких твердых частиц Гели - состоят, по крайней мере, из двух компонентов, один из которых образует непрерывную трёхмерную макромолекулярную сетку, выступающую в роли каркаса, пустоты в которой заполнены низкомолекулярным растворителем — дисперсионной средой.
Дисперсные системы Суспензии (suspensio) — это такие системы, которые состоят из раздробленного твердого вещества и жидкой фазы. Размер частиц в них колеблется от 0, 1 до 50 мкм и более (грубодисперсные системы). Суспензии гетерогенны, но в отличие от коллоидных растворов это мутные жидкости, частицы которых видны под обычным микроскопом. Эти жидкости седиментируют, их частицы задерживаются даже крупнопористыми фильтрующими материалами. Они не склонны к диализу и диффузии. Эмульсии (emulsus) представляют собой дисперсные системы, в которых и дисперсная фаза, и дисперсионная среда представлены взаимонерастворимыми или мало взаиморастворимыми жидкостями. Эмульсии относятся к грубодисперсным системам, в которых размер дисперсных частиц (капелек) колеблется в пределах от 1 до 150 мкм, но в некоторых случаях они бывают и более высокодисперсными Золи - жидкая (лиозоль) или газообразная (аэрозоль) дисперсионная среда, в объеме которой распределена другая (дисперсная) фаза в виде капелек жидкости, пузырьков газа или мелких твердых частиц Гели - состоят, по крайней мере, из двух компонентов, один из которых образует непрерывную трёхмерную макромолекулярную сетку, выступающую в роли каркаса, пустоты в которой заполнены низкомолекулярным растворителем — дисперсионной средой.
 Процесс растворения твердого тела в жидкости является результатом явления сольватации – взаимодействия молекул растворителя с частицами растворяемого вещества. В результате этого взаимодействия возникают сольваты – образования молекулярных размеров, представляющие собой ассоциаты частиц растворяемого вещества (A) с молекулами растворителя (R): В случае, когда растворителем является вода, процесс называется гидратацией, а ассоциаты – гидратами. Процесс сольватации может приводить к распаду молекул растворяемого вещества на заряженные частицы - электролитическая диссоциация.
Процесс растворения твердого тела в жидкости является результатом явления сольватации – взаимодействия молекул растворителя с частицами растворяемого вещества. В результате этого взаимодействия возникают сольваты – образования молекулярных размеров, представляющие собой ассоциаты частиц растворяемого вещества (A) с молекулами растворителя (R): В случае, когда растворителем является вода, процесс называется гидратацией, а ассоциаты – гидратами. Процесс сольватации может приводить к распаду молекул растворяемого вещества на заряженные частицы - электролитическая диссоциация.
 Концентрации (размерные величины) ХАРАКТЕРИСТИКИ РАСТВОРОВ Процентная концентрация (массовая) – количество граммов растворенного вещества в 100 граммах раствора [%], или количество миллиграммов вещества в 100 граммах раствора [мг%] Процентная концентрация (объемная) – количество миллилитров растворенного вещества в 100 миллилитров раствора [об. %] Молярная концентрация (молярность) – количество молей растворенного вещества в литре раствора [моль/л] Массовая концентрация – масса растворенного вещества в литре раствора [г/л] Моляльная концентрация (моляльность) – количество молей растворенного вещества в 1000 граммах растворителя. [моль/1000 г р-рителя] Нормальная концентрация (нормальность) – количество молей химического эквивалента растворенного вещества в литре раствора [моль-экв/л] Доли (безразмерные величины) Мольная доля – отношение числа молей растворенного компонента к общему числу молей раствора. Массовая доля – отношение массы растворенного компонента к общей массе раствора. Объемная доля (для смесей газов и растворов ж-ж) – отношение объема растворенного компонента к сумме объемов растворителя и растворенного вещества до начала процесса растворения.
Концентрации (размерные величины) ХАРАКТЕРИСТИКИ РАСТВОРОВ Процентная концентрация (массовая) – количество граммов растворенного вещества в 100 граммах раствора [%], или количество миллиграммов вещества в 100 граммах раствора [мг%] Процентная концентрация (объемная) – количество миллилитров растворенного вещества в 100 миллилитров раствора [об. %] Молярная концентрация (молярность) – количество молей растворенного вещества в литре раствора [моль/л] Массовая концентрация – масса растворенного вещества в литре раствора [г/л] Моляльная концентрация (моляльность) – количество молей растворенного вещества в 1000 граммах растворителя. [моль/1000 г р-рителя] Нормальная концентрация (нормальность) – количество молей химического эквивалента растворенного вещества в литре раствора [моль-экв/л] Доли (безразмерные величины) Мольная доля – отношение числа молей растворенного компонента к общему числу молей раствора. Массовая доля – отношение массы растворенного компонента к общей массе раствора. Объемная доля (для смесей газов и растворов ж-ж) – отношение объема растворенного компонента к сумме объемов растворителя и растворенного вещества до начала процесса растворения.
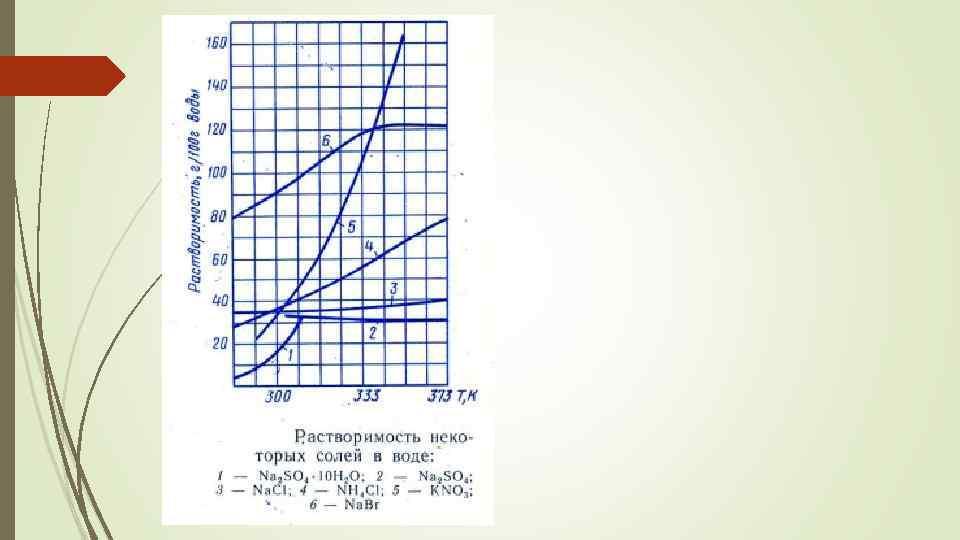
![Растворимость - предельное количество растворяющегося в растворе вещества. [г/100 г растворителя]. Чем более Растворимость - предельное количество растворяющегося в растворе вещества. [г/100 г растворителя]. Чем более](https://present5.com/presentation/331341122_451708367/image-7.jpg) Растворимость - предельное количество растворяющегося в растворе вещества. [г/100 г растворителя]. Чем более похожи по характеру и энергетике химических связей растворитель и растворяемое вещество, тем растворимость, как правило, больше ( «подобное растворяется в подобном» ) РАСТВОРЫ Am. Bn m. An+ + n. Bm- ненасыщенные содержание растворенного вещества в растворе меньше растворимости насыщенные содержание растворенного вещества в растворе равно растворимости пересыщенные содержание растворенного вещества в растворе больше растворимости
Растворимость - предельное количество растворяющегося в растворе вещества. [г/100 г растворителя]. Чем более похожи по характеру и энергетике химических связей растворитель и растворяемое вещество, тем растворимость, как правило, больше ( «подобное растворяется в подобном» ) РАСТВОРЫ Am. Bn m. An+ + n. Bm- ненасыщенные содержание растворенного вещества в растворе меньше растворимости насыщенные содержание растворенного вещества в растворе равно растворимости пересыщенные содержание растворенного вещества в растворе больше растворимости
 Понятие об идеальных растворах Идеальный раствор – это раствор, при образовании которого не изменяется внутренняя энергия системы ( ∆Us = 0), растворение не сопровождается тепловым эффектом (∆Hs =0) и остается постоянным объём системы ( ∆Vs = 0). Для газов, объем которых при переходе в раствор значительно уменьшается (имеется в виду объем чистого газа и объем раствора, содержащего то же количество компонента), зависимость растворимости от давления характеризуется законом Генри: где Pk – парциальное давление k-го газообразного компонента, находящегося над раствором, Kk – константа Генри для этого компонента. Влияние температуры на процесс растворения имеет сложный характер и зависит от знака теплового эффекта процесса растворения. Для экзотермического процесса растворения газов с ростом температуры растворимость уменьшается Для твердых тел возможно как увеличение, так и уменьшение растворимости с ростом температуры
Понятие об идеальных растворах Идеальный раствор – это раствор, при образовании которого не изменяется внутренняя энергия системы ( ∆Us = 0), растворение не сопровождается тепловым эффектом (∆Hs =0) и остается постоянным объём системы ( ∆Vs = 0). Для газов, объем которых при переходе в раствор значительно уменьшается (имеется в виду объем чистого газа и объем раствора, содержащего то же количество компонента), зависимость растворимости от давления характеризуется законом Генри: где Pk – парциальное давление k-го газообразного компонента, находящегося над раствором, Kk – константа Генри для этого компонента. Влияние температуры на процесс растворения имеет сложный характер и зависит от знака теплового эффекта процесса растворения. Для экзотермического процесса растворения газов с ростом температуры растворимость уменьшается Для твердых тел возможно как увеличение, так и уменьшение растворимости с ростом температуры
 Коллигативные свойства растворов Коллигативные (общие) свойства растворов – свойства, которые не зависят от природы растворенного вещества Поведение насыщенного пара Явление осмоса при растворении нелетучего компонента в поверхностном слое жидкости концентрация молекул растворителя уменьшается, уменьшается и давление ее пара P по сравнению с давлением насыщенного пара над чистым растворителем P 0 Закон Рауля: Отношение понижения давления пара растворителя над раствором нелетучего вещества к давлению пара чистого растворителя равно мольной доле растворенного вещества.
Коллигативные свойства растворов Коллигативные (общие) свойства растворов – свойства, которые не зависят от природы растворенного вещества Поведение насыщенного пара Явление осмоса при растворении нелетучего компонента в поверхностном слое жидкости концентрация молекул растворителя уменьшается, уменьшается и давление ее пара P по сравнению с давлением насыщенного пара над чистым растворителем P 0 Закон Рауля: Отношение понижения давления пара растворителя над раствором нелетучего вещества к давлению пара чистого растворителя равно мольной доле растворенного вещества.
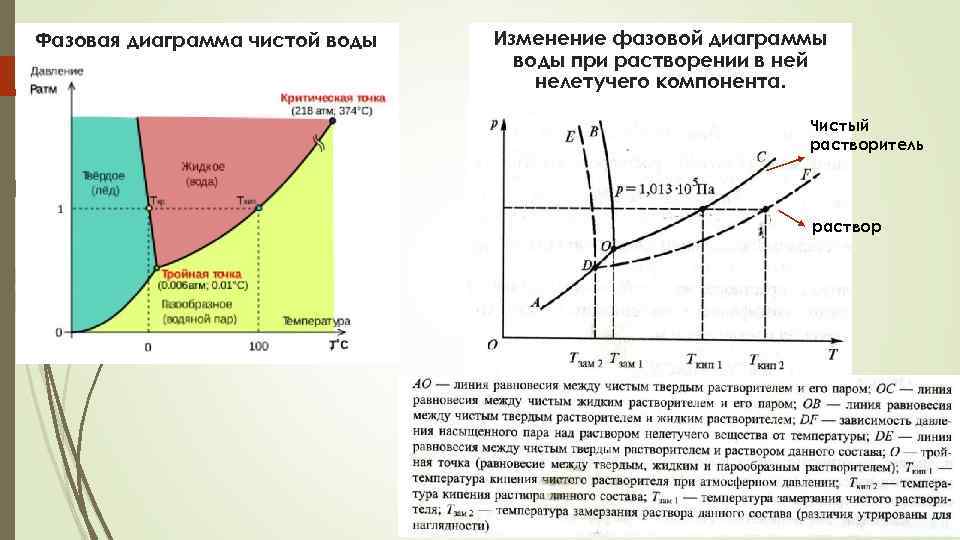 Фазовая диаграмма чистой воды Изменение фазовой диаграммы воды при растворении в ней нелетучего компонента. Чистый растворитель раствор
Фазовая диаграмма чистой воды Изменение фазовой диаграммы воды при растворении в ней нелетучего компонента. Чистый растворитель раствор
 Следствия из закона Рауля повышение температуры кипения раствора по сравнению с температурой кипения чистого растворителя Tкип. = Tкип Т 0 кип Tкип. = Екип. Сm Екип. – эбулиоскопическая постоянная растворителя Температура кипения раствора выше температуры кипения чистого растворителя для воды Екип. = 0, 52, Т 0 кип = 373, 1 К для этилового спирта Екип = 1, 20 Т 0 кип = 351, 4 К Сm - моляльная концентрация раствора понижение температуры кристаллизации растворителя из раствора по сравнению с температурой кристаллизации чистого растворителя Tкрист. = Т 0 крист. Tкрист. = Ккрист. Сm Ккрист. – криоскопическая постоянная растворителя для воды Ккрист. = 1, 86, Т 0 крист. = 273, 1 К для камфоры Ккрист. = 40 Т 0 крист. = 447, 4 К Для растворов неэлектролитов Температура замерзания раствора ниже температуры замерзания чистого растворителя
Следствия из закона Рауля повышение температуры кипения раствора по сравнению с температурой кипения чистого растворителя Tкип. = Tкип Т 0 кип Tкип. = Екип. Сm Екип. – эбулиоскопическая постоянная растворителя Температура кипения раствора выше температуры кипения чистого растворителя для воды Екип. = 0, 52, Т 0 кип = 373, 1 К для этилового спирта Екип = 1, 20 Т 0 кип = 351, 4 К Сm - моляльная концентрация раствора понижение температуры кристаллизации растворителя из раствора по сравнению с температурой кристаллизации чистого растворителя Tкрист. = Т 0 крист. Tкрист. = Ккрист. Сm Ккрист. – криоскопическая постоянная растворителя для воды Ккрист. = 1, 86, Т 0 крист. = 273, 1 К для камфоры Ккрист. = 40 Т 0 крист. = 447, 4 К Для растворов неэлектролитов Температура замерзания раствора ниже температуры замерзания чистого растворителя
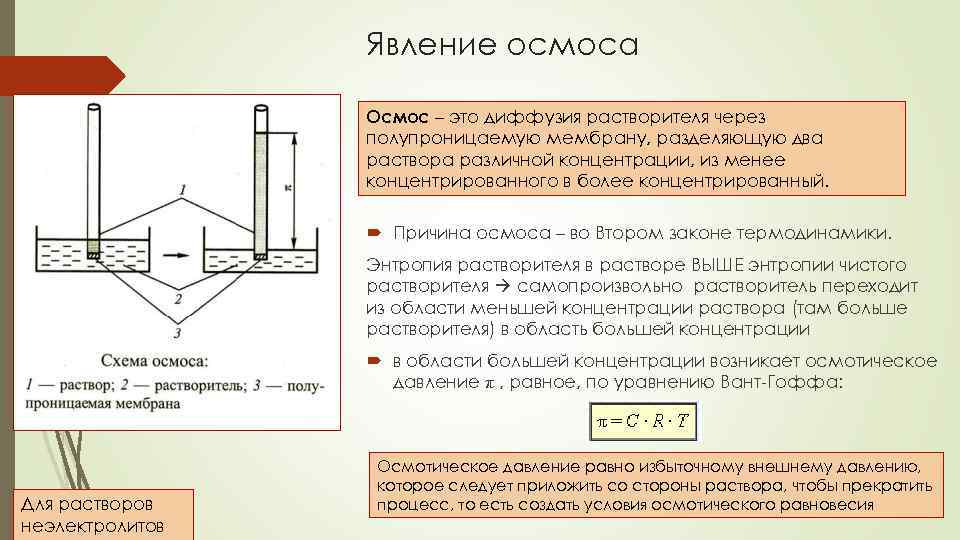 Явление осмоса Осмос – это диффузия растворителя через полупроницаемую мембрану, разделяющую два раствора различной концентрации, из менее концентрированного в более концентрированный. Причина осмоса – во Втором законе термодинамики. Энтропия растворителя в растворе ВЫШЕ энтропии чистого растворителя самопроизвольно растворитель переходит из области меньшей концентрации раствора (там больше растворителя) в область большей концентрации в области большей концентрации возникает осмотическое давление π , равное, по уравнению Вант-Гоффа: Для растворов неэлектролитов Осмотическое давление равно избыточному внешнему давлению, . которое следует приложить со стороны раствора, чтобы прекратить процесс, то есть создать условия осмотического равновесия
Явление осмоса Осмос – это диффузия растворителя через полупроницаемую мембрану, разделяющую два раствора различной концентрации, из менее концентрированного в более концентрированный. Причина осмоса – во Втором законе термодинамики. Энтропия растворителя в растворе ВЫШЕ энтропии чистого растворителя самопроизвольно растворитель переходит из области меньшей концентрации раствора (там больше растворителя) в область большей концентрации в области большей концентрации возникает осмотическое давление π , равное, по уравнению Вант-Гоффа: Для растворов неэлектролитов Осмотическое давление равно избыточному внешнему давлению, . которое следует приложить со стороны раствора, чтобы прекратить процесс, то есть создать условия осмотического равновесия
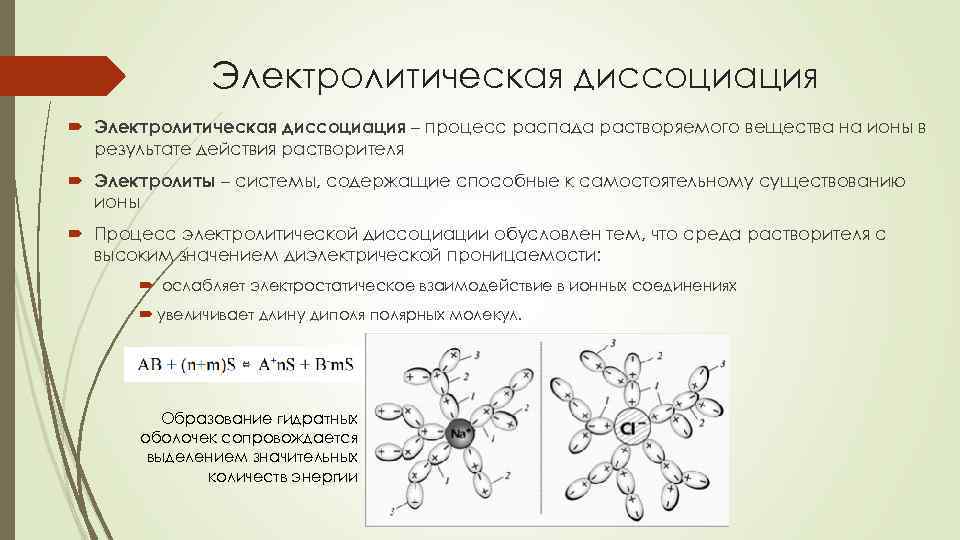 Электролитическая диссоциация – процесс распада растворяемого вещества на ионы в результате действия растворителя Электролиты – системы, содержащие способные к самостоятельному существованию ионы Процесс электролитической диссоциации обусловлен тем, что среда растворителя с высоким значением диэлектрической проницаемости: ослабляет электростатическое взаимодействие в ионных соединениях увеличивает длину диполярных молекул. Образование гидратных оболочек сопровождается выделением значительных количеств энергии
Электролитическая диссоциация – процесс распада растворяемого вещества на ионы в результате действия растворителя Электролиты – системы, содержащие способные к самостоятельному существованию ионы Процесс электролитической диссоциации обусловлен тем, что среда растворителя с высоким значением диэлектрической проницаемости: ослабляет электростатическое взаимодействие в ионных соединениях увеличивает длину диполярных молекул. Образование гидратных оболочек сопровождается выделением значительных количеств энергии
 Количественные характеристики электролитической диссоциации Константа электролитической диссоциации Кe. d. : Степень электролитической диссоциации α - отношение числа распавшихся на ионы частиц к общему числу перешедших в раствор молекул Коэффициент диссоциации i - количество частиц, в среднем возникающее при переходе в раствор одной молекулы растворенного вещества, n - число ионов, образующихся при полной Tкип. = i Екип. Сm диссоциации растворенного вещества Tкрист. = i Ккрист. Сm π. = i C R T i – изотонический коэффициент Вант-Гоффа, численно равен коэффициенту диссоциации
Количественные характеристики электролитической диссоциации Константа электролитической диссоциации Кe. d. : Степень электролитической диссоциации α - отношение числа распавшихся на ионы частиц к общему числу перешедших в раствор молекул Коэффициент диссоциации i - количество частиц, в среднем возникающее при переходе в раствор одной молекулы растворенного вещества, n - число ионов, образующихся при полной Tкип. = i Екип. Сm диссоциации растворенного вещества Tкрист. = i Ккрист. Сm π. = i C R T i – изотонический коэффициент Вант-Гоффа, численно равен коэффициенту диссоциации
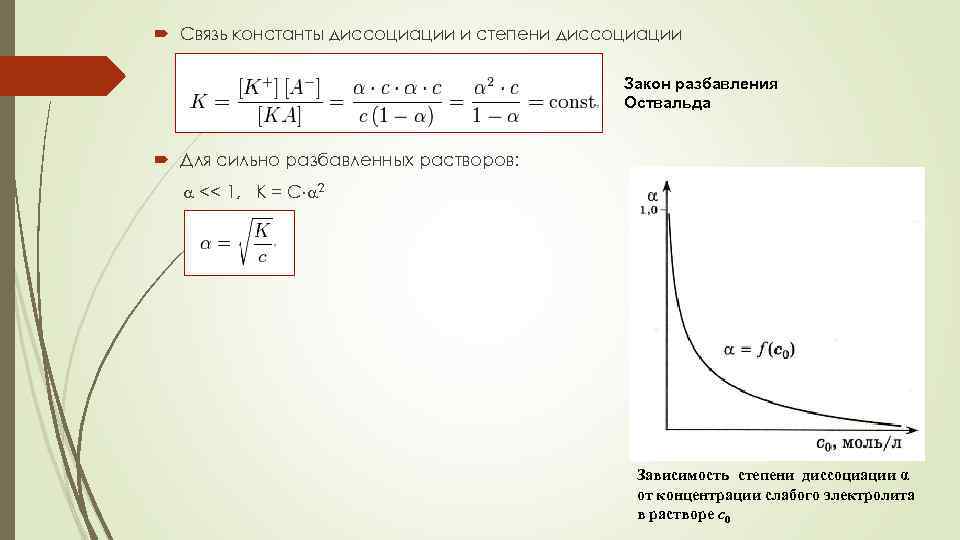 Связь константы диссоциации и степени диссоциации Закон разбавления Оствальда Для сильно разбавленных растворов: << 1, K = C 2 Зависимость степени диссоциации α от концентрации слабого электролита в растворе с0
Связь константы диссоциации и степени диссоциации Закон разбавления Оствальда Для сильно разбавленных растворов: << 1, K = C 2 Зависимость степени диссоциации α от концентрации слабого электролита в растворе с0
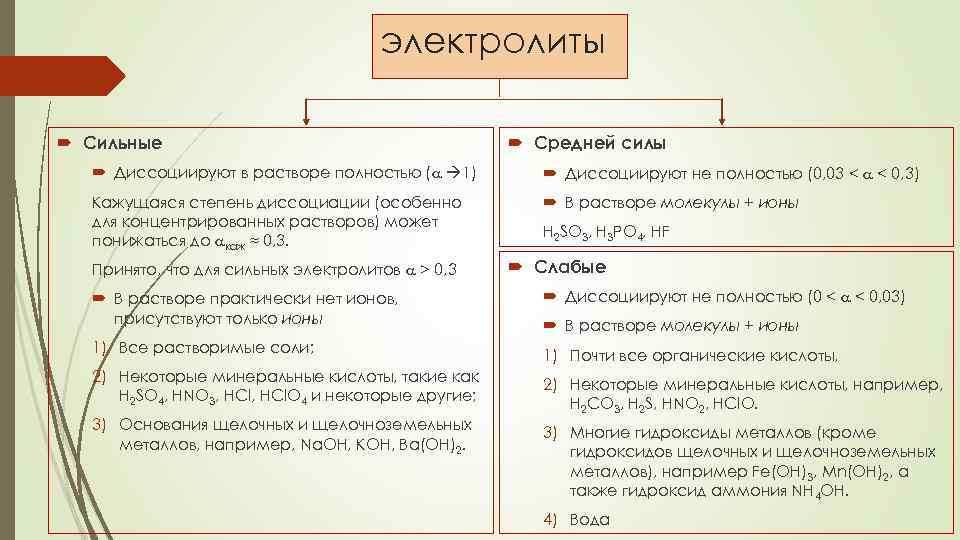 электролиты Сильные Средней силы Диссоциируют в растворе полностью ( 1) Диссоциируют не полностью (0, 03 < < 0, 3) Кажущаяся степень диссоциации (особенно для концентрированных растворов) может понижаться до каж ≈ 0, 3. В растворе молекулы + ионы Принято, что для сильных электролитов > 0, 3 H 2 SO 3, H 3 PO 4, HF Слабые В растворе практически нет ионов, присутствуют только ионы Диссоциируют не полностью (0 < < 0, 03) 1) Все растворимые соли; 1) Почти все органические кислоты, 2) Некоторые минеральные кислоты, такие как H 2 SO 4, HNO 3, HCl. O 4 и некоторые другие; 2) Некоторые минеральные кислоты, например, H 2 CO 3, H 2 S, HNO 2, HCl. O. 3) Основания щелочных и щелочноземельных металлов, например, Na. OH, KOH, Ba(OH)2. В растворе молекулы + ионы 3) Многие гидроксиды металлов (кроме гидроксидов щелочных и щелочноземельных металлов), например Fe(OH)3, Мn(OH)2, а также гидроксид аммония NH 4 OH. 4) Вода
электролиты Сильные Средней силы Диссоциируют в растворе полностью ( 1) Диссоциируют не полностью (0, 03 < < 0, 3) Кажущаяся степень диссоциации (особенно для концентрированных растворов) может понижаться до каж ≈ 0, 3. В растворе молекулы + ионы Принято, что для сильных электролитов > 0, 3 H 2 SO 3, H 3 PO 4, HF Слабые В растворе практически нет ионов, присутствуют только ионы Диссоциируют не полностью (0 < < 0, 03) 1) Все растворимые соли; 1) Почти все органические кислоты, 2) Некоторые минеральные кислоты, такие как H 2 SO 4, HNO 3, HCl. O 4 и некоторые другие; 2) Некоторые минеральные кислоты, например, H 2 CO 3, H 2 S, HNO 2, HCl. O. 3) Основания щелочных и щелочноземельных металлов, например, Na. OH, KOH, Ba(OH)2. В растворе молекулы + ионы 3) Многие гидроксиды металлов (кроме гидроксидов щелочных и щелочноземельных металлов), например Fe(OH)3, Мn(OH)2, а также гидроксид аммония NH 4 OH. 4) Вода
 Электролитическая диссоциация воды Вода – слабый электролит: при 18 °С степень диссоциации воды равна 1, 5 10 -9 молярная концентрация воды в воде CH 2 O=Const =55, 56 моль/л ионное произведение воды. Квод = 10 -14 моль2 /л 2 при 298 К p. H= -lg. CH+ p. ОH= -lg. CОН+ p. H + р. ОН= 14
Электролитическая диссоциация воды Вода – слабый электролит: при 18 °С степень диссоциации воды равна 1, 5 10 -9 молярная концентрация воды в воде CH 2 O=Const =55, 56 моль/л ионное произведение воды. Квод = 10 -14 моль2 /л 2 при 298 К p. H= -lg. CH+ p. ОH= -lg. CОН+ p. H + р. ОН= 14


