Лекция 1 МК Растворы_ПротолитичРеакции2014.ppt
- Количество слайдов: 50
 Растворы Лекция № 1 для студентов 1 курса, обучающихся по специальности 060609. 65 -Медицинская кибернетика Лектор: ст. преподаватель кафедры биохимии Руковец Татьяна Анатольевна 2014 1
Растворы Лекция № 1 для студентов 1 курса, обучающихся по специальности 060609. 65 -Медицинская кибернетика Лектор: ст. преподаватель кафедры биохимии Руковец Татьяна Анатольевна 2014 1
 Цель лекции Познакомиться с основными понятиями тем: «Растворы» , «Равновесия в растворах слабых электролитов» , «Кислоты и основания Аррениуса и Бренстеда» Рассмотреть гидролиз солей как один из видов протолитического равновесия. Научиться рассчитывать р. Н растворов кислот, оснований и солей.
Цель лекции Познакомиться с основными понятиями тем: «Растворы» , «Равновесия в растворах слабых электролитов» , «Кислоты и основания Аррениуса и Бренстеда» Рассмотреть гидролиз солей как один из видов протолитического равновесия. Научиться рассчитывать р. Н растворов кислот, оснований и солей.
 Актуальность Растворы очень широко распространены в природе. Растворами являются все ткани живого организма. Питьевая вода, вода рек, морей и океанов – это тоже растворы. Свойства растворов определяются природой растворенных веществ, их составом и концентрацией.
Актуальность Растворы очень широко распространены в природе. Растворами являются все ткани живого организма. Питьевая вода, вода рек, морей и океанов – это тоже растворы. Свойства растворов определяются природой растворенных веществ, их составом и концентрацией.
 Актуальность Многие реакции (протолитические, окислительно-восстановительные, комплексообразования) протекают зачастую в водных растворах. Знание свойств водных растворов позволяет понять механизмы осмотического и протолитического гомеостаза (постоянства состава), причины нарушения осмотической и протолитической регуляции и способы их корректировки.
Актуальность Многие реакции (протолитические, окислительно-восстановительные, комплексообразования) протекают зачастую в водных растворах. Знание свойств водных растворов позволяет понять механизмы осмотического и протолитического гомеостаза (постоянства состава), причины нарушения осмотической и протолитической регуляции и способы их корректировки.
 План Понятие и классификация растворов. Ионизация воды, ионное произведение, водородный показатель. Реакция среды. Диссоциация кислот и оснований Аррениуса (электролитическая теория кислот и оснований). Состав слюны. 5
План Понятие и классификация растворов. Ионизация воды, ионное произведение, водородный показатель. Реакция среды. Диссоциация кислот и оснований Аррениуса (электролитическая теория кислот и оснований). Состав слюны. 5
 План Расчёт р. Н водных растворов кислот и оснований; Индикаторы. Кислоты и основания Бренстеда (протолитическая теория), показатели р. Ка и р. Кb. Гидролиз солей, Расчёт р. Н их растворов. 6
План Расчёт р. Н водных растворов кислот и оснований; Индикаторы. Кислоты и основания Бренстеда (протолитическая теория), показатели р. Ка и р. Кb. Гидролиз солей, Расчёт р. Н их растворов. 6
 Понятие «растворы» Растворы - это гомогенные (однородные) системы, состоящие из двух и более компонентов. 7
Понятие «растворы» Растворы - это гомогенные (однородные) системы, состоящие из двух и более компонентов. 7
 Растворитель - вещество, которое не меняет своего агрегатного состояния при растворении. Обычно, растворитель – это просто преобладающий компонент раствора. 8
Растворитель - вещество, которое не меняет своего агрегатного состояния при растворении. Обычно, растворитель – это просто преобладающий компонент раствора. 8
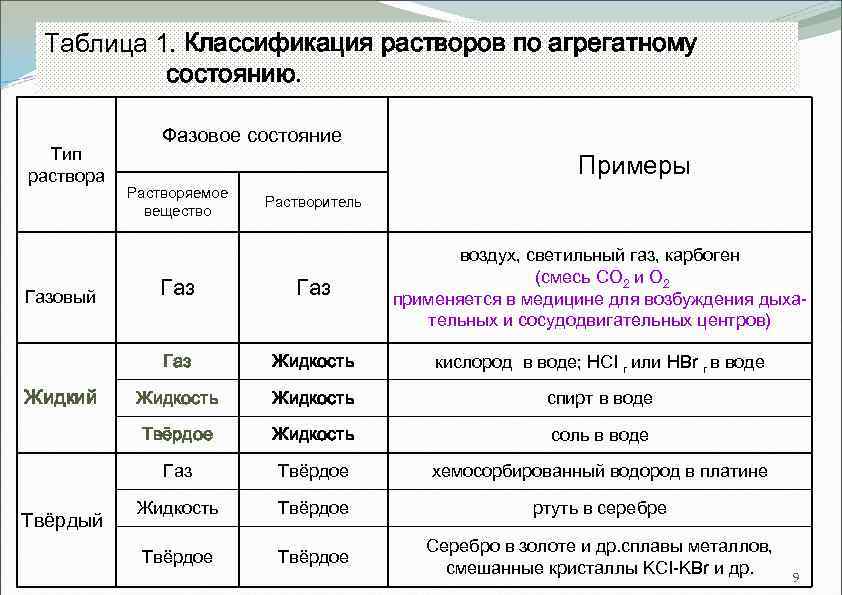 Таблица 1. Классификация растворов по агрегатному состоянию. Тип раствора Фазовое состояние Растворяемое вещество Примеры Растворитель Жидкость кислород в воде; НСI г или HBr г в воде Жидкость спирт в воде Жидкость соль в воде Газ Твёрдый Газ Твёрдое Жидкий Газ Газовый воздух, светильный газ, карбоген (смесь СО 2 и О 2 применяется в медицине для возбуждения дыхательных и сосудодвигательных центров) Твёрдое хемосорбированный водород в платине Жидкость Твёрдое ртуть в серебре Твёрдое Серебро в золоте и др. сплавы металлов, смешанные кристаллы KCI-KBr и др. 9
Таблица 1. Классификация растворов по агрегатному состоянию. Тип раствора Фазовое состояние Растворяемое вещество Примеры Растворитель Жидкость кислород в воде; НСI г или HBr г в воде Жидкость спирт в воде Жидкость соль в воде Газ Твёрдый Газ Твёрдое Жидкий Газ Газовый воздух, светильный газ, карбоген (смесь СО 2 и О 2 применяется в медицине для возбуждения дыхательных и сосудодвигательных центров) Твёрдое хемосорбированный водород в платине Жидкость Твёрдое ртуть в серебре Твёрдое Серебро в золоте и др. сплавы металлов, смешанные кристаллы KCI-KBr и др. 9
 Жидкие растворы вода морей и океанов, и даже водопроводная вода; биологические жидкости с растворенными в них низкомолекулярными и высокомолекулярными веществами: ü кровь, лимфа; ü моча; ü спинномозговая жидкость; ü пот; ü желудочный и кишечный соки; ü слюна; ü желчь; ü цитозоль; ü матрикс митохондрий. 10
Жидкие растворы вода морей и океанов, и даже водопроводная вода; биологические жидкости с растворенными в них низкомолекулярными и высокомолекулярными веществами: ü кровь, лимфа; ü моча; ü спинномозговая жидкость; ü пот; ü желудочный и кишечный соки; ü слюна; ü желчь; ü цитозоль; ü матрикс митохондрий. 10
 КЛАССИФИКАЦИЯ РАСТВОРОВ По строению частиц растворённого вещества ●Истинные растворы (размер частиц 10 -10 – 10 -9 м) ●Коллоидные растворы (размер частиц 10 -9 – 10 -6 м) ●Растворы ВМС 11
КЛАССИФИКАЦИЯ РАСТВОРОВ По строению частиц растворённого вещества ●Истинные растворы (размер частиц 10 -10 – 10 -9 м) ●Коллоидные растворы (размер частиц 10 -9 – 10 -6 м) ●Растворы ВМС 11
 ●Истинные растворы - растворы, где частицы растворенного вещества находятся в воде или другом растворителе в виде молекул, атомов или ионов. Это растворы низкомолекулярных соединений (НМС). ● Примеры НМС: соли, кислоты, щелочи.
●Истинные растворы - растворы, где частицы растворенного вещества находятся в воде или другом растворителе в виде молекул, атомов или ионов. Это растворы низкомолекулярных соединений (НМС). ● Примеры НМС: соли, кислоты, щелочи.
 ● Коллоидные растворы – это растворы, относящиеся к дисперсным системам, где частицы дисперсной фазы находятся в дисперсионной среде в виде мицелл, размеры которых превышают молекулярные. Мицелла коллоидного раствора 13
● Коллоидные растворы – это растворы, относящиеся к дисперсным системам, где частицы дисперсной фазы находятся в дисперсионной среде в виде мицелл, размеры которых превышают молекулярные. Мицелла коллоидного раствора 13
 ● растворы высокомолекулярных соединений (ВМС) занимают промежуточное положение между истинными и коллоидными растворами. Это растворы белков, нуклеиновых кислот и полисахаридов. ДНК Альбумин Крахмал
● растворы высокомолекулярных соединений (ВМС) занимают промежуточное положение между истинными и коллоидными растворами. Это растворы белков, нуклеиновых кислот и полисахаридов. ДНК Альбумин Крахмал
 Ионизация воды. Водородный показатель р. Н. Вода – слабый электролит. Уравнение диссоциации воды: HOH + HOH ⇆ НО⁻ + Н 3 О + ⇨ Н О Н + Н Катион гидроксония Гидратированный протон водорода + HOH ⇆ НО⁻ + Н (1) + [Н ]·[НО⁻] Кр = Кд (НОН) = = const при данной t 0 (2) [НОН] при 25 0 С Кд (НОН) = 1, 8 · 10 -16 15
Ионизация воды. Водородный показатель р. Н. Вода – слабый электролит. Уравнение диссоциации воды: HOH + HOH ⇆ НО⁻ + Н 3 О + ⇨ Н О Н + Н Катион гидроксония Гидратированный протон водорода + HOH ⇆ НО⁻ + Н (1) + [Н ]·[НО⁻] Кр = Кд (НОН) = = const при данной t 0 (2) [НОН] при 25 0 С Кд (НОН) = 1, 8 · 10 -16 15
![Далее, молярная концентрация молекул воды – тоже const [НОН] = СМ (НОН) = m Далее, молярная концентрация молекул воды – тоже const [НОН] = СМ (НОН) = m](https://present5.com/presentation/-76494013_328934115/image-16.jpg) Далее, молярная концентрация молекул воды – тоже const [НОН] = СМ (НОН) = m (НОН) М (НОН). Vл 1000 = = 55, 6 моль/л 18 1 Сгруппируем постоянные величины в уравнении (2) и обозначим их произведение – Кw : Кw = Кд(НОН) · [НОН] = [H+]·[HО⁻] = =1, 8· 10 -16 · 55, 6 ≈ 10 -14 ионное при 250 С (3) произведение воды Ионное произведение воды Кw – есть величина постоянная при данной температуре. # С увеличением температуры Кw тоже увеличивается. Постоянство ионного произведения [H+][HО-] характерно не только для чистой воды, но и для любых водных растворов. 16
Далее, молярная концентрация молекул воды – тоже const [НОН] = СМ (НОН) = m (НОН) М (НОН). Vл 1000 = = 55, 6 моль/л 18 1 Сгруппируем постоянные величины в уравнении (2) и обозначим их произведение – Кw : Кw = Кд(НОН) · [НОН] = [H+]·[HО⁻] = =1, 8· 10 -16 · 55, 6 ≈ 10 -14 ионное при 250 С (3) произведение воды Ионное произведение воды Кw – есть величина постоянная при данной температуре. # С увеличением температуры Кw тоже увеличивается. Постоянство ионного произведения [H+][HО-] характерно не только для чистой воды, но и для любых водных растворов. 16
 Роль Кw : зная Кw и концентрацию одного из ионов воды, можно всегда найти концентрацию другого иона : [HO⁻] = Кw [H+] = 10 -14 [H+] ( при t 0 =25 0 С) (4) Для чистой воды: [H+] = [HO⁻] среда нейтральная [H+] = 10 -7 моль/л 17
Роль Кw : зная Кw и концентрацию одного из ионов воды, можно всегда найти концентрацию другого иона : [HO⁻] = Кw [H+] = 10 -14 [H+] ( при t 0 =25 0 С) (4) Для чистой воды: [H+] = [HO⁻] среда нейтральная [H+] = 10 -7 моль/л 17
![Таблица 2. Оценка реакции среды. Характеристика p. H = - lg [H+] [HО-] 10 Таблица 2. Оценка реакции среды. Характеристика p. H = - lg [H+] [HО-] 10](https://present5.com/presentation/-76494013_328934115/image-18.jpg) Таблица 2. Оценка реакции среды. Характеристика p. H = - lg [H+] [HО-] 10 -7 7 (- lg 10 -7) Кислая > 10 -7 <7 Щелочная < 10 -7 >7 среда Нейтральная Поскольку концентрации ионов очень малы, то для удобства оценки реакции среды (или кислотности среды) используют не сами концентрации, а их показатели: р. Н, р. ОН. p. H = - lg [H+] p. OH = - lg [HO–] (5) 18
Таблица 2. Оценка реакции среды. Характеристика p. H = - lg [H+] [HО-] 10 -7 7 (- lg 10 -7) Кислая > 10 -7 <7 Щелочная < 10 -7 >7 среда Нейтральная Поскольку концентрации ионов очень малы, то для удобства оценки реакции среды (или кислотности среды) используют не сами концентрации, а их показатели: р. Н, р. ОН. p. H = - lg [H+] p. OH = - lg [HO–] (5) 18
 # На практике больше используется показатель р. Н, чем р. ОН. Чем сильнее кислотность среды (больше [H+]), тем меньше будет р. Н. И, наоборот, с ростом р. Н кислотность ослабевает, но растёт щелочность среды. среда слабокислая среда слабощелочная [H+] ___|____|____|____|___ 10 -4 10 -5 10 -6 10 -7 10 -8 10 -9 10 -10 среда нейтральная кислотность увеличивается среда слабокислая р. Н среда слабощелочная ___|____|____|____|___ 4 5 6 7 8 нейтральная среда 9 10 11 19
# На практике больше используется показатель р. Н, чем р. ОН. Чем сильнее кислотность среды (больше [H+]), тем меньше будет р. Н. И, наоборот, с ростом р. Н кислотность ослабевает, но растёт щелочность среды. среда слабокислая среда слабощелочная [H+] ___|____|____|____|___ 10 -4 10 -5 10 -6 10 -7 10 -8 10 -9 10 -10 среда нейтральная кислотность увеличивается среда слабокислая р. Н среда слабощелочная ___|____|____|____|___ 4 5 6 7 8 нейтральная среда 9 10 11 19
 Далее, выражение для ионного произведения воды (3) переведём в логарифмическую шкалу. Для этого прологарифмируем (3) с отрицательным знаком: -lg [H+]·[HO–] = - lg 10 -14 -lg[H+] - lg[HO–] = -(-14); откуда р. Н р. ОН р. Н + р. ОН = 14 при t 0 =25 0 С (6) р. Н = 14 – р. ОН, р. ОН = 14 – р. Н 20
Далее, выражение для ионного произведения воды (3) переведём в логарифмическую шкалу. Для этого прологарифмируем (3) с отрицательным знаком: -lg [H+]·[HO–] = - lg 10 -14 -lg[H+] - lg[HO–] = -(-14); откуда р. Н р. ОН р. Н + р. ОН = 14 при t 0 =25 0 С (6) р. Н = 14 – р. ОН, р. ОН = 14 – р. Н 20
 р. Н биологических жидкостей колеблется в зоне 1÷ 9 üр. Н желудочного сока 1; üр. Н кишечного сока 9 üр. Н крови 7, 36 (7, 25 ÷ 7, 44) üр. Н мочи 4, 8 ÷ 7, 5 (из крови сбрасываются лишние кислоты или основания) üр. Н пищевых продуктов 3÷ 6 (в большинстве случаев; только молоко щелочнее этой среды). 21
р. Н биологических жидкостей колеблется в зоне 1÷ 9 üр. Н желудочного сока 1; üр. Н кишечного сока 9 üр. Н крови 7, 36 (7, 25 ÷ 7, 44) üр. Н мочи 4, 8 ÷ 7, 5 (из крови сбрасываются лишние кислоты или основания) üр. Н пищевых продуктов 3÷ 6 (в большинстве случаев; только молоко щелочнее этой среды). 21
 р. Н среды, оптимальное для развития патогенных для человека бактерий практически совпадает с р. Н плазмы крови: ü р. Н для стрептококков и менингококков 7, 4 ÷ 7, 6 ü р. Н для стафилококков 7, 4 ü р. Н для пневмококков 7, 0 ÷ 7, 4 Для измерения р. Н среды используются индикаторы кислотно-основного типа или р. Н-метры. 22
р. Н среды, оптимальное для развития патогенных для человека бактерий практически совпадает с р. Н плазмы крови: ü р. Н для стрептококков и менингококков 7, 4 ÷ 7, 6 ü р. Н для стафилококков 7, 4 ü р. Н для пневмококков 7, 0 ÷ 7, 4 Для измерения р. Н среды используются индикаторы кислотно-основного типа или р. Н-метры. 22
 СЛЮНА p. H от 5, 6 до 7, 6. На 98, 5 % и более состоит из воды, Слюна содержит : соли различных кислот микроэлементы и катионы некоторых щелочных металлов муцин (формирует и склеивает пищевой комок) лизоцим (бактерицидный агент) ферменты амилазу и мальтазу, расщепляющие углеводы до олиго- и моносахаридов, а также другие ферменты, некоторые витамины.
СЛЮНА p. H от 5, 6 до 7, 6. На 98, 5 % и более состоит из воды, Слюна содержит : соли различных кислот микроэлементы и катионы некоторых щелочных металлов муцин (формирует и склеивает пищевой комок) лизоцим (бактерицидный агент) ферменты амилазу и мальтазу, расщепляющие углеводы до олиго- и моносахаридов, а также другие ферменты, некоторые витамины.
 СЛЮНА Величина р. Н слюны изменяется в зависимости от характера патологического процесса в полости рта. При инфекционных заболеваниях реакция слюны кислая. При ряде общих заболеваний, например, при нефрите, сопровождающемся уремией, в слюне возрастает количество остаточного азота (среда щелочная) содержание азота увеличивается также при язвенной болезни желудка и двенадцатиперстной кишки. !!! Исследование состава слюны можно предпринимать с диагностической целью.
СЛЮНА Величина р. Н слюны изменяется в зависимости от характера патологического процесса в полости рта. При инфекционных заболеваниях реакция слюны кислая. При ряде общих заболеваний, например, при нефрите, сопровождающемся уремией, в слюне возрастает количество остаточного азота (среда щелочная) содержание азота увеличивается также при язвенной болезни желудка и двенадцатиперстной кишки. !!! Исследование состава слюны можно предпринимать с диагностической целью.
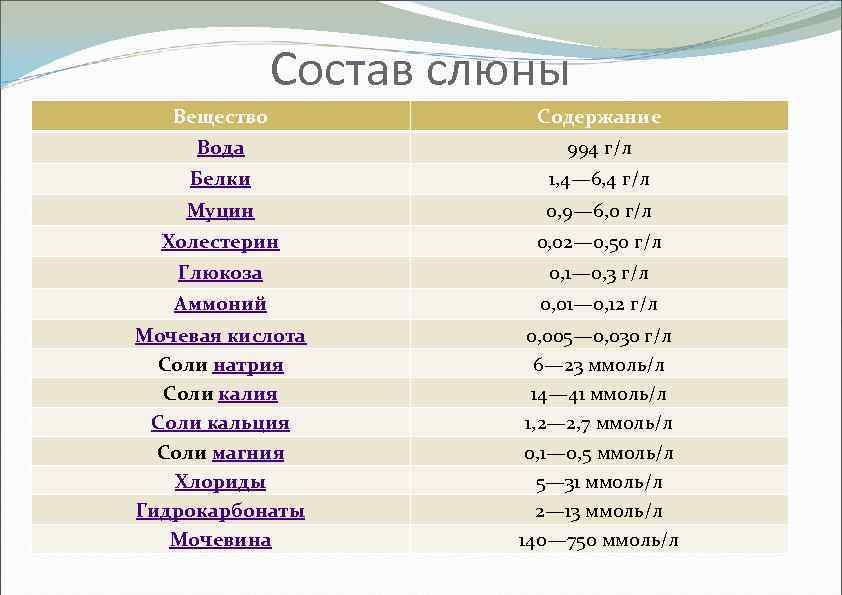 Состав слюны Вещество Содержание Вода 994 г/л Белки 1, 4— 6, 4 г/л Муцин 0, 9— 6, 0 г/л Холестерин 0, 02— 0, 50 г/л Глюкоза 0, 1— 0, 3 г/л Аммоний 0, 01— 0, 12 г/л Мочевая кислота Соли натрия Соли кальция Соли магния Хлориды Гидрокарбонаты Мочевина 0, 005— 0, 030 г/л 6— 23 ммоль/л 14— 41 ммоль/л 1, 2— 2, 7 ммоль/л 0, 1— 0, 5 ммоль/л 5— 31 ммоль/л 2— 13 ммоль/л 140— 750 ммоль/л
Состав слюны Вещество Содержание Вода 994 г/л Белки 1, 4— 6, 4 г/л Муцин 0, 9— 6, 0 г/л Холестерин 0, 02— 0, 50 г/л Глюкоза 0, 1— 0, 3 г/л Аммоний 0, 01— 0, 12 г/л Мочевая кислота Соли натрия Соли кальция Соли магния Хлориды Гидрокарбонаты Мочевина 0, 005— 0, 030 г/л 6— 23 ммоль/л 14— 41 ммоль/л 1, 2— 2, 7 ммоль/л 0, 1— 0, 5 ммоль/л 5— 31 ммоль/л 2— 13 ммоль/л 140— 750 ммоль/л
 Ионизация кислот По теории Аррениуса: vкислоты – это молекулы или ионы, которые при растворении в воде освобождают Н+ НА + НОН ⇆ А– + Н 3 О+, (7) где НА – кислота в общем виде, А– - кислотный остаток. Упрощённо (без учёта гидратации): НА ⇆ А – + Н+ (8) ! Вероятность нахождения Н + в свободном виде чрезвычайно мала 26
Ионизация кислот По теории Аррениуса: vкислоты – это молекулы или ионы, которые при растворении в воде освобождают Н+ НА + НОН ⇆ А– + Н 3 О+, (7) где НА – кислота в общем виде, А– - кислотный остаток. Упрощённо (без учёта гидратации): НА ⇆ А – + Н+ (8) ! Вероятность нахождения Н + в свободном виде чрезвычайно мала 26
![константа кислотности Ка Кр = Ка (НА) = [А– ]·[Н+] [НА] = const при константа кислотности Ка Кр = Ка (НА) = [А– ]·[Н+] [НА] = const при](https://present5.com/presentation/-76494013_328934115/image-27.jpg) константа кислотности Ка Кр = Ка (НА) = [А– ]·[Н+] [НА] = const при данной t 0. (9) где Ка (НА) – константа ионизации кислоты НА , или константа кислотности НА, которая характеризует силу кислоты: с увеличением Ка кислотность НА растёт. р. Ка = - lg Ка (10) Отсюда, чем больше Ка и меньше р. Ка, тем сильнее кислота. # Для сильных кислот р. Ка < 0, для слабых кислот р. Ка > 0 27
константа кислотности Ка Кр = Ка (НА) = [А– ]·[Н+] [НА] = const при данной t 0. (9) где Ка (НА) – константа ионизации кислоты НА , или константа кислотности НА, которая характеризует силу кислоты: с увеличением Ка кислотность НА растёт. р. Ка = - lg Ка (10) Отсюда, чем больше Ка и меньше р. Ка, тем сильнее кислота. # Для сильных кислот р. Ка < 0, для слабых кислот р. Ка > 0 27
 Физический смысл Ка и р. Ка Обратимся к реакции ионизации кислоты (8). Положение равновесия этой реакции зависит от кислотности среды. В кислой среде равновесие (8) будет смещено влево, в сторону молекулярных форм, а в щелочной среде – вправо, в сторону ионных форм. Очевидно, найдётся такая среда, в которой кислота окажется ионизированной на 50%, т. е. [HA] = [A– ]. При этом условии константа равновесия примет значение: 28
Физический смысл Ка и р. Ка Обратимся к реакции ионизации кислоты (8). Положение равновесия этой реакции зависит от кислотности среды. В кислой среде равновесие (8) будет смещено влево, в сторону молекулярных форм, а в щелочной среде – вправо, в сторону ионных форм. Очевидно, найдётся такая среда, в которой кислота окажется ионизированной на 50%, т. е. [HA] = [A– ]. При этом условии константа равновесия примет значение: 28
![Кр = Ка = [H+] а её логарифмирование с отрицательным знаком даст: - lg Кр = Ка = [H+] а её логарифмирование с отрицательным знаком даст: - lg](https://present5.com/presentation/-76494013_328934115/image-29.jpg) Кр = Ка = [H+] а её логарифмирование с отрицательным знаком даст: - lg Kа = - lg [H+] р. Ка = р. Н преобладают молекулярные формы ׀ р. Ка 50/50 преобладают ионные формы Таким образом, р. Ка – это есть р. Н среды, при которой кислота ионизируется на 50%. Для каждой кислоты существует своё значение р. Ка в зависимости от её строения. 29
Кр = Ка = [H+] а её логарифмирование с отрицательным знаком даст: - lg Kа = - lg [H+] р. Ка = р. Н преобладают молекулярные формы ׀ р. Ка 50/50 преобладают ионные формы Таким образом, р. Ка – это есть р. Н среды, при которой кислота ионизируется на 50%. Для каждой кислоты существует своё значение р. Ка в зависимости от её строения. 29
 Ионизация оснований По теории Аррениуса: v. Основания – это молекулы или ионы, которые при растворении в воде освобождают ОН – Рассмотрим основания, дающие при ионизации одну ОН -группу : Э – ОН ⇆ Э+ + ОН – К р = Кb = [Э+] [НО– ] (11) = const при данной t [ Э – ОН ] р. Кb = - lg. Кb (12) 30
Ионизация оснований По теории Аррениуса: v. Основания – это молекулы или ионы, которые при растворении в воде освобождают ОН – Рассмотрим основания, дающие при ионизации одну ОН -группу : Э – ОН ⇆ Э+ + ОН – К р = Кb = [Э+] [НО– ] (11) = const при данной t [ Э – ОН ] р. Кb = - lg. Кb (12) 30
 Физический смысл р. Кb # Физический смысл р. Кb для оснований устанавливают также как р. Ка для кислот: р. Кb – это р. ОН – среды, при котором основание ионизируется на 50%. Для каждого основания существует своё значение р. Кb , зависящее от его строения. 31
Физический смысл р. Кb # Физический смысл р. Кb для оснований устанавливают также как р. Ка для кислот: р. Кb – это р. ОН – среды, при котором основание ионизируется на 50%. Для каждого основания существует своё значение р. Кb , зависящее от его строения. 31
 Расчет р. Н разбавленных растворов сильных и слабых кислот и оснований КИСЛОТЫ сильные слабые одноосновные двухосновные 32
Расчет р. Н разбавленных растворов сильных и слабых кислот и оснований КИСЛОТЫ сильные слабые одноосновные двухосновные 32
 р. Н растворов сильных кислот (HCl, HNO 3, HCl. O 4, H 2 SO 4 и др. ) р. Н(сильн. к-ты)= -lg[H+] = -lg. Cэ(НА) = р. Сэ(сильн. к-ты)(НА) (13) кислотность среды для растворов сильных кислот определяется показателем их эквивалентной концентрации: р. Н сильн. к-ты = р. Сэ(сильн. к-ты) 33
р. Н растворов сильных кислот (HCl, HNO 3, HCl. O 4, H 2 SO 4 и др. ) р. Н(сильн. к-ты)= -lg[H+] = -lg. Cэ(НА) = р. Сэ(сильн. к-ты)(НА) (13) кислотность среды для растворов сильных кислот определяется показателем их эквивалентной концентрации: р. Н сильн. к-ты = р. Сэ(сильн. к-ты) 33
 р. Н растворов сильных оснований (КОН, Na. OH и др. ) р. ОН(сильн. осн. )= -lg[ОH-] = -lg. Cэ(осн) = р. Сэ(сильн. осн)(13) р. Н сильн. осн. = 14 - р. Сэ(сильн. осн. ) 34
р. Н растворов сильных оснований (КОН, Na. OH и др. ) р. ОН(сильн. осн. )= -lg[ОH-] = -lg. Cэ(осн) = р. Сэ(сильн. осн)(13) р. Н сильн. осн. = 14 - р. Сэ(сильн. осн. ) 34
 р. Н растворов слабых кислот (CH 3 COOH, HCN, HNO 2 , H 2 SO 3 , H 2 CO 3 и др. ) 1. Слабые одноосновные кислоты диссоциируют обратимо: НА ⇆ Н+ + А- (14) p. Hслабой кислоты = p + p. CМ (HA) a- степень диссоциации (показывает долю ионизированных молекул). -lg. Ka - lg. Cм р. Ka + р. Cм р. Нслаб. к-ты = 2 2 (15) 35
р. Н растворов слабых кислот (CH 3 COOH, HCN, HNO 2 , H 2 SO 3 , H 2 CO 3 и др. ) 1. Слабые одноосновные кислоты диссоциируют обратимо: НА ⇆ Н+ + А- (14) p. Hслабой кислоты = p + p. CМ (HA) a- степень диссоциации (показывает долю ионизированных молекул). -lg. Ka - lg. Cм р. Ka + р. Cм р. Нслаб. к-ты = 2 2 (15) 35
 Расчет р. ОН растворов слабых оснований 1) через α: р. ОНслаб. осн. = рα + р. См(осн. ) (16) где α – степень ионизации р. Н = 14 – (р + р. СМ(основ) ) 2) через Кb : р. Нслаб. основ. = 14 – р. ОН = 14 – р. Кb + р. См (17) (18) 2 36
Расчет р. ОН растворов слабых оснований 1) через α: р. ОНслаб. осн. = рα + р. См(осн. ) (16) где α – степень ионизации р. Н = 14 – (р + р. СМ(основ) ) 2) через Кb : р. Нслаб. основ. = 14 – р. ОН = 14 – р. Кb + р. См (17) (18) 2 36
 Кислотно-основные индикаторы v В качестве индикаторов для определения р. Н растворов используют слабые органические кислоты и основания, у которых молекулярная и ионная формы отличаются по цвету (см. табл. 3) 37
Кислотно-основные индикаторы v В качестве индикаторов для определения р. Н растворов используют слабые органические кислоты и основания, у которых молекулярная и ионная формы отличаются по цвету (см. табл. 3) 37
 р. Н среды, при котором индикатор ионизирован на 50% и цвет раствора смешанный, называется точкой перехода цвета индикатора р. Т (инд. ) = р. Ка (инд. ) = - lg Ка (инд. ) - это силовая характеристика индикатора. р. Т ± 1 - это зона перехода цвета индикатора. Ведь наш глаз замечает смешанный цвет не только при условии равенства концентраций молекулярных и ионных форм индикатора, но и когда концентрация одной из форм преобладает над другой в 10 раз (lg 10 = 1). HInd ↔ Ind- + H+ нейтральная форма окраска 1 (при р. Н < p. Ka – 1) смесь форм заряженная форма переходная окраска 2 окраска (при р. Н > p. Ka + 1) (Δр. Н = p. Ka ± 1) 38
р. Н среды, при котором индикатор ионизирован на 50% и цвет раствора смешанный, называется точкой перехода цвета индикатора р. Т (инд. ) = р. Ка (инд. ) = - lg Ка (инд. ) - это силовая характеристика индикатора. р. Т ± 1 - это зона перехода цвета индикатора. Ведь наш глаз замечает смешанный цвет не только при условии равенства концентраций молекулярных и ионных форм индикатора, но и когда концентрация одной из форм преобладает над другой в 10 раз (lg 10 = 1). HInd ↔ Ind- + H+ нейтральная форма окраска 1 (при р. Н < p. Ka – 1) смесь форм заряженная форма переходная окраска 2 окраска (при р. Н > p. Ka + 1) (Δр. Н = p. Ka ± 1) 38
 Таблица 3. Примеры индикаторов. Окраска II Смешанная окраска (в точке р. Т 1) фенолфталеин бесцветный яркомалиновый розовый метилоранж красный жёлтый оранжевый лакмус красный синий фиолетовый Индикатор 39
Таблица 3. Примеры индикаторов. Окраска II Смешанная окраска (в точке р. Т 1) фенолфталеин бесцветный яркомалиновый розовый метилоранж красный жёлтый оранжевый лакмус красный синий фиолетовый Индикатор 39
 Протолитическая теория кислот и оснований Кислоты и основания Бренстеда v Кислоты Бренстеда – это нейтральные молекулы или ионы, способные отдавать протон водорода (доноры Н+). v Основания Бренстеда – это нейтральные молекулы или ионы, способные принимать протон водорода (акцепторы Н+). 40
Протолитическая теория кислот и оснований Кислоты и основания Бренстеда v Кислоты Бренстеда – это нейтральные молекулы или ионы, способные отдавать протон водорода (доноры Н+). v Основания Бренстеда – это нейтральные молекулы или ионы, способные принимать протон водорода (акцепторы Н+). 40
 # Существенно, что основность, с точки зрения протолитической теории, проявляется только в присутствии кислоты, а кислотность – в присутствии основания: . . В + АН ⇆ +ВН + А⁻ (21) Осн. К-та 2 1 К-та 1 Осн. 2 Сопряжённая кислотно-основная пара – это две формы одного и того же соединения, отличающиеся на один Н+. v Записывается сопряжённая пара так: + . . кислота/ основание. В данном случае ВН/ В и АН/А⁻ - две сопряжённые кислотно-основные пары в одной реакции 41
# Существенно, что основность, с точки зрения протолитической теории, проявляется только в присутствии кислоты, а кислотность – в присутствии основания: . . В + АН ⇆ +ВН + А⁻ (21) Осн. К-та 2 1 К-та 1 Осн. 2 Сопряжённая кислотно-основная пара – это две формы одного и того же соединения, отличающиеся на один Н+. v Записывается сопряжённая пара так: + . . кислота/ основание. В данном случае ВН/ В и АН/А⁻ - две сопряжённые кислотно-основные пары в одной реакции 41
 Кислотно-основное взаимодействие — это перенос Н+ с кислоты на основание, с образованием новой кислоты и нового основания, сопряжённых исходным. !!! Сильной кислоте соответствует слабое сопряжённое основание, и наоборот. 42
Кислотно-основное взаимодействие — это перенос Н+ с кислоты на основание, с образованием новой кислоты и нового основания, сопряжённых исходным. !!! Сильной кислоте соответствует слабое сопряжённое основание, и наоборот. 42
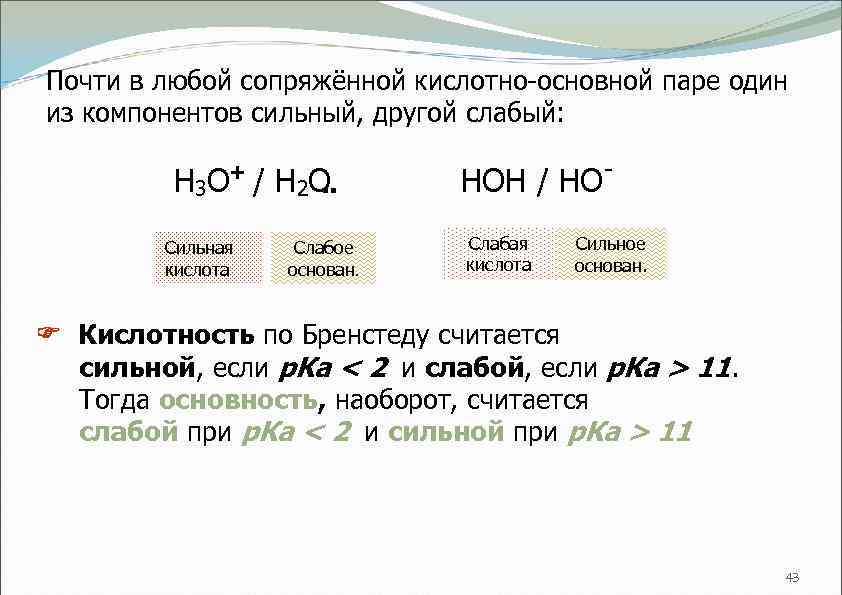 Почти в любой сопряжённой кислотно-основной паре один из компонентов сильный, другой слабый: + Н 3 О / Н 2 О. . Сильная кислота Слабое основан. НОН / НО¯ Слабая кислота Сильное основан. Кислотность по Бренстеду считается сильной, если р. Ка < 2 и слабой, если р. Ка > 11. Тогда основность, наоборот, считается слабой при р. Ка < 2 и сильной при р. Ка > 11 43
Почти в любой сопряжённой кислотно-основной паре один из компонентов сильный, другой слабый: + Н 3 О / Н 2 О. . Сильная кислота Слабое основан. НОН / НО¯ Слабая кислота Сильное основан. Кислотность по Бренстеду считается сильной, если р. Ка < 2 и слабой, если р. Ка > 11. Тогда основность, наоборот, считается слабой при р. Ка < 2 и сильной при р. Ка > 11 43
 Силовая характеристика кислотно-основных свойств р. Ка - показатель кислотности, характеризующий оба компонента этой пары: чем меньше р. Ка , тем сильнее кислотность и слабее основность в данной сопряжённой паре. Так, . . р. Ка(Н 3 О+ / Н 2 О) = -1, 7 В этой паре очень сильная кислотность (Н 3 О+) и очень слабая основность (Н 2 О). 44
Силовая характеристика кислотно-основных свойств р. Ка - показатель кислотности, характеризующий оба компонента этой пары: чем меньше р. Ка , тем сильнее кислотность и слабее основность в данной сопряжённой паре. Так, . . р. Ка(Н 3 О+ / Н 2 О) = -1, 7 В этой паре очень сильная кислотность (Н 3 О+) и очень слабая основность (Н 2 О). 44
 Гидролиз солей v. Гидролиз солей – это реакция обменного разложения между солью и водой. v. Гидролиз солей – это реакция взаимодействия ионов слабого электролита, входящего в состав соли, с водой, в результате которой получается слабый электролит. v. Гидролиз соли – это слабое кислотноосновное взаимодействие ионов соли с водой, приводящее к разрушению не только соли, но и воды. 45
Гидролиз солей v. Гидролиз солей – это реакция обменного разложения между солью и водой. v. Гидролиз солей – это реакция взаимодействия ионов слабого электролита, входящего в состав соли, с водой, в результате которой получается слабый электролит. v. Гидролиз соли – это слабое кислотноосновное взаимодействие ионов соли с водой, приводящее к разрушению не только соли, но и воды. 45
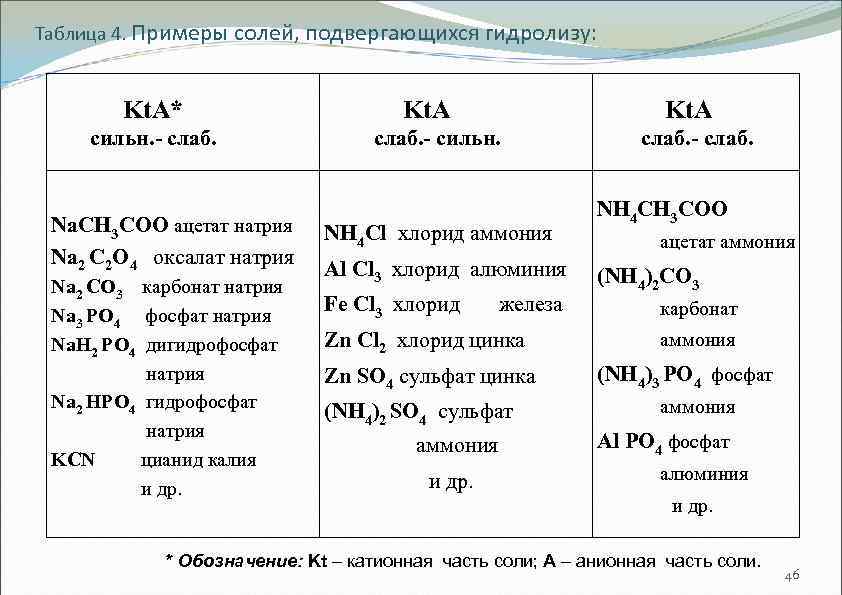 Таблица 4. Примеры солей, подвергающихся гидролизу: Kt. A* сильн. - слаб. Na. CH 3 COO ацетат натрия Na 2 C 2 O 4 оксалат натрия Na 2 CO 3 карбонат натрия Na 3 PO 4 фосфат натрия Na. H 2 PO 4 дигидрофосфат натрия Na 2 HPO 4 гидрофосфат натрия KCN цианид калия и др. Kt. A слаб. - сильн. NH 4 Cl хлорид аммония Al Cl 3 хлорид алюминия Fe Cl 3 хлорид железа Zn Cl 2 хлорид цинка Zn SO 4 сульфат цинка (NH 4)2 SO 4 сульфат аммония и др. слаб. - слаб. NH 4 CH 3 COO ацетат аммония (NH 4)2 CO 3 карбонат аммония (NH 4)3 PO 4 фосфат аммония Al PO 4 фосфат алюминия и др. * Обозначение: Kt – катионная часть соли; A – анионная часть соли. 46
Таблица 4. Примеры солей, подвергающихся гидролизу: Kt. A* сильн. - слаб. Na. CH 3 COO ацетат натрия Na 2 C 2 O 4 оксалат натрия Na 2 CO 3 карбонат натрия Na 3 PO 4 фосфат натрия Na. H 2 PO 4 дигидрофосфат натрия Na 2 HPO 4 гидрофосфат натрия KCN цианид калия и др. Kt. A слаб. - сильн. NH 4 Cl хлорид аммония Al Cl 3 хлорид алюминия Fe Cl 3 хлорид железа Zn Cl 2 хлорид цинка Zn SO 4 сульфат цинка (NH 4)2 SO 4 сульфат аммония и др. слаб. - слаб. NH 4 CH 3 COO ацетат аммония (NH 4)2 CO 3 карбонат аммония (NH 4)3 PO 4 фосфат аммония Al PO 4 фосфат алюминия и др. * Обозначение: Kt – катионная часть соли; A – анионная часть соли. 46
 Расчет р. Н растворов солей Для солей, гидролизующихся по аниону (р. Н > 7) р. Н = 7 + Для солей, гидролизующихся по катиону (р. Н < 7) р. Н = 7 Для солей, гидролизующихся по катиону и аниону (р. Н ≈ 7) р. Н = 7 +
Расчет р. Н растворов солей Для солей, гидролизующихся по аниону (р. Н > 7) р. Н = 7 + Для солей, гидролизующихся по катиону (р. Н < 7) р. Н = 7 Для солей, гидролизующихся по катиону и аниону (р. Н ≈ 7) р. Н = 7 +
 Степень гидролиза – это отношение числа гидролизованных молекул соли к общему числу растворённых молекул (выражается в долях к единице или в процентах). Степень гидролиза α зависит: ü от природы соли (характеристики р. Ка и р. Кb). ü от температуры (повышается t 0 - растёт гидролиз, так как гидролиз – это эндотермический процесс); ü от концентрации (чем меньше концентрация соли, тем лучше идёт гидролиз); ü от р. Н среды: кислоты и щёлочи будут усиливать определённый тип гидролиза (соответственно, по аниону или катиону, а также по обоим ионам). 48
Степень гидролиза – это отношение числа гидролизованных молекул соли к общему числу растворённых молекул (выражается в долях к единице или в процентах). Степень гидролиза α зависит: ü от природы соли (характеристики р. Ка и р. Кb). ü от температуры (повышается t 0 - растёт гидролиз, так как гидролиз – это эндотермический процесс); ü от концентрации (чем меньше концентрация соли, тем лучше идёт гидролиз); ü от р. Н среды: кислоты и щёлочи будут усиливать определённый тип гидролиза (соответственно, по аниону или катиону, а также по обоим ионам). 48
 Литература Основная: 1. Слесарев В. И. – Химия: Основы химии живого: Учебник для вузов. – 3 -е изд. , испр. – СПб: Химиздат. – 2007. – 784 с Дополнительная: Пузаков С. А. – Химия: Учебник, 2 -е изд. испр. и доп. М. : ГЭОТАР-Медиа Медицина, - 2006. – 624 с Артеменко А. И. – Справочное руководство по химии. – М. : Высшая школа, 2003 49
Литература Основная: 1. Слесарев В. И. – Химия: Основы химии живого: Учебник для вузов. – 3 -е изд. , испр. – СПб: Химиздат. – 2007. – 784 с Дополнительная: Пузаков С. А. – Химия: Учебник, 2 -е изд. испр. и доп. М. : ГЭОТАР-Медиа Медицина, - 2006. – 624 с Артеменко А. И. – Справочное руководство по химии. – М. : Высшая школа, 2003 49
 Литература Электронные ресурсы: 1. Электронный каталог Крас ГМУ 2. Электронная библиотека по дисциплине химия: общая и неорганическая. -/ гл. ред. М. А. Пальцев. -М. : Русский врач, 2005 3. Ресурсы Интернет 50
Литература Электронные ресурсы: 1. Электронный каталог Крас ГМУ 2. Электронная библиотека по дисциплине химия: общая и неорганическая. -/ гл. ред. М. А. Пальцев. -М. : Русский врач, 2005 3. Ресурсы Интернет 50


