ХИМИЯ растворы неэлектролитов и электролитов.ppt
- Количество слайдов: 48

Растворы. Коллигативные свойства растворов.

Существование абсолютно чистых веществ невозможно – любое вещество обязательно содержит примеси, т. е. гомогенная система многокомпонентна. Если имеющиеся в веществе примеси в пределах точности описания системы не оказывают влияния на изучаемые свойства, можно считать систему однокомпонентной; в противном случае гомогенную систему считают раствором. Раствор – гомогенная система, состоящая из двух или более компонентов, состав которой может непрерывно изменяться в некоторых пределах без изменения её свойств.

Раствор может иметь любое агрегатное состояние, поэтому различают твердые, жидкие и газообразные (последние называют газовыми смесями) растворы. Компонентами раствора являются растворитель и растворенное вещество. Растворителем считают компонент, присутствующий в растворе в большем количестве или компонент, который кристаллизуется первым при охлаждении раствора; если одним из компонентов раствора является жидким в чистом виде веществом, а остальные – твердыми веществами или газами, то растворителем считают жидкость.

Существуют вещества с неограниченной способностью растворяться друг в друге (например, серная кислота и вода или этиловый спирт и вода) и с ограниченной способностью. Для количественной характеристики одного вещества ограниченно растворяться в другом пользуются понятием растворимость, которая выражается концентрацией насыщенного раствора.

1)Насыщенный раствор получается, когда дальнейшее растворение данного компонента в растворе прекращается. В насыщенном растворе концентрация данного компонента максимальна при данных условиях. Насыщенный раствор всегда должен находиться в равновесии с кристаллическим компонентом (осадком). Концентрация этого компонента в растворе называется его растворимостью (обозначается как Р, выраженная в г/100 г растворителя дается в справочниках). Растворимость вещества увеличивается с повышением температуры и при перемешивании.

2)Раствор, в котором концентрация этого компонента ниже его растворимости, называется ненасыщенным. Такие растворы гомогенны. 3)Раствор, в котором концентрация растворенного вещества выше его растворимости, называется пересыщенным. Их получают при переохлаждении раствора ниже температуры, при которой он становится насыщенным. Такой раствор является гетерогенным, т. к. при понижении температуры появляется фаза компонента и фаза растворителя.

Для большинства веществ растворимость значительно зависит от температуры. Для определения растворимости при разных температурах используют справочные таблицы или кривые растворимости. Если приготовить насыщенный раствор при температуре t 2, содержащий m 2 г вещества на 100 г воды, а затем охладить до температуры t 1, при которой растворимость составляет m 1 г, то выпадет осадок (при условии, что не произошло переохлаждения и не образовался пересыщенный раствор) массой (m – m ) г.
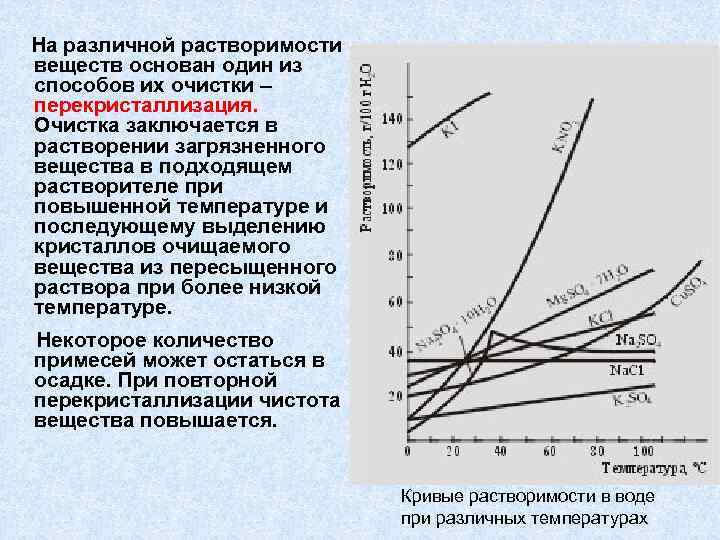
На различной растворимости веществ основан один из способов их очистки – перекристаллизация. Очистка заключается в растворении загрязненного вещества в подходящем растворителе при повышенной температуре и последующему выделению кристаллов очищаемого вещества из пересыщенного раствора при более низкой температуре. Некоторое количество примесей может остаться в осадке. При повторной перекристаллизации чистота вещества повышается. Кривые растворимости в воде при различных температурах

В общем случае при растворении происходит изменение свойств растворителя и растворенного вещества, что обусловлено взаимодействием частиц между собой по различным типам взаимодействия. Очевидно, что чем больше концентрация раствора, тем интенсивнее взаимодействие частиц. Поэтому количественная теория разработана только для идеальных растворов (газовые растворы и растворы неполярных жидкостей), в которых энергия взаимодействия разнородных частиц близка к энергиям взаимодействия одинаковых частиц. Идеальными считаются и бесконечно разбавленные растворы.

Идеальные растворы – это растворы, в которых можно пренебречь взаимодействием частиц растворителя и растворенного вещества между собой. Свойства таких растворов зависят только от концентрации растворенного вещества, но не зависят от его природы. Такие свойства называются коллигативными.

Растворимость газов в газах Газообразное состояние вещества характеризуется слабым взаимодействием между частицами за счет больших расстояний между ними. Поэтому газы смешиваются в любых соотношениях (при очень высоких давлениях, когда плотность газов приближается к плотности жидкостей, может наблюдаться ограниченная растворимость). Газовые смеси описываются законом Дальтона: Общее давление газовой смеси равно сумме парциальных давлений всех входящих в неё газов. Парциальное давление газа в смеси – это давление, которое производил бы этот газ, занимая при тех же условиях объем всей газовой смеси.

Растворимость газов в жидкостях зависит от ряда факторов: -природы газа и жидкости, -температуры, -давления, -концентрации растворенных в жидкости веществ. Наибольшее влияние на растворимость газов в жидкостях оказывает природа веществ. Так, в 1 л воды (t = 18 °С, P = 1 атм) растворяется 0. 017 л N 2, 748. 8 л NH 3 или 427. 8 л HCl. Аномально высокая растворимость газов в жидкостях обусловливается их специфическим взаимодействием с растворителем – образованием химического соединения или диссоциацией в растворе на ионы. Газы, молекулы которых неполярны, растворяются, как правило, лучше в неполярных жидкостях – и наоборот.

Зависимость растворимости газов от давления выражается законом Генри – Дальтона: Растворимость газа в жидкости прямо пропорциональна его давлению над жидкостью. С = к · Р где С – концентрация раствора газа в жидкости, k – коэффициент пропорциональности, зависящий от природы газа. Закон Генри – Дальтона справедлив только для разбавленных растворов при малых давлениях, когда газы можно считать идеальными. Газы, способные к специфическому взаимодействию с растворителем, данному закону не подчиняются.

Взаимная растворимость жидкостей В зависимости от природы жидкости могут смешиваться в любых соотношениях (неограниченная взаимная растворимость), быть практически нерастворимыми друг в друге или обладать ограниченной растворимостью. Например, для системы анилин – вода при смешивании равных количеств воды и анилина, система состоит из двух слоев жидкости: верхний слой – раствор анилина в воде, нижний – раствор воды в анилине. Для каждой температуры оба раствора имеют строго определенный состав, не зависящий от количества каждого из веществ.
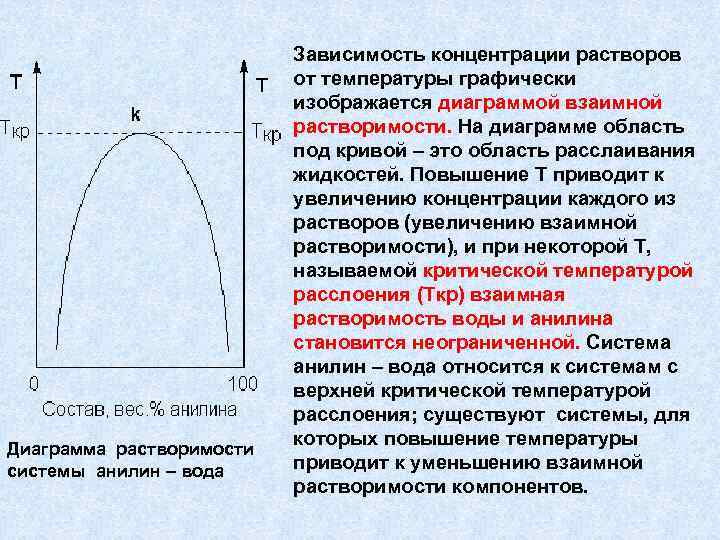
Диаграмма растворимости системы анилин – вода Зависимость концентрации растворов от температуры графически изображается диаграммой взаимной растворимости. На диаграмме область под кривой – это область расслаивания жидкостей. Повышение Т приводит к увеличению концентрации каждого из растворов (увеличению взаимной растворимости), и при некоторой Т, называемой критической температурой расслоения (Ткр) взаимная растворимость воды и анилина становится неограниченной. Система анилин – вода относится к системам с верхней критической температурой расслоения; существуют системы, для которых повышение температуры приводит к уменьшению взаимной растворимости компонентов.

Растворимость твердых веществ в жидкостях определяется природой веществ и зависит от температуры. Качественным обобщением данных по растворимости является принцип "подобное в подобном": полярные растворители хорошо растворяют полярные вещества и плохо – неполярные, и наоборот.

Кривые растворимости некоторых солей в воде. 1 – КNО 3, 2 – Nа 2 SО 4· 10 Н 2 О, 3 – Nа 2 SО 4, 4 – Ва(NО 3)2 Зависимость растворимости Р от температуры обычно изображают графически в виде кривых растворимости. Теплота растворения твердых веществ в жидкостях может быть как положительной, так и отрицательной, следовательно, Р при увеличении Т может увеличиваться или уменьшаться.

Общие свойства растворов Зная свойства растворов, можно ответить на вопросы: Когда следует солить воду при варке картофеля – в начале или в конце? Что делать, если в радиатор автомобиля залита вода, а ночью обещают мороз – 10 °С, от которого мотор и радиатор разорвет замерзшая вода? Почему в пустыне среди сухих песков растут кактусы? Почему при купании в морской воде глаза не болят? Почему в варенье непроколотые сливы или вишни сморщиваются, а в компоте, наоборот, раздуваются и лопаются?

Давление насыщенного пара Одно из важнейших свойств жидкостей и растворов (и вообще всех веществ) – давление насыщенного пара вещества над поверхностью жидкости (или кристалла). Давление насыщенного пара воды имеет огромное значение для жизни природы. Листья на деревьях высыхают, когда давление паров воды в воздухе становится ниже некоторого предела. Выстиранное белье на берегу моря почти не сохнет. И такое же белье на морозе высыхает быстрее, чем при обычной температуре. Здесь мы имеем дело с давлением пара воды. Давление пара над раствором отличается от давления пара над чистым растворителем.

Допустим, что происходит испарение чистой жидкости А (рис. а) и раствора, состоящего из растворителя А и растворенного вещества В. При растворении вещества В в растворителе А число молекул А в единице объема жидкости уменьшается, а значит, снижается и их число, приходящееся на единицу поверхности испаряющейся жидкости (рис. б). Изза этого уменьшается скорость испарения растворителя и снижается давление (парциальное) насыщенного пара растворителя над раствором. Пар над чистым растворителем (а) и раствором (б) В системе, состоящей из растворителя А протекают одновременно процессы испарения и конденсации, которые находятся в состоянии динамического равновесия; при добавлении вещества В это равновесие нарушается и вновь устанавливается, но уже при другом давлении. Вывод: чем меньше мольная доля компонента А в растворе, тем меньше парциальное давление его насыщенных паров над раствором.

Для некоторых растворов выполняется закономерность, называемая первым законом Рауля: Парциальное давление насыщенного пара компонента раствора прямо пропорционально его мольной доле в растворе, причем коэффициент пропорциональности равен давлению насыщенного пара над чистым компонентом. Рi = P 0 i · Ni где Ni - мольная доля вещества в растворе, Р 0 i - давление насыщенного пара чистого вещества.

Поскольку сумма мольных долей всех компонентов раствора равна 1, для раствора, состоящего из компонентов А и В получают следующее соотношение, также являющееся формулировкой первого закона Рауля: Относительное понижение давления пара растворителя над раствором равно мольной доле растворенного вещества и не зависит от природы растворенного вещества. P 0 A – PA/ PA = NB

Растворы, для которых выполняется закон Рауля, называют идеальными растворами. Идеальный раствор – это раствор, в котором силы всех межмолекулярных взаимодействий молекул растворителя и растворенных веществ одинаковы. Идеальный раствор образуется без выделения или поглощения теплоты (∆Н = 0) и его объем в точности равен объемам смешиваемых компонентов (∆V = 0). Идеальными при любых концентрациях являются растворы, компоненты которых близки по физическим и химическим свойствам.

Давление пара идеальных и реальных растворов Если компоненты бинарного раствора летучи, то пар над раствором будет содержать оба компонента. Для раствора, состоящего из компонентов А и В, неограниченно растворимых друг в друге, общее давление пара согласно первому закону Рауля, равно: Р = Р 0 А ·NA+P 0 B·NB = P 0 B + P 0 A·(1 - NB) = = P 0 A – NB ·(P 0 A – P 0 B)
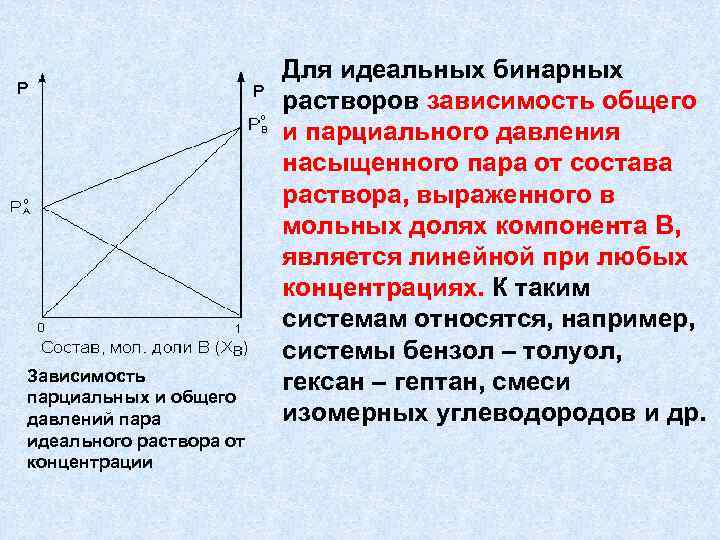
Зависимость парциальных и общего давлений пара идеального раствора от концентрации Для идеальных бинарных растворов зависимость общего и парциального давления насыщенного пара от состава раствора, выраженного в мольных долях компонента В, является линейной при любых концентрациях. К таким системам относятся, например, системы бензол – толуол, гексан – гептан, смеси изомерных углеводородов и др.

Реальные растворы с положительными отклонениями давления пара образуются из чистых компонентов с поглощением теплоты (ΔНраств > 0), растворы с отрицательными отклонениями Зависимость парциальных и общего образуются с давлений пара идеальных (штриховая выделением теплоты линия) и реальных (сплошная линия) бинарных растворов от состава при (ΔНраств < 0). положительных (слева) и отрицательных (справа) отклонениях от закона Рауля

В природе не существует идеальных растворов. Раствор тем ближе к идеальному раствору, чем он сильнее разбавлен. Давление насыщенного пара растворителя над идеальным раствором меньше, чем над чистым растворителем. И оно тем ниже, чем выше мольная доля (или концентрация) растворенного вещества.

Давление пара чистой воды при температуре 20 °С равно 2333 Па. Раствор С 12 Н 22 О 11 с мольной долей сахарозы 0, 1, в котором мольная доля воды составляет 0, 9, имеет давление пара воды 2333 • 0, 9 = 2100 Па. Это значение верно только для идеального раствора. У реального раствора с высокой концентрацией растворенного вещества давление пара воды будет другим, но мы будем полагать, что имеем дело с идеальными растворами. Точно так же себя ведут растворы глюкозы С 6 Н 12 О 6, мочевины СО(NН 2)2 и многих других веществ (правило выполняется для растворов неэлектролитов). Если вместо сахарозы взять раствор Na. Cl с той же мольной долей вещества (0, 1), то для давление пара воды будет составлять около 1866 Па. Раствор Ca. Cl 2 с той же мольной долей имеет давление пара воды ~ 1633 Па. Для раствора Аl. Cl 3 й давление насыщенного пара воды составляет около 1400 Па.
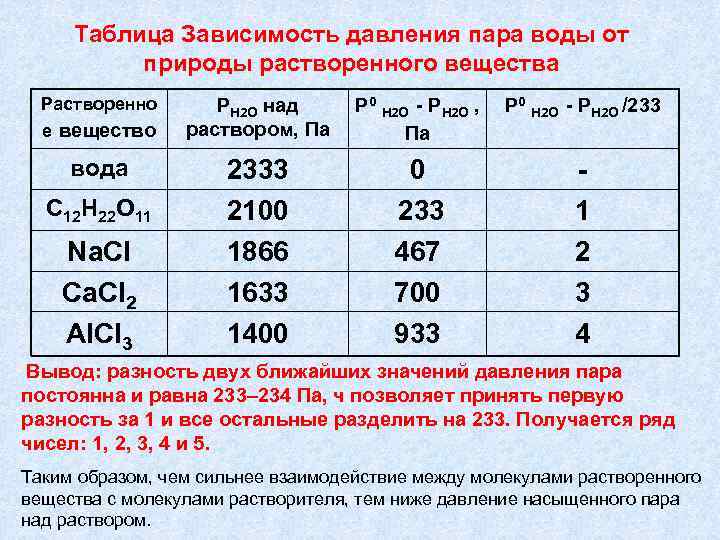
Таблица Зависимость давления пара воды от природы растворенного вещества Растворенно е вещество вода С 12 Н 22 О 11 Na. Cl Ca. Cl 2 Al. Cl 3 РН 2 О над раствором, Па Р 0 Н 2 О - РН 2 О /233 2333 2100 1866 1633 1400 0 233 467 700 933 1 2 3 4 Вывод: разность двух ближайших значений давления пара постоянна и равна 233– 234 Па, ч позволяет принять первую разность за 1 и все остальные разделить на 233. Получается ряд чисел: 1, 2, 3, 4 и 5. Таким образом, чем сильнее взаимодействие между молекулами растворенного вещества с молекулами растворителя, тем ниже давление насыщенного пара над раствором.

Для окончательного вывода воспользуемся методом, связанным с электропроводностью. При помещении электродов в чистую воду и растворы тех же веществ с той же мольной долей растворов пропускается электрический ток. Вода и раствор сахарозы (раствор неэлектролита) электрический ток почти не проводят, остальные растворы – хорошие проводники электрического тока (растворы электролитов). При сравнении электропроводности растворов Са. Cl 2 и Na. Cl оказывается, что электропроводность раствора Са. Cl 2 примерно в 2 раза выше электропроводности раствора Na. Cl той же концентрации, что объясняется в 2 раза большей концентрацией Сl--ионов в растворе Са. Cl 2 и в 2 раза большим зарядом иона Са 2+ по сравнению с зарядом иона натрия Nа+.

Сравнение электропроводностей растворов Al. Cl 3 и Na. Cl показывает, что электропроводность раствора Al. Cl 3 примерно в 3 раза выше, чем для раствора Na. Cl. Объяснение то же: в растворе Al. Cl 3 в 3 раза больше Сl--ионов, чем в растворе Na. Cl той же концентрации и заряд иона Аl 3+ в 3 раза выше заряда иона Nа+. Если принять электропроводность раствора хлорида натрия Na. Cl за единицу, то электропроводность раствора хлорида кальция Са. Cl 2 будет в два раза выше, а электропроводность раствора хлорида алюминия Al. Cl 3 – в три раза выше.

Многие другие методы исследования растворов подтверждают существование в природе веществ, которые не распадаются на ионы в водном растворе и распадаются, т. е. диссоциируют. Вещества, не диссоциирующие в водном растворе на ионы и не проводящие электрический ток, называются неэлектролитами. Вещества, которые распадаются на ионы в водном растворе и проводят электрический ток, называются электролитами.
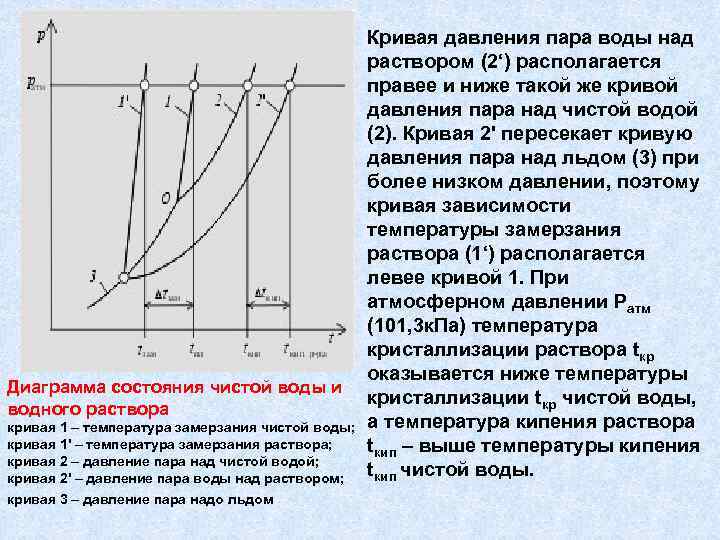
Диаграмма состояния чистой воды и водного раствора кривая 1 – температура замерзания чистой воды; кривая 1' – температура замерзания раствора; кривая 2 – давление пара над чистой водой; кривая 2' – давление пара воды над раствором; кривая 3 – давление пара надо льдом Кривая давления пара воды над раствором (2‘) располагается правее и ниже такой же кривой давления пара над чистой водой (2). Кривая 2' пересекает кривую давления пара над льдом (3) при более низком давлении, поэтому кривая зависимости температуры замерзания раствора (1‘) располагается левее кривой 1. При атмосферном давлении Ратм (101, 3 к. Па) температура кристаллизации раствора tкр оказывается ниже температуры кристаллизации tкр чистой воды, а температура кипения раствора tкип – выше температуры кипения tкип чистой воды.

Таким образом, понижение давления насыщенного пара воды (растворителя) над раствором приводит к повышению температуры кипения и понижению температуры замерзания раствора по сравнению с температурами кипения и замерзания чистого растворителя. Разность температур кипения раствора (tкип. р-ра) и чистой воды (tкип) называется повышением температуры кипения раствора: ∆tкип = tкип. р-ра – tкип Разность температуры кристаллизации чистой воды tкр и температуры кристаллизации раствора tкр. р-ра называется понижением температуры замерзания раствора: ∆tзам = tкр – tкр. р-ра

Раствор кипит при условии Ратм = Рпара и не при Т = const, а в некотором интервале температур. Повышение температуры кипения раствора тем больше, чем выше концентрация растворенного вещества См: ∆tкип = Кэб · См или ∆tкип = Кэб·mрв· 1000/mр-ля·Мрв где Кэб – коэффициент пропорциональности, называемый эбулиоскопической постоянной, которая показывает на сколько градусов повышается температура кипения раствора по сравнению с температурой кипения чистого растворителя при растворении 1 моль вещества в 1 кг растворителя; См – моляльная концентрация раствора, моль/ кг mрв – масса растворенного вещества, г mр-ля – масса растворителя, г Мрв – молярная масса растворенного вещества, г/моль

Понижение температуры замерзания раствора тем значительнее, чем выше концентрация растворенного вещества См: ∆tкр = Ккр См или ∆tкр = Ккр·mрв· 1000/mр-ля·Мрв где Ккр – коэффициент пропорциональности, называемый криоскопической постоянной, которая показывает на сколько градусов ниже будет кристаллизоваться раствор по сравнению с температурой кристаллизации чистого растворителя при растворении 1 моль вещества в 1 кг растворителя; См – моляльная концентрация раствора, моль/ кг mрв – масса растворенного вещества, г mр-ля – масса растворителя, г Мрв – молярная масса растворенного вещества, г/моль

Чтобы найти численные значения коэффициентов пропорциональности Е и К, достаточно для одного раствора известной концентрации определить повышение температуры кипения и понижение температуры замерзания. Так, 0, 1 М раствор сахарозы С 12 Н 22 О 11 в воде начинает кипеть при 100, 052 °С. Следовательно, эбулиоскопическая постоянная Е воды равна: Е = ∆tкип/См = (100, 052 – 100, 000)/0, 1 = 0, 52. 0, 1 М раствор сахарозы С 12 Н 22 О 11 в воде замерзает при температуре – 0, 186 °С. Следовательно, криоскопическая постоянная К воды равна: К = ∆tкр /См = (0 – (– 0, 186)/0, 1 = 1, 86. В 1 л воды насыпали одну полную чайную ложку поваренной соли. Какова приблизительно температура кипения супа с таким содержанием соли? Чтобы картофель быстрее сварился, когда нужно солить воду: в начале варки или в конце?
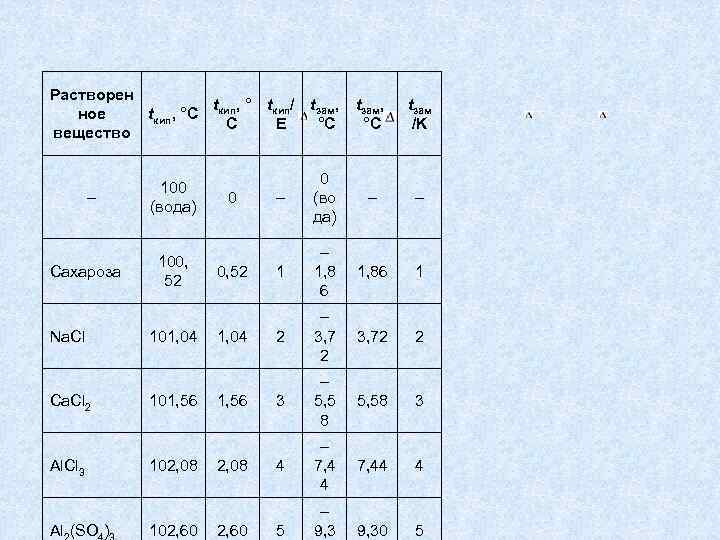
Растворен t , ° tкип/ tзам, ное tкип, °С кип С E °С вещество – Cахароза Na. Cl Са. Cl 2 Al. Cl 3 Al (SО ) 100 (вода) 100, 52 101, 04 101, 56 102, 08 102, 60 0 0, 52 1, 04 1, 56 2, 08 2, 60 tзам, °С tзам /K – 0 (во да) – – 1, 8 6 1, 86 1 2 – 3, 7 2 3, 72 2 3 – 5, 5 8 5, 58 3 4 – 7, 4 4 7, 44 4 9, 30 5 5 – 9, 3

Пример. При какой приблизительно температуре будет кристаллизоваться 40%-ный водный раствор этилового спирта С 2 Н 5 ОН? Криоскопическая константа воды 1, 86 о. Решение. По следствию из закона Рауля понижение температуры кристаллизации по сравнению с температурой кристаллизации растворителя выражаются уравнением: ∆tкр = Ккр Сm, Сm= р. в. /mр-ля= mв-ва/(М mр-ля) Понижение температуры кристаллизации 40 %-ного раствора C 2 H 5 OН находим по формуле ∆tкр = Ккр mв-ва/(М mр-ля)= 1, 86· 40 / (46· 0, 06)= 270 Температура кристаллизации чистой воды 00 С, следовательно, температура кристаллизации раствора tкр = 0 – 27 = -270. Ответ: -27 о. С.

Все три метода исследования растворов: определение давления насыщенного пара, методы криоскопии и эбулиоскопии взаимосвязаны между собой. Среди других методов изучения растворов очень интересен метод осмотического давления. Растворенное вещество по своему поведению во многих отношениях похоже на газ, т. к. оно стремится равномерно распределиться по всему объему раствора. Если неокрашенный растворитель привести в соприкосновение с окрашенным раствором можно увидеть, что окрашенное растворенное вещество проникает в неокрашенную жидкость (растворитель), т. е. происходит диффузия.

Диффузия – переход молекул растворенного вещества через поверхность раздела в растворитель и одновременно молекул растворителя в раствор. Такую диффузию называют двухсторонней: диффузия растворенного вещества и растворителя продолжается до тех пор, пока система не придет в состояние равновесия или пока энтропия системы не станет максимальной.

Диффузия может быть односторонней, если разделить некоторый раствор и растворитель полупроницаемой перегородкой (мембраной), проницаемой для молекул растворителя и непроницаемой для молекул растворенного вещества. Если сосуд 1, закрытый внизу полупроницаемой перегородкой 2 и наполненный водным раствором какого-либо вещества, поместить в сосуд 3 с водой, то вода будет проходить из сосуда 3 в сосуд 1 (рис. ). Явление самопроизвольного перехода растворителя через полупроницаемую перегородку в раствор называется осмосом. Прибор для определения осмотического давления: 1 – сосуд с раствором; 2 – полупроницаемая перегородка; 3 – сосуд с растворителем Через некоторое время объем раствора в сосуде 1 увеличится и его уровень поднимется выше уровня растворителя в сосуде 3 на высоту h. В результате увеличения объема раствора в сосуде 1 возникает гидростатическое давление, называемое осмотическим давлением, которое количественно оценивается высотой h подъема жидкости в сосуде 1.

Процесс перехода растворителя в раствор самопроизволен, но обратный процесс самопроизвольно осуществляться не может: для разделения раствора на растворитель и растворенное вещество следует затратить работу. Если в сосуде 1 с раствором увеличить давление, то растворитель будет переходить в обратном направлении через мембрану 2 в сосуд 3. Этот процесс называется обратным осмосом, его используют для опреснения морской воды.

Осмотическое давление зависит от концентрации растворенного вещества и температуры. Так, при увеличении концентрации с сахарозы в воде в 2 раза осмотическое давление возрастает примерно в 2 раза, при увеличении концентрации c в 3 раза осмотическое давление возрастает почти во столько же и т. д. Это можно записать следующим образом: ~ с, где с – молярная концентрация, выраженная в моль/м 3 (для точности измерений пользуются моляльной концентрацией).

При повышении температуры на 1 градус осмотическое давление возрастает на 1/273 часть своего первоначального значения. При повышении температуры на 10 градусов осмотическое давление возрастает на 10/273 и т. д. При повышении температуры Т (в К) в два раза осмотическое давление возрастает также в 2 раза. Таким образом, выполняется зависимость: ~ Т. Объединяя обе зависимости (от концентрации и температуры) и вводя коэффициент пропорциональности R, получаем: = RСТ.

Эта зависимость осмотического давления от концентрации и температуры называется законом Вант-Гоффа: Осмотическое давление равно тому давлению, которое оказывало бы растворенное вещество, если бы оно, находясь в газообразном состоянии при данной температуре, занимало тот же объем, который занимает раствор. = RСТ

Пользуясь осмотическим давлением, несложно определить мольную массу вещества в растворенном состоянии. Мольная масса равна числу граммов растворенного вещества, содержащихся в 22, 4 л раствора при температуре 0 °С, когда осмотическое давление раствора равно 101 325 Па. Пример. Найти мольную массу М глюкозы, если раствор, который содержит в 250 мл 9, 04 г глюкозы, имеет осмотическое давление 4, 56 • 105 Па при температуре 0°С. Решение Воспользуемся уравнением Вант-Гоффа: = RСТ Выразим молярную концентрацию: С = /RТ С = 4, 56 • 105 /8, 314 • 273 = 200, 9 моль/л = 0, 2 моль/м 3 Выражение для молярной концентрации запишем как С = m/(M · V), тогда молярная масса глюкозы равна: M = m/ CV= 9, 04 кг /(0, 2 моль/м 3 · 250· 10 -6 м 3) = 180 кмоль/кг = 180 г/ моль Мольная масса глюкозы С 6 Н 12 О 6 равна 180 г/моль.

Осмос и осмотическое давление имеют огромное значение в биологических явлениях, т. к. оболочки клеток биологических тканей являются полупроницаемыми перегородками. Осмотическое давление клеточного сока растений изменяется от 2, 0 • 105 Па (у болотных растений) до 4, 5 • 106 Па (у степных). Вследствие осмоса вода и питательные растворы поднимаются из почвы по корням и далее по стволу растения на значительную высоту. Тканевые жидкости млекопитающих имеют осмотическое давление 6, 7 • 105– 8, 1 • 105 Па. Осмотическое давление крови млекопитающих близко к осмотическому давлению океанской воды (изотонические растворы), поэтому клетки организма сохраняют свой размер и нормально функционируют. Осмотическое давление внутри живых клеток обусловливает прочность и упругость тканей (тургор клеток), и благодаря ему осуществляется солевой обмен живой ткани с окружающей средой.
ХИМИЯ растворы неэлектролитов и электролитов.ppt