Растворы.ppt
- Количество слайдов: 19
 Растворы и их свойства Растворы делятся: на истинные - (однородные гомогенные системы с размером частиц на уровне 10 -10 – 10 -9 м) И дисперсные -(неоднородные гетерогенные системы с размером частиц 10 -9 — 10 -6 м). Истинным раствором называется термодинамически устойчивая гомогенная равновесная система переменного состава, состоящая из двух и более компонентов.
Растворы и их свойства Растворы делятся: на истинные - (однородные гомогенные системы с размером частиц на уровне 10 -10 – 10 -9 м) И дисперсные -(неоднородные гетерогенные системы с размером частиц 10 -9 — 10 -6 м). Истинным раствором называется термодинамически устойчивая гомогенная равновесная система переменного состава, состоящая из двух и более компонентов.
 • Свойства растворов: • 1. гомогенность- нет границ раздела фаз • 2. Переменность состава • 3. Термический эффект растворения • Q р-ра = Qкристал. +Q гидратации • Qкристал тратится на разрушение структуры вещества • Q гидратации выделяется за счет • гидратации
• Свойства растворов: • 1. гомогенность- нет границ раздела фаз • 2. Переменность состава • 3. Термический эффект растворения • Q р-ра = Qкристал. +Q гидратации • Qкристал тратится на разрушение структуры вещества • Q гидратации выделяется за счет • гидратации
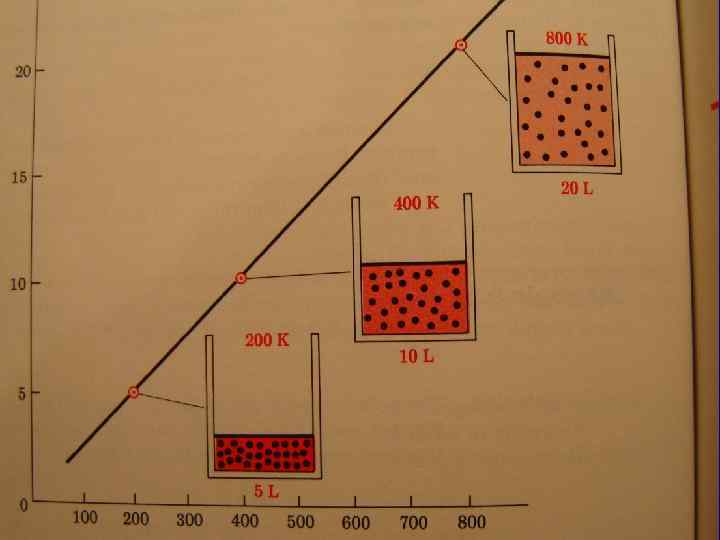
 Растворимость газов в жидкости зависит : 1) от природы газа и жидкости 2) от температуры, т. к. растворимость газа идет с выделением тепла, поэтому с повышением тепла растворимость газа уменьшается
Растворимость газов в жидкости зависит : 1) от природы газа и жидкости 2) от температуры, т. к. растворимость газа идет с выделением тепла, поэтому с повышением тепла растворимость газа уменьшается
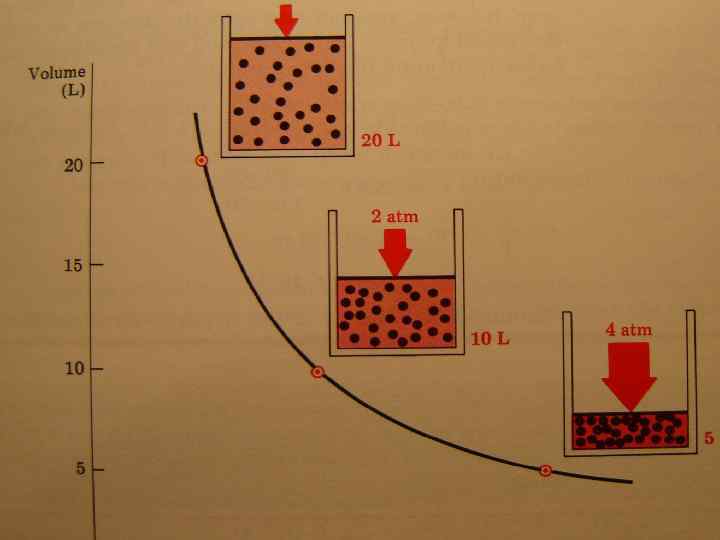
 • Влияние давления на растворимость газа в жидкости закон Генри (1803 г. ) количество газа, растворенного в определенном объеме жидкости, пропорционально давлению газа С= Кг Р, закон Дальтона Растворимость каждого из компонентов газовой смеси при постоянной температуре пропорциональна парциальному давлению компонента над жидкостью и не зависит от от общего давления смеси газов Р=Робщ Х, где Х- МОЛЬНАЯ ДОЛЯ
• Влияние давления на растворимость газа в жидкости закон Генри (1803 г. ) количество газа, растворенного в определенном объеме жидкости, пропорционально давлению газа С= Кг Р, закон Дальтона Растворимость каждого из компонентов газовой смеси при постоянной температуре пропорциональна парциальному давлению компонента над жидкостью и не зависит от от общего давления смеси газов Р=Робщ Х, где Х- МОЛЬНАЯ ДОЛЯ
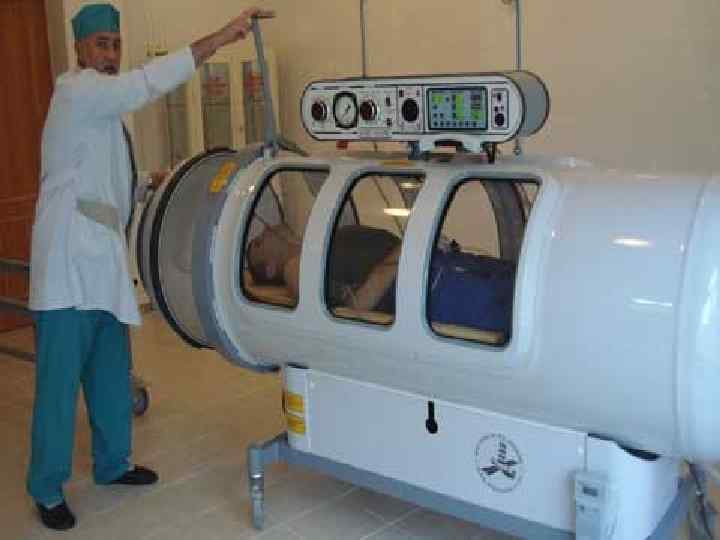
 • Применение законов Генри и Дальтона • Кессоннная болезнь- газы • закупоривают мелкие сосуды при быстром подъеме водолазов с большой глубины, что приводит к закупорке сосудов. Для лечения - барокамеры ; при повышенном давлении увеличивается концентрация кислорода в крови , что используется при лечении гангрены, сосудистой реабилитации после инсультов.
• Применение законов Генри и Дальтона • Кессоннная болезнь- газы • закупоривают мелкие сосуды при быстром подъеме водолазов с большой глубины, что приводит к закупорке сосудов. Для лечения - барокамеры ; при повышенном давлении увеличивается концентрация кислорода в крови , что используется при лечении гангрены, сосудистой реабилитации после инсультов.

 • Растворимость газов в растворах электролитов • Закон Сеченова : . Растворимость газа в растворе электролита прямо пропорциональна растворимости газа в растворителе и обратно пропорциональна концентрации электролита. • С= Со е -Кс. Сэ • где С– растворимость газа в присутствии • • • электролита со-растворимость газа в чистом растворителе, сэ -конц электролита Кс –константа Сеченова, зависящая от природы газа. электролита и Т.
• Растворимость газов в растворах электролитов • Закон Сеченова : . Растворимость газа в растворе электролита прямо пропорциональна растворимости газа в растворителе и обратно пропорциональна концентрации электролита. • С= Со е -Кс. Сэ • где С– растворимость газа в присутствии • • • электролита со-растворимость газа в чистом растворителе, сэ -конц электролита Кс –константа Сеченова, зависящая от природы газа. электролита и Т.
![Вода, свойства, биологическая роль Наше тело [по массе] на 70% состоит из воды; минимальная Вода, свойства, биологическая роль Наше тело [по массе] на 70% состоит из воды; минимальная](https://present5.com/presentation/4098870_133207947/image-11.jpg) Вода, свойства, биологическая роль Наше тело [по массе] на 70% состоит из воды; минимальная потеря воды за сутки 1700 мл, причём 50% воды выделяется из организма почками, 5% — кишечником, 13% — лёгкими, остальная вода выделяется кожей.
Вода, свойства, биологическая роль Наше тело [по массе] на 70% состоит из воды; минимальная потеря воды за сутки 1700 мл, причём 50% воды выделяется из организма почками, 5% — кишечником, 13% — лёгкими, остальная вода выделяется кожей.
 За всю жизнь человек выпивает около 25 тонн воды; вода поступает с продуктами, часть воды образуется при обмене веществ как конечный продукт. При окислении 100 г жира образуется 107 мл, 100 г углеводов — 55 мл воды 100 г белка — 41 мл воды.
За всю жизнь человек выпивает около 25 тонн воды; вода поступает с продуктами, часть воды образуется при обмене веществ как конечный продукт. При окислении 100 г жира образуется 107 мл, 100 г углеводов — 55 мл воды 100 г белка — 41 мл воды.
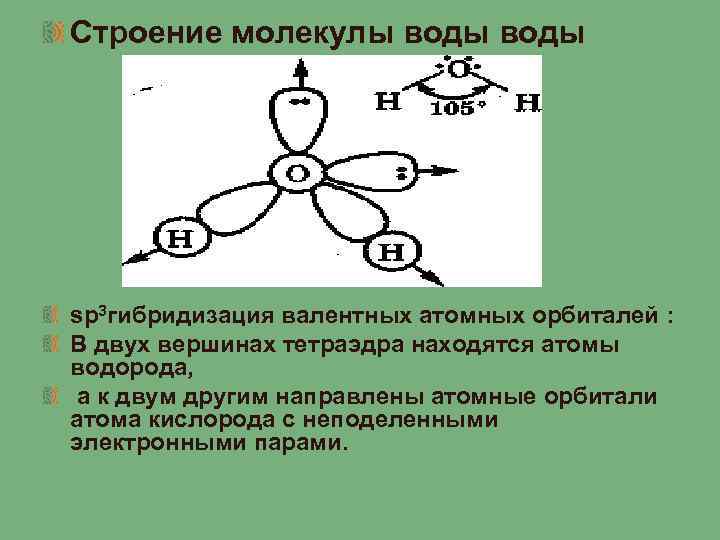 Строение молекулы воды sp 3 гибридизация валентных атомных орбиталей : В двух вершинах тетраэдра находятся атомы водорода, а к двум другим направлены атомные орбитали атома кислорода с неподеленными электронными парами.
Строение молекулы воды sp 3 гибридизация валентных атомных орбиталей : В двух вершинах тетраэдра находятся атомы водорода, а к двум другим направлены атомные орбитали атома кислорода с неподеленными электронными парами.
 Уникальные свойства воды – высокая теплоемкость (75, 3 Дж/моль • К) и большая теплота испарения (40, 8 к. Дж/моль) обеспечивают термостатирование нашего организма. высокая диэлектрическая проницаемость воды (е = 78, 5) способствует растворению и диссоциации на ионы, что обуславливает: высокие скорости протекания биохимических реакций, быструю миграцию ионов через биологические мембраны практически мгновенную передачу нервных импульсов Причина – образование определенных структур водных ассоциатов за счет полярности воды и образованию водородных связей
Уникальные свойства воды – высокая теплоемкость (75, 3 Дж/моль • К) и большая теплота испарения (40, 8 к. Дж/моль) обеспечивают термостатирование нашего организма. высокая диэлектрическая проницаемость воды (е = 78, 5) способствует растворению и диссоциации на ионы, что обуславливает: высокие скорости протекания биохимических реакций, быструю миграцию ионов через биологические мембраны практически мгновенную передачу нервных импульсов Причина – образование определенных структур водных ассоциатов за счет полярности воды и образованию водородных связей
 Роль воды – • • 1. составная часть всех клеток и тканей организма. 2. средой, в которой протекают все химические превращения. 3. Вода — источник минеральных солей, поступающих в организм. 4. Транспортировка элементов питания и продуктов обмена 5. Вода —активный участник многих реакций обмена [например, реакций гидролиза]. 6. Механическая роль — вода облегчает скольжение трущихся поверхностей [суставов, связок, мышц и т. д. ]. 7. Испарение воды кожей — мощный фактор терморегуляции организма. 8. С водой связаны осмотические явления. 9. Только в водной среде сохраняется коллоидное состояние протоплазмы.
Роль воды – • • 1. составная часть всех клеток и тканей организма. 2. средой, в которой протекают все химические превращения. 3. Вода — источник минеральных солей, поступающих в организм. 4. Транспортировка элементов питания и продуктов обмена 5. Вода —активный участник многих реакций обмена [например, реакций гидролиза]. 6. Механическая роль — вода облегчает скольжение трущихся поверхностей [суставов, связок, мышц и т. д. ]. 7. Испарение воды кожей — мощный фактор терморегуляции организма. 8. С водой связаны осмотические явления. 9. Только в водной среде сохраняется коллоидное состояние протоплазмы.
![o В организме различают две формы воды: внутриклеточную и внеклеточную. Общая вода [70%] Внутриклеточная o В организме различают две формы воды: внутриклеточную и внеклеточную. Общая вода [70%] Внутриклеточная](https://present5.com/presentation/4098870_133207947/image-16.jpg) o В организме различают две формы воды: внутриклеточную и внеклеточную. Общая вода [70%] Внутриклеточная [50%] Интерстициальная [15%] o o Внеклеточная [20%] Внутрисосудистая [5%] Внутриклеточная вода —связанную воду протоплазмы, воду притяжения на поверхности коллоидных мицелл и воду капиллярности (в ней растворены электролиты) Внутриклеточная вода связана с К+ и РО 43 -, а для внеклеточная –Na+ , Cl-, HCO 3 Интерстициальная жидкость окружает непосредственно клетки. Внутрисосудистая жидкость — плазма крови, ликвор, лимфа (содержит белок)
o В организме различают две формы воды: внутриклеточную и внеклеточную. Общая вода [70%] Внутриклеточная [50%] Интерстициальная [15%] o o Внеклеточная [20%] Внутрисосудистая [5%] Внутриклеточная вода —связанную воду протоплазмы, воду притяжения на поверхности коллоидных мицелл и воду капиллярности (в ней растворены электролиты) Внутриклеточная вода связана с К+ и РО 43 -, а для внеклеточная –Na+ , Cl-, HCO 3 Интерстициальная жидкость окружает непосредственно клетки. Внутрисосудистая жидкость — плазма крови, ликвор, лимфа (содержит белок)
 Растворимость жидкости в жидкости: Неограниченная –(C 2 H 5 OH в H 2 O) Ограниченная –(фенол в H 2 O) Полная нерастворимость (бензол в H 2 O) Растворимость зависит: - от природы в-ва и р-ля (полярные в полярных…. ) Ø -от температуры: Ø Ø Ø Ø T
Растворимость жидкости в жидкости: Неограниченная –(C 2 H 5 OH в H 2 O) Ограниченная –(фенол в H 2 O) Полная нерастворимость (бензол в H 2 O) Растворимость зависит: - от природы в-ва и р-ля (полярные в полярных…. ) Ø -от температуры: Ø Ø Ø Ø T
 Растворимость твердых веществ в жидкости Факторы, влияющие на растворимость: u Природа вещества и растворителяля u Температура повышает эндотерм. процесс и понижает экзотерм.
Растворимость твердых веществ в жидкости Факторы, влияющие на растворимость: u Природа вещества и растворителяля u Температура повышает эндотерм. процесс и понижает экзотерм.
 Закон Нернста –Шилова: Коэффициент распределения в-ва в 2 -х несмешивающихся жидкостях есть величина постоянная при данной температуре u С I 2 в CCl 4/ С I 2 в H 2 O= К распред. =85 u Экстракция вещества – это извлечение одного из компонентов раствора с помощью растворителя, который не смешивается с раствором u
Закон Нернста –Шилова: Коэффициент распределения в-ва в 2 -х несмешивающихся жидкостях есть величина постоянная при данной температуре u С I 2 в CCl 4/ С I 2 в H 2 O= К распред. =85 u Экстракция вещества – это извлечение одного из компонентов раствора с помощью растворителя, который не смешивается с раствором u


