Растворы и их свойства.ppt
- Количество слайдов: 37
 Растворы и их свойства.
Растворы и их свойства.
 Классификация растворов по фазовому состоянию: • твердые (сплавы), • жидкие (раствор сахара в воде), • газообразные (воздух). Классификация растворов по размерам растворенных частиц: • истинный растворы (~ 1 нм), • Колойдные растворы (1 -100 нм), • Грубодисперсные (>100 нм).
Классификация растворов по фазовому состоянию: • твердые (сплавы), • жидкие (раствор сахара в воде), • газообразные (воздух). Классификация растворов по размерам растворенных частиц: • истинный растворы (~ 1 нм), • Колойдные растворы (1 -100 нм), • Грубодисперсные (>100 нм).
 Образование растворов. • Процесс растворения – обратимый процесс • раствор называется насыщенным – скорость кристаллизации равна скорости растворения, • Концентрация насыщенного раствора – мера растворимости (определяется в граммах растворенного вещества в ста граммах растворителя). • Не существует абсолютно нерастворимых веществ.
Образование растворов. • Процесс растворения – обратимый процесс • раствор называется насыщенным – скорость кристаллизации равна скорости растворения, • Концентрация насыщенного раствора – мера растворимости (определяется в граммах растворенного вещества в ста граммах растворителя). • Не существует абсолютно нерастворимых веществ.
 Растворители: • Вода универсальный и самый распространенный растворитель в неорганической химии; • Также используют безводные жидкий NH 3, HF, SO 2, CS 2, H 2 SO 4, HCl.
Растворители: • Вода универсальный и самый распространенный растворитель в неорганической химии; • Также используют безводные жидкий NH 3, HF, SO 2, CS 2, H 2 SO 4, HCl.
 Правило: • Подобное растворяется в подобном. • Минимальная (наименьшая) растворимость солей наблюдается при отношении радиусов катиона и аниона соли раной 0, 7 – 1, 1
Правило: • Подобное растворяется в подобном. • Минимальная (наименьшая) растворимость солей наблюдается при отношении радиусов катиона и аниона соли раной 0, 7 – 1, 1
 Закон Генри. Согласно Генри У. (1803 г. ) растворимость газа: где K – коэффициент пропорциональности зависящий от природы газа, растворителя и температуры.
Закон Генри. Согласно Генри У. (1803 г. ) растворимость газа: где K – коэффициент пропорциональности зависящий от природы газа, растворителя и температуры.
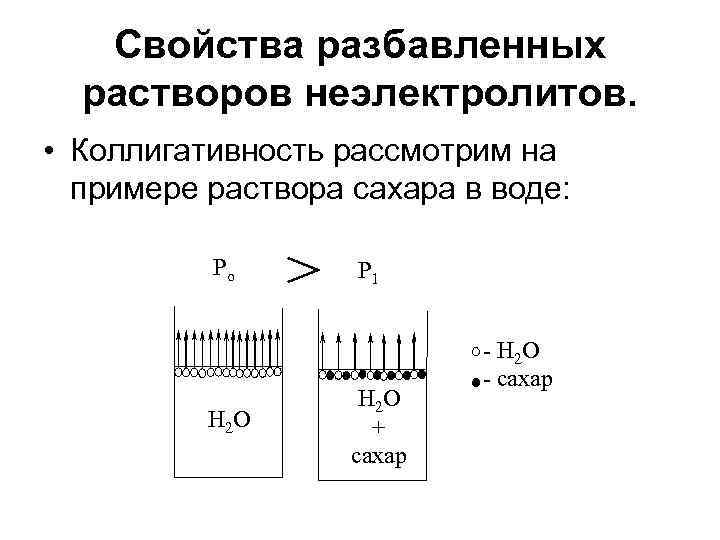 Свойства разбавленных растворов неэлектролитов. • Коллигативность рассмотрим на примере раствора сахара в воде: Po H 2 O P 1 H 2 O + сахар - H 2 O - сахар
Свойства разбавленных растворов неэлектролитов. • Коллигативность рассмотрим на примере раствора сахара в воде: Po H 2 O P 1 H 2 O + сахар - H 2 O - сахар
 Обозначения: • P 1 - парциальное (индивидуальное) давление насыщенного пара над раствором, • Po – давление насыщенного пара над чистым растворителем. • N 1 – мольная доля растворителя (H 2 O), • N 2 – мольная доля растворенного вещества (сахара), • n 1 – масса растворителя в граммах, • n 2 – масса растворенного вещества в граммах.
Обозначения: • P 1 - парциальное (индивидуальное) давление насыщенного пара над раствором, • Po – давление насыщенного пара над чистым растворителем. • N 1 – мольная доля растворителя (H 2 O), • N 2 – мольная доля растворенного вещества (сахара), • n 1 – масса растворителя в граммах, • n 2 – масса растворенного вещества в граммах.
 Закон Рауля. • Понижение давления пара растворителя (воды) над раствором равно: или
Закон Рауля. • Понижение давления пара растворителя (воды) над раствором равно: или
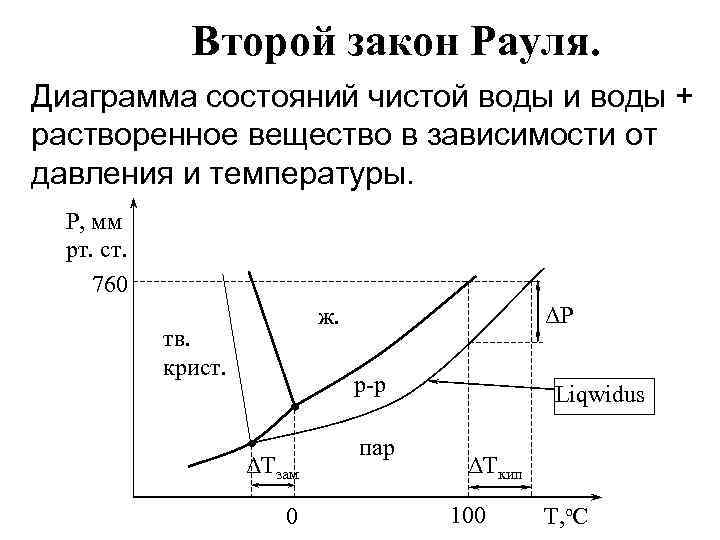 Второй закон Рауля. Диаграмма состояний чистой воды и воды + растворенное вещество в зависимости от давления и температуры. P, мм рт. ст. 760 ΔP ж. тв. крист. р-р ΔTзам 0 пар Liqwidus ΔTкип 100 T, о. С
Второй закон Рауля. Диаграмма состояний чистой воды и воды + растворенное вещество в зависимости от давления и температуры. P, мм рт. ст. 760 ΔP ж. тв. крист. р-р ΔTзам 0 пар Liqwidus ΔTкип 100 T, о. С
 Второй закон Рауля. • Второй закон Рауля для процесса кипения выражается формулой: где E – эбуллиоскопическая константа растворителя, Cm – моляльная концентрация растворенного вещества.
Второй закон Рауля. • Второй закон Рауля для процесса кипения выражается формулой: где E – эбуллиоскопическая константа растворителя, Cm – моляльная концентрация растворенного вещества.
 Второй закон Рауля. • Понижение температуры замерзания (кристаллизации) раствора определяется формулой: где K – криоскопическая постоянная растворителя, где g 1, g 2 – масса растворителя и вещества соответственно в граммах, M 2 – молекулярная масса растворенного вещества.
Второй закон Рауля. • Понижение температуры замерзания (кристаллизации) раствора определяется формулой: где K – криоскопическая постоянная растворителя, где g 1, g 2 – масса растворителя и вещества соответственно в граммах, M 2 – молекулярная масса растворенного вещества.
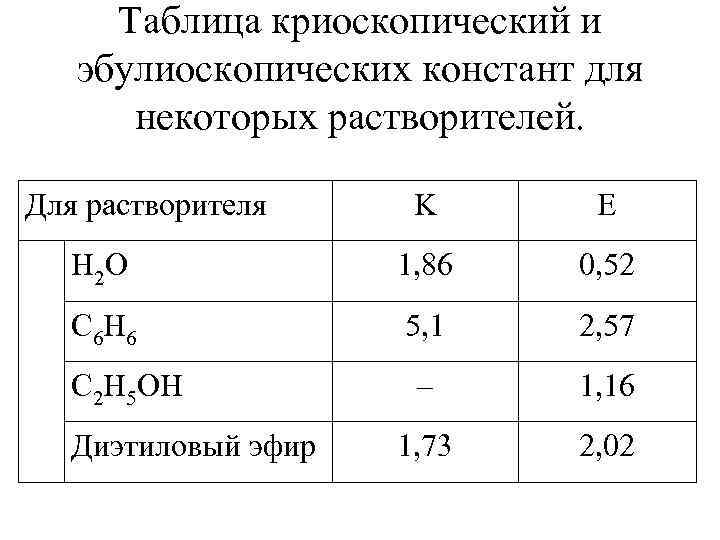 Таблица криоскопический и эбулиоскопических констант для некоторых растворителей. Для растворителя K E H 2 O 1, 86 0, 52 C 6 H 6 5, 1 2, 57 – 1, 16 1, 73 2, 02 C 2 H 5 OH Диэтиловый эфир
Таблица криоскопический и эбулиоскопических констант для некоторых растворителей. Для растворителя K E H 2 O 1, 86 0, 52 C 6 H 6 5, 1 2, 57 – 1, 16 1, 73 2, 02 C 2 H 5 OH Диэтиловый эфир
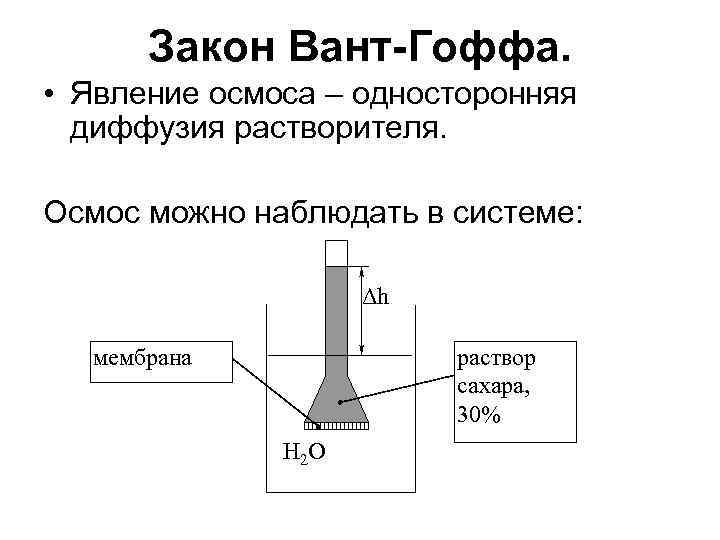 Закон Вант-Гоффа. • Явление осмоса – односторонняя диффузия растворителя. Осмос можно наблюдать в системе: Δh мембрана раствор сахара, 30% H 2 O
Закон Вант-Гоффа. • Явление осмоса – односторонняя диффузия растворителя. Осмос можно наблюдать в системе: Δh мембрана раствор сахара, 30% H 2 O
 Закон для идеальных газов: Вант-Гофф преобразовал в уравнение: где π – осмотическое давление, CM – молярная концентрация, R = 8, 31 Дж/моль·К, T – температура К, n – число молей растворенного вещества, V – объем раствора.
Закон для идеальных газов: Вант-Гофф преобразовал в уравнение: где π – осмотическое давление, CM – молярная концентрация, R = 8, 31 Дж/моль·К, T – температура К, n – число молей растворенного вещества, V – объем раствора.
 Мембрана не пропускает крупные молекулы сахара. Молекулы воды проникая через мембрану в сосуд с капилляром и поднимает уровень на высоту Δh. Осмотическое давление можно определить исходя из уравнения: где d – плотность раствора, g=9, 8 – ускорение свободного падения, Δh – высота. Δh мембрана H 2 O раствор сахара, 30%
Мембрана не пропускает крупные молекулы сахара. Молекулы воды проникая через мембрану в сосуд с капилляром и поднимает уровень на высоту Δh. Осмотическое давление можно определить исходя из уравнения: где d – плотность раствора, g=9, 8 – ускорение свободного падения, Δh – высота. Δh мембрана H 2 O раствор сахара, 30%
 Электролитическая диссоциация. • Электролиты — вещества, которые в водном растворе или расплаве существуют в виде ионов: катионов и анионов. • Растворы и расплавы электролитов проводят электрический ток. • К электролитам относятся кислоты, щелочи и соли. • Распад электролитов на ионы при растворении в воде или расплавлении называется электролитической диссоциацией.
Электролитическая диссоциация. • Электролиты — вещества, которые в водном растворе или расплаве существуют в виде ионов: катионов и анионов. • Растворы и расплавы электролитов проводят электрический ток. • К электролитам относятся кислоты, щелочи и соли. • Распад электролитов на ионы при растворении в воде или расплавлении называется электролитической диссоциацией.
 Теория электролитической диссоциации создана великим шведским ученым Сванте Аррениусом (1887) • Согласно этой теории электролиты при растворении в воде (или расплавлении) распадаются на ионы:
Теория электролитической диссоциации создана великим шведским ученым Сванте Аррениусом (1887) • Согласно этой теории электролиты при растворении в воде (или расплавлении) распадаются на ионы:
 Механизм диссоциации соединений с ионным типом связи (солей и щелочей). Схема растворения и электролитической диссоциации ионного кристалла KCl
Механизм диссоциации соединений с ионным типом связи (солей и щелочей). Схема растворения и электролитической диссоциации ионного кристалла KCl
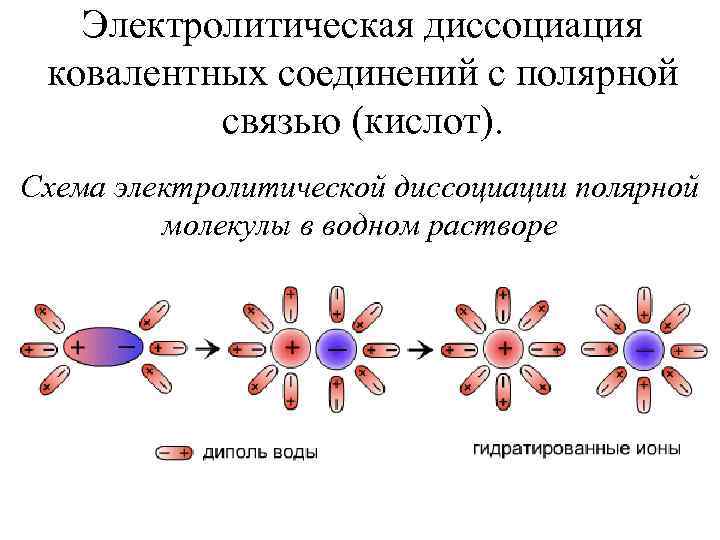 Электролитическая диссоциация ковалентных соединений с полярной связью (кислот). Схема электролитической диссоциации полярной молекулы в водном растворе
Электролитическая диссоциация ковалентных соединений с полярной связью (кислот). Схема электролитической диссоциации полярной молекулы в водном растворе
 • Вант-Гофф 1877 г. установил, что при измерении осматического давления, температуры замерзания и кипения электролитов не совпадает с расчетными выше указанными уравнениями. • Вант-Гофф ввел поправочный коэффициент – i и назвал его изотонический коэффициент.
• Вант-Гофф 1877 г. установил, что при измерении осматического давления, температуры замерзания и кипения электролитов не совпадает с расчетными выше указанными уравнениями. • Вант-Гофф ввел поправочный коэффициент – i и назвал его изотонический коэффициент.
 Законы, описывающие общие физические свойства растворов неэлектролитов и электролитов.
Законы, описывающие общие физические свойства растворов неэлектролитов и электролитов.
 При полной диссоциации электролитов изотонический коэффициент приближается к значению равному числу ионов в молекуле:
При полной диссоциации электролитов изотонический коэффициент приближается к значению равному числу ионов в молекуле:
 Исследования коэффициента i при сильном разбавлении для KCl i=1, 85 ≠ 2 Sr. Cl 2 i=2, 5 ≠ 3 CH 3 COOH i=1, 05 ≠ 2
Исследования коэффициента i при сильном разбавлении для KCl i=1, 85 ≠ 2 Sr. Cl 2 i=2, 5 ≠ 3 CH 3 COOH i=1, 05 ≠ 2
 Недостаток теории Аррениуса. • Аррениус рассматривал раствор электролита как механическую смесь из молекул растворителя, ионов и молекул электролита, не учитывалось взаимодействие между частицами. • Дальнейшее развитие теории электролитической диссоциации отражено в работах И. А. Каблукова, Нернста, Хюккеля и др.
Недостаток теории Аррениуса. • Аррениус рассматривал раствор электролита как механическую смесь из молекул растворителя, ионов и молекул электролита, не учитывалось взаимодействие между частицами. • Дальнейшее развитие теории электролитической диссоциации отражено в работах И. А. Каблукова, Нернста, Хюккеля и др.
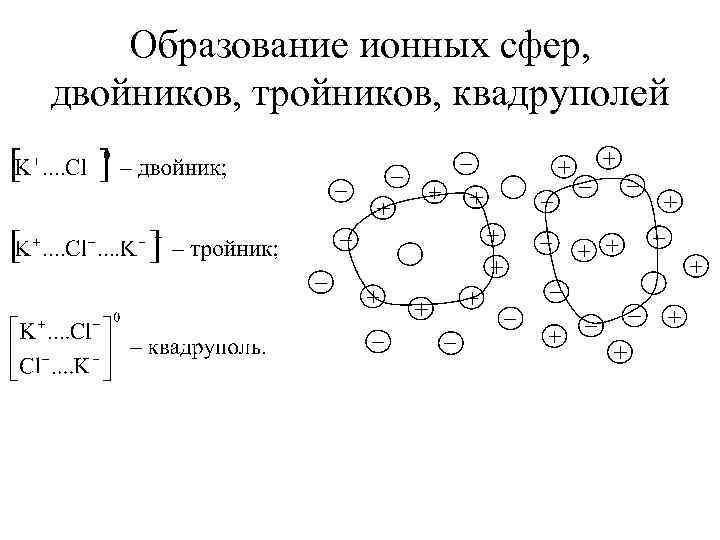 Образование ионных сфер, двойников, тройников, квадруполей
Образование ионных сфер, двойников, тройников, квадруполей
 Сильные и слабые электролиты. Электролиты условно делят на две группы: сильные и слабые, средней силы. • Сильные электролиты: почти все соли, щелочи, некоторые кислоты (HCl, HBr, HI, HNO 3, H 2 SO 4, HCl. O 4 и др. ) • Слабые и средние электролиты: HF, HCN, HCl. O, H 2 S, CH 3 COOH, раствор аммиака NH 3 и др.
Сильные и слабые электролиты. Электролиты условно делят на две группы: сильные и слабые, средней силы. • Сильные электролиты: почти все соли, щелочи, некоторые кислоты (HCl, HBr, HI, HNO 3, H 2 SO 4, HCl. O 4 и др. ) • Слабые и средние электролиты: HF, HCN, HCl. O, H 2 S, CH 3 COOH, раствор аммиака NH 3 и др.
 Количественная характеристика силы электролита - степень электролитической диссоциации (α) • Nдис - число молекул распавшихся на ионы • Nо - общее число молекул введенных в раствор (или расплав).
Количественная характеристика силы электролита - степень электролитической диссоциации (α) • Nдис - число молекул распавшихся на ионы • Nо - общее число молекул введенных в раствор (или расплав).
 • Для неэлектролитов диссоциация полностью отсутствует, α = 0. • К сильным электролитам относятся электролиты, где α>30%, к слабым α<5% и к средним 5%<α<30%. Пример: для CH 3 COOH α=1, 4%. Это значит что из 1000 молекул уксусной кислоты 14 распалось на ионы. CH 3 COOH ↔CH 3 COO– + H+ • Степень электролитической диссоциации зависит от природы электролита, его концентрации и температуры раствора. С разбавлением раствора и ростом температуры увеличивается степень электролитической диссоциации.
• Для неэлектролитов диссоциация полностью отсутствует, α = 0. • К сильным электролитам относятся электролиты, где α>30%, к слабым α<5% и к средним 5%<α<30%. Пример: для CH 3 COOH α=1, 4%. Это значит что из 1000 молекул уксусной кислоты 14 распалось на ионы. CH 3 COOH ↔CH 3 COO– + H+ • Степень электролитической диссоциации зависит от природы электролита, его концентрации и температуры раствора. С разбавлением раствора и ростом температуры увеличивается степень электролитической диссоциации.
 Для слабого электролита ставят знак обратимости: • CH 3 COOH ↔ CH 3 COO– + H+ • NH 3·H 2 O ↔ NH 4+ + OH– Для сравнения силы электролита используют константу диссоциации:
Для слабого электролита ставят знак обратимости: • CH 3 COOH ↔ CH 3 COO– + H+ • NH 3·H 2 O ↔ NH 4+ + OH– Для сравнения силы электролита используют константу диссоциации:
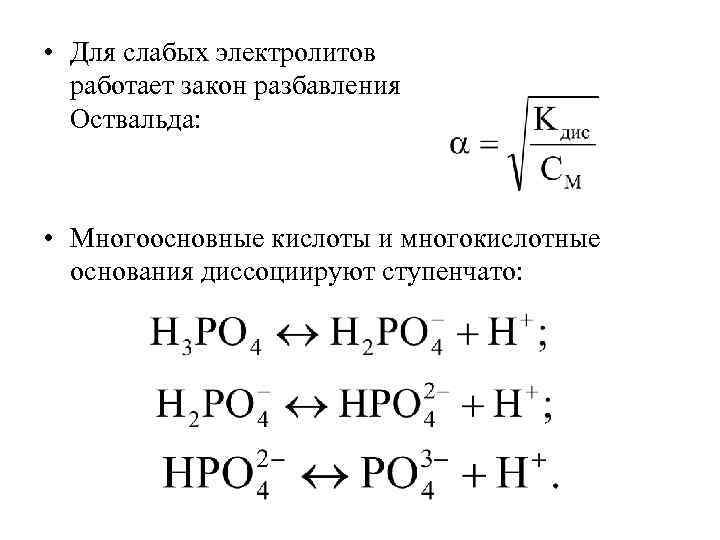 • Для слабых электролитов работает закон разбавления Оствальда: • Многоосновные кислоты и многокислотные основания диссоциируют ступенчато:
• Для слабых электролитов работает закон разбавления Оствальда: • Многоосновные кислоты и многокислотные основания диссоциируют ступенчато:
 Сильные электролиты диссоциируют теоретически на 100%. Для записи процесса диссоциации сильного электролита в уравнении обычно ставят одну стрелку:
Сильные электролиты диссоциируют теоретически на 100%. Для записи процесса диссоциации сильного электролита в уравнении обычно ставят одну стрелку:
 Константа диссоциации для сильных электролитов выражается через активность.
Константа диссоциации для сильных электролитов выражается через активность.
 Кажущаяся степень диссоциации:
Кажущаяся степень диссоциации:
 Диссоциация молекул электролитов имеющие различные виды химической связи: 1 K 2 H O O S O 3 O
Диссоциация молекул электролитов имеющие различные виды химической связи: 1 K 2 H O O S O 3 O
 Влияние диэлектрической проницаемости растворителя на распределение ионов в растворе: • вода – • этиловый спирт – По закону Кулона: распределение ионов в воде и следовательно диссоциация в воде будет сильнее, чем в спирте.
Влияние диэлектрической проницаемости растворителя на распределение ионов в растворе: • вода – • этиловый спирт – По закону Кулона: распределение ионов в воде и следовательно диссоциация в воде будет сильнее, чем в спирте.
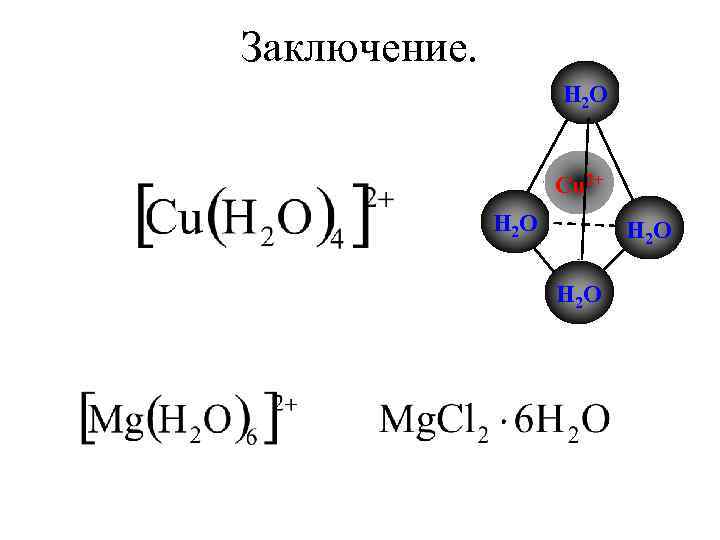 Заключение. H 2 O Cu 2+ H 2 O
Заключение. H 2 O Cu 2+ H 2 O


