ХИМИЯ Растворы электролитов.ppt
- Количество слайдов: 44
 Растворы электролитов
Растворы электролитов
 Теория электролитической диссоциации ( С. Аррениус, 1887 г. ) 1. При растворении в воде (или расплавлении) электролиты распадаются на положительно и отрицательно заряженные ионы, т. е. подвергаются диссоциации. 2. Под действием электрического тока катионы (+) двигаются к катоду (-), а анионы (-) к аноду (+). 3. Степень электролитической диссоциации (α) зависит от природы электролита и растворителя, температуры и концентрации. Она показывает долю молекул, распавшихся на ионы (Сдис) к общему числу молекул, находящихся в растворе (С). α = Сдис / С 0<α<1
Теория электролитической диссоциации ( С. Аррениус, 1887 г. ) 1. При растворении в воде (или расплавлении) электролиты распадаются на положительно и отрицательно заряженные ионы, т. е. подвергаются диссоциации. 2. Под действием электрического тока катионы (+) двигаются к катоду (-), а анионы (-) к аноду (+). 3. Степень электролитической диссоциации (α) зависит от природы электролита и растворителя, температуры и концентрации. Она показывает долю молекул, распавшихся на ионы (Сдис) к общему числу молекул, находящихся в растворе (С). α = Сдис / С 0<α<1
 Механизм электролитической диссоциации ионных веществ При растворении соединений с ионными связями процесс диссоциации начинается с ориентации диполей воды вокруг всех выступов и граней кристаллов соли. Ориентируясь вокруг ионов кристаллической решетки, молекулы воды образуют с ними или водородные, или донорно-акцепторные связи. При этом выделяется большое количество энергии (энергия гидратации). Энергия гидратации идет на разрушение кристаллической решетки. При этом гидратированные ионы переходят в растворитель и, перемешиваясь с его молекулами, образуют раствор.
Механизм электролитической диссоциации ионных веществ При растворении соединений с ионными связями процесс диссоциации начинается с ориентации диполей воды вокруг всех выступов и граней кристаллов соли. Ориентируясь вокруг ионов кристаллической решетки, молекулы воды образуют с ними или водородные, или донорно-акцепторные связи. При этом выделяется большое количество энергии (энергия гидратации). Энергия гидратации идет на разрушение кристаллической решетки. При этом гидратированные ионы переходят в растворитель и, перемешиваясь с его молекулами, образуют раствор.
 Механизм электролитической диссоциации полярных веществ Аналогично диссоциируют вещества с ковалентной полярной связью (полярные молекулы). Вокруг каждой полярной молекулы (например, HCl) определенным образом ориентируются диполи воды. В результате взаимодействия с диполями воды полярная молекула еще больше поляризуется и превращается в ионную, после чего образуются свободные гидратированные ионы.
Механизм электролитической диссоциации полярных веществ Аналогично диссоциируют вещества с ковалентной полярной связью (полярные молекулы). Вокруг каждой полярной молекулы (например, HCl) определенным образом ориентируются диполи воды. В результате взаимодействия с диполями воды полярная молекула еще больше поляризуется и превращается в ионную, после чего образуются свободные гидратированные ионы.
 При растворении в воде HCl (cвязь между атомами ковалентная сильнополярная) происходит изменение характера химической связи. Под влиянием полярных молекул воды ковалентная полярная связь превращается в ионную. Образующиеся ионы остаются связанными с молекулами воды и они называются гидратированными. Если растворитель неводный, то ионы называют сольватированными.
При растворении в воде HCl (cвязь между атомами ковалентная сильнополярная) происходит изменение характера химической связи. Под влиянием полярных молекул воды ковалентная полярная связь превращается в ионную. Образующиеся ионы остаются связанными с молекулами воды и они называются гидратированными. Если растворитель неводный, то ионы называют сольватированными.
 Электролиты и неэлектролиты Электролитическая диссоциация веществ, идущая с образованием свободных ионов объясняет электрическую проводимость растворов. Процесс электролитической диссоциации принято записывать в виде схемы, не раскрывая его механизма и опуская растворитель (H 2 O), хотя он является основным участником. Ca. Cl 2 → Ca 2+ + 2 Cl. KAl(SO 4)2 → K+ + Al 3+ + 2 SO 42 HNO 3 → H+ + NO 3 Ba(OH)2 → Ba 2+ + 2 OHИз электронейтральности молекул вытекает, что суммарный заряд катионов и анионов должен быть равен нулю.
Электролиты и неэлектролиты Электролитическая диссоциация веществ, идущая с образованием свободных ионов объясняет электрическую проводимость растворов. Процесс электролитической диссоциации принято записывать в виде схемы, не раскрывая его механизма и опуская растворитель (H 2 O), хотя он является основным участником. Ca. Cl 2 → Ca 2+ + 2 Cl. KAl(SO 4)2 → K+ + Al 3+ + 2 SO 42 HNO 3 → H+ + NO 3 Ba(OH)2 → Ba 2+ + 2 OHИз электронейтральности молекул вытекает, что суммарный заряд катионов и анионов должен быть равен нулю.
 Неэлектролиты – это вещества, водные растворы и расплавы которых не проводят электрический ток. Они содержат ковалентные неполярные или малополярные связи, вследствие чего не распадаются на ионы. Электрический ток не проводят газы, твердые вещества (неметаллы), органические соединения (сахароза, бензин, спирт).
Неэлектролиты – это вещества, водные растворы и расплавы которых не проводят электрический ток. Они содержат ковалентные неполярные или малополярные связи, вследствие чего не распадаются на ионы. Электрический ток не проводят газы, твердые вещества (неметаллы), органические соединения (сахароза, бензин, спирт).
 Электролиты: сильные и слабые Сильные электролиты - это вещества, которые при растворении в воде практически полностью распадаются на ионы (α~100%). Как правило, к сильным электролитам относятся вещества с ионными или сильно полярными связями: все хорошо растворимые соли, сильные кислоты (HCl, HBr, HI, HCl. O 4, H 2 SO 4, HNO 3) и сильные основания (Li. OH, Na. OH, KOH, Rb. OH, Cs. OH, Вa(OH)2, Sr(OH)2, Ca(OH)2). В растворе сильного электролита растворённое вещество находится в виде ионов (катионов и анионов); недиссоциированные молекулы практически отсутствуют. Ca. Cl 2 → Ca 2+ + 2 Cl. HNO 3 → H+ + NO 3 Ba(OH)2 → Ba 2+ + 2 OH-
Электролиты: сильные и слабые Сильные электролиты - это вещества, которые при растворении в воде практически полностью распадаются на ионы (α~100%). Как правило, к сильным электролитам относятся вещества с ионными или сильно полярными связями: все хорошо растворимые соли, сильные кислоты (HCl, HBr, HI, HCl. O 4, H 2 SO 4, HNO 3) и сильные основания (Li. OH, Na. OH, KOH, Rb. OH, Cs. OH, Вa(OH)2, Sr(OH)2, Ca(OH)2). В растворе сильного электролита растворённое вещество находится в виде ионов (катионов и анионов); недиссоциированные молекулы практически отсутствуют. Ca. Cl 2 → Ca 2+ + 2 Cl. HNO 3 → H+ + NO 3 Ba(OH)2 → Ba 2+ + 2 OH-
 Вещества, частично диссоциирующие в растворе на ионы, называются слабыми электролитами (α < 3%). Растворы слабых электролитов наряду с ионами содержат недиссоциированные молекулы и имеют невысокую концентрацию ионов в растворе. К слабым электролитам относятся: 1)почти все органические кислоты (CH 3 COOH, C 2 H 5 COOH и др. ) и некоторые неорганические кислоты (H 2 CO 3, H 2 S и др. ); 2) почти все малорастворимые в воде соли, основания и гидроксид аммония (Ca 3(PO 4)2; Cu(OH)2; Al(OH)3; NH 4 OH); 3)вода.
Вещества, частично диссоциирующие в растворе на ионы, называются слабыми электролитами (α < 3%). Растворы слабых электролитов наряду с ионами содержат недиссоциированные молекулы и имеют невысокую концентрацию ионов в растворе. К слабым электролитам относятся: 1)почти все органические кислоты (CH 3 COOH, C 2 H 5 COOH и др. ) и некоторые неорганические кислоты (H 2 CO 3, H 2 S и др. ); 2) почти все малорастворимые в воде соли, основания и гидроксид аммония (Ca 3(PO 4)2; Cu(OH)2; Al(OH)3; NH 4 OH); 3)вода.
 Диссоциация слабых электролитов Растворы слабых электролитов плохо (или почти не проводят) электрический ток, процесс диссоциации обратим. СH 3 COOH ↔ CH 3 COO- + H+ Cu(OH)2 ↔ [Cu. OH]+ + OH- (первая ступень) [Cu. OH]+ ↔ Cu 2+ + OH- (вторая ступень) H 2 CO 3 ↔ H+ + HCO 3 - (первая ступень) HCO 3 - ↔ H+ + CO 32 - (вторая ступень)
Диссоциация слабых электролитов Растворы слабых электролитов плохо (или почти не проводят) электрический ток, процесс диссоциации обратим. СH 3 COOH ↔ CH 3 COO- + H+ Cu(OH)2 ↔ [Cu. OH]+ + OH- (первая ступень) [Cu. OH]+ ↔ Cu 2+ + OH- (вторая ступень) H 2 CO 3 ↔ H+ + HCO 3 - (первая ступень) HCO 3 - ↔ H+ + CO 32 - (вторая ступень)
 Степень диссоциации. Константа диссоциации Концентрация ионов в растворах электролитов зависит от степени диссоциации. В растворах сильных электролитов, диссоциацию которых можно считать полной, концентрацию ионов легко определить по концентрации (c) и составу молекулы электролита (стехиометрическим индексам), например: c 2 c c H 2 SO 4 → 2 H+ + SO 42 - Концентрации ионов в растворах слабых электролитов качественно характеризуют степенью и константой диссоциации. Степень диссоциации (α) - отношение концентрации молекул, распавшихся на ионы (Сдис) к общей концентрации электролита в растворе (С): α = Сдис / С
Степень диссоциации. Константа диссоциации Концентрация ионов в растворах электролитов зависит от степени диссоциации. В растворах сильных электролитов, диссоциацию которых можно считать полной, концентрацию ионов легко определить по концентрации (c) и составу молекулы электролита (стехиометрическим индексам), например: c 2 c c H 2 SO 4 → 2 H+ + SO 42 - Концентрации ионов в растворах слабых электролитов качественно характеризуют степенью и константой диссоциации. Степень диссоциации (α) - отношение концентрации молекул, распавшихся на ионы (Сдис) к общей концентрации электролита в растворе (С): α = Сдис / С
 Степень диссоциации зависит от: 1)концентрации раствора слабого электролита: при разбавлении водой (уменьшении концентрации электролита) степень диссоциации всегда увеличивается, т. к. увеличивается число молекул H 2 O на одну молекулу растворенного вещества (выполняется принцип Ле Шателье). 2)температуры раствора: при увеличении температуры степень диссоциации растет, т. к. активируются связи в молекулах, они становятся более подвижными и легче ионизируются.
Степень диссоциации зависит от: 1)концентрации раствора слабого электролита: при разбавлении водой (уменьшении концентрации электролита) степень диссоциации всегда увеличивается, т. к. увеличивается число молекул H 2 O на одну молекулу растворенного вещества (выполняется принцип Ле Шателье). 2)температуры раствора: при увеличении температуры степень диссоциации растет, т. к. активируются связи в молекулах, они становятся более подвижными и легче ионизируются.
 Пример: Определить молярную концентрацию катионов и анионов в 0, 01 М растворах NH 4 OH, Ba(OH)2, H 2 SO 4 и CH 3 COOH. Степень диссоциации слабых электролитов α = 0, 03. Решение Ba(OH)2 и H 2 SO 4 - сильные электролиты, α = 1. Ba(OH)2 → Ba 2+ + 2 OH[Ba 2+] = 0, 01 M, [OH-] = 2 · 0, 01 = 0, 02 M H 2 SO 4 → 2 H+ + SO 42[H+] = 0, 01· 2 = 0, 02 M, [SO 42 -] = 0, 01 M NH 4 OH и CH 3 COOH – слабые электролиты (α = 0, 03) NH 4 OH↔NH 4+ + OH[NH 4+] = [OH-] = 0, 03 • 0, 01 = 0, 0003 M CH 3 COOH ↔ CH 3 COO- + H+ [H+] = [CH 3 COO-] = 0, 03 • 0, 01 = 0, 0003 M
Пример: Определить молярную концентрацию катионов и анионов в 0, 01 М растворах NH 4 OH, Ba(OH)2, H 2 SO 4 и CH 3 COOH. Степень диссоциации слабых электролитов α = 0, 03. Решение Ba(OH)2 и H 2 SO 4 - сильные электролиты, α = 1. Ba(OH)2 → Ba 2+ + 2 OH[Ba 2+] = 0, 01 M, [OH-] = 2 · 0, 01 = 0, 02 M H 2 SO 4 → 2 H+ + SO 42[H+] = 0, 01· 2 = 0, 02 M, [SO 42 -] = 0, 01 M NH 4 OH и CH 3 COOH – слабые электролиты (α = 0, 03) NH 4 OH↔NH 4+ + OH[NH 4+] = [OH-] = 0, 03 • 0, 01 = 0, 0003 M CH 3 COOH ↔ CH 3 COO- + H+ [H+] = [CH 3 COO-] = 0, 03 • 0, 01 = 0, 0003 M
 Пример: Определить концентрацию недиссоциированных молекул и ионов в 0, 1 М раствора NH 4 OH, если α = 0, 01. Решение Концентрация молекул NH 4 OH, не распавшихся на ионы, равна С - αС. Концентрация ионов NH 4+ и OH- равна концентрации продиссоциировавших молекул и равна αС NH 4 OH ↔ NH 4+ + OH- С - αС αС [NH 4+] = [OH-] = αС = 0, 01 • 0, 1 = 0, 001 моль/л [NH 4 OH] = С - αС = 0, 1 – 0, 001 = 0, 099 моль/л
Пример: Определить концентрацию недиссоциированных молекул и ионов в 0, 1 М раствора NH 4 OH, если α = 0, 01. Решение Концентрация молекул NH 4 OH, не распавшихся на ионы, равна С - αС. Концентрация ионов NH 4+ и OH- равна концентрации продиссоциировавших молекул и равна αС NH 4 OH ↔ NH 4+ + OH- С - αС αС [NH 4+] = [OH-] = αС = 0, 01 • 0, 1 = 0, 001 моль/л [NH 4 OH] = С - αС = 0, 1 – 0, 001 = 0, 099 моль/л
 Константа диссоциации (Kд) - отношение произведения равновесных концентраций ионов, образующихся при диссоциации в степенях соответствующих стехиометрических коэффициентов к концентрации недиссоциированных молекул. Она является константой равновесия процесса электролитической диссоциации: характеризует способность вещества распадаться на ионы. Чем выше Kд, тем больше концентрация ионов в растворе.
Константа диссоциации (Kд) - отношение произведения равновесных концентраций ионов, образующихся при диссоциации в степенях соответствующих стехиометрических коэффициентов к концентрации недиссоциированных молекул. Она является константой равновесия процесса электролитической диссоциации: характеризует способность вещества распадаться на ионы. Чем выше Kд, тем больше концентрация ионов в растворе.
 Диссоциации слабых многоосновных кислот или многокислотных оснований протекают по ступеням, соответственно для каждой ступени существует своя константа диссоциации: 1 ст. : H 3 PO 4 ↔ H+ + H 2 PO 4 KD 1 = ([H+][H 2 PO 4 -]) / [H 3 PO 4] = 7, 1 • 10 -3 2 ст. : H 2 PO 4 - ↔ H+ + HPO 42 K 2 D = ([H+][HPO 42 -]) / [H 2 PO 4 -] = 6, 2 • 10 -8 3 ст. : HPO 42 -↔ H+ + PO 43 KD 3 = ([H+][PO 43 -]) / [HPO 42 -] = 5, 0 • 10 -13 KD 1 > K D 2 > K D 3
Диссоциации слабых многоосновных кислот или многокислотных оснований протекают по ступеням, соответственно для каждой ступени существует своя константа диссоциации: 1 ст. : H 3 PO 4 ↔ H+ + H 2 PO 4 KD 1 = ([H+][H 2 PO 4 -]) / [H 3 PO 4] = 7, 1 • 10 -3 2 ст. : H 2 PO 4 - ↔ H+ + HPO 42 K 2 D = ([H+][HPO 42 -]) / [H 2 PO 4 -] = 6, 2 • 10 -8 3 ст. : HPO 42 -↔ H+ + PO 43 KD 3 = ([H+][PO 43 -]) / [HPO 42 -] = 5, 0 • 10 -13 KD 1 > K D 2 > K D 3
 Пример: Получить уравнение, связывающее степень электролитической диссоциации слабого электролита (α) с константой диссоциации для слабой одноосновной кислоты НА. HA↔ H+ + A+ KD = ([H+][A-]) / [HA] Общую концентрацию слабого электролита обозначим как c, равновесные концентрации Н+ и A- равны αc, а концентрация недиссоциированных молекул НА равна c - αc = c (1 - α) KD = (αc • αc) / c(1 - α) = α 2 c / (1 - α) В случае очень слабых электролитов (α 0, 01): KD = c • α 2 или α = (KD / c) (закон разбавления Оствальда)
Пример: Получить уравнение, связывающее степень электролитической диссоциации слабого электролита (α) с константой диссоциации для слабой одноосновной кислоты НА. HA↔ H+ + A+ KD = ([H+][A-]) / [HA] Общую концентрацию слабого электролита обозначим как c, равновесные концентрации Н+ и A- равны αc, а концентрация недиссоциированных молекул НА равна c - αc = c (1 - α) KD = (αc • αc) / c(1 - α) = α 2 c / (1 - α) В случае очень слабых электролитов (α 0, 01): KD = c • α 2 или α = (KD / c) (закон разбавления Оствальда)
 Реакции в растворе между ионами Реакции ионного обмена - это реакции между ионами, образовавшимися в результате диссоциации электролитов. Правила составления ионных уравнений реакций: 1. Нерастворимые в воде соединения (простые вещества, оксиды, некоторые кислоты, основания и соли) не диссоциируют (в уравнениях записываются в виде молекул). 2. Если в результате реакции образуется малорастворимое вещество, то при записи ионного уравнения его считают нерастворимым. 3. Сумма электрических зарядов ионов в левой и в правой части уравнения должна быть одинаковой.
Реакции в растворе между ионами Реакции ионного обмена - это реакции между ионами, образовавшимися в результате диссоциации электролитов. Правила составления ионных уравнений реакций: 1. Нерастворимые в воде соединения (простые вещества, оксиды, некоторые кислоты, основания и соли) не диссоциируют (в уравнениях записываются в виде молекул). 2. Если в результате реакции образуется малорастворимое вещество, то при записи ионного уравнения его считают нерастворимым. 3. Сумма электрических зарядов ионов в левой и в правой части уравнения должна быть одинаковой.
 Порядок составления ионных уравнений реакции 1. Запись молекулярного уравнения реакции: Mg. Cl 2 + 2 Ag. NO 3 ® 2 Ag. Cl + Mg(NO 3)2 2. Определение растворимости каждого из веществ с помощью таблицы растворимости p p H p Mg. Cl 2 + 2 Ag. NO 3 ® 2 Ag. Cl + Mg(NO 3)2 3. Запись полного ионного уравнения реакции (молекулы, диссоциирующие в растворе, записываются в виде ионов) Mg 2+ + 2 Cl- + 2 Ag+ + 2 NO 3 - → 2 Ag. Cl+ Mg 2+ + 2 NO 3 - 4. Запись сокращенного ионного уравнения (сокращают одинаковые ионы в правой и левой частях уравнения): Ag+ + Cl- → Ag. Cl
Порядок составления ионных уравнений реакции 1. Запись молекулярного уравнения реакции: Mg. Cl 2 + 2 Ag. NO 3 ® 2 Ag. Cl + Mg(NO 3)2 2. Определение растворимости каждого из веществ с помощью таблицы растворимости p p H p Mg. Cl 2 + 2 Ag. NO 3 ® 2 Ag. Cl + Mg(NO 3)2 3. Запись полного ионного уравнения реакции (молекулы, диссоциирующие в растворе, записываются в виде ионов) Mg 2+ + 2 Cl- + 2 Ag+ + 2 NO 3 - → 2 Ag. Cl+ Mg 2+ + 2 NO 3 - 4. Запись сокращенного ионного уравнения (сокращают одинаковые ионы в правой и левой частях уравнения): Ag+ + Cl- → Ag. Cl
 Условия необратимости реакций ионного обмена 1. Образование осадка (¯) (таблица растворимости) Pb(NO 3)2 + 2 KI ® Pb. I 2¯ + 2 KNO 3 Pb 2+ + 2 I- ® Pb. I 2¯ 2. Выделение газа ( ) Na 2 CO 3 + H 2 SO 4 ® Na 2 SO 4 + H 2 O + CO 2 CO 32 - + 2 H+ ® H 2 O + CO 2 3. Образование малодиссоциирующего вещества (H 2 O) Ca(OH)2 + 2 HNO 3 ® Ca(NO 3)2 + 2 H 2 O H+ + OH- ® H 2 O 4. Образование комплексного соединения (малодиссоциированные комплексные ионы) Cu. SO 4 • 5 H 2 O + 4 NH 3 ® [Cu(NH 3)4]SO 4 + 5 H 2 O Cu 2+ + 4 NH 3 ® [Cu(NH 3)4]2+ В тех случаях, когда нет ионов, которые могут связываться между собой с образованием осадка, газа, малодиссоциированных соединений (H 2 O) или комплексных ионов реакции обмена обратимы «.
Условия необратимости реакций ионного обмена 1. Образование осадка (¯) (таблица растворимости) Pb(NO 3)2 + 2 KI ® Pb. I 2¯ + 2 KNO 3 Pb 2+ + 2 I- ® Pb. I 2¯ 2. Выделение газа ( ) Na 2 CO 3 + H 2 SO 4 ® Na 2 SO 4 + H 2 O + CO 2 CO 32 - + 2 H+ ® H 2 O + CO 2 3. Образование малодиссоциирующего вещества (H 2 O) Ca(OH)2 + 2 HNO 3 ® Ca(NO 3)2 + 2 H 2 O H+ + OH- ® H 2 O 4. Образование комплексного соединения (малодиссоциированные комплексные ионы) Cu. SO 4 • 5 H 2 O + 4 NH 3 ® [Cu(NH 3)4]SO 4 + 5 H 2 O Cu 2+ + 4 NH 3 ® [Cu(NH 3)4]2+ В тех случаях, когда нет ионов, которые могут связываться между собой с образованием осадка, газа, малодиссоциированных соединений (H 2 O) или комплексных ионов реакции обмена обратимы «.
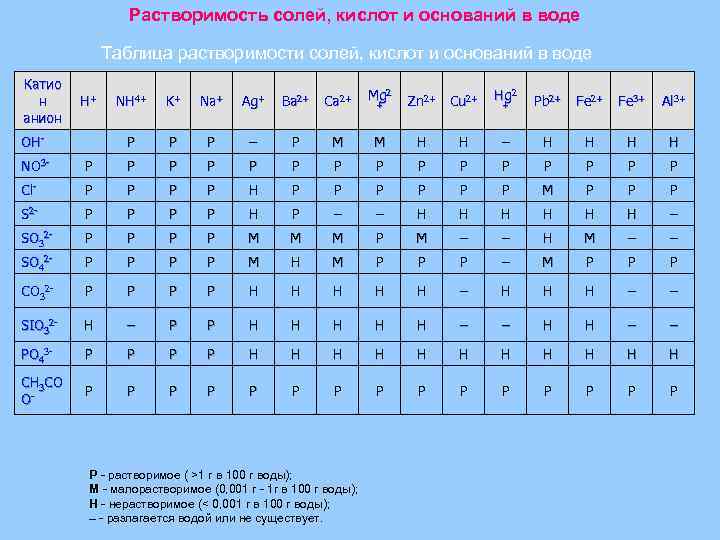 Растворимость солей, кислот и оснований в воде Таблица растворимости солей, кислот и оснований в воде Катио н анион H+ NH 4+ K+ Na+ Ag+ Ba 2+ Ca 2+ Mg 2 Hg 2 + Pb 2+ Fe 3+ Al 3+ OH- P P P – P M M H H – H H NO 3 - P P P P Cl- P P H P P P M P P P S 2 - P P H P – – H H H – SO 32 - P P M M M P M – – H M – – SO 42 - P P M H M P P P – M P P P CO 32 - P P H H H – – SIO 32 - H – P P H H H – – PO 43 - P P H H H CH 3 CO O- P P P P - растворимое ( >1 г в 100 г воды); M - малорастворимое (0, 001 г - 1 г в 100 г воды); H - нерастворимое (< 0, 001 г в 100 г воды); – - разлагается водой или не существует. + Zn 2+ Cu 2+
Растворимость солей, кислот и оснований в воде Таблица растворимости солей, кислот и оснований в воде Катио н анион H+ NH 4+ K+ Na+ Ag+ Ba 2+ Ca 2+ Mg 2 Hg 2 + Pb 2+ Fe 3+ Al 3+ OH- P P P – P M M H H – H H NO 3 - P P P P Cl- P P H P P P M P P P S 2 - P P H P – – H H H – SO 32 - P P M M M P M – – H M – – SO 42 - P P M H M P P P – M P P P CO 32 - P P H H H – – SIO 32 - H – P P H H H – – PO 43 - P P H H H CH 3 CO O- P P P P - растворимое ( >1 г в 100 г воды); M - малорастворимое (0, 001 г - 1 г в 100 г воды); H - нерастворимое (< 0, 001 г в 100 г воды); – - разлагается водой или не существует. + Zn 2+ Cu 2+
 Ионное произведение воды Вода является слабым электролитом и в незначительной степени диссоциирует на ионы по реакции: H 2 O « H+ + OHK = ([H+][OH-]) / [H 2 O] = 1, 8 • 10 -16 (при 22°С) В знаменателе дроби - концентрация недиссоциированных молекул воды, которую можно считать постоянной и определить в 1 л, приняв массу 1 л воды за 1000 г. [H 2 O] = 1000 / 18 = 55, 56 моль Тогда K = ([H+][OH-]) / 55, 56 = 1, 8 • 10 -16 или ([H+][OH -] = 1 • 10 -14 (ионное произведение воды)
Ионное произведение воды Вода является слабым электролитом и в незначительной степени диссоциирует на ионы по реакции: H 2 O « H+ + OHK = ([H+][OH-]) / [H 2 O] = 1, 8 • 10 -16 (при 22°С) В знаменателе дроби - концентрация недиссоциированных молекул воды, которую можно считать постоянной и определить в 1 л, приняв массу 1 л воды за 1000 г. [H 2 O] = 1000 / 18 = 55, 56 моль Тогда K = ([H+][OH-]) / 55, 56 = 1, 8 • 10 -16 или ([H+][OH -] = 1 • 10 -14 (ионное произведение воды)
 p. H раствора Величина p. H используется для характеристики кислотности раствора. Если концентрация ионов водорода равна [H+], то p. H = -lg [H+] В чистой воде [H+] = [OH-] = 10 -7 моль/л В кислых растворах [H+] > [OH-] и p. H < 7 например, в 10 -3 М растворе HCl p. H = 3 В щелочных растворах [H+] < [OH-] и p. H > 7 например, в 10 -2 М растворе Na. OH p. OH = -lg 2 • 10 -2 = 2 - lg 2 = 1, 7 p. H = 14 - p. OH = 14 - 1, 7 = 12, 3
p. H раствора Величина p. H используется для характеристики кислотности раствора. Если концентрация ионов водорода равна [H+], то p. H = -lg [H+] В чистой воде [H+] = [OH-] = 10 -7 моль/л В кислых растворах [H+] > [OH-] и p. H < 7 например, в 10 -3 М растворе HCl p. H = 3 В щелочных растворах [H+] < [OH-] и p. H > 7 например, в 10 -2 М растворе Na. OH p. OH = -lg 2 • 10 -2 = 2 - lg 2 = 1, 7 p. H = 14 - p. OH = 14 - 1, 7 = 12, 3
 Таблица. Изменение окраски кислотно-основных индикаторов в зависимости от p. H раствора Название Окраска индикатора в среде Кислая [H+] > [OH-] р. Н < 7 Нейтральная [H+] = [OH-] р. Н = 7 Щелочная [OH-] > [H+] р. Н > 7 Лакмус красный фиолетовый синий бесцветный малиновый розовый оранжевый желтый Фенолфталеин Метилоранж Для более точного определения значения p. H растворов используют сложную смесь нескольких индикаторов, нанесенную на фильтровальную бумагу. Полоску индикаторной бумаги обмакивают в исследуемый раствор, кладут на белую непромокаемую подложку и быстро сравнивают окраску полоски с эталонной шкалой для p. H: Реакция раствора сильнокислая слабокислая ¯ слабощелочная сильнощелочная ¬ нейтраль ная ® Усиление кислотности среды Усиление основности среды
Таблица. Изменение окраски кислотно-основных индикаторов в зависимости от p. H раствора Название Окраска индикатора в среде Кислая [H+] > [OH-] р. Н < 7 Нейтральная [H+] = [OH-] р. Н = 7 Щелочная [OH-] > [H+] р. Н > 7 Лакмус красный фиолетовый синий бесцветный малиновый розовый оранжевый желтый Фенолфталеин Метилоранж Для более точного определения значения p. H растворов используют сложную смесь нескольких индикаторов, нанесенную на фильтровальную бумагу. Полоску индикаторной бумаги обмакивают в исследуемый раствор, кладут на белую непромокаемую подложку и быстро сравнивают окраску полоски с эталонной шкалой для p. H: Реакция раствора сильнокислая слабокислая ¯ слабощелочная сильнощелочная ¬ нейтраль ная ® Усиление кислотности среды Усиление основности среды
 Гидролиз - это химическая реакция ионного обмена между водой и растворённым в ней веществом с образованием слабого электролита. В большинстве случаев гидролиз сопровождается изменением p. H раствора. Большинство реакций гидролиза - обратимы: Pb(NO 3)2 + H 2 O « Pb(OH)(NO 3) + HNO 3 Na 2 HPO 4 + H 2 O « Na. H 2 PO 4 + Na. OH Некоторые реакции гидролиза протекают необратимо: Al 2 S 3 + 6 H 2 O = 2 Al(OH)3¯ + 3 H 2 S Причиной гидролиза является взаимодействие ионов соли с молекулами воды из гидратной оболочки с образованием малодиссоциированных соединений или ионов. Способность солей подвергаться гидролизу зависит от двух факторов: 1) свойств ионов, образующих соль; 2) внешних факторов.
Гидролиз - это химическая реакция ионного обмена между водой и растворённым в ней веществом с образованием слабого электролита. В большинстве случаев гидролиз сопровождается изменением p. H раствора. Большинство реакций гидролиза - обратимы: Pb(NO 3)2 + H 2 O « Pb(OH)(NO 3) + HNO 3 Na 2 HPO 4 + H 2 O « Na. H 2 PO 4 + Na. OH Некоторые реакции гидролиза протекают необратимо: Al 2 S 3 + 6 H 2 O = 2 Al(OH)3¯ + 3 H 2 S Причиной гидролиза является взаимодействие ионов соли с молекулами воды из гидратной оболочки с образованием малодиссоциированных соединений или ионов. Способность солей подвергаться гидролизу зависит от двух факторов: 1) свойств ионов, образующих соль; 2) внешних факторов.
 Отсутствие гидролиза в растворах солей Соли, образованные катионом сильного основания и анионом сильной кислоты (Li. Br, K 2 SO 4, Na. Cl. O 4, Ba. Cl , Ca(NO 3)2 и др. ) гидролизу не подвергаются, т. к. ни катион, ни анион соли не могут при взаимодействии с водой образовать молекулы слабых электролитов. Водные растворы таких солей имеют нейтральную реакцию среды (p. H = 7). Практически не гидролизуются также и труднорастворимые соли (Ca. CO 3, Mg 3(PO 4)2 и др. ) изза очень низкой концентрации ионов в водных растворах этих солей.
Отсутствие гидролиза в растворах солей Соли, образованные катионом сильного основания и анионом сильной кислоты (Li. Br, K 2 SO 4, Na. Cl. O 4, Ba. Cl , Ca(NO 3)2 и др. ) гидролизу не подвергаются, т. к. ни катион, ни анион соли не могут при взаимодействии с водой образовать молекулы слабых электролитов. Водные растворы таких солей имеют нейтральную реакцию среды (p. H = 7). Практически не гидролизуются также и труднорастворимые соли (Ca. CO 3, Mg 3(PO 4)2 и др. ) изза очень низкой концентрации ионов в водных растворах этих солей.
 Гидролиз по катиону Соли слабого основания и сильной кислоты гидролизуются по катиону: NH 4 Cl + H 2 O « NH 4 OH + HCl; NH 4+ + H 2 O « NH 4 OH + H+ Гидролиз солей, образованных многовалентным катионом протекает ступенчато, через стадии образования основных солей: 1 ступень: Al(NO 3)3 + H 2 O « Al(OH)(NO 3)2 + HNO 3 Al 3+ + H 2 O « [Al(OH)]2+ + H+ 2 ступень: Al(OH)(NO 3)2 + H 2 O « Al(OH)2(NO 3) + HNO 3 [Al(OH)]2+ + H 2 O « [Al(OH)2]+ + H+ 3 ступень: Al(OH)2(NO 3) + H 2 O « Al(OH)3 + HNO 3 [Al(OH)2]+ + H 2 O « Al(OH)3 + H+ Гидролиз протекает в большей степени по первой ступени и практически не протекает по второй и третьей ступени (ввиду накопления ионов водорода, процесс смещается в сторону исходных веществ). Более полному гидролизу способствует разбавление раствора и повышение температуры. (В этом случае можно учитывать гидролиз и по третьей ступени. ) При гидролизе по катиону реакция раствора кислая p. H < 7.
Гидролиз по катиону Соли слабого основания и сильной кислоты гидролизуются по катиону: NH 4 Cl + H 2 O « NH 4 OH + HCl; NH 4+ + H 2 O « NH 4 OH + H+ Гидролиз солей, образованных многовалентным катионом протекает ступенчато, через стадии образования основных солей: 1 ступень: Al(NO 3)3 + H 2 O « Al(OH)(NO 3)2 + HNO 3 Al 3+ + H 2 O « [Al(OH)]2+ + H+ 2 ступень: Al(OH)(NO 3)2 + H 2 O « Al(OH)2(NO 3) + HNO 3 [Al(OH)]2+ + H 2 O « [Al(OH)2]+ + H+ 3 ступень: Al(OH)2(NO 3) + H 2 O « Al(OH)3 + HNO 3 [Al(OH)2]+ + H 2 O « Al(OH)3 + H+ Гидролиз протекает в большей степени по первой ступени и практически не протекает по второй и третьей ступени (ввиду накопления ионов водорода, процесс смещается в сторону исходных веществ). Более полному гидролизу способствует разбавление раствора и повышение температуры. (В этом случае можно учитывать гидролиз и по третьей ступени. ) При гидролизе по катиону реакция раствора кислая p. H < 7.
 Гидролиз по аниону Соли, образованные сильным основанием и слабой (ассоциированной) кислотой гидролизуются по аниону: CH 3 COOK + H 2 O « CH 3 COOH + KOH; CH 3 COO- + H 2 O « CH 3 COOH +OH Соли многоосновных кислот гидролизуются ступенчато (с образованием кислых солей): 1 ступень: K 2 CO 3 + H 2 O « KHCO 3 + KOH CO 2 -3 + H 2 O « HCO 3 - + OH 2 ступень: KHCO 3 + H 2 O « H 2 CO 3+ KOH HCO 3 - + H 2 O « H 2 CO 3 + OH Первая ступень гидролиза протекает достаточно сильно, а вторая – слабо. Только при сильном разбавлении и нагревании следует учитывать гидролиз образующейся кислой соли. При взаимодействии с водой анионов слабых кислот образуются ионы OH-, водные растворы таких солей имеют щелочную реакцию (p. H > 7).
Гидролиз по аниону Соли, образованные сильным основанием и слабой (ассоциированной) кислотой гидролизуются по аниону: CH 3 COOK + H 2 O « CH 3 COOH + KOH; CH 3 COO- + H 2 O « CH 3 COOH +OH Соли многоосновных кислот гидролизуются ступенчато (с образованием кислых солей): 1 ступень: K 2 CO 3 + H 2 O « KHCO 3 + KOH CO 2 -3 + H 2 O « HCO 3 - + OH 2 ступень: KHCO 3 + H 2 O « H 2 CO 3+ KOH HCO 3 - + H 2 O « H 2 CO 3 + OH Первая ступень гидролиза протекает достаточно сильно, а вторая – слабо. Только при сильном разбавлении и нагревании следует учитывать гидролиз образующейся кислой соли. При взаимодействии с водой анионов слабых кислот образуются ионы OH-, водные растворы таких солей имеют щелочную реакцию (p. H > 7).
 Гидролиз по катиону и аниону Соли, образованные слабым основанием и слабой кислотой, гидролизуются и по катиону и по аниону: CH 3 COONH 4 + H 2 O « CH 3 COOH + NH 4 OH или в ионной форме: CH 3 COO- + NH 4+ + H 2 O « CH 3 COOH + NH 4 OH Гидролиз таких солей протекает очень сильно, т. к. в результате образуются и слабое основание, и слабая кислота. Реакция среды в этом случае зависит от сравнительной силы основания и кислоты, т. е. от их констант диссоциации (KD). Если KD(основания) > KD(кислоты) , то p. H > 7; если KD(основания) < KD(кислоты), то p. H < 7. В случае гидролиза CH 3 COONH 4: KD(NH 4 OH) = 1, 8 • 10 -5; KD(CH 3 COOH)=1, 8 • 10 -5 поэтому реакция водного раствора этой соли будет почти нейтральной (p. H = 7– 8). Если основание и кислота, образующие соль, являются не только слабыми электролитами, но и малорастворимы или неустойчивы и разлагаются с образованием летучих продуктов, то в этом случае гидролиз соли протекает необратимо: Al 2 S 3 + 6 H 2 O = 2 Al(OH)3¯ + 3 H 2 S Поэтому сульфид алюминия не может существовать в виде водных растворов, может быть получен только "сухим способом", например, из элементов при высокой температуре: 2 Al + 3 S t°® Al 2 S 3 и должен храниться в герметических сосудах, исключающих попадание влаги.
Гидролиз по катиону и аниону Соли, образованные слабым основанием и слабой кислотой, гидролизуются и по катиону и по аниону: CH 3 COONH 4 + H 2 O « CH 3 COOH + NH 4 OH или в ионной форме: CH 3 COO- + NH 4+ + H 2 O « CH 3 COOH + NH 4 OH Гидролиз таких солей протекает очень сильно, т. к. в результате образуются и слабое основание, и слабая кислота. Реакция среды в этом случае зависит от сравнительной силы основания и кислоты, т. е. от их констант диссоциации (KD). Если KD(основания) > KD(кислоты) , то p. H > 7; если KD(основания) < KD(кислоты), то p. H < 7. В случае гидролиза CH 3 COONH 4: KD(NH 4 OH) = 1, 8 • 10 -5; KD(CH 3 COOH)=1, 8 • 10 -5 поэтому реакция водного раствора этой соли будет почти нейтральной (p. H = 7– 8). Если основание и кислота, образующие соль, являются не только слабыми электролитами, но и малорастворимы или неустойчивы и разлагаются с образованием летучих продуктов, то в этом случае гидролиз соли протекает необратимо: Al 2 S 3 + 6 H 2 O = 2 Al(OH)3¯ + 3 H 2 S Поэтому сульфид алюминия не может существовать в виде водных растворов, может быть получен только "сухим способом", например, из элементов при высокой температуре: 2 Al + 3 S t°® Al 2 S 3 и должен храниться в герметических сосудах, исключающих попадание влаги.
 Реакции обмена, сопровождаемые гидролизом К таким реакциям относятся взаимодействия солей двухвалентных катионов (кроме Ca 2+, Sr 2+, Ba 2+) с водными растворами карбонатов натрия или калия, сопровождающиеся образованием осадков менее растворимых основных карбонатов 2 Cu(NO 3)2 + 2 Na 2 CO 3 + H 2 O ® Cu 2(OH)2 CO 3¯ + 4 Na. NO 3 + CO 2 А также реакции взаимодействия солей Al 3+, Cr 3+ и Fe 3+ с водными растворами карбонатов и сульфидов щелочных металлов: 2 Al. Cl + 3 Na 2 CO 3 + 3 H 2 O ® 2 Al(OH)3¯ + 3 CO 2 + 6 Na. Cl Cr 2(SO 4)3 + 3 Na 2 S + 6 H 2 O ® 2 Cr(OH)3¯ + 3 H 2 S + 3 Na 2 SO 4 При взаимодействии водных растворов солей трёхвалентного железа с сульфидами щелочных металлов протекает окислительновосстановительная реакция: 2 Fe 3+ + S 2 - = 2 Fe 2+ + S 0
Реакции обмена, сопровождаемые гидролизом К таким реакциям относятся взаимодействия солей двухвалентных катионов (кроме Ca 2+, Sr 2+, Ba 2+) с водными растворами карбонатов натрия или калия, сопровождающиеся образованием осадков менее растворимых основных карбонатов 2 Cu(NO 3)2 + 2 Na 2 CO 3 + H 2 O ® Cu 2(OH)2 CO 3¯ + 4 Na. NO 3 + CO 2 А также реакции взаимодействия солей Al 3+, Cr 3+ и Fe 3+ с водными растворами карбонатов и сульфидов щелочных металлов: 2 Al. Cl + 3 Na 2 CO 3 + 3 H 2 O ® 2 Al(OH)3¯ + 3 CO 2 + 6 Na. Cl Cr 2(SO 4)3 + 3 Na 2 S + 6 H 2 O ® 2 Cr(OH)3¯ + 3 H 2 S + 3 Na 2 SO 4 При взаимодействии водных растворов солей трёхвалентного железа с сульфидами щелочных металлов протекает окислительновосстановительная реакция: 2 Fe 3+ + S 2 - = 2 Fe 2+ + S 0
 Количественные характеристики реакции гидролиза Количественно гидролиз солей может быть охарактеризован степенью гидролиза и константой гидролиза. h - степень гидролиза - отношение числа гидролизованных молекул к общему числу растворённых молекул (выражается в процентах): h. = (Cгидр. / Cраств. ) • 100% Степень гидролиза не является константой, т. е. не постоянна и зависит от химической природы образующейся при гидролизе кислоты (основания) и будет тем больше, чем слабее кислота (основание) (в определённых равных условиях). Изменяется с температурой, зависит от концентрации солевого раствора.
Количественные характеристики реакции гидролиза Количественно гидролиз солей может быть охарактеризован степенью гидролиза и константой гидролиза. h - степень гидролиза - отношение числа гидролизованных молекул к общему числу растворённых молекул (выражается в процентах): h. = (Cгидр. / Cраств. ) • 100% Степень гидролиза не является константой, т. е. не постоянна и зависит от химической природы образующейся при гидролизе кислоты (основания) и будет тем больше, чем слабее кислота (основание) (в определённых равных условиях). Изменяется с температурой, зависит от концентрации солевого раствора.
 Константа гидролиза Кг - константа равновесия обратимой реакции. Зависит от температуры, но не зависит от концентрации раствора. Рассмотрим соль гипохлорит натрия, образованную сильным основанием и слабой кислотой: Константа равновесия данной обратимой реакции равна: Поскольку вода - очень слабый электролит, её равновесную концентрацию можно считать константой: Kp · [H 2 O]p= KГ. В результате перемножения двух констант получается новая константа - константа гидролиза соли.
Константа гидролиза Кг - константа равновесия обратимой реакции. Зависит от температуры, но не зависит от концентрации раствора. Рассмотрим соль гипохлорит натрия, образованную сильным основанием и слабой кислотой: Константа равновесия данной обратимой реакции равна: Поскольку вода - очень слабый электролит, её равновесную концентрацию можно считать константой: Kp · [H 2 O]p= KГ. В результате перемножения двух констант получается новая константа - константа гидролиза соли.
 Константа гидролиза соли, образованной сильным гидроксидом и слабой кислотой, равна ионному произведению воды, деленному на Kд слабой кислоты.
Константа гидролиза соли, образованной сильным гидроксидом и слабой кислотой, равна ионному произведению воды, деленному на Kд слабой кислоты.
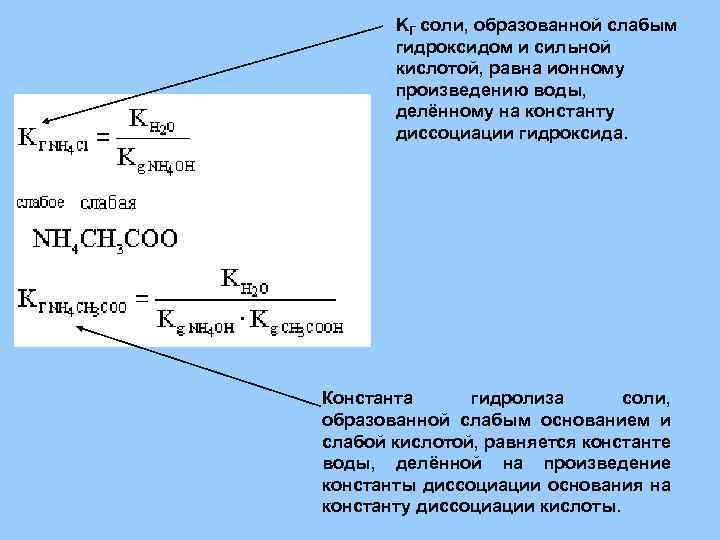 KГ соли, образованной слабым гидроксидом и сильной кислотой, равна ионному произведению воды, делённому на константу диссоциации гидроксида. Константа гидролиза соли, образованной слабым основанием и слабой кислотой, равняется константе воды, делённой на произведение константы диссоциации основания на константу диссоциации кислоты.
KГ соли, образованной слабым гидроксидом и сильной кислотой, равна ионному произведению воды, делённому на константу диссоциации гидроксида. Константа гидролиза соли, образованной слабым основанием и слабой кислотой, равняется константе воды, делённой на произведение константы диссоциации основания на константу диссоциации кислоты.
 Связь степени и константы гидролиза Для данной реакции:
Связь степени и константы гидролиза Для данной реакции:
 Равновесие в гетерогенных растворах. Произведение растворимости
Равновесие в гетерогенных растворах. Произведение растворимости
 Рассмотрим систему, в которой имеется осадок труднорастворимой соли, находящийся в соприкосновении с насыщенным раствором этой соли. При этом происходят два взаимно противоположных процесса: 1) Переход ионов из осадка в раствор: скорость этого процесса можно считать постоянной при Т = const и не зависит от концентрации труднорастворимого соединения: V 1=K 1; 2) Осаждение ионов из раствора: скорость этого процесса V 2 зависит от концентрации ионов Ag+ и Cl- в растворе. По закону действующих масс: V 2 = k 2 • [Ag+] • [Cl-]
Рассмотрим систему, в которой имеется осадок труднорастворимой соли, находящийся в соприкосновении с насыщенным раствором этой соли. При этом происходят два взаимно противоположных процесса: 1) Переход ионов из осадка в раствор: скорость этого процесса можно считать постоянной при Т = const и не зависит от концентрации труднорастворимого соединения: V 1=K 1; 2) Осаждение ионов из раствора: скорость этого процесса V 2 зависит от концентрации ионов Ag+ и Cl- в растворе. По закону действующих масс: V 2 = k 2 • [Ag+] • [Cl-]
 Так как данная система находится в состоянии равновесия, то: V 1 = V 2, тогда k 2 = k 1 • [Ag +] • [Cl - ] [Ag + ] • [Cl - ] = k 2 / k 1 = const (при T = const) Таким образом, произведение концентраций ионов в насыщенном растворе труднорастворимого электролита при постоянной температуре является постоянной величиной и называется произведением растворимости ПР. ПР(Аg. Cl) = [Ag + ] • [Cl - ]
Так как данная система находится в состоянии равновесия, то: V 1 = V 2, тогда k 2 = k 1 • [Ag +] • [Cl - ] [Ag + ] • [Cl - ] = k 2 / k 1 = const (при T = const) Таким образом, произведение концентраций ионов в насыщенном растворе труднорастворимого электролита при постоянной температуре является постоянной величиной и называется произведением растворимости ПР. ПР(Аg. Cl) = [Ag + ] • [Cl - ]
 В тех случаях, когда электролит содержит два или несколько одинаковых ионов, концентрация этих ионов, при вычислении произведения растворимости должна быть возведена в соответствующую степень. ПР(Ag 2 S) = [Ag+]2 • [S 2 -]; ПР(Pb. I 2) = [Pb 2+] • [I-]2 В общем случае выражение произведения растворимости для электролита Am. Bn ПР(Am. Bn)= [A]m· [B]n Значения произведения растворимости для разных веществ различны. Например, ПР(Ca. CO 3) = 4, 8 • 10 -9; ПР(Ag. Cl) = 1, 56 • 10 -10.
В тех случаях, когда электролит содержит два или несколько одинаковых ионов, концентрация этих ионов, при вычислении произведения растворимости должна быть возведена в соответствующую степень. ПР(Ag 2 S) = [Ag+]2 • [S 2 -]; ПР(Pb. I 2) = [Pb 2+] • [I-]2 В общем случае выражение произведения растворимости для электролита Am. Bn ПР(Am. Bn)= [A]m· [B]n Значения произведения растворимости для разных веществ различны. Например, ПР(Ca. CO 3) = 4, 8 • 10 -9; ПР(Ag. Cl) = 1, 56 • 10 -10.
 ПР легко вычислить, зная раcтворимость соединения при данной t°. Пример: Растворимость Ca. CO 3 равна 0, 0069 или 6, 9 • 103 г/л. Найти ПР(Ca. CO ). 3 Решение: Выразим растворимость (Р) в молях: Р(Ca. CO 3)=(6, 9 • 10 -3)/100 = 6, 9 • 10 -5 моль/л M(Ca. CO 3) = 100 г/моль Так каждая молекула Ca. CO 3 дает при растворении по одному иону Ca 2+ и CO 32 -, то [Ca 2+] = [ CO 32 -] = 6, 9 • 10 -5 моль/л, Следовательно: ПР(Ca. CO 3) = [Ca 2+] • [CO 32 -]=6, 9 • 10– 5 • 6, 9 • 10 -5 = 4, 8 • 10 -9
ПР легко вычислить, зная раcтворимость соединения при данной t°. Пример: Растворимость Ca. CO 3 равна 0, 0069 или 6, 9 • 103 г/л. Найти ПР(Ca. CO ). 3 Решение: Выразим растворимость (Р) в молях: Р(Ca. CO 3)=(6, 9 • 10 -3)/100 = 6, 9 • 10 -5 моль/л M(Ca. CO 3) = 100 г/моль Так каждая молекула Ca. CO 3 дает при растворении по одному иону Ca 2+ и CO 32 -, то [Ca 2+] = [ CO 32 -] = 6, 9 • 10 -5 моль/л, Следовательно: ПР(Ca. CO 3) = [Ca 2+] • [CO 32 -]=6, 9 • 10– 5 • 6, 9 • 10 -5 = 4, 8 • 10 -9
 Зная величину ПР, можно в свою очередь вычислить растворимость вещества в моль/л или г/л. Пример: Произведение растворимости ПР(Pb. SO 4) = 2, 2 • 10 - 8 г/л. Чему равна растворимость Pb. SO 4? Решение Обозначим растворимость Pb. SO 4 через X моль/л. Перейдя в раствор, X молей Pb. SO 4 дадут X ионов Pb 2+ и X ионов SO 42 -, т. е. : [Pb 2+] = [SO 42 -] = X ПР(Pb. SO 4) = [Pb 2+] = [SO 42 -] = X • X = X 2 X = ПР(Pb. SO 4) = (2, 2 • 10 -8) = 1, 5 • 10 -4 моль/л. Чтобы перейти к растворимости, выраженной в г/л, найденную величину умножим на молекулярную массу, после чего получим: 1, 5 • 10 -4 • 303 = 4, 5 • 10 -2 г/л.
Зная величину ПР, можно в свою очередь вычислить растворимость вещества в моль/л или г/л. Пример: Произведение растворимости ПР(Pb. SO 4) = 2, 2 • 10 - 8 г/л. Чему равна растворимость Pb. SO 4? Решение Обозначим растворимость Pb. SO 4 через X моль/л. Перейдя в раствор, X молей Pb. SO 4 дадут X ионов Pb 2+ и X ионов SO 42 -, т. е. : [Pb 2+] = [SO 42 -] = X ПР(Pb. SO 4) = [Pb 2+] = [SO 42 -] = X • X = X 2 X = ПР(Pb. SO 4) = (2, 2 • 10 -8) = 1, 5 • 10 -4 моль/л. Чтобы перейти к растворимости, выраженной в г/л, найденную величину умножим на молекулярную массу, после чего получим: 1, 5 • 10 -4 • 303 = 4, 5 • 10 -2 г/л.
![Условия образования осадков [Ag+] • [Cl-] < ПР(Ag. Cl) - ненасыщенный раствор (осадок не Условия образования осадков [Ag+] • [Cl-] < ПР(Ag. Cl) - ненасыщенный раствор (осадок не](https://present5.com/presentation/-34950989_50598270/image-42.jpg) Условия образования осадков [Ag+] • [Cl-] < ПР(Ag. Cl) - ненасыщенный раствор (осадок не образуется) [Ag+] • [Cl-] = ПР(Ag. Cl) - насыщенный раствор (осадок не образуется) [Ag+] • [Cl-] > ПР(Ag. Cl) - перенасыщенный раствор (осадок образуется) Осадок образуется в том случае, если произведение концентраций ионов малорастворимого электролита превысит величину его произведения растворимости при данной температуре. Когда ионное произведение станет равным величине ПР, выпадение осадка прекращается.
Условия образования осадков [Ag+] • [Cl-] < ПР(Ag. Cl) - ненасыщенный раствор (осадок не образуется) [Ag+] • [Cl-] = ПР(Ag. Cl) - насыщенный раствор (осадок не образуется) [Ag+] • [Cl-] > ПР(Ag. Cl) - перенасыщенный раствор (осадок образуется) Осадок образуется в том случае, если произведение концентраций ионов малорастворимого электролита превысит величину его произведения растворимости при данной температуре. Когда ионное произведение станет равным величине ПР, выпадение осадка прекращается.
 Зная объем и концентрацию смешиваемых растворов, можно рассчитать, будет ли выпадать осадок образующейся соли. Пример: Выпадает ли осадок при смешении равных объемов 0, 2 M растворов Pb(NO 3)2 и Na. Cl. ПР(Pb. Cl 2) = 2, 4 • 10 -4. Решение: При смешении объем раствора увеличивается в 2 раза и концентрация каждого из веществ уменьшится в 2 раза, т. е. станет 0, 1 M. Таковы же будут концентрации Pb 2+ и Cl-. Следовательно, [Pb 2+] • [Cl-]2 = 0, 1 • 0, 12 = 10 -3. Полученная величина превышает ПР(Pb. Cl 2)=2, 4 • 10 -4. Поэтому часть соли Pb. Cl 2 выпадает в осадок.
Зная объем и концентрацию смешиваемых растворов, можно рассчитать, будет ли выпадать осадок образующейся соли. Пример: Выпадает ли осадок при смешении равных объемов 0, 2 M растворов Pb(NO 3)2 и Na. Cl. ПР(Pb. Cl 2) = 2, 4 • 10 -4. Решение: При смешении объем раствора увеличивается в 2 раза и концентрация каждого из веществ уменьшится в 2 раза, т. е. станет 0, 1 M. Таковы же будут концентрации Pb 2+ и Cl-. Следовательно, [Pb 2+] • [Cl-]2 = 0, 1 • 0, 12 = 10 -3. Полученная величина превышает ПР(Pb. Cl 2)=2, 4 • 10 -4. Поэтому часть соли Pb. Cl 2 выпадает в осадок.
 Факторы, влияющие на образование осадков 1) Влияние концентрации растворов Труднорастворимый электролит с достаточно большой величиной ПР нельзя осадить из разбавленных растворов. 2) Влияние количества осадителя Для более полного осаждения употребляют избыток осадителя. 3) Влияние одноименного иона Растворимость осадков снижается в присутствии других сильных электролитов, имеющих одноименные ионы. Если к ненасыщенному раствору Ba. SO 4 понемногу прибавлять раствор Na 2 SO 4, то ионное произведение, которое было сначала меньше ПР(Ba. SO 4) = 1, 1 • 10 -10, постепенно достигнет ПР и превысит его. Начнется выпадение осадка. 4) Влияние температуры ПР является постоянной величиной при постоянной температуре. С увеличением температуры ПР возрастает, поэтому осаждение лучше проводить из охлажденных растворов.
Факторы, влияющие на образование осадков 1) Влияние концентрации растворов Труднорастворимый электролит с достаточно большой величиной ПР нельзя осадить из разбавленных растворов. 2) Влияние количества осадителя Для более полного осаждения употребляют избыток осадителя. 3) Влияние одноименного иона Растворимость осадков снижается в присутствии других сильных электролитов, имеющих одноименные ионы. Если к ненасыщенному раствору Ba. SO 4 понемногу прибавлять раствор Na 2 SO 4, то ионное произведение, которое было сначала меньше ПР(Ba. SO 4) = 1, 1 • 10 -10, постепенно достигнет ПР и превысит его. Начнется выпадение осадка. 4) Влияние температуры ПР является постоянной величиной при постоянной температуре. С увеличением температуры ПР возрастает, поэтому осаждение лучше проводить из охлажденных растворов.


